Câu 1 [251493]: Khi calcium phản ứng với nước, nhiệt độ thay đổi từ 18°C đến 39°C. Phản ứng của calcium với nước là
A, phản ứng thu nhiệt.
B, phản ứng phân hủy.
C, phản ứng tỏa nhiệt.
D, phản ứng thuận nghịch.
HD: Nhiệt độ tăng nên phản ứng tỏa nhiệt. Đáp án: C
Câu 2 [251495]: Nung KNO3 lên 550oC xảy ra phản ứng:
2KNO3(s) → 2KNO2(s) + O2(g). ∆H?
Phản ứng nhiệt phân KNO3 là
2KNO3(s) → 2KNO2(s) + O2(g). ∆H?
Phản ứng nhiệt phân KNO3 là
A, tỏa nhiệt, có ∆H < 0.
B, thu nhiệt, có ∆H > 0.
C, tỏa nhiệt, có ∆H > 0.
D, thu nhiệt, có ∆H < 0.
HD: Phản ứng cần cung cấp nhiệt độ nên là phản ứng thu nhiệt. Đáp án: B
Câu 3 [251497]: Sự thay đổi nhiệt độ trong phản ứng của calcium oxide với nước được minh họa trong vẽ. Phản ứng của calcium với nước là


A, phản ứng thu nhiệt.
B, phản ứng phân hủy.
C, phản ứng tỏa nhiệt.
D, phản ứng thuận nghịch.
HD: Nhiệt độ tăng nên phản ứng tỏa nhiệt. Đáp án: C
Câu 4 [251522]: Dựa vào phương trình nhiệt hóa học của các phản ứng sau:
(1) CS2(l) + 3O2(g) –––to–→ CO2(g) + 2SO2(g); ΔrHo298 = – 1110,21 kJ;
(2) CO2(g) → CO(g) + 1/2O2(g); ΔrHo298 = + 280,00 kJ;
(3) Na(s) + 2H2O(l) → NaOH(aq) + H2(g); ΔrHo298 = – 367,50 kJ;
(4) ZnSO4(s) → ZnO(s) + SO3(g); ΔrHo298 = + 235,21 kJ;
Cặp phản ứng tỏa nhiệt là
(1) CS2(l) + 3O2(g) –––to–→ CO2(g) + 2SO2(g); ΔrHo298 = – 1110,21 kJ;
(2) CO2(g) → CO(g) + 1/2O2(g); ΔrHo298 = + 280,00 kJ;
(3) Na(s) + 2H2O(l) → NaOH(aq) + H2(g); ΔrHo298 = – 367,50 kJ;
(4) ZnSO4(s) → ZnO(s) + SO3(g); ΔrHo298 = + 235,21 kJ;
Cặp phản ứng tỏa nhiệt là
A, (1) và (2).
B, (3) và (4).
C, (1) và (3).
D, (2) và (4).
HD: Phản ứng tỏa nhiệt có biến thiên enthalpy < 0. Đáp án: C
Câu 5 [193301]: Xét sự thay đổi enthalpy khi phản ứng xảy ra giữa Fe2O3 với kim loại aluminium theo phương trình:
Fe2O3(s) + 2Al(s) → Al2O3(s) + 2Fe(l).
Cho biết enthalpy tạo thành chuẩn của Fe2O3(s) là – 825,5 kJ/mol; của Al2O3(s) là – 1675,7 kJ/mol. Biến thiên enthalpy của phản ứng khi dùng 5,00 g Fe2O3 là
Fe2O3(s) + 2Al(s) → Al2O3(s) + 2Fe(l).
Cho biết enthalpy tạo thành chuẩn của Fe2O3(s) là – 825,5 kJ/mol; của Al2O3(s) là – 1675,7 kJ/mol. Biến thiên enthalpy của phản ứng khi dùng 5,00 g Fe2O3 là
A, – 21,8 kJ.
B, – 26,6 kJ.
C, – 52,4 kJ.
D, – 77,9 kJ.
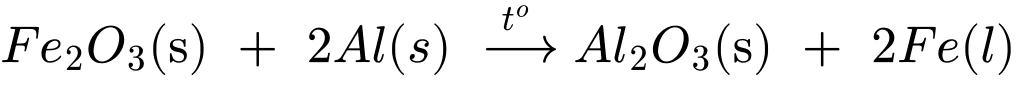
Biến thiên enthalpy của phản ứng trên là
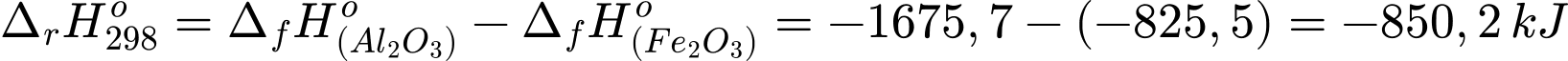
1 mol Fe2O3 khi tham gia phản ứng nhiệt lượng tỏa ra là 850,2 kJ
5 gam Fe2O3 khi tham gia phản ứng nhiệt lượng tỏa ra là
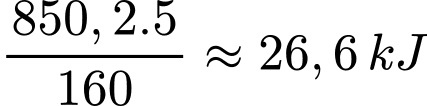
⟹Chọn đáp án B Đáp án: B
Câu 6 [251701]: Biến thiên enthalpy chuẩn của phản ứng: 2CuO(s) → Cu2O(s) + 1/2O2(g) là (biết enthalpy tạo thành chuẩn của CuO(s) là –156,1 kJ/mol; Cu2O(s) là –170,7 kJ/mol).
A, 141,5 kJ.
B, 14,6 kJ.
C, –14,6 kJ.
D, –141,5 kJ.
HD: ΔrH0298 = – 170,7 – 2 × (– 156,1) = 141,5 kJ. Đáp án: A
Câu 7 [251702]: Khi tạo ra 1 mol HCl từ các đơn chất bền có giải phóng ra một lượng nhiệt là 91,98 kJ/mol. Nếu phân huỷ 365 gam khí HCl thành các đơn chất thì lượng nhiệt kèm theo quá trình đó là bao nhiêu?
A, + 459,9 kJ.
B, – 459,9 kJ.
C, – 919,8 kJ.
D, + 919,8 kJ.
HD: 1 mol HCl giải phóng ra một lượng nhiệt là 91,98 kJ/mol
Nếu phân huỷ 1 mol khí HCl thành các đơn chất thì lượng nhiệt kèm theo quá trình đó là 91,98 kJ/mol. 365 gam HCl tương ứng với 10ml thì lượng nhiệt kèm theo quá trình đó là 919, 8 kJ/mol. Đáp án: D
Nếu phân huỷ 1 mol khí HCl thành các đơn chất thì lượng nhiệt kèm theo quá trình đó là 91,98 kJ/mol. 365 gam HCl tương ứng với 10ml thì lượng nhiệt kèm theo quá trình đó là 919, 8 kJ/mol. Đáp án: D
Câu 8 [251703]: Phản ứng đốt cháy methane xảy ra như sau:
CH4(g) + 2O2(g) –––to–→ CO2(g) + 2H2O(l).
Giá trị biến thiên enthalpy phản ứng tính theo enthalpy tạo thành có giá trị là
(biết enthalpy tạo thành chuẩn của các chất CH4(g) = –74,8 kJ/mol; CO2(g) = –393,5 kJ/mol; H2O(l) = –285,8 kJ/mol).
CH4(g) + 2O2(g) –––to–→ CO2(g) + 2H2O(l).
Giá trị biến thiên enthalpy phản ứng tính theo enthalpy tạo thành có giá trị là
(biết enthalpy tạo thành chuẩn của các chất CH4(g) = –74,8 kJ/mol; CO2(g) = –393,5 kJ/mol; H2O(l) = –285,8 kJ/mol).
A, –604,5 kJ.
B, + 890,3 kJ.
C, –997,7 kJ.
D, –890,3 kJ.
HD: ΔrHo298 = –393,5 + 2.(–285,8 ) – ( –74,8) = –890,3 kJ. Đáp án: D
Câu 9 [251704]: Đốt cháy 3,6 gam butanol (C4H9OH) thấy có 134 kJ nhiệt được giải phóng. Biến thiên enthalpy của quá trình đốt cháy 1 mol butanol là
A, –134 kJ/mol.
B, 2754,44 kJ/mol.
C, –2754,44 kJ/mol.
D, –268 kJ/mol.
HD: nC4H9OH = 3,6 ÷ 74 = 9/185 mol.
Phản ứng giải phóng năng lượng nên biến thiên enthalpy có giá trị âm.
⇒ Biến thiên enthalpy của quá trình đốt cháy1 mol butanol là: – 9/185 × 134 = – 2754,44 kJ. Đáp án: C
Phản ứng giải phóng năng lượng nên biến thiên enthalpy có giá trị âm.
⇒ Biến thiên enthalpy của quá trình đốt cháy1 mol butanol là: – 9/185 × 134 = – 2754,44 kJ. Đáp án: C
Câu 10 [251705]: Propane (C3H8) là một hydrocarbon phổ biến thường được dùng làm nhiên liệu do quá trình cháy giải phóng lượng nhiệt lớn. Khi đốt cháy 1 mol propane thì giải phóng −2219,2 kJ nhiệt lượng. Nhiệt tạo thành chuẩn của propane là (biết nhiệt tạo thành chuẩn của H2O(l) = −285,8 kJ/ mol; CO2(g) = −393,5 kJ/mol).
A, +1539,9 kJ.
B, –1539,9 kJ.
C, –104,5 kJ.
D, +212,2 kJ.
HD: C3H8(g) + O2(g) –––to–→ 3CO2(g) + 4H2O(l).
ΔrHo298 = 3 × (−393,5) + 4 × (−285,8) – ΔfHo298 (C3H8) = −2219,2.
⇒ ΔfHo298 (C3H8) = –104,5 kJ. Đáp án: C
ΔrHo298 = 3 × (−393,5) + 4 × (−285,8) – ΔfHo298 (C3H8) = −2219,2.
⇒ ΔfHo298 (C3H8) = –104,5 kJ. Đáp án: C
Câu 11 [251706]: Hydrogen peroxide, H2O2 được sử dụng để cung cấp lực đẩy cho tên lửa do dễ dàng bị phân hủy theo phương trình:
2H2O2(l) → 2H2O(g) + O2(g).
Lượng nhiệt được tạo ra khi phân hủy chính xác 1 mol H2O2 ở điều kiện chuẩn là (biết nhiệt tạo thành chuẩn của H2O(g) = −241,8 kJ/ mol; H2O2(l) = −187,8 kJ/mol).
2H2O2(l) → 2H2O(g) + O2(g).
Lượng nhiệt được tạo ra khi phân hủy chính xác 1 mol H2O2 ở điều kiện chuẩn là (biết nhiệt tạo thành chuẩn của H2O(g) = −241,8 kJ/ mol; H2O2(l) = −187,8 kJ/mol).
A, −108 kJ.
B, –54 kJ.
C, +54 kJ.
D, +108 kJ.
HD: ΔrHo298 = 2 × (−241,8) – 2 × (−187,8) = −108 kJ.
Lượng nhiệt được tạo ra khi phân hủy chính xác 1 mol H2O2 ở điều kiện chuẩn là:
ΔrHo298 = −108 ÷ 2 = –54kJ
⇒ Chọn đáp án B Đáp án: B
Lượng nhiệt được tạo ra khi phân hủy chính xác 1 mol H2O2 ở điều kiện chuẩn là:
ΔrHo298 = −108 ÷ 2 = –54kJ
⇒ Chọn đáp án B Đáp án: B
Câu 12 [251709]: Giai đoạn đầu tiên trong quá trình sản xuất nitric acid từ ammonia xảy ra theo phương trình phản ứng sau:
4NH3(g) + 5O2(g) ⇄ 4NO(g) + 6H2O(g).
Sử dụng dữ liệu được cho trong bảng sau biến thiên enthalpy chuẩn của phản ứng trên tính theo nhiệt tạo thành chuẩn có giá trị là
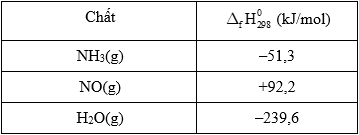
4NH3(g) + 5O2(g) ⇄ 4NO(g) + 6H2O(g).
Sử dụng dữ liệu được cho trong bảng sau biến thiên enthalpy chuẩn của phản ứng trên tính theo nhiệt tạo thành chuẩn có giá trị là

A, +863,6 kJ/mol.
B, +1274 kJ/mol.
C, –863,6 kJ/mol.
D, –1274 kJ/mol.
Biến thiên enthalpy chuẩn của phản ứng trên là:
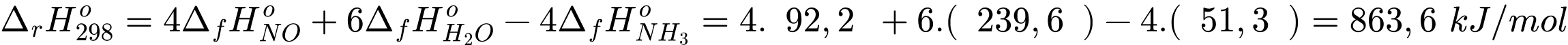
Đáp án: C. –863,6 kJ/mol. Đáp án: C
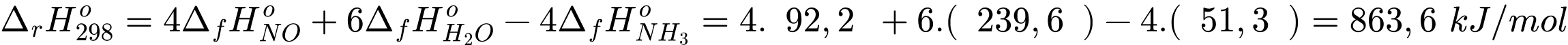
Đáp án: C. –863,6 kJ/mol. Đáp án: C
Câu 13 [251710]: Nhiệt lượng tỏa ra từ quá trình đốt cháy 6,44 gam sulfur trong oxygen theo phương trình:
2S(s) + 3O2(g) –––to–→ 2SO3(l); ΔrHo298 = – 791,4 kJ
có giá trị là
2S(s) + 3O2(g) –––to–→ 2SO3(l); ΔrHo298 = – 791,4 kJ
có giá trị là
A, +395,7 kJ.
B, –395,7 kJ.
C, –79,63 kJ.
D, +79,63 kJ.
HD: Dùng 2 mol S cần ΔrHo298 = – 791,4 kJ.
⇒ Tương ứng số mol S là 0,20125 thì cần –79,63 kJ. Đáp án: C
Câu 14 [251711]: Phản ứng giữa hydrogen và bromine xảy ra như sau:
H2(g) + Br2(g) → 2HBr(g) cần cung cấp 72,80 kJ nhiệt lượng.
Nhiệt lượng cần cung cấp khi lấy 38,2 gam bromine phản ứng với hydrogen là
H2(g) + Br2(g) → 2HBr(g) cần cung cấp 72,80 kJ nhiệt lượng.
Nhiệt lượng cần cung cấp khi lấy 38,2 gam bromine phản ứng với hydrogen là
A, +36,40 kJ.
B, 8,69 kJ.
C, –36,40 kJ.
D, 17,38 kJ.
HD: Dùng 1 mol bromine cần cung cấp 72,80 kJ nhiệt lượng
⇒ Số mol bromine là 0,23875 thì cần cung cấp 17,38 kJ nhiệt lượng. Đáp án: D
⇒ Số mol bromine là 0,23875 thì cần cung cấp 17,38 kJ nhiệt lượng. Đáp án: D
Câu 15 [251717]: Khi đốt cháy glucose (C6H12O6) thấy giải phóng –2816 kJ/mol nhiệt lượng ở 25oC. Enthalpy tạo thành chuẩn của C6H12O6 nhận giá trị là (biết enthalpy tạo thành chuẩn của CO2(g) và H2O(l) lần lượt là –393,5 kJ/mol và –285,9 kJ/mol).
A, +1260,4 kJ.
B, –2136,6 kJ.
C, –1260,4 kJ.
D, +2136,6 kJ.
HD: C6H12O6(s) + 6O2(g) → 6CO2(g) + 6H2O(l); ΔrHo298 = – 2816 kJ.
– 2816 = 6 × (–393,5) + 6 × (– 285,9) – ΔfHo298 (C6H12O6)
ΔfHo298 (C6H12O6) = –1260,4 kJ. Đáp án: C
– 2816 = 6 × (–393,5) + 6 × (– 285,9) – ΔfHo298 (C6H12O6)
ΔfHo298 (C6H12O6) = –1260,4 kJ. Đáp án: C
Câu 16 [251719]: Tiến hành đốt cháy 1 mol benzene ở điều kiện chuẩn, phản ứng sinh ra CO2(g), H2O(l) đồng thời giải phóng 3267 kJ nhiệt lượng. Enthalpy tạo thành chuẩn của benzene nhận giá trị là (biết enthalpy tạo thành chuẩn của CO2(g) và H2O(l) lần lượt là –393,5 kJ/mol; –285,83 kJ/mol).
A, –48,51 kJ/mol.
B, –24,5 kJ/mol.
C, +48,51 kJ/mol.
D, +24,5 kJ/mol.
HD: C6H6 + 15/2O2(g) –––to–→ 6CO2(g) + 3H2O(l)
–3267 = 6 × (–393,5) + 3 × (–285,83) – ΔfHo298 (C6H6)
⇒ ΔfHo298 (C6H6) = +48,51 kJ. Đáp án: C
–3267 = 6 × (–393,5) + 3 × (–285,83) – ΔfHo298 (C6H6)
⇒ ΔfHo298 (C6H6) = +48,51 kJ. Đáp án: C
Câu 17 [193203]: Cho biết biến thiên enthalpy của phản ứng sau ở điều kiện chuẩn:
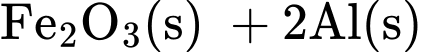
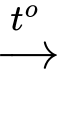
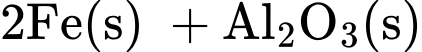
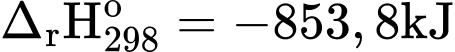
Biết
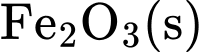 = –822,2 kJ/mol. Enthalpy tạo thành chuẩn của
= –822,2 kJ/mol. Enthalpy tạo thành chuẩn của 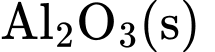 là
là
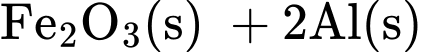
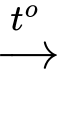
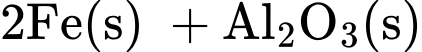
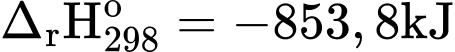
Biết

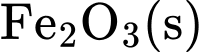 = –822,2 kJ/mol. Enthalpy tạo thành chuẩn của
= –822,2 kJ/mol. Enthalpy tạo thành chuẩn của 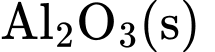 là
là A, 1676 kJ/mol.
B, –1676 kJ/mol.
C, 31,6 kJ/mol.
D, –31,6 kJ/mol.
Fe2O3(s) + 2Al(s) 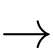 2Fe(s) + Al2O3(s)
2Fe(s) + Al2O3(s) 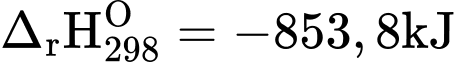
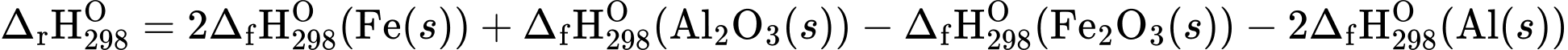
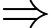
= (–822,2) + 2.0 – 2.0 + (–853,8) = –1676 kJ/mol. Đáp án: B
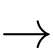 2Fe(s) + Al2O3(s)
2Fe(s) + Al2O3(s) 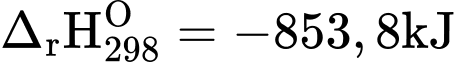
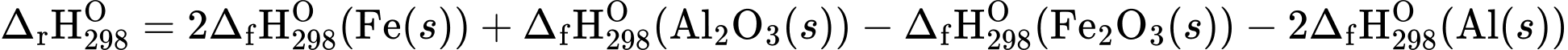
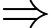
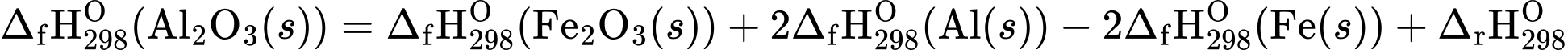
= (–822,2) + 2.0 – 2.0 + (–853,8) = –1676 kJ/mol. Đáp án: B
Câu 18 [706009]: Sơ đồ phản ứng của phản ứng giữa sodium hydroxide và sulfuric acid loãng được thể hiện như sau:
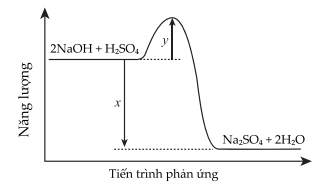
Giá trị biến thiên enthalpy của quá trình trung hòa bên trên là bao nhiêu?

Giá trị biến thiên enthalpy của quá trình trung hòa bên trên là bao nhiêu?
A, 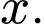
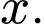
B, 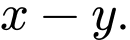
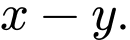
C, 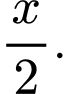
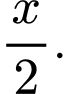
D, 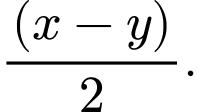
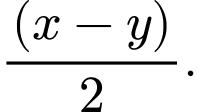
Biến thiên enthalpy của phản ứng đuơc xác định bằng hiệu số giữa tổng nhiệt tạo thành các chất sản phẩm (sp) và tổng nhiêt tạo thành của các chất đầu (cđ).
Từ sơ đồ biến thiên enthalpy của quá trình trung hòa trên là x
⇒ Chọn đáp án A Đáp án: A
Từ sơ đồ biến thiên enthalpy của quá trình trung hòa trên là x
⇒ Chọn đáp án A Đáp án: A
Câu 19 [193209]: Cho biết enthalpy tạo thành chuẩn của các chất KClO3(s) và KCl(s) là –391,2 kJ/mol và –435,9 kJ/mol. Sơ đồ biểu diễn tiến trình phản ứng: 2KClO3(s)  2KCl(s) + 3O2(g) là
2KCl(s) + 3O2(g) là
 2KCl(s) + 3O2(g) là
2KCl(s) + 3O2(g) là A, a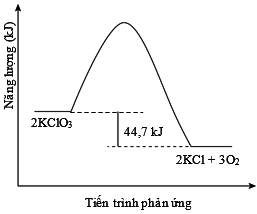

B, 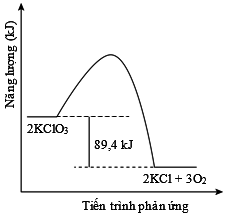

C, 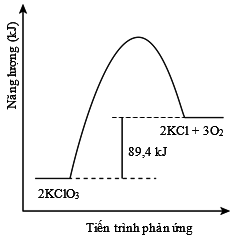

D, 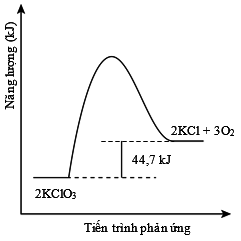

2KClO3(s)  2KCl(s) + 3O2(g)
2KCl(s) + 3O2(g) 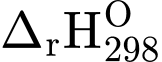 = x kJ
= x kJ
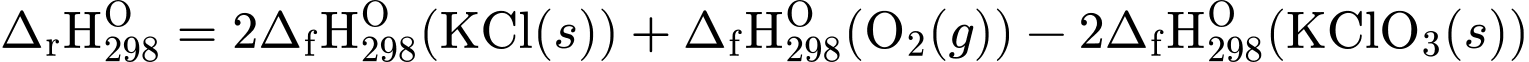
= 2.(–435,9) + 0 – 2.(–391,2) = –89,4 kJ.
Do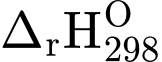 = –89,4 kJ < 0 nên tổng năng lượng của chất phản ứng lớn hơn tổng năng lượng của sản phẩm tạo thành là 89,4 kJ.
= –89,4 kJ < 0 nên tổng năng lượng của chất phản ứng lớn hơn tổng năng lượng của sản phẩm tạo thành là 89,4 kJ.
 Đáp án: B
Đáp án: B
 2KCl(s) + 3O2(g)
2KCl(s) + 3O2(g) 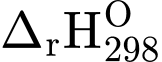 = x kJ
= x kJ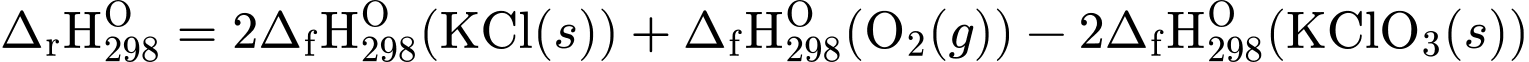
= 2.(–435,9) + 0 – 2.(–391,2) = –89,4 kJ.
Do
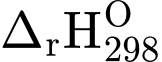 = –89,4 kJ < 0 nên tổng năng lượng của chất phản ứng lớn hơn tổng năng lượng của sản phẩm tạo thành là 89,4 kJ.
= –89,4 kJ < 0 nên tổng năng lượng của chất phản ứng lớn hơn tổng năng lượng của sản phẩm tạo thành là 89,4 kJ. Đáp án: B
Đáp án: B
Câu 20 [706143]: Quá trình chuyển hóa ammonium chloride từ dạng khan sang dạng dung dịch (bằng cách hòa tan vào nước) là một quá trình thu nhiệt.
NH4Cl(s) NH4Cl(aq);
NH4Cl(aq); 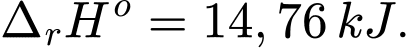
Sự giảm nhiệt độ khi phản ứng hòa tan ammonium chloride vào nước giúp nó được ứng dụng trong các túi chườm giúp giảm đau, giảm viêm một cách tạm thời. Nếu mỗi túi chườm lạnh chứa 20 gam muối và 100 mL nước cất (có D = 1 g/mL) thì khi hoạt động, nhiệt độ của túi chườm hạ xuống là t2 (oC). Biết nhiệt lượng cần để nâng nhiệt độ của 1,0 gam sản phẩm lên 1 oC là 4,184 J. Xác định giá trị của t2 (làm tròn đến hàng đơn vị).
NH4Cl(s)
 NH4Cl(aq);
NH4Cl(aq); 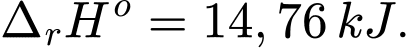
Sự giảm nhiệt độ khi phản ứng hòa tan ammonium chloride vào nước giúp nó được ứng dụng trong các túi chườm giúp giảm đau, giảm viêm một cách tạm thời. Nếu mỗi túi chườm lạnh chứa 20 gam muối và 100 mL nước cất (có D = 1 g/mL) thì khi hoạt động, nhiệt độ của túi chườm hạ xuống là t2 (oC). Biết nhiệt lượng cần để nâng nhiệt độ của 1,0 gam sản phẩm lên 1 oC là 4,184 J. Xác định giá trị của t2 (làm tròn đến hàng đơn vị).
Số mol của NH4Cl là n NH4Cl = 20 ÷ 53,5 mol
⟶ Lượng nhiệt tạo ra : 20 ÷ 53,5 × 14,76 × 1000 (J)
Nhiệt lượng NH4Cl hấp thụ khi hòa tan vào nước là:
20 ÷ 53,5 × 14,76 × 1000 = 100 × 4,184 × (t2 - 25 )
→ t2 = 11,8oC.
⟹ Điền đáp án: 12
⟶ Lượng nhiệt tạo ra : 20 ÷ 53,5 × 14,76 × 1000 (J)
Nhiệt lượng NH4Cl hấp thụ khi hòa tan vào nước là:
20 ÷ 53,5 × 14,76 × 1000 = 100 × 4,184 × (t2 - 25 )
→ t2 = 11,8oC.
⟹ Điền đáp án: 12
Câu 21 [830085]: Phương trình nhiệt của phản ứng nung vôi và đốt cháy methane như sau:
(1) CaCO3(s)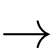 CaO(s) + CO2(s)
CaO(s) + CO2(s)
Phản ứng (2) được thực hiện để cung cấp nhiệt lượng cho phản ứng (1):
(2) CH4(g) + 2O2(g)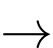 CO2(g) + 2H2O(g)
CO2(g) + 2H2O(g)
Biết nhiệt tạo thành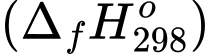 của các chất ở điều kiện chuẩn được cho trong bảng sau:
của các chất ở điều kiện chuẩn được cho trong bảng sau:
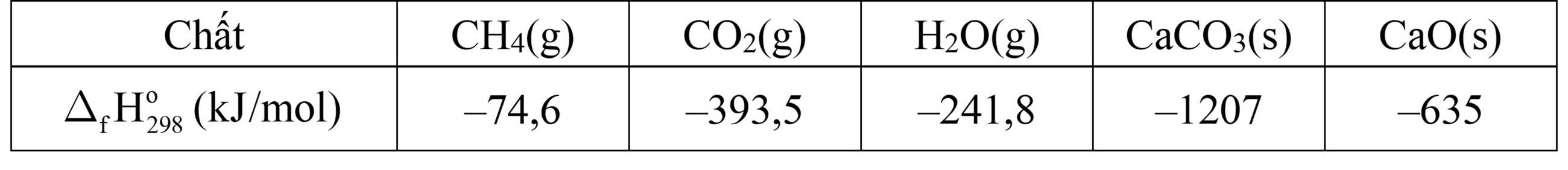
Ở điều kiện chuẩn, cần phải đốt cháy hoàn toàn bao nhiêu gam methane CH4(g) (làm tròn kết quả đến hàng phần trăm) để cung cấp nhiệt cho phản ứng tạo 1,5 mol CaO bằng cách nung CaCO3. Giả thiết hiệu suất các quá trình đều là 100%.
(1) CaCO3(s)
 CaO(s) + CO2(s)
CaO(s) + CO2(s)Phản ứng (2) được thực hiện để cung cấp nhiệt lượng cho phản ứng (1):
(2) CH4(g) + 2O2(g)
 CO2(g) + 2H2O(g)
CO2(g) + 2H2O(g) Biết nhiệt tạo thành
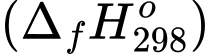 của các chất ở điều kiện chuẩn được cho trong bảng sau:
của các chất ở điều kiện chuẩn được cho trong bảng sau:
Ở điều kiện chuẩn, cần phải đốt cháy hoàn toàn bao nhiêu gam methane CH4(g) (làm tròn kết quả đến hàng phần trăm) để cung cấp nhiệt cho phản ứng tạo 1,5 mol CaO bằng cách nung CaCO3. Giả thiết hiệu suất các quá trình đều là 100%.
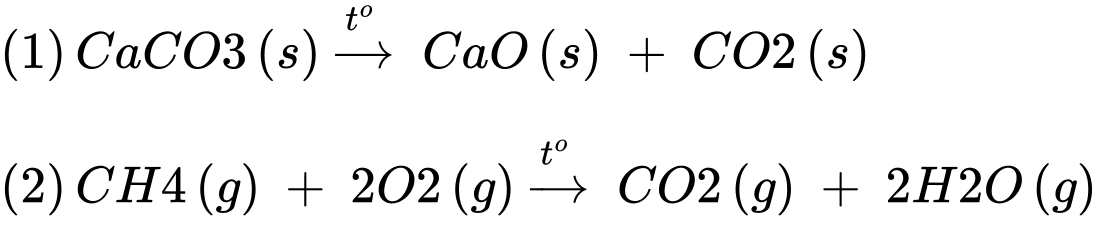
Biến thiên enthalpy của phản ứng (1) va (2) là
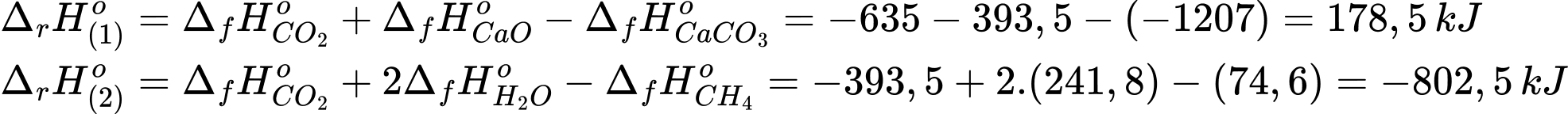
Để thu được 1 mol CaO(s) cần phải cung cấp 178,5 kJ nhiệt lượng.
Khi đốt cháy hoàn toàn 1 mol CH4 sẽ giải phóng một nhiệt lượng là 802,5 kJ
→ 1 mol CH4 sẽ cung cấp lượng nhiệt phân hủy 802,5/178,5 ≈ 4,4958 mol CaCO3 tạo ra CaO cần phải đốt cháy hoàn toàn số gam methane CH4(g) (làm tròn kết quả đến hàng phần trăm) để cung cấp nhiệt cho phản ứng tạo 1,5 mol CaO
mCH4 = 16.1,5/4,4958 = 5,34 gam
⇒ Điền đáp án: 5,34
Câu 22 [830087]: Acetylene thường được dùng làm nhiên liệu, ví dụ đèn xì oxygen - acetylene dùng để hàn cắt kim loại. Khí methane là thành phần chính của khí thiên nhiên cũng được sử dụng làm nhiên liệu. Methane và acetylene cháy theo phương trình hóa học sau:
CH4(g) + 2O2(g) → CO2(g) + 2H2O(g) (1)
2C2H2(g) + 5O2(g) → 4CO2(g) + 2H2O(g) (2)
Cho biết nhiệt tạo thành chuẩn của một số chất như sau:
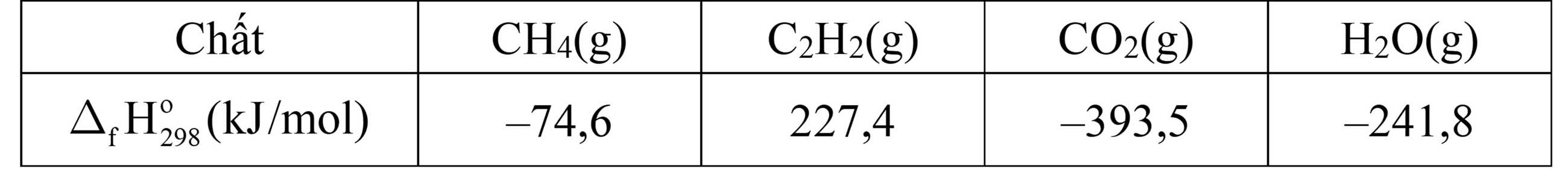
Nếu xét cùng số mol thì lượng nhiệt tỏa ra từ C2H2 gấp CH4 bao nhiêu lần (làm tròn kết quả đến hàng phần trăm)?
CH4(g) + 2O2(g) → CO2(g) + 2H2O(g) (1)
2C2H2(g) + 5O2(g) → 4CO2(g) + 2H2O(g) (2)
Cho biết nhiệt tạo thành chuẩn của một số chất như sau:

Nếu xét cùng số mol thì lượng nhiệt tỏa ra từ C2H2 gấp CH4 bao nhiêu lần (làm tròn kết quả đến hàng phần trăm)?
ΔΗ1 = ΔrΗo298 (CO2) +2ΔrΗo298(H2O) – ΔrΗo298(CH4) – 2ΔrΗo298(O2)
= - 393,5 + 2(- 241,8) - (- 74,6) - 0 = - 802,5 kJ/mol
Nhiệt lượng tỏa ra khi đốt 1 mol Methane là: - 802,5 kJ/mol
ΔΗ2 = 4ΔrΗo298(CO2) + 2ΔrΗo298(H2O) – 2ΔrΗo298 (C2H2) - 5ΔrΗo298(O2)
= 4(- 393,5) + 2(- 241,8) - 2.227,4 - 0 = - 2512,4 kJ/mol
Nhiệt lượng tỏa ra khi đốt 1mol C2H2 là: - 2512,4 : 2 = -1256,2 kJ/mol
Tỉ lệ : -1256,2 / - 802,5 = 1,5653 lần
⇒ Điền đáp án: 1,57
= - 393,5 + 2(- 241,8) - (- 74,6) - 0 = - 802,5 kJ/mol
Nhiệt lượng tỏa ra khi đốt 1 mol Methane là: - 802,5 kJ/mol
ΔΗ2 = 4ΔrΗo298(CO2) + 2ΔrΗo298(H2O) – 2ΔrΗo298 (C2H2) - 5ΔrΗo298(O2)
= 4(- 393,5) + 2(- 241,8) - 2.227,4 - 0 = - 2512,4 kJ/mol
Nhiệt lượng tỏa ra khi đốt 1mol C2H2 là: - 2512,4 : 2 = -1256,2 kJ/mol
Tỉ lệ : -1256,2 / - 802,5 = 1,5653 lần
⇒ Điền đáp án: 1,57
Câu 23 [705583]:
Khí Biogas còn gọi là khí sinh học. Thành phần chính của khí sinh học Biogas có khí methane chiếm 60% thể tích còn lại là carbon dioxide và các khí khác. Một bình gas (khí hóa lỏng) chứa hỗn hợp propane và butane với tỉ lệ mol 1 : 2. Trung bình 60 ngày một hộ gia đình cần dùng hết một bình “ga” loại 12 kg (giả thiết hiệu suất hấp thụ nhiệt các chất bằng nhau). Thể tích khí Biogas tối thiểu cần dùng để tạo ra lượng nhiệt tương đương khi đốt cháy 1 bình “ga” loại 12 kg là bao nhiêu m3 (đkc)? (Làm tròn đến hàng phần mười)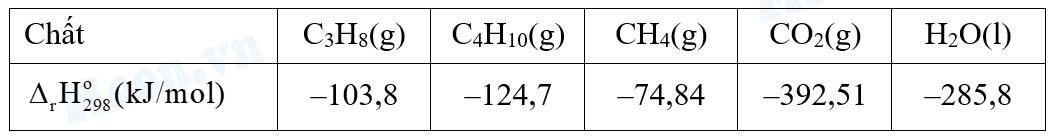
Trong 12kg có : C3H8: x mol ; C4H10 : 2x mol
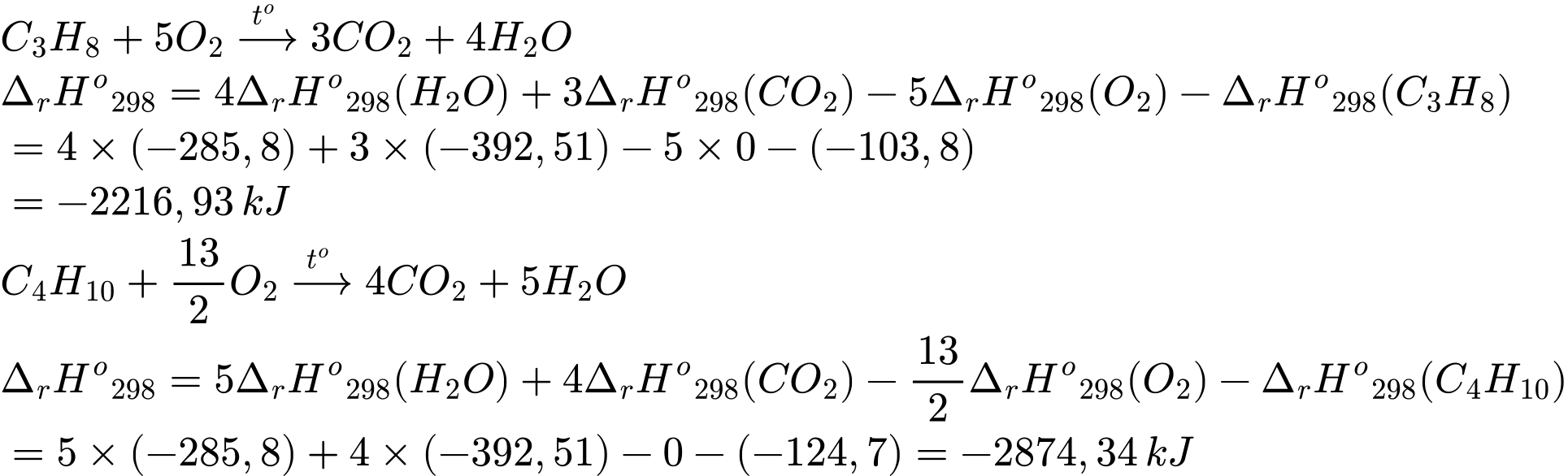
Nhiệt tỏa ra khi đốt bình ga : Q tỏa = x.(2216,93) + 2x.(2874,34) = 597420,75 kJ
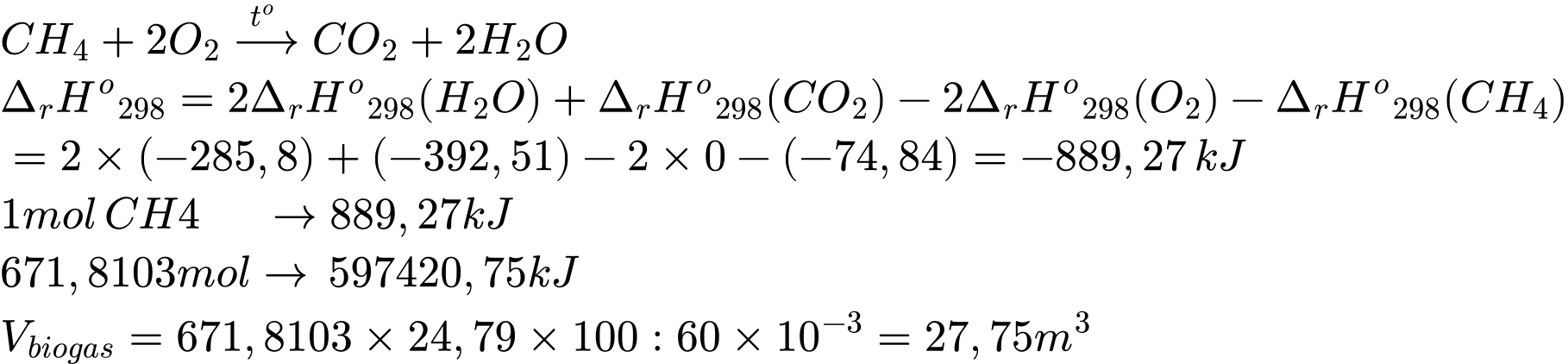
⇒ Điền đáp án: 27,8
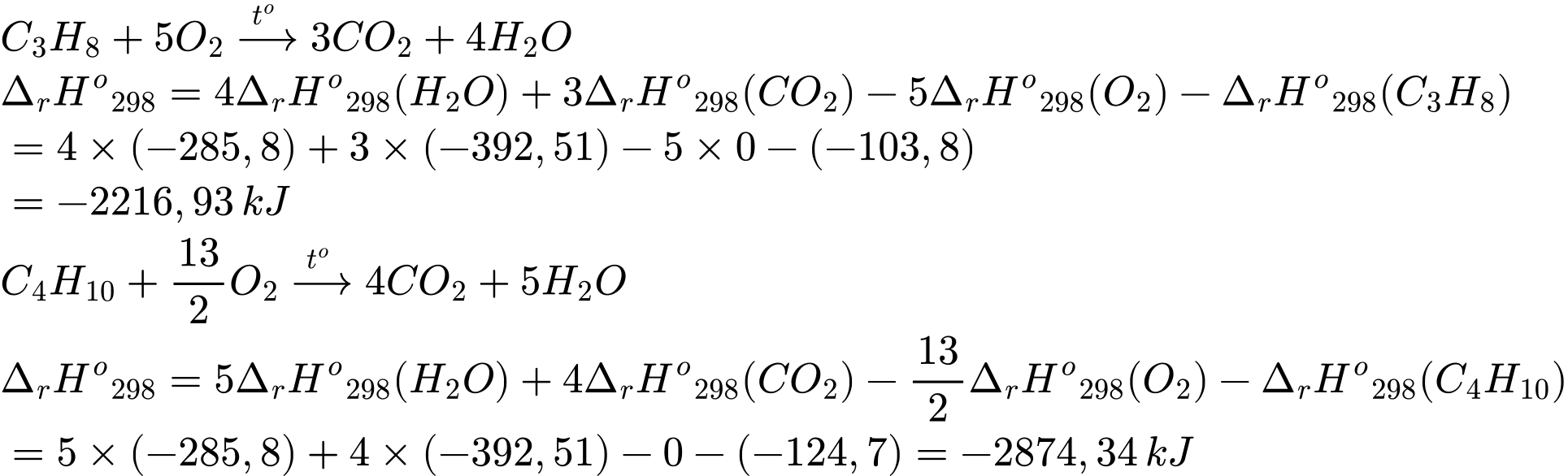
Nhiệt tỏa ra khi đốt bình ga : Q tỏa = x.(2216,93) + 2x.(2874,34) = 597420,75 kJ
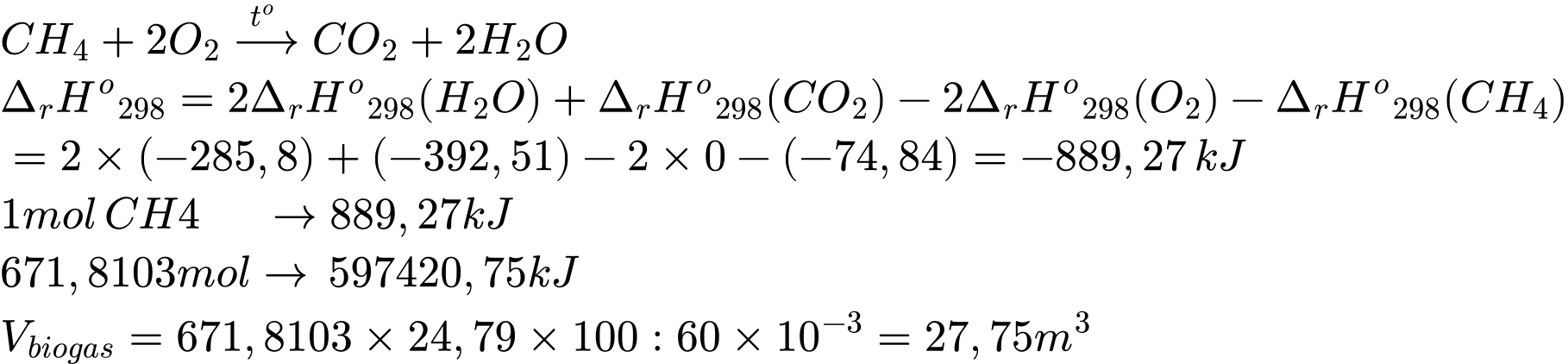
⇒ Điền đáp án: 27,8
Đọc đoạn thông tin sau và trả lời các câu hỏi từ 24 đến 26:
ENTHALPY
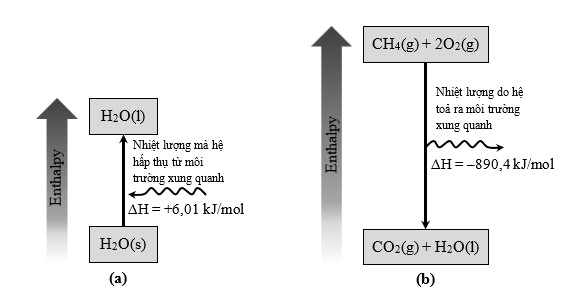
Trong điều kiện khí quyển bình thường ở mực nước biển, băng tan chảy tạo thành nước lỏng khi tiếp xúc với nhiệt độ trên 0 °C. Các phép đo cho thấy rằng cứ mỗi một mol băng chuyển thành nước lỏng trong điều kiện này thì hệ (một mol băng) hấp thụ 6,01 kJ năng lượng nhiệt.
Enthalpy (ΔH) là lượng nhiệt kèm theo của quá trình. Đây là một quá trình thu nhiệt
(ΔH > 0), vì nhiệt được băng hấp thụ từ môi trường xung quanh để chuyển thành nước lỏng [Hình (a)]. Phương trình cho sự thay đổi vật lý này là
(ΔH > 0), vì nhiệt được băng hấp thụ từ môi trường xung quanh để chuyển thành nước lỏng [Hình (a)]. Phương trình cho sự thay đổi vật lý này là
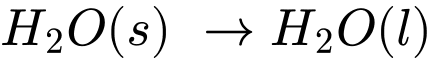
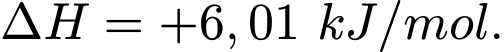
Bây giờ hãy xem xét quá trình đốt cháy khí methane (CH4), thành phần chính của khí tự nhiên:
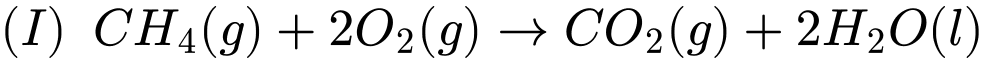
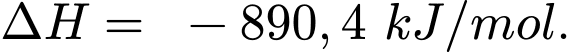
Theo những gì đã trải nghiệm, chúng ta biết rằng việc đốt khí tự nhiên sẽ thải nhiệt ra môi trường xung quanh nên đây là một quá trình tỏa nhiệt [Hình (b)]. Khi 1 mol CH4(g) phản ứng với 2 mol O2(g) tạo ra 1 mol CO2(g) và 2 mol H2O(l), 890,4 kJ nhiệt được giải phóng ra môi trường xung quanh.
Giá trị ΔH tính bằng kJ/mol không có nghĩa đây là năng lượng trên mỗi một mol của một chất phản ứng hay một chất sản phẩm cụ thể nào cả. Nó sẽ liên quan đến tất cả các chất trong một phản ứng với số lượng mol được xác định bởi các hệ số trong phương trình hóa học. Do đó, đối với quá trình đốt cháy khí methane, giá trị ΔH = −890,4 kJ/mol có thể được biểu thị theo bất kỳ cách nào sau đây:
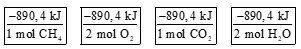
Khi viết phương trình nhiệt hóa học, chúng ta phải luôn phải xác định trạng thái vật lý của tất cả các chất phản ứng và sản phẩm, vì chúng giúp xác định sự thay đổi enthalpy thực tế. Ví dụ, trong phương trình đốt cháy khí methane, việc thay đổi sản phẩm nước ở thể lỏng thành nước ở thể hơi sẽ làm thay đổi giá trị của ΔH.
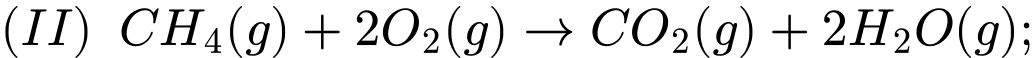
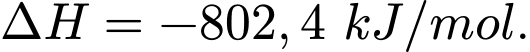
Câu 24 [382523]: Một quá trình có giá trị enthalpy âm thì quá trình đó
A, thu nhiệt.
B, tỏa nhiệt.
C, không trao đổi nhiệt.
D, có thể xảy ra.
Biến thiên enthalpy của phản ứng có giá trị âm thì phản ứng là phản ứng tỏa nhiệt. Biến thiên enthalpy càng âm, phản ứng tỏa ra càng nhiều nhiệt.
⇒ Chọn đáp án B Đáp án: B
⇒ Chọn đáp án B Đáp án: B
Câu 25 [382524]: Dựa vào các giá trị enthalpy của phương trình (I) và (II), xác định giá trị enthalpy của quá trình sau:
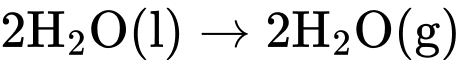
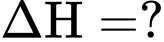
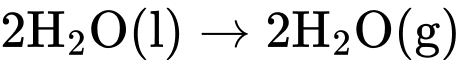
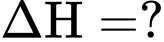
A, +44.0 kJ/mol.
B, +88.0 kJ/mol.
C, –68.0 kJ/mol.
D, –50.0 kJ/mol.
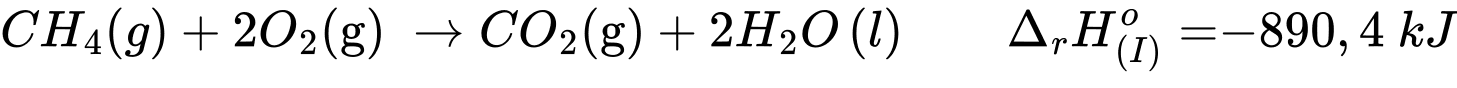
→ Khi đảo ngược lại phải ứng
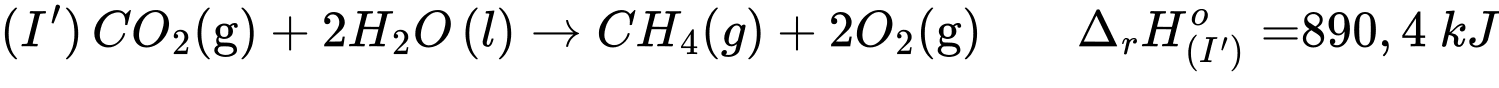
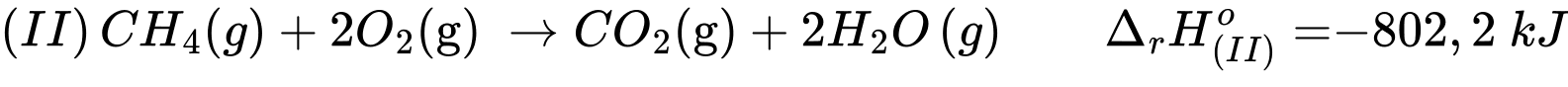
Ta có: Khi phương trình (I) + (II)
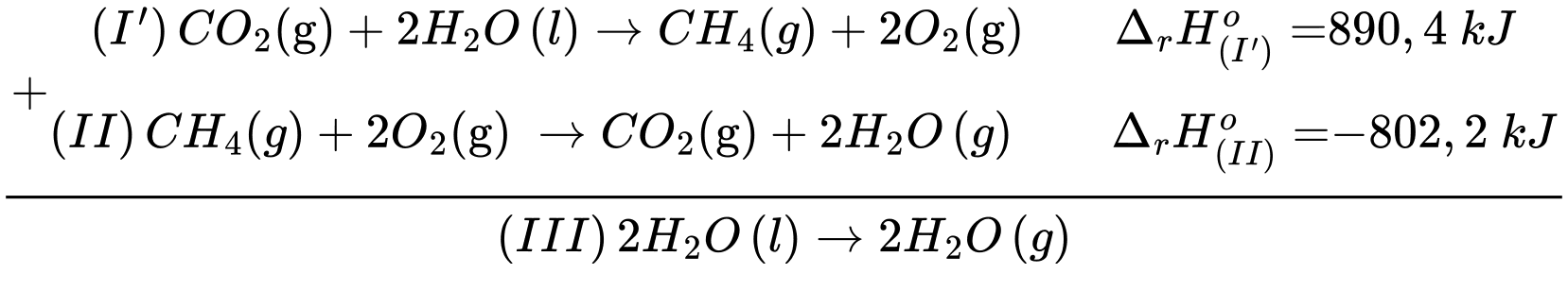
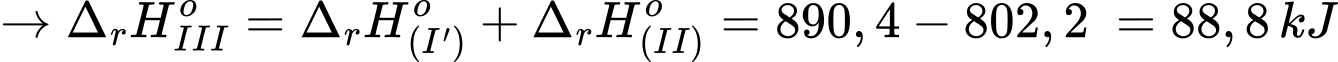
⇒ Chọn đáp án B Đáp án: B
Câu 26 [382525]: Cho sơ đồ thể hiện các chất trong hệ trước và sau phản ứng của hai quá trình hóa học liên quan như sau:
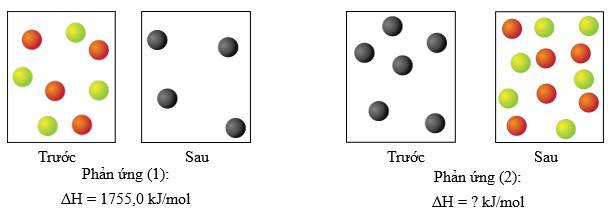
Cho biết ΔH của phản ứng đầu tiên là 1755,0 kJ/mol. Giá trị ∆H của phản ứng thứ hai là

Cho biết ΔH của phản ứng đầu tiên là 1755,0 kJ/mol. Giá trị ∆H của phản ứng thứ hai là
A, +2452.3 kJ/mol.
B, +1569.6 kJ/mol.
C, –4263,0 kJ/mol.
D, –2632.5 kJ/mol.
Phản ứng (1) ngược lại so với phản ứng (2) → phản ứng số (2) là phản ứng tỏa nhiệt
Số phân tử của phản ứng số (2) gấp 1,5 lần số phân tử của phản ứng số (1)
→ Biến thiên enthalpy của phản ứng số (2) là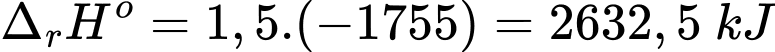
⇒ Chọn đáp án D Đáp án: D
Số phân tử của phản ứng số (2) gấp 1,5 lần số phân tử của phản ứng số (1)
→ Biến thiên enthalpy của phản ứng số (2) là
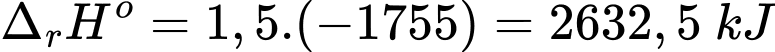
⇒ Chọn đáp án D Đáp án: D