
Nước nhận nhiệt từ nguồn nóng (bếp, điện trở...) và nhiệt độ tăng từ 20°C → 100°C.
Nếu tiếp tục đun cho nước bay hơi, entropy còn tăng mạnh hơn do sự chuyển pha Đáp án: A
Entropy của quá trình hoà tan này sẽ có xu hướng
Khi hòa tan, các ion phân tán trong dung môi, trạng thái trở nên hỗn loạn hơn, số vi trạng thái tăng.
→ Entropy của hệ (ion + nước) tăng.
➔ Đáp án đúng: A. Tăng lên. Đáp án: A
Ta biết rằng entropy
(S) phản ánh mức độ hỗn loạn hay mức độ tự do chuyển động của các
hạt.
CO₂ (s): trật tự cao nhất
(rắn, sắp xếp cố định) → entropy nhỏ nhất.
CO₂ (l): trật tự giảm (các
phân tử chuyển động linh hoạt hơn) → entropy lớn hơn.
CO₂ (g): hỗn loạn cao nhất
→ entropy lớn nhất.
Đáp án đúng: A. CO2(s)
< CO2(l) < CO2(g).
(1) CaCO3(s) → CO2(g) + CaO(s)
(2) CH4(g) + 2O2(g) → CO2(g) + 2H2O(l)
(3) 2SO2(g) + O2(g) → 2SO3(g)
Các phản ứng có giá trị biến thiên entropy chuẩn nhỏ hơn 0 là
Các phản ứng có giá trị biến thiên entropy chuẩn nhỏ hơn 0 là:
(1) CaCO3(s)
 CO2(g) + CaO(s)
CO2(g) + CaO(s)Sau phản ứng sinh ra chất khí, độ hỗn loạn tăng lên. → ΔS° > 0
(2) CH4(g) + 2O2(g)
 CO2(g) + 2H2O(l)
CO2(g) + 2H2O(l)Sau phản ứng số mol khí giảm mạnh, đồng thời xuất hiện pha lỏng (trật tự hơn) → ΔS° < 0
(3) 2SO2(g) + O2(g)
 2SO3(g)
2SO3(g)Trước: 3 mol khí. Sau: 2 mol khí
⇒ Số mol khí giảm ⇒ entropy giảm
Đáp án: C. (2) và (3). Đáp án: C
a) Bỏ nước và propanol thu được dung dịch propanol.
b) Hòa tan đường vào nước thu được dung dịch đường.
c) Đun nóng tinh thể NaCl.
d) Đun nóng Br2 lỏng.
Có bao nhiêu quá trình làm entropy của hệ tăng?
Nhận định (b) - Chất rắn (đường) tan ra → các phân tử đường phân tán trong nước → trật tự giảm, entropy tăng.→ ΔS > 0
Nhận định (c) - Tinh thể rắn được đun nóng → dao động mạnh hơn, nhưng chưa tan chảy (nếu chưa nóng chảy thì cấu trúc vẫn trật tự).→ Nếu chỉ “đun nóng” mà không nóng chảy, entropy tăng rất ít, nhưng vẫn tăng vì nhiệt độ tăng.→ ΔS > 0
Nhận định (d) - Khi nhiệt độ tăng, Br₂(l) có thể bay hơi một phần → chuyển dần sang khí, hỗn loạn tăng mạnh. → ΔS > 0
Đáp án đúng: D. 4 Đáp án: D
(a) 2NO(g) + O2(g) → 2NO2(g)
(b) H2(g) + Cl2(g) → 2HCl(g)
(c) CaCO3(s) → CaO(s) + CO2(g)
(d) H2O(l) → H2O(g)
Có bao nhiêu phản ứng có
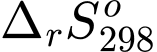 mang giá trị dương?
mang giá trị dương? (a) 2NO(g) + O2(g)
 2NO2(g)
2NO2(g)Sau phản ứng số mol khí giảm, giá trị entropy giảm ΔS° < 0
(b) H2(g) + Cl2(g)
 2HCl(g)
2HCl(g) Sau phản ứng số mol khí không thay đổi, giá trị entropy gần như không đổi.
(c) CaCO3(s)
 CaO(s) + CO2(g)
CaO(s) + CO2(g) Sau phản ứng sinh ra chất khí, độ hỗn loạn tăng lên. → ΔS° > 0
(d) H2O(l)
 H2O(g)
H2O(g)Sau phản ứng chuyển đổi trạng thái lỏng sang trạng thái khí, giá trị entropy tăng lên → ΔS° > 0
Đáp án: B. 2. Đáp án: B
a) C(s) + CO2(g) → 2CO(g)
b) CO(g) + 1/2O2(g) → CO2(g)
c) H2(g) + Cl2(g) → 2HCl(g)
d) S(s) + O2(g) → SO2(g)
e) Zn(s) + 2HCl(aq) → ZnCl2(aq) + H2(g)
Số phản ứng có giá trị ∆S ≈ 0 là bao nhiêu?
 2CO(g)
2CO(g)Sau phản ứng sinh ra nhiều mol khí hơn, giá trị entropy tăng lên → ΔS° > 0
b) CO(g) + 1/2O2(g)
 CO2(g)
CO2(g)Sau phản ứng số mol khí giảm, giá trị entropy giảm ΔS° < 0
c) H2(g) + Cl2(g)
 2HCl(g)
2HCl(g)Sau phản ứng số mol khí không thay đổi, giá trị entropy gần như không đổi.
d) S(s) + O2(g)
 SO2(g)
SO2(g)Sau phản ứng số mol khí không thay đổi, giá trị entropy gần như không đổi.
e) Zn(s) + 2HCl(aq)
 ZnCl2(aq) + H2(g)
ZnCl2(aq) + H2(g)Sau phản ứng sinh ra chất khí, độ hỗn loạn tăng lên. → ΔS° > 0
Đáp án: B. 2. Đáp án: B
Khi trộn hai dung dịch muối NaCl và KNO₃ loãng với nhau, các ion trong
mỗi dung dịch như Na⁺, Cl⁻, K⁺ và NO₃⁻ sẽ hòa trộn và phân tán đều trong cùng một
dung môi. Trước khi trộn, mỗi dung dịch chỉ chứa một loại cặp ion riêng biệt,
nhưng sau khi trộn, các ion này có thể tự do chuyển động và sắp xếp lẫn lộn với
nhau theo nhiều cách khác nhau. Do số trạng thái vi mô có thể có của hệ tăng
lên, mức độ hỗn loạn của hệ cũng tăng, dẫn đến entropy của hệ tăng. Vì vậy, quá
trình trộn hai dung dịch này là quá trình có biến thiên entropy dương (ΔS
> 0).
Đáp án đúng: B. Entropy tăng vì các ion phân tán hỗn loạn hơn.
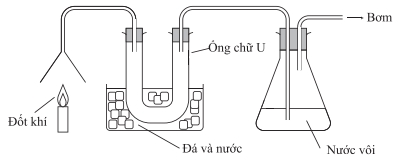
Entropy của quá trình xảy ra trong ống chữ U thay đổi như thế nào?
Khi đốt nến sinh ra khí CO2 và hơi nước. Khi hỗn hợp CO2 và hơi nước điqua ống chữ U bên dưới có đá và nước nhận thấy rằng Entropy của quá trình xảyra trong ống chữ U giảm xuống nguyên do khi giảm nhiệt độ sẽ ngưng tụ hơi nước.
Đáp án: B. Giảm.
I2(s) →I2(g)
Entropy của quá trình này thay đổi như nào?
- Khi đun nóng iodine (I2) sẽ xuất hiện sự thăng hoa của iodine. I2(s)  I2(g)
I2(g)
- Iodine thay đổi trạng thái từ rắn sang trạng thái khí, entropy của hệ
tăng lên.
- Trong trạng thái rắn,
các phân tử I₂ sắp xếp có trật tự cao, dao động quanh vị trí cố định. Khi chuyển
sang khí, các phân tử chuyển động tự do, phân tán rộng khắp không
gian, trật tự giảm mạnh, mức độ hỗn loạn tăng lên rõ rệt.→ Số vi trạng thái tăng, nên entropy tăng đáng kể.
Đáp án: D. Tăng do ở thế rắn iodine có độ hỗn loạn ít hơn so với
thể khí
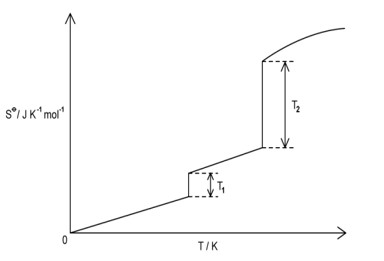
Tại sao sự thay đổi entropy ở T2 (quá trình bay hơi) lại lớn hơn so với ở T1 (quá trình nóng chảy)?
Sự thay đổi entropy ở
T2 (quá trình bay hơi) lại lớn hơn so với ở T1 (quá trình nóng chảy) nguyên do
sự chuyển từ chất lỏng sang chất khí làm độ hỗn loạn của hệ tăng nhiều hơn so với
chuyển từ rắn sang lỏng.
Đáp án: B. Vì sự
chuyển từ chất lỏng sang chất khí làm độ hỗn loạn của hệ tăng nhiều hơn so với
chuyển từ rắn sang lỏng.
- Hòa tan NaOH rắn
vào nước: NaOH rắn có cấu trúc tinh thể rất gọn. Khi
hòa tan, các ion Na+ và OH- tự do di chuyển trong dung dịch. Tức là tăng độ hỗn
loạn của hệ, do đó ∆S > 0.
- Nung nóng chảy khối kim
loại đồng: Kim loại rắn có mạng tinh thể cố định.
Khi tan chảy thành lỏng, các nguyên tử có thể di chuyển tự do hơn, nhưng vẫn
còn tương tác giữa các nguyên tử. Entropy tăng, nhưng không bằng khi chuyển rắn
→ khí ∆S > 0.
- Đốt cháy khí butane: Số phân tử tăng và sản phẩm chủ yếu là khí, chuyển từ dạng ít
phân tán (butane + O2) sang nhiều phân tử khí, tăng mức độ hỗn loạn.
Entropy tăng ∆S > 0.
Đáp án: D. cả A, B và C.
H2O(l) → H2O(g)
biết entropy tạo thành chuẩn của H2O(l) là 70,0 (J/mol.K); H2O(g) là 188,7 (J/mol.K).
Biến thiên entroly của
quá trình trên là:
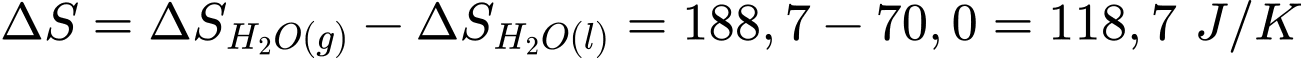
Đáp án: D. 118,7
J/K.
2H2(g) + O2(g) → 2H2O(g)
biết entropy tạo thành chuẩn của H2(g) là 130,7 (J/mol.K); O2(g) là 205,2 (J/mol.K); H2O(g) là 188,7 (J/mol.K).
Biến thiên entroly của
quá trình trên là:
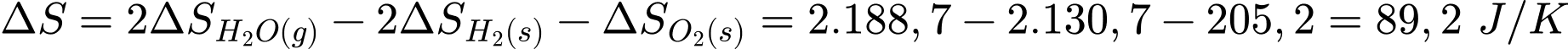
Đáp án: C. –89,2
J/K.
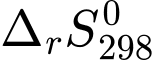 của phản ứng đốt cháy CH3OH sinh ra CO2 và H2O.
của phản ứng đốt cháy CH3OH sinh ra CO2 và H2O.CH3OH(l) + 1,5O2(g) → CO2(g) + 2H2O(l)
Cho biết entropy chuẩn của H2O(l), CO2(g), CH3OH(l) và O2(g) lần lượt bằng 69,94; 213,6; 126,8 và 205 J/mol.K.
CH3OH(l) +1,5O2(g) 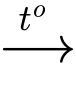 CO2(g) + 2H2O(l)
CO2(g) + 2H2O(l)
Biến thiên entroly củaquá trình trên là
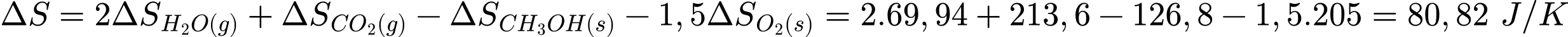
Đáp án đúng là A
4FeS2(s) + 11O2(g) → 2Fe2O3(s) + 8SO2(g);
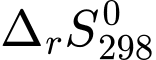 = –307 J/mol.K
= –307 J/mol.KBiết entropy chuẩn của SO2(khí), Fe2O3(rắn) và O2(khí) lần lượt là 248,1; 87,4 và 205 J/mol.K. Entropy chuẩn của FeS2(rắn) là
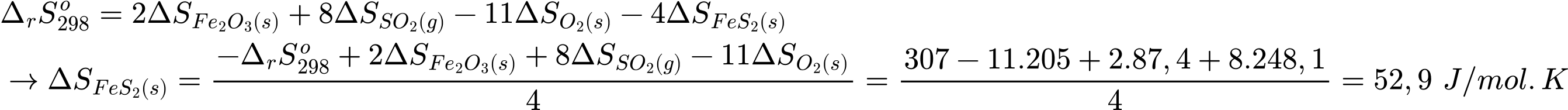
Đáp án: D. 52,9 J/mol.K. Đáp án: D
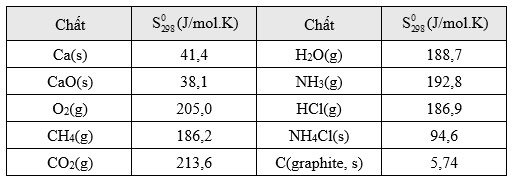
Quá trình nào sau đây có giá trị biến thiên entropy chuẩn của phản ứng là nhỏ nhất?
Biến thiên entroly của quá trình trên là:
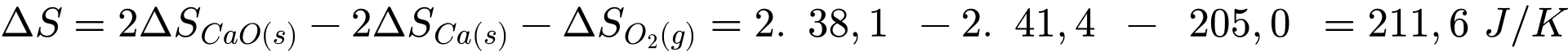
B. NH3(g) + HCl(g) →NH4Cl(s).
Biến thiên entroly của quá trình trên là:
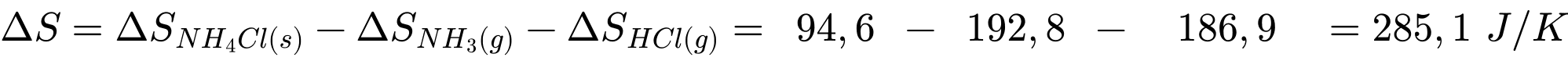
C. C(graphite, s) + O2(g) →2CO2(g).
Biến thiên entroly của quá trình trên là:
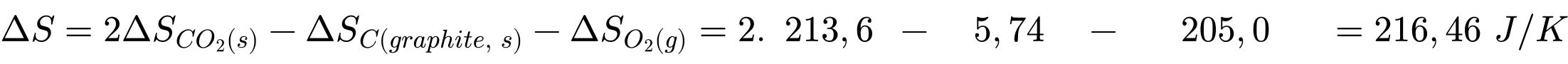
D. CH4(g) + 2O2(g) → CO2(g) + 2H2O(g).
Biến thiên entroly của quá trình trên là:
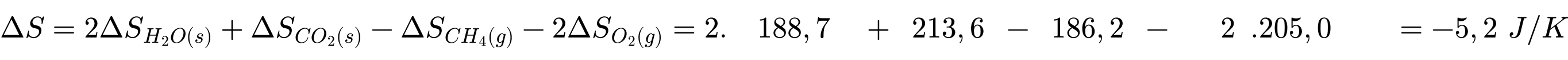
Đáp án: B. NH3(g) + HCl(g) →NH4Cl(s). Đáp án: B
Đọc đoạn thông tin sau và trả lời các câu hỏi từ 18 đến 20:
- ΔSo > 0: Mức độ hỗn loạn của hệ tăng.
- ΔSo < 0: Mức độ hỗn loạn của hệ giảm.
Để nghiên cứu sự biến đổi giá trị entropy tiêu chuẩn (ΔSo) của một phản ứng, tiến hành thí nghiệm như sau: Nung một mẫu khí SiH4 ở nhiệt độ cao, lúc này SiH4 bị phân hủy tạo thành silicon rắn và khí hydrogen.
SiH4(khí) → Si(rắn) + 2H2(khí)
(*) Bảng dưới đây cho biết giá trị entropy tiêu chuẩn của các chất.

SiH4(khí)
 Si(rắn) + 2H2(khí)
Si(rắn) + 2H2(khí)=> 1 mol SiH4 tạo 2 mol H2
Đáp án đúng là A Đáp án: A
Mức độ hỗn loạn của hệ (hay còn gọi là độ hỗn loạn, entropy – S) phụ thuộc vào số cách sắp xếp vi mô mà các hạt có thể có. Khi số mol chất khí tăng, nghĩa là số lượng phân tử khí tăng, các hạt có nhiều cách phân bố trong không gian hơn, do đó entropy (độ hỗn loạn) tăng.
→ Mức độ hỗn loạn của hệ càng lớn. Đáp án: A
 Si(rắn) + 2H2(khí) (*)
Si(rắn) + 2H2(khí) (*)Xác định giá trị biến thiên entropy của phản ứng (*)
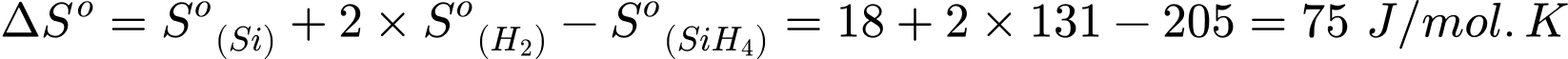
Sau phản ứng số mol khí tăng, mức độ hỗn loạn của hệ tăng.
Đáp án: A. ΔSo = 75 J/mol.K và mức độ hỗn loạn của hệ tăng. Đáp án: A