Câu 1 [1073590]: Biến thiên năng lượng của Gibbs có thể được tính theo biểu thức nào dưới đây?
A, ΔG = Τ × ΔΗ – ΔS.
B, ΔG = ΔS – Τ × ΔΗ.
C, ΔG = ΔH – T × ΔS.
D, ΔG = T × ΔS – ΔH.
Biến thiên năng lượng của Gibbs có thể được tính theo biểu thức
ΔG = ΔH – T × ΔS.
Đáp án: C. ΔG = ΔH – T × ΔS. Đáp án: C
ΔG = ΔH – T × ΔS.
Đáp án: C. ΔG = ΔH – T × ΔS. Đáp án: C
Câu 2 [1073591]: Ethene được sản xuất theo phương pháp tổng hợp pha khí sau:
2C(s) + 2H2(g) →C2H4(g)
Phản ứng trên có ∆H = a (kJ/mol); ∆S = b (J/mol.K). Biến thiên năng lượng tự do Gibbs tại 298 K được tính theo công thức nào sau đây?
2C(s) + 2H2(g) →C2H4(g)
Phản ứng trên có ∆H = a (kJ/mol); ∆S = b (J/mol.K). Biến thiên năng lượng tự do Gibbs tại 298 K được tính theo công thức nào sau đây?
A, ∆G = a – 298 × b (kJ/mol).
B, ∆G = a – 0,298 × b (kJ/mol).
C, ∆G = 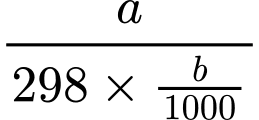 (kJ/mol).
(kJ/mol).
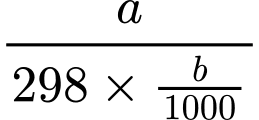 (kJ/mol).
(kJ/mol).D, ∆G = 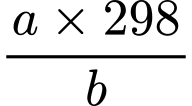 (kJ/mol).
(kJ/mol).
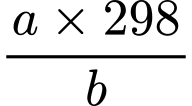 (kJ/mol).
(kJ/mol).
Ethene được sản xuất theo phương pháp tổng hợp pha khí sau:
2C(s) + 2H2(g) → C2H4(g)
Biến thiên năng lượng tự do Gibbs tại 298 K là:
∆G = a – 0,298×b (kJ/mol)
Đáp án: A. ∆G = a – 0,298×b (kJ/mol)
Đáp án: B
2C(s) + 2H2(g) → C2H4(g)
Biến thiên năng lượng tự do Gibbs tại 298 K là:
∆G = a – 0,298×b (kJ/mol)
Đáp án: A. ∆G = a – 0,298×b (kJ/mol)
Đáp án: B
Câu 3 [1073592]: Cho phản ứng hóa học sau xảy ra ở 25 °C:
SnCl4(l) + 2H2O(l) → SnO2(s) + 4HCl(g)
Biết phản ứng có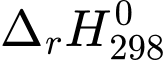 = 133,0 kJ;
= 133,0 kJ; 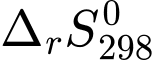 = 401,5 J/K. Xác định giá trị biến thiên năng lượng tự do Gibbs (
= 401,5 J/K. Xác định giá trị biến thiên năng lượng tự do Gibbs (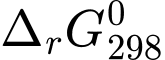 ) của phản ứng trên.
) của phản ứng trên.
SnCl4(l) + 2H2O(l) → SnO2(s) + 4HCl(g)
Biết phản ứng có
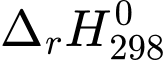 = 133,0 kJ;
= 133,0 kJ; 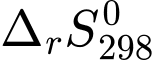 = 401,5 J/K. Xác định giá trị biến thiên năng lượng tự do Gibbs (
= 401,5 J/K. Xác định giá trị biến thiên năng lượng tự do Gibbs (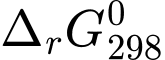 ) của phản ứng trên.
) của phản ứng trên. A, –252,6 kJ.
B, –13,4 kJ.
C, 13,4 kJ.
D, 252,6 kJ.
Cho phản ứng hoá học sau xảy ra ở 25 °C: SnCl4(l) + 2H2O(l) → SnO2(s) + 4HCl(g)
giá trị biến thiên năng lượng tự do Gibbs của phản ứng trên là:
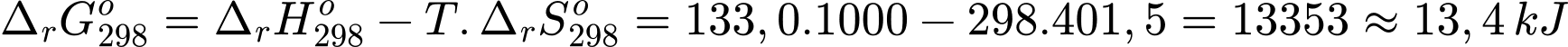
Đáp án: C. 13,4 kJ. Đáp án: C
giá trị biến thiên năng lượng tự do Gibbs của phản ứng trên là:
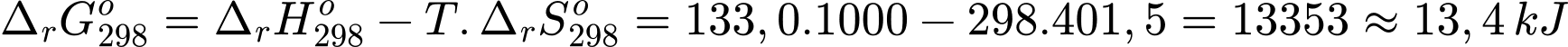
Đáp án: C. 13,4 kJ. Đáp án: C
Câu 4 [1073593]: Người ta nghiên cứu phản ứng phân huỷ calcium carbonate:
CaCO3(s) → CaO(s) + CO2(g)
Tại 25 oC phản ứng hầu như không xảy ra nhưng khi nung đến 900 oC thì phản ứng xảy ra mạnh mẽ. Biết phản ứng có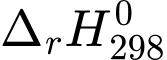 = 178 (kJ/mol) và
= 178 (kJ/mol) và 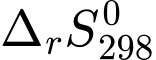 = 160 (J/mol.K). Biến thiên năng lượng tự do Gibbs tại 25 oC và 900 oC lần lượt là
= 160 (J/mol.K). Biến thiên năng lượng tự do Gibbs tại 25 oC và 900 oC lần lượt là
CaCO3(s) → CaO(s) + CO2(g)
Tại 25 oC phản ứng hầu như không xảy ra nhưng khi nung đến 900 oC thì phản ứng xảy ra mạnh mẽ. Biết phản ứng có
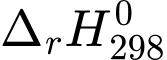 = 178 (kJ/mol) và
= 178 (kJ/mol) và 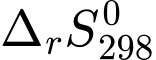 = 160 (J/mol.K). Biến thiên năng lượng tự do Gibbs tại 25 oC và 900 oC lần lượt là
= 160 (J/mol.K). Biến thiên năng lượng tự do Gibbs tại 25 oC và 900 oC lần lượt là A, 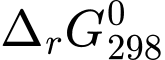 = 130,32 (kJ/mol) và
= 130,32 (kJ/mol) và 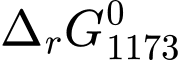 = –9,68 (kJ/mol).
= –9,68 (kJ/mol).
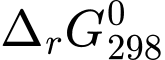 = 130,32 (kJ/mol) và
= 130,32 (kJ/mol) và 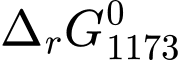 = –9,68 (kJ/mol).
= –9,68 (kJ/mol).B, 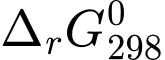 = –130,32 (kJ/mol) và
= –130,32 (kJ/mol) và 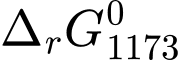 = 9,68 (kJ/mol).
= 9,68 (kJ/mol).
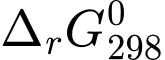 = –130,32 (kJ/mol) và
= –130,32 (kJ/mol) và 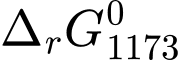 = 9,68 (kJ/mol).
= 9,68 (kJ/mol).C, 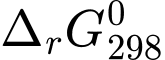 = 30,32 (kJ/mol) và
= 30,32 (kJ/mol) và 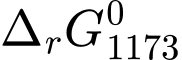 = –19,68 (kJ/mol).
= –19,68 (kJ/mol).
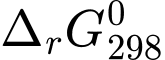 = 30,32 (kJ/mol) và
= 30,32 (kJ/mol) và 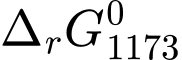 = –19,68 (kJ/mol).
= –19,68 (kJ/mol).D, 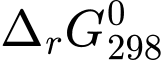 = –30,32 (kJ/mol) và
= –30,32 (kJ/mol) và 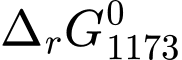 = 19,68 (kJ/mol).
= 19,68 (kJ/mol).
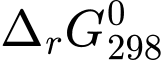 = –30,32 (kJ/mol) và
= –30,32 (kJ/mol) và 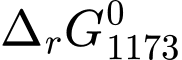 = 19,68 (kJ/mol).
= 19,68 (kJ/mol).
Đổi 25oC = 298 K; 900oC = 1173 oK
Biến thiên năng lượng tự do Gibbs tại 25oC và 900oC lần lượt là:
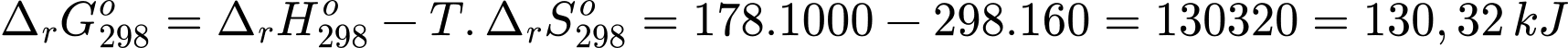
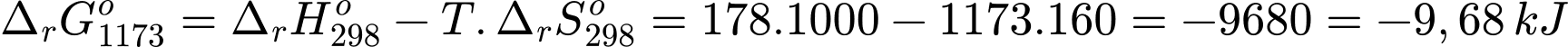
Đáp án: A.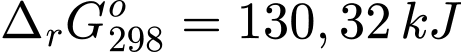 và
và 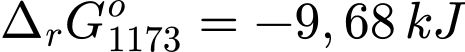 Đáp án: A
Đáp án: A
Biến thiên năng lượng tự do Gibbs tại 25oC và 900oC lần lượt là:
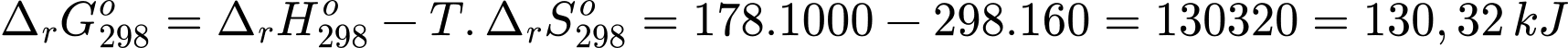
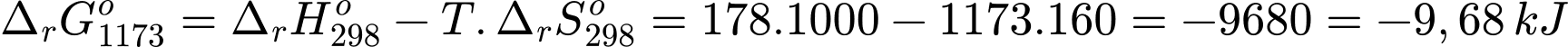
Đáp án: A.
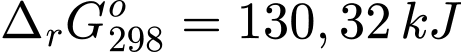 và
và 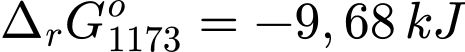 Đáp án: A
Đáp án: A
Câu 5 [1073594]: Hydrochloric acid (HCl) phản ứng với sodium hydroxide (NaOH) tạo thành sodium chloride (NaCl) và nước. Biết 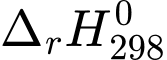 = - 56,13 kJ/mol;
= - 56,13 kJ/mol; 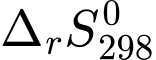 = 79,11 J/mol.K. Cho các phát biểu sau:
= 79,11 J/mol.K. Cho các phát biểu sau:
(1) Phản ứng trên là phản ứng tỏa nhiệt.
(2) Ở nhiệt độ 20 °C, phản ứng trên có AG = –79,31 kJ/mol.
(3) Phản ứng tự xảy ra ở 25 °C.
Các phát biểu đúng là
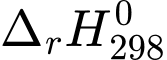 = - 56,13 kJ/mol;
= - 56,13 kJ/mol; 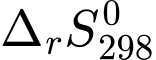 = 79,11 J/mol.K. Cho các phát biểu sau:
= 79,11 J/mol.K. Cho các phát biểu sau: (1) Phản ứng trên là phản ứng tỏa nhiệt.
(2) Ở nhiệt độ 20 °C, phản ứng trên có AG = –79,31 kJ/mol.
(3) Phản ứng tự xảy ra ở 25 °C.
Các phát biểu đúng là
A, chỉ (1).
B, chỉ (1) và (3).
C, chỉ (1) và (2).
D, cả (1), (2) và (3).
Nhận định (1) – Đúng. Phản ứng trên là phản ứng thu nhiệt với giá trị
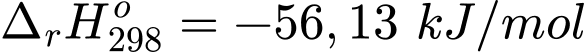
Nhận định (2) – Đúng. Đổi 20oC = 293 oK
Biến thiên năng lượng tự do Gibbs là:
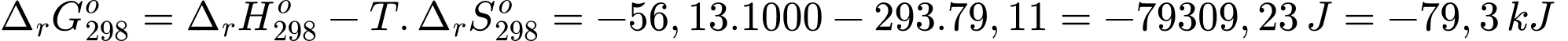
Nhận định (3) – Đúng.
Đổi 25oC = 298 K
Biến thiên năng lượng tự do Gibbs là:
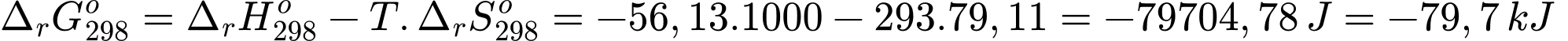
Phản ứng tự xảy ra
Đáp án: D. cả (1), (2) và (3). Đáp án: D
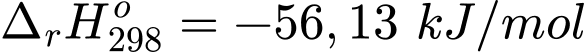
Nhận định (2) – Đúng. Đổi 20oC = 293 oK
Biến thiên năng lượng tự do Gibbs là:
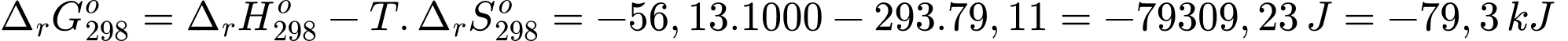
Nhận định (3) – Đúng.
Đổi 25oC = 298 K
Biến thiên năng lượng tự do Gibbs là:
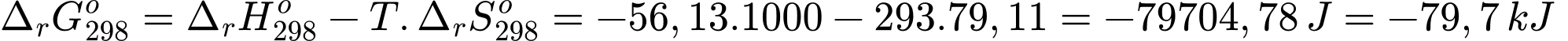
Phản ứng tự xảy ra
Đáp án: D. cả (1), (2) và (3). Đáp án: D
Câu 6 [1073595]: Một phản ứng hóa học có ∆rHo = 119 kJ và ∆rSo = 263 J/K. Ở nhiệt độ nào sau đây thì phản ứng trên tự xảy ra?
A, 500 K.
B, 382 K.
C, 363 K.
D, 200 K.
Ta có:
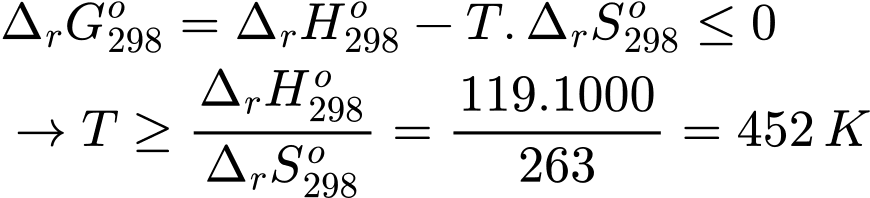
Ở nhiệt độ 500 K thì phản ứng trên tự xảy ra
Đáp án: A. 500 K Đáp án: A
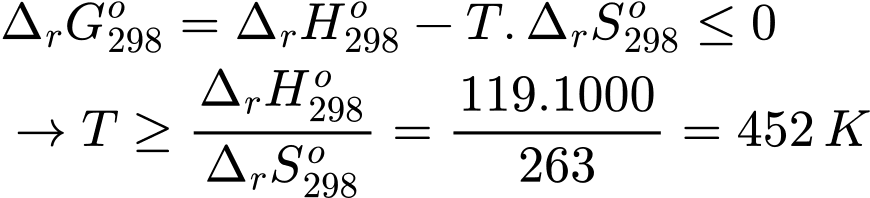
Ở nhiệt độ 500 K thì phản ứng trên tự xảy ra
Đáp án: A. 500 K Đáp án: A
Câu 7 [1073596]: Một phản ứng thu nhiệt và không xảy ra ở một điều kiện xác định. Ở điều kiện đó, mệnh đề nào sau đây đúng?
A, ∆S > 0.
B, ∆H > 0.
C, ∆G = 0.
D, ∆S < 0.
ΔG = ΔH – T × ΔS với AH > 0 thì ΔS < 0 thì giá trị trị ΔG sẽ luôn dương, phản ứng không tự xảy ra.
Đáp án đúng là: D. ∆S < 0. Đáp án: D
Đáp án đúng là: D. ∆S < 0. Đáp án: D
Câu 8 [1073597]: Phản ứng luôn tự diễn biến có đặc điểm nào sau đây?
A, Phản ứng vừa toả nhiệt (∆H < 0), vừa làm giảm độ hỗn loạn của hệ (∆S < 0).
B, Phản ứng vừa thu nhiệt (∆H > 0), vừa làm hệ hỗn loạn hơn (∆S > 0).
C, Phản ứng vừa toả nhiệt (∆H < 0), vừa làm hệ hỗn loạn hơn (∆S > 0).
D, Phản ứng vừa thu nhiệt (∆H > 0), vừa làm giảm độ hỗn loạn của hệ (∆S < 0).
Để xác định phản ứng luôn tự diễn biến, ta phải xét năng lượng Gibbs tự do (∆G)
Nhận định A. Phản ứng vừa toả nhiệt (∆H < 0), vừa làm giảm độ hỗn loạn của hệ (∆S < 0).
ΔG = ΔH – T × ΔS → ∆G có thể dương hoặc âm tùy T → Không luôn tự phát.
Nhận định B. Phản ứng vừa thu nhiệt (∆H > 0), vừa làm hệ hỗn loạn hơn (∆S > 0).
ΔG = ΔH – T × ΔS → ∆G có thể dương hoặc âm tùy T → Không luôn tự phát.
Nhận định C. Phản ứng vừa toả nhiệt (∆H < 0), vừa làm hệ hỗn loạn hơn (∆S > 0).
ΔG = ΔH – T × ΔS → luôn âm, phản ứng luôn tự phát.
Nhận định D. Phản ứng vừa thu nhiệt (∆H > 0), vừa làm giảm độ hỗn loạn của hệ (∆S < 0).
ΔG = ΔH – T × ΔS → ∆G có thể dương hoặc âm tùy T → Không luôn tự phát.
Đáp án: C. Phản ứng vừa toả nhiệt (∆H < 0), vừa làm hệ hỗn loạn hơn (∆S > 0). Đáp án: C
Nhận định A. Phản ứng vừa toả nhiệt (∆H < 0), vừa làm giảm độ hỗn loạn của hệ (∆S < 0).
ΔG = ΔH – T × ΔS → ∆G có thể dương hoặc âm tùy T → Không luôn tự phát.
Nhận định B. Phản ứng vừa thu nhiệt (∆H > 0), vừa làm hệ hỗn loạn hơn (∆S > 0).
ΔG = ΔH – T × ΔS → ∆G có thể dương hoặc âm tùy T → Không luôn tự phát.
Nhận định C. Phản ứng vừa toả nhiệt (∆H < 0), vừa làm hệ hỗn loạn hơn (∆S > 0).
ΔG = ΔH – T × ΔS → luôn âm, phản ứng luôn tự phát.
Nhận định D. Phản ứng vừa thu nhiệt (∆H > 0), vừa làm giảm độ hỗn loạn của hệ (∆S < 0).
ΔG = ΔH – T × ΔS → ∆G có thể dương hoặc âm tùy T → Không luôn tự phát.
Đáp án: C. Phản ứng vừa toả nhiệt (∆H < 0), vừa làm hệ hỗn loạn hơn (∆S > 0). Đáp án: C
Câu 9 [1073598]: Đồ thị sau đây cho thấy sự thay đổi của ∆G theo nhiệt độ T (K) của một phản ứng.
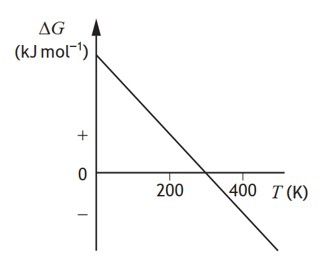
Nhận định nào sau đây đúng?

Nhận định nào sau đây đúng?
A, Phản ứng không bao giờ tự diễn biến.
B, Phản ứng luôn tự diễn biến.
C, Phản ứng tự diễn biến tại nhiệt độ dưới 300 K.
D, Phản ứng tự diễn biến tại nhiệt độ trên 300 K.
Nhận định A – Sai. Phản ứng tự diễn biến khi nhiệt độ trên 300 K
Nhận định B – Sai. Khi nhiệt độ nhoe hơn 300 K phản ứng không xảy ra
Nhận định C – Sai. Phản ứng tự diễn biến tại nhiệt độ trên 300 K.
Nhận định D – Đúng. Phản ứng tự diễn biến tại nhiệt độ trên 300 K.
Đáp án đúng là D Đáp án: D
Nhận định B – Sai. Khi nhiệt độ nhoe hơn 300 K phản ứng không xảy ra
Nhận định C – Sai. Phản ứng tự diễn biến tại nhiệt độ trên 300 K.
Nhận định D – Đúng. Phản ứng tự diễn biến tại nhiệt độ trên 300 K.
Đáp án đúng là D Đáp án: D
Câu 10 [1073599]: Cho phản ứng hóa học: H2O2(l) → H2O(l) + 0,5O2(g) và các dữ kiện:
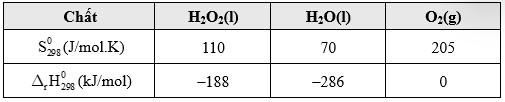
Nhận định nào sau đây đúng với phản ứng trên?

Nhận định nào sau đây đúng với phản ứng trên?
A, Tự diễn biến ở mọi nhiệt độ.
B, Chỉ diễn biến ở nhiệt độ thấp.
C, Chỉ diễn biến ở nhiệt độ cao.
D, Không tự diễn biến ở mọi nhiệt độ.
H2O2(l)  H2O(l) + 0,5O2(g)
H2O(l) + 0,5O2(g)
Biến thiên enthalpy của phản ứng là:
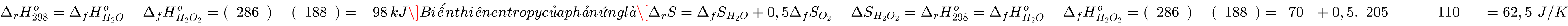
Ta có: ∆S > 0 và ∆H < 0 → ∆G luôn âm với mọi nhiệt độ, phản ứng tự xảy ra.
Đáp án: A. Tự diễn biến ở mọi nhiệt độ. Đáp án: A
 H2O(l) + 0,5O2(g)
H2O(l) + 0,5O2(g)Biến thiên enthalpy của phản ứng là:
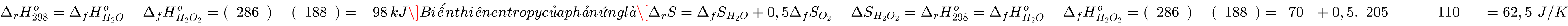
Ta có: ∆S > 0 và ∆H < 0 → ∆G luôn âm với mọi nhiệt độ, phản ứng tự xảy ra.
Đáp án: A. Tự diễn biến ở mọi nhiệt độ. Đáp án: A
Câu 11 [1073600]: Một phương pháp điều chế ethyl acetate (ester có mùi của dung môi sơn móng tay) là phản ứng giữa ethanol và acetic acid trong điều kiện xúc tác acid:
CH3COOH + C2H5OH ⇌ CH3COOC2H5 + H2O
Phản ứng có ∆H = –6,0 kJ/mol và ∆S = –8,614 J/mol.K. Giả sử các giá trị ∆H, ∆S của phản ứng không phụ thuộc vào nhiệt độ. Nhiệt độ T (K) để phản ứng tự diễn biến nằm trong khoảng giá trị nào sau đây?
CH3COOH + C2H5OH ⇌ CH3COOC2H5 + H2O
Phản ứng có ∆H = –6,0 kJ/mol và ∆S = –8,614 J/mol.K. Giả sử các giá trị ∆H, ∆S của phản ứng không phụ thuộc vào nhiệt độ. Nhiệt độ T (K) để phản ứng tự diễn biến nằm trong khoảng giá trị nào sau đây?
A, –298 < T < 298.
B, 298 < T < 700.
C, 353 < T < 696.
D, 635 < T < 983.
∆H = –6,0 kJ/mol và ∆S = –8,614 J/mol.K.
Ta có:
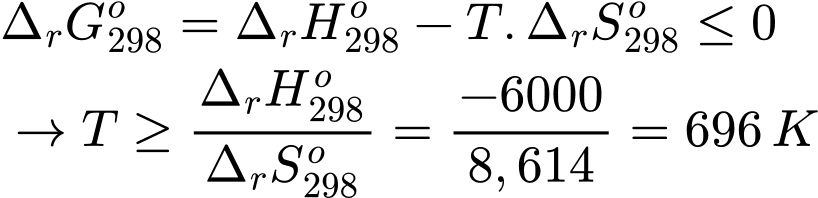
Đáp án: D. 635 < T < 983. Đáp án: D
Ta có:
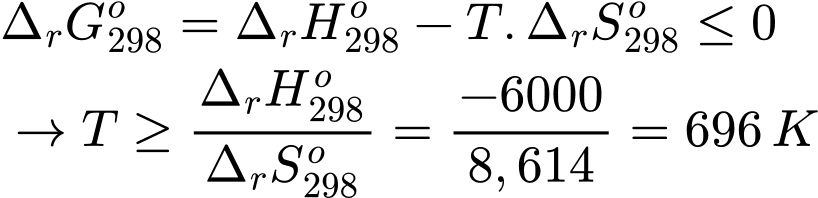
Đáp án: D. 635 < T < 983. Đáp án: D
Câu 12 [1073601]: Phản ứng tách nước phân tử ethanol:
C2H5OH →C2H4 + H2O
Đồ thị cho thấy phản ứng trên có biến thiên năng lượng tự do Gibbs (∆G) phụ thuộc vào nhiệt độ T (K) được cho như sau:
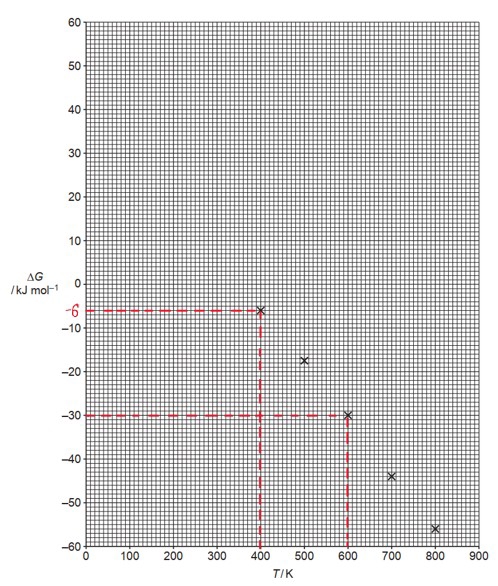
Từ nhiệt độ T (K) phản ứng tự diễn biến. Giá trị T (K) là bao nhiêu?
C2H5OH →C2H4 + H2O
Đồ thị cho thấy phản ứng trên có biến thiên năng lượng tự do Gibbs (∆G) phụ thuộc vào nhiệt độ T (K) được cho như sau:

Từ nhiệt độ T (K) phản ứng tự diễn biến. Giá trị T (K) là bao nhiêu?
A, T = 250 (K).
B, T = 350 (K).
C, T = 850 (K).
D, T = 1005 (K).
Từ đồ thị nhận thấy rằng khi nhiệt độ từ 350K thì phản ứng tự diễn biến
Đáp án: B. T = 350 (K). Đáp án: B
Đáp án: B. T = 350 (K). Đáp án: B
Câu 13 [1073602]: Khi luộc trứng lòng trắng trứng thể lỏng sẽ chuyển thành thể rắn. Thành phần chính của lòng trắng trứng là protein albumin ở thể lỏng, có cấu trúc chặt chẽ và trật tự nhờ các liên kết hydrogen. Việc phá vỡ cấu trúc của albumin cần cung cấp năng lượng (∆H > 0), chuyển albumin thành một cấu trúc cực kỳ hỗn loạn, các phân tử kết tụ thành một chất rắn không có tổ chức (∆S > 0). Ở nhiệt độ lớn hơn 373 (K): T∆S > ∆H. Nhận định nào sau đây đúng khi nói về quá trình này?
A, Quá trình chuyển từ trứng sống thành trứng luộc chín là một quá trình không thể đảo ngược và tự phát trên 373 K.
B, Quá trình chuyển từ trứng sống thành trứng luộc chín là một quá trình có thể đảo ngược và tự phát trên 373 K.
C, Quá trình chuyển từ trứng sống thành trứng luộc chín là một quá trình không thể đảo ngược và không tự phát trên 373 K.
D, Quá trình chuyển từ trứng sống thành trứng luộc chín là một quá trình không thể đảo ngược và tự phát dưới 373 K.
Hiện tượng: Lòng trắng trứng lỏng → rắn khi luộc.
- Protein albumin: Cấu trúc chặt chẽ (rắn lỏng?) nhờ liên kết H. Phá vỡ cấu trúc cần năng lượng → ∆H > 0 phản ứng thu nhiệt. Phân tử trở nên cực kỳ hỗn loạn, các phân tử kết tụ thành chất rắn không tổ chức → ∆S > 0
- ΔG = ΔH – T × ΔS → ∆G nhỏ hơn không, khi giá trị T > 373K→ Phản ứng luôn tự phát. Khả năng đảo ngược: khi trứng luộc, protein đã denature (biến tính) và kết tụ vĩnh viễn, không thể trở lại trạng thái lỏng ban đầu.
Đáp án: A. Quá trình chuyển từ trứng sống thành trứng luộc chín là một quá trình không thể đảo ngược và tự phát trên 373 K. Đáp án: A
- Protein albumin: Cấu trúc chặt chẽ (rắn lỏng?) nhờ liên kết H. Phá vỡ cấu trúc cần năng lượng → ∆H > 0 phản ứng thu nhiệt. Phân tử trở nên cực kỳ hỗn loạn, các phân tử kết tụ thành chất rắn không tổ chức → ∆S > 0
- ΔG = ΔH – T × ΔS → ∆G nhỏ hơn không, khi giá trị T > 373K→ Phản ứng luôn tự phát. Khả năng đảo ngược: khi trứng luộc, protein đã denature (biến tính) và kết tụ vĩnh viễn, không thể trở lại trạng thái lỏng ban đầu.
Đáp án: A. Quá trình chuyển từ trứng sống thành trứng luộc chín là một quá trình không thể đảo ngược và tự phát trên 373 K. Đáp án: A
Đọc đoạn thông tin sau và trả lời các câu hỏi từ 14 đến 16:
Biến thiên năng lượng tự do Gibbs (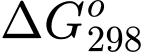 ) cho biết khả năng tự xảy ra của một phản ứng hóa học. Ở nhiệt độ và áp suất không đổi (p = 1 bar), biến thiên năng lượng tự do của phản ứng ΔG° (kJ) được tính theo công thức sau:
) cho biết khả năng tự xảy ra của một phản ứng hóa học. Ở nhiệt độ và áp suất không đổi (p = 1 bar), biến thiên năng lượng tự do của phản ứng ΔG° (kJ) được tính theo công thức sau:
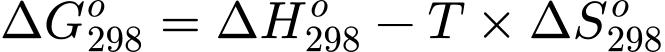
Trong đó: T là nhiệt độ tính theo thang Kelvin (K);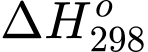 là biến thiên enthalpy (J);
là biến thiên enthalpy (J); 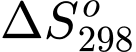 là biến thiên entropy (J/K);
là biến thiên entropy (J/K); 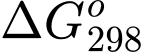 là biến thiên năng lượng tự do Gibbs (J).
là biến thiên năng lượng tự do Gibbs (J).
-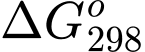 < 0: Phản ứng tự xảy ra.
< 0: Phản ứng tự xảy ra.
-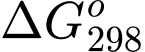 > 0: Phản ứng không tự xảy ra.
> 0: Phản ứng không tự xảy ra.
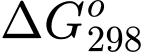 ) cho biết khả năng tự xảy ra của một phản ứng hóa học. Ở nhiệt độ và áp suất không đổi (p = 1 bar), biến thiên năng lượng tự do của phản ứng ΔG° (kJ) được tính theo công thức sau:
) cho biết khả năng tự xảy ra của một phản ứng hóa học. Ở nhiệt độ và áp suất không đổi (p = 1 bar), biến thiên năng lượng tự do của phản ứng ΔG° (kJ) được tính theo công thức sau: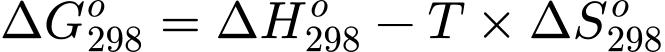
Trong đó: T là nhiệt độ tính theo thang Kelvin (K);
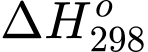 là biến thiên enthalpy (J);
là biến thiên enthalpy (J); 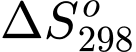 là biến thiên entropy (J/K);
là biến thiên entropy (J/K); 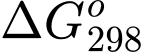 là biến thiên năng lượng tự do Gibbs (J).
là biến thiên năng lượng tự do Gibbs (J).-
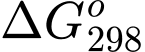 < 0: Phản ứng tự xảy ra.
< 0: Phản ứng tự xảy ra.-
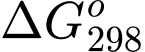 > 0: Phản ứng không tự xảy ra.
> 0: Phản ứng không tự xảy ra.
Câu 14 [1073361]: Với một phản ứng có 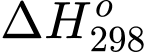 dương thì để phản ứng đó luôn tự xảy ra (
dương thì để phản ứng đó luôn tự xảy ra (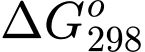 < 0) tại mọi nhiệt độ thì
< 0) tại mọi nhiệt độ thì
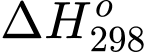 dương thì để phản ứng đó luôn tự xảy ra (
dương thì để phản ứng đó luôn tự xảy ra (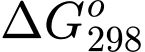 < 0) tại mọi nhiệt độ thì
< 0) tại mọi nhiệt độ thì A, 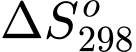 > 0.
> 0.
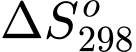 > 0.
> 0.B, 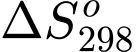 < 0.
< 0.
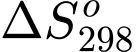 < 0.
< 0.C, 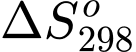 = 0.
= 0.
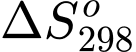 = 0.
= 0.D, 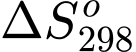 không xác định.
không xác định.
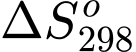 không xác định.
không xác định.
Với một phản ứng có 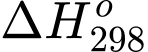 dương thì để phản ứng đó luôn tự xảy ra
(
dương thì để phản ứng đó luôn tự xảy ra
( 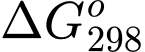 < 0 ) tại mọi nhiệt độ thì
< 0 ) tại mọi nhiệt độ thì 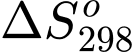 > 0. Khi đó giá trị
> 0. Khi đó giá trị 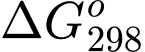 có thể tự xảy ra.
có thể tự xảy ra.
Đáp án: A.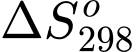 > 0.
Đáp án: A
> 0.
Đáp án: A
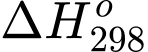 dương thì để phản ứng đó luôn tự xảy ra
(
dương thì để phản ứng đó luôn tự xảy ra
( 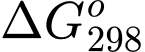 < 0 ) tại mọi nhiệt độ thì
< 0 ) tại mọi nhiệt độ thì 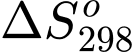 > 0. Khi đó giá trị
> 0. Khi đó giá trị 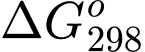 có thể tự xảy ra.
có thể tự xảy ra.Đáp án: A.
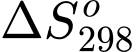 > 0.
Đáp án: A
> 0.
Đáp án: A
Câu 15 [1073362]: Cho phản ứng: 2NO(g) + O2(g)  2NO2(g).
2NO2(g).
Biến thiên enthalpy và entropy ở 25 oC lần lượt là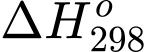 = −120 (kJ) và
= −120 (kJ) và 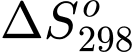 = −150 (J/K). Xác định giá trị
= −150 (J/K). Xác định giá trị 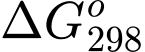 và cho biết phản ứng có thể tự xảy ra ở 25 oC được hay không?
và cho biết phản ứng có thể tự xảy ra ở 25 oC được hay không?
 2NO2(g).
2NO2(g).Biến thiên enthalpy và entropy ở 25 oC lần lượt là
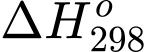 = −120 (kJ) và
= −120 (kJ) và 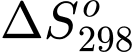 = −150 (J/K). Xác định giá trị
= −150 (J/K). Xác định giá trị 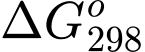 và cho biết phản ứng có thể tự xảy ra ở 25 oC được hay không?
và cho biết phản ứng có thể tự xảy ra ở 25 oC được hay không? A, 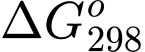 = 41,9 kJ và phản ứng có thể tự xảy ra.
= 41,9 kJ và phản ứng có thể tự xảy ra.
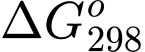 = 41,9 kJ và phản ứng có thể tự xảy ra.
= 41,9 kJ và phản ứng có thể tự xảy ra.B, 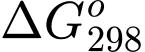 = 180,4 kJ và phản ứng không thể tự xảy ra.
= 180,4 kJ và phản ứng không thể tự xảy ra.
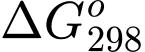 = 180,4 kJ và phản ứng không thể tự xảy ra.
= 180,4 kJ và phản ứng không thể tự xảy ra.C, 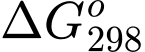 = −75,3 kJ và phản ứng có thể tự xảy ra.
= −75,3 kJ và phản ứng có thể tự xảy ra.
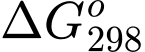 = −75,3 kJ và phản ứng có thể tự xảy ra.
= −75,3 kJ và phản ứng có thể tự xảy ra.D, 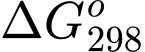 = −152,8 kJ và phản ứng không thể tự xảy ra.
= −152,8 kJ và phản ứng không thể tự xảy ra.
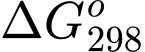 = −152,8 kJ và phản ứng không thể tự xảy ra.
= −152,8 kJ và phản ứng không thể tự xảy ra.
Đổi 25 oC = 298 K
Giá trị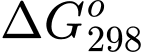 của phản ứng là:
của phản ứng là:
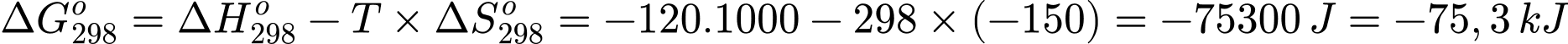
=> Phản ứng tự xảy ra.
Đáp án: D.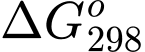 = −75,3 kJ và phản ứng có thể tự xảy ra.
Đáp án: D
= −75,3 kJ và phản ứng có thể tự xảy ra.
Đáp án: D
Giá trị
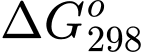 của phản ứng là:
của phản ứng là: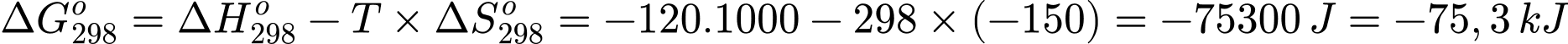
=> Phản ứng tự xảy ra.
Đáp án: D.
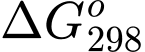 = −75,3 kJ và phản ứng có thể tự xảy ra.
Đáp án: D
= −75,3 kJ và phản ứng có thể tự xảy ra.
Đáp án: D
Câu 16 [1073363]: Xét phản ứng tổng quát: X + Y  Z + T. Giả sử giá trị enthalpy và entropy của phản ứng không thay đổi theo nhiệt độ. Mối liên hệ giữa
Z + T. Giả sử giá trị enthalpy và entropy của phản ứng không thay đổi theo nhiệt độ. Mối liên hệ giữa 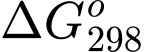 và T (K) của phản ứng trên như sau:
và T (K) của phản ứng trên như sau:
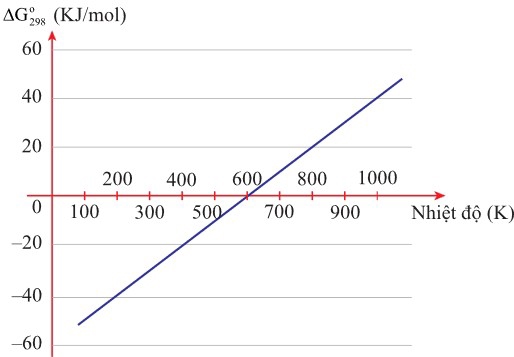
Trong số các phát biểu sau:
(a) Khi tăng nhiệt độ, phản ứng diễn ra càng thuận lợi.
(b) Phản ứng trên thuộc loại phản ứng thu nhiệt.
(c) Tại nhiệt độ 300 K, phản ứng có thể tự xảy ra.
(d) Từ khoảng nhiệt độ lớn hơn 600 K, phản ứng luôn tự xảy ra.
Số phát biểu đúng là
 Z + T. Giả sử giá trị enthalpy và entropy của phản ứng không thay đổi theo nhiệt độ. Mối liên hệ giữa
Z + T. Giả sử giá trị enthalpy và entropy của phản ứng không thay đổi theo nhiệt độ. Mối liên hệ giữa 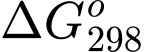 và T (K) của phản ứng trên như sau:
và T (K) của phản ứng trên như sau:
Trong số các phát biểu sau:
(a) Khi tăng nhiệt độ, phản ứng diễn ra càng thuận lợi.
(b) Phản ứng trên thuộc loại phản ứng thu nhiệt.
(c) Tại nhiệt độ 300 K, phản ứng có thể tự xảy ra.
(d) Từ khoảng nhiệt độ lớn hơn 600 K, phản ứng luôn tự xảy ra.
Số phát biểu đúng là
A, 1.
B, 2.
C, 3.
D, 4.
Nhận định (a) – Sai. Từ đồ thị, khi tăng nhiệt độ, giá trị tăng lên → Phản ứng không tự diễn biến → phản ứng diễn ra càng khó khăn.
Nhận định (b) – Sai. Phản ứng trên thuộc loại phản ứng tỏa nhiệt, nguyên do khi tăng nhiệt độ thì cân bằng của phản ứng chuyển dịch sang chiều nghịch, phản ứng thuận càng khó khăn.
Nhận định (c) – Đúng. Từ đồ thị tại nhiệt độ 300 K giá trị < 0, phản ứng có thể tự xảy ra
Nhận định (d) – Sai. Từ khoảng nhiệt độ lớn hơn 600 K giá trị > 0, phản ứng không tự xảy ra.
Đáp án: A. 1. Đáp án: A
Nhận định (b) – Sai. Phản ứng trên thuộc loại phản ứng tỏa nhiệt, nguyên do khi tăng nhiệt độ thì cân bằng của phản ứng chuyển dịch sang chiều nghịch, phản ứng thuận càng khó khăn.
Nhận định (c) – Đúng. Từ đồ thị tại nhiệt độ 300 K giá trị < 0, phản ứng có thể tự xảy ra
Nhận định (d) – Sai. Từ khoảng nhiệt độ lớn hơn 600 K giá trị > 0, phản ứng không tự xảy ra.
Đáp án: A. 1. Đáp án: A