Câu 1 [241772]: Hạt nhân của nguyên tử nào có số hạt neutron là 30?
A, 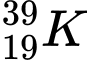 .
.
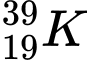 .
.B, 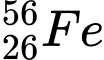 .
.
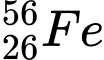 .
.C, 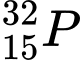 .
.
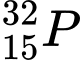 .
.D, 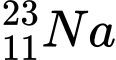 .
.
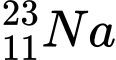 .
.
HƯỚNG DẪN GIẢI:
Số hạt neutron (N) = Số khối (A) – Số hạt proton (P).
Xét hạt nhân của các nguyên tử:
❌ A.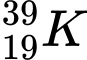 : N = 39 – 19 = 20
: N = 39 – 19 = 20
✔️ B.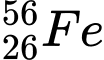 : N = 56 – 26 = 30
: N = 56 – 26 = 30
❌ C.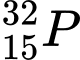 : N = 32 – 15 = 17
: N = 32 – 15 = 17
❌ D.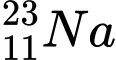 : N = 23 – 11 = 12
: N = 23 – 11 = 12
⇒ Chọn đáp án B Đáp án: B
Số hạt neutron (N) = Số khối (A) – Số hạt proton (P).
Xét hạt nhân của các nguyên tử:
❌ A.
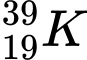 : N = 39 – 19 = 20
: N = 39 – 19 = 20✔️ B.
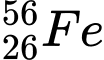 : N = 56 – 26 = 30
: N = 56 – 26 = 30❌ C.
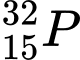 : N = 32 – 15 = 17
: N = 32 – 15 = 17❌ D.
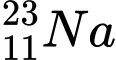 : N = 23 – 11 = 12
: N = 23 – 11 = 12⇒ Chọn đáp án B Đáp án: B
Câu 2 [247270]: Cấu hình electron nào sau đây không đúng?
A, 1s22s22p5.
B, 1s22s22p63s2.
C, 1s22s22p63s23p5.
D, 1s22s22p63s23p34s2.
HƯỚNG DẪN GIẢI:
1s22s22p63s23p34s2
- Phân lớp 3p chưa bão hòa. Cần phải "lấp đầy" 6 electron vào 3p rồi mới điền sang 4s.
⟹ Chọn đáp án D Đáp án: D
1s22s22p63s23p34s2
- Phân lớp 3p chưa bão hòa. Cần phải "lấp đầy" 6 electron vào 3p rồi mới điền sang 4s.
⟹ Chọn đáp án D Đáp án: D
Câu 3 [247263]: Nguyên tử của nguyên tố hóa học nào sau đây có cấu hình electron là 1s22s22p63s2?
A, Ca (Z = 20).
B, K (Z = 19).
C, Mg (Z = 12).
D, Na (Z = 11).
HƯỚNG DẪN GIẢI:
Phân tích các đáp án:
Cấu hình electron của các nguyên tố:
❌A. Ca(Z=20): 1s22s22p63s23p64s2
❌B. K(Z=19): 1s22s22p63s23p64s1
✔️C. Mg(Z=12): 1s22s22p63s2
❌D. Na(Z=11): 1s22s22p63s1
⟹Chọn đáp án C Đáp án: C
Phân tích các đáp án:
Cấu hình electron của các nguyên tố:
❌A. Ca(Z=20): 1s22s22p63s23p64s2
❌B. K(Z=19): 1s22s22p63s23p64s1
✔️C. Mg(Z=12): 1s22s22p63s2
❌D. Na(Z=11): 1s22s22p63s1
⟹Chọn đáp án C Đáp án: C
Câu 4 [575571]: Nguyên tử của nguyên tố hóa học nào sau đây có cấu hình electron là 1s22s22p5?
A, Mg (Z = 12).
B, F (Z = 9).
C, Cl (Z = 17).
D, P (Z = 15).
HƯỚNG DẪN GIẢI:
Phân tích các đáp án:
Cấu hình electron của các nguyên tố:
❌A.Mg (Z = 12): 1s22s22p53s2
✔️B.F (Z = 9): 1s22s22p5
❌C.Cl (Z = 17): 1s22s22p53s23p5
❌D.P (Z = 15): 1s22s22p53s23p3
⟹ Chọn đáp án B Đáp án: B
Phân tích các đáp án:
Cấu hình electron của các nguyên tố:
❌A.Mg (Z = 12): 1s22s22p53s2
✔️B.F (Z = 9): 1s22s22p5
❌C.Cl (Z = 17): 1s22s22p53s23p5
❌D.P (Z = 15): 1s22s22p53s23p3
⟹ Chọn đáp án B Đáp án: B
Câu 5 [575573]: Nguyên tử copper có cấu hình electron là [Ar]3d104s1. Số hiệu nguyên tử của copper là
A, 26.
B, 29.
C, 22.
D, 27.
HƯỚNG DẪN GIẢI:
- Cấu hình electron của copper là: 1s2 2s2 2p6 3s2 3p6 3d10 4s1
- Nguyên tử của nguyên tố có 2 + 2 + 6 + 2 + 6 + 10 + 1 = 29 electron ⇒ Số hiệu nguyên tử của copper là 29.
⇒ Chọn đáp án B Đáp án: B
- Cấu hình electron của copper là: 1s2 2s2 2p6 3s2 3p6 3d10 4s1
- Nguyên tử của nguyên tố có 2 + 2 + 6 + 2 + 6 + 10 + 1 = 29 electron ⇒ Số hiệu nguyên tử của copper là 29.
⇒ Chọn đáp án B Đáp án: B
Câu 6 [574686]: Nguyên tố X thuộc vào chu kì 2, nhóm VA trong bảng tuần hoàn. X là nguyên tố nào sau đây?
A, B (Z = 5).
B, N (Z = 7).
C, Na (Z = 11).
D, P (Z = 15).
HƯỚNG DẪN GIẢI:
- Nguyên tố X thuộc chu kì 2
→ X có 2 lớp electron.
- Nguyên tố X thuộc nhóm VA trong bảng tuần hoàn
→ X có 5 electron ở lớp ngoài cùng.
→ Cấu hình electron của X là: 1s2 2s2 2p3
→ ZX = 7 (N)
⟹ Chọn đáp án B Đáp án: B
- Nguyên tố X thuộc chu kì 2
→ X có 2 lớp electron.
- Nguyên tố X thuộc nhóm VA trong bảng tuần hoàn
→ X có 5 electron ở lớp ngoài cùng.
→ Cấu hình electron của X là: 1s2 2s2 2p3
→ ZX = 7 (N)
⟹ Chọn đáp án B Đáp án: B
Câu 7 [246706]: Nguyên tử của nguyên tố B thuộc chu kì 3, nhóm VIIA. Cấu hình electron thu gọn nào sau đây phù hợp với nguyên tố B?
A, [Ne]3s23p4.
B, [Ar]3s23p5.
C, [Ne]3s23p5.
D, [Ar]4s24p5.
HƯỚNG DẪN GIẢI:
- Nguyên tố B thuộc chu kì 3 ⇒ có 3 lớp electron.
- Nguyên tố B thuộc nhóm VIIA ⇒ Có 7 electron lớp ngoài cùng.
⟶ Cấu hình electron của B là: [Ne]3s23p5.
⇒ Chọn đáp án C Đáp án: C
- Nguyên tố B thuộc chu kì 3 ⇒ có 3 lớp electron.
- Nguyên tố B thuộc nhóm VIIA ⇒ Có 7 electron lớp ngoài cùng.
⟶ Cấu hình electron của B là: [Ne]3s23p5.
⇒ Chọn đáp án C Đáp án: C
Câu 8 [246689]: Một nguyên tử có cấu hình electron: 1s22s22p4. Nguyên tố này thuộc nhóm
A, IVA.
B, VIA.
C, IIA.
D, VIIIA.
Cấu hình electron: 1s22s22p4
Nguyên tử có 6e lớp ngoài cùng nên thuộc nhóm VIA
⟹ Chọn đáp án B
Đáp án: B
Nguyên tử có 6e lớp ngoài cùng nên thuộc nhóm VIA
⟹ Chọn đáp án B
Đáp án: B
Câu 9 [246697]: Nguyên tử nguyên tố X có chứa 9 proton và 10 hạt neutron. X thuộc nhóm nào trong bảng tuần hoàn?
A, VIIA.
B, VIIIA.
C, IIIA.
D, IA.
Cấu hình electron của X 1s22s22p5.
X có 7e lớp ngoài cùng ⟹ X thuộc nhóm VIIA trong bảng tuần hoàn.
⟹ Chọn đáp án A Đáp án: A
X có 7e lớp ngoài cùng ⟹ X thuộc nhóm VIIA trong bảng tuần hoàn.
⟹ Chọn đáp án A Đáp án: A
Câu 10 [246579]: Nguyên tử sulfur (Z = 16) có bao nhiêu electron hóa trị?
A, 4.
B, 6.
C, 16.
D, 8.
Cấu hình electron của Sulfur: 1s22s22p63s23p4
⟹ Sulfur có 6 electron hóa trị.
⟹ Chọn đáp án B Đáp án: B
⟹ Sulfur có 6 electron hóa trị.
⟹ Chọn đáp án B Đáp án: B
Câu 11 [680857]: Nguyên tố natri (sodium, Na ) có số hiệu nguyên tử là 11 . Ở trạng thái cơ bản, cấu hình electron của ion Na+ là
A, 1s22s22p63s1.
B, 1s22s22p6.
C, 1s22s22p5.
D, 1s22s22p63s2.
Cấu hình electron của Sodium là: 1s22s22p63s1
⟶ Sodium có 1 electron lớp ngoài cùng cần nhường 1 eletron để tạo thành ion Na+
Na ⟶ Na+ + 1e
Cấu hình electron của ion Na+ là: 1s22s22p6
⟹ Chọn đáp án B Đáp án: B
⟶ Sodium có 1 electron lớp ngoài cùng cần nhường 1 eletron để tạo thành ion Na+
Na ⟶ Na+ + 1e
Cấu hình electron của ion Na+ là: 1s22s22p6
⟹ Chọn đáp án B Đáp án: B
Câu 12 [247271]: Khi nguyên tử chlorine (Z=17) nhận thêm 1e thì cấu hình electron của ion tương ứng là
A, 1s2 2s2 2p6 3s1.
B, 1s2 2s2 2p6.
C, 1s2 2s2 2p6 3s3.
D, 1s2 2s2 2p6 3s2 3p6.
HƯỚNG DẪN GIẢI:
Cấu hình e của Cl: 1s22s22p63s23p5
⟶ Nhận thêm 1e ⟶ Cấu hình e của Y: 1s22s22p63s23p6
⟹ Chọn đáp án D Đáp án: D
Cấu hình e của Cl: 1s22s22p63s23p5
⟶ Nhận thêm 1e ⟶ Cấu hình e của Y: 1s22s22p63s23p6
⟹ Chọn đáp án D Đáp án: D
Câu 13 [247272]: Ion X2+ có cấu hình electron là 1s2 2s2 2p6. Nguyên tố X là
A, Ne (Z= 10).
B, Mg (Z = 12).
C, Na (Z = 11).
D, O (Z = 8).
HƯỚNG DẪN GIẢI:
X2+ có cấu hình electron là 1s2 2s2 2p6 đã nhường đi 2e.
⟶ Cấu hình electron của X: 1s2 2s2 2p63s2
Vậy số hiệu nguyên tử của X bằng số hạt electron và bằng: 2 + 2 + 6 + 2 = 12.
⟶ X là Mg
⟹ Chọn đáp án B Đáp án: B
X2+ có cấu hình electron là 1s2 2s2 2p6 đã nhường đi 2e.
⟶ Cấu hình electron của X: 1s2 2s2 2p63s2
Vậy số hiệu nguyên tử của X bằng số hạt electron và bằng: 2 + 2 + 6 + 2 = 12.
⟶ X là Mg
⟹ Chọn đáp án B Đáp án: B
Câu 14 [823553]: Cặp nguyên tử nào sau đây có cùng số neutron?
A, 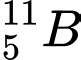 và
và 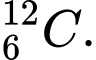
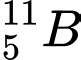 và
và 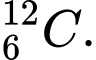
B, 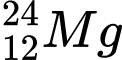 và
và 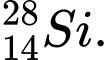
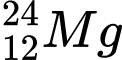 và
và 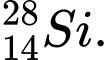
C, 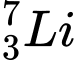 và
và 
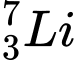 và
và 
D, 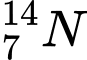 và
và 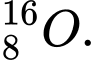
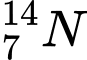 và
và 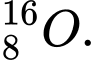
Công thức tính Số neutron (N) = Số khối (A) - Số proton (Z)
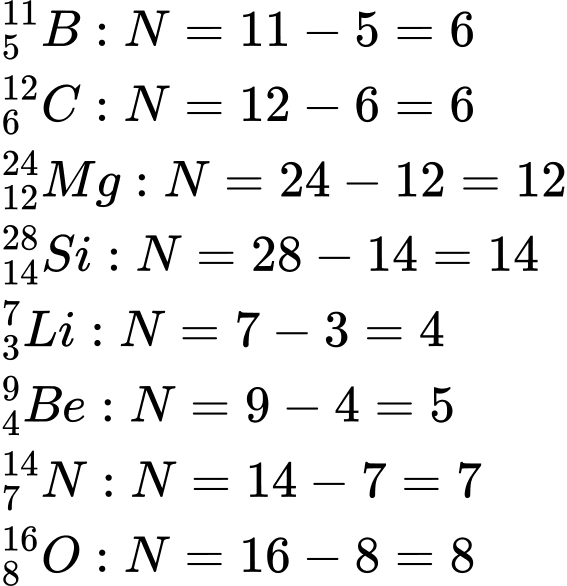
Phân tích các đáp án:
✔️Đúng. A.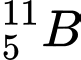 và
và 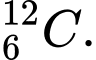 . Có cùng số neutron
. Có cùng số neutron
❌Sai. B.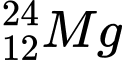 và
và 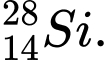 . Có số neutron khác nhau.
. Có số neutron khác nhau.
❌Sai. C.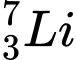 và
và  . Có số neutron khác nhau.
. Có số neutron khác nhau.
❌Sai. D.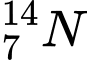 và
và 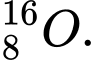 . Có số neutron khác nhau
. Có số neutron khác nhau
⟹ Chọn đáp án A Đáp án: A
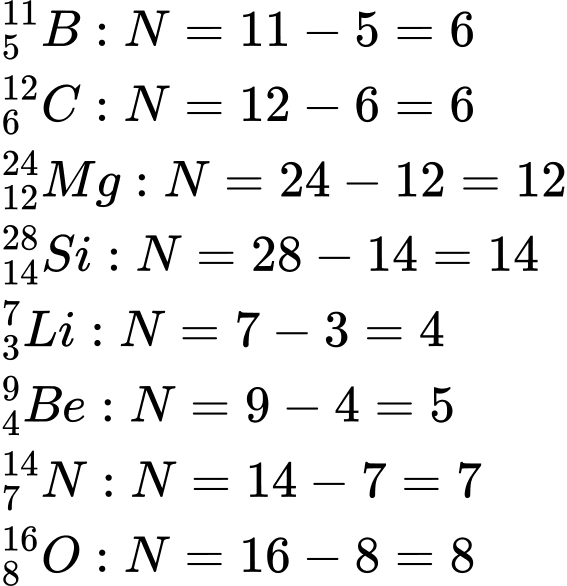
Phân tích các đáp án:
✔️Đúng. A.
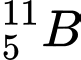 và
và 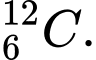 . Có cùng số neutron
. Có cùng số neutron❌Sai. B.
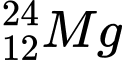 và
và 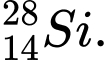 . Có số neutron khác nhau.
. Có số neutron khác nhau.❌Sai. C.
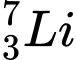 và
và  . Có số neutron khác nhau.
. Có số neutron khác nhau.❌Sai. D.
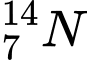 và
và 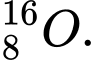 . Có số neutron khác nhau
. Có số neutron khác nhau⟹ Chọn đáp án A Đáp án: A
Câu 15 [823555]: Cặp nào sau đây có số electron khác nhau?
A, 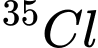 và
và 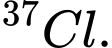
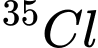 và
và 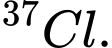
B,  và
và 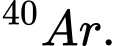
 và
và 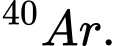
C, 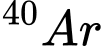 và
và 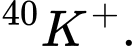
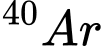 và
và 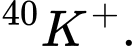
D, 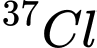 và
và 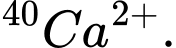
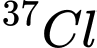 và
và 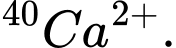
⭐Ta có: Số hiệu nguyên tử (Z) = Số elctron (e) = Số proton (p)
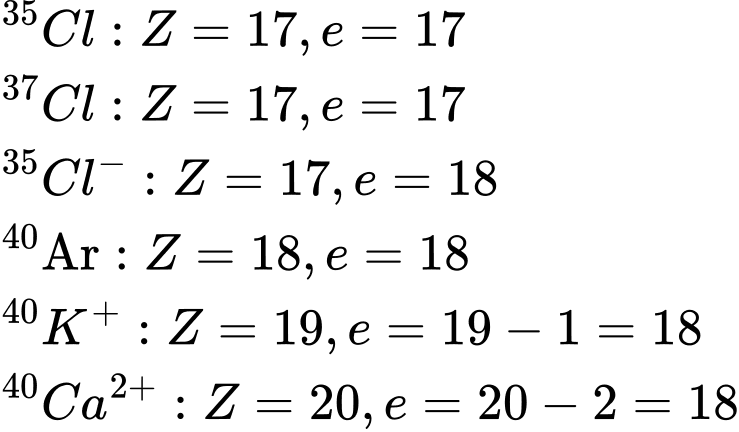
Phân tích các đáp án:
❌Sai. A. Cặp nguyên tử có số electron bằng nhau e= 17
❌Sai. B. Cặp nguyên tử có số electron bằng nhau e= 18
❌Sai. C. Cặp nguyên tử có số electron bằng nhau e= 18
✔️Đúng. D. Cặp nguyên tử có số electron khác nhau e = 17 và e = 18
⟹ Chọn đáp án D Đáp án: D
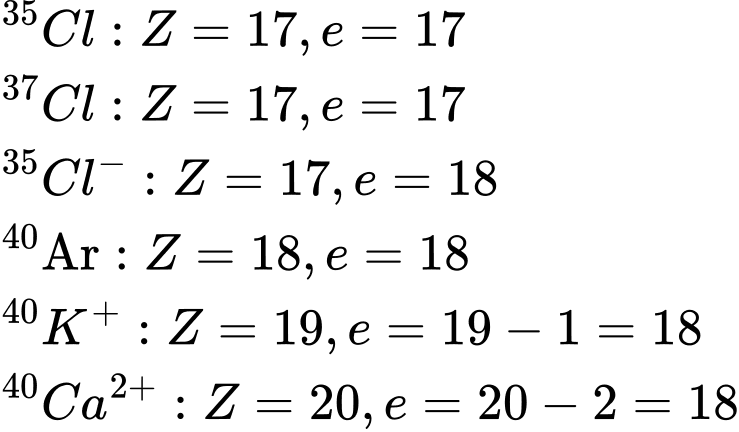
Phân tích các đáp án:
❌Sai. A. Cặp nguyên tử có số electron bằng nhau e= 17
❌Sai. B. Cặp nguyên tử có số electron bằng nhau e= 18
❌Sai. C. Cặp nguyên tử có số electron bằng nhau e= 18
✔️Đúng. D. Cặp nguyên tử có số electron khác nhau e = 17 và e = 18
⟹ Chọn đáp án D Đáp án: D
Câu 16 [823556]: Hạt X có 18 electron và 20 neutron. Kí hiệu của hạt X không thể là
A, 
B, 
C, 
D, 
Các em ơi, chú ý💥
Nhập liệu câu này trong sách của chúng ta đang bị lỗi, vì vậy các em sửa giống trên web để chọn đáp án nhé́!
Sách mới không tránh khỏi những lỗi sai nên rất mong sự góp ý yêu thương của các em để nhóm tác giả hoàn thiện sách cho lần tái bản sau nha. Cảm ơn các em nhiều.
Phân tích các đáp án
✔️Đúng. A. có 18 electron và 20 neutron.
có 18 electron và 20 neutron.
✔️Đúng. B. có 18 electron và 20 neutron.
có 18 electron và 20 neutron.
❌Sai. C. có 17 electron và 18 neutron.
có 17 electron và 18 neutron.
✔️Đúng D. có 18 electron và 20 neutron.
có 18 electron và 20 neutron.
⟹ Chọn đáp án C Đáp án: C
Nhập liệu câu này trong sách của chúng ta đang bị lỗi, vì vậy các em sửa giống trên web để chọn đáp án nhé́!
Sách mới không tránh khỏi những lỗi sai nên rất mong sự góp ý yêu thương của các em để nhóm tác giả hoàn thiện sách cho lần tái bản sau nha. Cảm ơn các em nhiều.
Phân tích các đáp án
✔️Đúng. A.
✔️Đúng. B.
❌Sai. C.
✔️Đúng D.
⟹ Chọn đáp án C Đáp án: C
Câu 17 [823557]: Hạt nào sau đây có số electron nhỏ nhất?
A, B3+.
B, H+.
C, He+.
D, Be2+.
Phân tích các đáp án:
❌Sai. A. B3+ Z = 5, e = 5 - 3 =2
✔️Đúng. B. H+ Z= 1, e = 1 - 1 = 0
❌Sai. C. He+ Z= 2, e = 2 - 1 = 1
❌Sai. D. Be2+ Z= 4, e = 4 - 2 = 2
⟹ Chọn đáp án B Đáp án: B
❌Sai. A. B3+ Z = 5, e = 5 - 3 =2
✔️Đúng. B. H+ Z= 1, e = 1 - 1 = 0
❌Sai. C. He+ Z= 2, e = 2 - 1 = 1
❌Sai. D. Be2+ Z= 4, e = 4 - 2 = 2
⟹ Chọn đáp án B Đáp án: B
Câu 18 [850745]: Nguyên tử của một nguyên tố X có tổng số các loại hạt bằng 82, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22 hạt. Cấu hình electron của nguyên tử nguyên tố X là
A, 1s22s22p63s23p64s23d4.
B, 1s22s22p63s23p63d44s2.
C, 1s22s22p63s23p63d54s1.
D, 1s22s22p63s23p63d64s2.
Nguyên tử của một nguyên tố X có tổng số các loại hạt bằng 82, hay: p + n + e = 82.
Mà nguyên tử trung hòa về điện nên p = e nên có thể viết biểu thức tổng số hạt dưới dạng: 2p + n = 82 (1)
Lại có số hạt mang điện nhiều hơn số hạt không mang điện là 22 hạt, hay: 2p - n = 22 (2)
Từ (1) và (2) ⇒ n = 30; p = e = 26.
X có cấu hình: 1s22s22p63s23p64s23d4. Tuy nhiên, cấu hình này không bền nên 1e ở phân lớp 4s sẽ lập tức di chuyển sang phân lớp 3d để nguyên tử trở nên bền vững hơn, thỏa mãn nguyên tắc bán bão hòa.
⇒ Cấu hình electron của nguyên tử nguyên tố X1s22s22p63s23p63d54s1.
⇒ Chọn đáp án C
Đáp án: C
Mà nguyên tử trung hòa về điện nên p = e nên có thể viết biểu thức tổng số hạt dưới dạng: 2p + n = 82 (1)
Lại có số hạt mang điện nhiều hơn số hạt không mang điện là 22 hạt, hay: 2p - n = 22 (2)
Từ (1) và (2) ⇒ n = 30; p = e = 26.
X có cấu hình: 1s22s22p63s23p64s23d4. Tuy nhiên, cấu hình này không bền nên 1e ở phân lớp 4s sẽ lập tức di chuyển sang phân lớp 3d để nguyên tử trở nên bền vững hơn, thỏa mãn nguyên tắc bán bão hòa.
⇒ Cấu hình electron của nguyên tử nguyên tố X1s22s22p63s23p63d54s1.
⇒ Chọn đáp án C
Đáp án: C
Câu 19 [247359]: Anion Y- có cấu hình electron 1s22s22p63s23p6. Vị trí của Y trong bảng tuần hoàn là
A, chu kì 3, nhóm VIIA.
B, chu kì 3, nhóm VIA.
C, chu kì 4, nhóm IA.
D, chu kì 4, nhóm IIA.
Cấu hình electron của Y 1s22s22p63s23p5. Đáp án: A
Câu 20 [243454]: X là một trong những khoáng chất cần thiết đối với cơ thể; trong mỗi tế bào X chiếm tỉ lệ khoảng 0,004% khối lượng. X có vai trò hỗ trợ cho quá trình tổng hợp hemoglobin và myoglobin. Cấu hình electron của ion X2+ là 1s22s22p63s23p63d7. Trong bảng tuần hoàn các nguyên tố hóa học, nguyên tố X thuộc
A, chu kì 4, nhóm VIIIB.
B, chu kì 4, nhóm VIIIA.
C, chu kì 3, nhóm VIB.
D, chu kì 4, nhóm IIA.
Cấu hình electron của ion X2+ 1s22s22p63s23p63d7 được hình thành khi nguyên tử của nguyên tố X nhường đi 2 electron.
→ Cấu hình electron nguyên tử của nguyên tố X là: 1s22s22p63s23p63d74s2
→ Nguyên tố X thuộc chu kì 4, nhóm VIIIB.
Đáp án: A
→ Cấu hình electron nguyên tử của nguyên tố X là: 1s22s22p63s23p63d74s2
→ Nguyên tố X thuộc chu kì 4, nhóm VIIIB.
Đáp án: A
Câu 21 [246532]: Trong tự nhiên, nguyên tố copper có hai đồng vị là 63Cu và 65Cu. Nguyên tử khối trung bình của Copper là 63,54. Thành phần % số nguyên tử của đồng vị 65Cu là
A, 27%.
B, 50%.
C, 54%.
D, 73%.
HƯỚNG DẪN GIẢI:
- Gọi % số lượng nguyên tử 63Cu và 65Cu lần lượt là x và y
⟹ x + y = 1 (1)
- Nguyên tử khối trung bình của Cu là 63,54% nên ta có:
⟹ 63x + 65y / (x + y) = 63,54 |
⟺ 63x + 65y = 63,54 (Do x + y = 1) (2)
- Từ (1) và (2) ⟺ x = 0,73; y = 0,27
Vậy thành phần % số nguyên tử của đồng vị 65Cu là 27%
⟹ Chọn đáp án: A Đáp án: A
- Gọi % số lượng nguyên tử 63Cu và 65Cu lần lượt là x và y
⟹ x + y = 1 (1)
- Nguyên tử khối trung bình của Cu là 63,54% nên ta có:
⟹ 63x + 65y / (x + y) = 63,54 |
⟺ 63x + 65y = 63,54 (Do x + y = 1) (2)
- Từ (1) và (2) ⟺ x = 0,73; y = 0,27
Vậy thành phần % số nguyên tử của đồng vị 65Cu là 27%
⟹ Chọn đáp án: A Đáp án: A
Câu 22 [246534]: Nguyên tử khối trung bình của nguyên tố X là 79,91. Biết X có hai đồng vị bền trong đó đồng vị 79X chiếm 54,5% số nguyên tử. Số khối của đồng vị còn lại là
A, 80.
B, 81.
C, 82.
D, 83.
HƯỚNG DẪN GIẢI
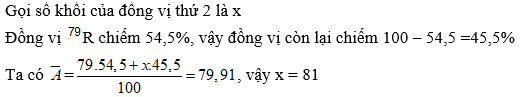
⟹ Chọn đáp án: B Đáp án: B
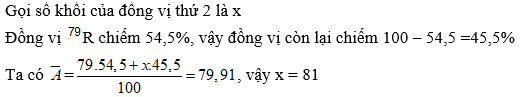
⟹ Chọn đáp án: B Đáp án: B
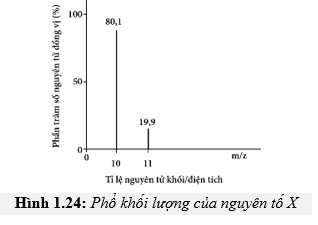
Câu 23 [246512]: Phổ khối lượng của nguyên tố X được cho ở hình 1.24. Nguyên tử khối trung bình của nguyên tố này là bao nhiêu?

A, 10.
B, 10,8.
C, 10,2.
D, 11.
HƯỚNG DẪN GIẢI:
- Từ phổ khối lượng ta xác định được có hai đồng vị của nguyên tố X:
+) Đồng vị 10X chiếm 80,1% số lượng nguyên tử.
+) Đồng vị 11X chiếm 19,9% số lượng nguyên tử.
- Ta có công thức tính nguyên tử khối trung bình như sau:
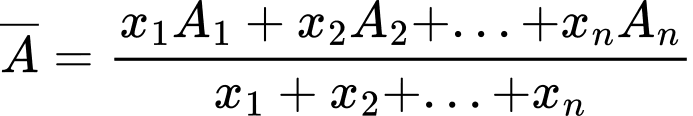
+) Với A1, A2, ... là số khối của các đồng vị tương ứng.
+) x1, x2, ... là phần trăm số nguyên tử của mỗi đồng vị tương ứng.
- Vậy nguyên tử khối trung bình của x là:
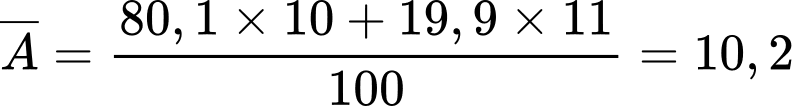
⟹ Chọn đáp án C Đáp án: C
- Từ phổ khối lượng ta xác định được có hai đồng vị của nguyên tố X:
+) Đồng vị 10X chiếm 80,1% số lượng nguyên tử.
+) Đồng vị 11X chiếm 19,9% số lượng nguyên tử.
- Ta có công thức tính nguyên tử khối trung bình như sau:
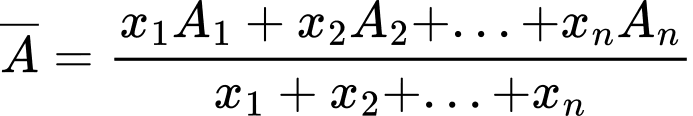
+) Với A1, A2, ... là số khối của các đồng vị tương ứng.
+) x1, x2, ... là phần trăm số nguyên tử của mỗi đồng vị tương ứng.
- Vậy nguyên tử khối trung bình của x là:
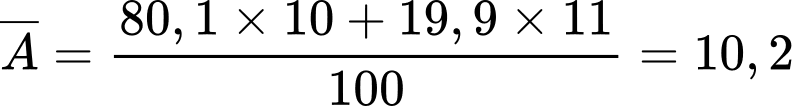
⟹ Chọn đáp án C Đáp án: C
Câu 24 [575379]: Phổ khối lượng của zirconium được biểu diễn như hình sau đây (điện tích z của các ion đồng vị zirconium đều bằng 1+).
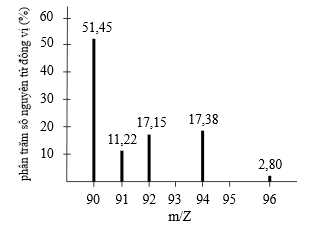
Số lượng đồng vị bền và nguyên tử khối trung bình của zirconium là:

Số lượng đồng vị bền và nguyên tử khối trung bình của zirconium là:
A, 5 đồng vị, nguyên tử khối trung bình bằng 92,60.
B, 5 đồng vị, nguyên tử khối trung bình bằng 91,32.
C, 4 đồng vị, nguyên tử khối trung bình bằng 91,18.
D, 4 đồng vị, nguyên tử khối trung bình bằng 92,00.
HƯỚNG DẪN GIẢI:
- Quan sát phổ khối lượng của zirconium xác định được nguyên tố này có 5 đồng vị.
+) 90Zr chiếm 51,45% số lượng nguyên tử.
+) 91Zr chiếm 11,22% số lượng nguyên tử.
+) 92Zr chiếm 17,15% số lượng nguyên tử.
+) 94Zr chiếm 17,38% số lượng nguyên tử.
+) 96Zr chiếm 2,8% số lượng nguyên tử.
- Công thức tính nguyên tử khối trung bình như sau:
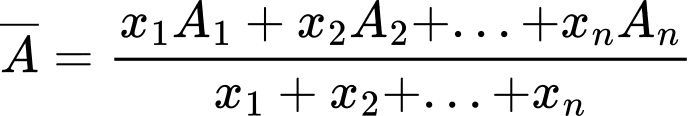
+) Với A1, A2, ... là số khối của các đồng vị tương ứng.
+) x1, x2, ... là phần trăm số nguyên tử của mỗi đồng vị tương ứng.
- Nguyên tử khối trung bình của zirconium:
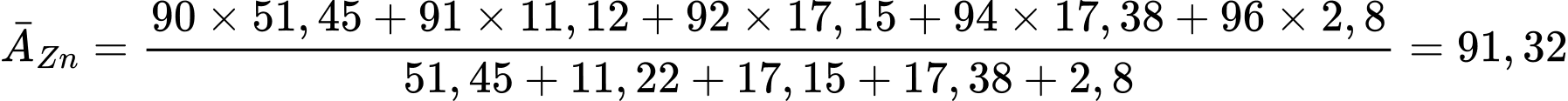
→ Nguyên tố này có 5 đồng vị, nguyên tử khối trung bình bằng 91,32.
⟹ Chọn đáp án B Đáp án: B
- Quan sát phổ khối lượng của zirconium xác định được nguyên tố này có 5 đồng vị.
+) 90Zr chiếm 51,45% số lượng nguyên tử.
+) 91Zr chiếm 11,22% số lượng nguyên tử.
+) 92Zr chiếm 17,15% số lượng nguyên tử.
+) 94Zr chiếm 17,38% số lượng nguyên tử.
+) 96Zr chiếm 2,8% số lượng nguyên tử.
- Công thức tính nguyên tử khối trung bình như sau:
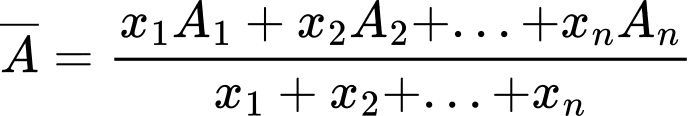
+) Với A1, A2, ... là số khối của các đồng vị tương ứng.
+) x1, x2, ... là phần trăm số nguyên tử của mỗi đồng vị tương ứng.
- Nguyên tử khối trung bình của zirconium:
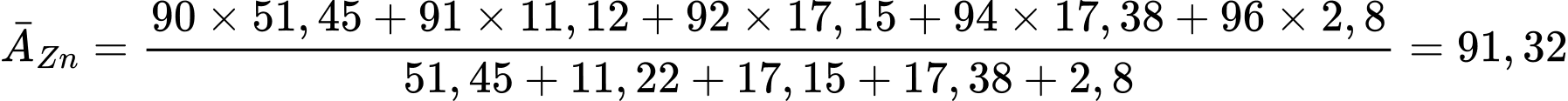
→ Nguyên tố này có 5 đồng vị, nguyên tử khối trung bình bằng 91,32.
⟹ Chọn đáp án B Đáp án: B
Câu 25 [575358]: Nguyên tử của nguyên tố X có tổng số hạt cơ bản (proton, electron, neutron) là 49, trong đó số hạt không mang điện bằng 53,125% số hạt mang điện. Xác định số khối của X.
HƯỚNG DẪN GIẢI:
- Gọi số hạt proton, neutron, electron trong nguyên tử nguyên tố X lần lượt là p, n, e; trong đó p = e (do nguyên tử trung hòa về điện)
- Nguyên tử nguyên tố X có tổng số hạt cơ bản (hạt proton, neutron, electron) là 49 nên ta có:
⟺ p + n + e = 49 ⟺ 2p + n = 49 (do p = e) (1)
- Trong đó số hạt không mang điện (hạt neutron) bằng 53,125% số hạt mang điện (hạt proton và electron) nên ta có:
⟺ n = 53,125%(p + e) ⟺ 1,0625p - n = 0 (do p = e) (2)
- Từ (1) và (2) ⟺ p = e = 16, n = 17
Vậy số khối của X là: A = p + n = 16 + 17 = 33.
⟹ Điền đáp án: 33
- Gọi số hạt proton, neutron, electron trong nguyên tử nguyên tố X lần lượt là p, n, e; trong đó p = e (do nguyên tử trung hòa về điện)
- Nguyên tử nguyên tố X có tổng số hạt cơ bản (hạt proton, neutron, electron) là 49 nên ta có:
⟺ p + n + e = 49 ⟺ 2p + n = 49 (do p = e) (1)
- Trong đó số hạt không mang điện (hạt neutron) bằng 53,125% số hạt mang điện (hạt proton và electron) nên ta có:
⟺ n = 53,125%(p + e) ⟺ 1,0625p - n = 0 (do p = e) (2)
- Từ (1) và (2) ⟺ p = e = 16, n = 17
Vậy số khối của X là: A = p + n = 16 + 17 = 33.
⟹ Điền đáp án: 33
Câu 26 [575356]: 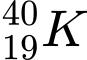 là một đồng vị phóng xạ của nguyên tố potassium có mặt trong cơ thể con người. Tổng số các loại hạt (proton, neutron và electron) trong đồng vị này là bao nhiêu?
là một đồng vị phóng xạ của nguyên tố potassium có mặt trong cơ thể con người. Tổng số các loại hạt (proton, neutron và electron) trong đồng vị này là bao nhiêu?
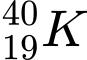 là một đồng vị phóng xạ của nguyên tố potassium có mặt trong cơ thể con người. Tổng số các loại hạt (proton, neutron và electron) trong đồng vị này là bao nhiêu?
là một đồng vị phóng xạ của nguyên tố potassium có mặt trong cơ thể con người. Tổng số các loại hạt (proton, neutron và electron) trong đồng vị này là bao nhiêu?
HƯỚNG DẪN GIẢI:
- Dựa vào ký hiệu của đồng vị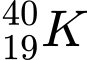 ta có:
ta có:
+) Z = 19 ⟺ K có số proton bằng số electron và bằng 19 (do nguyên tử trung hòa về điện)
+) A = 40 ⟺ n = A -- Z = 40 - 19 = 21 (hạt)
Tổng số các loại hạt trong đồng vị này là: p + n + e = 19 + 19 + 21 = 59 (hạt)
⇒ Điền đáp án: 59
- Dựa vào ký hiệu của đồng vị
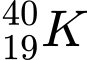 ta có:
ta có:+) Z = 19 ⟺ K có số proton bằng số electron và bằng 19 (do nguyên tử trung hòa về điện)
+) A = 40 ⟺ n = A -- Z = 40 - 19 = 21 (hạt)
Tổng số các loại hạt trong đồng vị này là: p + n + e = 19 + 19 + 21 = 59 (hạt)
⇒ Điền đáp án: 59
Câu 27 [575391]: Phổ khối lượng của nguyên tố A được biểu diễn tại hình vẽ dưới đây (điện tích z của các ion đồng vị A đều bằng 1+):
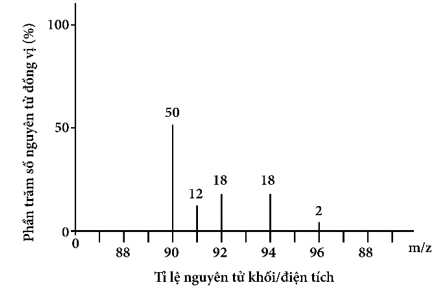
Tính nguyên tử khối trung bình của nguyên tố A. (làm tròn kết quả đến phần chục).

Tính nguyên tử khối trung bình của nguyên tố A. (làm tròn kết quả đến phần chục).
HƯỚNG DẪN GIẢI:
- Từ phổ khối lượng ta có các đồng vị của A là:
+) 90A có phần trăm số lượng nguyên tử là 50%
+) 91A có phần trăm số lượng nguyên tử là 12%
+) 92A có phần trăm số lượng nguyên tử là 18%
+) 94A có phần trăm số lượng nguyên tử là 18%
+) 96A có phần trăm số lượng nguyên tử là 2%
- Công thức tính nguyên tử khối trung bình là:
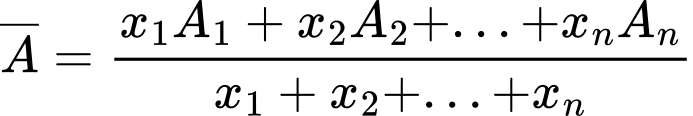
- Trong đó:
+) A1, A2, ... là số khối của đồng vị tương ứng.
+) x1, x2, ... là phần trăm số lượng nguyên tử của đồng vị tương ứng.
⟹ Nguyên tử khối trung bình của A là:
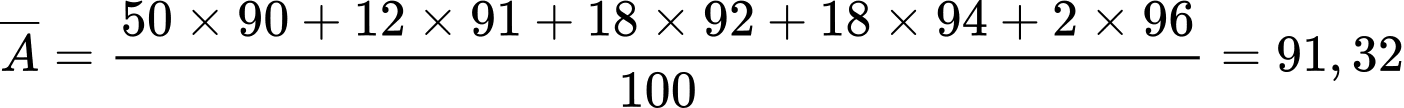
⟹ Điền đáp án: 91,3
- Từ phổ khối lượng ta có các đồng vị của A là:
+) 90A có phần trăm số lượng nguyên tử là 50%
+) 91A có phần trăm số lượng nguyên tử là 12%
+) 92A có phần trăm số lượng nguyên tử là 18%
+) 94A có phần trăm số lượng nguyên tử là 18%
+) 96A có phần trăm số lượng nguyên tử là 2%
- Công thức tính nguyên tử khối trung bình là:
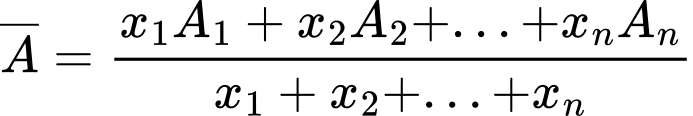
- Trong đó:
+) A1, A2, ... là số khối của đồng vị tương ứng.
+) x1, x2, ... là phần trăm số lượng nguyên tử của đồng vị tương ứng.
⟹ Nguyên tử khối trung bình của A là:
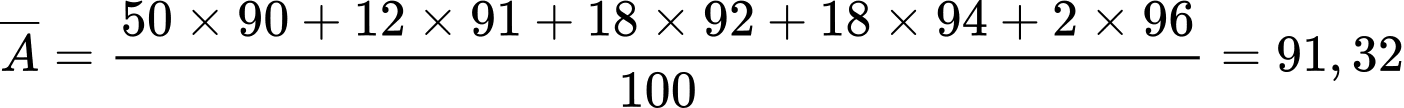
⟹ Điền đáp án: 91,3
Đọc đoạn thông tin sau và trả lời các câu hỏi từ 28 đến 30:
Vào đầu thế kỉ 20, một số mô hình nguyên tử được ra đời để giải thích cho cấu tạo của nguyên tử nhưng tuy nhiên các mô hình này không cung cấp một mô tả đầy đủ về trạng thái của các electron trong nguyên tử cũng như nhiều tính chất khác.
Từ đó dẫn đến việc phải có một mô hình mới ra đời: Mô hình hiện đại được đề xuất bởi nhà vật lý người Áo Erwin Schrödinger vào năm 1926. Theo mô hình hiện đại về nguyên tử, electron chuyển động rất nhanh trong cả khu vực không gian xung quanh hạt nhân với xác xuất tìm thấy các hạt electron là khác nhau, sự chuyển động này không theo một quỹ đạo nhất định và nó tạo thành một hình ảnh giống như đám mây electron (Hình vẽ dưới). Tuy nhiên, ta có thể xác định được vùng không gian xung quanh hạt nhân mà tại đó xác xuất tìm thấy electron là lớn nhất (khoảng 90%) và vùng không gian này gọi là Orbital nguyên tử (Atomic orbital – kí hiệu là AO).

Từ đó dẫn đến việc phải có một mô hình mới ra đời: Mô hình hiện đại được đề xuất bởi nhà vật lý người Áo Erwin Schrödinger vào năm 1926. Theo mô hình hiện đại về nguyên tử, electron chuyển động rất nhanh trong cả khu vực không gian xung quanh hạt nhân với xác xuất tìm thấy các hạt electron là khác nhau, sự chuyển động này không theo một quỹ đạo nhất định và nó tạo thành một hình ảnh giống như đám mây electron (Hình vẽ dưới). Tuy nhiên, ta có thể xác định được vùng không gian xung quanh hạt nhân mà tại đó xác xuất tìm thấy electron là lớn nhất (khoảng 90%) và vùng không gian này gọi là Orbital nguyên tử (Atomic orbital – kí hiệu là AO).

Hình vẽ. Đám mây electron
Các electron sẽ được chia thành các lớp gọi là lớp electron. Số lớp electron (n) thể hiện kích thước của orbital nguyên tử. Giá trị n càng nhỏ thì kích thước orbital nguyên tử càng nhỏ, electron thuộc các lớp này càng gần hạt nhân và sẽ càng bị hút mạnh hơn về phía hạt nhân, dẫn đến electron sẽ có mức năng lượng thấp hơn so với electron thuộc các lớp ở xa hạt nhân, giá trị n lớn. Số lớp electron có thể có các giá trị nguyên là 1, 2, 3, …
Câu 28 [382276]: Orbital nguyên tử là gì?
A, Khu vực không gian xung quanh hạt nhân có thể tìm thấy electron.
B, Khu vực không gian xung quanh hạt nhân.
C, Khu vực không gian xung quanh hạt nhân mà tại đó xác xuất tìm thấy electron khoảng 90%.
D, Khu vực không gian xung quanh hạt nhân mà tại đó xác xuất tìm thấy electron khoảng 95%.
HƯỚNG DẪN GIẢI:
- Orbital nguyên tử (AO - Atomic Orbital) là vùng không gian xung quanh hạt nhân nguyên tử, nơi có xác suất cao nhất tìm thấy electron, khoảng trên 90%
⇒ Chọn đáp án C Đáp án: C
- Orbital nguyên tử (AO - Atomic Orbital) là vùng không gian xung quanh hạt nhân nguyên tử, nơi có xác suất cao nhất tìm thấy electron, khoảng trên 90%
⇒ Chọn đáp án C Đáp án: C
Câu 29 [382277]: Theo mô hình hiện đại và mô hình Rutherford – Bohr
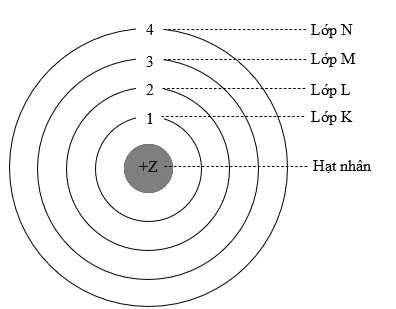
Electron thuộc lớp n = 1 sẽ có mức năng lượng như thế nào so với electron thuộc lớp n = 4?

Electron thuộc lớp n = 1 sẽ có mức năng lượng như thế nào so với electron thuộc lớp n = 4?
A, Bằng nhau.
B, Lớn hơn.
C, Nhỏ hơn.
D, Không xác định.
HƯỚNG DẪN GIẢI:
n = 1 có mức năng lượng thấp nhất, vì gần hạt nhân nhất.
n = 4 xa hạt nhân hơn, lực hút yếu hơn, dễ bị kích thích hoặc tách ra khỏi nguyên tử hơn.
⇒ Chọn đáp án C Đáp án: C
n = 1 có mức năng lượng thấp nhất, vì gần hạt nhân nhất.
n = 4 xa hạt nhân hơn, lực hút yếu hơn, dễ bị kích thích hoặc tách ra khỏi nguyên tử hơn.
⇒ Chọn đáp án C Đáp án: C
Câu 30 [382278]: Mỗi một lớp electron chỉ chứa được một lượng electron nhất định. Số electron tối đa trên một lớp được tính bằng công thức: a = 2×n2 với 
Trong đó: a là số electron tối đa trong một lớp.
n là số thứ tự của lớp electron.
Nguyên tử bromine (Br) có số hiệu nguyên tử là 35, số lớp electron tối thiểu cần để chứa hết các electron trong nguyên tử bromine là

Trong đó: a là số electron tối đa trong một lớp.
n là số thứ tự của lớp electron.
Nguyên tử bromine (Br) có số hiệu nguyên tử là 35, số lớp electron tối thiểu cần để chứa hết các electron trong nguyên tử bromine là
A, 4 lớp.
B, 3 lớp.
C, 5 lớp.
D, 2 lớp.
- Số hiệu nguyên tử của Br là 35, thay n = 4 vào công thức ta có:
a = 2×n2 = 2×42 = 32 < 35
- Nếu thay n = 5 thì a = 50 > 35 ( loại )
⇒ Chọn đáp án A Đáp án: A
a = 2×n2 = 2×42 = 32 < 35
- Nếu thay n = 5 thì a = 50 > 35 ( loại )
⇒ Chọn đáp án A Đáp án: A