Câu 1 [247336]: Trong một nhóm khi đi từ trên xuống dưới theo chiều tăng của điện tích hạt nhân bán kính nguyên tử
A, tăng.
B, giảm.
C, không đổi.
D, không có quy luật.
Trong một nhóm A, theo chiều tăng của điện tích hạt nhân, bán kính nguyên tử có xu hướng tăng dần. Đáp án: A
Câu 2 [247343]: Hình dưới đây biểu thị ngẫu nhiên bán kính của các nguyên tử Na, Mg, Al, K (không theo thứ tự):
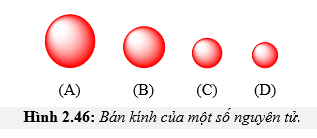 Các chất (A), (B), (C), (D) tương ứng theo thứ tự sẽ là
Các chất (A), (B), (C), (D) tương ứng theo thứ tự sẽ là

A, Na, Mg, Al, K.
B, K, Na, Mg, Al.
C, Al, Mg, Na, K.
D, K, Al, Mg, Na.
Đi từ A đến D bán kính giảm, điện tích hạt nhân tăng dần.Các chất (A), (B), (C), (D) tương ứng theo thứ tự sẽ là K, Na, Mg, Al. Đáp án: B
Câu 3 [247352]: Nguyên tử của nguyên tố nào trong nhóm VA có bán kính nguyên tử lớn nhất?
A, 7N.
B, 15P.
C, 83Bi.
D, 33As.
Trong một nhóm A, theo chiều tăng của điện tích hạt nhân, bán kính nguyên tử có xu hướng tăng dần. Đáp án: C
Câu 4 [575692]: Nguyên tử của nguyên tố nào trong nhóm VIA sau đây có bán kính nguyên tử lớn nhất?
A, 8O.
B, 16S.
C, 34Se.
D, 52Te.
Trong một nhóm, theo chiều tăng dần của điện tích hạt nhân thì bán kính nguyên tử tăng dần. Đáp án: D
Câu 5 [575693]: Nguyên tử của nguyên tố nào sau đây có bán kính nhỏ nhất?
A, Si (Z = 14).
B, P (Z = 15).
C, Ge (Z = 32).
D, As (Z = 33).
- Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân thì bán kính nguyên tử giảm dần nên bán kính của: P < Si; As < Ge.
- Trong một nhóm, theo chiều tăng dần của điện tích hạt nhân thì bán kính nguyên tử giảm dần nên bán kính của: Si < Ge; P < As.
Sắp xếp các nguyên tố theo chiều tăng dần bán kính nguyên tử là: P < Si < As < Ge Đáp án: B
- Trong một nhóm, theo chiều tăng dần của điện tích hạt nhân thì bán kính nguyên tử giảm dần nên bán kính của: Si < Ge; P < As.
Sắp xếp các nguyên tố theo chiều tăng dần bán kính nguyên tử là: P < Si < As < Ge Đáp án: B
Câu 6 [575694]: Cho các nguyên tố sau: Li, Na, K, Cs. Nguyên tử của nguyên tố có bán kính bé nhất là
A, Li.
B, Na.
C, K.
D, Cs.
Li (Z = 3), Na (Z = 11), K (Z = 19), Cs ( Z = 55) cùng thuộc nhóm IA
⇒ Bán kính Li < Na < K < Cs Đáp án: A
⇒ Bán kính Li < Na < K < Cs Đáp án: A
Câu 7 [575695]: Dãy nguyên tử nào sau đây có bán kính tăng dần?
A, F < S < Si < Ge < Ca < Rb.
B, F < Si < S < Ca < Ge < Rb.
C, Rb < Ca < Ge < Si < S < F.
D, F < Si < S < Ge < Ca < Rb.
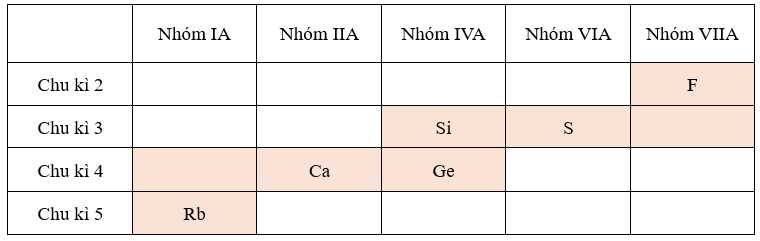
Theo quy luật biến đổi bán kính trong 1 chu kì và nhóm có bán kính các nguyên tử tăng dần theo thứ tự: F < S < Si < Ge < Ca < Rb.
Đáp án đúng là A Đáp án: A
Câu 8 [575697]: Phát biểu nào sau đây không đúng?
A, Nguyên tử có Z = 11 có bán kính nhỏ hơn nguyên tử có Z = 19.
B, Nguyên tử có Z = 12 có bán kính lớn hơn nguyên tử có Z = 10.
C, Nguyên tử có Z = 11 có bán kính nhỏ hơn nguyên tử có Z = 13.
D, Các nguyên tố kim loại kiềm có bán kính nguyên tử lớn nhất trong chu kì.
A. Nguyên tử có Z = 11 và Z = 19 thuộc cùng nhóm A (số hiệu nguyên tử chênh nhau 8 nguyên tử).
⇒ Trong một nhóm theo chiều tăng dần số hiệu nguyên tử, bán kính nguyên tử tăng dần
⇒ Nguyên tử có Z = 11 có bán kính nhỏ hơn nguyên tử có Z = 19.
⇒ Phát biểu A đúng.
B. Xét nguyên tử có Z = 12 và Z = 4 thuộc cùng nhóm A (số hiệu nguyên tử chênh nhau 8 nguyên tử) nên nguyên tử Z = 12 có bán kính lớn hơn nguyên tử có Z = 4. (1)
Xét nguyên tử có Z = 4 và Z = 10 thuộc cùng một chu kì nguyên tử có Z = 4 có bán kính lớn hơn nguyên tử có Z = 10. (2)
Từ (1) và (2) ⇒ Nguyên tử có Z = 12 có bán kính lớn hơn nguyên tử có Z = 10.
⇒ Phát biểu B đúng.
C. Nguyên tử có Z = 11 và Z = 13 thuộc cùng một chu kì
⇒ Trong một chu kì theo chiều tăng dần bán kính nguyên tử, bán kính nguyên tử giảm dần
⇒ Nguyên tử có Z = 11 có bán kính lớn hơn nguyên tử có Z = 13.
⇒ Phát biểu C sai.
D. Các nguyên tố kim loại kiềm đứng đầu chu kì nên có bán kính nguyên tử lớn nhất trong chu kì.
⇒ Phát biểu D đúng. Đáp án: C
⇒ Trong một nhóm theo chiều tăng dần số hiệu nguyên tử, bán kính nguyên tử tăng dần
⇒ Nguyên tử có Z = 11 có bán kính nhỏ hơn nguyên tử có Z = 19.
⇒ Phát biểu A đúng.
B. Xét nguyên tử có Z = 12 và Z = 4 thuộc cùng nhóm A (số hiệu nguyên tử chênh nhau 8 nguyên tử) nên nguyên tử Z = 12 có bán kính lớn hơn nguyên tử có Z = 4. (1)
Xét nguyên tử có Z = 4 và Z = 10 thuộc cùng một chu kì nguyên tử có Z = 4 có bán kính lớn hơn nguyên tử có Z = 10. (2)
Từ (1) và (2) ⇒ Nguyên tử có Z = 12 có bán kính lớn hơn nguyên tử có Z = 10.
⇒ Phát biểu B đúng.
C. Nguyên tử có Z = 11 và Z = 13 thuộc cùng một chu kì
⇒ Trong một chu kì theo chiều tăng dần bán kính nguyên tử, bán kính nguyên tử giảm dần
⇒ Nguyên tử có Z = 11 có bán kính lớn hơn nguyên tử có Z = 13.
⇒ Phát biểu C sai.
D. Các nguyên tố kim loại kiềm đứng đầu chu kì nên có bán kính nguyên tử lớn nhất trong chu kì.
⇒ Phát biểu D đúng. Đáp án: C
Câu 9 [575698]: Cấu hình electron nào sau đây ứng với nguyên tố có độ âm điện lớn nhất?
A, 1s22s22p5.
B, 1s22s22p6.
C, 1s22s22p63s1.
D, 1s22s22p63s23p2.
Ta có: 1s22s22p5 là cấu hình electron của fluorine (Z = 9), đây là nguyên tố có độ âm điện lớn nhất trong bảng tuần hoàn (3,98). Đáp án: A
Câu 10 [575699]: Độ âm điện của các nguyên tố F, Cl, Br và I xếp theo chiều giảm dần là
A, Cl > F > I > Br.
B, I > Br > Cl > F.
C, F > Cl > Br > I.
D, I > Br > F > Cl.
F, Cl, Br, I cùng thuộc nhóm VIIA. Trong một nhóm theo chiều tăng dần của điện tích hạt nhân, độ âm điện giảm dần.
⇒ Độ âm điện xếp theo chiều giảm dần là F > Cl > Br > I Đáp án: C
⇒ Độ âm điện xếp theo chiều giảm dần là F > Cl > Br > I Đáp án: C
Câu 11 [247381]: Sự biến đổi độ âm điện của các nguyên tố: 11Na, 12Mg, 13Al, 15P, 17Cl là
A, không thay đổi.
B, tăng dần.
C, không xác định.
D, giảm dần.
Các nguyên tố: 11Na, 12Mg, 13Al, 15P, 17Cl thuộc cùng một chu kì.
⇒ Trong một chu kì, độ âm điện tăng dần. Đáp án: B
⇒ Trong một chu kì, độ âm điện tăng dần. Đáp án: B
Câu 12 [247342]: Cho các nguyên tử X, Y, T, R thuộc cùng một chu kỳ và thuộc nhóm A trong bảng tuần hoàn hóa học. Bán kính nguyên tử của các nguyên tố được biểu diễn như hình sau:
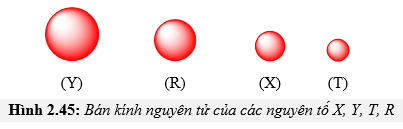 Nguyên tố có độ âm điện lớn nhất là
Nguyên tố có độ âm điện lớn nhất là

A, Y.
B, T.
C, X.
D, R.
Đi từ Y đến T bán kính giảm dần, độ âm điện tăng dần ⇒ Nguyên tố có độ âm điện lớn nhất là T. Đáp án: B
Câu 13 [575700]: Trong liên kết H-X (với X là F, Cl, Br), cặp electron trong liên kết sẽ bị lệch về nguyên tử X do chúng có độ âm điện lớn hơn H. Hãy sắp xếp các nguyên tử X theo chiều giảm dần mức độ lệch của cặp electron liên kết về phía nó.
A, Br > Cl > F.
B, Cl > F > Br.
C, F > Cl > Br.
D, Mức độ lệch của cặp electron là như nhau trong ba trường hợp.
Thứ tự đúng là: F > Cl > Br vì độ âm điện F > Cl > Br (các nguyên tố trong cùng một nhóm VIIA). Đáp án: C
Câu 14 [575701]: Dãy các nguyên tố nào sau đây được sắp xếp theo chiều giảm dần tính kim loại?
A, Sr > Al > P > Si > N.
B, Sr > Al > P > N > Si.
C, Sr > Al > Si > P > N.
D, Sr > Si > Al > P > N.
- Trong một nhóm theo chiều tăng dần của điện tích hạt nhân, tính kim loại tăng dần.
- Trong một chu kì theo chiều tăng dần của điện tích hạt nhân, tính kim loại giảm dần.
→ Thứ tự giảm dần tính kim loại: Sr > Al > Si > P > N. Đáp án: C
- Trong một chu kì theo chiều tăng dần của điện tích hạt nhân, tính kim loại giảm dần.
→ Thứ tự giảm dần tính kim loại: Sr > Al > Si > P > N. Đáp án: C
Câu 15 [247347]: Cho các nguyên tố 4Be, 3Li, 11Na, 19K. Nguyên tố có tính kim loại mạnh nhất là
A, Be.
B, Li.
C, Na.
D, K.
11Na, 19K thuộc nhóm IA, tính kim loại tăng theo chiều tăng điện tích hạt nhân.
Nguyên tố có tính kim loại mạnh nhất là K. Đáp án: D
Nguyên tố có tính kim loại mạnh nhất là K. Đáp án: D
Câu 16 [247345]: Hình 2.48 biểu thị bán kính nguyên tử theo chiều tăng dần điện tích hạt nhân của nguyên tử a, b, c, d tử thuộc cùng một chu kỳ trong bảng tuần hoàn.
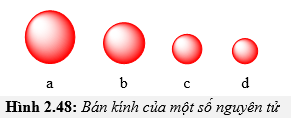 Tính kim loại giảm dần theo thứ tự nào sau đây?
Tính kim loại giảm dần theo thứ tự nào sau đây?

A, a > b > c > d.
B, d > c > b > a.
C, a > c > b > d.
D, d > b > c > a.
Trong 1 chu kì bán kính giảm dần theo thứ tự đi từ a đến d.
Tính kim loại giảm dần ⇒ a > b > c > d. Đáp án: A
Tính kim loại giảm dần ⇒ a > b > c > d. Đáp án: A
Câu 17 [575703]: Phát biểu nào sau đây là đúng về xu hướng biến đổi tính kim loại trong bảng tuần hoàn các nguyên tố hóa học?
A, Tính kim loại của các nguyên tố tăng theo chiều từ trái sang phải trong một chu kì và từ trên xuống dưới trong một nhóm.
B, Tính kim loại giảm dần theo chiều từ trái sang phải trong một chu kì và tăng dần từ trên xuống dưới trong một nhóm.
C, Tính kim loại giảm dần theo chiều từ trái sang phải trong một chu kì và từ trên xuống dưới trong một nhóm.
D, Tính kim loại tăng dần theo chiều từ trái sang phải trong một chu kì và giảm dần từ trên xuống dưới trong một nhóm.
Tính kim loại giảm dần theo chiều từ trái sang phải trong một chu kì và tăng dần từ trên xuống dưới trong một nhóm. Đáp án: B
Câu 18 [247346]: Cho các nguyên tố 9F, 14Si, 16S, 17Cl. Chiều giảm dần tính phi kim của chúng là
A, F > Cl > S > Si.
B, F > Cl > Si > S.
C, Si > S > F > Cl.
D, Si > S > Cl > F.
14Si, 16S, 17Cl thuộc cùng 1 chu kì ⇒ tính phi kim tăng dần, vậy Cl > Si > S.
9F và 17Cl thuộc cùng 1 nhóm ⇒ tính phi kim giảm dần, vậy F > Cl. Đáp án: A
9F và 17Cl thuộc cùng 1 nhóm ⇒ tính phi kim giảm dần, vậy F > Cl. Đáp án: A
Câu 19 [247337]: Nguyên tử của nguyên tố nào sau đây có tính phi kim mạnh nhất? Cho biết nguyên tố này có trong thành phần của hợp chất teflon, được sử dụng để tráng chảo chống dính.


Hình 2.44. Teflon tạo ra độ chống dính cho chảo
A, Fluorine.
B, Bromine.
C, Phosphorus.
D, Iodine.
HƯỚNG DẪN GIẢI:
- Trong một nhóm, theo chiều tăng dần số khối thì tính phi kim giảm dần.
- Trong một chu kỳ, theo chiều tăng dần số khối thì tính phi kim tăng dần
⟹ Fluorine có tính phi kim mạnh nhất.
⟹ Chọn đáp án: A Đáp án: A
- Trong một nhóm, theo chiều tăng dần số khối thì tính phi kim giảm dần.
- Trong một chu kỳ, theo chiều tăng dần số khối thì tính phi kim tăng dần
⟹ Fluorine có tính phi kim mạnh nhất.
⟹ Chọn đáp án: A Đáp án: A
Câu 20 [575704]: Trong các nguyên tố O, F, Cl, Se, nguyên tố có tính phi kim mạnh nhất là
A, O.
B, F.
C, Se.
D, Cl.
- Trong một nhóm, tính phi kim giảm dần theo chiều tăng của điện tích hạt nhân.
F (Z = 9) và Cl (Z = 17) đều thuộc nhóm VIIA nên tính phi kim của F > Cl.
O (Z = 8) và Se (Z = 34) đều thuộc nhóm VIA nên tính phi kim của O > Se.
- Trong một chu kì, tính phi kim tăng dần theo chiều tăng của điện tích hạt nhân.
O (Z = 8) và F (Z =9) đều thuộc chu kì 2 nên tính phi kim của F > O. Đáp án: B
F (Z = 9) và Cl (Z = 17) đều thuộc nhóm VIIA nên tính phi kim của F > Cl.
O (Z = 8) và Se (Z = 34) đều thuộc nhóm VIA nên tính phi kim của O > Se.
- Trong một chu kì, tính phi kim tăng dần theo chiều tăng của điện tích hạt nhân.
O (Z = 8) và F (Z =9) đều thuộc chu kì 2 nên tính phi kim của F > O. Đáp án: B
Câu 21 [575705]: Cho các nguyên tố X, Y, Z có số hiệu nguyên tử lần lượt là 6, 9, 14. Thứ tự tính phi kim tăng dần của các nguyên tố đó là
A, X < Z < Y.
B, Z < X < Y.
C, Z < Y < X.
D, Y < X < Z.
Cấu hình electron:
6X: 1s22s22p2
9Y: 1s22s22p5
14Z: 1s22s22p63s23p2
6X và 9Y thuộc chu kì 2 và 14Z thuộc chu kì 3.
9Y thuộc nhóm VIIA, 6X thuộc nhóm IVA, 14Z thuộc nhóm IVA.
Tính phi kim giảm dần trong một trong một nhóm và tăng dần tròn một chu kì theo chiều tăng dần của điện tích hạt nhân.
→ Thứ tự tính phi kim tăng dần là Z < X < Y. Đáp án: B
6X: 1s22s22p2
9Y: 1s22s22p5
14Z: 1s22s22p63s23p2
6X và 9Y thuộc chu kì 2 và 14Z thuộc chu kì 3.
9Y thuộc nhóm VIIA, 6X thuộc nhóm IVA, 14Z thuộc nhóm IVA.
Tính phi kim giảm dần trong một trong một nhóm và tăng dần tròn một chu kì theo chiều tăng dần của điện tích hạt nhân.
→ Thứ tự tính phi kim tăng dần là Z < X < Y. Đáp án: B
Câu 22 [575706]: Dãy nguyên tố nào sau đây được xếp theo chiều tăng dần tính phi kim?
A, N, P, As, Bi.
B, F, Cl, Br, I.
C, C, Si, Ge, Sn.
D, Te, Se, S, O.
A. N, P, As, Bi thuộc cùng một nhóm.
⇒ Tính phi kim tăng dần theo chiều Bi < As < P < N.
B. F, Cl, Br, I thuộc cùng một nhóm.
⇒ Tính phi kim tăng dần theo chiều I < Br < Cl < F.
C. C, Si, Ge, Sn thuộc cùng một nhóm.
⇒ Tính phi kim tăng dần theo chiều Sn < Ge < Si < C.
D. Te, Se, S, O thuộc cùng một nhóm.
⇒ Tính phi kim tăng dần theo chiều Te < Se < S < O
⇒ Chọn D Đáp án: D
⇒ Tính phi kim tăng dần theo chiều Bi < As < P < N.
B. F, Cl, Br, I thuộc cùng một nhóm.
⇒ Tính phi kim tăng dần theo chiều I < Br < Cl < F.
C. C, Si, Ge, Sn thuộc cùng một nhóm.
⇒ Tính phi kim tăng dần theo chiều Sn < Ge < Si < C.
D. Te, Se, S, O thuộc cùng một nhóm.
⇒ Tính phi kim tăng dần theo chiều Te < Se < S < O
⇒ Chọn D Đáp án: D
Câu 23 [575707]: Bốn nguyên tố A, E, M, Q cùng thuộc một nhóm A trong bảng tuần hoàn, có số hiệu nguyên tử lần lượt là 9, 17, 35, 53. Các nguyên tố này được sắp xếp theo chiều tính phi kim tăng dần theo dãy nào sau đây?
A, A, Q, E, M.
B, Q, M, E, A.
C, A, E, M, Q.
D, A, M, E, Q.
Xét vị trí các nguyên tố trong bảng tuần hoàn:
A: số hiệu nguyên tử = 9 ⇒ nhóm VIIA, chu kì 2
E: số hiệu nguyên tử = 17 ⇒ nhóm VIIA, chu kì 3
M: số hiệu nguyên tử = 35 ⇒ nhóm VIIA, chu kì 4
Q: số hiệu nguyên tử = 53 ⇒ nhóm VIIA, chu kì 5
- Cả 4 nguyên tố đều thuộc nhóm VIIA.
- Trong cùng 1 nhóm, theo chiều tăng dần điện tích hạt nhân, tính phi kim giảm dần
⇒ Sắp xếp theo chiều tính phi kim tăng dần: Q < M < E < A Đáp án: B
A: số hiệu nguyên tử = 9 ⇒ nhóm VIIA, chu kì 2
E: số hiệu nguyên tử = 17 ⇒ nhóm VIIA, chu kì 3
M: số hiệu nguyên tử = 35 ⇒ nhóm VIIA, chu kì 4
Q: số hiệu nguyên tử = 53 ⇒ nhóm VIIA, chu kì 5
- Cả 4 nguyên tố đều thuộc nhóm VIIA.
- Trong cùng 1 nhóm, theo chiều tăng dần điện tích hạt nhân, tính phi kim giảm dần
⇒ Sắp xếp theo chiều tính phi kim tăng dần: Q < M < E < A Đáp án: B
Câu 24 [575708]: Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân nguyên tử thì
A, bán kính nguyên tử và độ âm điện đều giảm.
B, bán kính nguyên tử và độ âm điện đều tăng.
C, bán kính nguyên tử tăng, độ âm điện giảm.
D, bán kính nguyên tử giảm, độ âm điện tăng.
- Trong một chu kì, tuy nguyên tử các nguyên tố có cùng số lớp electron, nhưng khi điện tích hạt nhân tăng, lực hút giữa hạt nhân với các electron lớp ngoài cùng cũng tăng theo, do đó bán kính nguyên tử giảm dần.
- Trong một chu kì, theo chiều tăng của điện tích hạt nhân thì năng lượng ion hóa, độ âm điện tăng dần. Đáp án: D
- Trong một chu kì, theo chiều tăng của điện tích hạt nhân thì năng lượng ion hóa, độ âm điện tăng dần. Đáp án: D
Câu 25 [247333]: Trong một chu kì, khi đi từ trái sang phải theo chiều tăng dần của điện tích hạt nhân, giá trị nào dưới đây không thay đổi?
A, Độ âm điện.
B, Năng lượng ion hóa.
C, Điện tích hạt nhân.
D, Số lớp electron.
Chu kì là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron, được xếp theo chiều điện tích hạt nhân tăng dần. Đáp án: D
Câu 26 [247334]: Khoảng cách trung bình giữa hạt nhân và electron lớp ngoài cùng được gọi là
A, số nguyên tử.
B, khối lượng nguyên tử.
C, bán kính nguyên tử.
D, độ âm điện.
Khoảng cách trung bình giữa hạt nhân và electron lớp ngoài cùng được gọi là bán kính nguyên tử. Đáp án: C
Câu 27 [575712]: Trong một nhóm A (trừ nhóm VIIIA), theo chiều tăng của điện tích hạt nhân nguyên tử,
A, tính kim loại tăng dần, độ âm điện tăng dần.
B, tính phi kim giảm dần, bán kính nguyên tử tăng dần.
C, độ âm điện giảm dần, tính phi kim tăng dần.
D, tính kim loại tăng dần, bán kính nguyên tử giảm dần.
Trong một nhóm A (trừ nhóm VIIIA) theo chiều tăng dần của điện tích hạt nhân:
- Số lớp electron tăng dần, bán kính nguyên tử các nguyên tố tăng theo, mặc dù điện tích hạt nhân tăng nhanh → D sai.
- Độ âm điện các nguyên tố giảm dần → C sai.
- Do năng lượng ion hóa, độ âm điện giảm dần đồng thời bán kính nguyên tử tăng nhanh làm cho khả năng nhường electron tăng nên tính kim loại tăng, khả năng nhận electron giảm nên tính phi kim giảm → A sai.
→ Chọn B. Đáp án: B
- Số lớp electron tăng dần, bán kính nguyên tử các nguyên tố tăng theo, mặc dù điện tích hạt nhân tăng nhanh → D sai.
- Độ âm điện các nguyên tố giảm dần → C sai.
- Do năng lượng ion hóa, độ âm điện giảm dần đồng thời bán kính nguyên tử tăng nhanh làm cho khả năng nhường electron tăng nên tính kim loại tăng, khả năng nhận electron giảm nên tính phi kim giảm → A sai.
→ Chọn B. Đáp án: B
Câu 28 [246577]: Trong chu kì 2 và chu kì 3, đi từ trái sang phải theo chiều tăng của điện tích hạt nhân thì nhận xét nào sau đây đúng?
A, Tính kim loại và phi kim đều giảm.
B, Tính kim loại và phi kim đều tăng.
C, Tính kim loại tăng dần, tính phi kim giảm dần.
D, Tính kim loại giảm dần, tính phi kim tăng dần.
Trong 1 chu kì theo chiều tăng dần của điện tích hạt nhân, tính kim loại giảm dần, tính phi kim tăng dần. Đáp án: D
Câu 29 [575711]: Phát biểu nào sau đây không đúng?
A, Nguyên tử có bán kính nhỏ nhất có Z = 1.
B, Kim loại yếu nhất trong nhóm IA có Z = 3.
C, Nguyên tố có độ âm điện lớn nhất có Z = 9.
D, Phi kim mạnh nhất trong nhóm VA có Z = 7.
Trong cùng một chu kì, theo chiều tăng dần của điện tích hạt nhân thì bán kính nguyên tử có xu hướng giảm dần nên rH (Z = 1) > rHe (Z = 2)
→ Nguyên tử có bán kính nhỏ nhất có Z = 2 Đáp án: A
→ Nguyên tử có bán kính nhỏ nhất có Z = 2 Đáp án: A
Câu 30 [575718]: Cho các tính chất và đặc điểm cấu tạo nguyên tử của các nguyên tố hoá học:
(a) Hoá trị cao nhất đối với oxygen. (b) Khối lượng nguyên tử.
(c) Số electron hóa trị. (d) Tính phi kim.
(e) Bán kính nguyên tử. (g) Tính kim loại.
Có bao nhiêu tính chất biến đổi tuần hoàn theo chiều tăng điện tích hạt nhân nguyên tử?
(a) Hoá trị cao nhất đối với oxygen. (b) Khối lượng nguyên tử.
(c) Số electron hóa trị. (d) Tính phi kim.
(e) Bán kính nguyên tử. (g) Tính kim loại.
Có bao nhiêu tính chất biến đổi tuần hoàn theo chiều tăng điện tích hạt nhân nguyên tử?
Các tính chất biến đổi tuần hoàn theo chiều tăng điện tích hạt nhân nguyên tử gồm có:
(a) Hoá trị cao nhất đối với oxygen.
(c) Số electron hóa trị.
(d) Tính phi kim.
(e) Bán kính nguyên tử.
(g) Tính kim loại.
⇒ Điền đáp án: 5
(a) Hoá trị cao nhất đối với oxygen.
(c) Số electron hóa trị.
(d) Tính phi kim.
(e) Bán kính nguyên tử.
(g) Tính kim loại.
⇒ Điền đáp án: 5
Câu 31 [575719]: Bốn nguyên tố A, E, M, Q cùng thuộc một nhóm A trong bảng tuần hoàn, có số hiệu nguyên tử lần lượt là 9, 17, 35, 53. Số hiệu nguyên tử của nguyên tố có tính phi kim mạnh nhất là bao nhiêu?
Trong một nhóm, theo chiều tăng dần của điện tích hạt nhân, tính kim loại của các nguyên tố tăng dần, tính phi kim giảm dần.
⇒ Sắp xếp theo chiều tính phi kim tăng dần: Q < M < E < A.
⇒ Số hiệu nguyên tử của nguyên tố có tính phi kim mạnh nhất là 9
⇒ Điền đáp án: 9
⇒ Sắp xếp theo chiều tính phi kim tăng dần: Q < M < E < A.
⇒ Số hiệu nguyên tử của nguyên tố có tính phi kim mạnh nhất là 9
⇒ Điền đáp án: 9
Câu 32 [575720]: Cho X, Y, Z, T là các nguyên tố khác nhau trong số bốn nguyên tố: 11Na, 12Mg, 13Al, 19K và các tính chất được ghi trong bảng sau:
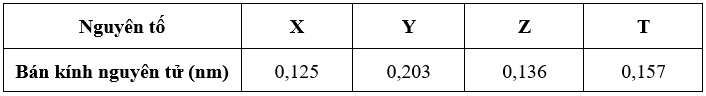
Số hiệu nguyên tử của nguyên tố Y là bao nhiêu?

Số hiệu nguyên tử của nguyên tố Y là bao nhiêu?
Từ trên xuống dưới trong 1 nhóm, bán kính nguyên tử tăng dần ⟹ K > Na
Trong cùng 1 chu kì thì từ trái sang phải, bán kính nguyên tử giảm
⟹ Na > Mg > Al
⟹ K > Na > Mg > Al
⟹ Y > T > Z > X.
⟹ Số hiệu nguyên tử của nguyên tố Y là 19
⟹ Điền đáp án: 19
Trong cùng 1 chu kì thì từ trái sang phải, bán kính nguyên tử giảm
⟹ Na > Mg > Al
⟹ K > Na > Mg > Al
⟹ Y > T > Z > X.
⟹ Số hiệu nguyên tử của nguyên tố Y là 19
⟹ Điền đáp án: 19
Đọc đoạn thông tin sau và trả lời các câu hỏi từ 33 đến 35:
BÁN KÍNH NGUYÊN TỬ
Theo trực giác, chúng ta thường nghĩ bán kính nguyên tử (r) là khoảng cách giữa hạt nhân của một nguyên tử với lớp vỏ electron hóa trị của nó (tức là lớp vỏ ngoài cùng bị chiếm giữ bởi một hoặc nhiều electron), điều này cũng dễ hiểu bởi vì chúng ta thường hình dung các nguyên tử giống như những quả cầu có ranh giới rời rạc.Tuy nhiên, theo mô hình cơ học lượng tử của nguyên tử, không có khoảng cách cụ thể nào từ hạt nhân mà ngoài đó không thể tìm thấy electron. Do đó, bán kính nguyên tử đòi hỏi phải có một định nghĩa cụ thể.
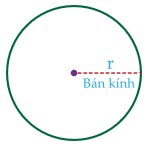
Có hai cách xác định bán kính nguyên tử. Một là bán kính kim loại, bằng một nửa khoảng cách giữa hạt nhân của hai nguyên tử kim loại giống hệt nhau và liền kề với nhau hình 1. Cách còn lại là bán kính cộng hóa trị, bằng một nửa khoảng cách giữa các hạt nhân giống hệt nhau, liền kề nhau trong một phân tử hình 2.
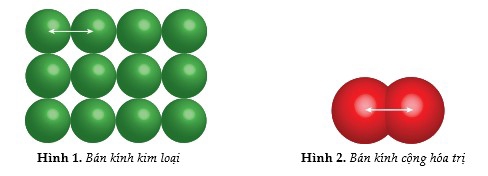
Hình 3 cho thấy bán kính nguyên tử của các nguyên tố nhóm chính theo vị trí của chúng trong bảng tuần hoàn. Có hai xu hướng biến đổi riêng biệt: Xu hướng biến đổi theo chu kì và xu hướng biến đổi theo nhóm.
Câu 33 [382291]: Một nửa khoảng cách giữa các hạt nhân giống hệt nhau, liền kề nhau trong một phân tử gọi là
A, Bán kính phân tử.
B, Bán kính kim loại.
C, Đường kính nguyên tử.
D, Bán kính cộng hóa trị.
HƯỚNG DẪN GIẢI:
- Gọi bán kính của một nguyên tử (khoảng cách từ hạt nhân đến lớp ngoài cùng) là R.
- Khoảng cách giữa hai hạt nhân giống hệt nhau, hai nguyên tử đặt cạnh nhau là 2R. Vậy một nửa của 2R là R, tức là bán kính nguyên tử, hay bán kính cộng hóa trị.
⟹ Chọn đáp án: D Đáp án: D
- Gọi bán kính của một nguyên tử (khoảng cách từ hạt nhân đến lớp ngoài cùng) là R.
- Khoảng cách giữa hai hạt nhân giống hệt nhau, hai nguyên tử đặt cạnh nhau là 2R. Vậy một nửa của 2R là R, tức là bán kính nguyên tử, hay bán kính cộng hóa trị.
⟹ Chọn đáp án: D Đáp án: D
Câu 34 [382292]: Dựa vào kích thước và chỉ sử dụng hình 7.6, hãy chỉ ra rằng:
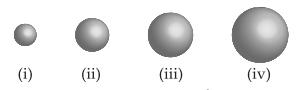
Các nguyên tử của các nguyên tố: Al, B, Mg và Sr tương ứng với quả cầu nào?

Các nguyên tử của các nguyên tố: Al, B, Mg và Sr tương ứng với quả cầu nào?
A, Quả cầu (iv) là Mg.
B, Quả cầu (i) là Al.
C, Quả cầu (iii) là Mg.
D, Quả cầu (ii) là B.
HƯỚNG DẪN GIẢI:
- Sr nằm cùng nhóm với Mg và có ZSr > ZMg nên RSr > RMg
- Mg nằm cùng chu kỳ với Al và có ZMg < ZAl nên RMg > RAl
- Al nằm cùng nhóm với B và có ZAl > ZB nên RAl > RB
⟹ Vậy RSr > RMg > RAl > RB
⟹ Chọn đáp án: C Đáp án: C
- Sr nằm cùng nhóm với Mg và có ZSr > ZMg nên RSr > RMg
- Mg nằm cùng chu kỳ với Al và có ZMg < ZAl nên RMg > RAl
- Al nằm cùng nhóm với B và có ZAl > ZB nên RAl > RB
⟹ Vậy RSr > RMg > RAl > RB
⟹ Chọn đáp án: C Đáp án: C
Câu 35 [247358]: Khẳng định nào đúng khi nói về bán kính nguyên tử?
A, Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, bán kính nguyên tử có xu hướng tăng dần.
B, Trong một nhóm, theo chiều từ trên xuống dưới, bán kính nguyên tử có xu hướng giảm dần.
C, Trong một chu kì, số lớp electron giữ nguyên, điện tích hạt nhân tăng dần làm tăng lực hút, dẫn tới bán kính nguyên tử giảm dần.
D, Trong một nhóm, theo chiều từ trên xuống dưới, số lớp electron tăng dần nên bán kính nguyên tử có xu hướng giảm dần.
Trong 1 chu kì theo chiều tăng dần điện tích hạt nhân, bán kính nguyên tử giảm dần do số lớp electron giữ nguyên, điện tích hạt nhân tăng dần làm tăng lực hút, dẫn tới bán kính nguyên tử giảm dần. Đáp án: C