Câu 1 [575865]: Cặp nguyên tố nào sau đây có thể tạo thành hợp chất ion?
A, Argon và chlorine.
B, Calcium và bromine.
C, Sodium và potassium.
D, Aluminium và magnesium.
Liên kết ion được tạo thành giữa kim loại điển hình và phi kim điển hình.
Vậy liên kết giữa calcium và bromine là liên kết ion. Đáp án: B
Vậy liên kết giữa calcium và bromine là liên kết ion. Đáp án: B
Câu 2 [244132]: Cặp nguyên tử nào dưới đây liên kết với nhau tạo hợp chất cộng hoá trị?
A, H và He.
B, Na và F.
C, Li và F.
D, H và Cl.
HƯỚNG DẪN GIẢI:
❌ A SAI. Neon là khí hiếm, không có khả năng tạo liên kết với các nguyên tử nguyên tố khác.
❌ B SAI. Na là một kim loại điển hình, F là phi kim điển hình ⟹ Liên kết trong phân tử NaF là liên kết ion, Na cho 1 electron để đạt cấu hình bền, F nhận thêm 1 e để đạt cấu hình bền.
❌ C SAI. Giống như trường hợp của NaF.
✔️ D ĐÚNG. Phân tử HCl có liên kết cộng hóa trị, H góp 1e, Cl góp 1e tạo thành 2 e dùng chung.
⟹ Chọn đáp án: D Đáp án: D
❌ A SAI. Neon là khí hiếm, không có khả năng tạo liên kết với các nguyên tử nguyên tố khác.
❌ B SAI. Na là một kim loại điển hình, F là phi kim điển hình ⟹ Liên kết trong phân tử NaF là liên kết ion, Na cho 1 electron để đạt cấu hình bền, F nhận thêm 1 e để đạt cấu hình bền.
❌ C SAI. Giống như trường hợp của NaF.
✔️ D ĐÚNG. Phân tử HCl có liên kết cộng hóa trị, H góp 1e, Cl góp 1e tạo thành 2 e dùng chung.
⟹ Chọn đáp án: D Đáp án: D
Câu 3 [243437]: Nguyên tử fluorine có cấu hình electron là: 1s22s22p5. Sau khi tạo liên kết ion, trong hợp chất nó tồn tại dưới dạng ion fluoride. Kí hiệu của ion fluoride là
A, F–.
B, F+.
C, F2–.
D, F.
Nguyên tử fluorine có 9 electron nên khi tham gia liên kết có xu hướng nhận thêm 1 electron để đạt cấu hình của nguyên tử nguyên tố khí hiếm gần nhất là neon (Z = 10), tạo thành anion F- Đáp án: A
Câu 4 [575862]: Công thức phân tử của hợp chất tạo thành giữa ion Al3+ và S2- là
A, Al2S3.
B, AlS.
C, Al3S2.
D, AlS2.
HD:
+) Ion Al³⁺: mang điện tích +3.
+) Ion S²⁻: mang điện tích –2.
Để trung hòa điện tích: Cần 2 ion Al³⁺ (tổng +6) và 3 ion S²⁻ (tổng –6).
➱ Công thức phân tử: Al₂S₃.
Đáp án đúng: A. Al2S3 Đáp án: A
+) Ion Al³⁺: mang điện tích +3.
+) Ion S²⁻: mang điện tích –2.
Để trung hòa điện tích: Cần 2 ion Al³⁺ (tổng +6) và 3 ion S²⁻ (tổng –6).
➱ Công thức phân tử: Al₂S₃.
Đáp án đúng: A. Al2S3 Đáp án: A
Câu 5 [560599]: Liên kết kim loại được hình thành bởi
A, Lực hút tĩnh điện giữa các nguyên tử.
B, Lực hút tĩnh điện giữa các hạt tích điện dương và các electron hóa trị tự do.
C, Lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
D, Lực hút tĩnh điện giữa hạt nhân hai nguyên tử và cặp electron dùng chung.
Liên kết kim loại là liên kết hình thành từ lực hút tĩnh điện giữa các cation kim loại và các electron hóa trị tự do trong tinh thể kim loại. Đáp án: B
Câu 6 [244127]: Liên kết hóa học trong phân tử Br2 thuộc loại liên kết
A, cộng hoá trị không cực.
B, hydrogen.
C, cộng hoá trị có cực.
D, ion.
HƯỚNG DẪN GIẢI:
- Công thức Lewis của Br2 như sau:
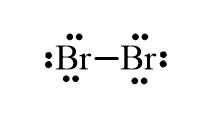
- Liên kết giữa hai nguyên tử Br được hình thành do sự dùng chung 1 cặp electron ⟹ Đây là liên kết cộng hoá trị.
- Do hai nguyên tử Br giống nhau nên lực hút lên cặp electron giống nhau ⟹ Cặp e không lệch về bên nào nên phân tử Br2 không phân cực.
⟹ Chọn đáp án: A Đáp án: A
- Công thức Lewis của Br2 như sau:
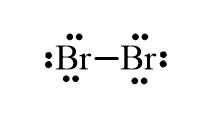
- Liên kết giữa hai nguyên tử Br được hình thành do sự dùng chung 1 cặp electron ⟹ Đây là liên kết cộng hoá trị.
- Do hai nguyên tử Br giống nhau nên lực hút lên cặp electron giống nhau ⟹ Cặp e không lệch về bên nào nên phân tử Br2 không phân cực.
⟹ Chọn đáp án: A Đáp án: A
Câu 7 [244128]: Liên kết hoá học giữa các nguyên tử trong phân tử H2O là liên kết
A, cộng hoá trị không phân cực.
B, hydrogen.
C, cộng hoá trị có cực.
D, ion.
HƯỚNG DẪN GIẢI:
- Công thức Lewis của phân tử H2O là:
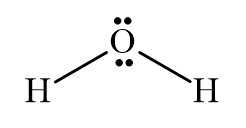
- Liên kết trong phân tử H2O được hình thành bằng sự dùng chung cặp electron giữa O và H nên đây là liên kết cộng hoá trị.
- Do O có độ âm điện lớn hơn H nên cặp electron dùng chung lệch về nguyên tử O ⟹ Phân tử H2O phân cực
⟹ Chọn đáp án: C
Đáp án: C
- Công thức Lewis của phân tử H2O là:

- Liên kết trong phân tử H2O được hình thành bằng sự dùng chung cặp electron giữa O và H nên đây là liên kết cộng hoá trị.
- Do O có độ âm điện lớn hơn H nên cặp electron dùng chung lệch về nguyên tử O ⟹ Phân tử H2O phân cực
⟹ Chọn đáp án: C
Đáp án: C
Câu 8 [242120]: Phân tử nào dưới đây “không tuân theo” quy tắc octet?
A, PCl5.
B, CH4.
C, H2S.
D, NH3.
Nguyên tử P trong PCl5 khi tham gia liên kết có 10 electron, không tuân thủ quy tắc Octet. Đáp án: A
Câu 9 [242121]: Phân tử nào dưới đây có các nguyên tử đều đạt cấu hình electron bão hòa theo quy tắc octet?
A, PCl5.
B, CH4.
C, BF3.
D, SF6.
HƯỚNG DẪN GIẢI:
- Công thức Lewis của các chất được biểu diễn như sau:
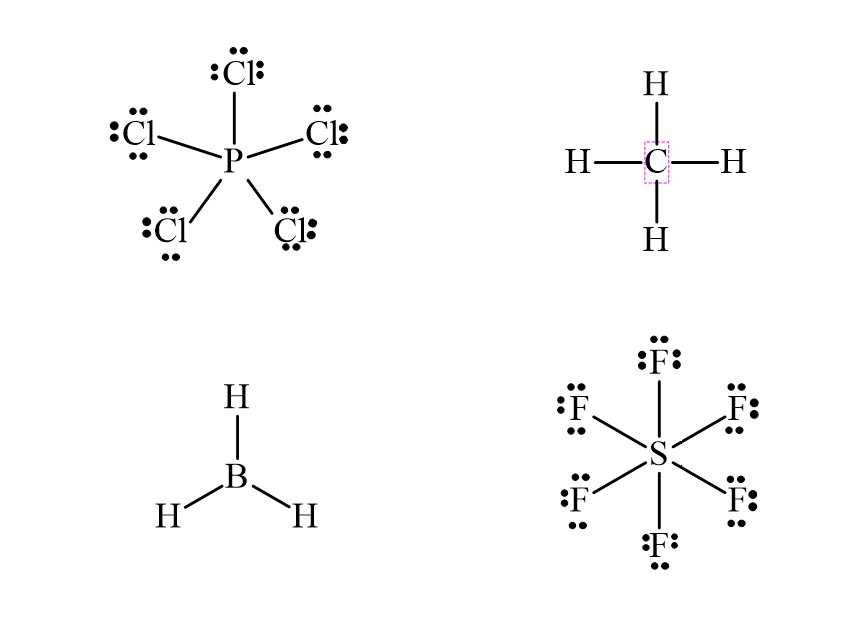
Nhìn vào hình vẽ ta nhận thấy chỉ có nguyên tử C trong CH4 có 8 electron xung quanh (Với mỗi một liên kết ứng với 2 electron)
⟹ Chọn đáp án: B Đáp án: B
- Công thức Lewis của các chất được biểu diễn như sau:

Nhìn vào hình vẽ ta nhận thấy chỉ có nguyên tử C trong CH4 có 8 electron xung quanh (Với mỗi một liên kết ứng với 2 electron)
⟹ Chọn đáp án: B Đáp án: B
Câu 10 [244164]: Phân tử nào chỉ chứa liên kết đơn?
A, N2.
B, O2.
C, F2.
D, CO2.
Giải thích:
A. N2 (Khí Nitrogen): Chứa một liên kết ba (N≡N).
B. O2 (Khí Oxygen): Chứa một liên kết đôi (O=O).
C. F2 (Khí Fluorine): Chứa một liên kết đơn (F−F).
D. CO2 (Khí Carbon dioxide): Chứa hai liên kết đôi (O=C=O).
-> Đáp án đúng là C Đáp án: C
A. N2 (Khí Nitrogen): Chứa một liên kết ba (N≡N).
B. O2 (Khí Oxygen): Chứa một liên kết đôi (O=O).
C. F2 (Khí Fluorine): Chứa một liên kết đơn (F−F).
D. CO2 (Khí Carbon dioxide): Chứa hai liên kết đôi (O=C=O).
-> Đáp án đúng là C Đáp án: C
Câu 11 [244166]: Dãy các chất nào chỉ chứa liên kết đơn?
A, C2H4; C2H6.
B, CH4; C2H6.
C, C2H4; C2H2.
D, CH4; C2H2.
Giải thích: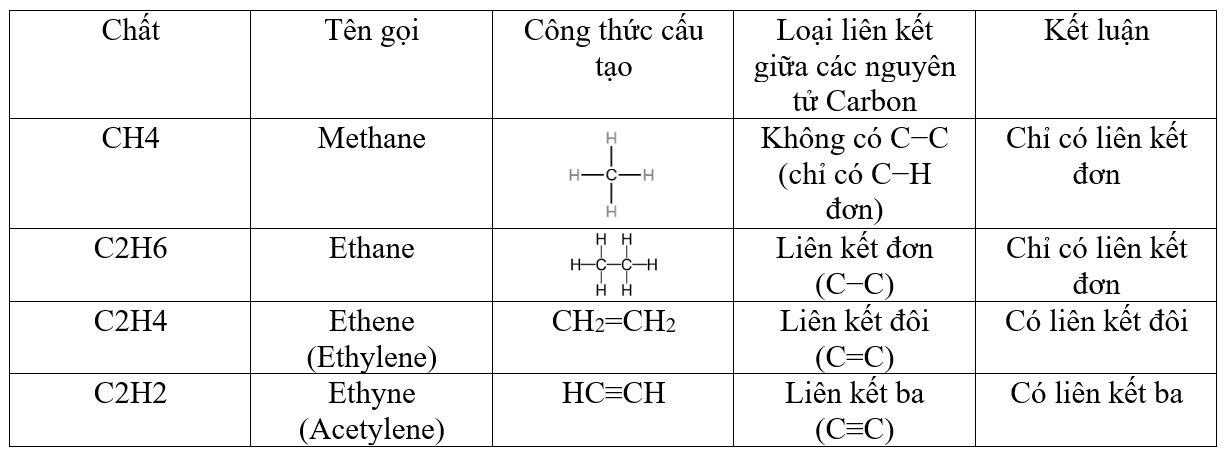
-> Đáp án đúng là: B Đáp án: B
Câu 12 [244167]: Cho các phân tử sau: C2H4, C2H2, O3, N2, CO2, CH4, NH3. Có bao nhiêu phân tử có liên kết đôi và có bao nhiêu phân tử có liên kết ba?
A, 2 và 2.
B, 3 và 2.
C, 3 và 1.
D, 2 và 1.
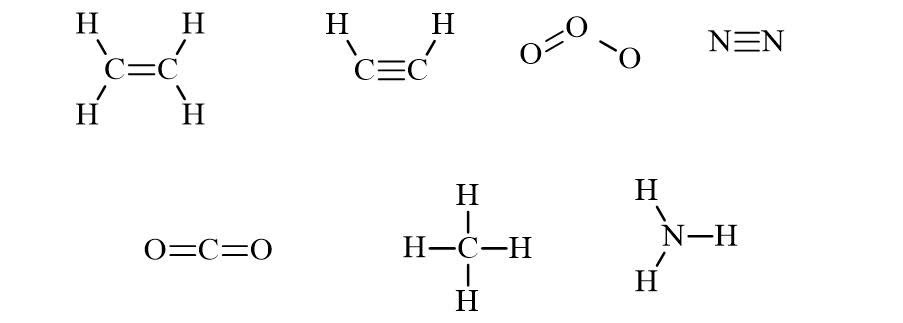
Các
phân tử có liên kết đôi là C2H4; O3; CO2
Các
phân tử có liên kết ba là C2H2, N2
Đáp
án: B. 3 và 2.
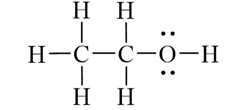
Câu 13 [1052083]: Trong phân tử CH3–CH2–OH (ethanol), nguyên tử O có bao nhiêu cặp electron không tham gia liên kết?

A, 0.
B, 1.
C, 2.
D, 3.
Từ công thức cấu tạo của ethanol, thấy rằng nguyên tử O có 2 cặp electron tham gia hình thành liên kết
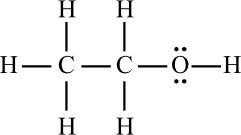
➔ Đáp án đúng C. 2. Đáp án: C

➔ Đáp án đúng C. 2. Đáp án: C
Câu 14 [1052084]: Trong công thức electron của ethylene, số electron tham gia tạo thành liên kết đôi C=C là
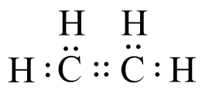
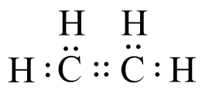
A, 2.
B, 4.
C, 6.
D, 8.
Trong công thức electron của ethylene (hình bên), số electron tham gia tạo thành liên kết đôi C=C là 4

➔ Đáp án đúng B. 4. Đáp án: B

➔ Đáp án đúng B. 4. Đáp án: B
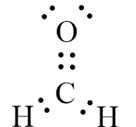
Câu 15 [1052085]: Trong phân tử HCHO (formaldehyde), giữa nguyên tử C và O có

A, 1 liên kết đơn.
B, 1 liên kết đôi.
C, 1 liên kết ba.
D, không có liên kết.
Công thức cấu tạo của HCHO là
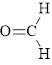
Trong công thức phân tử của HCHO (formaldehyde), giữa nguyên tử C và O có 1 liên kết đôi.
➔ Đáp án đúng B. 1 liên kết đôi. Đáp án: B

Trong công thức phân tử của HCHO (formaldehyde), giữa nguyên tử C và O có 1 liên kết đôi.
➔ Đáp án đúng B. 1 liên kết đôi. Đáp án: B
Câu 16 [244137]: Cho công thức electron của phân tử N2H4 như hình 3. Mỗi nguyên tử nitrogen còn mấy cặp electron chưa tham gia liên kết?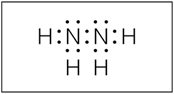

Hình 3.53. Cấu trúc của phân tử N2H4
A, 0.
B, 2.
C, 3.
D, 1.
HƯỚNG DẪN GIẢI:
- Cặp electron chưa liên kết là cặp electron không có sự dùng chung mà là "của riêng". Quan sát trong hình ta thấy mỗi nguyên tử N đều có 1 cặp e chưa liên kết.
⟹ Chọn đáp án: D Đáp án: D
- Cặp electron chưa liên kết là cặp electron không có sự dùng chung mà là "của riêng". Quan sát trong hình ta thấy mỗi nguyên tử N đều có 1 cặp e chưa liên kết.
⟹ Chọn đáp án: D Đáp án: D
Câu 17 [1052087]: CCl4 (carbon tetrachloride) được xem là một hợp chất hữu cơ vì nó chứa carbon và là dẫn xuất của methane (CH4).
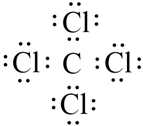
Dựa vào công thức electron của CCl4, cho biết công thức nào sau đây là công thức cấu tạo đúng của CCl4?

Dựa vào công thức electron của CCl4, cho biết công thức nào sau đây là công thức cấu tạo đúng của CCl4?
A, 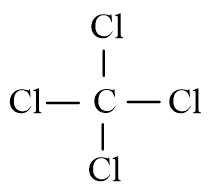
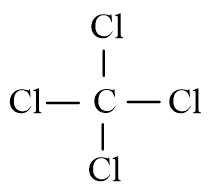
B, 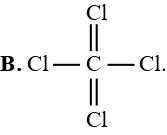

C, 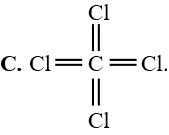
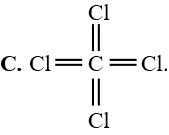
D, 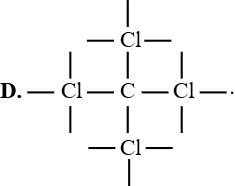

Dựa vào công thức electron của CCl4 (hình bên), cho biết công thức cấu tạo đúng
của CCl4 là
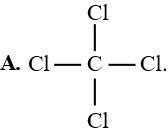
Đáp án đúng A Đáp án: A
của CCl4 là

Đáp án đúng A Đáp án: A
Câu 18 [243455]: Cho mô hình cấu tạo nguyên tử của nguyên tố X và Y như hình dưới. Nguyên tố X và Y có thể tham gia liên kết với nhau. Công thức hợp chất ion tạo thành giữa X và Y là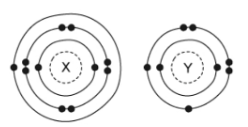

Hình 3.41. Mô hình cấu tạo nguyên tử của nguyên tố X và Y.
A, X2Y.
B, X2Y2.
C, X2Y4.
D, XY.
Để đạt cấu hình của khí hiếm bền vững thì X nhường đi 1e, Y nhận thêm 2e
=> Hình thành ion X+ và Y2-
=> Hợp chất ion tạo thành giữa X và Y là X2Y Đáp án: A
=> Hình thành ion X+ và Y2-
=> Hợp chất ion tạo thành giữa X và Y là X2Y Đáp án: A
Câu 19 [243457]: Cấu trúc nguyên tử của P và Q được biểu diễn như hình sau. Q và R hình thành nên một hợp chất ion. Công thức hợp chất tạo bởi Q và R là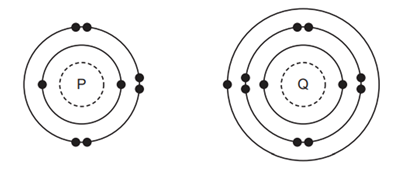

Hình . Mô hình cấu tạo nguyên tử của P và Q
A, Q2P.
B, QP2.
C, QP.
D, Q3P.
Để đạt cấu hình của khí hiếm bền vững thì P nhận thêm 2e, Q nhường đi 1e
=> Hình thành ion P2- và Q+
=> Hợp chất ion tạo thành giữa P và Q là Q2P Đáp án: A
=> Hình thành ion P2- và Q+
=> Hợp chất ion tạo thành giữa P và Q là Q2P Đáp án: A
Câu 20 [244134]: Hình dưới biểu diễn sự hình thành liên kết cộng hóa trị giữa hai nguyên tử A, B. Liên kết tạo thành có tên gọi là
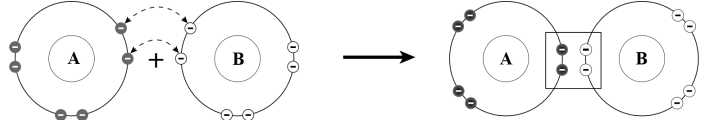

A, liên kết đơn.
B, liên kết đôi.
C, liên kết ba.
D, liên kết pi.
Trong hình ảnh, hai nguyên tử A và B góp chung hai cặp electron để tạo thành liên kết. Liên kết được hình thành do sự góp chung hai cặp electron được gọi là liên kết đôi.
⟹ Chọn đáp án B Đáp án: B
⟹ Chọn đáp án B Đáp án: B
Câu 21 [244136]: Cho mô hình cấu tạo nguyên tử của 4 nguyên tố X, Y, Z, T như hình sau:
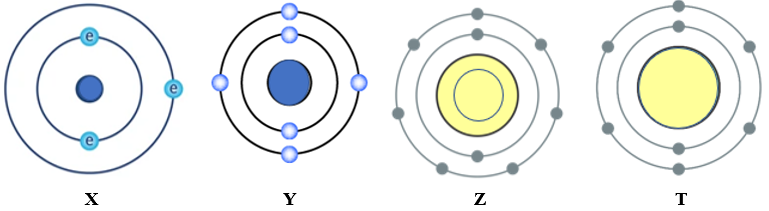

Hình 3.52. Mô hình cấu tạo nguyên tử của một số nguyên tố.
Những nguyên tố có khả năng tham gia hình thành liên kết cộng hóa trị là
A, X và Y.
B, X, Y và Z.
C, X và T.
D, Y, Z và T.
HƯỚNG DẪN GIẢI:
- Những nguyên tố có khả năng tham gia liên kết cộng hóa trị là các nguyên tố có từ 4 electron ở lớp ngoài cùng (trừ H)
⟹ Các nguyên tố thỏa mãn là: Y, Z, T
⟹ Chọn đáp án: D Đáp án: D
- Những nguyên tố có khả năng tham gia liên kết cộng hóa trị là các nguyên tố có từ 4 electron ở lớp ngoài cùng (trừ H)
⟹ Các nguyên tố thỏa mãn là: Y, Z, T
⟹ Chọn đáp án: D Đáp án: D
Câu 22 [243476]: Nguyên tử X có 20 hạt proton và nguyên tử Y có 17 hạt electron. Hợp chất hình thành giữa 2 nguyên tố này có công thức và loại liên kết tương ứng là
A, X2Y, liên kết cộng hóa trị.
B, XY2, liên kết ion.
C, XY, liên kết ion.
D, X3Y2, liên kết cộng hóa trị.
Nguyên tử X có 20 hạt proton có xu hướng nhường đi 2 electron để đạt cấu hình khí hiếm gần nhất là Argon (Z = 18) khi tham gia liên kết.
Nguyên tử Y có 17 hạt electron có xu hướng nhận thêm 1 electron để đạt cấu hình khí hiếm gần nhất là Argon (Z = 18) khi tham gia liên kết.
→ Hợp chất hình thành giữa 2 nguyên tố này có công thức là XY2 bằng liên kết ion.
Đáp án: B
Nguyên tử Y có 17 hạt electron có xu hướng nhận thêm 1 electron để đạt cấu hình khí hiếm gần nhất là Argon (Z = 18) khi tham gia liên kết.
→ Hợp chất hình thành giữa 2 nguyên tố này có công thức là XY2 bằng liên kết ion.
Đáp án: B
Câu 23 [244140]: Bảng dưới đây cho thấy cấu trúc điện tử (sự phân bố electron trên các lớp vỏ) của bốn nguyên tử X, Y, Z, W.
Hai nguyên tử nguyên tố nào có thể kết hợp với nhau tạo thành hợp chất chứa liên kết cộng hoá trị?
| Nguyên tử | Sự phân bố electron trên các lớp vỏ |
| W | 2, 8, 1 |
| X | 2, 8, 4 |
| Y | 2, 8, 7 |
| Z | 2, 8, 8 |
Hai nguyên tử nguyên tố nào có thể kết hợp với nhau tạo thành hợp chất chứa liên kết cộng hoá trị?
A, W và X.
B, W và Y.
C, X và Y.
D, X và Z.
HƯỚNG DẪN GIẢI:
- Liên kết cộng hóa trị được hình thành nhờ sự dùng chung cặp e, thường xảy ra ở các nguyên tử nguyên tố phi kim.
- Có hai nguyên tử nguyên tố phi kim là X và Y ⟹ Giữa X và Y có thể hình thành liên kết cộng hóa trị.
⟹ Chọn đáp án: C Đáp án: C
- Liên kết cộng hóa trị được hình thành nhờ sự dùng chung cặp e, thường xảy ra ở các nguyên tử nguyên tố phi kim.
- Có hai nguyên tử nguyên tố phi kim là X và Y ⟹ Giữa X và Y có thể hình thành liên kết cộng hóa trị.
⟹ Chọn đáp án: C Đáp án: C
Câu 24 [244147]: Trong các sơ đồ dưới đây các gạch chéo biểu diễn kí hiệu các electron của nguyên tử oxygen, các chấm biểu diễn các electron của carbon. Sơ đồ chấm và gạch chéo nào cho thấy sự sắp xếp các electron ở lớp vỏ ngoài cùng trong phân tử của khí carbon dioxide?
A, 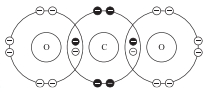

B, 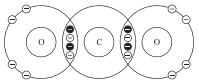

C, 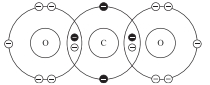

D, 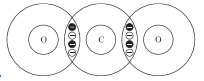

Cấu hình electron của carbon (C) và oxygen (O):
C (Z = 6): 1s22s22p2→ có 4 electron lớp ngoài cùng
O (Z = 8): 1s22s22p4 → có 6 electron lớp ngoài cùng
Theo quy tắc bát tử C cần 4 electron để đạt được cấu hình bát tử. Oxygen cần 2 electron để được cấu hình bát tử.
Suy ra mỗi nguyên tử Oxygen sẽ góp chung 2 electron và mỗi nguyên tử Carbon sẽ góp chung 4 electron chia đều cho cả hai bên.
Phân tích các phát biểu
❌Sai. A. Không đúng. Carbon không đủ liên kết
✔️Đúng. B. Carbon có 4 liên kết (4 cặp electron chia sẻ).
Oxygen có 2 liên kết (2 cặp electron chia sẻ) và 4 electron tự do (2 cặp electron không chia sẻ).
❌Sai. C. Carbon chỉ có 2 liên kết, không đủ 4 liên kết cần thiết.
Oxygen cũng không đủ electron tự do.
❌Sai. D. Carbon chỉ có 2 liên kết, không đủ 4 liên kết cần thiết.
Oxygen cũng không đủ electron tự do.
⟹ Chọn đáp án B Đáp án: B
C (Z = 6): 1s22s22p2→ có 4 electron lớp ngoài cùng
O (Z = 8): 1s22s22p4 → có 6 electron lớp ngoài cùng
Theo quy tắc bát tử C cần 4 electron để đạt được cấu hình bát tử. Oxygen cần 2 electron để được cấu hình bát tử.
Suy ra mỗi nguyên tử Oxygen sẽ góp chung 2 electron và mỗi nguyên tử Carbon sẽ góp chung 4 electron chia đều cho cả hai bên.
Phân tích các phát biểu
❌Sai. A. Không đúng. Carbon không đủ liên kết
✔️Đúng. B. Carbon có 4 liên kết (4 cặp electron chia sẻ).
Oxygen có 2 liên kết (2 cặp electron chia sẻ) và 4 electron tự do (2 cặp electron không chia sẻ).
❌Sai. C. Carbon chỉ có 2 liên kết, không đủ 4 liên kết cần thiết.
Oxygen cũng không đủ electron tự do.
❌Sai. D. Carbon chỉ có 2 liên kết, không đủ 4 liên kết cần thiết.
Oxygen cũng không đủ electron tự do.
⟹ Chọn đáp án B Đáp án: B
Câu 25 [575909]: Trong các hợp chất sau: CaCl2, HF, NH3, Fe(NO3)2, FeSO4, CO2. Những hợp chất nào chứa liên kết cộng hóa trị?
Các hợp chất chứa liên kết cộng hóa trị (phi kim - phi kim) là: HF, NH3, Fe(NO3)2, FeSO4, CO2
- HF: H-F => Liên kết cộng hoá trị có cực mạnh
- NH3: N-H => Liên kết cộng hoá trị
- Fe(NO3)2: N-O => Liên kết cộng hoá trị
- FeSO4: S-O => Liên kết cộng hoá trị
- CO2: C-O => Liên kết cộng hoá trị
⇒ Điền đáp án: 5
- HF: H-F => Liên kết cộng hoá trị có cực mạnh
- NH3: N-H => Liên kết cộng hoá trị
- Fe(NO3)2: N-O => Liên kết cộng hoá trị
- FeSO4: S-O => Liên kết cộng hoá trị
- CO2: C-O => Liên kết cộng hoá trị
⇒ Điền đáp án: 5
Câu 26 [575854]: Cho nguyên tử các nguyên tố sau: Na (Z=11), Mg (Z=12), F (Z=9), Al (Z=13), S (Z=16), Cl (Z = 17), O (Z = 8). Có bao nhiêu nguyên tử có xu hướng nhận 2 electron khi tham gia hình thành liên kết hóa học?
Số hiệu nguyên tử của các nguyên tố khí hiếm là: 10Ne, 18Ar, ...
- Na (Z = 11), Mg (Z = 12), Al (Z = 13) có xu hướng nhường electron khi tham gia hình thành liên kết hóa học.
- F (Z = 9), Cl (Z =17) có xu hướng nhận thêm 1 electron khi tham gia hình thành liên kết hóa học.
- S (Z = 16) và O (Z = 8) có xu hướng nhận thêm 2 electron khi tham gia hình thành liên kết hóa học.
Có 2 nguyên tử có xu hướng nhận 2 electron khi tham gia hình thành liên kết hóa học là S và O.
⇒ Điền đáp án: 2
- Na (Z = 11), Mg (Z = 12), Al (Z = 13) có xu hướng nhường electron khi tham gia hình thành liên kết hóa học.
- F (Z = 9), Cl (Z =17) có xu hướng nhận thêm 1 electron khi tham gia hình thành liên kết hóa học.
- S (Z = 16) và O (Z = 8) có xu hướng nhận thêm 2 electron khi tham gia hình thành liên kết hóa học.
Có 2 nguyên tử có xu hướng nhận 2 electron khi tham gia hình thành liên kết hóa học là S và O.
⇒ Điền đáp án: 2
Câu 27 [575852]: Nguyên tử nguyên tố nitrogen chuyển thành ion thì cần nhận thêm bao nhiêu electron để thoả mãn quy tắc octet?
Nguyên tử nguyên tố nitrogen có số electron là 7, có xu hướng nhận thêm 3 electron để thoả mãn quy tắc octet.
⇒ Điền đáp án: 3
⇒ Điền đáp án: 3
Đọc đoạn thông tin sau và trả lời các câu hỏi từ 28 đến 30:
CẤU TRÚC LEWIS
Các cấu trúc sử dụng để biểu diễn liên kết cộng hóa trị trong cấu tạo của phân tử, chẳng hạn như H2 và F2, được gọi là cấu trúc Lewis.
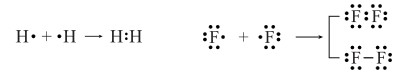
Cấu trúc Lewis là một cách biểu diễn của liên kết cộng hóa trị trong đó các cặp electron dùng chung được biểu thị dưới dạng dấu gạch ngang (–) hoặc cặp dấu chấm (..) nằm giữa hai nguyên tử, ngoài ra các cặp electron chưa tham gia liên kết được biểu thị dưới dạng cặp dấu chấm trên từng nguyên tử. Chú ý: chỉ các electron hóa trị được thể hiện trong cấu trúc Lewis.
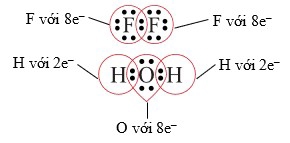
Trong các phân tử F2 và H2O, mỗi nguyên tử F, H và O đều đạt được cấu hình electron của khí hiếm ổn định bằng cách dùng chung các electron, quy tắc bát tử được minh họa như hình bên (trừ trường hợp của H).
Câu 28 [382303]: Trong các phát biểu sau, phát biểu nào đúng?
A, Cấu trúc Lewis là một cách biểu diễn của liên kết ion.
B, Trong cấu trúc Lewis, mỗi một electron được biểu diễn dưới dạng một dấu chấm.
C, Trong cấu trúc Lewis, tất cả các electron của mỗi nguyên tử đều được biểu diễn.
D, Xung quanh nguyên tử H luôn có tám electron phù hợp theo quy tắc bát tử.
HƯỚNG DẪN GIẢI:
❌ A SAI. Công thức Lewis là một cách biểu diễn của liên kết cộng hoá trị.
✔️ B ĐÚNG. Mỗi một chấm thể hiện một electron.
❌ C SAI. Công thức Lewis chỉ biểu diễn các electron hoá trị ở lớp ngoài cùng.
❌ D SAI. Hydrogen chỉ có tối đa 2 electron ở lớp ngoài cùng.
⟹ Chọn đáp án: B Đáp án: B
❌ A SAI. Công thức Lewis là một cách biểu diễn của liên kết cộng hoá trị.
✔️ B ĐÚNG. Mỗi một chấm thể hiện một electron.
❌ C SAI. Công thức Lewis chỉ biểu diễn các electron hoá trị ở lớp ngoài cùng.
❌ D SAI. Hydrogen chỉ có tối đa 2 electron ở lớp ngoài cùng.
⟹ Chọn đáp án: B Đáp án: B
Câu 29 [382304]: Dựa vào cấu trúc Lewis của phân tử H2O, có bao nhiêu electron đã tham gia để tạo thành liên kết?
A, 2.
B, 4.
C, 6.
D, 8.
HƯỚNG DẪN GIẢI:
- Công thức Lewis của H2O được biểu diễn như sau:
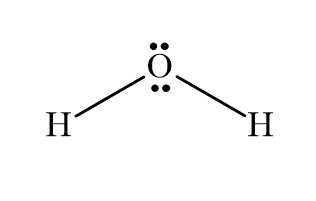
- Một liên kết (-) là một cặp electron dùng chung.
- Có hai liên kết, vậy có tổng cộng 4 electron tham gia hình thành liên kết.
⟹ Chọn đáp án: B Đáp án: B
- Công thức Lewis của H2O được biểu diễn như sau:

- Một liên kết (-) là một cặp electron dùng chung.
- Có hai liên kết, vậy có tổng cộng 4 electron tham gia hình thành liên kết.
⟹ Chọn đáp án: B Đáp án: B
Câu 30 [382305]: Một bình đựng khí NO2 sau một thời gian thì thường bị nhạt màu dần do các phân tử NO2 sẽ có xu hướng kết hợp với nhau tạo thành phân tử X (chứa 14 electron đã tham gia tạo liên kết). Dựa vào cấu trúc Lewis của NO2 dưới đây:
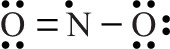
Công thức cấu tạo của X là
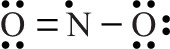
Công thức cấu tạo của X là
A, N2O5.
B, N2O4.
C, NO3.
D, N2O.
HƯỚNG DẪN GIẢI:
- Ta nhận thấy một phân tử NO2, xung quanh nguyên tử N có 7 electron, chưa đạt cấu hình bền vững.
- Vậy ta lấy hai phân tử NO2, mỗi nguyên tử N đưa ra 1 electron dư tạo thành liên kết cộng hoá trị N - N.
⟹ Ta được công thức của N2O4 như sau:
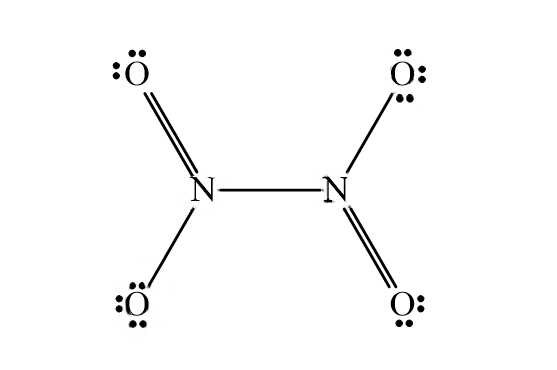
⟹ Chọn đáp án: B Đáp án: B
- Ta nhận thấy một phân tử NO2, xung quanh nguyên tử N có 7 electron, chưa đạt cấu hình bền vững.
- Vậy ta lấy hai phân tử NO2, mỗi nguyên tử N đưa ra 1 electron dư tạo thành liên kết cộng hoá trị N - N.
⟹ Ta được công thức của N2O4 như sau:

⟹ Chọn đáp án: B Đáp án: B