Câu 1 [252212]: Biết rằng khi nhiệt độ tăng lên 10oC thì tốc độ của một phản ứng tăng lên 2 lần. Khi tăng nhiệt độ từ 20oC đến 100oC tốc độ phản ứng tăng
A, 16 lần.
B, 256 lần.
C, 64 lần.
D, 14 lần.
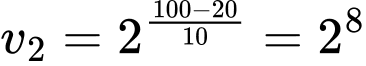 Đáp án: B
Đáp án: B
Câu 2 [252213]: Để hoà tan một tấm Zn trong dung dịch acid HCl ở 20oC thì cần 27 phút, cũng tấm Zn đó tan hết trong dung dịch acid HCl nói trên ở 40oC trong 3 phút. Hỏi để hoà tan hết tấm Zn đó trong dung dịch acid HCl trên ở 55oC thì cần bao nhiêu thời gian?
A, 60 s.
B, 34,64 s.
C, 20 s.
D, 40 s.
Ta có: 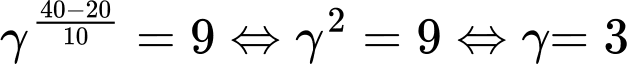
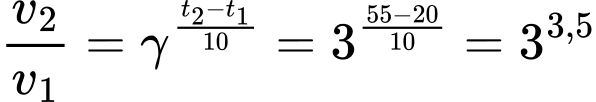
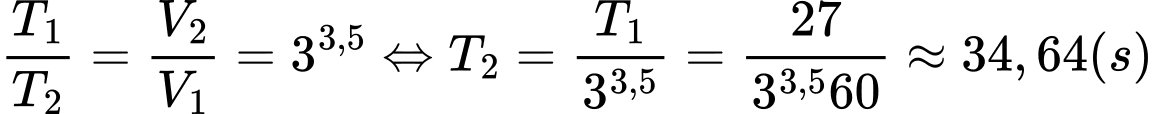 Đáp án: B
Đáp án: B
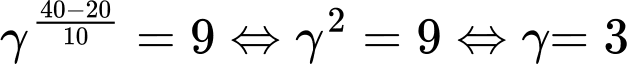
Nhiệt độ tăng từ 20oC tới 50oC, tỉ số tốc độ phản ứng:
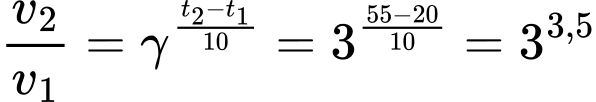
→Tỉ số thời gian phản ứng:
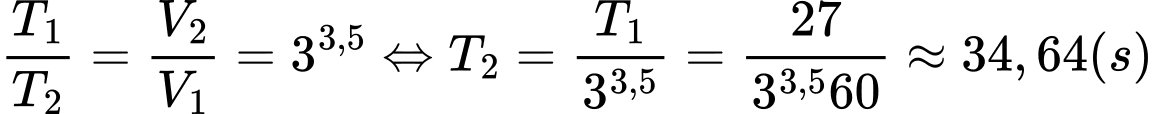
Câu 3 [252214]: Khi nhiệt độ tăng thêm 10oC, tốc độ phản ứng hoá học tăng thêm 4 lần. Tốc độ phản ứng đó sẽ giảm đi bao nhiêu lần nhiệt khi nhiệt độ giảm từ 70oC xuống 40oC?
A, 32 lần.
B, 64 lần.
C, 8 lần.
D, 16 lần.
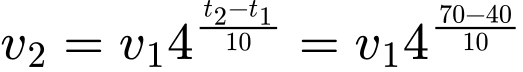 = 43v1 = V1.64
= 43v1 = V1.64Vậy, chọn đáp án B Đáp án: B
Câu 4 [252255]: Cho phản ứng hoá học: 2KClO3(s) → 2KCl(s) + 3O2(g). Yếu tố nào sau đây không ảnh hưởng tới tốc độ của phản ứng trên?
A, Nhiệt độ.
B, Chất xúc tác.
C, Áp suất.
D, Kích thước tinh thể KClO3.
Do đây là phản ứng 1 chiều và không có chất khí tham gia phản ứng nên yếu tố áp suất không ảnh hưởng tới tốc độ phản ứng. Đáp án: C
Câu 5 [252262]: Ở cùng một nồng độ, phản ứng nào dưới đây có tốc độ phản ứng xảy ra chậm nhất?
A, Al + dung dịch NaOH ở 25oC.
B, Al + dung dịch NaOH ở 30oC.
C, Al + dung dịch NaOH ở 40oC.
D, Al + dung dịch NaOH ở 50oC.
⭐ Ảnh hưởng của nhiệt độ đến tốc độ phản ứng: nhiệt độ càng thấp, tốc độ phản ứng càng giảm.
- Ở cùng nồng độ, Al phản ứng với dung dịch NaOH ở nhiệt độ thấp nhất trong 4 thí nghiệm thì tốc độ phản ứng chậm nhất → Thí nghiệm Al phản ứng với dung dịch NaOH ở 25oC có tốc độ phản ứng xảy ra chậm nhất.
➔ Đáp án A. Đáp án: A
- Ở cùng nồng độ, Al phản ứng với dung dịch NaOH ở nhiệt độ thấp nhất trong 4 thí nghiệm thì tốc độ phản ứng chậm nhất → Thí nghiệm Al phản ứng với dung dịch NaOH ở 25oC có tốc độ phản ứng xảy ra chậm nhất.
➔ Đáp án A. Đáp án: A
Câu 6 [252263]: Khi cho cùng một lượng magnesium vào cốc đựng dung dịch acid HCl, tốc độ phản ứng sẽ lớn nhất khi dùng magnesium ở dạng nào?
A, Viên nhỏ.
B, Bột mịn, khuấy đều.
C, Lá mỏng.
D, Thỏi lớn.
Ở dạng bột diện tích tiếp xúc là lớn nhất mà diện tích tiếp xúc càng lớn thì tốc độ phản ứng xảy ra càng nhanh.
➔ Đáp án B. Bột mịn, khuấy đều. Đáp án: B
➔ Đáp án B. Bột mịn, khuấy đều. Đáp án: B
Câu 7 [252274]: Khi diện tích bề mặt tăng, tốc độ phản ứng tăng với phản ứng có chất nào tham gia?
A, Chất lỏng.
B, Chất khí.
C, Chất rắn.
D, Cả A, B, C đều đúng.
Sự thay đổi diện tích bề mặt chất rắn làm tốc độ phản ứng tăng Đáp án: C
Câu 8 [252246]: Nhận định nào dưới đây là đúng?
A, Nồng độ chất phản ứng tăng thì tốc độ phản ứng tăng.
B, Nồng độ chất phản ứng giảm thì tốc độ phản ứng tăng.
C, Nồng độ chất phản ứng tăng thì tốc độ phản ứng giảm.
D, Sự thay đổi nồng độ chất phản ứng không ảnh hưởng tới tốc độ phản ứng.
Nồng độ chất phản ứng tăng thì tốc độ phản ứng tăng. Đáp án: A
Câu 9 [252254]: Hai nhóm học sinh làm thí nghiệm nghiên cứu tốc độ phản ứng zinc với dung dịch hydrochloric acid
- Nhóm thứ nhất: Cân 1 gam zinc miếng và thả vào cốc đựng 200 ml dung dịch acid HCl 2M.
- Nhóm thứ hai: Cân 1 gam zinc bột và thả vào cốc đựng 300 ml dung dịch acid HCl 2M.
Kết quả cho thấy bọt khí thoát ra ở thí nghiệm của nhóm thứ hai mạnh hơn là do nguyên nhân nào?
- Nhóm thứ nhất: Cân 1 gam zinc miếng và thả vào cốc đựng 200 ml dung dịch acid HCl 2M.
- Nhóm thứ hai: Cân 1 gam zinc bột và thả vào cốc đựng 300 ml dung dịch acid HCl 2M.
Kết quả cho thấy bọt khí thoát ra ở thí nghiệm của nhóm thứ hai mạnh hơn là do nguyên nhân nào?
A, Nhóm thứ hai dùng acid nhiều hơn.
B, Diện tích bề mặt zinc bột lớn hơn zinc miếng.
C, Nồng độ zinc bột lớn hơn.
D, Cả ba nguyên nhân đều sai.
Diện tích bề mặt zinc bột lớn hơn zinc miếng nên bọt khí thoát ra ở thí nghiệm của nhóm thứ hai mạnh hơn. Đáp án: B
Câu 10 [252257]: Thực hiện hai thí nghiệm lấy cùng một lượng CaCO3 với dung dịch HCl dư có nồng độ khác nhau. Thể tích khí CO2 thoát ra theo thời gian được ghi lại trên đồ thị sau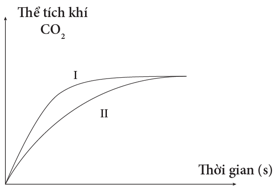
Hình 6.46. Đồ thị biểu diễn sự phụ thuộc thể tích khí CO2 theo nồng độ acid
Phản ứng nào đã dùng nồng độ HCl cao hơn?

Hình 6.46. Đồ thị biểu diễn sự phụ thuộc thể tích khí CO2 theo nồng độ acid
Phản ứng nào đã dùng nồng độ HCl cao hơn?
A, Phản ứng (1).
B, Phản ứng (2).
C, Nồng độ hydrochloric acid ở hai phản ứng là như nhau.
D, Không xác định được.
Phản ứng (1) xảy ra với tốc độ nhanh hơn. Đáp án: A
Câu 11 [252260]: Khi tăng áp suất của chất phản ứng, tốc độ phản ứng nào sau đây sẽ bị thay đổi?
A, 2Al(s) + Fe2O3(s) → Al2O3(s) + 2Fe(s).
B, CaCO3(s) → CaO(s) + CO2(g).
C, CaCO3(s) + 2HCl(aq) → CaCl2(aq) + CO2(g) + 2H2O(aq).
D, H2(g) + Cl2(g) → 2HCl(g).
Do đây là phản ứng 1 chiều và có chất khí tham gia phản ứng nên yếu tố áp suất ảnh hưởng tới tốc độ phản ứng. Đáp án: D
Câu 12 [252266]: Phản ứng phân huỷ hydrogen peroxide có xúc tác được biểu diễn:
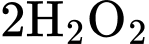
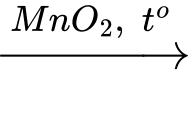
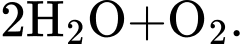
Yếu tố không ảnh hưởng đến tốc độ phản ứng là
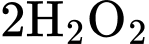
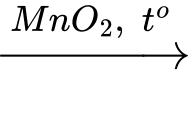
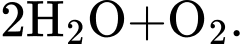
Yếu tố không ảnh hưởng đến tốc độ phản ứng là
A, nồng độ H2O2.
B, nồng độ của H2O.
C, nhiệt độ.
D, chất xúc tác MnO2.
Nồng độ sản phẩm k ảnh hưởng tới tốc độ phản ứng. Đáp án: B
Câu 13 [252269]: Cho 5 gam zinc viên vào cốc đựng 50 mL dung dịch H2SO4 4 M ở nhiệt độ thường (25oC). Trường hợp nào tốc độ phản ứng không đổi?
A, Thay 5 gam zinc viên bằng 5 gam zinc bột.
B, Thay dung dịch H2SO4 4 M bằng dung dịch H2SO4 2 M.
C, Thực hiện phản ứng ở 50oC.
D, Dùng gấp đôi thể tích dung dịch H2SO4 4 M.
Tăng thể tích dung dịch H2SO4 nhưng với nồng độ không đổi thì không làm thay đổi tốc độ phản ứng Đáp án: D
Câu 14 [252271]: Trong phòng thí nghiệm, có thể điều chế khí oxygen từ muối potassium chlorate (KClO3). Người ta sử dụng cách nào sau đây nhằm mục đích tăng tốc độ phản ứng?
A, Nung potassium chlorate ở nhiệt độ cao.
B, Nung hỗn hợp potassium chlorate và manganese dioxide ở nhiệt độ cao.
C, Dùng phương pháp dời nước để thu khí oxygen.
D, Dùng phương pháp dời không khí để thu khí oxygen.
Sử dụng MnO2 làm chất xúc tác Đáp án: B
Câu 15 [252277]: Thực hiện thí nghiệm sau:
(1) Zn (hạt) + 3 mL dung dịch HCl 20%. (2) Zn (hạt) + 3 mL dung dịch HCl 10%.
(3) Zn (hạt) + 3 mL dung dịch HCl 12%. (4) Zn (hạt) + 3 mL dung dịch HCl 23%.
Phản ứng nào xảy ra nhanh nhất?
(1) Zn (hạt) + 3 mL dung dịch HCl 20%. (2) Zn (hạt) + 3 mL dung dịch HCl 10%.
(3) Zn (hạt) + 3 mL dung dịch HCl 12%. (4) Zn (hạt) + 3 mL dung dịch HCl 23%.
Phản ứng nào xảy ra nhanh nhất?
A, (1).
B, (2).
C, (4).
D, (3).
Trường hợp 4 nồng độ HCl lớn nhất nên phản ứng xảy ra nhanh nhất. Đáp án: C
Câu 16 [252278]: Thực hiện 2 thí nghiệm theo hình vẽ sau.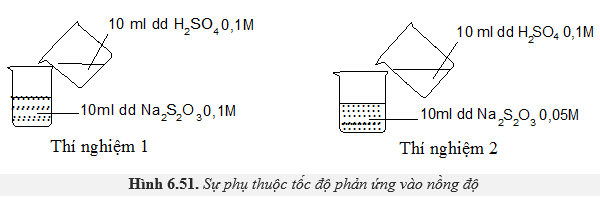
Ở thí nghiệm nào có kết tủa xuất hiện trước?

Ở thí nghiệm nào có kết tủa xuất hiện trước?
A, TN1 có kết tủa xuất hiện trước.
B, TN2 có kết tủa xuất hiện trước.
C, Kết tủa xuất hiện đồng thời.
D, Không có kết tủa xuất hiện.
TN1 có kết tủa xuất hiện trước do Na2S2O3 có nồng độ lớn hơn. Đáp án: A
Câu 17 [252279]: Cho 2 mẫu BaSO3 có khối lượng bằng nhau và 2 cốc chứa 50ml dung dịch HCl 0,1 M như hình sau. Hỏi ở cốc nào mẫu BaSO3 tan nhanh hơn?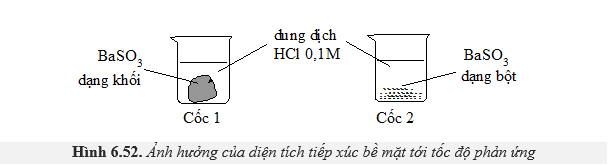

A, Cốc 1 tan nhanh hơn.
B, Cốc 2 tan nhanh hơn.
C, Tốc độ tan ở 2 cốc như nhau.
D, BaSO3 tan nhanh nên không quan sát được.
Cốc 1: BaSO3 ở dạng khối
Câu 2: BaSO3 ở dạng bột
Dạng bột có diện tích tiếp xúc lớn hơn dạng khối mà diện tích tiếp xúc càng lớn thì tốc độ phản ứng càng nhanh
Nên cốc 2 có tốc độ phản ứng nhanh hơn cốc 1
➔ Đáp án B. Cốc 2 tan nhanh hơn. Đáp án: B
Câu 2: BaSO3 ở dạng bột
Dạng bột có diện tích tiếp xúc lớn hơn dạng khối mà diện tích tiếp xúc càng lớn thì tốc độ phản ứng càng nhanh
Nên cốc 2 có tốc độ phản ứng nhanh hơn cốc 1
➔ Đáp án B. Cốc 2 tan nhanh hơn. Đáp án: B
Câu 18 [252281]: Cho một viên đá vôi nặng 1 gam vào dung dịch HCl 2 M, ở nhiệt độ 25oC. Biến đổi nào sau đây không làm bọt khí thoát ra mạnh hơn?
A, Tăng thể tích dung dịch HCl lên gấp đôi.
B, Thay viên đá vôi bằng 1 gam bột đá vôi.
C, Thay dung dịch HCl 2 M bằng dung dịch HCl 4 M.
D, Tăng nhiệt độ lên 50oC.
tăng thể tích nhưng nồng độ HCl không thay đổi nên tốc độ không tăng. Đáp án: A
Câu 19 [252286]: Có hai mẫu đá vôi:
▪ Mẫu 1: đá vôi có dạng khối.
▪ Mẫu 2: đá vôi có dạng hạt nhỏ.
Hòa tan cả hai mẫu đá vôi bằng cùng một thể tích dung dịch HCl dư có cùng nồng độ. Ta thấy thời gian để mẫu 1 phản ứng hết nhiều hơn mẫu 2. Thí nghiệm trên chứng minh điều gì?
▪ Mẫu 1: đá vôi có dạng khối.
▪ Mẫu 2: đá vôi có dạng hạt nhỏ.
Hòa tan cả hai mẫu đá vôi bằng cùng một thể tích dung dịch HCl dư có cùng nồng độ. Ta thấy thời gian để mẫu 1 phản ứng hết nhiều hơn mẫu 2. Thí nghiệm trên chứng minh điều gì?
A, Tốc độ phản ứng phụ thuộc vào nhiệt độ tiến hành phản ứng.
B, Tốc độ phản ứng phụ thuộc vào diện tích tiếp xúc giữa các chất phản ứng.
C, Tốc độ phản ứng phụ thuộc vào thời gian xảy ra phản ứng.
D, Tốc độ phản ứng không phụ thuộc vào nồng độ các chất tham gia phản ứng.
Tốc độ phản ứng phụ thuộc vào diện tích tiếp xúc giữa các chất phản ứng. Đáp án: B
Câu 20 [252290]: Khi tiến hành các thí nghiệm.
a. Zn (hạt) + 3mL dung dịch H2SO4 15%.
b. Zn (hạt) + 3mL dung dịch H2SO4 15% (đun nóng).
c. Zn (bột) + 3mL dung dịch H2SO4 15% (đun nóng).
d. Zn (hạt) + 3mL dung dịch H2SO4 10%.
Tốc độ phản ứng giảm dần theo thứ tự nào?
a. Zn (hạt) + 3mL dung dịch H2SO4 15%.
b. Zn (hạt) + 3mL dung dịch H2SO4 15% (đun nóng).
c. Zn (bột) + 3mL dung dịch H2SO4 15% (đun nóng).
d. Zn (hạt) + 3mL dung dịch H2SO4 10%.
Tốc độ phản ứng giảm dần theo thứ tự nào?
A, a > c > b > d.
B, b > a > c > d.
C, c > b > a > d.
D, d > a > b > c.
Kẽm bột và H2SO4 15% (đun nóng). Có tốc độ lớn nhất Đáp án: C
Câu 21 [252291]: Cho ba mẫu đá vôi (100% CaCO3) có cùng khối lượng: mẫu 1 dạng khối, mẫu 2 dạng viên nhỏ, mẫu 3 dạng bột mịn vào ba cốc đựng cùng thể tích dung dịch HCl (dư, cùng nồng độ, ở điều kiện thường). Thời gian để đá vôi tan hết trong ba cốc tương ứng là t1, t2, t3 giây. So sánh nào sau đây đúng?
A, t3 < t2 < t1.
B, t1 < t2 < t3.
C, t1 = t2 = t3.
D, t2 < t1 < t3.
(Đá vôi càng nhỏ, mịn thì phản ứng xảy ra càng nhanh, thời gian xảy ra càng ngắn nên tương ứng với mẫu 1: dạng khối; mẫu 2: dạng viên; mẫu 3: dạng bột mịn thì tương ứng với thời gian t3 < t2 < t1). Đáp án: A
Câu 22 [252292]: Thí nghiệm nghiên cứu tốc độ phản ứng zinc với dung dịch hydrochloric acid của hai nhóm học sinh được mô tả bằng hình sau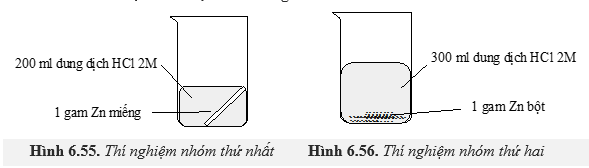
Kết quả cho thấy bọt khí thoát ra ở thí nghiệm của nhóm thứ hai mạnh hơn là do:

Kết quả cho thấy bọt khí thoát ra ở thí nghiệm của nhóm thứ hai mạnh hơn là do:
A, Nhóm thứ hai dùng acid nhiều hơn.
B, Diện tích bề mặt zinc bột lớn hơn zinc miếng.
C, Nồng độ zinc bột lớn hơn.
D, Áp suất tiến hành thí nghiệm nhóm thứ hai cao hơn nhóm thứ nhất.
Diện tích bề mặt zinc bột lớn hơn zinc miếng. Đáp án: B
Câu 23 [252301]: Tác động nào dưới đây không ảnh hưởng đến vận tốc phản ứng phân hủy CaCO3: CaCO3(s) → CaO(s) + CO2(g)?
A, Đun nóng.
B, Thêm đá vôi.
C, Đập nhỏ đá vôi.
D, Nghiền mịn đá vôi.
Thêm đá vôi không ảnh hưởng đến vận tốc phản ứng phân hủy. Đáp án: B
Câu 24 [252295]: Quá trình phân hủy hydrogen peroxide diễn ra nhanh hơn khi có mặt chất xúc tác là MnO2. Đồ thị nào dưới đây biểu thị đúng khối lượng của chất xúc tác khi phản ứng xảy ra?
A, 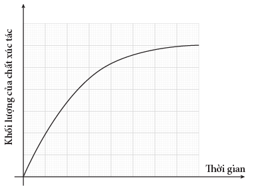

B, 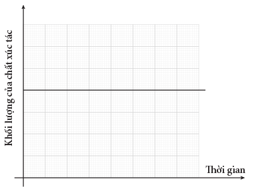

C, 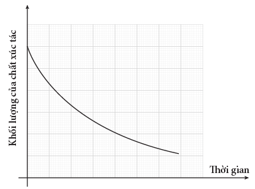

D, 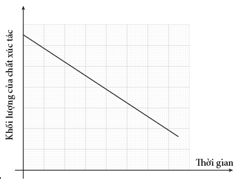

Đồ thị B, khối lượng chất xúc tác không đổi trong phản ứng. Đáp án: B
Câu 25 [252306]: Hai nhóm học sinh làm thí nghiệm: nghiên cứu tốc độ phản ứng zinc tan trong dung dịch hydrochloric acid:
▪ Nhóm 1 : Cân miếng kẽm 1 gam và thả vào cốc đựng 200 ml dung dịch acid HCl 2M.
▪ Nhóm 2 : Cân 1 gam bột kẽm và thả vào cốc đựng 300 ml dung dịch acid HCl 2M
Kết quả cho thấy bọt khí thoát ra ở thí nghiệm của nhóm 2 mạnh hơn là do
▪ Nhóm 1 : Cân miếng kẽm 1 gam và thả vào cốc đựng 200 ml dung dịch acid HCl 2M.
▪ Nhóm 2 : Cân 1 gam bột kẽm và thả vào cốc đựng 300 ml dung dịch acid HCl 2M
Kết quả cho thấy bọt khí thoát ra ở thí nghiệm của nhóm 2 mạnh hơn là do
A, diện tích tiếp xúc bề mặt bột zinc lớn hơn.
B, nhóm 2 dùng acid nhiều hơn.
C, nồng độ zinc bột lớn hơn.
D, số mol của acid lớn hơn.
Diện tích tiếp xúc bề mặt bột zinc lớn hơn. Đáp án: A
Câu 26 [850749]: Cho lần lượt 100 gam đá vôi (CaCO3) phản ứng với dung dịch HCl 2 M dư. Đá vôi được dùng ở dạng hạt kích cỡ được kí hiệu như sau:
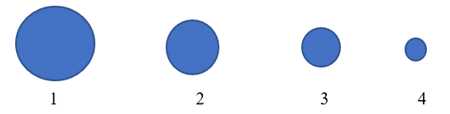
Phản ứng dùng ở dạng hạt kích cỡ nào sẽ có tốc độ phản ứng xảy ra chậm nhất?

Phản ứng dùng ở dạng hạt kích cỡ nào sẽ có tốc độ phản ứng xảy ra chậm nhất?
Yếu tố ảnh hưởng đến tốc độ phản ứng ở đây là kích thước hạt CaCO3, ảnh hưởng trực tiếp đến diện tích bề mặt tiếp xúc với acid HCl.
+ Hạt càng nhỏ → diện tích tiếp xúc càng lớn → tốc độ phản ứng càng nhanh.
+ Hạt càng to → diện tích tiếp xúc nhỏ hơn → tốc độ phản ứng chậm hơn.
Kích thước hạt theo đề bài: 1 > 2 > 3 > 4
→ Hạt 1 có kích thước to nhất, là loại hạt có diện tích tiếp xúc nhỏ nhất nên có tốc độ phản ứng xảy ra chậm nhất.
⇒ Điền đáp án: 1
+ Hạt càng nhỏ → diện tích tiếp xúc càng lớn → tốc độ phản ứng càng nhanh.
+ Hạt càng to → diện tích tiếp xúc nhỏ hơn → tốc độ phản ứng chậm hơn.
Kích thước hạt theo đề bài: 1 > 2 > 3 > 4
→ Hạt 1 có kích thước to nhất, là loại hạt có diện tích tiếp xúc nhỏ nhất nên có tốc độ phản ứng xảy ra chậm nhất.
⇒ Điền đáp án: 1
Câu 27 [850765]: Cho phản ứng sau: 2KClO3(s) 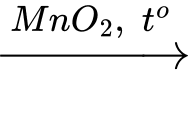 2KCl(s) + 3O2(g). Hãy cho biết trong các tác động sau đây: (1) tăng áp suất; (2) tăng to phản ứng; (3) tăng xúc tác MnO2; (4) nghiền nhỏ KClO3; (5) thêm lượng KCl. Sắp xếp những tác động làm thay đổi tốc độ phản ứng theo trình tự tăng dần (ví dụ: 123, 245,...)
2KCl(s) + 3O2(g). Hãy cho biết trong các tác động sau đây: (1) tăng áp suất; (2) tăng to phản ứng; (3) tăng xúc tác MnO2; (4) nghiền nhỏ KClO3; (5) thêm lượng KCl. Sắp xếp những tác động làm thay đổi tốc độ phản ứng theo trình tự tăng dần (ví dụ: 123, 245,...)
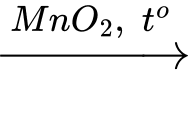 2KCl(s) + 3O2(g). Hãy cho biết trong các tác động sau đây: (1) tăng áp suất; (2) tăng to phản ứng; (3) tăng xúc tác MnO2; (4) nghiền nhỏ KClO3; (5) thêm lượng KCl. Sắp xếp những tác động làm thay đổi tốc độ phản ứng theo trình tự tăng dần (ví dụ: 123, 245,...)
2KCl(s) + 3O2(g). Hãy cho biết trong các tác động sau đây: (1) tăng áp suất; (2) tăng to phản ứng; (3) tăng xúc tác MnO2; (4) nghiền nhỏ KClO3; (5) thêm lượng KCl. Sắp xếp những tác động làm thay đổi tốc độ phản ứng theo trình tự tăng dần (ví dụ: 123, 245,...)
Phản ứng: 2KClO3(s) 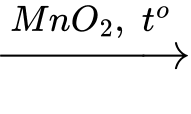 2KCl(s) + 3O2(g)
2KCl(s) + 3O2(g)
Phân tích các tác động:
❌ (1) Áp suất chỉ ảnh hưởng tới các phản ứng có mặt của chất khí tham gia. Ở đây phản ứng xảy ra 1 chiều, chất tham gia chỉ có KClO3(s) nên áp suất không làm thay đổi tốc độ phản ứng.
✔️ (2) Đây là phản ứng phân hủy, cần nhiệt độ nên khi tăng nhiệt độ thì phản ứng phân hủy xảy ra mạnh mẽ (do tăng năng lượng hoạt hóa) → Tăng tốc độ đáng kể.
✔️ (3) MnO2 là xúc tác, giúp tăng tốc độ phản ứng nhưng không làm thay đổi thành phần phản ứng. Tuy nhiên, ban đầu đã có mặt xúc tác này. Nếu lượng xúc tác đã đủ, hiệu quả tăng thêm không nhiều. → Tăng tốc độ trung bình.
✔️ (4) Nghiền nhỏ KClO3 làm tăng diện tích tiếp xúc → phản ứng phân hủy xảy ra nhanh hơn.
❌ (5) Tăng lượng sản phẩm cho phản ứng 1 chiều không làm thay đổi tốc độ phản ứng.
⇒ Điền đáp án: 234
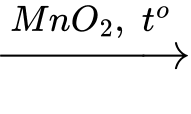 2KCl(s) + 3O2(g)
2KCl(s) + 3O2(g)Phân tích các tác động:
❌ (1) Áp suất chỉ ảnh hưởng tới các phản ứng có mặt của chất khí tham gia. Ở đây phản ứng xảy ra 1 chiều, chất tham gia chỉ có KClO3(s) nên áp suất không làm thay đổi tốc độ phản ứng.
✔️ (2) Đây là phản ứng phân hủy, cần nhiệt độ nên khi tăng nhiệt độ thì phản ứng phân hủy xảy ra mạnh mẽ (do tăng năng lượng hoạt hóa) → Tăng tốc độ đáng kể.
✔️ (3) MnO2 là xúc tác, giúp tăng tốc độ phản ứng nhưng không làm thay đổi thành phần phản ứng. Tuy nhiên, ban đầu đã có mặt xúc tác này. Nếu lượng xúc tác đã đủ, hiệu quả tăng thêm không nhiều. → Tăng tốc độ trung bình.
✔️ (4) Nghiền nhỏ KClO3 làm tăng diện tích tiếp xúc → phản ứng phân hủy xảy ra nhanh hơn.
❌ (5) Tăng lượng sản phẩm cho phản ứng 1 chiều không làm thay đổi tốc độ phản ứng.
⇒ Điền đáp án: 234
Câu 28 [850757]: Cho iron (hạt) phản ứng với dung dịch hydrochloric 1 M dư. Thay đổi các yếu tố sau:
(1) Thêm vào hệ một lượng nhỏ tinh thể CuSO4.
(2) Thêm dung dịch HCl 1 M lên thể tích gấp đôi.
(3) Nghiền nhỏ hạt iron thành bột iron.
(4) Pha loãng dung dịch HCl bằng nước cất lên thể tích gấp đôi.
Có bao nhiêu cách thay đổi tốc độ phản ứng?
(1) Thêm vào hệ một lượng nhỏ tinh thể CuSO4.
(2) Thêm dung dịch HCl 1 M lên thể tích gấp đôi.
(3) Nghiền nhỏ hạt iron thành bột iron.
(4) Pha loãng dung dịch HCl bằng nước cất lên thể tích gấp đôi.
Có bao nhiêu cách thay đổi tốc độ phản ứng?
Theo lý thuyết, có 5 yếu tố ảnh hưởng tới tốc độ phản ứng: nồng độ, nhiệt độ, áp xuất, chất xúc tác và diện tích tiếp xúc.
Phân tích các yếu tố:
✔️ (1) Cu2+ trong CuSO4 có thể hoạt động như chất xúc tác (gây hiệu ứng điện cực, giúp tăng tốc độ phản ứng khử).Ngoài ra, nó còn có thể gây hiện tượng thế điện hóa, tạo lớp Cu trên bề mặt Fe → cũng có thể tăng tốc độ phản ứng ban đầu.
❌ (2) Thêm thể tích dung dịch HCl 1 M không làm ảnh hưởng tới tốc độ của phản ứng.
✔️ (3) Nghiền nhỏ hạt iron thành bột iron là tăng diện tích tiếp xúc giữa iron với dung dịch hydrochloric nên giúp tăng tốc độ phản ứng.
✔️ (4) Pha loãng dung dịch HCl bằng nước cất lên thể tích gấp đôi là làm giảm nồng độ của dung dịch HCl nên làm tốc độ phản ứng giảm.
Vậy các cách làm thay đổi tốc độ phản ứng là (1) (3) (4)
⇒ Điền đáp án: 3
Phân tích các yếu tố:
✔️ (1) Cu2+ trong CuSO4 có thể hoạt động như chất xúc tác (gây hiệu ứng điện cực, giúp tăng tốc độ phản ứng khử).Ngoài ra, nó còn có thể gây hiện tượng thế điện hóa, tạo lớp Cu trên bề mặt Fe → cũng có thể tăng tốc độ phản ứng ban đầu.
❌ (2) Thêm thể tích dung dịch HCl 1 M không làm ảnh hưởng tới tốc độ của phản ứng.
✔️ (3) Nghiền nhỏ hạt iron thành bột iron là tăng diện tích tiếp xúc giữa iron với dung dịch hydrochloric nên giúp tăng tốc độ phản ứng.
✔️ (4) Pha loãng dung dịch HCl bằng nước cất lên thể tích gấp đôi là làm giảm nồng độ của dung dịch HCl nên làm tốc độ phản ứng giảm.
Vậy các cách làm thay đổi tốc độ phản ứng là (1) (3) (4)
⇒ Điền đáp án: 3
Đọc đoạn thông tin sau và trả lời các câu hỏi từ 29 đến 30:
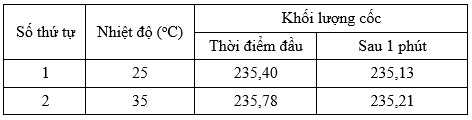
Cho 10 gam đá vôi ở dạng viên ở nhiệt độ phòng (25 oC) vào cốc đựng 100 gam hydrochloric acid loãng và nhanh chóng cho lên một cân điện tử. Đọc giá trị khối lượng cốc tại thời điểm ban đầu và sau 1 phút. Lặp lại thí nghiệm khi nhiệt độ phòng là 35 oC. Kết quả thí nghiệm được ghi trong bảng sau:

Câu 29 [252218]: Đọc đoạn thông tin sau và trả lời các câu hỏi từ 7 đến 8:
Cho 10 gam đá vôi ở dạng viên ở nhiệt độ phòng (25 oC) vào cốc đựng 100 gam hydrochloric acid loãng và nhanh chóng cho lên một cân điện tử. Đọc giá trị khối lượng cốc tại thời điểm ban đầu và sau 1 phút. Lặp lại thí nghiệm khi nhiệt độ phòng là 35 oC. Kết quả thí nghiệm được ghi trong bảng sau: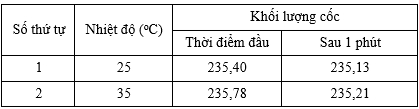
7. Hệ số nhiệt độ của phản ứng là
Cho 10 gam đá vôi ở dạng viên ở nhiệt độ phòng (25 oC) vào cốc đựng 100 gam hydrochloric acid loãng và nhanh chóng cho lên một cân điện tử. Đọc giá trị khối lượng cốc tại thời điểm ban đầu và sau 1 phút. Lặp lại thí nghiệm khi nhiệt độ phòng là 35 oC. Kết quả thí nghiệm được ghi trong bảng sau:

7. Hệ số nhiệt độ của phản ứng là
A, 2,11.
B, 2,14.
C, 2,34.
D, 2,21.
Tốc độ phản ứng ở 25 ℃ là 0,25 gam/phút; tốc độ phản ứng ở 35 ℃ là 0,57 gam/phút.=> Hệ số nhiệt độ của phản ứng là: g = 0,57 : 0,27 = 2,11. Đáp án: A
Câu 30 [252219]: Giả sử ban đầu cốc chứa dung dịch HCl và đá vôi có khối lượng 235,40 gam. Thực hiện thí nghiệm ở 45oC. Sau 1 phút khối lượng cốc là (bỏ qua khối lượng nước bay hơi)
A, 220,34 gam.
B, 234,20 gam.
C, 238,2 gam.
D, 225,20 gam.
Tốc độ phản ứng ở 45 ℃ là 1,2 gam/phút. Khối lượng cốc sau 1 phút là: 235,40 – 1,2 = 234,20 gam. Đáp án: B