(1) thêm 1 mL dung dịch acetaldehyde;
(2) thêm 4-5 giọt dung dịch copper(II) sulfate 5%;
(3) thêm 1 mL dung dịch NaOH 10%;
(4) đun nhẹ trên ngọn lửa đèn cồn.
Trình tự đúng khi tiến hành thí nghiệm là
Bước 1: Thêm 4-5 giọt dung dịch Copper (II) sulfate 5%. (2)
Bước 2: Thêm 1mL dung dịch NaOH 10%.(3)
Bước 3: Lắc ống nghiệm, nhỏ từ từ khoảng 1mL dung dịch acetaldehyde (CH3CHO)vào ống nghiệm. (1)
Bước 4: Đun nhẹ trên ngọn lửa đèn cồn. (4)
Thứ tự thực hiện thí nghiệm: (2) - (3) - (1) - (4)
Chọn đáp án: C Đáp án: C
Thuốc thử Tollens chỉ propanal tạo thành kết tủa sáng bóng bám vào thành ống nghiệm là Ag, propanone không có.
Cu(OH)2/NaOH chỉ propanal tạo thành kết tủa đỏ gạch là Cu2O, propanone không có.
Đáp án D Đáp án: D
Trong sơ đồ trên mỗi mũi tên là một phản ứng, X là chất nào sau đây?
 CH3CH=O
CH3CH=OCH3CH=O + Br2 + H2O → CH3COOH + 2HBr
Đáp án D Đáp án: D
![541368[de].png](https://asset.moon.vn/img/ai/Teachers/rongden_167/ProS2018/BAI%2018/541368[de].png)
![541368[lg].png](https://asset.moon.vn/img/ai/Teachers/rongden_167/ProS2018/BAI%2018/541368[lg].png)
Đáp án: A
![541516[de].png](https://asset.moon.vn/img/ai/Teachers/rongden_167/ProS2018/BAI%2018/541516[de].png)
Phát biểu nào sau đây là sai?
♦ không phản ứng Na, AgNO3/NH3 ⇒ Z là acetone.
♦ không phản ứng Na, có phản ứng với AgNO3/NH3 → Ag ⇒ Y là andehyde C2H5CHO.
♦ phản ứng với Na, không + AgNO3/NH3 ⇒ X là alcohol CH2=CH–CH2OH.
Phân tích các phát biểu:
✔️A. Đúng. X có công thức cấu tạo là CH2=CH-CH2OH có tên gọi là prop-2-en-1-ol.
❌B. Sai. Z là acetone . Acetone thường không phản ứng lam mất màu nước bromine ở điều kiện thường.
✔️C. Đúng. Y có công thức cấu tạo là C2H5CHO có tên gọi là propanal.
✔️D. Đúng. X là prop-2-en-1-ol có chứa liên kết đôi C=C nên có phản ứng cộng bromine.
Chọn đáp án B
Đáp án: B
![541370[lg].png](https://asset.moon.vn/img/ai/Teachers/rongden_167/ProS2018/BAI%2018/541370[lg].png)
Đáp án: D
![541515[de].png](https://asset.moon.vn/img/ai/Teachers/rongden_167/ProS2018/BAI%2018/541515[de].png)
Nhận xét: C trong nhóm –CHO có số oxi hóa là +1; trong nhóm –COO là +3;
trong –CH2OH là –1 ⇒ CH3CHO thể hiện tính oxi ở phản ứng (c);
còn trong các phản ứng (a); (b); (d) đều thể hiện tính khử.
⇒ theo yêu cầu → chọn đáp án C. ♣.
Đáp án: C
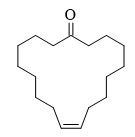
Cho các phát biểu sau:
(a) Civetone là hợp chất carbonyl.
(b) Civetone là ketone không no, đơn chức, mạch vòng.
(c) Civetone tham gia phản ứng với LiAlH4 tạo thành hợp chất có khối lượng phân tử là 252.
(d) Civetone có khả năng tham gia phản ứng với nước bromine, thuốc thử Tollens.
Số phát biểu đúng là
Nhận định (a) – Đúng. Civetone là hợp chất carbonyl → Vì có nhóm C=O.
Nhận định (b) – Đúng. Civetone là ketone không no, đơn chức, mạch vòng
Nhận định (c) – Đúng. Civetone tham giaphản ứng với LiAlH₄ → tạo alcohol. Khi khử bằng LiAlH₄, nhóm C=O của ketonechuyển thành –CH(OH)– → tạo rượu bậc hai.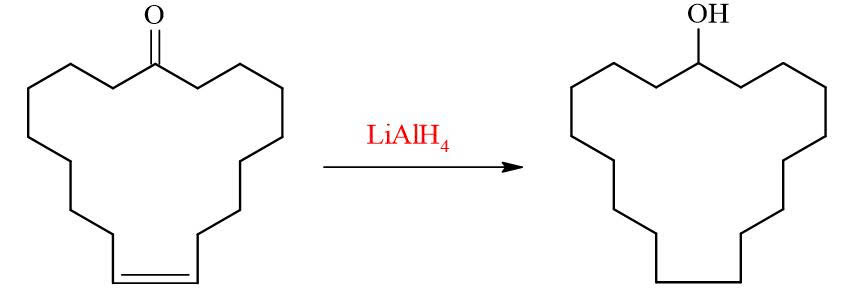
Nhận định (d) – Sai. Có nối đôi → phản ứng với Br₂ .Nhưng thuốc thửTollens chỉ oxi hoá aldehyde, không phản ứng với ketone.
Đáp án: C. 3.
Bước 1: Cho vào hai khác nhau ống nghiệm khoảng 1 mL dung dịch I2 trong KI và khoảng 1 mL dung dịch NaOH 10%.
Bước 2: Nhỏ từ từ 5-7 giọt acetaldehyde vào một ống nghiệm, ghi nhãn (1) và 5-7 giọt acetone vào ống nghiệm còn lại, ghi nhãn (2). Lắc đều.
Cho các phát biểu sau:
(a) I2 tan nhiều khi dung dịch có hòa tan muối KI.
(b) Phản ứng có thể được thực hiện trong môi trường acid.
(c) Ống nghiệm (1) xuất hiện kết tủa màu vàng còn ống nghiệm (2) xuất hiện kết tủa xanh.
(d) Phản ứng được dùng để nhận biết các aldehyde, ketone có nhóm methyl cạnh nhóm carbonyl.
Số phát biểu đúng là
Đáp án: B. 2.
Nhận định (a) – Đúng. I₂ hòa tan trong KI tạo thành KI₃ (I₃⁻),
dung dịch màu nâu vàng, tăng khả năng tan.
Nhận định (b) – Sai. Phản ứng iodoform yêu cầu môi trường kiềm.
Trong môi trường acid, phản ứng này không xảy ra.
Nhận định (c) – Sai. Cả acetaldehyde (ống 1) và acetone (ống
2) đều tạo kết tủa vàng CHI₃, không có kết tủa xanh.
Nhận định (d) – Đúng. Phản ứng được dùng để nhận biết các aldehyde,
ketone có nhóm methyl cạnh nhóm carbonyl. Đây là ứng dụng chính của phản ứng
iodoform.
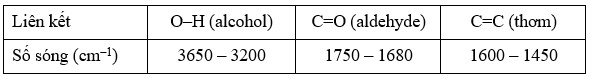
Cho các phát biểu sau:
(a) Tín hiệu tại 1690 cm–1 trên phổ IR cho thấy S chứa nhóm chức aldehyde.
(b) S có thể phản ứng với NaBH4, tạo ra sản phẩm chứa nhóm –CH2.
(c) Khi oxi hóa S bằng KMnO4, sản phẩm thu được không có khả năng phản ứng với dung dịch Br2.
(d) Phân tử S có liên kết đôi C=C trong vòng thơm, thể hiện tính không bão hòa.
Số phát biểu đúng là
Đáp án: C. 3.
(a) Đúng. Tín hiệu mạnh ở 1690 cm⁻¹ nằm trong khoảng 1750–1680
cm⁻¹ — vùng đặc trưng cho C=O của aldehyde → chứng tỏ S chứa nhóm
aldehyde.
(b) Đúng. NaBH₄ là tác nhân khử chọn lọc aldehyde/ketone,
khử –CHO → –CH₂OH (tức nguyên tử C của nhóm carbonyl trở thành –CH₂– trong sản
phẩm rượu bậc 1). Do đó S có thể phản ứng với NaBH₄ và sinh sản phẩm chứa nhóm –CH₂
(chính xác hơn là –CH₂OH).
(c) Sai. Nếu oxi hóa S bằng KMnO₄ thu được một axit thơm có nhóm
–OH phenol (ví dụ salicylic acid nếu S là salicylaldehyde), thì sản phẩm này vẫn
có thể làm mất màu Br₂/CCl₄ do vòng thơm đã được hoạt hóa bởi nhóm –OH. Do
đó phát biểu nói sản phẩm thu được không phản ứng với Br₂ là không đúng.
(d) Đúng. S làm mất màu Br₂/CCl₄ cho thấy có điểm không bão
hòa trong phân tử — trong hợp chất thơm đó là các liên kết π (C=C) của vòng thơm. Vì vậy phát biểu rằng phân tử S có liên kết đôi C=C trong vòng thơm,
thể hiện tính không bão hòa là hợp lý.
Cho các phát biểu sau:
(a) A có công thức phân tử là C9H8O.
(b) S có thể phản ứng với NaBH4, tạo ra sản phẩm chứa nhóm –CH2.
(c) Chất A làm mất màu dung dịch Br2/CCl4 chứng tỏ phân tử A có chứa nhóm chức aldehyde.
(d) Có thể kết luận công thức cấu tạo của A là C6H5CH2CH2CHO.
Số phát biểu đúng là
Nhận định (a) – đúng. Gọi công thức phân tử của A là CxHyOz
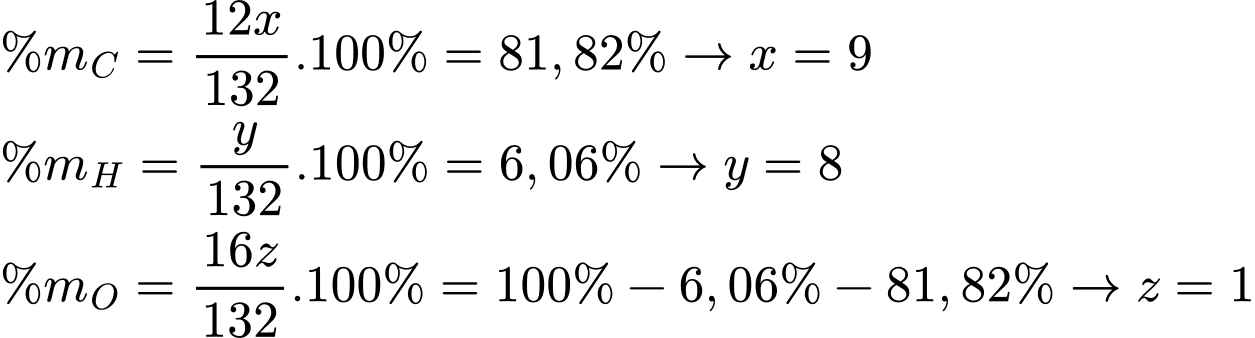
Công thức phân tử của A là C9H8O2
Nhận định (b) – đúng. NaBH₄ là tác nhân khử chọn lọc các nhóm cacbonyl như aldehyde → chuyển –CHO thành –CH₂OH (rượu bậc 1). Sau phản ứng ta có nguyên tử C đó mang hai H (một nhóm –CH₂– xuất hiện trong sản phẩm như –CH₂OH).
Nhận định (c) – sai. Dung dịch Br₂ trong CCl₄ bị làm mất màu chủ yếu khi có đôi nối C=C (phản ứng cộng với brom); đó không phải là phép thử đặc hiệu cho aldehyde. Aldehyde thường dùng các phản ứng như Tollens (tráng bạc), Fehling, hay oxi hóa nhẹ. Ở đề bài A có phản ứng tráng bạc, nên aldehyde đã được chứng minh bằng Tollens; nhưng việc làm mất màu Br₂/CCl₄ cho thấy có liên kết đôi (C=C) chứ không chứng minh aldehyde.
Nhận định (d) – sai. Công thức đó tương đương C₉H₁₀O (không phải C₉H₈O), nên không khớp với số liệu nguyên tố và MS. Đáp án: B
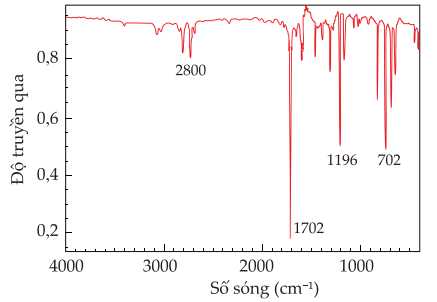
Ngoài tín hiệu 1702 cm–1 của nhóm C=O thì dùng thêm tín hiệu 2800 cm–1 để kết luận đây là một aldehyde.
⇒ Điền đáp án: 2800

Trong đó, X, Y và Z đều là các hợp chất hữu cơ. Xác định khối lượng phân tử của Z.
(1)
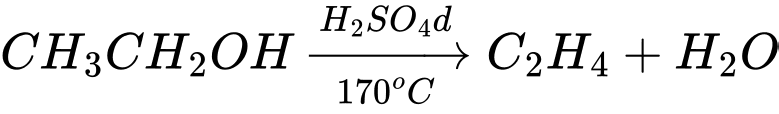
(2)
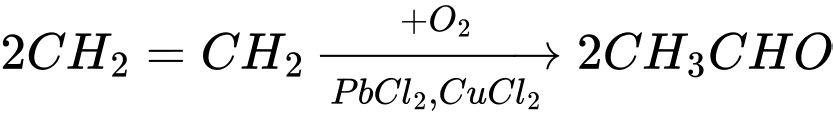
(3)
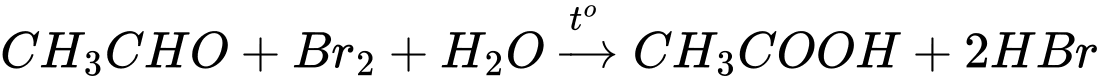
Công thức cấu tạo của Z là: CH3COOH
Khối lượng phân tử của Z là : 12 × 2 + 1 × 4 + 16 × 2 = 60
⇒ Điền đáp án: 60
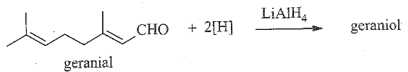
Khi phản ứng khử xảy ra, geranial bị phá vỡ bao nhiêu liên kết π?
→ geranial chỉ có 1 liên kết trong nhóm CHO bị phá vỡ.
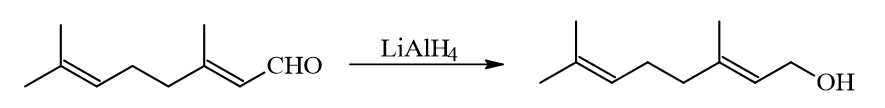
Điền đáp án : 1
Ứng với công thức phân tử C4H8O các hợp chất mạch hở tác dụng với NaBH4 tạo ra alcohol bậc 1:
(1). CH3 – CH2 – CH2 – CHO
(2). CH3 – CH(CH3)– CHO
⇒ Điền đáp án: 2
CH2(CHO)2+ 4[ Ag(NH3)2]OH ⟶ CH2(COONH4)2 + 4Ag + 6NH3 + 2H2O
nX= 7,2 ÷ 72 = 0,1 (mol)
Theo phương trình: nAg= nX = 0,1 × 4 = 0,4 mol
Khối lượng của Ag là: mAg = 0,4 × 108 = 43,2 gam.
⇒ Điền đáp án: 43,2
Đọc đoạn thông tin sau và trả lời các câu hỏi từ 18 đến 20:
Nhóm carboxyl COO tạo ra hai sự hấp thụ đặc trưng trong quang phổ hồng ngoại. Một trong số này xảy ra trong vùng 1700 – 1725 cm–1 liên quan đến nhóm carbonyl C=O. Phạm vi hấp thụ này về cơ bản giống như phạm vi hấp thụ của nhóm carbonyl của aldehyde CHO và ketone C=O.
Đặc điểm hấp thụ hồng ngoại khác của nhóm carboxyl là vùng 3300 cm–1 do dao động của liên kết nhóm O–H, thường chồng chéo lên sự hấp thụ của liên kết C–H. Sự hấp thụ của liên kết O–H thường rất rộng do liên kết hydrogen giữa các phân tử của carboxylic acid.
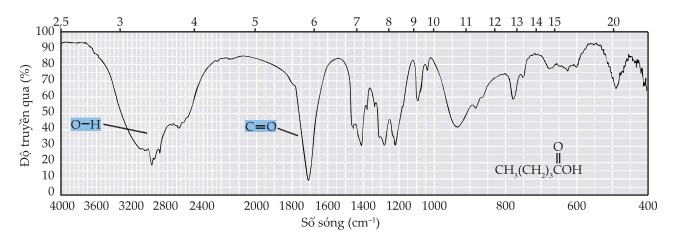
Đáp án: B. xuất hiện
liên kết hydrogen.
Liên kết O–H
(trong rượu, acid, nước, v.v.) thường tham gia tạo liên kết hydrogen giữa
các phân tử.
→ Các liên kết
hydrogen này làm thay đổi năng lượng dao động của liên kết O–H theo nhiều
mức khác nhau → vùng hấp thụ bị kéo giãn và mở rộng, tạo ra phổ hấp
thụ rất rộng trong phổ hồng ngoại (IR).
Đáp án: C. 1720
cm⁻¹.
Liên kết C=O
(carbonyl) có dao động kéo giãn mạnh trong vùng 1700 ± 50 cm⁻¹ trên
phổ hồng ngoại (IR). Với nhóm carboxyl (–COOH), tần số hấp thụ của liên
kết C=O thường nằm khoảng 1710 – 1730 cm⁻¹.
→ Vì vậy, 1720 cm⁻¹ là giá trị đặc trưng cho dao động của liên kết
C=O trong nhóm carboxyl.
Đáp án: D. Tín
hiệu liên kết O–H và C=O.
Nhóm carboxyl (–COOH)
gồm hai phần đặc trưng:
- Liên kết C=O
(carbonyl) → hấp thụ mạnh khoảng 1700 – 1720 cm⁻¹,
- Liên kết O–H (acid)
→ hấp thụ rất rộng trong vùng 2500 – 3300 cm⁻¹.
→ Khi trên phổ hồng
ngoại (IR) xuất hiện cả hai tín hiệu này cùng lúc, ta xác định được sự có mặt của
nhóm –COOH.