Câu 1 [190911]: Malic acid là hợp chất hữu cơ tạp chức, có mạch carbon không phân nhánh, là nguyên nhân chính gây nên vị chua của quả táo. Biết rằng 1 mol malic acid phản ứng được với tối đa 2 mol NaHCO3. Công thức của malic acid là
A, HOOC-CH(OH)-CH2-COOH.
B, HOOC-CH(OH)-CH(OH)-CHO.
C, HOOC-CH(CH3)-CH2-COOH.
D, CH3OOC-CH(OH)-COOH.
R(COOH)n + nNaHCO3 → R(COONa)n + nCO2 + nH2O
Mol acid : mol NaHCO3 = 1 : n = 1 : 2 => n = 2.
Vậy malic acid có 2 nhóm chức -COOH và do có mạch carbon không phân nhánh nên công thức cấu tạo của malic acid là HOOC-CH(OH)CH2-COOH.
Đáp án A. Đáp án: A
Mol acid : mol NaHCO3 = 1 : n = 1 : 2 => n = 2.
Vậy malic acid có 2 nhóm chức -COOH và do có mạch carbon không phân nhánh nên công thức cấu tạo của malic acid là HOOC-CH(OH)CH2-COOH.
Đáp án A. Đáp án: A
Câu 2 [190913]: Cho các nhận định sau:
(1) Giấm ăn làm đỏ quỳ tím.
(2) Nước ép tử quả chanh không hòa tan được CaCO3.
(3) Dùng acetic acid để tẩy sạch cặn bám ở trong phích nước nóng.
(4) Phản ứng của acetic acid với ethanol là phản ứng trung hòa.
(5) Acetic acid là acid yếu nhưng vẫn mạnh hơn carbonic acid; còn phenol có tính acid yếu hơn carbonic acid.
Số nhận đính đúng là
(1) Giấm ăn làm đỏ quỳ tím.
(2) Nước ép tử quả chanh không hòa tan được CaCO3.
(3) Dùng acetic acid để tẩy sạch cặn bám ở trong phích nước nóng.
(4) Phản ứng của acetic acid với ethanol là phản ứng trung hòa.
(5) Acetic acid là acid yếu nhưng vẫn mạnh hơn carbonic acid; còn phenol có tính acid yếu hơn carbonic acid.
Số nhận đính đúng là
A, 2.
B, 5.
C, 3.
D, 4.
(1) Đúng, giấm ăn chứa acetic acid nên là quỳ tím hoá đỏ.
(2) Sai, nước ép quả chanh chứa citric acid có công thức
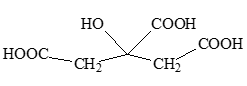
Nên hoà tan được CaCO3.
(3) Đúng, acetic acid hoà tan cặn bám phích nước nóng có thành phần chính là CaCO3 theo phản ứng
CaCO3 + 2CH3COOH (CH3COO)2Ca + CO2 + H2O
(CH3COO)2Ca + CO2 + H2O
(4) Sai, phản ứng thuộc loại phản ứng ester hoá.
(5) Đúng,
Acetic acid "đẩy" được H2CO3 ra khỏi muối carbonate
CaCO3 + 2CH3COOH (CH3COO)2Ca + CO2 + H2O
(CH3COO)2Ca + CO2 + H2O
Phenol có tính acid (phản ứng với NaOH), nhưng không làm đổi màu quỳ (rất yếu).
Đáp án C. Đáp án: C
(2) Sai, nước ép quả chanh chứa citric acid có công thức

Nên hoà tan được CaCO3.
(3) Đúng, acetic acid hoà tan cặn bám phích nước nóng có thành phần chính là CaCO3 theo phản ứng
CaCO3 + 2CH3COOH
 (CH3COO)2Ca + CO2 + H2O
(CH3COO)2Ca + CO2 + H2O
(4) Sai, phản ứng thuộc loại phản ứng ester hoá.
(5) Đúng,
Acetic acid "đẩy" được H2CO3 ra khỏi muối carbonate
CaCO3 + 2CH3COOH
 (CH3COO)2Ca + CO2 + H2O
(CH3COO)2Ca + CO2 + H2O
Phenol có tính acid (phản ứng với NaOH), nhưng không làm đổi màu quỳ (rất yếu).
Đáp án C. Đáp án: C
Câu 3 [190914]: Hai hợp chất hữu cơ X, Y có cùng công thức phân tử C3H6O2. Cả X và Y đều tác dụng với Na ; X tác dụng được với NaHCO3 còn Y có khả năng tham gia phản ứng tráng bạc. Công thức cấu tạo của X và Y lần lượt là
A, C2H5COOH và HCOOC2H5.
B, HCOOC2H5 và HOCH2OCH3.
C, HCOOC2H5 và HOCH2CH2CHO.
D, C2H5COOH và CH3CH(OH)CHO.
- X tác dụng với Na và NaHCO3 => X có nhóm chức -COOH. Vậy X là C2H5COOH.
- Y 2 oxygen, phản ứng với Na (có OH hoặc -COOH) và tráng bạc nên nhóm chức còn lại là -CH=O. Vậy Y vừa có OH, vừa có -CH=O. Vậy Y là HOCH2CH2CH=O hoặc CH3CH(OH)CH=O.
Đáp án D. Đáp án: D
- Y 2 oxygen, phản ứng với Na (có OH hoặc -COOH) và tráng bạc nên nhóm chức còn lại là -CH=O. Vậy Y vừa có OH, vừa có -CH=O. Vậy Y là HOCH2CH2CH=O hoặc CH3CH(OH)CH=O.
Đáp án D. Đáp án: D
Câu 4 [190915]: Ba chất hữu X, Y, Z mạch không phân nhánh cùng công thức phân tử C2H4O2 và có tính chất như sau:
▪ X tác dụng với Na2CO3 giải phóng CO2.
▪ Y tác dụng với Na và có phản ứng tráng gương.
▪ Z tác dụng với dung dịch NaOH, không tác dụng với Na.
Các chât X, Y, Z là
▪ X tác dụng với Na2CO3 giải phóng CO2.
▪ Y tác dụng với Na và có phản ứng tráng gương.
▪ Z tác dụng với dung dịch NaOH, không tác dụng với Na.
Các chât X, Y, Z là
A, X: HCOOCH3, Y: CH3COOH, Z: CH2(OH)CHO.
B, X: CH3COOH, Y: CH2(OH)CHO, Z: HCOOCH3.
C, X: CH2(OH)CHO, Y: CH3COOH, Z: HCOOCH3.
D, X: CH3COOH, Y: HCOOCH3, Z: CH2(OH)CHO.
X tác dụng được với Na2CO3 nên X phải có nhóm chức -COOH. Vậy X là CH3COOH.
Loại đáp án A và C.
Y có phản ứng với Na (OH hoặc COOH) và phản ứng tráng gương (-CH=O) => cấu tạo của Y phải là HOCH2CH=O.
Vậy Z là HCOOCH3.
=> Đáp án B Đáp án: B
Y có phản ứng với Na (OH hoặc COOH) và phản ứng tráng gương (-CH=O) => cấu tạo của Y phải là HOCH2CH=O.
Vậy Z là HCOOCH3.
=> Đáp án B Đáp án: B
Câu 5 [190919]: Trung hòa 2,7 gam carboxylic acid A cần vừa đủ 60 mL dung dịch NaOH 1 M. Acid A có công thức phân tử là
A, C2H4O2.
B, C3H4O2.
C, C4H6O4.
D, C2H2O4.
Ta có: nNaOH = 0,06 × 1 = 0,06mol
Phương trình phản ứng:
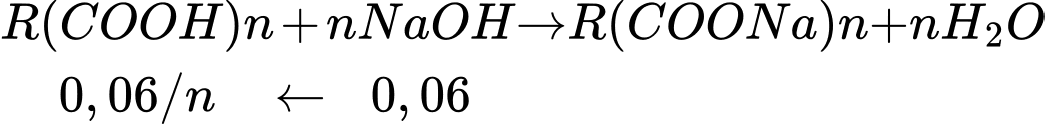
Theo phương trình: nR(COOH)n = nNaOH = 0,06/n
Giả sử: n=1 ⟹ R + 45 = 2,7 : 0,06 = 45 ⟹ R=0 (loại)
Giả sử: n=2 ⟹ R + 45 = 2,7 : 0,03 = 90 ⟹ R = 45 ( thoả mãn)
Vậy A có 2 nhóm COOH
Công thức cấu tạo của A là: HOOC-COOH
Có công thức phân tử là: C2H2O4
Chọn đáp án: D Đáp án: D
Phương trình phản ứng:
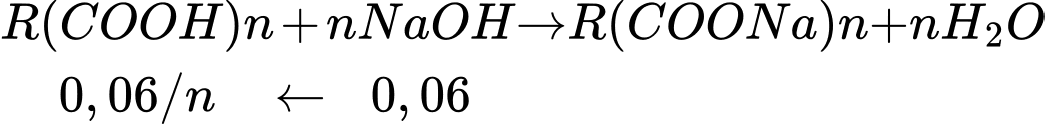
Theo phương trình: nR(COOH)n = nNaOH = 0,06/n
Giả sử: n=1 ⟹ R + 45 = 2,7 : 0,06 = 45 ⟹ R=0 (loại)
Giả sử: n=2 ⟹ R + 45 = 2,7 : 0,03 = 90 ⟹ R = 45 ( thoả mãn)
Vậy A có 2 nhóm COOH
Công thức cấu tạo của A là: HOOC-COOH
Có công thức phân tử là: C2H2O4
Chọn đáp án: D Đáp án: D
Câu 6 [190920]: Trung hòa 500 mL dung dịch carboxylic acid đơn chức X bằng 200 mL dung dịch NaOH 0,1 M, thu được 1,92 gam muối. Công thức của X và nồng độ mol của dung dịch X là
A, C2H5COOH với nồng độ 0,4 M.
B, C2H5COOH với nồng độ 0,04 M.
C, CH3COOH với nồng độ 0,4 M.
D, CH3COOH với nồng độ 0,04 M.
Đặt công thức của X là RCOOH
Số mol NaOH = CM.V = 0,1.0,2 = 0,02 mol.
Phản ứng
RCOOH + NaOH → RCOONa + H2O
0,02 ← 0,02 → 0,02 (mol)
- Nồng độ X = n/V = 0,02/0,5 = 0,04M
- Khối lượng mol RCOONa =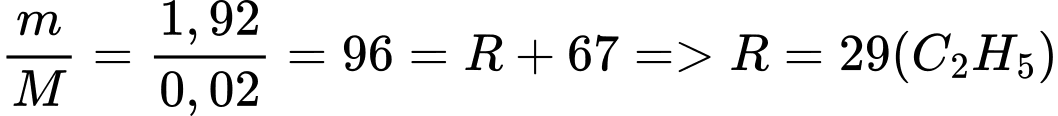
Vậy công thức của X là C2H5COOH.
Đáp án B Đáp án: B
Số mol NaOH = CM.V = 0,1.0,2 = 0,02 mol.
Phản ứng
RCOOH + NaOH → RCOONa + H2O
0,02 ← 0,02 → 0,02 (mol)
- Nồng độ X = n/V = 0,02/0,5 = 0,04M
- Khối lượng mol RCOONa =
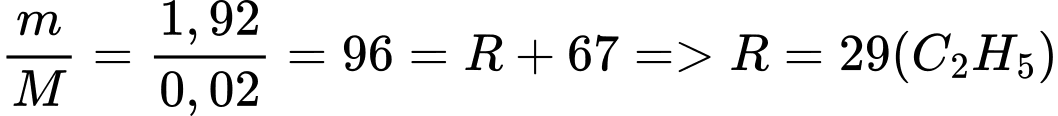
Vậy công thức của X là C2H5COOH.
Đáp án B Đáp án: B
Câu 7 [190921]: Tiến hành thí nghiệm với hợp chất Z thu được kết quả thể hiện trong bảng:
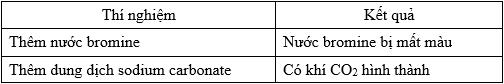
Hợp chất Z là

Hợp chất Z là
A, 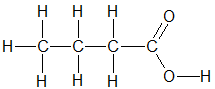

B, 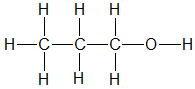

C, 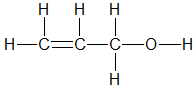

D, 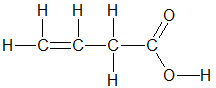

Z làm mất màu nước bromine => Z là hợp chất không no (có liên kết bội carbon-carbon) hoặc nhóm chức carbonyl aldehyde (-CH=O).
Z phản ứng với sodium carbonate => Z có nhóm chức carboxylic acid.
Đáp án D Đáp án: D
Z phản ứng với sodium carbonate => Z có nhóm chức carboxylic acid.
Đáp án D Đáp án: D
Câu 8 [190922]: Dưới đây là một số thông tin về hợp chất hữu cơ X:
▪ Phản ứng với potassium carbonate tạo ra khí carbon dioxide.
▪ Phản ứng với ethanol tạo ra chất lỏng có mùi thơm
▪ Phản ứng với sodium hydroxide tạo ra muối
Chất X là
▪ Phản ứng với potassium carbonate tạo ra khí carbon dioxide.
▪ Phản ứng với ethanol tạo ra chất lỏng có mùi thơm
▪ Phản ứng với sodium hydroxide tạo ra muối
Chất X là
A, ethanol.
B, ethanoic acid.
C, phenol.
D, acetaldehyde.
Từ các dữ kiện => X là ethanoic acid
2CH3COOH + K2CO3 → 2CH3COOK + CO2 + H2O
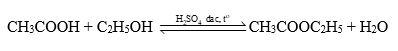
CH3COOH + C2H5OH CH3COOC2H5 + H2O
CH3COOH + NaOH → CH3COONa + H2O
Đáp án B. Đáp án: B
2CH3COOH + K2CO3 → 2CH3COOK + CO2 + H2O
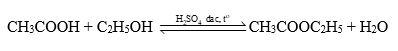
CH3COOH + C2H5OH CH3COOC2H5 + H2O
CH3COOH + NaOH → CH3COONa + H2O
Đáp án B. Đáp án: B
Câu 9 [190923]: MCPA và 2,4-D là hai loại thuốc diệt cỏ chọn lọc được sử dụng rộng rãi. Công thức cấu tạo của MCPA và 2,4-D như sau:
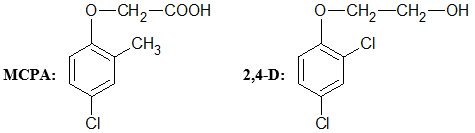
Chất nào sau đây có thể dùng để phân biệt MCPA với 2,4-D?

Chất nào sau đây có thể dùng để phân biệt MCPA với 2,4-D?
A, Acid hoá, AgNO3.
B, Thuốc thử Tollens.
C, Na kim loại.
D, Dung dịch Na2CO3.
MCPA có nhóm chức -COOH, 2,4-D không có nên có thể dùng Na2CO3 để phân biệt 2 chất. Khi đó, MCPA sẽ sủi bọt khí không màu, không mùi là CO2. 2,4-D không có hiện tượng.
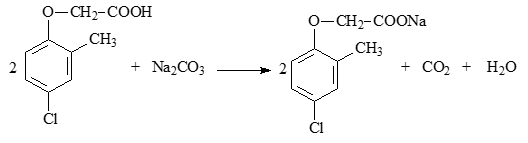 Đáp án: D
Đáp án: D
 Đáp án: D
Đáp án: D
Câu 10 [190930]: Cho các dung dịch sau: ethanol, glycerol, acetaldehyde, acetic acid. Để nhận biết các dung dịch trên, ta có thể sử dụng (xem như điều kiện phản ứng đủ)
A, Br2, NaOH.
B, Na2CO3, Cu(OH)2.
C, Na, Cu(OH)2.
D, Br2, AgNO3/NH3.
- Trích mẫu thử
- Cho Na2CO3 lần lượt vào 4 mẫu thử, mẫu thử có khí thoát ra là acetic acid
2CH3COOH + Na2CO3 → 2CH3COONa + CO2 + H2O
- Cho lần lượt từng mẫu vào kết tủa Cu(OH)2 mới điều chế (từ NaOH và CuSO4), mẫu thử hoà tan Cu(OH)2 tạo dung dịch màu xanh lam đậm là glycerol
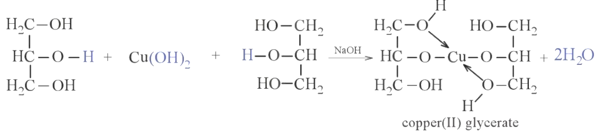
Đun nóng 2 mẫu còn lại, mẫu cho kết tủa màu đỏ gạch là acetaldehyde.
CH3CHO + 2Cu(OH)2 + NaOH → CH3COONa + Cu2O + 3H2O
Mẫu thử còn lại là ethanol Đáp án B. Đáp án: B
- Cho Na2CO3 lần lượt vào 4 mẫu thử, mẫu thử có khí thoát ra là acetic acid
2CH3COOH + Na2CO3 → 2CH3COONa + CO2 + H2O
- Cho lần lượt từng mẫu vào kết tủa Cu(OH)2 mới điều chế (từ NaOH và CuSO4), mẫu thử hoà tan Cu(OH)2 tạo dung dịch màu xanh lam đậm là glycerol

Đun nóng 2 mẫu còn lại, mẫu cho kết tủa màu đỏ gạch là acetaldehyde.
CH3CHO + 2Cu(OH)2 + NaOH → CH3COONa + Cu2O + 3H2O
Mẫu thử còn lại là ethanol Đáp án B. Đáp án: B
Câu 11 [190931]: Để trung hòa 6,72 gam một carboxylic acid no, đơn chức, mạch hở X cần dùng 200 gam dung dịch sodium hydroxide 2,24 %. Công thức của X là
A, CH3COOH.
B, HCOOH.
C, C2H5COOH.
D, C3H7COOH.
Gọi công thức của X là CnH2n+1COOH
Số mol sodium hydroxide =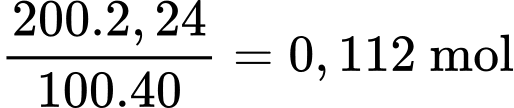
Phản ứng: CnH2n+1COOH + NaOH → CnH2n+1COONa + H2O
0,112 ← 0,112 (mol)
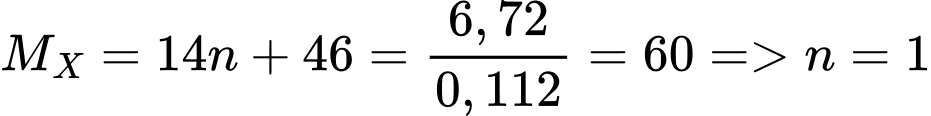
Vậy X là CH3COOH.
Đáp án A. Đáp án: A
Số mol sodium hydroxide =
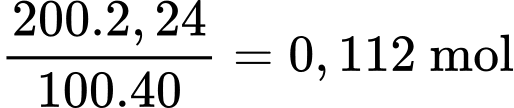
Phản ứng: CnH2n+1COOH + NaOH → CnH2n+1COONa + H2O
0,112 ← 0,112 (mol)
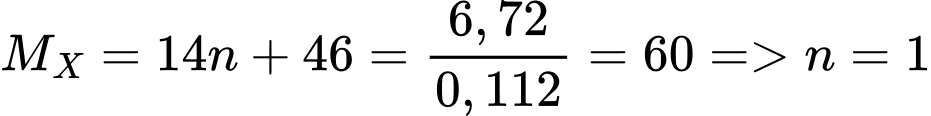
Vậy X là CH3COOH.
Đáp án A. Đáp án: A
Câu 12 [190932]: Cho thí nghiệm: Chuẩn độ acetic acid bằng dung dịch sodium hydroxide 0,15 M. Sau khi thực hiện thí nghiệm chuẩn độ này 3 lần, thu được bảng dưới đây:
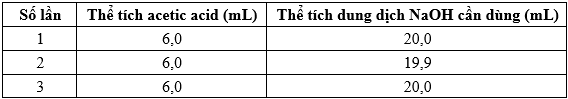
Nồng độ mol của acetic acid là

Nồng độ mol của acetic acid là
A, 0,1 M.
B, 0,5 M.
C, 0,3 M.
D, 0,2 M.
Thể tích trung bình của dung dịch NaOH 3 lần đo:
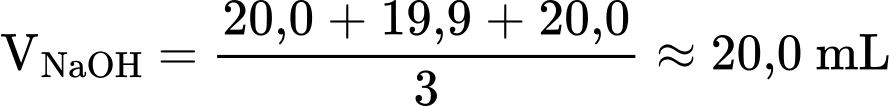 ;
;
Thể tích của acetic acid: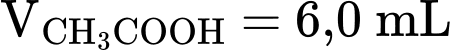 ;
;
Ta có:
Nồng độ mol của acetic acid: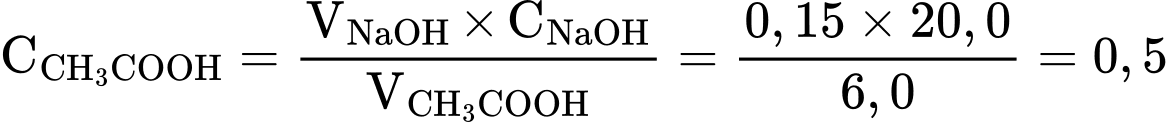 M
Đáp án: B
M
Đáp án: B
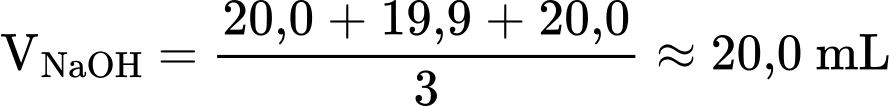 ;
; Thể tích của acetic acid:
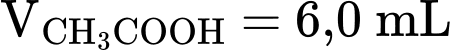 ;
;Ta có:

Nồng độ mol của acetic acid:
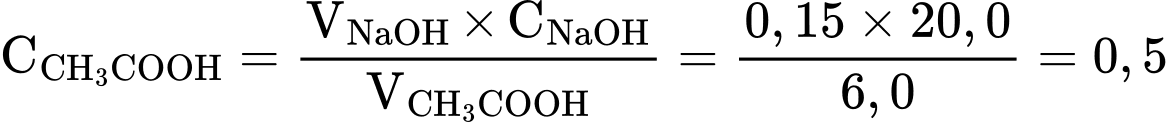 M
Đáp án: B
M
Đáp án: B
Câu 13 [705933]: Chanh là một loài thực vật cho quả nhỏ, thuộc chỉ cam chanh (citrus). Quả chanh được sử dụng làm thực phẩm. Nước ép chanh chứa khoảng 5% citric acid nên chanh có vị chua và độ pH khoảng 2 – 3. Công thức (X) được cho ở hình bên.
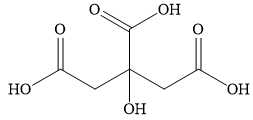
Chọn phát biểu đúng về citric acid

Chọn phát biểu đúng về citric acid
A, Công thức phân tử của citric acid là C4H6O7.
B, 1 mol citric acid tác dụng với Na tạo ra 2 mol H2.
C, Citric acid thuộc loại hợp chất đa chức.
D, Citric acid tác dụng với NaOH theo tỉ lệ mol 1 : 4.
Phân tích các phát biểu:
❌A – Sai. Công thức phân tử của citric acid là C6H8O7.
✔️B – Đúng. Citric acid có 1 nhóm OH (alcohol) và 3 nhóm (carboxylic acid) nên tác dụng với Na theo tỉ lệ 1:4
HOC3H4(COOH)3 + 4Na → NaOC3H4(COONa)3 + 2H2
❌C – Sai. Citric acid thuộc loại hợp chất tạp chức, citric acid có 1 nhóm OH (alcohol) và 3 nhóm (carboxylic acid)
❌D – Sai. Citric acid có 1 nhóm OH (alcohol) và 3 nhóm (carboxylic acid) nên tác dụng với NaOH theo tỉ lệ 1:3
Chọn đáp án B Đáp án: B
❌A – Sai. Công thức phân tử của citric acid là C6H8O7.
✔️B – Đúng. Citric acid có 1 nhóm OH (alcohol) và 3 nhóm (carboxylic acid) nên tác dụng với Na theo tỉ lệ 1:4
HOC3H4(COOH)3 + 4Na → NaOC3H4(COONa)3 + 2H2
❌C – Sai. Citric acid thuộc loại hợp chất tạp chức, citric acid có 1 nhóm OH (alcohol) và 3 nhóm (carboxylic acid)
❌D – Sai. Citric acid có 1 nhóm OH (alcohol) và 3 nhóm (carboxylic acid) nên tác dụng với NaOH theo tỉ lệ 1:3
Chọn đáp án B Đáp án: B
Câu 14 [1072396]: Benzoic acid là một chất phụ gia được dùng để bảo quản thực phẩm. Để điều chế benzoic acid từ toluene, thực hiện theo các bước sau:
Bước 1: Cho 10 mL toluene vào bình phản ứng dung tích 100 mL có lắp sinh hàn phía trên. Thêm khoảng 20 mL lượng dư dung dịch KMnO4 0,1 M. Khuấy đều và đun sôi 10 phút.
Bước 2: Vừa lắc hỗn hợp phản ứng vừa thêm từng lượng nhỏ oxalic acid đến khi mất màu tím. Lọc bỏ bỏ chất rắn, cô đặc phần dung dịch lọc.
Bước 3: Acid hóa phần dung dịch lọc bằng hydrochloric acid. Lọc lấy chất rắn, kết tinh lại bằng nước để cho sản phẩm sạch.
Cho các phát biểu sau:
(a) Sau bước 1, xuất hiện chất rắn màu đen.
(b) Sử dụng oxalic acid ở bước 2 có thể loại bỏ KMnO4 dư.
(c) Acid hóa bằng HCl thu được benzoic acid có thể chứng minh tính acid của HCl mạnh hơn benzoic acid.
(d) Kết tinh benzoic acid dựa trên nguyên lí độ tan của benzoic acid tại các nhiệt độ khác nhau là khác nhau.
Số phát biểu đúng là
Bước 1: Cho 10 mL toluene vào bình phản ứng dung tích 100 mL có lắp sinh hàn phía trên. Thêm khoảng 20 mL lượng dư dung dịch KMnO4 0,1 M. Khuấy đều và đun sôi 10 phút.
Bước 2: Vừa lắc hỗn hợp phản ứng vừa thêm từng lượng nhỏ oxalic acid đến khi mất màu tím. Lọc bỏ bỏ chất rắn, cô đặc phần dung dịch lọc.
Bước 3: Acid hóa phần dung dịch lọc bằng hydrochloric acid. Lọc lấy chất rắn, kết tinh lại bằng nước để cho sản phẩm sạch.
Cho các phát biểu sau:
(a) Sau bước 1, xuất hiện chất rắn màu đen.
(b) Sử dụng oxalic acid ở bước 2 có thể loại bỏ KMnO4 dư.
(c) Acid hóa bằng HCl thu được benzoic acid có thể chứng minh tính acid của HCl mạnh hơn benzoic acid.
(d) Kết tinh benzoic acid dựa trên nguyên lí độ tan của benzoic acid tại các nhiệt độ khác nhau là khác nhau.
Số phát biểu đúng là
A, 1.
B, 2.
C, 3.
D, 4.
Nhận định (a) – Đúng. Khi KMnO₄
khử trong phản ứng oxy hoá, tạo các sản phẩm MnO₂ (màu nâu/đen) → có chất rắn
đen.
Nhận định (b) – Đúng. Acid oxalic là chất
khử làm mất màu tím của KMnO₄ (KMnO₄ → Mn²⁺/MnO₂) — dùng để loại KMnO₄ dư.
Nhận định (c) – Đúng. Acid hóa bằng HCl
làm proton hoá anion benzoate → tạo benzoic acid kết tủa; điều này phản ánh HCl
là acid mạnh hơn benzoic acid.
Nhận định (d) – Đúng. Kết tinh (tinh chế)
dựa trên sự khác nhau về độ tan của benzoic acid ở nhiệt độ cao và thấp.
Đáp án: D. 4.
Câu 15 [684516]: Một loại giấm ăn có chứa hàm lượng 4,5 % acetic acid về thể tích. Thể tích dung dịch NaOH 2 M cần để trung hòa hết 5 lít lượng giấm trên là bao nhiêu lít? Biết khối lượng riêng của acetic acid là D = 1,05 g/mL. Kết quả làm tròn đến phần trăm.
Thể tích acetic acid có trong 5 lít giấm ăn là: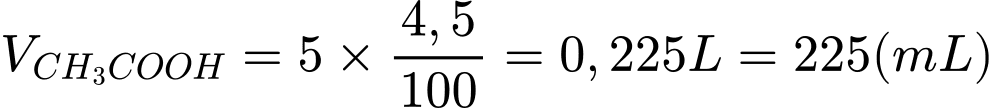
Khối lượng acetic acid tương ứng là: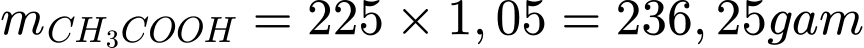
Phương trình phản ứng:
CH3COOH + NaOH → CH3COONa + H2O
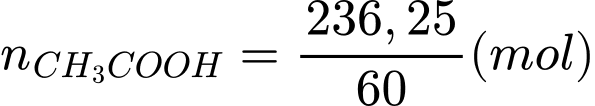
Theo phương trình: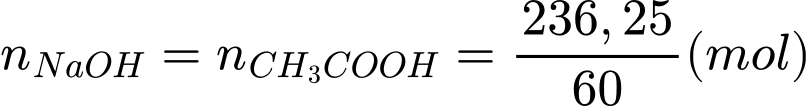
Thể tích dung dịch NaOH cần dùng là: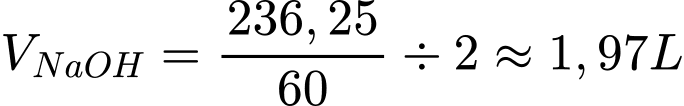
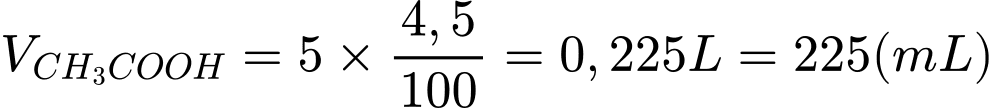
Khối lượng acetic acid tương ứng là:
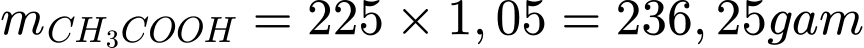
Phương trình phản ứng:
CH3COOH + NaOH → CH3COONa + H2O
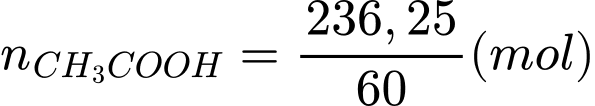
Theo phương trình:
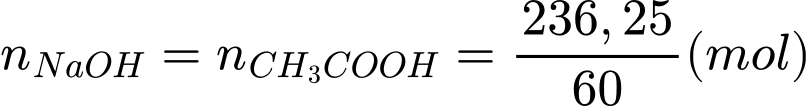
Thể tích dung dịch NaOH cần dùng là:
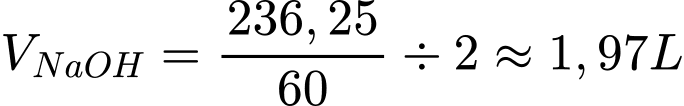
⟹ Điền đáp án: 1,97
Câu 16 [705945]: Tartaric acid HOOC–CH(OH)–CH(OH)–COOH có trong nho nhưng cũng có trong me, chuối, bơ. Tiến hành cho 1 mol tartaric acid phản ứng tối đa với a mol NaOH. Giá trị của a là bao nhiêu?
Tartaric acid có 2 nhóm COOH (carboxylic acid) nên 1 mol tartaric acid nên sẽ phản ứng với 2 mol NaOH.
Phương trình :
HOOC–CH(OH)–CH(OH)–COOH + 2NaOH ⟶ NaOOC–CH(OH)–CH(OH)–COONa
Điền đáp án : 2
Phương trình :
HOOC–CH(OH)–CH(OH)–COOH + 2NaOH ⟶ NaOOC–CH(OH)–CH(OH)–COONa
Điền đáp án : 2
Câu 17 [684514]: Formic acid là một chất lỏng, mùi xốc mạnh và gây bỏng da, acid này được chưng cất lần đầu từ loài kiến lửa có tên là Formicarufa. Kiến khi cắn sẽ “tiêm” dung dịch chứa 50% thể tích formic acid vào da. Trung bình mỗi lần cắn, kiến có thể “tiêm” khoảng 6,0.10-3 cm3 dung dịch formic acid. Để làm giảm lượng formic acid trong vết cắn, bác sĩ thường dùng thuốc có chứa thành phần là sodium hydrogencarbonate (NaHCO3). Khối lượng sodium hydrogencarbonate cần dùng để trung hoà hoàn toàn lượng formic acid từ vết kiến cắn (biết khối lượng riêng của formic acid là 1,22 g/cm3) là bao nhiêu mg?
Phương trình phản ứng:
HCOOH + NaHCO3 ⟶ HCOONa + CO2↑ + H2O
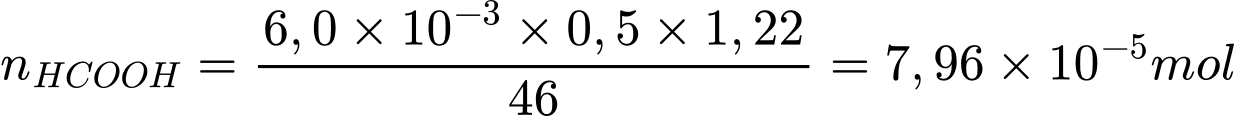
Theo phương trình hoá học: nNaHCO3 = nHCOOH=7,96×10-5mol
Khối lượng sodium hydrogencarbonate cần dùng là:mNaHCO3= 7,96 10-5 × 84 = 6,69×10-3 (g) = 6,69 (mg).
⟹ Điền đáp án: 6,69
HCOOH + NaHCO3 ⟶ HCOONa + CO2↑ + H2O
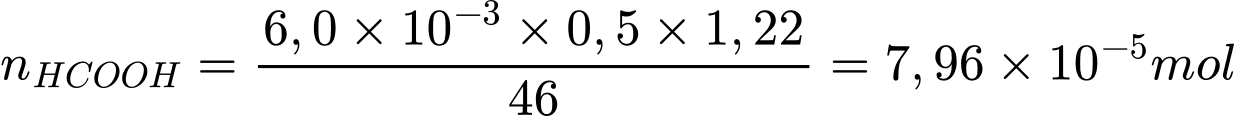
Theo phương trình hoá học: nNaHCO3 = nHCOOH=7,96×10-5mol
Khối lượng sodium hydrogencarbonate cần dùng là:mNaHCO3= 7,96 10-5 × 84 = 6,69×10-3 (g) = 6,69 (mg).
⟹ Điền đáp án: 6,69
Đọc ngữ cảnh dưới đây và trả lời các ID hỏi từ 18 đến 20.
Hàm lượng vitamin C (ascorbic acid, C6H8O6) có trong các loại đồ uống thể thao có thể được bằng cách chuẩn độ với dung dịch iodine. Phản ứng có thể được biểu diễn bằng phương trình:
I2(aq) + C6H8O6(aq) → 2I−(aq) + C6H6O6(aq) + 2H+(aq)
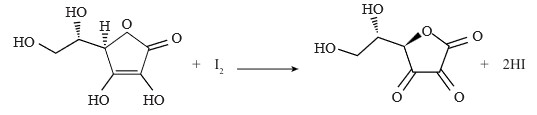
Trong phép chuẩn độ oxi hóa khử này, một chất chỉ thị riêng biệt đã được sử dụng là hồ tinh bột. Khi tất cả chất khử đã được phản ứng hết, lượng iodine dư sẽ kết hợp với chất chỉ thị hồ tinh bột để tạo ra chất có màu xanh lam đậm. Khi dung dịch iodine được sử dụng làm chất chuẩn độ, sự xuất hiện của màu xanh lam cho biết phản ứng đã hoàn tất. Khi đó chúng ra sẽ tiến hành ngừng phản ứng lại.
I2(aq) + C6H8O6(aq) → 2I−(aq) + C6H6O6(aq) + 2H+(aq)
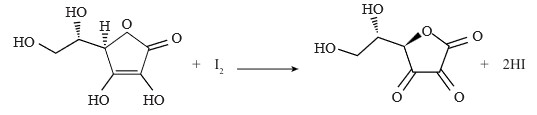
Trong phép chuẩn độ oxi hóa khử này, một chất chỉ thị riêng biệt đã được sử dụng là hồ tinh bột. Khi tất cả chất khử đã được phản ứng hết, lượng iodine dư sẽ kết hợp với chất chỉ thị hồ tinh bột để tạo ra chất có màu xanh lam đậm. Khi dung dịch iodine được sử dụng làm chất chuẩn độ, sự xuất hiện của màu xanh lam cho biết phản ứng đã hoàn tất. Khi đó chúng ra sẽ tiến hành ngừng phản ứng lại.
Câu 18 [382324]: Trong các phát biểu dưới đây, phát biểu nào đúng?
A, Hồ tinh bột đóng vai trò là chất chỉ thị.
B, Iodine có phản ứng với hồ tinh bột tạo ra hợp chất màu xanh lam đậm.
C, Ascorbic acid bị oxi hóa tạo thành glucose C6H6O6.
D, Trước điểm tương đương, dung dịch sẽ có màu xanh lam.
Phân tích các phát biểu:
✔️ A. Đúng. Hồ tinh bột đóng vai trò là chất chỉ thị.
❌ B. Sai. Iodine không có phản ứng với hồ tinh bột mà chỉ bị hấp phụ (quá trình vật lí)
❌ C. Sai. C6H6O6 có cùng công thức phân tử với glucose nhưng không phải glucose.
❌ D. Sai. Trước điểm tương đương không có I2 dư do phản ứng ngay với vitamin C nên không hấp phụ hồ tinh bột để chuyển thành dung dịch màu xanh lam.
⇒ Chọn đáp án A Đáp án: A
✔️ A. Đúng. Hồ tinh bột đóng vai trò là chất chỉ thị.
❌ B. Sai. Iodine không có phản ứng với hồ tinh bột mà chỉ bị hấp phụ (quá trình vật lí)
❌ C. Sai. C6H6O6 có cùng công thức phân tử với glucose nhưng không phải glucose.
❌ D. Sai. Trước điểm tương đương không có I2 dư do phản ứng ngay với vitamin C nên không hấp phụ hồ tinh bột để chuyển thành dung dịch màu xanh lam.
⇒ Chọn đáp án A Đáp án: A
Câu 19 [382325]: Lấy 25,0 mL một mẫu nước thể thao, tiến hành chuẩn độ thì thấy cần dùng 29,25 mL dung dịch I2 0,00125 M để đạt đến điểm tương đương. Khối lượng vitamin C (tính bằng mg) chứa trong chai 350 mL dung dịch đồ uống thể thao đó là bao nhiêu?
A, 60 mg.
B, 50 mg.
C, 90 mg.
D, 80 mg.
HD:
nI2 = 29,25 . 0,00125 = 0,0365625 (mol)
Phương trình phản ứng:
→ mvitamin C (trong 25mL) = 0,0365625 . 176 = 6,435 (mg)
→ mvitamin C (trong 1mL) = 6,435 ÷ 25 = 0,2574 (mg)
→ mvitamin C (trong 350mL) = 0,2574 . 350 = 90,09 (g) ≈ 90(mg)
⇒ Chọn đáp án C Đáp án: C
nI2 = 29,25 . 0,00125 = 0,0365625 (mol)
Phương trình phản ứng:
I2 (aq) + C6H8O6 (aq) → 2I- (aq) + C6H8O6 (aq) + 2H+ (aq)
Theo tỉ lệ phản ứng trên phương trình: nI2 = nvitamin C = 0,0365625 (mol)→ mvitamin C (trong 25mL) = 0,0365625 . 176 = 6,435 (mg)
→ mvitamin C (trong 1mL) = 6,435 ÷ 25 = 0,2574 (mg)
→ mvitamin C (trong 350mL) = 0,2574 . 350 = 90,09 (g) ≈ 90(mg)
⇒ Chọn đáp án C Đáp án: C
Câu 20 [382326]: Vì phân tử iodine không tan nhiều trong nước nên dung dịch “iodine” được sử dụng trong chuẩn độ oxi hóa khử thường chứa ion triiodide (I3−). Do đó, phương trình chuẩn độ oxy hóa khử của vitamin C bằng iodine có thể được viết là
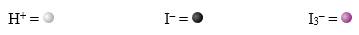
C6H8O6(aq) + I3−(aq) → C6H6O6(aq) + 3I−(aq) + 2H+(aq)
Coi như các ion khác không được hiển thị. Sơ đồ nào thể hiện rõ nhất lượng ion còn lại trong dung dịch tại điểm tương đương khi chuẩn độ vitamin C bằng triiodide?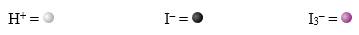
A, 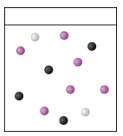

B, 

C, 

D, 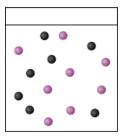

- Tại thời điểm tương đương, các chất phản ứng sẽ hết, còn sản phẩm gồm H+ và I- → Loại B và D vì không có ion H+.
- Sản phẩm có 3I- và 2H+ → tỉ lệ I- : H+ là 3 : 2
+ Sơ đồ A có 2H+, 4I- và 6I3-
+ Sơ đồ C có 4H+, 4I- và 4I3-
- Theo tỉ lệ phương trình thì số ion I- phải nhiều hơn số ion H+
→ Sơ đồ thể hiện rõ nhất lượng ion còn lại trong dung dịch tại điểm tương đương khi chuẩn độ vitamin C bằng triiodide là sơ đồ A.
(Khi có I3- thì có thể xảy ra quá trình phân li của I3-: I3- → I2 + I-. Có đóng góp vào dung dịch thêm ion I- nên sơ đồ biểu thị 4I-) Đáp án: A
- Sản phẩm có 3I- và 2H+ → tỉ lệ I- : H+ là 3 : 2
+ Sơ đồ A có 2H+, 4I- và 6I3-
+ Sơ đồ C có 4H+, 4I- và 4I3-
- Theo tỉ lệ phương trình thì số ion I- phải nhiều hơn số ion H+
→ Sơ đồ thể hiện rõ nhất lượng ion còn lại trong dung dịch tại điểm tương đương khi chuẩn độ vitamin C bằng triiodide là sơ đồ A.
(Khi có I3- thì có thể xảy ra quá trình phân li của I3-: I3- → I2 + I-. Có đóng góp vào dung dịch thêm ion I- nên sơ đồ biểu thị 4I-) Đáp án: A