Câu 1 [186166]: Cho phản ứng thuận nghịch:
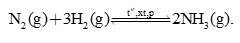
Đồ thị hình bên biểu diễn nồng độ các chất trong phản ứng theo thời gian.
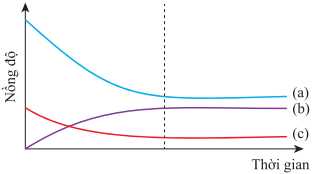
Đường biểu diễn nồng độ của NH3 là
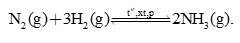
Đồ thị hình bên biểu diễn nồng độ các chất trong phản ứng theo thời gian.

Đường biểu diễn nồng độ của NH3 là
A, đường (a).
B, đường (b).
C, đường (c).
D, cả đường (a) và (b).
Tại thời điểm bắt đầu phản ứng, chưa có sản phẩm NH3 được tạo thành nên nồng độ của nó bằng 0.
→ Theo đó, Đường biểu diễn nồng độ của NH3 phù hợp là đường (b)
⇒ Chọn đáp án B Đáp án: B
→ Theo đó, Đường biểu diễn nồng độ của NH3 phù hợp là đường (b)
⇒ Chọn đáp án B Đáp án: B
Câu 2 [186167]: Cho đồ thị biểu diễn sự thay đổi nồng độ các chất tham gia và chất sản phẩm theo thời gian như hình sau:
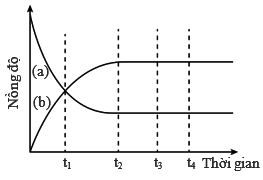
Phản ứng bắt đầu đạt trạng thái cân bằng vào thời điểm nào sau đây?

Phản ứng bắt đầu đạt trạng thái cân bằng vào thời điểm nào sau đây?
A, t1.
B, t2.
C, t3.
D, t4.
HD: Nhiều bạn nhanh ẩu chọn thời điểm t1 vì cho rằng điểm cắt nhau là điểm cần tìm. Tuy nhiên, không đơn giản như vậy, các bạn cần ngẫm kỹ lại một chút.
► Hình vẽ biểu diễn mối quan hệ NỒNG ĐỘ - thời gian.
⇝ cần nhớ lại về cân bằng liên quan đến nồng độ: đó là nồng độ các chất tại cân bằng không đổi.
⇒ quan sát hình vẽ, bắt đầu từ thời điểm t2 thì nồng độ các chất không thay đổi ⇝ Chọn đáp án B. Đáp án: B
► Hình vẽ biểu diễn mối quan hệ NỒNG ĐỘ - thời gian.
⇝ cần nhớ lại về cân bằng liên quan đến nồng độ: đó là nồng độ các chất tại cân bằng không đổi.
⇒ quan sát hình vẽ, bắt đầu từ thời điểm t2 thì nồng độ các chất không thay đổi ⇝ Chọn đáp án B. Đáp án: B
Câu 3 [186168]: Cho hai đồ thị (a) và (b) dưới đây:
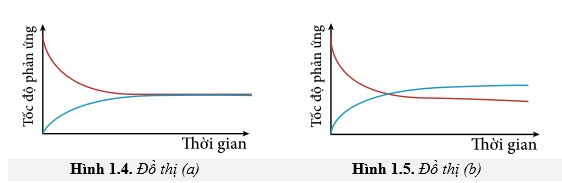
Đồ thị nào biểu diễn đúng sự thay đổi tốc độ phản ứng thuận và tốc độ phản ứng nghịch theo thời gian?

Đồ thị nào biểu diễn đúng sự thay đổi tốc độ phản ứng thuận và tốc độ phản ứng nghịch theo thời gian?
A, Đồ thị (a).
B, Đồ thị (b).
C, Cả 2 đồ thị (a) và (b) đều đúng.
D, Cả 2 đồ thị (a), (b) đều sai.
HD: Phân tích: tại thời điểm cân bằng, tốc độ phản ứng thuận và phản ứng nghịch bằng nhau.
⇝ có nghĩa là 2 đường biểu diễn tốc độ phản ứng thuận và nghịch sẽ trùng nhau trong khoảng thời gian cân bằng.
Theo đó, đồ thi (a) thỏa mãn và (b) không thỏa mãn ⇝ Chọn đáp án A. Đáp án: A
⇝ có nghĩa là 2 đường biểu diễn tốc độ phản ứng thuận và nghịch sẽ trùng nhau trong khoảng thời gian cân bằng.
Theo đó, đồ thi (a) thỏa mãn và (b) không thỏa mãn ⇝ Chọn đáp án A. Đáp án: A
Câu 4 [186162]: Cho phản ứng thuận nghịch sau:
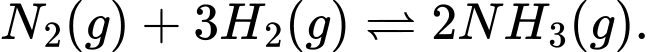
Phát biểu nào sau đây đúng?
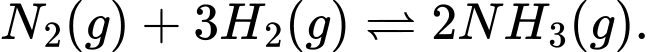
Phát biểu nào sau đây đúng?
A, Tại thời điểm cân bằng, nồng độ các chất trong phản ứng bằng nhau.
B, Tại thời điểm cân bằng, tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
C, Tại thời điểm cân bằng, nồng độ NH3 gấp hai lần nồng độ của N2.
D, Tại thời điểm cân bằng, các chất không tham gia phản ứng với nhau nữa.
HD: Phân tích các phát biểu:
❌ A. sai vì tại cân bằng, nồng độ các chất không đổi, còn bằng nhau hay không thì chưa khẳng định được.
✔️ B. đúng theo khái niệm.
❌ C. sai vì tương tự ý A, tùy thuộc vào lượng chất cho tham gia, chưa thể biết được mối quan hệ các chất ở cân bằng, chỉ biết nó không đổi thôi.
❌ D. sai vì cân bằng hóa học là cân bằng động, nghĩa là tại cân bằng các chất vẫn tiếp tục phản ứng với nhau nhưng lượng mất đi và tạo ra chất đó là bằng nhau nên nồng độ các chất bất kỳ sẽ vẫn không đổi. Đáp án: B
❌ A. sai vì tại cân bằng, nồng độ các chất không đổi, còn bằng nhau hay không thì chưa khẳng định được.
✔️ B. đúng theo khái niệm.
❌ C. sai vì tương tự ý A, tùy thuộc vào lượng chất cho tham gia, chưa thể biết được mối quan hệ các chất ở cân bằng, chỉ biết nó không đổi thôi.
❌ D. sai vì cân bằng hóa học là cân bằng động, nghĩa là tại cân bằng các chất vẫn tiếp tục phản ứng với nhau nhưng lượng mất đi và tạo ra chất đó là bằng nhau nên nồng độ các chất bất kỳ sẽ vẫn không đổi. Đáp án: B
Câu 5 [186163]: Cho phản ứng thuận nghịch sau:
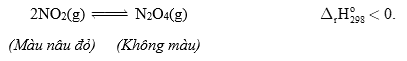
Phát biểu nào sau đây đúng?
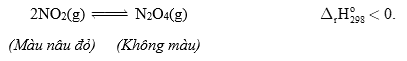
Phát biểu nào sau đây đúng?
A, Theo thời gian màu nâu đỏ đậm dần.
B, Tại cân bằng, nồng độ NO2 và nồng độ N2O4 bằng nhau.
C, Cân bằng là cân bằng tĩnh vì nồng độ các chất không thay đổi.
D, Khi đạt trạng thái cân bằng, phản ứng thuận và phản ứng nghịch vẫn diễn biến và có tốc độ bằng nhau.
HD: Phân tích các phát biểu:
❌ A. sai vì theo thời gian NO2 (màu nâu) phản ứng tạo N2O4 (không màu) nên màu nâu phải nhạt dần.
❌ B. sai vì tại cân bằng, nồng độ NO2 và N2O4 không đổi chứ chưa biết được bằng nhau hay không.
❌ C. sai vì cân bằng hóa học là cân bằng động do phản ứng thuận và phản ứng nghịch vẫn tiếp diễn tại cân bằng và có tốc độ bằng nhau.
✔️ D. đúng theo phân tích trên. Đáp án: D
❌ A. sai vì theo thời gian NO2 (màu nâu) phản ứng tạo N2O4 (không màu) nên màu nâu phải nhạt dần.
❌ B. sai vì tại cân bằng, nồng độ NO2 và N2O4 không đổi chứ chưa biết được bằng nhau hay không.
❌ C. sai vì cân bằng hóa học là cân bằng động do phản ứng thuận và phản ứng nghịch vẫn tiếp diễn tại cân bằng và có tốc độ bằng nhau.
✔️ D. đúng theo phân tích trên. Đáp án: D
Câu 6 [186390]: Ý nào biểu diễn đúng hằng số cân bằng của phản ứng sau:
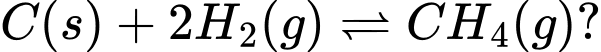
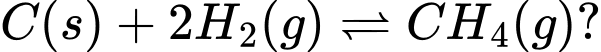
A, 

B, 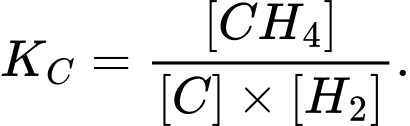
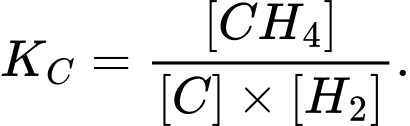
C, 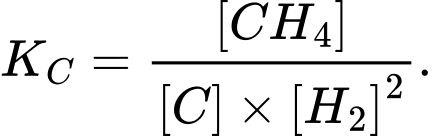
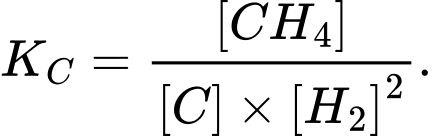
D, 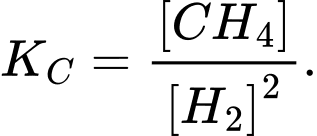
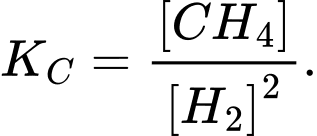
HƯỚNG DẪN GIẢI:
Chú ý: Nồng độ của chất rắn trong biểu thức hằng số cân bằng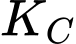 được coi bằng 1 (M).
được coi bằng 1 (M).
Áp dụng biểu thức tính hằng số cân bằng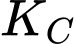 cho phản ứng trên:
cho phản ứng trên: 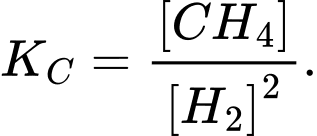
⟹ Chọn đáp án: D Đáp án: D
Chú ý: Nồng độ của chất rắn trong biểu thức hằng số cân bằng
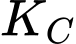 được coi bằng 1 (M).
được coi bằng 1 (M). Áp dụng biểu thức tính hằng số cân bằng
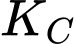 cho phản ứng trên:
cho phản ứng trên: 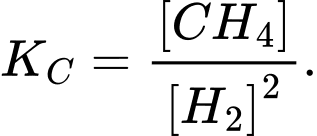
⟹ Chọn đáp án: D Đáp án: D
Câu 7 [186391]: Ý nào biểu diễn đúng hằng số cân bằng của phản ứng sau:
CaCO3(s)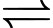 CaO(s) + CO2(g)?
CaO(s) + CO2(g)?
CaCO3(s)
 CaO(s) + CO2(g)?
CaO(s) + CO2(g)? A, 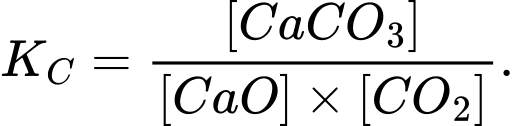
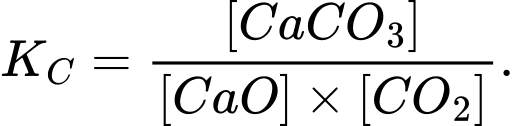
B, 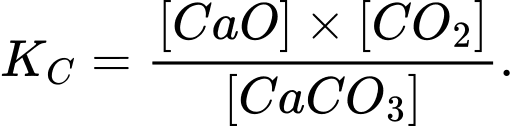
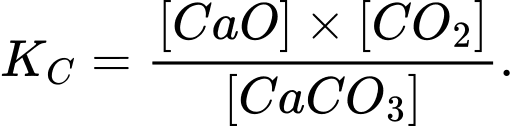
C, 

D, 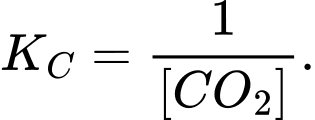
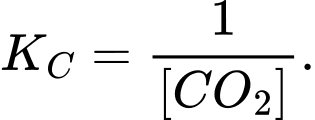
HƯỚNG DẪN GIẢI:
- Chú ý: Nồng độ của chất rắn trong biểu thức hằng số cân bằng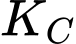 được coi bằng 1 (M).
được coi bằng 1 (M).
Áp dụng biểu thức tính hằng số cân bằng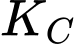 cho phản ứng trên:
cho phản ứng trên: 
⟹ Chọn đáp án: C Đáp án: C
- Chú ý: Nồng độ của chất rắn trong biểu thức hằng số cân bằng
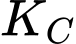 được coi bằng 1 (M).
được coi bằng 1 (M). Áp dụng biểu thức tính hằng số cân bằng
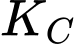 cho phản ứng trên:
cho phản ứng trên: 
⟹ Chọn đáp án: C Đáp án: C
Câu 8 [1072295]: Người ta cho N2 và H2 vào trong bình kín dung tích không đổi và thực hiện phản ứng: N2(g) + 3H2(g) ⇌ 2NH3(g). Sau một thời gian, nồng độ các chất trong bình như sau: [N2] = 2 M ; [H2] = 3 M ; [NH3] = 2 M. Nồng độ mol/L của N2 ban đầu là bao nhiêu?
A, 1,0.
B, 1,8.
C, 2,5.
D, 3,0.
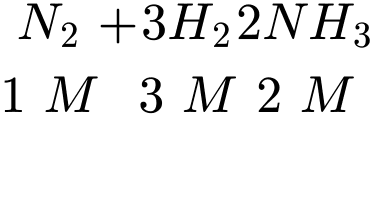
Theo PTHH nồng độ N2 phản ứng là 1 M
Nồng độ của N2 ban đầu là C = 1 + 2 = 3 M
Đáp án: D. 3,0. Đáp án: D
Câu 9 [1072296]: Trong công nghiệp, hydrogen được sản xuất từ phản ứng:
CH4(g) + H2O(g) ⇌ 3H2(g) + CO(g)
Tính hằng số cân bằng KC của phản ứng trên ở 760 oC. Biết ở nhiệt độ này nồng độ mol của CH4, H2O, H2 và CO ở trạng thái cân bằng lần lượt là 0,126 M; 0,242 M; 1,150 M và 0,126 M.
CH4(g) + H2O(g) ⇌ 3H2(g) + CO(g)
Tính hằng số cân bằng KC của phản ứng trên ở 760 oC. Biết ở nhiệt độ này nồng độ mol của CH4, H2O, H2 và CO ở trạng thái cân bằng lần lượt là 0,126 M; 0,242 M; 1,150 M và 0,126 M.
A, 5,14.
B, 6,28.
C, 8,47.
D, 9,85.
Hằng số cân bằng KC của phản ứng trên là:
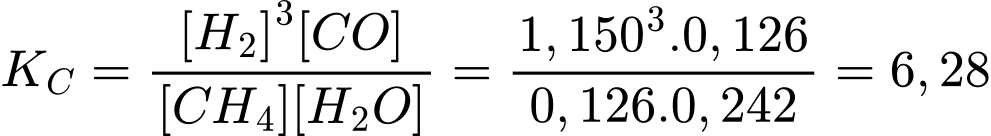
Đáp án: B. 6,28. Đáp án: B
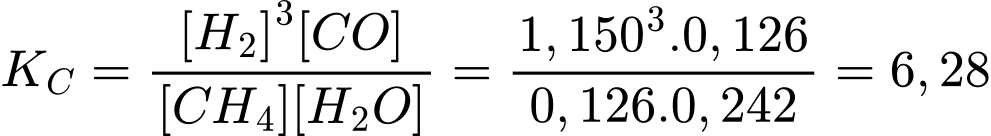
Đáp án: B. 6,28. Đáp án: B
Câu 10 [186404]: Cho phản ứng sau: 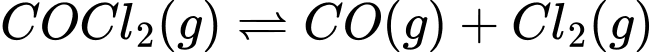 có
có 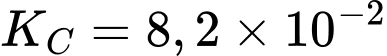 (ở
(ở 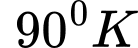 ). Ở trạng thái cân bằng, nồng độ CO và
). Ở trạng thái cân bằng, nồng độ CO và 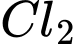 đều bằng 0,150 M thì nồng độ
đều bằng 0,150 M thì nồng độ 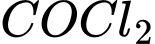 là bao nhiêu?
là bao nhiêu?
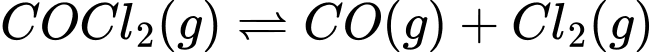 có
có 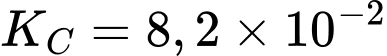 (ở
(ở 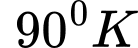 ). Ở trạng thái cân bằng, nồng độ CO và
). Ở trạng thái cân bằng, nồng độ CO và 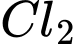 đều bằng 0,150 M thì nồng độ
đều bằng 0,150 M thì nồng độ 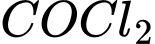 là bao nhiêu?
là bao nhiêu? A, 0,274 M.
B, 0,018 M.
C, 0,075 M.
D, 0,225 M.
Chọn A
HD:
Hằng số cân bằng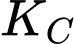 cho phản ứng trên tại nhiệt độ 900 K là:
cho phản ứng trên tại nhiệt độ 900 K là:
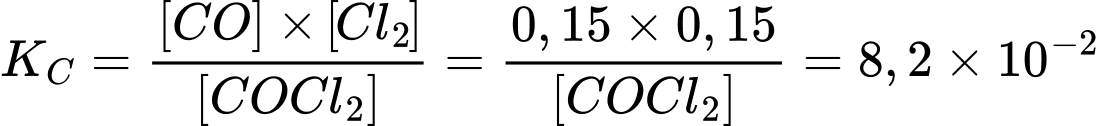 →
→ 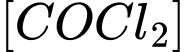 = 0,274 M.
Đáp án: A
= 0,274 M.
Đáp án: A
HD:
Hằng số cân bằng
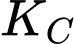 cho phản ứng trên tại nhiệt độ 900 K là:
cho phản ứng trên tại nhiệt độ 900 K là: 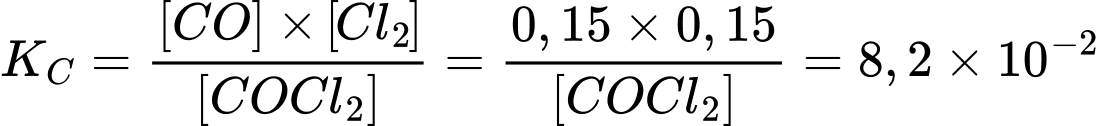 →
→ 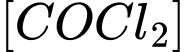 = 0,274 M.
Đáp án: A
= 0,274 M.
Đáp án: A
Câu 11 [186396]: Cho phương trình phản ứng: 2A(g) + B(g) 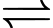 2X(g) + 2Y(g).
2X(g) + 2Y(g).
Người ta trộn bốn chất, mỗi chất 1 mol vào bình kín dung tích 2 lít (không đổi). Khi cân bằng, lượng chất X có trong bình là 1,6 mol. Nồng độ chất B ở trạng thái cân bằng tương ứng là
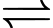 2X(g) + 2Y(g).
2X(g) + 2Y(g).Người ta trộn bốn chất, mỗi chất 1 mol vào bình kín dung tích 2 lít (không đổi). Khi cân bằng, lượng chất X có trong bình là 1,6 mol. Nồng độ chất B ở trạng thái cân bằng tương ứng là
A, 0,70 M.
B, 0,80 M.
C, 0,35 M.
D, 0,50 M.
HƯỚNG DẪN GIẢI:
- Nồng độ các chất tại thời điểm ban đầu: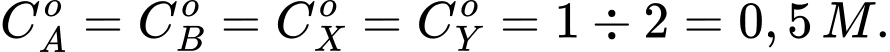
* Lập giản đồ quá trình: giả sử lượng A đã phản ứng là 2a M.
2A(g) + B(g)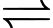 2X(g) + 2Y(g).
2X(g) + 2Y(g).
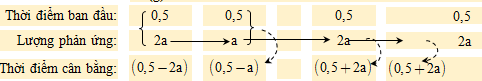
Nồng độ chất X tại thời điểm cân bằng: [X] = 1,6 ÷ 2 = 0,8 M.
Mặt khác, [X] = 0,5 + 2a = 0,8 → a = 0,15.
Vậy nồng độ chất B tại trạng thái cân bằng tương ứng là 0,5 – a = 0,5 – 0,15 = 0,35 M.
⟹ Chọn đáp án: C Đáp án: C
- Nồng độ các chất tại thời điểm ban đầu:
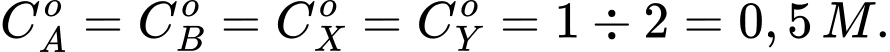
* Lập giản đồ quá trình: giả sử lượng A đã phản ứng là 2a M.
2A(g) + B(g)
 2X(g) + 2Y(g).
2X(g) + 2Y(g).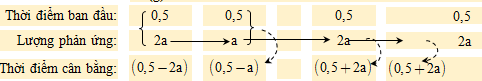
Nồng độ chất X tại thời điểm cân bằng: [X] = 1,6 ÷ 2 = 0,8 M.
Mặt khác, [X] = 0,5 + 2a = 0,8 → a = 0,15.
Vậy nồng độ chất B tại trạng thái cân bằng tương ứng là 0,5 – a = 0,5 – 0,15 = 0,35 M.
⟹ Chọn đáp án: C Đáp án: C
Câu 12 [186397]: Cho phản ứng: A(g) + B(g) 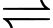 C(g). Nồng độ ban đầu của chất A là 0,12 mol/L; của chất B là 0,1 mol/L. Sau 10 phút, nồng độ của B giảm xuống chỉ còn 0,078 mol/L. Nồng độ còn lại (mol/l) của chất A tương ứng là
C(g). Nồng độ ban đầu của chất A là 0,12 mol/L; của chất B là 0,1 mol/L. Sau 10 phút, nồng độ của B giảm xuống chỉ còn 0,078 mol/L. Nồng độ còn lại (mol/l) của chất A tương ứng là
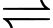 C(g). Nồng độ ban đầu của chất A là 0,12 mol/L; của chất B là 0,1 mol/L. Sau 10 phút, nồng độ của B giảm xuống chỉ còn 0,078 mol/L. Nồng độ còn lại (mol/l) của chất A tương ứng là
C(g). Nồng độ ban đầu của chất A là 0,12 mol/L; của chất B là 0,1 mol/L. Sau 10 phút, nồng độ của B giảm xuống chỉ còn 0,078 mol/L. Nồng độ còn lại (mol/l) của chất A tương ứng là A, 0,042.
B, 0,098.
C, 0,020.
D, 0,034.
HƯỚNG DẪN GIẢI:
Nồng độ chất B đã phản ứng = 0,1 – 0,078 = 0,022 M.
*Lập giản đồ quá trình phản ứng:
A(g) + B(g) C(g)..
C(g)..
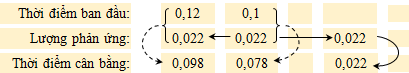
Nồng độ chất A còn lại tương ứng là 0,12 – 0,022 = 0,098 M.
⟹ Chọn đáp án: B Đáp án: B
Nồng độ chất B đã phản ứng = 0,1 – 0,078 = 0,022 M.
*Lập giản đồ quá trình phản ứng:
A(g) + B(g)
 C(g)..
C(g)..
Nồng độ chất A còn lại tương ứng là 0,12 – 0,022 = 0,098 M.
⟹ Chọn đáp án: B Đáp án: B
Câu 13 [186398]: Cho phản ứng: 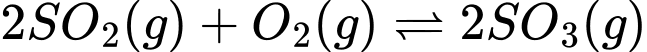 . Nồng độ ban đầu của
. Nồng độ ban đầu của 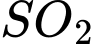 và
và 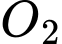 tương ứng trong bình kín có thể tích không đổi là 4 mol/L và 2 mol/L. Khi phản ứng cân bằng, thấy có 80% lượng khí
tương ứng trong bình kín có thể tích không đổi là 4 mol/L và 2 mol/L. Khi phản ứng cân bằng, thấy có 80% lượng khí 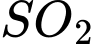 đã phản ứng, khi đó nồng độ của
đã phản ứng, khi đó nồng độ của 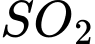 và
và 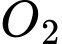 lần lượt là
lần lượt là
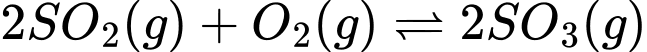 . Nồng độ ban đầu của
. Nồng độ ban đầu của 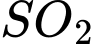 và
và 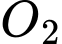 tương ứng trong bình kín có thể tích không đổi là 4 mol/L và 2 mol/L. Khi phản ứng cân bằng, thấy có 80% lượng khí
tương ứng trong bình kín có thể tích không đổi là 4 mol/L và 2 mol/L. Khi phản ứng cân bằng, thấy có 80% lượng khí 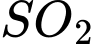 đã phản ứng, khi đó nồng độ của
đã phản ứng, khi đó nồng độ của 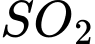 và
và 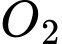 lần lượt là
lần lượt là A, 3,2 M và 3,2 M.
B, 1,6 M và 3,2 M.
C, 0,8 M và 0,4 M.
D, 3,2 M và 1,6 M.
HƯỚNG DẪN GIẢI:
Nồng độ chất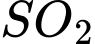 đã phản ứng = 80 x 4 ÷ 100 = 3,2 M.
đã phản ứng = 80 x 4 ÷ 100 = 3,2 M.
*Lập giản đồ quá trình phản ứng:
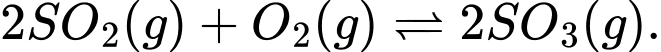

Nồng độ của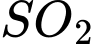 và
và 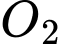 lần lượt là 0,8 M và 0,4 M.
lần lượt là 0,8 M và 0,4 M.
⟹ Chọn đáp án: C Đáp án: C
Nồng độ chất
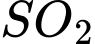 đã phản ứng = 80 x 4 ÷ 100 = 3,2 M.
đã phản ứng = 80 x 4 ÷ 100 = 3,2 M. *Lập giản đồ quá trình phản ứng:
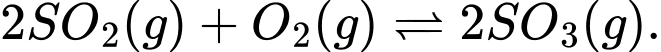

Nồng độ của
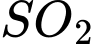 và
và 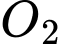 lần lượt là 0,8 M và 0,4 M.
lần lượt là 0,8 M và 0,4 M.⟹ Chọn đáp án: C Đáp án: C
Câu 14 [186224]: Hệ cân bằng sau được thực hiện trong bình kín:
 ;
; 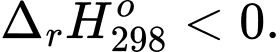
Cân bằng trên chuyển dịch theo chiều nghịch khi
 ;
; 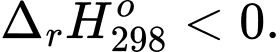
Cân bằng trên chuyển dịch theo chiều nghịch khi
A, thêm khí H2 vào hệ.
B, tăng áp suất chung của hệ.
C, cho chất xúc tác vào hệ.
D, giảm nhiệt độ của hệ.
Đáp án A.
+) Khi thêm khí H2 vào hệ → Cân bằng chuyển dịch theo chiều giảm H2 tức là chiều nghịch.
+) Khi tăng áp suất chung của hệ thì cân bằng không bị chuyển dịch do số mol khí ở trước và sau phản ứng bằng nhau.
+) Khi tăng áp suất chung của hệ thì cân bằng không bị chuyển dịch do số mol khí ở trước và sau phản ứng bằng nhau.
+) Khi thêm chất xúc tác thì cân bằng không bị chuyển dịch mà chỉ làm cho phản ứng nhanh đạt trạng thái cân bằng tức là thay đổi tốc độ phản ứng.
+) Phản ứng theo chiều thuận là phản ứng tỏa nhiệt, khi giảm nhiệt độ thì cân bằng sẽ chuyển dịch theo chiều thuận.
Đáp án: A
Câu 15 [186225]: Hệ cân bằng sau được thực hiện trong bình kín:
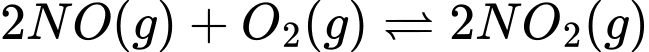 ;
; 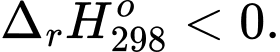
Cân bằng trên chuyển dịch theo chiều thuận khi
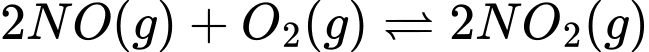 ;
; 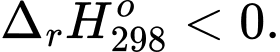
Cân bằng trên chuyển dịch theo chiều thuận khi
A, thêm khí NO2 vào hệ.
B, tăng áp suất chung của hệ.
C, cho chất xúc tác vào hệ.
D, tăng nhiệt độ của hệ.
Đáp án B.
A. thêm khí NO2 vào hệ làm tăng nồng độ NO2, CBCD theo chiều làm giảm nồng độ NO2 → chiều nghịch.
B. tăng áp suất chung của hệ cân bằng chuyển dịch theo chiều thuận.
2NO(g) + O2(g)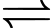 2NO2(g);
2NO2(g); 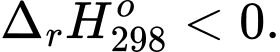
3 mol khí 2 mol khíC. cho chất xúc tác vào hệ: Chất xúc tác không làm chuyển dịch cân bằng hóa học nên cân bằng không chuyển dịch.
D. tăng nhiệt độ của hệ: phản ứng tỏa nhiệt nên tăng nhiệt độ CBCD theo chiều nghịch. Đáp án: B
A. thêm khí NO2 vào hệ làm tăng nồng độ NO2, CBCD theo chiều làm giảm nồng độ NO2 → chiều nghịch.
B. tăng áp suất chung của hệ cân bằng chuyển dịch theo chiều thuận.
2NO(g) + O2(g)
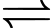 2NO2(g);
2NO2(g); 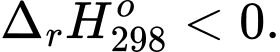
3 mol khí 2 mol khíC. cho chất xúc tác vào hệ: Chất xúc tác không làm chuyển dịch cân bằng hóa học nên cân bằng không chuyển dịch.
D. tăng nhiệt độ của hệ: phản ứng tỏa nhiệt nên tăng nhiệt độ CBCD theo chiều nghịch. Đáp án: B
Câu 16 [186226]: Cho phản ứng: 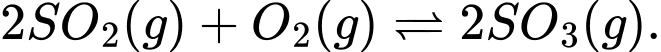
Nếu thêm chất xúc tác thì cân bằng sẽ chuyển dịch như thế nào?
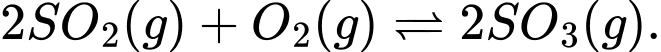
Nếu thêm chất xúc tác thì cân bằng sẽ chuyển dịch như thế nào?
A, Theo chiều thuận.
B, Theo chiều nghịch.
C, Không chuyển dịch.
D, Chưa xác định.
Đáp án C
Chất xúc tác không làm chuyển dịch cân bằng hóa học nên cân bằng không chuyển dịch. Đáp án: C
Chất xúc tác không làm chuyển dịch cân bằng hóa học nên cân bằng không chuyển dịch. Đáp án: C
Câu 17 [186229]: Cho các cân bằng sau:
(1)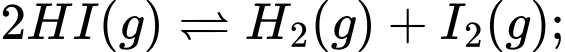
(2)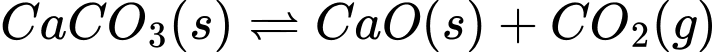 ;
;
(3)
(4)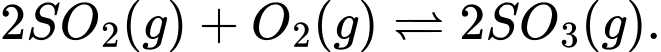
Khi tăng áp suất của hệ, có bao nhiêu cân bằng bị chuyển dịch theo chiều nghịch?
(1)
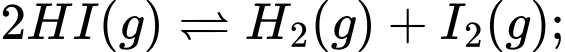
(2)
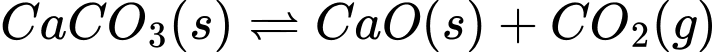 ;
;(3)

(4)
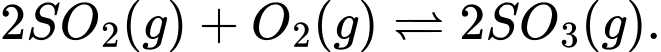
Khi tăng áp suất của hệ, có bao nhiêu cân bằng bị chuyển dịch theo chiều nghịch?
A, 4.
B, 3.
C, 1.
D, 2.
Đáp án C
Khi tăng áp suất của hệ, cân bằng bị chuyển dịch theo chiều nghịch nghĩa là số mol khí vế phải < số mol khí vế trái => CBCD theo chiều nghịch là (2). Đáp án: C
Khi tăng áp suất của hệ, cân bằng bị chuyển dịch theo chiều nghịch nghĩa là số mol khí vế phải < số mol khí vế trái => CBCD theo chiều nghịch là (2). Đáp án: C
Câu 18 [186230]: Phản ứng  ;
; 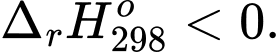
Xét các tác động sau đến cân bằng:
(1) tăng áp suất;
(2) tăng nhiệt độ;
(3) tăng nồng độ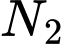 và
và 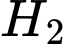 ;
;
(4) tăng nồng độ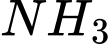 .
.
Trong những tác động trên, các tác động làm làm tăng hiệu suất của phản ứng trên là
 ;
; 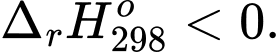
Xét các tác động sau đến cân bằng:
(1) tăng áp suất;
(2) tăng nhiệt độ;
(3) tăng nồng độ
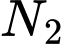 và
và 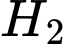 ;
; (4) tăng nồng độ
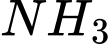 .
.Trong những tác động trên, các tác động làm làm tăng hiệu suất của phản ứng trên là
A, (2), (4).
B, (1), (3).
C, (2).
D, (3), (4).
Đáp án B
Tăng hiệu suất phản ứng = CBCD theo chiều thuận ta có.
Tăng áp suất: 3H2(g) + N2(g)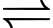 2NH3(g);
2NH3(g);
4 mol khí 2 mol khí => CBCD theo chiều thuận.
Phản ứng tỏa nhiệt nên cần giảm nhiệt độ.
Tăng nồng độ N2 và H2 => CBCD theo chiều thuận.
Tăng nồng độ NH3 => CBCD theo chiều nghịch. Đáp án: B
Tăng hiệu suất phản ứng = CBCD theo chiều thuận ta có.
Tăng áp suất: 3H2(g) + N2(g)
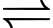 2NH3(g);
2NH3(g); 4 mol khí 2 mol khí => CBCD theo chiều thuận.
Phản ứng tỏa nhiệt nên cần giảm nhiệt độ.
Tăng nồng độ N2 và H2 => CBCD theo chiều thuận.
Tăng nồng độ NH3 => CBCD theo chiều nghịch. Đáp án: B
Câu 19 [186236]: Xét phản ứng thuận nghịch sau tại thời điểm cân bằng:
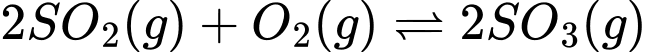 ;
; 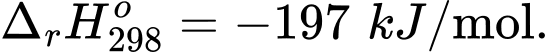
Sự thay đổi nào về áp suất và nhiệt độ sẽ làm chuyển dịch vị trí cân bằng về phía sản phẩm.
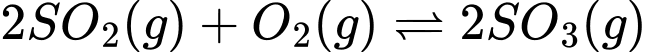 ;
; 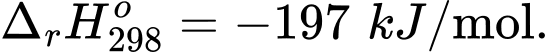
Sự thay đổi nào về áp suất và nhiệt độ sẽ làm chuyển dịch vị trí cân bằng về phía sản phẩm.
A, Giảm áp suất và giảm nhiệt độ.
B, Giảm áp suất và tăng nhiệt độ.
C, Tăng áp suất và giảm nhiệt độ.
D, Tăng áp suất và tăng nhiệt độ.
Đáp án C.
CBCD theo chiều thuận cần giảm nhiệt độ do đây là phản ứng tỏa nhiệt => loại đáp án B, D.
2SO2(g) + O2(g)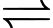 2SO3(g);
2SO3(g);
3 mol khí 2 mol khí
Tăng áp suất làm CBCD theo chiều thuận Đáp án: C
CBCD theo chiều thuận cần giảm nhiệt độ do đây là phản ứng tỏa nhiệt => loại đáp án B, D.
2SO2(g) + O2(g)
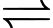 2SO3(g);
2SO3(g); 3 mol khí 2 mol khí
Tăng áp suất làm CBCD theo chiều thuận Đáp án: C
Câu 20 [186239]: Cho các cân bằng sau:
(1)
(2)
(3)
(4)
Ở cùng một nhiệt độ xác định, nếu giá trị của cân bằng (1) bằng 64 thì giá trị
của cân bằng (1) bằng 64 thì giá trị  bằng 0,125 là của cân bằng nào trên?
bằng 0,125 là của cân bằng nào trên?
(1)
(2)
(3)
(4)
Ở cùng một nhiệt độ xác định, nếu giá trị
A, (4).
B, (2).
C, (3).
D, cả (2) và (3).
Đáp án C
 Đáp án: C
Đáp án: C
Câu 21 [186240]: Cho hai hệ cân bằng sau trong bình kín:
(a) ;
; 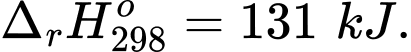
(b) ;
; 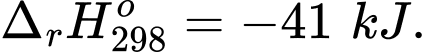
Xét các tác động sau đến cân bằng:
(1) tăng nhiệt độ;
(2) thêm lượng hơi nước vào;
(3) thêm khí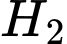 vào;
vào;
(4) tăng áp suất;
(5) thêm lượng CO vào.
(6) Dùng chất xúc tác
Trong các tác động trên, số tác động làm hai cân bằng (a) và (b) chuyển dịch theo chiều ngược nhau là
(a)
 ;
; 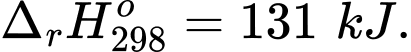
(b)
 ;
; 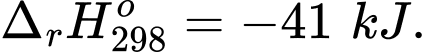
Xét các tác động sau đến cân bằng:
(1) tăng nhiệt độ;
(2) thêm lượng hơi nước vào;
(3) thêm khí
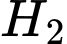 vào;
vào; (4) tăng áp suất;
(5) thêm lượng CO vào.
(6) Dùng chất xúc tác
Trong các tác động trên, số tác động làm hai cân bằng (a) và (b) chuyển dịch theo chiều ngược nhau là
A, 3.
B, 4.
C, 1.
D, 2.
Đáp án D
Khi tăng nhiệt độ, (1) chuyển dịch theo chiều thuận, (2) chuyển dịch theo chiều nghịch.
Khi thêm hơi nước vào, (1) và (2) đều chuyển dịch theo chiều thuận.
Khi thêm H2 vào, (1) và (2) đều chuyển dịch theo chiều nghịch.
Khi tăng áp suất, (1) chuyển dịch theo chiều nghịch, (2) không chuyển dịch.
Khi thêm CO vào thì (1) chuyển dịch theo chiều nghịch, (2) chuyển dịch theo chiều thuận.
(1), (5) làm các cân bằng trên dịch chuyển ngược chiều nhau Chọn D Đáp án: D
Khi tăng nhiệt độ, (1) chuyển dịch theo chiều thuận, (2) chuyển dịch theo chiều nghịch.
Khi thêm hơi nước vào, (1) và (2) đều chuyển dịch theo chiều thuận.
Khi thêm H2 vào, (1) và (2) đều chuyển dịch theo chiều nghịch.
Khi tăng áp suất, (1) chuyển dịch theo chiều nghịch, (2) không chuyển dịch.
Khi thêm CO vào thì (1) chuyển dịch theo chiều nghịch, (2) chuyển dịch theo chiều thuận.
(1), (5) làm các cân bằng trên dịch chuyển ngược chiều nhau Chọn D Đáp án: D
Câu 22 [186242]: Xét phản ứng thuận nghịch:
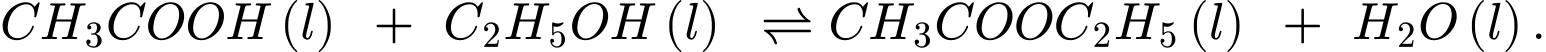
Biện pháp nào sau đây không làm tăng hiệu suất quá trình điều chế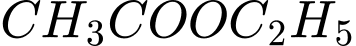 ?
?
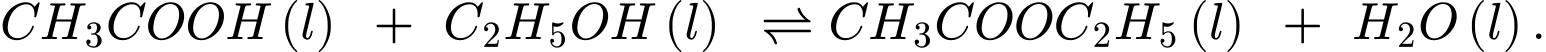
Biện pháp nào sau đây không làm tăng hiệu suất quá trình điều chế
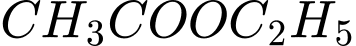 ?
? A, Loại bỏ bớt H2O(l) ra khỏi hỗn hợp.
B, Thêm một lượng C2H5OH(l) vào hỗn hợp.
C, Sử dụng chất xúc tác H2SO4 đặc.
D, Thêm một lượng CH3COOC2H5(l) vào hỗn hợp.
Tăng hiệu suất đồng nghĩa với CBCD theo chiều thuận.
❌A. Loại bỏ bớt H2O(l) ra khỏi hỗn hợp => làm giảm nồng độ H2O => CBCD theo chiều thuận.
❌B. Thêm một lượng C2H5OH(l) vào hỗn hợp => làm tăng nồng độ H2O => CBCD theo chiều thuận.
❌C. Sử dụng chất xúc tác H2SO4 đặc.H2SO4 đặc có tính háo nước nên sẽ hấp thụ nước làm cân bằng chuyển dịch theo chiều thuận làm tăng hiệu suất nhé
✔️D. Thêm một lượng CH3COOC2H5(l) vào hỗn hợp => làm tăng nồng độ CH3COOC2H5(l) => CBCD theo chiều nghịch.
⟹ Chọn đáp án D Đáp án: D
❌A. Loại bỏ bớt H2O(l) ra khỏi hỗn hợp => làm giảm nồng độ H2O => CBCD theo chiều thuận.
❌B. Thêm một lượng C2H5OH(l) vào hỗn hợp => làm tăng nồng độ H2O => CBCD theo chiều thuận.
❌C. Sử dụng chất xúc tác H2SO4 đặc.H2SO4 đặc có tính háo nước nên sẽ hấp thụ nước làm cân bằng chuyển dịch theo chiều thuận làm tăng hiệu suất nhé
✔️D. Thêm một lượng CH3COOC2H5(l) vào hỗn hợp => làm tăng nồng độ CH3COOC2H5(l) => CBCD theo chiều nghịch.
⟹ Chọn đáp án D Đáp án: D
Câu 23 [584844]: Xét phản ứng A 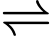 B. Sơ đồ đầu tiên (hình bên) biểu diễn một hệ đang ở trạng thái cân bằng trong đó
B. Sơ đồ đầu tiên (hình bên) biểu diễn một hệ đang ở trạng thái cân bằng trong đó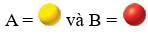

Trong các sơ đồ sau từ (1) đến (4)
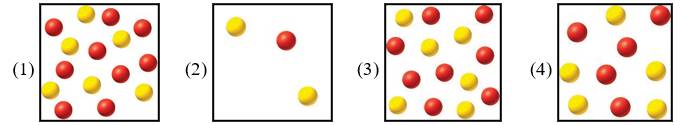
Sơ đồ cũng biểu diễn hệ ở trạng thái cân bằng là
 B. Sơ đồ đầu tiên (hình bên) biểu diễn một hệ đang ở trạng thái cân bằng trong đó
B. Sơ đồ đầu tiên (hình bên) biểu diễn một hệ đang ở trạng thái cân bằng trong đó

Trong các sơ đồ sau từ (1) đến (4)

Sơ đồ cũng biểu diễn hệ ở trạng thái cân bằng là
HƯỚNG DẪN GIẢI:
- Công thức tính KC của hệ ở trạng thái cân bằng là KC = [B]/[A].
⟹ KC = 4/4 = 1
- Ta thấy trong các hình chỉ có hình (2) là có tỉ lệ 1/1.
⟹ Điền đáp án: 4
- Công thức tính KC của hệ ở trạng thái cân bằng là KC = [B]/[A].
⟹ KC = 4/4 = 1
- Ta thấy trong các hình chỉ có hình (2) là có tỉ lệ 1/1.
⟹ Điền đáp án: 4
Câu 24 [584846]: Một số phân tử H2O và CO được đặt trong một bình chứa có dung tích 1,0 L được minh họa bên hình dưới đây:
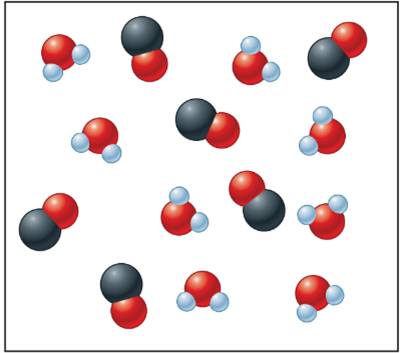
Khi hệ đạt trạng thái cân bằng, tổng số phân tử có trong hệ bằng bao nhiêu?

Khi hệ đạt trạng thái cân bằng, tổng số phân tử có trong hệ bằng bao nhiêu?
Cân bằng xảy ra: H2O(g) + CO(g) ⇌ CO2(g) + H2(g)
Trong một cân bằng, tổng số phân tử khí trước phản ứng và sau phản ứng bằng nhau nên tổng số phân tử khí trong hệ không đổi → Khi hệ đạt trạng thái cân bằng, tổng số phân tử có trong hệ bằng 14.
⇒ Điền đáp án: 14
Trong một cân bằng, tổng số phân tử khí trước phản ứng và sau phản ứng bằng nhau nên tổng số phân tử khí trong hệ không đổi → Khi hệ đạt trạng thái cân bằng, tổng số phân tử có trong hệ bằng 14.
⇒ Điền đáp án: 14
Câu 25 [584859]: Xét phản ứng: 
Một hỗn hợp phản ứng chứa trong bình dung tích 3,67 lít ở một nhiệt độ thấp nhất định, ban đầu chứa 0,763 gam H2 và 96,6 gam I2. Ở trạng thái cân bằng, bình chứa 90,4 gam HI. Tính hằng số cân bằng KC. cho phản ứng ở nhiệt độ này (làm tròn kết quả đến hàng đơn vị).

Một hỗn hợp phản ứng chứa trong bình dung tích 3,67 lít ở một nhiệt độ thấp nhất định, ban đầu chứa 0,763 gam H2 và 96,6 gam I2. Ở trạng thái cân bằng, bình chứa 90,4 gam HI. Tính hằng số cân bằng KC. cho phản ứng ở nhiệt độ này (làm tròn kết quả đến hàng đơn vị).
Chú ý: Tuyệt đối không làm tròn các bước trung gian để tránh sai lệch kết quả cuối cùng (lời giải trên có làm tròn để bạn đọc có thể hình dung cách làm)
⟹Điền đáp án: 647
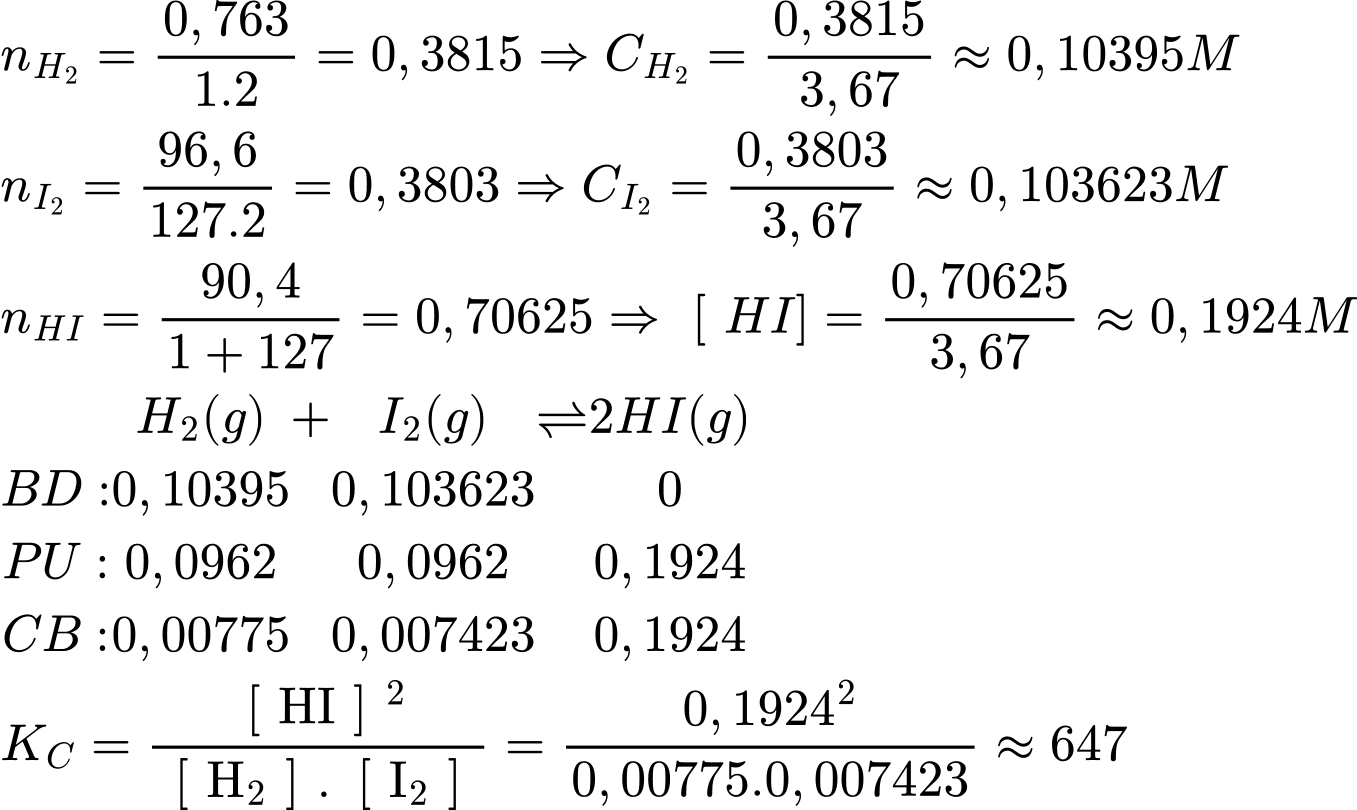
⟹Điền đáp án: 647
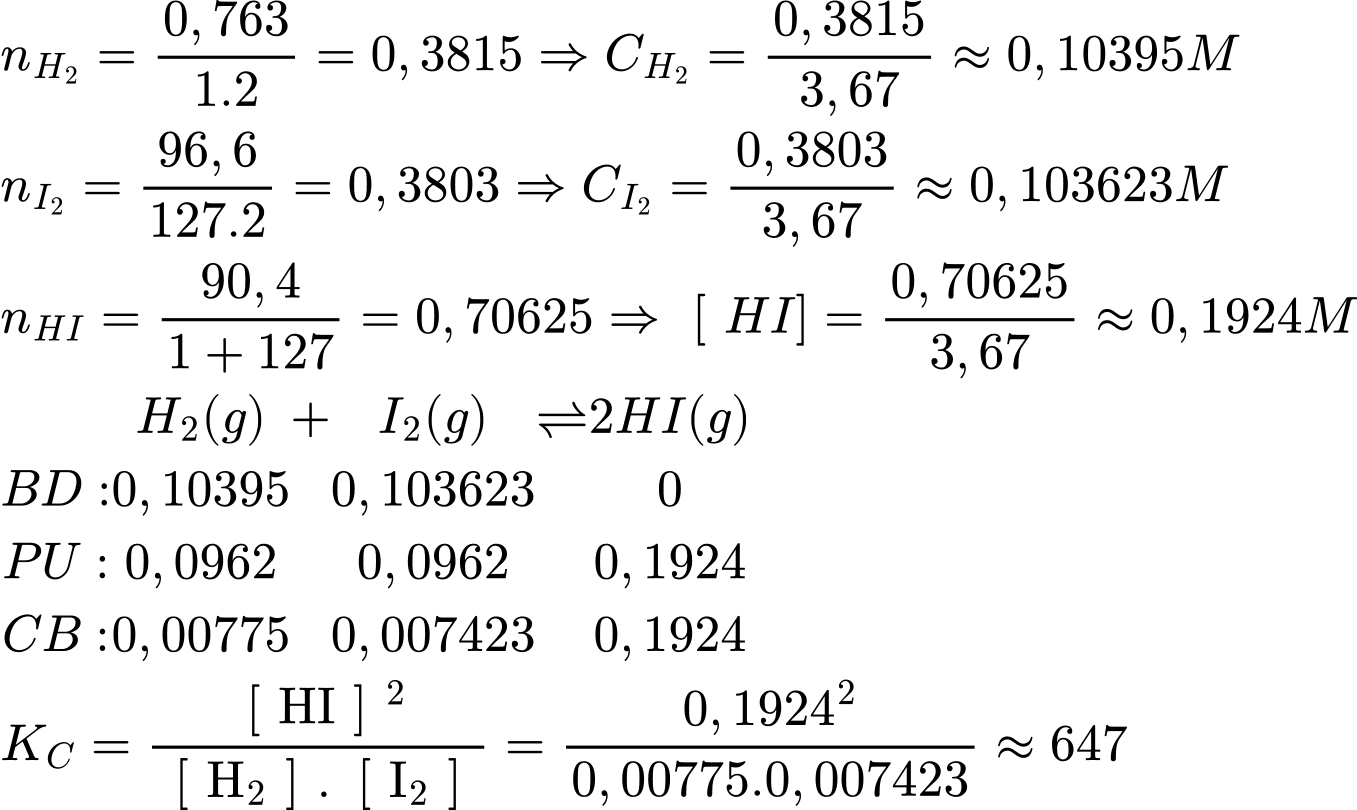
Câu 26 [584892]: Trong bình kín có hệ cân bằng hóa học sau:
CO2(g) + H2(g)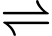 CO(g) + H2O(g) ;
CO(g) + H2O(g) ; 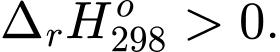
Thay đổi các yếu tố sau của hệ cân bằng:
(a) tăng nhiệt độ;
(b) thêm một lượng hơi nước;
(c) giảm áp suất chung của hệ;
(d) dùng chất xúc tác;
(e) thêm một lượng CO2.
Trong những tác động trên, có bao nhiêu sự thay đổi làm cân bằng chuyển dịch theo chiều thuận?
CO2(g) + H2(g)
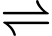 CO(g) + H2O(g) ;
CO(g) + H2O(g) ; 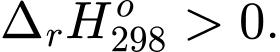
Thay đổi các yếu tố sau của hệ cân bằng:
(a) tăng nhiệt độ;
(b) thêm một lượng hơi nước;
(c) giảm áp suất chung của hệ;
(d) dùng chất xúc tác;
(e) thêm một lượng CO2.
Trong những tác động trên, có bao nhiêu sự thay đổi làm cân bằng chuyển dịch theo chiều thuận?
Phản ứng trên có biến thiên enthalpy lớn hơn 0 nên chiều thuận thu nhiệt, chiều nghịch toả nhiệt.
(a) Khi tăng nhiệt độ thì cân bằng chuyển dịch theo chiều làm giảm nhiệt độ (thu nhiệt) ⇒ chiều thuận.
(b) Khi thêm một lượng hơi nước thì cân bằng chuyển dịch theo chiều làm giảm nồng độ H2O ⇒ chiều nghịch.
(c) Khi giảm áp suất chung của hệ thì cân bằng chuyển dịch theo chiều tăng số mol khí ⇒ cân bằng không bị chuyển dịch.
(d) Khi thêm chất xúc tác ⇒ cân bằng không chuyển dịch vì chất xúc tác không ảnh hưởng đến cân bằng.
(e) Khi thêm một lượng CO2 thì cân bằng chuyển dịch theo chiều làm giảm CO2 ⇒ chiều thuận.
Những tác động làm cân bằng chuyển dịch theo chiều thuận là: (a) và (e)
⇒ Điền đáp án: 2
(a) Khi tăng nhiệt độ thì cân bằng chuyển dịch theo chiều làm giảm nhiệt độ (thu nhiệt) ⇒ chiều thuận.
(b) Khi thêm một lượng hơi nước thì cân bằng chuyển dịch theo chiều làm giảm nồng độ H2O ⇒ chiều nghịch.
(c) Khi giảm áp suất chung của hệ thì cân bằng chuyển dịch theo chiều tăng số mol khí ⇒ cân bằng không bị chuyển dịch.
(d) Khi thêm chất xúc tác ⇒ cân bằng không chuyển dịch vì chất xúc tác không ảnh hưởng đến cân bằng.
(e) Khi thêm một lượng CO2 thì cân bằng chuyển dịch theo chiều làm giảm CO2 ⇒ chiều thuận.
Những tác động làm cân bằng chuyển dịch theo chiều thuận là: (a) và (e)
⇒ Điền đáp án: 2
Câu 27 [584893]: Xét phản ứng tổng hợp ammonia
N2(g) + 3H2(g)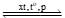 2NH3(g);
2NH3(g);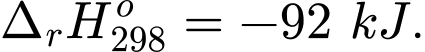
Trong các biện pháp sau có bao nhiêu biện pháp làm tăng hiệu suất phản ứng tổng hợp NH3?
(a) Lấy bớt NH3 ra khỏi hệ sản phẩm.
(b) Giảm nhiệt độ của phản ứng.
(c) Tăng áp suất.
(d) Tăng nhiệt độ của phản ứng.
(e) Thêm chất xúc tác Fe.
(g) Thêm H2 vào hệ phản ứng.
N2(g) + 3H2(g)
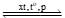 2NH3(g);
2NH3(g);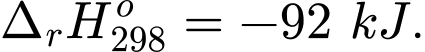
Trong các biện pháp sau có bao nhiêu biện pháp làm tăng hiệu suất phản ứng tổng hợp NH3?
(a) Lấy bớt NH3 ra khỏi hệ sản phẩm.
(b) Giảm nhiệt độ của phản ứng.
(c) Tăng áp suất.
(d) Tăng nhiệt độ của phản ứng.
(e) Thêm chất xúc tác Fe.
(g) Thêm H2 vào hệ phản ứng.
Để tăng hiệu suất tổng hợp NH3 thì cân bằng phải chuyển dịch theo chiều thuận.
→ Các biện pháp làm cân bằng chuyển dịch theo chiều thuận là:
(a) Lấy bớt NH3 ra khỏi hệ sản phẩm.
(b) Giảm nhiệt độ của phản ứng.
(c) Tăng áp suất.
(g) Thêm H2 vào hệ phản ứng.
⇒ Điền đáp án: 4
→ Các biện pháp làm cân bằng chuyển dịch theo chiều thuận là:
(a) Lấy bớt NH3 ra khỏi hệ sản phẩm.
(b) Giảm nhiệt độ của phản ứng.
(c) Tăng áp suất.
(g) Thêm H2 vào hệ phản ứng.
⇒ Điền đáp án: 4
Đọc đoạn thông tin sau và trả lời các câu hỏi từ 28 đến 30
CÂN BẰNG HOÁ HỌC
Sự phân hủy dinitrogen tetroxide (N2O4) để tạo ra nitrogen dioxide (NO2) là một ví dụ hóa học điển hình về trạng thái cân bằng. Phản ứng này là một phản ứng thuận nghịch:N2O4(g) ⇌ 2NO2(g) (*)
N2O4 là chất khí không màu, còn NO2 là chất khí có màu nâu. Nếu chúng ta bắt đầu bằng cách cho một mẫu N2O4 tinh khiết vào bình chân không và tiến hành ngâm bình chân không này vào trong một cốc nước nóng thì phần khí chứa trong bình sẽ chuyển từ không màu sang màu nâu (Hình vẽ dưới). Lúc đầu, màu nâu đậm hơn khi nồng độ NO2 tăng. Tuy nhiên, cuối cùng cường độ của màu nâu ngừng tăng, cho thấy nồng độ NO2 đã ngừng thay đổi. Tại thời điểm này, cả quá trình thuận và nghịch đều diễn ra với tốc độ bằng nhau và hệ đã đạt đến trạng thái cân bằng.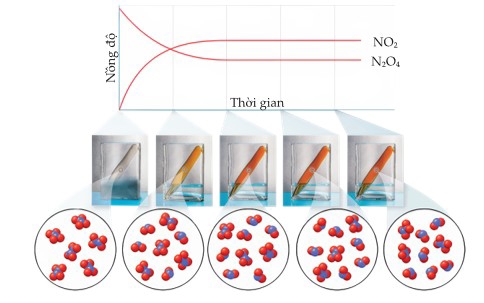
Hình vẽ. Đồ thị biểu diễn sự thay đổi nồng độ của N2O4 và NO2 theo thời gian.
Câu 28 [382559]: Khi ngâm bình chân không chứa khí N2O4 nguyên chất vào trong cốc nước nóng thì màu sắc của bình chân không sẽ
A, từ không màu chuyển thành màu nâu.
B, từ màu nâu chuyển thành không màu.
C, không có sự thay đổi màu sắc.
D, không thể xác định.
Khí N2O4 tồn tại ở trạng thái cân bằng với khí NO2.
N2O4 (không màu) ⇌ 2NO2 (màu nâu)
Khi ngâm bình chân không chứa khí N2O4 vào trong cốc nước nóng, nhiệt độ tăng lên. Do đó, cân bằng sẽ dịch chuyển theo chiều thuận, làm tăng lượng khí NO2 trong bình.
Khi ngâm bình chân không chứa khí N2O4 nguyên chất vào trong cốc nước nóng thì màu sắc của bình chân không sẽ từ không màu chuyển thành màu nâu (NO2).
Chọn đáp án A Đáp án: A
N2O4 (không màu) ⇌ 2NO2 (màu nâu)
Khi ngâm bình chân không chứa khí N2O4 vào trong cốc nước nóng, nhiệt độ tăng lên. Do đó, cân bằng sẽ dịch chuyển theo chiều thuận, làm tăng lượng khí NO2 trong bình.
Khi ngâm bình chân không chứa khí N2O4 nguyên chất vào trong cốc nước nóng thì màu sắc của bình chân không sẽ từ không màu chuyển thành màu nâu (NO2).
Chọn đáp án A Đáp án: A
Câu 29 [382560]: Phản ứng phân hủy N2O4 tạo thành NO2 có
A, giá trị ΔH < 0, phản ứng tỏa nhiệt.
B, giá trị ΔH < 0, phản ứng thu nhiệt.
C, giá trị ΔH > 0, phản ứng tỏa nhiệt.
D, giá trị ΔH > 0, phản ứng thu nhiệt.
Khí N2O4 tồn tại ở trạng thái cân bằng với khí NO2:
N2O4 (không màu) ⇌ 2NO2 (màu nâu)
Phản ứng này là phản ứng thu nhiệt (ΔH > 0), nghĩa là khi tăng nhiệt độ, cân bằng sẽ dịch chuyển theo chiều thuận, tức là chiều tạo ra NO2 (khí màu nâu).
Chọn đáp án D Đáp án: D
N2O4 (không màu) ⇌ 2NO2 (màu nâu)
Phản ứng này là phản ứng thu nhiệt (ΔH > 0), nghĩa là khi tăng nhiệt độ, cân bằng sẽ dịch chuyển theo chiều thuận, tức là chiều tạo ra NO2 (khí màu nâu).
Chọn đáp án D Đáp án: D
Câu 30 [249129]: Trong một bình kín có cân bằng hóa học sau:

Tỉ khối hơi của hỗn hợp khí trong bình so với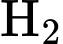 ở nhiệt độ
ở nhiệt độ 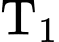 bằng 27,6 và ở nhiệt độ
bằng 27,6 và ở nhiệt độ 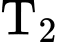 bằng 34,5. Biết
bằng 34,5. Biết 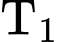 >
> 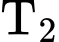 . Phát biểu nào sau đây về cân bằng trên là đúng?
. Phát biểu nào sau đây về cân bằng trên là đúng?

Tỉ khối hơi của hỗn hợp khí trong bình so với
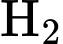 ở nhiệt độ
ở nhiệt độ 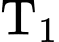 bằng 27,6 và ở nhiệt độ
bằng 27,6 và ở nhiệt độ 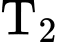 bằng 34,5. Biết
bằng 34,5. Biết 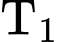 >
> 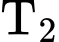 . Phát biểu nào sau đây về cân bằng trên là đúng?
. Phát biểu nào sau đây về cân bằng trên là đúng? A, Phản ứng thuận là phản ứng tỏa nhiệt.
B, Khi tăng nhiệt độ, áp suất chung của hệ cân bằng giảm
C, Khi giảm nhiệt độ, áp suất chung của hệ cân bằng tăng
D, Phản ứng nghịch là phản ứng tỏa nhiệt
HD:
Tỷ khối hơi của hỗn hợp khí tại nhiệt độ T1 < T2 → số mol số hỗn hợp khí ở nhiệt độ T1 > T2.
Mặt khác lại có nhiệt độ T1 > T2 → Tiến hành giảm nhiệt độ cân bằng chuyển dịch theo chiều nghịch
(chiều làm giảm số mol ) → Phản ứng thuận tỏa nhiệt.
Chọn A.
Đáp án: A
Tỷ khối hơi của hỗn hợp khí tại nhiệt độ T1 < T2 → số mol số hỗn hợp khí ở nhiệt độ T1 > T2.
Mặt khác lại có nhiệt độ T1 > T2 → Tiến hành giảm nhiệt độ cân bằng chuyển dịch theo chiều nghịch
(chiều làm giảm số mol ) → Phản ứng thuận tỏa nhiệt.
Chọn A.
Đáp án: A