Đổi 20 mL = 0,02 L; 10 mL = 0,01 L
Số mol của NaOH là nNaOH = 0,02.0,1 = 0,002 mol
Theo PTHH số mol của HCl là: 0,002 mol
Nồng độ của dung dịch HCl là CM = 0,002/0,01 = 0,2 M
Đáp án: A. 0,2 M. Đáp án: A
H2SO4
+ 2NaOH → Na2SO4 + 2H2O
Số mol của H2SO4
là nH2SO4 = 0,01 mol
Theo PTHH số mol của
NaOH là nNaOH = 0,02 mol
Thể tích của dung dịch
NaOH là VNaOH = 0,02 L = 20 mL
Đáp án: B. 20
mL.
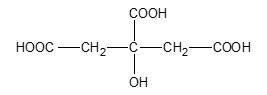
Lấy một vài quả chanh, ép lấy nước rồi định mức thành 100 mL dung dịch Z. Lấy 20 mL dung dịch Z rồi trung hòa bằng dung dịch NaOH 0,1 M thì thấy tiêu tốn hết 30 mL. Giả sử trong nước chanh chỉ có nhóm COOH trong acid xitric phản ứng với NaOH. Lượng citric acid trong nước chanh ban đầu là bao nhiêu?
Số mol của NaOH là nNaOH = 0,03.0,1 = 0,003 mol
Theo PTHH số mol của citric acid là: 0,001 mol
Khối lượng của citric acid trong chanh là:
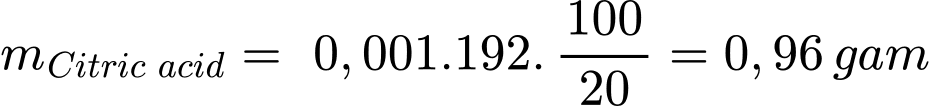
Đáp án: D. 0,96 gam. Đáp án: D
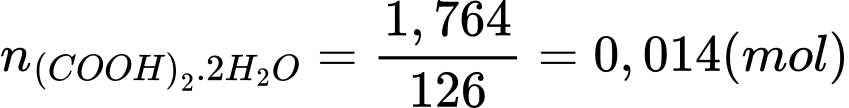 (trong 100 ml) => trong 50ml có chứa 0,007 mol
(trong 100 ml) => trong 50ml có chứa 0,007 mol 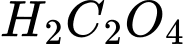
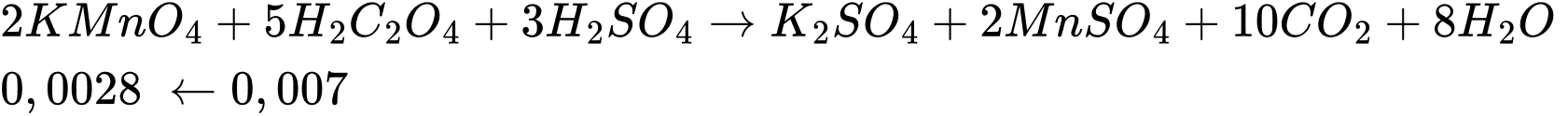 (mol)
(mol) 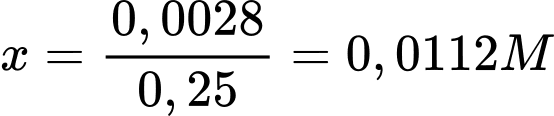
=> Đáp án C. Đáp án: C
C2H5OH + K2Cr2O7 + H2SO4
 CH3CHO + Cr2(SO4)3 + K2SO4 + H2O
CH3CHO + Cr2(SO4)3 + K2SO4 + H2OKhi chuẩn độ 25 gam huyết tương máu của một lái xe cần dùng 20 ml dung dịch K2Cr2O7 0,01M.
Hàm lượng ethanol trong máu (% theo khối lượng) của lái xe trên là bao nhiêu?
Giả sử các thành phần khác không ảnh hưởng đến phản ứng.
Số mol của K2Cr2O7 phản ứng là: nK2Cr2O7 = 0,02 × 0,01 = 0,0002 mol
3C2H5OH + K2Cr2O7 + 4H2SO4 → 3CH3CHO + K2SO4 + Cr2(SO4)3 + 7H2O
Từ phương trình số mol của C2H5OH là: nC2H5OH = 0,0006 mol
Hàm lượng ethanol trong máu là:
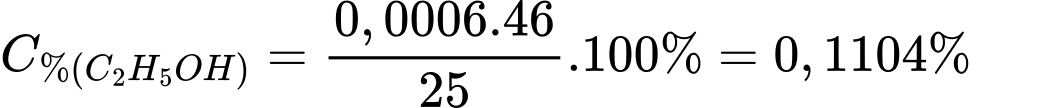
⇒ Chọn đáp án A Đáp án: A
Số mol của KMnO4 là nKMnO4 = 0,01.0,1 = 0,001 mol
Theo PTHH số mol của H2O2 là 0,0025 mol
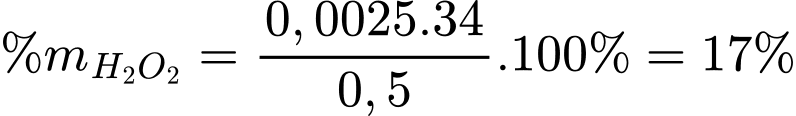
Đáp án: B. 17%. Đáp án: B
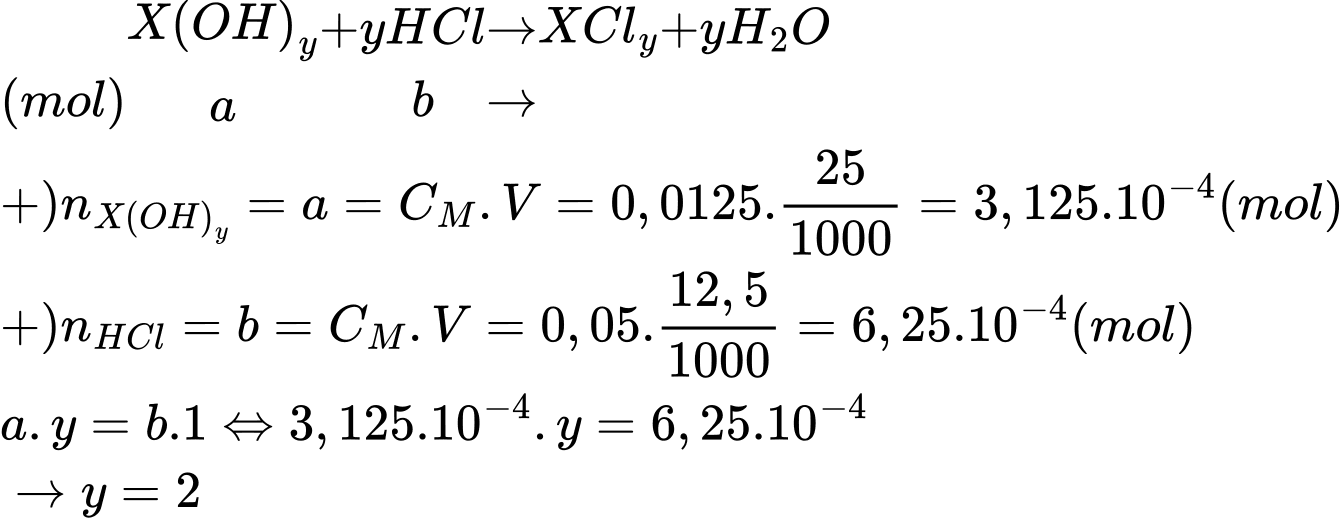
⇒ Chọn đáp án B Đáp án: B
Số mol của Sodium dichromate là nNa2Cr2O7 = 0,04296 × 0,0213 = 0,000915048 (mol)
6Fe2+ + 14H+ + Cr2O72- ⟶ 6Fe3+ + 2Cr3+ + 7H2O
Từ phương trình hóa học số mol của Fe2+ là: nFe2+ = 6nCr2O72- = 6 × 0,000915048 = 0,005490288 (mol)
Hàm lượng Fe trong quặng sắt limonite là:
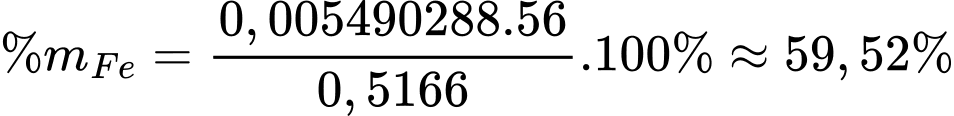
⇒ Chọn đáp án D Đáp án: D
Số mol FeSO4 dư là nFeSO4 dư = 0,0075.0,015 = 1,125.10−4 mol
25 ml FeSO4 tương đương với 35 mL dung dịch chuẩn K2Cr2O7
Số mol K2Cr2O7 là:
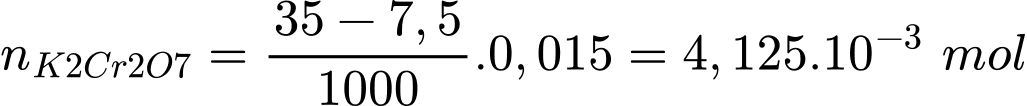
Số mol Cr trong quặng là:
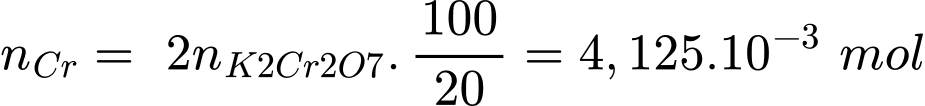
Hàm lượng của Cr trong quặng là:
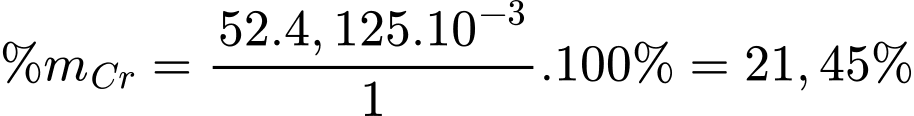
Đáp án: B. 21,450%. Đáp án: B
Thí nghiệm 1: thêm dung dịch NaOH từ từ tới dư vào 50,00 mL dung dịch X thấy xuất hiện kết tủa, lọc kết tủa, làm khô cẩn thận thu được 4,84 g kết tủa.
Thí nghiệm 2: thêm từ từ dung dịch KMnO4 0,50 M trong môi trường H2SO4 vào 50,00 mL dung dịch X, sau phản ứng thấy dùng hết 12,00 mL dung dịch KMnO4.
Nồng độ ban đầu của dung dịch FeSO4 là

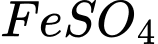 và
và  (màu vàng nâu là màu của muối sắt III). Muối sắt II kém bền nên dễ bị oxi hóa lên muối sắt III.
(màu vàng nâu là màu của muối sắt III). Muối sắt II kém bền nên dễ bị oxi hóa lên muối sắt III. Kết tủa thu được bao gồm
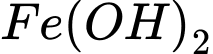 và
và 
TN2:
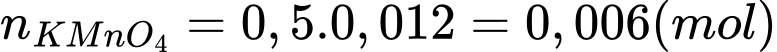
Trong môi trường axit,
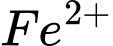 phản ứng với dung dịch
phản ứng với dung dịch 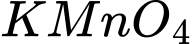 tạo thành
tạo thành 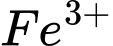 theo phương trình
theo phương trình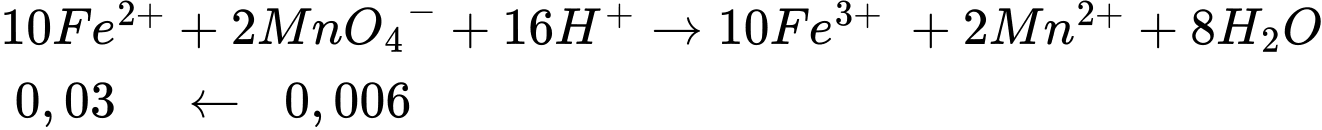
Nhưng cần lưu ý đây là số mol
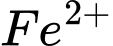 còn lại trong dung dịch chứ không phải
còn lại trong dung dịch chứ không phải 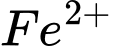 ban đầu, vì 1 lượng
ban đầu, vì 1 lượng 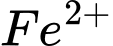 đã chuyển thành
đã chuyển thành 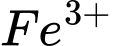
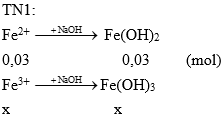
Ta có: 0,03.90 + 107x = 4,84 => x = 0,02 mol.
Vậy số mol
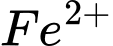 ban đầu = 0,02 + 0,02 = 0,05 (mol)
ban đầu = 0,02 + 0,02 = 0,05 (mol)Nồng độ của dung dịch muối sắt (II) sunfat là:
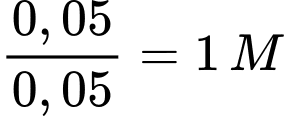 Đáp án: B
Đáp án: B Tiến hành lấy 10 mL dung dịch muối sắt(II) sulfate chưa rõ nồng độ vào bình erlenmeyer, thêm tiếp khoảng 50 mL dung dịch acid H2SO4 loãng. Sử dụng dung dịch KMnO4 0,1 M để chuẩn độ, tiến hành đo thể tích dung dịch KMnO4 thì thấy thể tích dung dịch KMnO4 0,1 M đã sử dụng là 19 mL. Nồng độ của dung dịch muối sắt(II) sulfate là
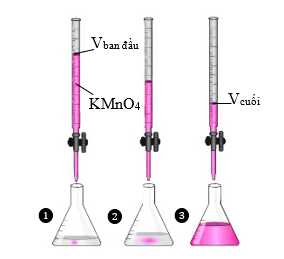
10FeSO4 + 2KMnO4 + 8H2SO4 ⟶ 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Số mol của dung dịch KMnO4 là:
nKMnO4 = 0,019 × 0,1 = 0,0019 (mol)
Từ phương trình hóa học số mol của FeSO4 là:
nFeSO4 = 5nKMnO4 = 0,0095 (mol)
Nồng độ của FeSO4 là: CM (FeSO4) = 0,0095 ÷ 0,01 = 0,95 (M)
⇒ Chọn đáp án A Đáp án: A
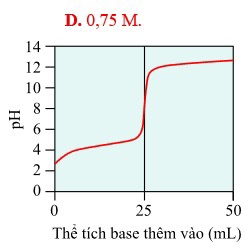
Cho các phát biểu sau:
(a) Độ pH của dung dịch tăng trong quá trình chuẩn độ.
(b) Tại điểm tương đương thì độ pH của dung dịch là 7.
(c) Thể tích dung dịch NaOH đã dùng để đạt điểm tương đương là 50 mL.
(d) Để có thể xác định được nồng độ của acid HX thì cần biết thêm khối lượng của acid HX trong dung dịch trước chuẩn độ.
Số phát biểu đúng là
Nhận định (a) – Đúng. Khi thêm NaOH (base) vào acid HX, acid bị trung
hòa → nồng độ H⁺ giảm → pH tăng dần.
Nhận định (b) – Sai.Quan sát đồ thị tại điểm nhảy vọt (vùng dốc đứng nhất), điểm tương đương nằm ở vị trí trung tâm của đoạn này. Tại đó, giá trị pH dóng sang trục tung đang ở mức khoảng pH = 9. Điều này chứng tỏ 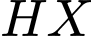 là một acid yếu, khi phản ứng vừa đủ với
là một acid yếu, khi phản ứng vừa đủ với 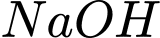 sẽ tạo ra muối base yếu làm pH > 7.
Nhận định (c) – Sai. Thể tích dung dịch NaOH đã dùng để đạt điểm
sẽ tạo ra muối base yếu làm pH > 7.
Nhận định (c) – Sai. Thể tích dung dịch NaOH đã dùng để đạt điểm
tương đương là 25 mL.
Nhận định (d) – Đúng. Để tính nồng độ (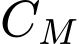 ) của acid
) của acid 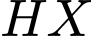 , thì khối lượng acid là một trong những yếu tố cần biết để tính. Đáp án: B
, thì khối lượng acid là một trong những yếu tố cần biết để tính. Đáp án: B
• Bước 1: Rót dung dịch KMnO4 0,002 M vào burette (tối màu), điều chỉnh đến vạch ‘0’.
• Bước 2: Dùng pipette lấy 10 mL dung dịch mẫu chứa H2C2O4 (nồng độ Co M) cho vào bình định mức, sau đó cho tiếp nước cất đến vạch định mức 100 mL (lắc đều). Lấy 10 mL dung dịch từ bình định mức cho vào bình tam giác, cho thêm 5 mL dung dịch HClO4 (dùng dư so với lượng phản ứng), rồi cho thêm nước cất đến khoảng 25 mL.
• Bước 3: Tiến hành chuẩn độ: Cho từ từ dung dịch KMnO4 0,002 M từ burette vào bình tam giác đã chứa hỗn hợp H2C2O4 và HClO4 ở bước 2 và lắc đều cho đến khi dung dịch ngã sang màu hồng (bền trong 30 giây) thì dừng chuẩn độ.
Lặp lại thí nghiệm trên thêm 2 lần, kết quả ghi nhận được thể tích dung dịch KMnO4 0,002 M là

Ngoài ra, có hai bạn học sinh A và B có cách quan sát thể tích dung dịch KMnO4 0,002 M trên burette ở bước 1 khác nhau được thể hiện dưới đây:
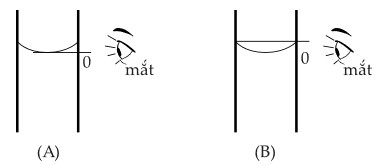
Cho các phát biểu sau:
(a) Cách quan sát của bạn B để xác định vạch ‘0’ đúng.
(b) Nồng độ Co của dung dịch H2C2O4 ban đầu là 5,85 × 10–3 M.
(c) Có thể thay dung dịch HClO4 bằng dung dịch HCl hoặc HBr.
(d) Do phép chuẩn độ KMnO4 có sự thay đổi màu sắc rõ rệt tại điểm tương đương nên không cần sử dụng chất chỉ thị.
Số phát biểu đúng là
Nhận định (b) – Sai.
Thể tích trung bình là:
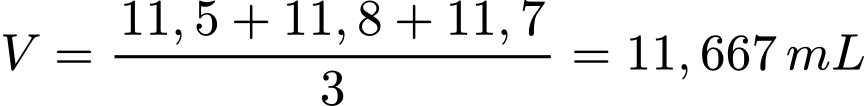
2KMnO4 + 5H2C2O4 + 6H+ → 2Mn2+ + 8H2O + 10CO2 + 2K+
Số mol của KMnO4 là nKMnO4 = 11,667.10-3.0,002 = 2,33.10-5 mol
Nồng độ H2C2O4 là:
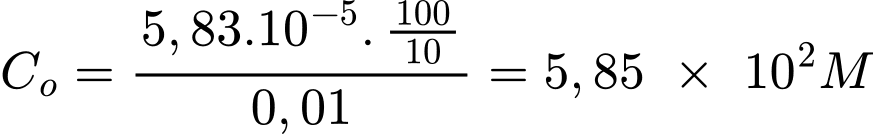
Nhận định (c) – Sai. Không thể thay dung dịch HClO4 bằng dung dịch HCl hoặc HBr, vì HCl và HBr khi phản ứng với dung dịch KMnO4 sẽ tạo khí Cl2 và Br2 gây ảnh hưởng đến quá trình chuẩn độ.
Nhận định (d) – Đúng. Do phép chuẩn độ KMnO4 có sự thay đổi màu sắc rõ rệt tại điểm tương đương nên không cần sử dụng chất chỉ thị, khi đến điểm tương đương dung dịch chuyển sang màu hồng nhạt bền trong 20 giây. Đây là phản ứng tự chỉ thị.
Đáp án: A. 1.
Cho các nhận định sau:
(1) Iodine tan được trong hexane tạo thành lớp dung dịch màu tím là do cả chất tan và dung môi đều không phân cực.
(2) Sulfuric acid chỉ đóng vai trò tạo môi trường, không tham gia vào quá trình phản ứng.
(3) Số mol sodium thiosulfate sử dụng là 5,3×10–6.
(4) Khối lượng iodua (theo µg) có trong 120 g cá là 134,62 µg.
Số nhận định đúng là bao nhiêu?
Nhận định (2) – Sai. Phản ứng chiết xuất iodine từ iodide là:
2I- + H2O2 + 2H+ → I2 + 2H2O
Sulfuric acid cung cấp ion H+ để acid hóa dung dịch, tạo môi trường phản ứng thích hợp cho quá trình oxy hóa iodide I- thành iodine. Do đó, nó không chỉ đóng vai trò tạo môi trường mà còn tham gia vào phản ứng như một chất phản ứng.
Nhận định (3) – Đúng.
Số mol của sodium thiosulfate là:
nNa2S2O3 = 5,3.10-3.0,001 = 5,3.10-6 mol
Nhận định (4) – Đúng.
2I- + H2O2 + 2H+ → I2 + 2H2O
2Na2S2O3 + I2 → Na2S4O6 + 2NaI
Số mol của sodium thiosulfate là:
nNa2S2O3 = 5,3.10-3.0,001 = 5,3.10-6 mol
Theo PTHH số mol của I2 là: 2,65.10-6 mol
Khối lượng của iodide trong 120 gam là:
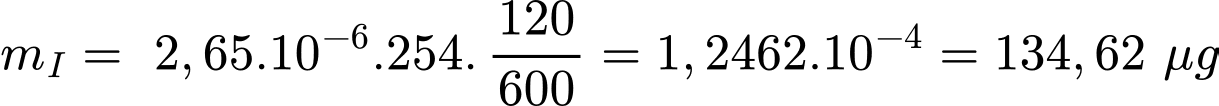
Đáp án: C. 3. Đáp án: C
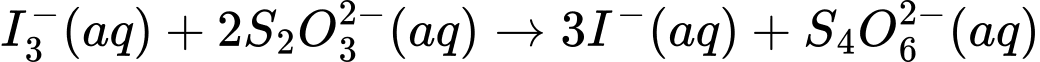
Khi xử lí 75,0 mL mẫu chất tẩy trắng dạng lỏng với lượng dư KI và acid, sau đó đem chuẩn độ với dung dịch sodium thiosulfate 0,0235 M. Quan sát được điểm cuối chuẩn độ là 21,23 mL. Nồng độ hypochlorite trong mẫu chất tẩy rửa là bao nhiêu mmol/L (mM)?
(1) ClO–(aq) + 3I–(aq) + 2H3O+(aq) ⟶ Cl–(aq) + I3–(aq) + 3H2O(l)
(2) I3–(aq) + 2S2O32–(aq) ⟶ 3I–(aq) + S4O62–(aq)
Số mol của sodium thiosulfate là 0,02123.0,0235 = 4,98905.10-4 (mol)
Từ phương trình (1) và (2) số mol của ClO– là 2,494525.10-4 (mol)
Nồng độ của hypochlorite là
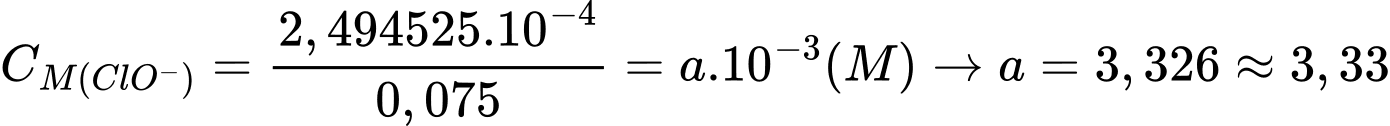
⇒ Điền đáp án: 3,33
pha thành 100,0 mL dung dịch Y. Chuẩn độ 10,00 mL dung dịch Y (trong môi trường sulfuric acid loãng, dư) bằng dung dịch KMnO4 nồng độ 0,012 M đến khi xuất hiện màu hồng nhạt thì dừng. Lặp lại thí nghiệm chuẩn độ thêm 2 lần nữa. Thể tích trung bình của dung dịch KMnO4 sau 3 lần chuẩn độ là 9,72 mL. Phần trăm khối lượng của muối Mohr trong X là a %. Tính giá trị của a (kết quả làm tròn đến hàng đơn vị).
Số mol của KMnO4 là: nKMnO4 = 0,00972 × 0,012 = 1,1664 × 10-4 mol
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Từ PTHH số mol của FeSO4 là: nFeSO4 = 5nKMnO4 = 5,832 × 10-4 mol
Phần trăm khối lượng của muối Mohr trong X là:
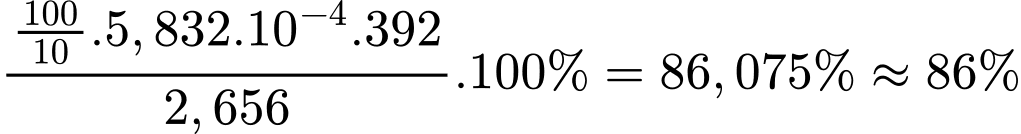
⇒ Điền đáp án: 86
Tiến hành chuẩn độ lượng I3– bằng Na2S2O3 với chất chỉ thị được sử dụng là hồ tinh bột, tại điểm tương đương màu xanh của dung dịch nhạt dần chuyển sang màu trắng đục.
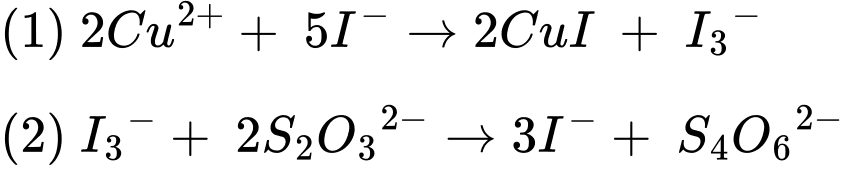
Đổi 15,4 mL = 0,0154 L
Số mol của Na2S2O3 là: nNa2S2O3 = 0,01 × 0,0154 = 1,54 × 10-4 mol
Từ PTHH số mol của Cu2+ là:
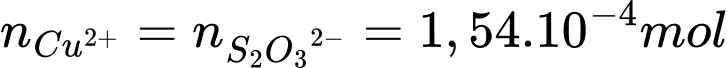
Nồng độ của Cu2+ là:
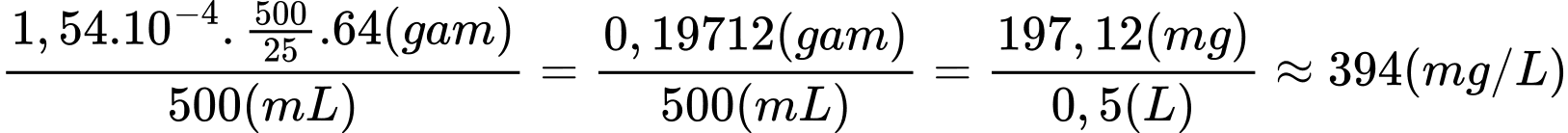
⇒ Điền đáp án: 394
Thí nghiệm 1: Cho lượng dư dung dịch BaCl2 vào 25 mL dung dịch Y, lọc kết tủa, sấy khô rồi đem cân thu được 4,66 gam chất rắn.
Thí nghiệm 2: Thêm dung dịch H2SO4 (loãng, dư) vào 25 mL dung dịch Y, thu được dung dịch Z. Chuẩn độ dung dịch Z bằng dung dịch chuẩn KMnO4 0,1 M đến khi đầu xuất hiện màu hồng (tồn tại khoảng 20 giây) thì hết 13,5 mL.
Phần trăm Fe(II) trong lượng muối ban đầu đã bị oxi hoá trong không khí là a%. Tính giá trị của a (ghi đủ 4 kí tự, ví dụ 00,0).
⭐ Thí nghiệm 1: Cho lượng dư dung dịch BaCl2 vào 25 mL dung dịch Y, thu được 4,66 gam kết tủa → kết tủa là BaSO4.
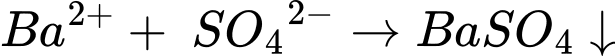
Số mol của kết tủa là:
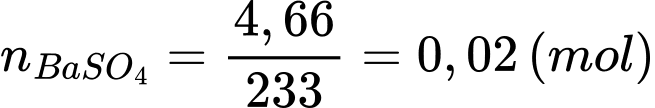
+) Số mol của H2SO4 trong 25 mL dung dịch là:
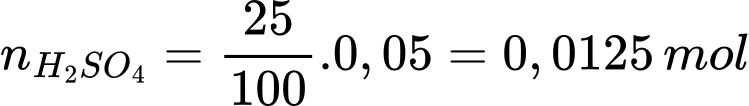
+) Bảo toàn nhóm SO42- trong 100 mL là:
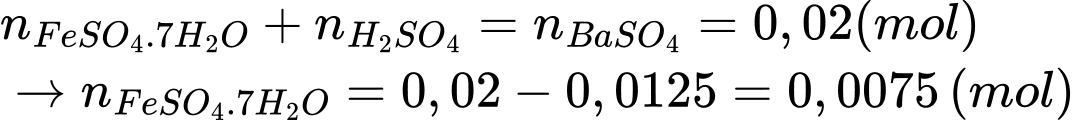
⭐Thí nghiệm 2: phần FeSO4 trong hỗn hợp X sẽ phản ứng với dung dịch KMnO4
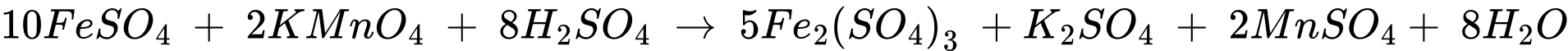
+) Số mol của KMnO4 phản ứng là:
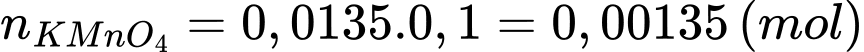
+) Số mol của FeSO4 phản ứng là:
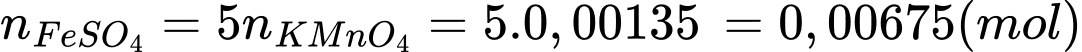
+) Phần trăm Fe(II) trong lượng muối bị oxi hóa trong không khí là
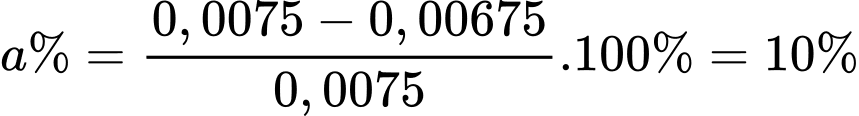
⇒ Điền đáp án: 10,0
Sử dụng đoạn thông tin dưới đây để trả lời câu 19 và câu 20:
Cl2 + 2e → 2Cl–; E° = 1,36 V.
Fe3+ + e → Fe2+; E° = 0,77 V.
MnO4– + 8H+ + 5e → Mn2+ + 4H2O; E° = 1,51 V.
SO42– + 4H+ + 2e → SO2 + 2H2O; E° = 0,17 V.
Để chuẩn hóa dung dịch KMnO4 (xác định nồng độ dung dịch), một học sinh đã cân 5,56 g FeSO4.7H2O, hòa tan nó trong H2SO4 và pha loãng đến tổng thể tích là 250,0 mL bằng nước cất. Lấy 3 phần vào 3 bình tam giác, mỗi phần lấy 25,0 mL dung dịch này và thêm 10 mL H2SO4 2,00 M. Sau đó chuẩn độ các phần này bằng dung dịch KMnO4. Thể tích dung dịch KMnO4 sử dụng trung bình là 21,2 mL.
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
Phân tích các đáp án:
⟹ Chọn đáp án C
Đổi 21,2 mL = 0,0212 L
Số mol của FeSO4.7H2O là nFeSO4.7H2O = 5,56 : 278 = 0,02 mol
Số mol FeSO4 trong 50 mL dung dịch là
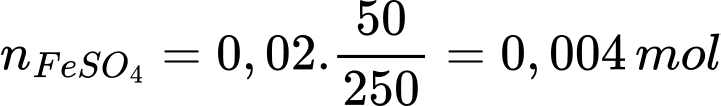
Từ PTHH số mol của KMnO4 là nKMnO4 = 0,0008 mol
Nồng độ của dung dịch KMnO4 là
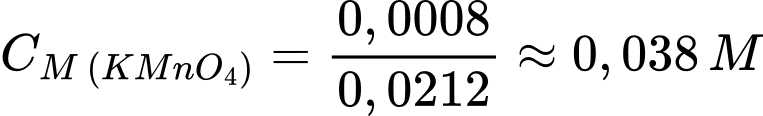
⟹ Chọn đáp án B Đáp án: B