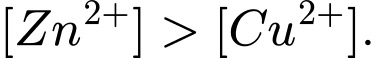
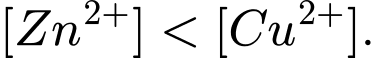
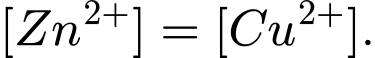
→ nồng độ mol của Zn2+ và Cu2+ trong dung dịch của từng điện cực đều bằng 1 M vì điều kiện chuẩn trong điện hóa học được định nghĩa là nồng độ 1 M cho các ion trong dung dịch.
→ Nồng độ mol của Zn2+ và Cu2+ trong dung dịch của từng điện cực là bằng nhau và đều là 1 M trong điều kiện chuẩn.
⟹ Chọn đáp án C Đáp án: C
⟹ Chọn đáp án D Đáp án: D
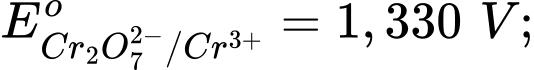
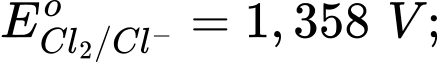
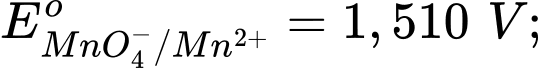
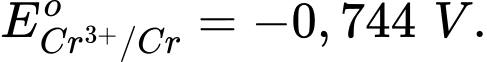 Chọn cách sắp xếp các ion và kim loại theo thứ tự tăng dần tính khử.
Chọn cách sắp xếp các ion và kim loại theo thứ tự tăng dần tính khử. Thứ tự tăng dần thế điện cực chuẩn là :
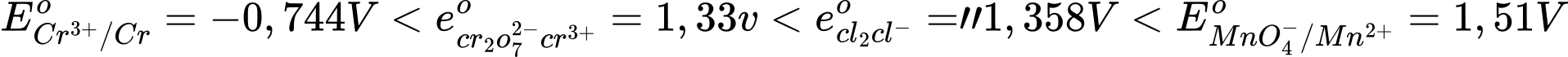 ""
"" ⟹Chọn đáp án B Đáp án: B
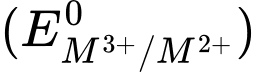 của các kim loại Cr, Mn, Fe và Co lần lượt là –0,408 V; 1,57 V; 0,771 V và 1,97 V. Kim loại nào thay đổi trạng thái oxi hóa từ +2 lên +3 dễ nhất?
của các kim loại Cr, Mn, Fe và Co lần lượt là –0,408 V; 1,57 V; 0,771 V và 1,97 V. Kim loại nào thay đổi trạng thái oxi hóa từ +2 lên +3 dễ nhất? Điều này có nghĩa là Cr2+ dễ dàng nhường electron nhất để trở thành Cr3+.
Vậy, kim loại dễ thay đổi trạng thái oxi hóa từ +2 lên +3 nhất là Cr.
⟹ Chọn đáp án A Đáp án: A
⇒ Có phản ứng Cr + Fe(NO3)2 → Cr(NO3)2 + Fe Đáp án: A
(a) Dung dịch thu được sau phản ứng có màu xanh nhạt.
(b) Khối lượng thanh đồng bị giảm sau phản ứng.
(c) Khối lượng thanh sắt tăng lên sau phản ứng.
Số nhận định không đúng là
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
sau một lúc nhúng tiếp một thanh sắt vào dung dịch này đến phản ứng hoàn toàn.
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu
Phân tích các nhận định:
✔️(a) – Đúng. Dung dịch thu được sau phản ứng có màu xanh nhạt, trong dung dịch có muối Fe(NO3)2 nên có màu xanh nhạt.
❌(b) – Sai. Sau phản ứng có Ag (M = 108 amu) bám vào thanh đồng Cu (M = 64 amu) nên khối lượng của thanh đồng tăng lên.
✔️(c) – Đúng. Khối lượng thanh sắt tăng lên sau phản ứng nguyên do Cu và Ag bám lên lên thanh Fe.
Số nhận định không đúng là: 1
⟹ Chọn đáp án B Đáp án: B
❌A – Sai. Thùng bằng kẽm không thể dùng để chứa dung dịch CuSO4. Do Zn có tính khử mạnh hơn Cu nên sẽ có phản ứng hóa học làm thùng kẽm bị ăn mòn dần.
Zn + CuSO4 → ZnSO4 + Cu
❌B – Sai. Thùng bằng kẽm không thể dùng để chứa dung dịch AgNO3. Do Zn có tính khử mạnh hơn Ag nên sẽ có phản ứng hóa học làm thùng kẽm bị ăn mòn dần.
Zn + 2AgNO3 → Zn(NO3)2 + 2Ag
❌C – Sai. Thùng bằng thiếc (Sn) không thể dùng để chứa dung dịch AgNO3. Do Sn có tính khử mạnh hơn Ag nên sẽ có phản ứng hóa học làm thùng thiếc bị ăn mòn dần.
Sn + 2AgNO3 → Sn(NO3)2 + 2Ag
✔️D – Đúng. Thùng bằng bạc (Ag) có thể dùng để chứa dung dịch CuSO4. Do Ag có tính khử yếu hơn Cu nên không có phản ứng hóa học với dung dịch CuSO4
⟹Chọn đáp án D Đáp án: D
Vì Xn+/X có thế điện cực chuẩn lớn hơn, nên Y có tính khử mạnh hơn X.
⟶ ion Xn+ dễ bị khử hơn ion Ym+
❌ A. Sai. Kim loại X không khử được ion Ym+
❌ B. Sai. Kim loại X có tính khử, không có tính oxi hóa.
❌ C. Sai. Ion Xn+ có tính oxi hóa, không có tính khử.
✔️ D. Đúng. Xn+ là chất oxi hóa, Ym+/Y có thế điện cực chuẩn nhỏ hơn, nên Y bị oxi hóa bởi Xn+.
⟹ Chọn đáp án D Đáp án: D
(a) X sẽ oxi hoá được Ym– nhưng không oxi hoá được Zk–.
(b) X sẽ oxi hoá được cả Ym– và Zk–.
(c) X sẽ oxi hoá được Zk– nhưng không oxi hoá được Ym–.
(d) X sẽ khử được cả Ym– và Zk–.
(e) Phản ứng giữa X và Ym– là phản ứng tự diễn biến.
Số phát biểu không đúng là
⟶Tính khử : Y > X > Z
⟶Tính oxi hóa : Zk– > Xn– > Ym–
Phân tích các phát biểu:
✔️(a) ĐÚNG. Vì X/Xn- > Y/Ym-, X có thể oxi hóa Ym-. Vì Z/Zk- > X/Xn-, X không thể oxi hóa Zk-.
Các phát biểu (b), (c), (d) là các phát biểu không đúng.
⟹ Chọn đáp án C
⟹ Chọn đáp án B
Đáp án: B
Dây dẫn có vai trò quan trọng trong công việc kết nối cực dương và cực âm, tạo thành mạch kín cho phép dòng electron chuyển từ cực âm sang cực dương.
⟹Chọn đáp án B Đáp án: B
- Duy trì tính trung hòa điện
- Đóng mạch điện
- Ngăn chặn sự trộn lẫn các dịch chuyển.
⟹Chọn đáp án B Đáp án: B
❌ B: Hai thanh Al (aluminium) cùng loại nên không tạo thành pin điện hóa.
❌C: Thanh nhựa và thanh thủy tinh không phải kim loại dẫn điện nên không tạo suất điện động.
❌D: Cu và Zn có tính chất điện hóa khác nhau, nhưng nước nguyên chất không phải chất điện ly mạnh nên không tạo ra suất điện động đáng kể. Đáp án: A
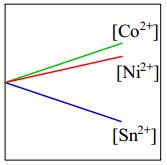
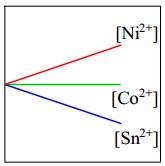
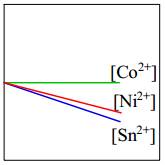
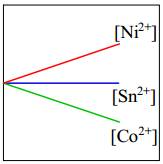
- Độ mạnh tính khử của Ni < Co nên Ni không thể đẩy Co2+ ra khỏi dung dịch muối.
⇒ Do đó [Co2+] giữ nguyên.
⇒ Chọn đáp án B Đáp án: B
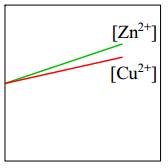
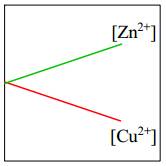
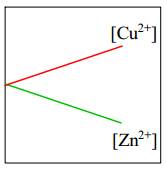

=> Eo Cu2+/Cu > Eo Zn+2/Zn
=> Cu2+/Cu là điện cực dương (cathode) và Zn2+/Zn là điện cực âm (anode).Tại cathode (+): Zn → Zn2+ + 2e ∣ Tại anode (-) : Cu2+ + 2e → Cu
Dựa vào phản ứng tại điện cực: [Zn2+] tăng dần
[Cu2+] giảm dần
⇒ Chọn đáp án B
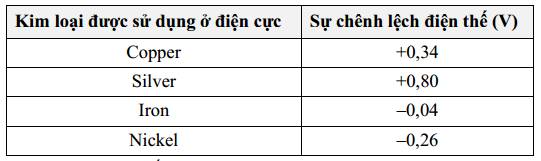
Cặp kim loại nào dưới đây khi lắp thành pin Galvani sẽ cho giá trị sức điện động của pin là lớn nhất?
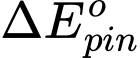 = 0,8 - (-0,26) = 1,06 V
= 0,8 - (-0,26) = 1,06 VB.
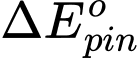 = 0,8 - (-0,04) = 0,84 V
= 0,8 - (-0,04) = 0,84 VC.
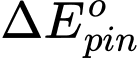 = 0,8 - 0,34 = 0,46 V
= 0,8 - 0,34 = 0,46 VD.
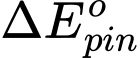 = 0,34 - (-0,26) = 0,6 V
= 0,34 - (-0,26) = 0,6 V⟶ Cặp kim loại nickel và silver khi lắp thành pin Galvani sẽ cho giá trị sức điện động của pin là lớn nhất.
(sức điện động của pin lớn nhất khi thế điện cực chuẩn ở cathode lớn nhất và thế điện cực ở anode nhỏ nhất.) Đáp án: A
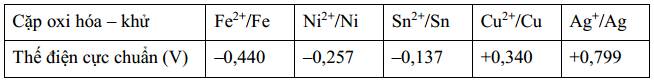
Biết sức điện động chuẩn của pin điện hoá gồm hai điện cực M2+/M và Ag+/Ag bằng 1,056 V. Kim loại nào sau đây phù hợp với M?
➝ Epin = Eo M2+/M - Eo Ag+/Ag
➝ Eo M2+/M = Eo Ag+/Ag + Epin = 0,799 + 1,056 = 1,855 (V)
➝ Không có giá trị Eo thỏa mãn.
TH2: Ag+/Ag đóng vai trò là điện cực dương (cathode)
➝ Epin = Eo Ag+/Ag - Eo M2+/M
➝ Eo M2+/M = Eo Ag+/Ag - Epin = 0,799 - 1,056 = -0,257 (V)
➝ Cặp oxh- khử Ni2+/ Ni thỏa mãn ➝ Chọn C Đáp án: C
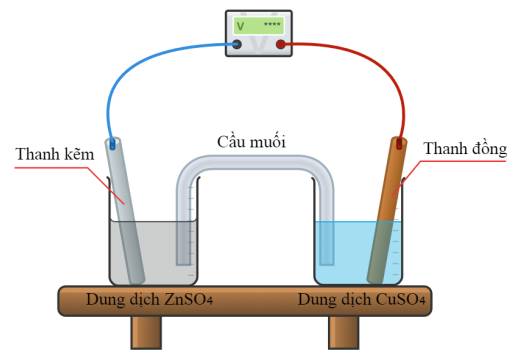
Phát biểu nào sau đây là đúng?
Ta có: Eo Cu2+/Cu = 0,34 (V); Eo Zn2+/Zn = -0,763 (V)
➝ Cu2+/Cu là điện cực dương (cathode); Zn2+/Zn là điện cực âm (anode)
❌ a. Sai. Quá trình xảy ra ở cathode là: Cu2+ +2e ➝ Cu.
❌ b. Sai. Quá trình xảy ra ở anode là: Zn ➝ Zn2+ +2e.
✔️ c. Đúng. Epin = Eo Cu2+/Cu - Eo Zn+/Zn = 0,34 - (- 0,763) = 1,103 (V)
❌ d. Sai. Sau phản ứng thấy xuất hiện kim loại Cu (đồng đỏ) bám lên bề mặt thanh copper ở cathode sau quá trình khử. Kim loại màu xám thường là zinc, nhưng nó không bám trên thanh copper mà có thể bị hòa tan ở anode (thanh zinc).
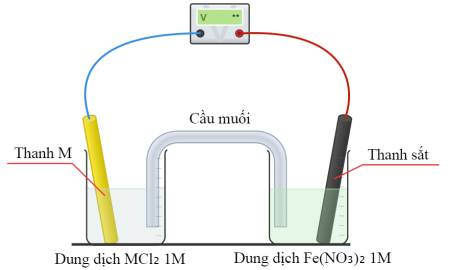
Trong mỗi pin điện, một nửa pin chứa dung dịch Fe(NO3)2(aq) 1,0 M với điện cực Fe. Thành phần của nửa pin còn lại như sau:
• Pin 1: Dung dịch CuCl2(aq) 1,0 M với điện cực Cu.
• Pin 2: Dung dịch NiCl2(aq) 1,0 M với điện cực Ni.
• Pin 3: Dung dịch ZnCl2(aq) 1,0 M với điện cực Zn.
Sắt đóng vai trò là cực dương trong (các) pin điện nào?
⇒ Điện cực anode phải có Eo bé hơn Eo Fe2+/Fe = -0,44
Biết: Eo Cu2+/Cu = +0,34 (V);
Eo Ni2+/Ni = -0,257 (V);
Eo Zn2+/Zn = -0,76 (V)
➝ Nhận thấy Eo Zn2+/Zn < Eo Fe2+/Fe
➝ Pin 3 là đáp án đúng.
⇒ Chọn đáp án C Đáp án: C
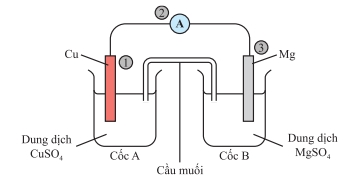
Thứ tự di chuyển của electron nào sau đây là đúng?

Cu có tính khử yếu hơn Mg.
➱ Cu2+ nhận 2 electron để trở thành Cu. Mg cho 2 electron để trở thành Mg2+.
➱ Electron di chuyển từ điện cực Mg về Cu.
➱ Đáp án B. Đáp án: B
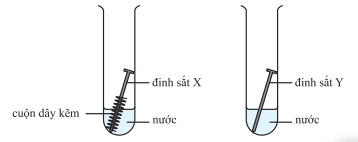
Câu nào sau đây là đúng khi nói về hiện tượng rỉ sét?
 Sai. Sắt trong X được bảo vệ bởi Kẽm nên tốc độ rỉ sét (ăn mòn) sẽ khác biệt rất lớn so với Y.
Sai. Sắt trong X được bảo vệ bởi Kẽm nên tốc độ rỉ sét (ăn mòn) sẽ khác biệt rất lớn so với Y.
Y sẽ rỉ sét nhanh hơn X do X được bảo vệ bằng kẽm.
 Đúng. Kẽm là kim loại hoạt động hóa học mạnh hơn Sắt nên Kẽm sẽ bị ăn mòn (hi sinh) để bảo vệ Sắt. Vì thế, Sắt Y (không được bảo vệ) sẽ rỉ sét nhanh hơn Sắt X (được bảo vệ).
Đúng. Kẽm là kim loại hoạt động hóa học mạnh hơn Sắt nên Kẽm sẽ bị ăn mòn (hi sinh) để bảo vệ Sắt. Vì thế, Sắt Y (không được bảo vệ) sẽ rỉ sét nhanh hơn Sắt X (được bảo vệ).
X sẽ rỉ sét nhanh hơn Y vì kẽm hoạt động hoá học mạnh hơn sắt.
 Sai. Kẽm hoạt động mạnh hơn sắt nên Kẽm sẽ bị ăn mòn, nhưng Sắt trong X thì chậm rỉ sét hơn Sắt trong Y.
Sai. Kẽm hoạt động mạnh hơn sắt nên Kẽm sẽ bị ăn mòn, nhưng Sắt trong X thì chậm rỉ sét hơn Sắt trong Y.
Y sẽ bị gỉ nhanh hơn X nếu thay thế kẽm bọc quanh X bằng đồng.
 Sai. Nếu thay Kẽm bằng Đồng (Cu), do Đồng hoạt động hóa học yếu hơn Sắt (
Sai. Nếu thay Kẽm bằng Đồng (Cu), do Đồng hoạt động hóa học yếu hơn Sắt (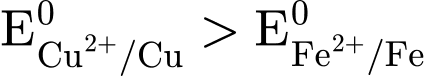 ), Sắt sẽ trở thành Anode và bị ăn mòn nhanh hơn nhiều so với Y.
), Sắt sẽ trở thành Anode và bị ăn mòn nhanh hơn nhiều so với Y.
=> Đáp án đúng là B Đáp án: B
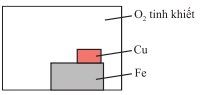
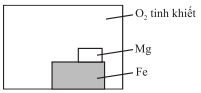
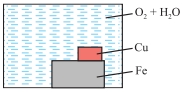
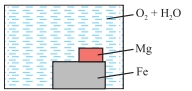
Để sắt bị gỉ cần có
đồng thời O₂ và H₂O → chỉ các sơ đồ có nước và oxygen mới thể hiện đúng điều
kiện này.
Để bảo vệ hy sinh,
kim loại gắn vào phải hoạt động mạnh hơn Fe → Mg dùng được, Cu thì không
(vì Cu kém hoạt động hơn Fe và sẽ làm Fe gỉ nhanh hơn).
Đáp án đúng: D
chuẩn về điện cực đồng ⇝ Điện cực đồng chứa ít electron, thế điện cực sẽ dương hơn và bằng +0,34 V
⇒ Điền đáp án: 0,34
• Điện cực 1: Zn2+(aq) + 2e
 Zn(s);
Zn(s); 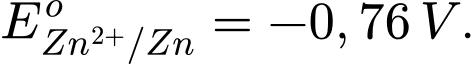
• Điện cực 2: Fe2+(aq) + 2e
 Fe(s);
Fe(s); 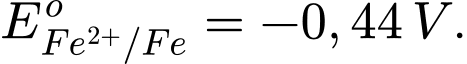
• Điện cực 3: Cu2+(aq) + 2e
 Cu(s);
Cu(s); 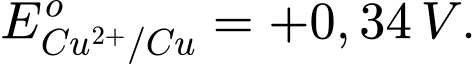
Tiến hành lắp pin điện từ hai trong ba điện cực để tạo thành pin thì giá trị sức điện động lớn nhất có thể thu được là bao nhiêu vôn?
PbO2(s) + CO(g) + H2SO4(aq) → PbSO4(s) + CO2(g) + H2O.
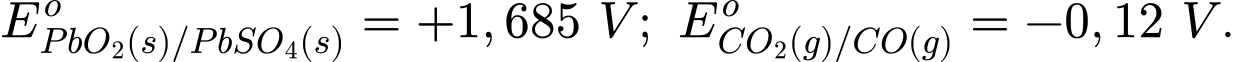
Nếu khối lượng riêng của dung dịch sulfuric acid trong acquy giảm từ 1,3 g/mL (40% H2SO4 theo khối lượng) xuống 1,2 g/mL (20% H2SO4 theo khối lượng) trong quá trình sử dụng, hãy xác định điện lượng của acquy đã tạo ra theo đơn vị ampere.giờ. Biết thể tích của acquy là 3,0 lít và thể tích thay đổi không đáng kể. (Làm tròn kết quả đến phần nguyên)
mH2SO4 sau phản ứng=V.D.C%=3000. 1,2. 20%= 720
⇒ ∆m = 1560 - 720= 840 g
⇒ nH2SO4= 60/7
⇒ ne trao đổi= 2.nH2SO4= 120/7 mol
⇒ Điền đáp án: 460
Lưu ý: Không làm tròn ở các bước tính trung gian, chỉ làm tròn kết quả ở phép tính cuối cùng
Anode (+): 2H2 + 4OH–
 4H2O + 4e
4H2O + 4eCathode (–): O2 + 4e + 2H2O
 4OH–
4OH–Một máy điện sử dụng các pin nhiên liệu để phát điện với nguyên liệu là khí hydrogen và có hiệu suất là 60% (nghĩa là có 60% năng lượng của phản ứng chuyển hoá thành điện năng). Mỗi ngày nhà máy sản xuất được 480 kWh. Tính khối lượng (theo kg) khí hydrogen tiêu thụ trong một ngày (Làm tròn đến hàng phần mười)? Cho biết:
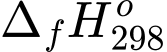 (H2O(l)) = –285,84 kJ/mol, 1 kWh = 3,6.106 J.
(H2O(l)) = –285,84 kJ/mol, 1 kWh = 3,6.106 J. 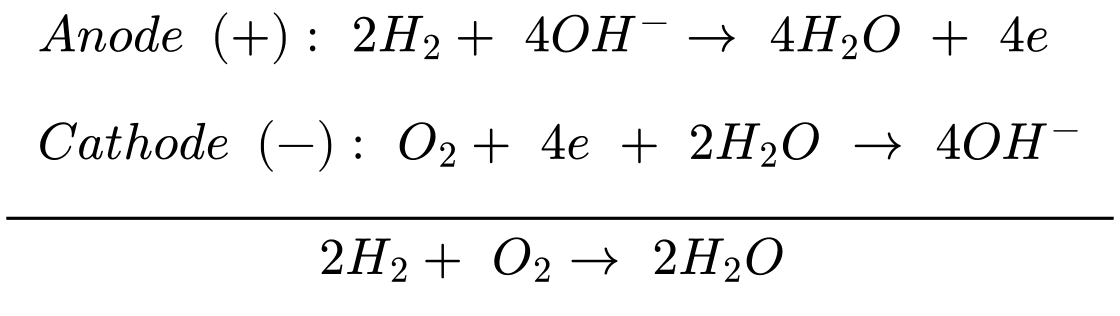
Biến thiên enthalpy của phản ứng là:
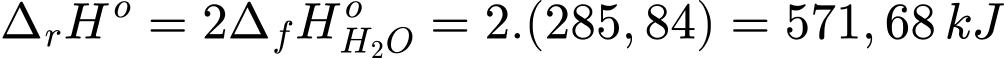
Hiệu suất chuyển hóa điện năng là 60%
2 mol H2 sẽ tạo ra năng lượng thực tế là 571,68 × 60% = 343,008 kJ
4 gam H2 sẽ tạo ra năng lượng thực tế là 343,008 kJ
x gam H2 sẽ tạo ra năng lượng thực tế là 480 × 3,6 × 103 kJ
→
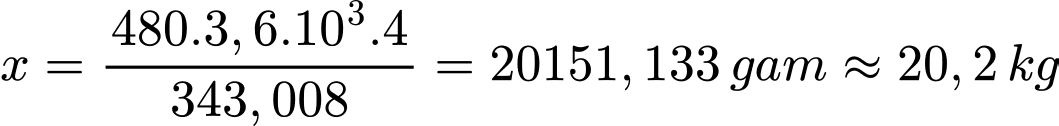
⇒ Điền đáp án: 20,2
Đọc đoạn thông tin sau và trả lời các câu hỏi từ 28 đến 30:
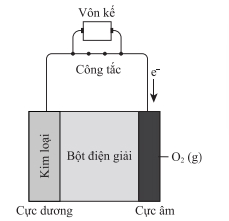

2Zn(s) + O2(g)
 2ZnO(s).
2ZnO(s).Sử dụng dữ liệu trong bảng trên, sức điện động chuẩn của pin đo được là bao nhiêu?
2Zn(s) + O2(g)
 2ZnO(s).
2ZnO(s).Anode: Zn(s) + 2OH–(aq)
 ZnO(s) + H2O(l) + 2e
ZnO(s) + H2O(l) + 2e Cathode: O2(g) + 2H2O(l) + 4e
 4OH−(aq)
4OH−(aq)Epin = E(+) – E(-) = 0,34 – (-1,31) = 1,65 V
Đáp án: A. 1,65 (V). Đáp án: A
Đáp án: B. Khối lượng pin giảm đi.
Pin kẽm – khí hoạt động dựa trên phản ứng oxi hóa của kẽm (Zn →
Zn²⁺ + 2e⁻) và giảm oxy trong khí.
Nguyên tử kẽm bị
oxi hóa, chuyển từ
kim loại rắn sang ion Zn²⁺ trong dung dịch, dẫn tới mất đi khối lượng của cực
kẽm.
Các phần khác của pin gần như không thay đổi khối lượng đáng kể.
Kim loại Na:
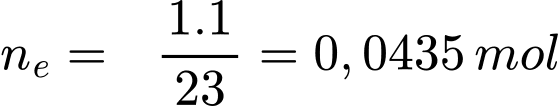
Kim loại Ca:
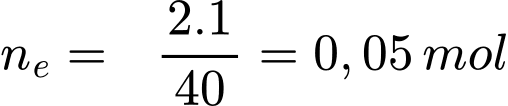
Kim loại Zn:
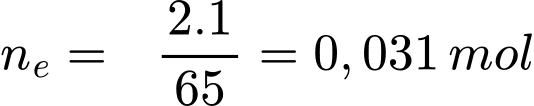
Một cực âm 1,0 g làm bằng kim loại Ca sẽ truyền nhiều electron hơn
Đáp án: B. Ca. Đáp án: B