- Để xảy ra điện phân, cần có dòng điện một chiều làm cho các ion dương (cation) di chuyển về cathode và các ion âm (anion) di chuyển về anode.
⇒ Điện phân là quá trình oxi hoá – khử xảy ra trên bề mặt các điện cực khi có dòng điện một chiều đi qua chất điện li nóng chảy hoặc dung dịch chất điện li.
⇒ Chọn đáp án D Đáp án: D
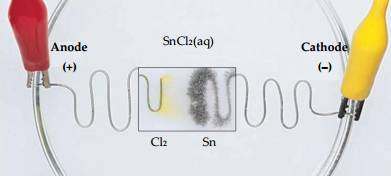
Ở anode xảy ra quá trình
2Cl- ➝ Cl2 + 2e.
⟹ Chọn đáp án A Đáp án: A
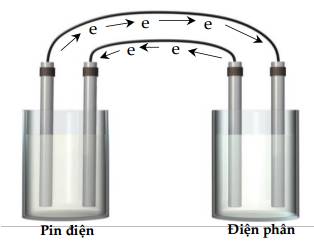
Dựa vào sơ đồ ta nhận thấy điện cực thứ nhất (từ trái sang phải) nhường electron ⇒ Anode.
Tương tự thế, ta có thứ tự điện cực: Anode, cathode, anode, cathode.
⇒ Chọn đáp án C Đáp án: C
Phương trình điện phân: 2NaCl + 2H2O ➝ 2NaOH + H2 + Cl2.
⟹ Chọn đáp án B
★ Cation không bị điện phân: Na+; K+ (nước sẽ bị điện phân)
★ Cation bị điện phân: Cu2+; H+
Cu2+ + 2e ➝ Cu
H+ + 2e ➝ H2
⟹ Dung dịch CuCl2 sẽ thu được kim loại ở cathode.
⟹ Chọn đáp án C Đáp án: C
Cation Cu2+ bị điện phân: Cu2+ + 2e ➝ Cu.
⇒ Chọn đáp án D Đáp án: D
Phương trình điện phân: 2NaCl + 2H2O ➝ 2NaOH + H2 + Cl2.
⟹ Chọn đáp án D Đáp án: D
⟹ Chọn đáp án D Đáp án: D
⋆ 2CuSO4 + H2O ➝ 2Cu + 2O2 + H2SO4
⋆ 2NaCl + 2H2O ➝ 2NaOH + H2 + Cl2
⋆ Điện phân K2SO4, KNO3 thực chất là điện phân H2O : H2O ➝ H2 + O2
⟹ Chọn đáp án B
⋆ H2O ➝ H2 + O2 ➝ Ở cả 2 điện cực có khí thoát ra ngay lúc mới bắt đầu điện phân.
⟹ Chọn đáp án C
(1) Cu2+ + 2e → Cu;
(2) 2Cl– → Cl2 + 2e;
(3) Fe3+ + 1e → Fe2+.
(4) Fe2+ + 2e → Fe;
(5) 2H+ + 2e → H2.
Khi điện phân hỗn hợp gồm các dung dịch: FeCl3, CuCl2, HCl. Quá trình xảy ra ở cathode và thứ tự xảy ra là
Các quá trình tham gia tại cathode là (1); (3); (4); (5).
Tại cathode, chất oxi hoá mạnh hơn sẽ bị khử trước.
Thứ tự điện phân các quá trình tại cathode là
(3) → (1) → (5) → (4)
⟹ Chọn đáp án A Đáp án: A
Các quá trình xảy ra khi mạ Au lên thanh đồng là:
Anode (+) Au → Au3+ + 3e
Cathode (-) Au3+ + 3e → Au.
⟹ Chọn đáp án C Đáp án: C
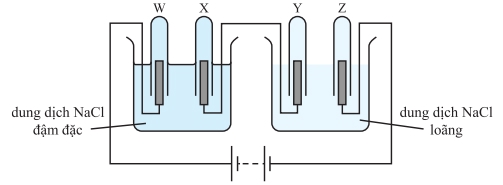
Những phát biểu nào sau đây là đúng?
(1) Thể tích khí được tạo ra và thu thập xấp xỉ bằng nhau trong các ống nghiệm W và X.
(2) Thể tích khí được tạo ra và thu thập xấp xỉ bằng nhau trong các ống nghiệm Y và Z.
(3) Ba loại khí khác nhau được tạo ra trong thí nghiệm.
Các phản ứng xảy ratrong quá trình điện phân
Cathode: 2H2O+ 2e → 2OH- + H2
Anode: 2Cl-→ Cl2 + 2e
- Nhận định (1) – Đúng.Số mol H₂ và Cl₂ sinh ra dùng cùng số electron (2e) → thể tích H₂ = Cl₂.
- Nhận định (2) – Sai.Dung dịch NaCl loãng (bên phải – ống Y và Z).
Dung dịch loãng → nênlượng Cl- ít sẽ xảy ra quá trình oxi hóa nước
Cathode: 2H2O+ 2e → 2OH- + H2
Anode: 2Cl-→ Cl2 + 2e; 2H2O → 4H++ 4e + O2
Để tạo 1 mol O₂ cần4e⁻ → tạo 2 mol H₂ (vì H₂ cần 2e). Số mol khí tạo ra và thu thập không bằngnhau.
- Nhận định (3) – Đúng.
Cathode: 2H2O+ 2e → 2OH- + H2
Anode: 2Cl-→ Cl2 + 2e; 2H2O → 4H++ 4e + O2
Ba loại khí tạo ra làCl2, O2 và H2.
Đáp án: D. (1)và (3).
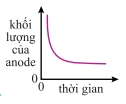
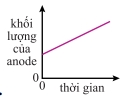
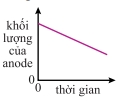
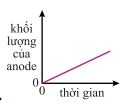
Trong điện phân dung dịch
CuSO₄ với điện cực đồng:
Anode (Cu) bị oxi hóa: Cu → Cu2+
+ 2e
→ Anode bị mòn dần, khối lượng giảm đều theo thời gian nếu
dòng điện không đổi.
Vì dòng điện không đổi → lượng chất oxi hóa theo thời gian tỉ lệ tuyến
tính (theo định luật Faraday).
Vậy đồ thị khối lượng anode theo thời gian là đường thẳng giảm đều.
Đáp án: C
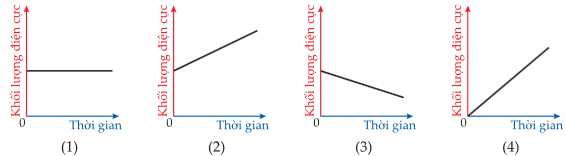
Quá trình xảy ra trên các điện cực
Anode (+) Cu → Cu2+ + 2e
Cathode (-) Cu2+ + 2e → Cu
Trong quá trình điện phân xảy ra hiện tượng dương cực tan, Cu trên Anode tan dần nên khối lượng điện cực anode sẽ giảm đi
Trên điện cực cathode có Cu sinh ra bám lên, nên khối lượng sẽ tăng lên.
Sơ đồ (3) biểu diễn cho anode
Sơ đồ (2) biểu diễn cho cathode.
⟹ Chọn đáp án A Đáp án: A
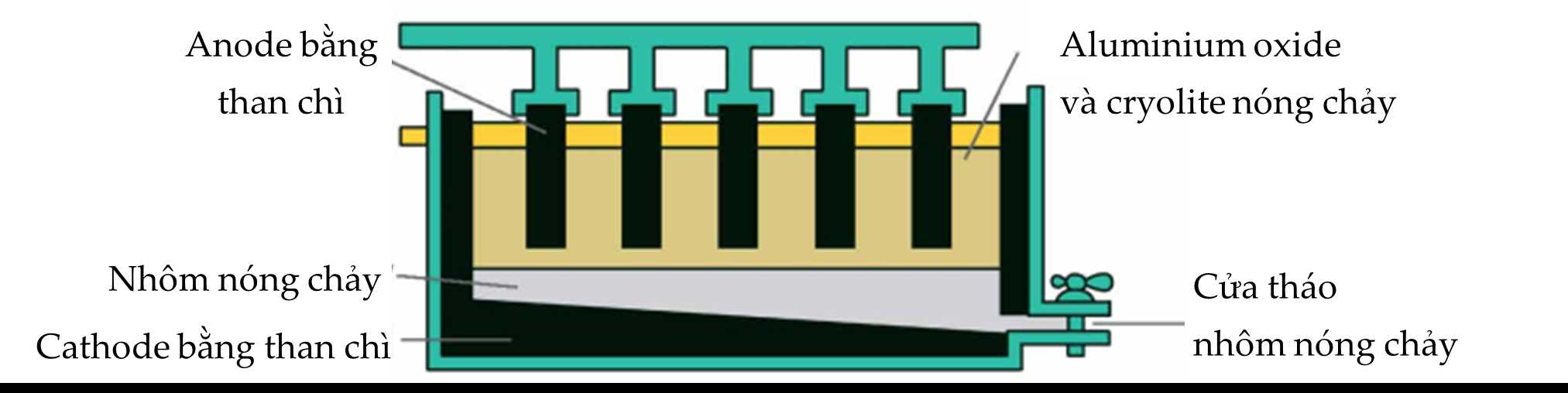
Cho các phát biểu sau:
(a) Cathode xảy ra quá trình khử Al3+ thành kim loại Al nóng chảy.
(b) Ở anode xuất hiện hỗn hợp khí O2, CO và CO2.
(c) Na3AlF6 được thêm vào sẽ nổi lên trên, bảo vệ nhôm nóng chảy khỏi bị oxi hóa bởi O2 không khí.
(d) Trong quá trình điện phân, cực âm luôn phải được thay mới do điện cực làm bằng than chì.Số phát biểu đúng là
✔️ (a) – Đúng. Cathode xảy ra quá trình khử Al3+ thành kim loại Al nóng chảy.
Điện phân nóng chảy:
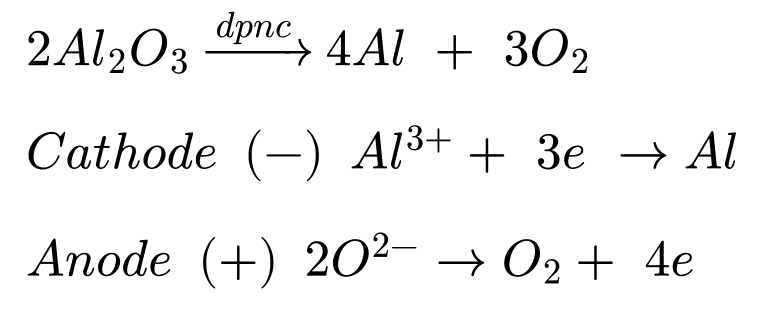
✔️ (b) – Đúng. Ở anode xuất hiện hỗn hợp khí O2, CO và CO2 nguyên do điện cực làm bằng than chì nên sẽ phản ứng với O2 sinh ra.
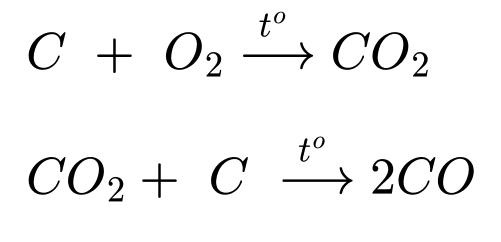
✔️ (c) – Đúng.
Cryolite (Na3AlF6) là nguyên liệu được dùng để sản xuất nhôm với mục đích:
- Làm giảm nhiệt độ nóng chảy của Al2O3.
- Tiết kiệm được năng lượng, tạo được chất lỏng có tính dẫn điện tốt hơn Al2O3.
- Tạo chất lỏng có tỉ khối nhỏ hơn nhôm, nổi lên bề mặt ngăn nhôm nóng chảy bị oxi hoá.
❌ (d) – Sai. Trong quá trình điện phân, cực dương (anode) luôn phải được thay mới do điện cực làm bằng than chì sẽ phản ứng với O2 sinh ra trong quá trình sản xuất nhôm.
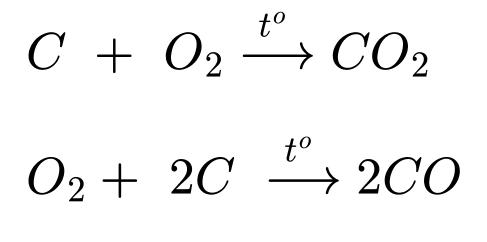
Các phát biểu đúng là (a) (b) (c)
⇒ Chọn đáp án C Đáp án: C
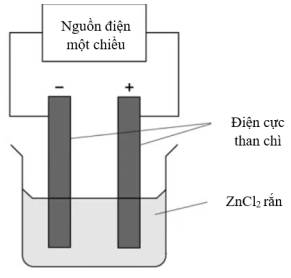
Lý do nào làm quá trình điện phân không xảy ra?
=> Chọn đáp án A Đáp án: A
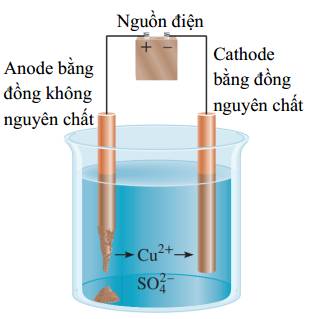
Giải thích cho hiện tượng này là
➔ Đáp án A. vàng chưa bị điện phân tại điện áp của đồng. Đáp án: A
Sau t phút, ở cathode(-) chưa có bọt khí => chỉ có Cu2+ bị khử
=> Áp dụng định luật Faraday ta có:
t = (mCu x F x n) / (MCu x I) = (1,92 x 96500 x 2) / (64 x 1,93) = 3 000 (s) = 50 phút
Đáp án: AKhối lượng của LiCl trong 1 tấn hỗn hợp là mLiCl = 1000 × 60% = 600 kg
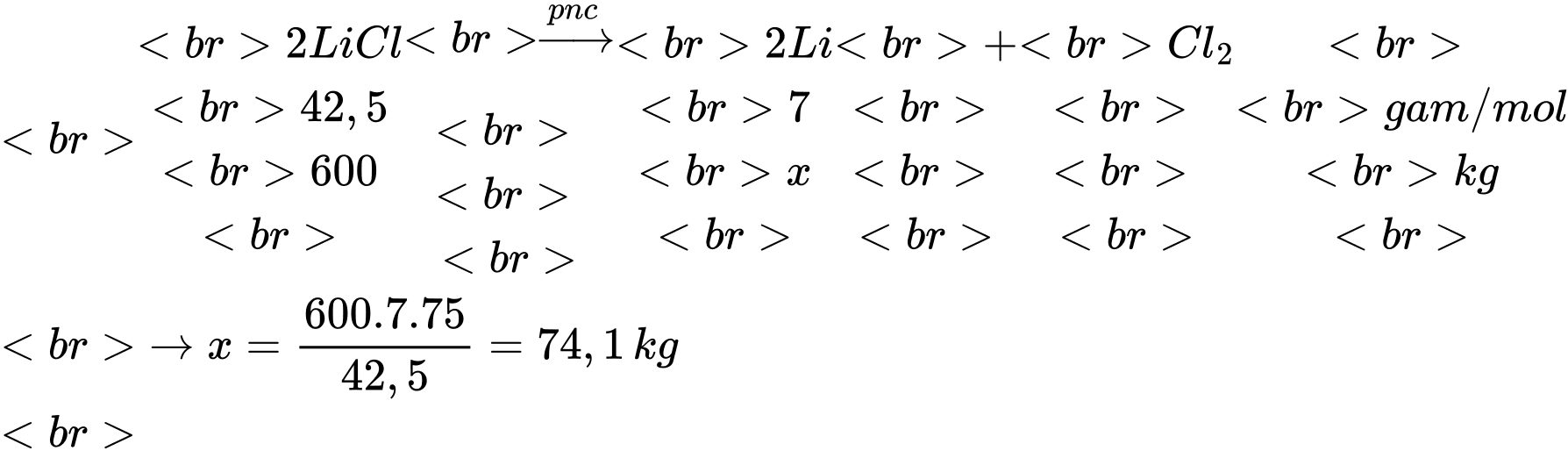
⟹ Điền đáp án: 74,1
Ta có phương trình:
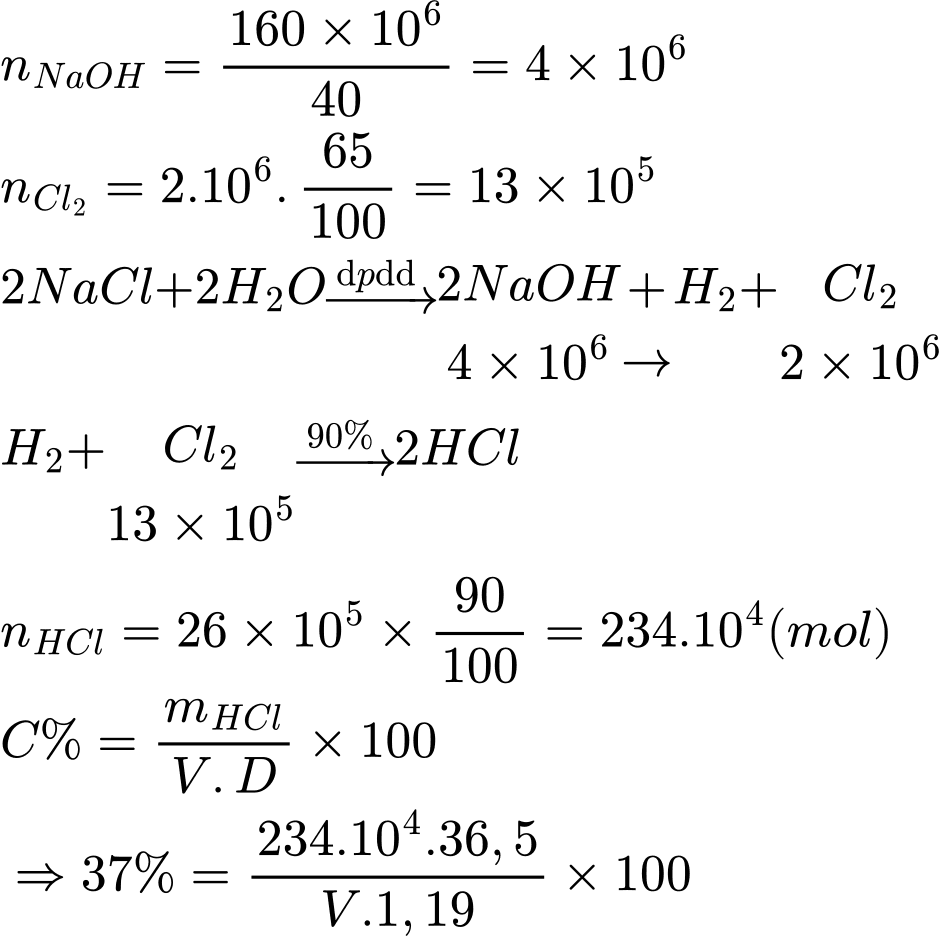
⟶ V = 193,98 (m3)
⟹ Điền đáp án 194
Khối lượng dung dịch NaOH là mdd NaOH = 10000 × 1,52 = 15200 gam
Khối lượng NaOH là mNaOH = 15200 × 50% = 7600 gam
Số mol của NaOH là nNaOH = 7600 ÷ 40 = 190 mol
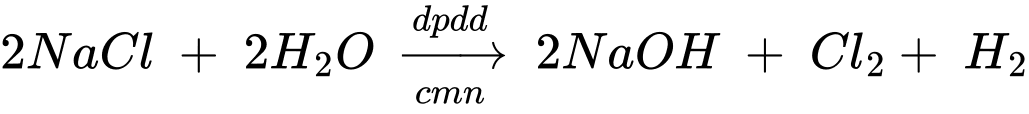
Theo phương trình số mol của NaCl là 190 mol
Khối lượng của NaCl là: x.(300 – 220) = 190 × 58,5 : 80% → x ≈ 173,67
⟹ Điền đáp án: 174
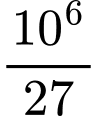
Phương trình phản ứng: 2Al2O3 ➝ 4Al + 3O2 => nO2 =
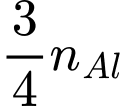 =
= 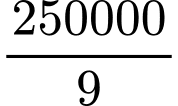
Điện cực than chì phản ứng với O2 theo 2 phương trình:
=> Số mol O2 phản ứng= 0,5x + x = 1,5x = 250000/9
=> x= 500000/27
=> nC phản ứng = 2.x= 1000000/27 => mC= 0,44 tấn
=> Điền đáp án: 0,44
Theo định luật Faraday, tại bình chứa dung dịch AgNO3:
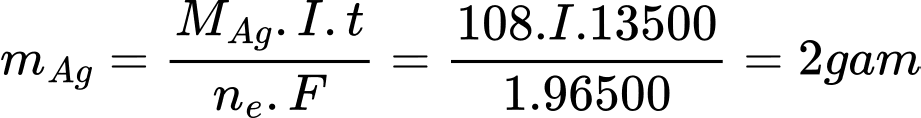
=> I = 0,132 A
Vì hai bình điện phân mắc nối tiếp nên cường độ dòng điện ở 2 bình bằng nhau (I= 0,132A)
=> Khối lượng đồng trong bình điện phân 2 là:
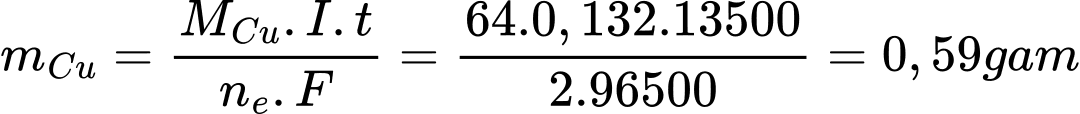
=> Điền đáp án: 0,59
Cr2O72−(aq) + 12e + 14H+(aq)
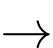 2Cr(s) + 7H2O(l)
2Cr(s) + 7H2O(l)Để mạ được lớp chromium dày 1,0×10−2 mm cho thanh cản ô tô có diện tích bề mặt 0,25 m2 trong một bình điện phân có cường độ dòng điện 25,0 A thì cần bao nhiêu thời gian (tính bằng giờ) biết khối lượng riêng của chromium là 7,19 g/cm3
(làm tròn đến hai chữ số thập phân)
V lớp mạ Cr = 10-3.2500 = 2,5 cm3
=> Khối lượng Cr:
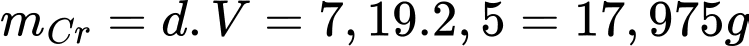
Từ phương trình phản ứng ta xác định được ne trao đổi = 6e
Áp dụng định luật Faraday:
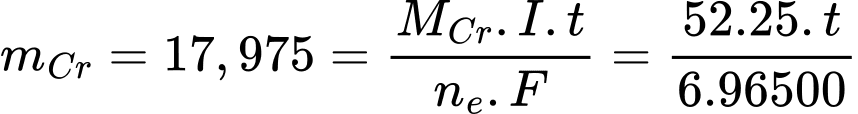
=> t= 8006 giây = 2,22 giờ
=> Điền đáp án: 2,22
(làm tròn đến số nguyên)
=> Diện tích toàn phần của miếng đồng = (5+ 1).2.0,1 + 2.5.1 = 11,2 cm2
Vì tất cả các mặt đều được mạ bằng bạc đến độ dày 1 micrometer (10-4 cm) => Thể tích lớp Ag: V= 11,2.10-4= 1,12.10-3 cm3
=> Khối lượng Ag cần mạ là m = D.V= 10,5. 1,12.10-3 =0,01176 gam
Áp dụng định luật Faraday:
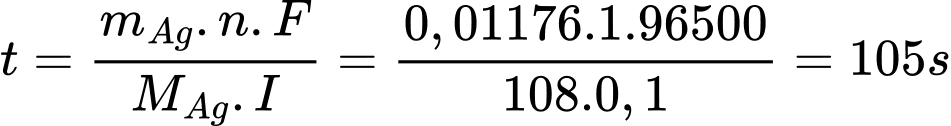
=> Điền đáp án: 105
Cho biết: MLi = 7 g/mol; hằng số Faraday là 96500 C/mol; I là cường độ dòng điện (A), t là thời gian (s), 1 năm = 365 ngày.
Nếu pin hoạt động ở cường độ dòng điện ổn định là 2,5.10-5 A thì một pin được chế tạo bởi 0,6 gam lithium có thể hoạt động tối đa trong thời gian bao nhiêu năm (Làm tròn đến hàng phần mười)?
Quá trình xảy ra trong pin:
Anode (-):
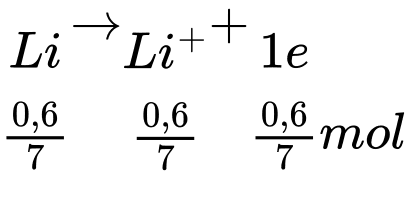
Số năm pin lithium có thể hoạt động tối đa là:
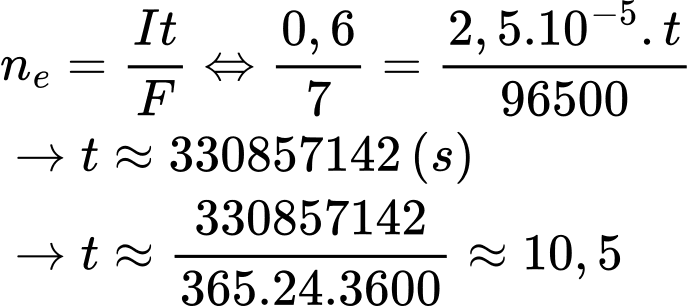
⇒ Điền đáp án: 10,5
Đọc đoạn thông tin sau và trả lời các câu hỏi từ 28 đến 30:
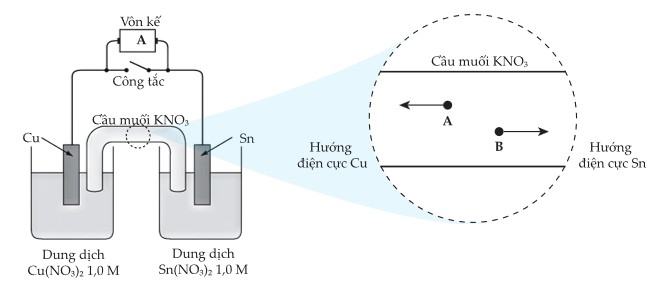
Trong khung mở rộng của phần trung tâm cầu muối được hiển thị trong sơ đồ bên dưới, quan sát thấy có các hạt A và B di chuyển ngược phía nhau về các điện cực khi pin bắt đầu hoạt động. Chú ý bỏ qua các phân tử dung môi.
Quá trình xảy ra trong pin:
Cathode (+) Cu2+ + 2e
→ Cu
Anode (-) Sn → Sn2+ + 2e
Đáp án: A. Cu2+ + 2e →
Cu.
Cu2+ + Sn ⟶ Cu + Sn2+
Từ phương trình hóa học: nSn = nCu = 0,15 mol
Khối lượng Sn mất đi là: mSn = 0,15 × 119 = 17,85 gam
⇒ Chọn đáp án B Đáp án: B
(i) Hạt A là hạt ion K+.
(ii) Hạt B là hạt ion NO3- .
(iii) Các electron di chuyển qua cầu muối.
(iv) Khối lượng điện cực Cu tăng lên bằng khối lượng điện cực Sn giảm đi.
(v) Khi điện cực Cu ngừng thì điện cực Sn cũng ngừng hoạt động.
Vai trò của cầu muối là trung hòa điện tích của 2 dung dịch: các ion dương Na+ hoặc K+ và Zn2+ di chuyển qua cầu muối đến cốc đựng dung dịch CuSO4. Ngược lại, các ion âm SO42- hoặc NO3- di chuyển qua cầu muối đến dung dịch ZnSO4.
Phân tích các nhận định:
✔️ (i) – Đúng. Tại điện cực Cathode mất đi cation Cu2+ nên bổ sung bằng 1 cation khác nên hạt A là hạt ion K+.
✔️ (ii) – Đúng. Tại điện cực Anode tạo ra thêm anion Sn2+ nên bổ sung bằng anion khác nên hạt B là hạt ion NO3-.
❌ (iii) – Sai. Các electron di chuyển qua dây dẫn.
❌ (iv) – Sai. Khối lượng điện cực Cu tăng lên khác khối lượng điện cực Sn giảm đi nguyên do có sự chênh lệch nguyên tử khối với tăng lên 1 mol Cu ứng với 64 gam thì sẽ giảm đi 1 mol Sn ứng với 119 gam.
✔️ (v) – Đúng. Khi điện cực Cu ngừng thì điện cực Sn cũng ngừng hoạt động.
Các phát biểu đúng là (i) (ii) (v).
⇒ Chọn đáp án C Đáp án: C