⟹ chọn đáp án C Đáp án: C
❌ A. Nước: 2H2O + 2Na → 2NaOH + H2↑.
❌ C. Giấm ăn: 2CH3COOH + 2Na → 2CH3COONa + H2↑.
❌ D. Ethanol: 2C2H5OH + 2Na → 2C2H5ONa + H2↑.
⟹ Chọn đáp án B Đáp án: B
- Vì khối lượng riêng của Na, K nặng hơn khối lượng riêng của dầu hỏa, chúng sẽ chìm xuống dưới bề mặt dầu hỏa.
⟹ Chọn đáp án A
Đáp án: A
(a) Có cấu hình electron lớp ngoài cùng là ns¹ (n > 1).
(b) Có số oxi hoá là +1 hoặc +2 trong các hợp chất.
(c) Có tính khử mạnh.
(d) Có bán kính nguyên tử nhỏ.
(e) Còn được gọi là các kim loại kiềm.
Số phát biểu đúng về các nguyên tố nhóm IA là
✔️(a) – Đúng. Nguyên tố nhóm IA là những nguyên tố s, chỉ có 1 electron hoá trị ở phân lớp ns1 và đứng đầu mỗi chu kì tương ứng.
❌(b) – Sai. trong các phản ứng hoá học, chúng dễ nhường 1 electron, thể hiện tính khử rất mạnh: M ⟶ M+ + 1e .Trong hợp chất, nguyên tử kim loại nhóm IA chỉ thể hiện số oxi hoá +1.
✔️(c) – Đúng. Kim loại nhóm IA là những kim loại hoạt động hoá học mạnh, có tính khử mạnh và tính khử tăng dần từ Li đến Cs.
❌(d) – Sai. Theo định luật tuần hoàn, trong 1 nhóm bán kính các nguyên tố giảm dần theo chiều tăng điện tích hạt, nên các nguyên tố kim loại kiềm đều đứng đầu nhóm nên có bán kính lớn
✔️(e) – Đúng. Các kim loại nhóm IA còn được gọi là kim loại kiềm.
Có 3 đáp án đúng.
⟹ Chọn đáp án C Đáp án: C
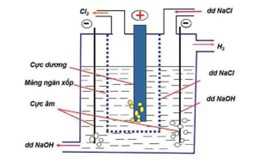
Phương pháp điều chế NaOH trong công nghiệp là Điện phân dung dịch NaCl bão hoà có màng ngăn
⟹ Chọn đáp án C Đáp án: C
⭐ Potassium (K): Thúc đẩy quá trình quang hợp, tăng sức mạnh đề kháng của cây, cải thiện chất lượng và năng suất nông sản.
⭐ Nitrogen (N) dạng nitrate (NO3-): hấp thu dễ dàng và thúc đẩy sự phát triển nhanh chóng của cây.
⇒ Chọn đáp án A Đáp án: A
- 2NaOH + CuCl2 → Cu(OH)2↓ + 2NaCl
- 3NaOH + AlCl3 → Al(OH)3↓ + 3NaCl; NaOH + Al(OH)3 → NaAlO2 + 2H2O
- 2NaOH + FeSO4 → Na2SO4 + Fe(OH)2↓
→ Có 3 trường hợp thu được kết tủa
→ Chọn đáp án C
Đáp án: C
– Dung dịch chất X và chất Y đều làm dung dịch phenolphthalein chuyển sang màu hồng.
– Trộn X và Y thu được kết tủa màu trắng.
– Chất X cháy với ngọn lửa màu lục trên đèn khí, trong khi chất Y cháy với ngọn lửa màu tím.
Biết mỗi chất X, Y đều chỉ chứa một loại cation và một loại anion. Phát biểu nào sau đây không đúng?
⟹ Cả X và Y đều có tính base, chứa nhóm OH-
Trộn X và Y thu được kết tủa màu trắng: Phản ứng tạo kết tủa cho thấy có sự kết hợp của cation và anion từ X và Y tạo thành chất không tan.
⟹ có khả năng chứa ion CO32- và SO42-
Tuy nhiên ion CO32- có khả năng :
CO32- + H2O ⟶ HCO3- + OH-
Tạo môi trường base làm đổi màu quỳ tím.
X cháy với ngọn lửa màu lục: Điều này cho thấy X chứa ion (Ba2+).
Y cháy với ngọn lửa màu tím: Điều này cho thấy Y chứa ion (K+).
⟹ Chứa 4 ion K+, Ba2+ , CO32- , OH-
Phân tích các đáp án:
✔️A. ĐÚNG. Phù hợp với kết quả thí nghiệm về màu ngọn lửa.
✔️B. ĐÚNG. Vì X chứa Ba2+ và có tính base (làm phenolphthalein chuyển màu hồng), nên X phải là một base của barium, ví dụ như Ba(OH)2 hoặc BaCO3, không thể là BaCl2 (muối trung tính).
❌C. SAI. Y chứa K+ và có tính base, nhưng không nhất thiết phải là K2CO3. Y có thể là KOH hoặc một base khác của potassium.
✔️D. ĐÚNG. Vì X chứa Ba2+, nên kết tủa tạo thành khi trộn X và Y phải chứa barium.
⟹ Chọn đáp án C Đáp án: C

Một mẫu khoáng vật calcite ở vùng Balkal, Nga
- Khoáng vật dolomite có thành phần chủ yếu là MgCO3.CaCO3.
- Mà CaCO3 và MgCO3 đều không tan trong nước.
⟶ Các khoáng vật calcite, dolomite,... hầu như không tan trong nước.
Chọn đáp án A Đáp án: A
• Barium hydroxyde tan trong nước tạo dung dịch điện li mạnh.
• Magnesium hydroxide không tan trong nước.
Khả năng phản ứng với barium với nước như nào so với magnesium với nước?
⇒ Ba(OH)2 phản ứng với nước mạnh hơn Mg(OH)2 do có độ hòa tan cao hơn và tính chất base mạnh hơn.
⇒ Chọn đáp án A Đáp án: A

Một số bọt khí hydrogen xuất hiện khi cho magnesium vào nước ở điều kiện thường
- Lớp màng này không tan trong nước, bền và có tác dụng ngăn cản sự tiếp xúc giữa kim loại Mg với nước, làm chậm phản ứng.
⟹ Chọn đáp án A. Đáp án: A
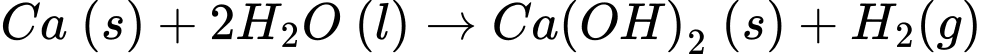
- Ca(OH)2 chỉ tan một phần, nên dung dịch sẽ có màu hồng nhạt do phenolphthalein đổi màu trong môi trường base.
- Do Ca(OH)2 không tan hết, trong cốc sẽ có hiện tượng vẩn đục do Ca(OH)2 rắn lắng xuống.
⟹ Chọn đáp án C Đáp án: C
(1) Barium có tính khử mạnh hơn magnesium.
(2) Độ tan của barium hydroxide trong nước cao hơn nhiều so với magnesium hydroxide.
(3) Bọt khí hydrogen sinh ra bám trên bề mặt magnesium nhiều hơn, cản trở phản ứng tiếp diễn.
✔️ 1. Ba có tính khử mạnh hơn Mg: Đây là đúng vì trong nhóm kim loại kiềm thổ, tính khử tăng dần từ trên xuống dưới bảng tuần hoàn. Ba nằm dưới Mg nên có tính khử mạnh hơn.
✔️ 2. Độ tan của barium hydroxide (Ba(OH2) cao hơn nhiều so với magnesium hydroxide (Mg(OH)2): Đúng vì Ba(OH)2 tan tốt trong nước, trong khi Mg(OH)2 rất ít tan, làm cho phản ứng của Ba diễn ra dễ hơn.
❌3. Ba hoạt động hoá học mạnh hơn nên tốc độ thoát khí của H2 mạnh hơn magnesium.
Chọn đáp án D Đáp án: D
❌ B. Barium chloride (BaCl2): Là một muối tan trong nước, không có đặc tính phù hợp với yêu cầu của thuốc diệt chuột.
❌ C. Barium hydroxide (Ba(OH)2): Là một base mạnh, tan trong nước và có tính kiềm cao, không phù hợp để làm thuốc diệt chuột.
❌ D. Barium sulfate (BaSO4): Là một muối không tan trong nước và cũng không có tính độc hại ở nồng độ bình thường, không phù hợp với mục đích diệt chuột.
⟹ Chọn đáp án A. Đáp án: A
- Z là CO2 (carbon dioxide), không phải là khí duy trì sự sống (oxygen, O2). CO2 là khí gây ra hiệu ứng nhà kính và không hỗ trợ sự sống của hầu hết các sinh vật trên trái đất.
Phương trình phản ứng giữa Y (CaCO3) và acid mạnh (ví dụ, hydrochloric acid HCl) để tạo ra Z (CO2) và các sản phẩm khác:
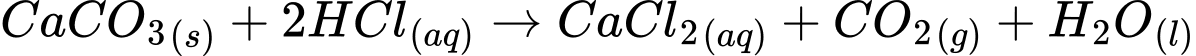
⟹ Chọn đáp án B Đáp án: B
❌ B. Dung dịch NH3: Dung dịch NH3 có thể phân biệt được dung dịch CaCl2 và BaCl2. Khi thêm dung dịch NH3 vào dung dịch CaCl2, sẽ không xảy ra hiện tượng gì rõ rệt.
✔️ C. Na2CrO4: Dung dịch Na2CrO4 sẽ tạo ra kết tủa màu vàng với dung dịch BaCl2 (do tạo ra BaCrO4), nhưng không phản ứng với CaCl2.
❌ D. Na2CO3: Khi thêm Na2CO3 vào dung dịch CaCl2, cả 2 sẽ tạo ra kết tủa CaCO3, BaCO3 trắng.
⟹ Chọn đáp án C
Đáp án: C
1. CaCl2 (Calcium chloride): Khi đốt, tạo ra màu cam đặc trưng.
2. BaCl2 (Barium chloride): Khi đốt, tạo ra màu lục
3. KCl (Potassium chloride): Khi đốt, tạo ra màu tím.
4. NaCl, Na2CO3 Khi đốt, tạo ra màu vàng đặc trưng.
⟹ Có thể phân biệt 3 chất.
⟹ Chọn đáp án B
Đáp án: B
✔️ A. Đúng. Các muối nitrate của nhóm IIA (ví dụ: Mg(NO3)2, Ca(NO3)2, Ba(NO3)2) đều tan tốt trong nước. Đây là quy tắc chung cho tất cả các muối nitrate (NO3-), chúng đều hòa tan trong nước.
✔️ B. Đúng. Muối magnesium sulfate (MgSO4) là chất tan trong nước, trong khi đó muối barium sulfate (BaSO4) lại là chất không tan trong nước.
✔️ C. Đúng. Các muối carbonate của nhóm IIA (MgCO3, CaCO3, SrCO3, BaCO3) đều không tan trong nước.
❌ D. Sai. Các hydroxide của nhóm IA (NaOH, KOH, LiOH) đều tan rất tốt trong nước. Tuy nhiên, hydroxide của nhóm IIA có độ tan khác nhau. Ví dụ, Mg(OH)2 rất ít tan.
⟹ Chọn đáp án D Đáp án: D
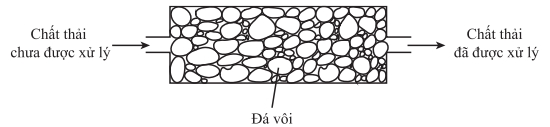
Sự thay đổi nào sau đây là đúng trong quá trình xử lý chất thải công nghiệp?
Đá vôi (chủ yếu là CaCO₃) là chất base yếu, thường được dùng để:
- Trung hòa chất thải acid
- Giảm độ ăn mòn và độc hại của nước thải công nghiệp
→ Nếu dung dịch ban đầu là acid, sau khi đi qua lớp đá vôi sẽ trởnên trung tính (nếu dùng lượng đá vôi vừa đủ).
Ngược lại, đá vôi không thể làm dung dịch trung tính hoặc kiềm trở thành acid, nên các phương án tạo ra môi trường acid sau xử lý đều sai.
Đáp án đúng: D. Acid → Trung tính.
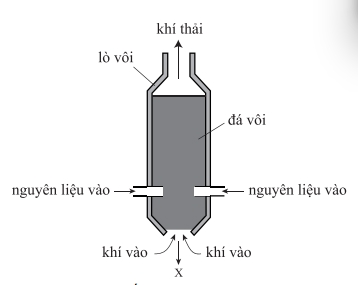
Chất X được đưa ra từ lò nung vôi là chất gì?
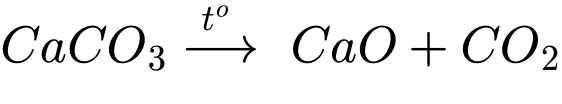
Chất X được đưa ra từ lò nung vôi là calcium oxide.
Đáp án: C. Calcium oxide. Đáp án: C
Ca(HCO3)2 + 2NaOH → CaCO3↓ + Na2CO3 + H2O
3Mg(HCO2)2 + 2Na3PO4 → Mg3(PO4)2↓ + 6NaHCO3
Ca(HCO3)2 + Na2CO3 → CaCO3↓ + 2NaHCO3
⟹ Chọn đáp án B
Đáp án: B
Nước chứa nhiều ion HCO3– là nước cứng tạm thời → SAI.
Nước cứng chứa nhiều ion HCO3– là nước cứng tạm thời → ĐÚNG.
Trước khi xét nước có tính cứng tạm thời/vĩnh cửu/toàn phần thì nước đó phải là nước cứng (chứa Ca2+, Mg2+)!
Đáp án: A
Nước cứng không phải tác nhân gây ô nhiễm nguồn nước hiện nay. A sai.
Nước tự nhiên thường chứa nhiều ion nên có cả tính cứng tạm thời và vĩnh cửu → cứng toàn phần. B đúng.
Đun nóng chỉ làm mềm được nước cứng tạm thời và làm mềm được 1 phần nước cứng toàn phần. C sai.
Nước cứng là nước chứa nhiều ion Ca2+ và Mg2+, tùy vào các ion âm trong nước cứng mà người ta chia ra các loại nước cứng khác nhau. D sai.
Đáp án: B
Nước cứng tạm thời là nước có chwuas các ion Ca2+, Mg2+, HCO3–
⇒ Tính cứng tạm thời gây nên bởi các muối Ca(HCO3)2 và Mg(HCO3)2.
Đáp án: D
(a) Nước có chứa nhiều ion HCO3– được gọi là nước có tính cứng tạm thời.
(b) Có thể làm mềm nước có tính cứng tạm thời bằng cách đun sôi nước.
(c) Có thể loại bỏ một phần tính cứng của nước có tính cứng vĩnh cửu bằng cách dùng một lượng vừa đủ Ca(OH)2.
(d) Không thể dùng cách đun sôi để loại bỏ hoàn toàn tính cứng của nước có chứa nhiều các ion sau: Mg2+, Ca2+, Cl–, HCO3–, SO42–.
(e) Nước cứng có thể là nguyên nhân gây nổ nồi hơi.Số phát biểu đúng là
❌(a) – Sai. Nước có chứa nhiều ion Mg2+, Ca2+, HCO3- được gọi là -nước có tính cứng tạm thời.
✔️(b) – Đúng. Có thể làm mềm nước có tính cứng tạm thời bằng cách đun sôi nước.
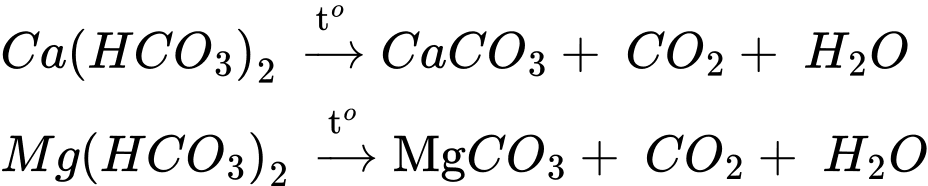
❌(c) – Sai. Không thể loại bỏ tính cứng của nước có tính cứng tạm thời bằng cách dùng một lượng vừa đủ Ca(OH)2.
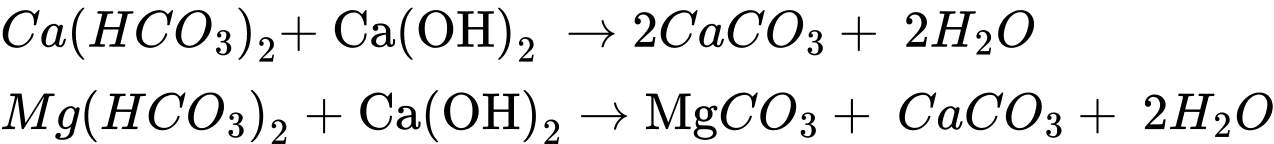
✔️(d) – Đúng. Không thể dùng cách đun sôi để loại bỏ hoàn toàn tính cứng của nước có chứa nhiều các ion sau: Mg2+, Ca2+, Сl-, НСО3- , SO42-. Chỉ loại bỏ được 1 phần Ca2+ và Mg2+ thông qua phản ứng phân hủy Ca(HCO3)2 và Mg(HCO3)2 làm nước cứng chuyển từ nước cứng toàn phần sang nước cứng vĩnh cữu.
✔️(e) – Đúng. nước cứng có thể gây đóng cặn CaCO3, MgCO3 trong nồi hơi tạo thành lớp cách nhiệt ngay dưới đáy nồi, làm cản trở quá trình dẫn nhiệt từ đó có thể gây hiện tượng nổ nồi hơi.
Có 3 phát biểu đúng.
⟹Chọn đáp án C Đáp án: C
(a) Cần sử dụng kính an toàn có bảo vệ mắt khi đốt magnesium.
(b) Các đám cháy magnesium tỏa ra một lượng nhiệt rất lớn.
(c) Có thể dập tắt các đám cháy kim loại magnesium bằng nước, cát.
(d) Khi có đám cháy kim loại cần làm mát các khu vực tiếp xúc và đảm bảo đám cháy không lan sang các khu vực xung quanh.
Các phát biểu đúng là
✔️ (a) Đúng. Khi cháy magnisium phát ra ánh sáng chứa tia cực tím có thể gây tổn thương cho mắt.
✔️ (b) Đúng. Khi cháy magnisium tỏa ra lượng nhiệt rất lớn.
❌ (c) Sai. Không dùng nước, cát khô để dập tắt đám cháy magie vì magie phản ứng với nước, cát nóng sinh ra hydrogen, silicon có thể xảy ra một vụ nổ hơi làm văng các kim loại này đi khắp nơi dẫn đến đám cháy lan rộng.
Mg + H2O
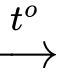 MgO + H2
MgO + H2SiO2 + 2Mg
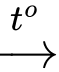 2MgO + Si
2MgO + Si✔️ (d) Đúng. Đám cháy Mg gần như không thể dập tắt, chỉ có thể hạn chế bằng cách không để đám cháy lan rộng và đợi cho kim loại Mg phản ứng hết.
⟶ Các phát biểu đúng là (a) (b) (d)
⇒ Chọn đáp án B Đáp án: B
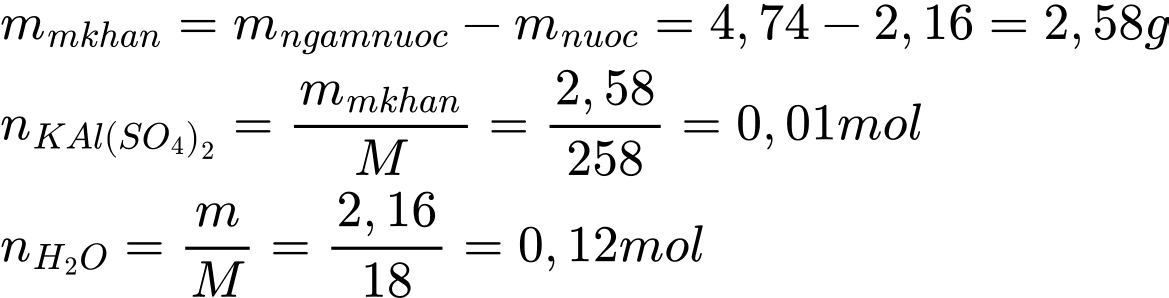
Trong công thức KAl(SO4)2⋅xH2O, số mol H2O tỉ lệ với số mol KAl(SO4)2
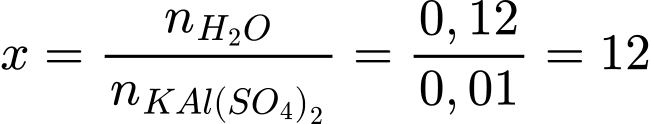
=> Công thức của hợp chất ngậm nước là KAl(SO4)2.12H2O
⟹ Chọn đáp án 12
Bước 1: Cân 30 gam “muối i-ốt” rồi hòa tan trong nước cất thu được 100 mL dung dịch X đựng trong bình nón 250 mL (có nút nhám) thêm dung dịch KI 1 M (dư), dung dịch H2SO4 1 M.
KIO3 + 5KI + 3H2SO4
 3K2SO4 + 3I2 + 3H2O
3K2SO4 + 3I2 + 3H2OBước 2: Đậy nắp và lắc nhanh mẫu, để mẫu yên tĩnh nơi tối 5 phút. Sau 5 phút, thêm 1 mL dung dịch hồ tinh bột 1%, rồi đem chuẩn độ chậm (4 giây một giọt) bằng dung dịch Na2S2O3 0,005 M tới khi mất màu thì thể tích dung dịch Na2S2O3 đã dùng là 11,0 mL.
I2 + 2Na2S2O3
 2NaI + Na2S4O6
2NaI + Na2S4O6Tính hàm lượng iodine (mg/kg muối) trong KIO3 của mẫu “muối i-ốt” trên (làm tròn đến hàng đơn vị)
(2) 2Na2S2O3 + I2 → Na2S4O6 + 2NaI
Đổi 11 mL = 0,011 L
Số mol Na2S2O3 đã phản ứng là nNa2S2O3 = 0,011.0,005 = 5,5.10-5 mol
Số mol I2 = nNa2S2O3 : 2 = 2,75×10−5 mol
Từ PTHH (1) và (2) số mol của KIO3 là: 11/1200000 mol
Hàm lượng iodine trong muối trên là:
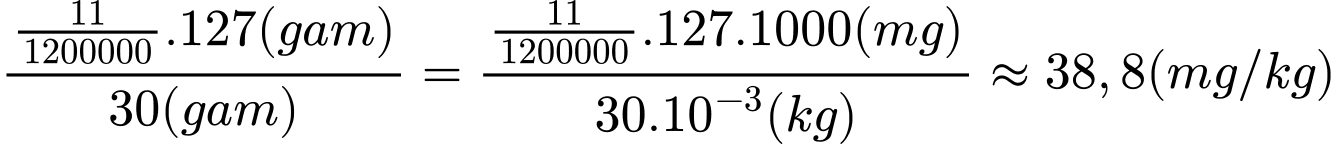
Làm tròn kết quả đến hàng đơn vị: 39mg/kg
⟹Điền đáp án : 39
mCa2+ = 300 × 2% = 6 gam
Số mol của Ca2+ là nCa2+ = 6 ÷ 40 = 0,15 mol
⟹ Điền đáp án: 0,15
 SrO(s) + N2(g) + 2CO2(g) + CO(g)
SrO(s) + N2(g) + 2CO2(g) + CO(g)Thể tích khí thoát ra (đkc) khi trộn 10,6 gam stronium nitrate với hỗn hợp pháo hoa.(làm tròn đến phần chục).
Điền đáp án: ..........
Số mol của Sr(NO3)2
n =10.6 : 211.6 = 0.05 mol.
Theo phương trình, số mol khí sinh ra:
nkhí = 4×nSr(NO3)2 = 4×0.05 = 0.2 mol.
V = nkhí×24,79 = 0,2.24,79 = 4,958L
Điền đáp án: 5,0
2Al(s) + 3Ca(OH)2(s) + 6 H2O(l)
 3CaO.Al2O3.6H2O(s) + 3H2(g)
3CaO.Al2O3.6H2O(s) + 3H2(g)Giả sử hỗn hợp các chất phản ứng chứa 0,56 g Al và lượng calcium hydroxide, nước dùng dư cho mỗi viên gạch. Thế tích khí hydrogen tối đa có thể tạo ra ở điều kiện chuẩn là bao nhiêu?
(Làm tròn đến hai chữ số thập phân)
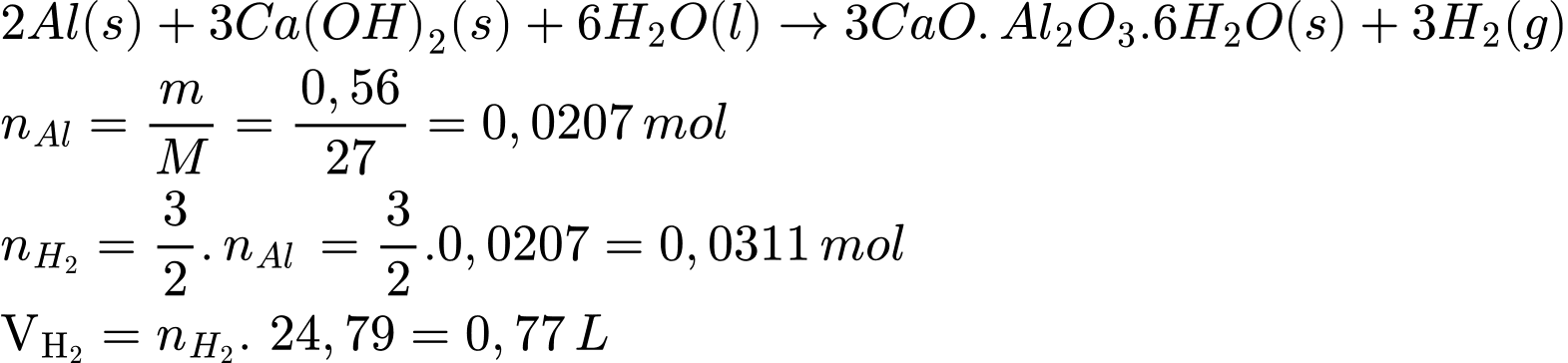
Điền đáp án: 0,77
Đọc đoạn thông tin sau và trả lời các câu hỏi từ 33 đến 35:
Phần 1: Lấy 20 mL dung dịch X chuẩn độ với dung dịch EDTA 0,01 M, thì dùng hết 1,85 mL dung dịch EDTA.
Phần 2: Lấy 20 mL dung dịch X, điểu chỉnh pH của dung dịch bằng cách thêm NaOH 0,2 M sao cho Ca2+ không kết tủa nhưng có thể loại ion Mg2+ dưới dạng kết tủa Mg(OH)2. Sau khi tách kết tủa, cũng tiến hành chuẩn độ với dung dịch EDTA 0,01 M thì thấy dùng hết 1,24 mL dung dịch EDTA. Phương trình chuẩn độ xảy ra như sau:
Mg2+(aq) + EDTA2–(aq) → Mg(EDTA)(aq)
Ca2+(aq) + EDTA2–(aq) → Ca(EDTA)(aq)
Khi
pha loãng 50 mL nước khoáng thành 100 mL dung dịch X, dung dịch X so với mẫu nước
ban đầu đã thay đổi nồng độ giảm một nửa.
Đáp án: B. Giảm một nửa.
- Thêm NaOH để điều chỉnh pH sao cho:
+ Ca²⁺ không kết tủa → pH < pH kết tủa Ca(OH)₂
+ Mg²⁺ kết tủa dưới dạng Mg(OH)₂ → Mg²⁺ bị loại bỏ
- Tách kết tủa Mg(OH)₂ → trong dung dịch còn lại chỉ còn Ca²⁺.
- Chuẩn độ bằng EDTA → EDTA chỉ phản ứng với ion Ca²⁺ còn trong dung dịch.
Kết luận: Dung dịch EDTA lúc này chỉ chuẩn độ với Ca²⁺.
Đáp án: B. Chỉ Ca2+.
Đáp án: BMg2+(aq) + EDTA2–(aq)  Mg(EDTA)(aq)
Mg(EDTA)(aq)
Ca2+(aq) + EDTA2–(aq)  Ca(EDTA)(aq)
Ca(EDTA)(aq)
Phần 1: số mol của EDTA2- là nEDTA2- = 0,01.0,00185 = 1,85.10-5 mol
Theo PTHH: nCa2+ + nMg2+ = 1,85.10-5 mol
Phần 2: số mol của EDTA2- là nEDTA 2- = 0,01.0,00124 = 1,24.10-5 mol = nCa2+
=> Số mol của Mg2+ là: 1,85.10-5 - 1,24.10-5 = 6,1.10-6 mol
=> Nồng độ Mg2+ trong 20 mL dung dịch X là:
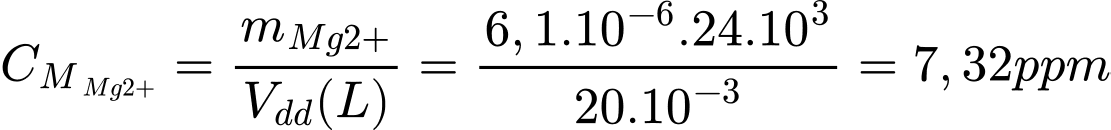
=> Nồng độ Mg2+ (ppm) trong mẫu nước khoáng ban đầu là:
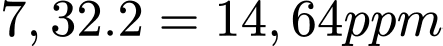
Đáp án: A. 14,64.