➔ Chọn đáp án A. Đáp án: A
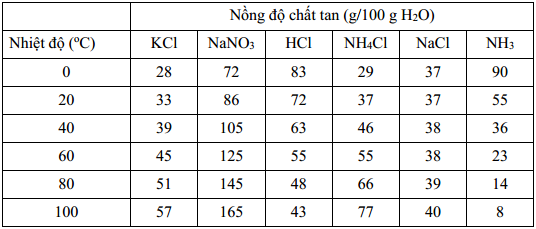
Theo bảng trên, dự đoán độ tan của HCl ở 70 oC là bao nhiêu?
Quan sát số liệu trong bảng thấy rằng khi tăng nhiệt độ từ 0 oC đến 80 oC thì độ tan của HCl giảm dần.
48 g < Độ tan của HCl ở 70 oC < 55 g => Loại A, B.
(Từ 0 oC đến 20 oC độ tan giảm 11 gam, từ 20 oC đến 40 oC giảm 9 gam, từ 40 oC đến 60 oC giảm 8 gam, từ 60 oC đến 80 oC giảm 7 gam).
Vậy đáp án phù hợp là D vì giảm 7 gam thì cứ 10 oC sẽ giảm 3,5gam. Đáp án: D
Khối
lượng dung môi là: m = 62,5 – 52,5 = 10 gam
Độ tan của của silver nitrate ở 60 oC là:
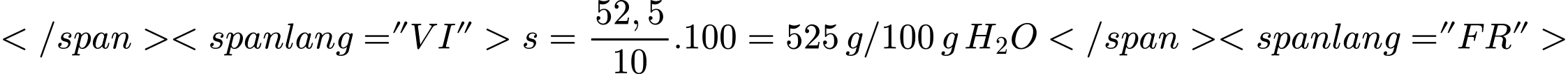
Đáp án: C. 525.
Gọi số gam chất tan
trong 200 gam dung dịch NaNO3 bão hòa ở 50oC là: a gam
Tại 50oC: 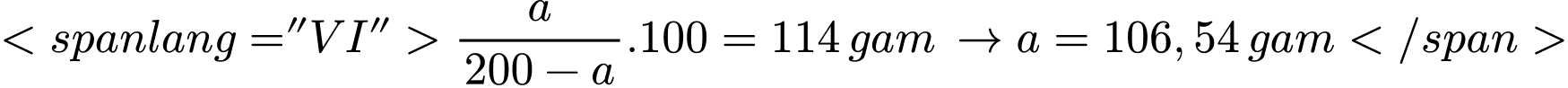
Gọi số gam chất tan
còn lại trong dung dịch tại 20 oC là: b gam
Tại 20oC: 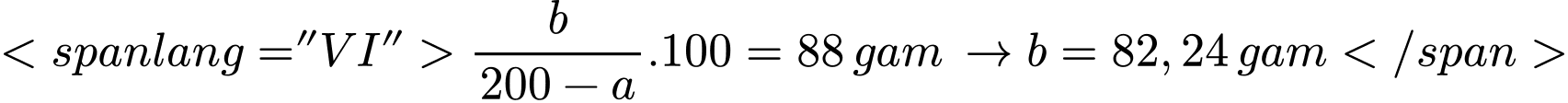
Khối lượng NaNO3 tách
ra là: 106,54 – 82,24 = 24,3 gam
Đáp án: A. 24,3.
CuO + H2SO4 → CuSO4 + H2O
Theo PTHH: nCuO = nCuSO4 = nH2SO4 =
0,2 mol
Khối lượng CuSO4 là mCuSO4 = 0,2.160 = 32 gam
Khối lượng dung dịch H2SO4 là mH2SO4 =
0,2.98:20% = 98 gam
Khối lượng H2O là mH2O = 98 – 0,2.98 = 78,4 gam
Gọi số mol của CuSO4. 5H2O tác ra là x mol
Ta có:
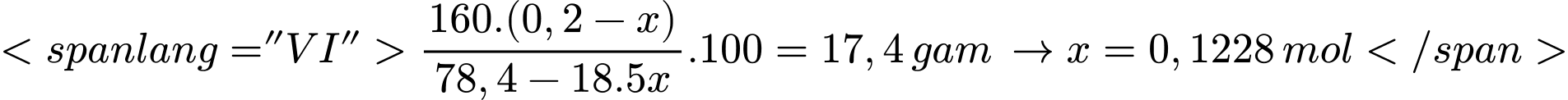
→ mCuSO5.5H2O = 0,1228.250 = 30,7 gam
Đáp án: B
mKAI(SO4)2 = 400.5,5% = 22 gam
Gọi số mol KAl(SO4)2. 12H2O tách ra là x mol
Ta có:
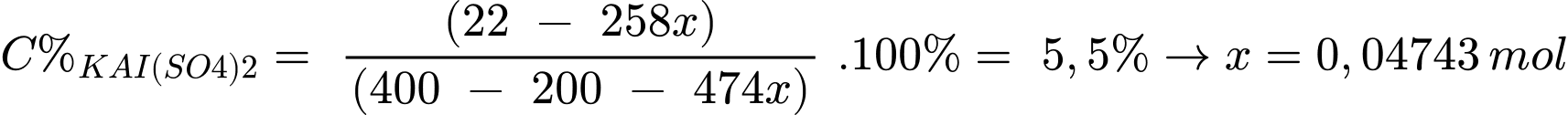
Khối lượng KAl(SO4)2. 12H2O tách ra là:
mKAl(SO4)2.12H2O = 474x = 22 ,48 gam
Đáp án: B. 22,5. Đáp án: B
Giả sử có a mol CuSO4.5H2O tách ra.
600 gam dung dịch CuSO4 10% ⇄ chứa 60 gam CuSO4.
☆ Xét ở 20oC, lúc này mdung dịch = 600 – 400 – 250a = (200 – 250a) gam.
mchất tan CuSO4 = 60 – 160a gam ⇒ C%CuSO4/dd ở 20oC = (60 – 160a) ÷ (200 – 250a) × 100% = 20%.
⇒ Giải ra a = 2/11 mol ⇒ mCuSO4.5H2O tách ra = 250a ≈ 45,45 gam. Đáp án: A
Nghĩa là 164,2 gam dung dịch bão hoà thì chứa 64,2 gam MgSO4.
⇒ 1642 gam dung dịch bão hoà chứa 642 gam MgSO4.
Giảm nhiệt độ từ 80oC xuống 20oC giả sử tách ra a mol MgSO4.6H2O.
Khi đó, phần dung dịch còn lại gồm (642 – 120a) gam MgSO4 và (1000 – 108a) gam H2O.
Độ tan lúc này ở 20oC là 100 gam H2O hoà tan 44,5 gam MgSO4
⇒ Tỉ lệ: (642 – 120a) ÷ (1000 – 108a) = 44,5 ÷ 100 ⇒ a ≈ 2,738 mol.
⇒ Yêu cầu m = 228a ≈ 624 gam. ⇝ Chọn đáp án D. ♠ Đáp án: D
Vừa đủ nên nH2SO4 = nCuO = 0,2 mol.
⇒ mdung dịch H2SO4 20% = 0,2 × 98 ÷ 0,2 = 98 gam.
Lại có mCuSO4 = 0,2 × 160 = 32 gam
và mdung dịch sau phản ứng = 0,2 × 80 + 98 = 114 gam.
Tương ứng gồm 32 gam chất tan CuSO4 và 82 gam nước.
Ở 10oC, cứ 100 gam H2O hoà tan tối đa 17,4 gam CuSO4 (1).
Giả sử có a mol CuSO4.5H2O tách ra thì dung dịch lúc này:
gồm (32 – 160a) gam CuSO4 và (82 – 90a) gam H2O (2).
Từ (1) và (2) có tỉ lệ: 17,4 × (82 – 90a) = 100 × (32 – 160a) ⇒ a ≈ 0,12285 mol
⇒ Yêu cầu mCuSO4.5H2O tách ra = 250a ≈ 30,71 gam. Đáp án: A
Giả thiết nAl2O3 = 27,54 ÷ 102 = 0,27 mol ⇒ nAl(NO3)3 = 0,54 mol.
⇒ 267,5 gam dung dịch X gồm 115,02 gam Al(NO3)3 + 152,48 gam H2O.
Giả sử có a mol Al(NO3)3.9H2O tách ra khi làm lạnh X về 20oC ⇒ m = 375a.
Dung dịch thu được gồm (115,02 – 213a) gam Al(NO3)3 và (152,48 – 162a) gam H2O.
Mà ở 10°C, cứ 100 gam H2O hòa tan được tối đa 67,25 gam Al(NO3)3
⇒ Tỉ lệ (115,02 – 213a) ÷ (152,48 – 162a) = 67,25 ÷ 100 ⇒ a ≈ 0,12 ⇒ m ≈ 45. Đáp án: D
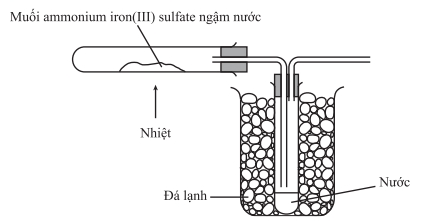
Muối ngậm nước bị phân hủy khi đun nóng nhẹ.
Phương trình phản ứng:
(NH4)2SO4.Fe2(SO4)3.xH2O → (NH4)2SO4.Fe2(SO4)3 + xH2O
Kết quả thí nghiệm thu được như sau:
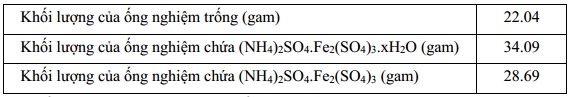
Giá trị x cần tìm trong công thức của muối ngậm nước là bao nhiêu?
Khối lượng của (NH4)2SO4. Fe2(SO4)3
là
m = 28,69 – 22,04 = 6,65 gam
Khối lượng nước tách ra là:
mH2O = 34,09 – 28,69 = 5,4 gam
Giá trị x cần tìm trong công thức của muối ngậm nước là
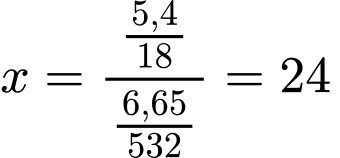
Đáp án: D
Theo đó ne trao đổi = 0,175 × 2 = 0,35 mol
⇒ Tỉ lệ 9,8 ÷ 0,35 = 28 = 56 ÷ 2 ⇝ cho biết kim loại là Fe.
Khối lượng muối FeSO4 thu được là 0,175 × 152 = 26,6 gam < 54,95 gam
⇝ Y là muối ngậm nước ⇒ nH2O = (54,95 – 26,6) ÷ 18 = 1,575 = 9 × 0,175
⇒ Muối Y là FeSO4.9H2O tương ứng %mO trong Y ≈ 66,24%. Đáp án: B
sp khí + 200 gam dung dịch NaOH → mdung dịch thu được = 206,48 gam.
Giả thiết cho 0,06 mol NaOH → 5,1 gam muối natri.
• Nếu muối dạng NaR ⇒ nNaR = 0,06 mol ⇒ R = 62 tương ứng là gốc NO3–.
• Nếu muối dạng NaaR thì bạn đọc không tìm được gốc R tương ứng ⇝ loại.
Theo đó, spk khí chứa NO2 và O2 vừa đủ theo đúng tỉ lệ 4 : 1 để:
4NO2 + 1O2 + 2H2O → 4HNO3
HNO3 + NaOH → NaNO3 + H2O.
Có 0,06 mol NaOH nên sp khí gồm 0,06 mol NO2 + 0,015 mol O2 và còn lại là 0,18 mol H2O.
Quay lại phản ứng nhiệt phân: 4M(NO3)n ––to→ 2M2On + 4nNO2 + nO2.
⇒ 1,6 gam oxit gồm 0,03 mol O và 1,12 gam M ⇒ tỉ lệ M ÷ n = 1,12 ÷ (0,03 × 2) = 56/3
⇝ cho biết M = 56; n = 3 là kim loại Fe ⇝ công thức muối A là Fe(NO3)3.9H2O.
⇝ Yêu cầu %mO trong A = 16 × 18 ÷ 404 ≈ 71,29% ⇝ Chọn đáp án C. ♣ Đáp án: C
Thực hiện: 6,8 ÷ 0,08 = 85 = 23 + 62 ⇒ cho biết muối là NaNO3.
Theo đó Y gồm hơi H2O và khí NO2 + O2 với đúng tỉ lệ 4 : 1 để sau đó:
4NO2 + O2 + 2H2O → 4HNO3.
NaOH + HNO3 → NaNO3 + H2O.
► Phân tích: muối dạng M(NO3)n ⇒ oxit dạng M2On: khối lượng 3,24 gam.
Mà nO trong oxit = ½nNO3 = 0,04 mol ⇒ mM = 2,6.
Ta có M ÷ n = 2,6 ÷ (0,04 × 2) = 65/2 cho biết M là kim loại kẽm (Zn); hóa trị II.
⇒ 11,88 gam X dạng Zn(NO3)2.nH2O với số mol 0,04 ⇒ n = 6.
Vậy, X là Zn(NO3)2.6H2O ⇝ yêu cầu %mO trong X ≈ 64,65%. Đáp án: B
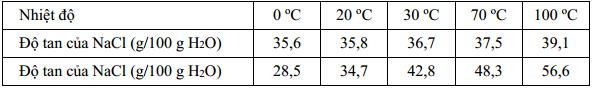
Một sinh viên tiến hành hòa tan hoàn toàn 100 gam quặng vào 130 gam nước ở 100 oC, sau đó đem làm lạnh dung dịch tới 20 oC thì thấy tách ra m gam chất rắn. Giá trị của m tính theo lí thuyết là
Ở 0°C thì khối lượng KCl tan trong 130 gam nước là: mKCl tan = 28,5.130/100 = 37,05 gam.
→ mKCl tách ra = 56 – 37,05 = 18,95 gam.
Vậy m gần nhất với số nguyên 19.
=> Chọn A. Đáp án: A
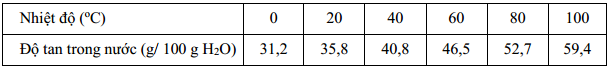
Tiến hành làm lạnh 200 gam dung dịch BaCl2 bão hòa từ 100 oC xuống 20 oC. Xác định công thức chất rắn tách ra biết phần dung dịch còn lại ở 20 oC có khối lượng 163 gam.
Độ tan (ký hiệu là S) của một chất trong nước là số gam chất đó hòa tan trong 100 gam nước để tạo thành dung dịch bão hòa ở một nhiệt độ xác định.
Ta thấy ở 100 oC, độ tan của BaCl2 là 59,4 gam
C% của dung dịch bão hòa =
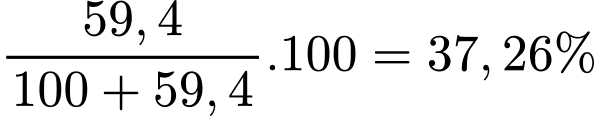
Khối lượng BaCl2 =
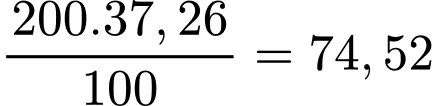 (gam)
(gam) Ở 20 oC, độ tan của BaCl2 là 35,8 gam
C% của dung dịch bão hòa =
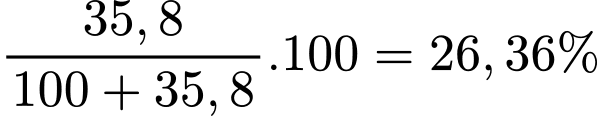
Tiến hành làm lạnh 200 gam dung dịch BaCl2 bão hòa từ 100 oC xuống 20 oC
Khối lượng chất rắn tách ra = 200 – 163 = 37 (gam)
Khối lượng BaCl2 kết tinh = a
Tại 20 oC, khối lượng BaCl2 = 74,52 - a
C% của dung dịch bão hòa =
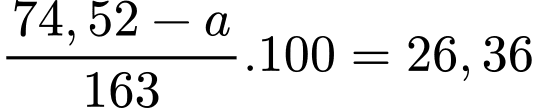 => a = 31,5 gam=> n BaCl2 = 63/416 mol.
=> a = 31,5 gam=> n BaCl2 = 63/416 mol.khối lượng nước tách ra = 37 – 31,5 = 5,5 gam => số phân tử H2O =
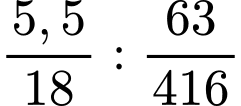 =2
=2=> Công thức chất rắn BaCl2.2H2O. Đáp án: C
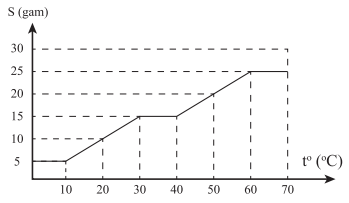
Nếu hạ nhiệt độ của 170 gam dung dịch bão hòa từ 70 oC xuống còn 30 oC thì có bao nhiêu gam chất rắn X (khan) tách ra khỏi dung dịch?
Độ tan (ký hiệu là S) của một chất trong nước là số gam chất đó hòa tan trong 100 gam nước để tạo thành dung dịch bão hòa ở một nhiệt độ xác định.
Ta thấy ở 70 oC, độ tan của X là 25 gam
C% của dung dịch bão hòa =
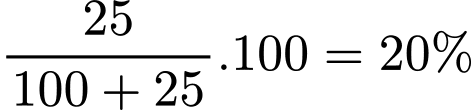
Khối lượng X =
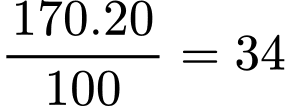 (gam)
(gam)Ở 30 oC, độ tan của X là 15 gam
C% của dung dịch bão hòa =
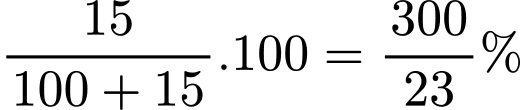 Sau khi hạ nhiệt độ của 170 gam dung dịch bão hòa từ 70 oC xuống còn 30 oC thì:Khối lượng X kết tinh = a (gam)
Sau khi hạ nhiệt độ của 170 gam dung dịch bão hòa từ 70 oC xuống còn 30 oC thì:Khối lượng X kết tinh = a (gam)Tại 30 oC, khối lượng X = 34 – a
Khối lượng dung dịch = 170 – a
C% của dung dịch bão hòa =
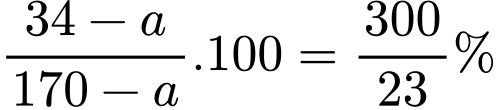 => a= 13,6 gam. Đáp án: A
=> a= 13,6 gam. Đáp án: A 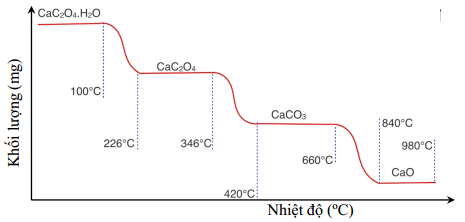
Phần trăm khối lượng chất rắn còn lại so với ban đầu tại nhiệt độ 840 oC là
Các phản ứng khi nung:
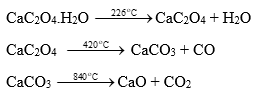
Tại 840 oC chỉ còn lại CaO: 1 mol (có thể tính theo phương trình, hoặc bảo toàn nguyên tố Ca thấy rằng = 1 mol).
%mchẩt rắn còn lại =
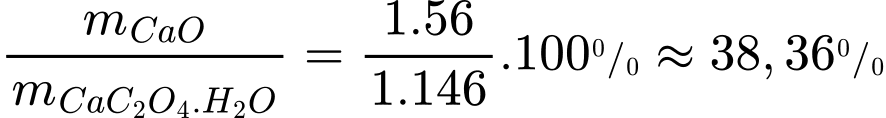
Đáp án đúng là B Đáp án: B
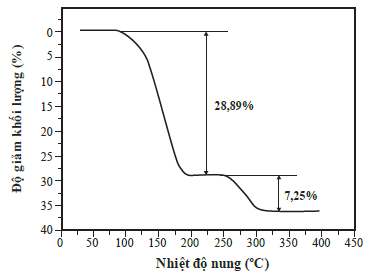
Thành phần gần nhất của chất rắn sau khi nhiệt độ đạt đến 325oC là
Khi nhiệt độ đạt đến 200°C thì độ giảm khối lượng là 28,89%.
Gọi công thức chất rắn khi đó là CuSO4.nH2O
160 + 18n = 250.(100% - 28,89%)
n = 0,9875 ≈ 1.
Vậy thành phần gần nhất của chất rắn sau khi nhiệt độ đạt đến 200°C là CuSO4.H2O. Đáp án: A
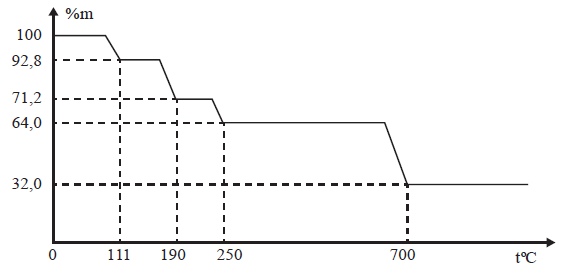
Thành phần gần nhất của chất rắn sau khi nhiệt độ đạt đến 190 oC là
Khi nhiệt độ đạt đến 190°C thì độ giảm khối lượng là 100 – 71,2 = 28,8%
Gọi công thức chất rắn khi đó là CuSO4.nH2O
160 + 18n = 250.(100% - 28,8%)
n = 0,98 ≈ 1.
Vậy thành phần gần nhất của chất rắn sau khi nhiệt độ đạt đến 190°C là CuSO4.H2O. Đáp án: B
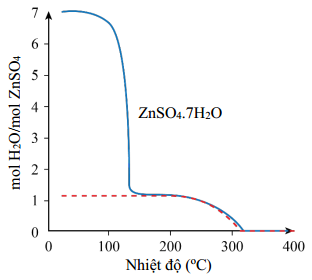
Gọi số mol của
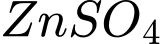 là 1 mol
là 1 molBan đầu có
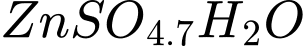
Tại
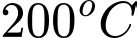 tỉ lệ mol
tỉ lệ mol 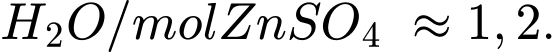
Phần trăm khối lượng chất rắn còn lại so với ban đầu tại nhiệt độ
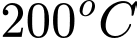 là
là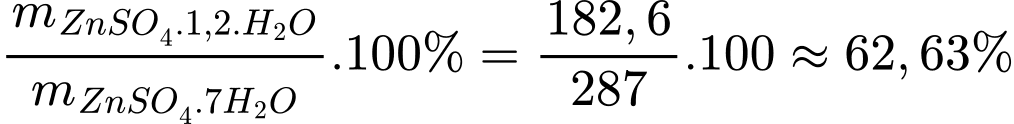
=> gần nhất với đáp án A Đáp án: A
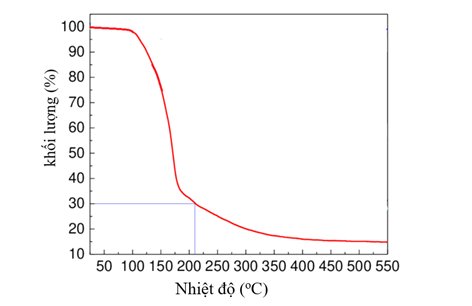
Biết rằng, khi nâng nhiệt độ, H2O tách ra trước, sau đó đến phản ứng nhiệt phân muối khan. Tại nhiệt độ 210°C, phần rắn còn lại (chứa ba nguyên tố) chiếm 30% theo khối lượng so với ban đầu. Thành phần % theo khối lượng của oxi có trong phần chất rắn tại 210°C là
Al(NO3)3.9H2O → Al(NO3)3 →Al2O3
Tại nhiệt độ 210°C, phần rắn còn lại (chứa ba nguyên tố) => Hỗn hợp chứa Al(NO3)3 và Al2O3 (3 nguyên tố là Al, N, O).
Coi số mol của Al(NO3)3.9H2O = 1 mol ta có:
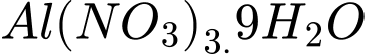

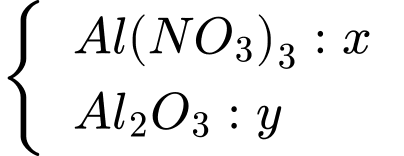 ta có
ta có 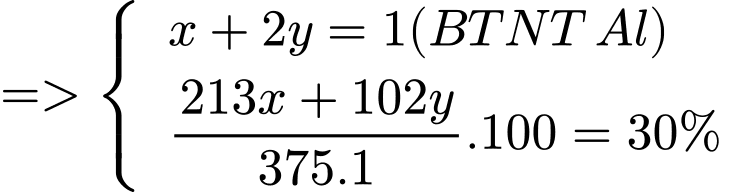
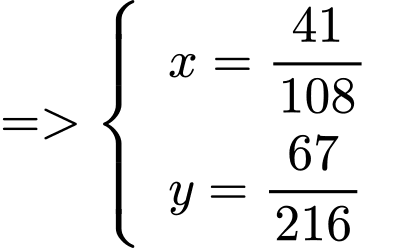
Thành phần % theo khối lượng của oxi có trong phần chất rắn tại 210°C là
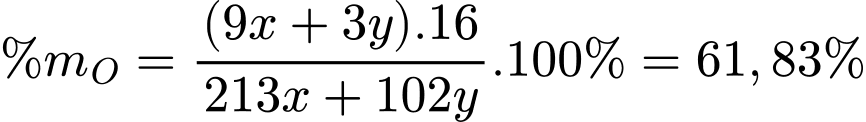
⇒ Chọn đáp án C Đáp án: C
• Bước 1: Lấy 20 gam dung dịch KOH 42% (đặc) cho vào bình nón, đặt bình trên lưới amiang rồi đun nóng, vừa đun vừa thêm thật từ từ tinh thể iodine vào khuấy thật kỹ đến khi xuất hiện màu vàng rơm nhạt thì ngừng thêm iodine.
• Bước 2: Để nguội rồi ngâm bình nón trong nước đá ở 3 oC trong vòng 15 – 20 phút để kết tinh sản phẩm. Lọc hỗn hợp trên phễu lọc để tách chất kết tinh, phần nước lọc đem cô cạn cẩn thận thì thu được chất rắn khan chứa tinh thể potassium iodide có lẫn một lượng nhỏ potassium iodate.
Biết các phản ứng xảy ra hoàn toàn, 99% potassium iodate và 2% potassium iodide (về khối lượng) bị kết tinh và được giữ lại trên phễu lọc.
Cho các phát biểu sau:
(a) Phản ứng ở bước 1 thuộc phản ứng oxi hóa khử nội phân tử.
(b) Màu vàng rơm nhạt xuất hiện ở bước 1 cho biết I2 bắt đầu dư.
(c) Tại nhiệt độ 3 oC, độ tan của potassium iodate lớn hơn potassium iodide.
(d) Độ tinh khiết (thành phần phần trăm khối lượng) của potassium iodide trong chất rắn thu được là 98,00%.
Có bao nhiêu phát biểu đúng?
- Nhân định (b) - Sai, vì:
• I₂ dư → màu nâu, không phải vàng rơm.
• Màu vàng rơm xuất hiện do sự tạo thành các ion oxyiod (IO⁻, IO₂⁻…), không phải do I₂ dư.
• Trong thí nghiệm, màu vàng rơm chỉ để báo hiệu sắp hết KOH, không phải dấu hiệu dư I₂.
- Nhận định (c) - Sai, vì:
• KI rất tan (≈ 140 g/100 g nước ở 0 °C).
• KIO₃ ít tan hơn rất nhiều (≈ 2 g/100 g nước ở 0 °C).
→ Vì vậy KIO₃ kết tinh trước
- Nhận định (d) - Sai, vì:Theo đề: trong chất rắn chỉ có 99% KIO₃ và 2% KI (tính theo khối lượng). → Thành phần KI chỉ khoảng 2%, không thể là 98%.
=> Đáp án đúng là A.1 Đáp án: A
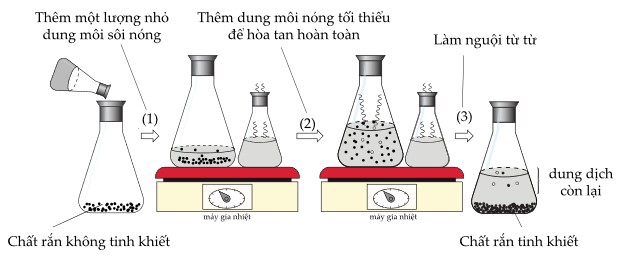
Cho các phát biểu sau:
(a) Khi để nguội, các tinh thể hình thành với độ tinh khiết cao.
(b) Các tạp chất không bị kết tinh và nằm lại trong dung dịch.
(c) Chất kết tinh có độ tan thấp khi tăng nhiệt độ và cao khi hạ nhiệt độ.
(d) Dung dịch sau kết tinh là dung dịch bão hòa của chất cần kết tinh.
Có bao nhiêu phát biểu đúng?
Nhận định (a) – Đúng. Khi dung dịch nóng dần nguội, chất cần tinh khiết
sẽ kết tinh trước, tạp chất thường vẫn ở lại trong dung dịch.
Nhận định (b) – Đúng. Đây là cơ chế chính của kết tinh: tách chất
tinh khiết ra khỏi tạp chất.
Nhận định (c) – Sai. Chất rắn thường có độ tan cao khi tăng nhiệt độ
và thấp khi hạ nhiệt độ, nhờ đó mới có thể kết tinh khi dung dịch nguội.
Nhận định (d) – Đúng. Sau khi kết tinh, dung dịch vẫn còn một lượng
nhỏ chất hòa tan → dung dịch gần bão hòa hoặc bão hòa.
Đáp án: C. 3.
100 gam H2O hòa tan 28,3 gam Na2SO4 tạo thành 128,3 gam dung dịch bão hòa
- Gọi x là số mol Na2SO4. 10H2O tách ra → Số mol H2O tách ra là 10x mol
⟹ Khối lượng H2O tách ra: 180x (g)
Khối lượng Na2SO4tách ra: 142x (gam)
- Ở 10oC, SNa2SO4= 9 gam
- Ta có phương trình:
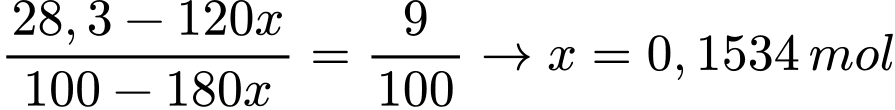
→ Khối lượng Na2SO4.10H2O kết tinh: 322.0,1534 ≈ 49,4 gam.
⟹Điền đáp án : 49,4
- Nghĩa là:100 gam H2O hòa tan 64,2 gam MgSO4 tạo thành 164,2 gam dung dịch bão hòa
a gam H2O hòa tan b gam MgSO4 tạo thành 1642 gam dung dịch bão hòa
→
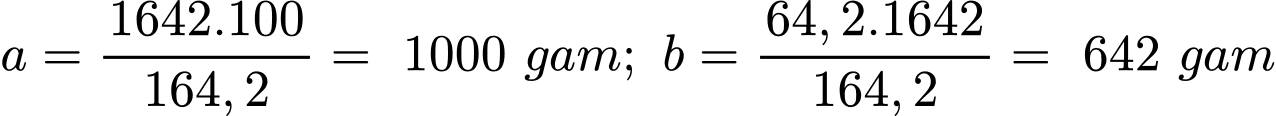
- Gọi x là số mol MgSO4.6H2O tách ra → Số mol H2O tách ra là 6x mol
⟹ Khối lượng H2O tách ra: 108x (g)
Khối lượng MgSO4 tách ra: 120x (gam)
- Ở 200C, S MgSO4= 44,5 gam
- Ta có phương trình:
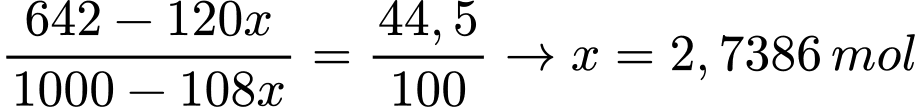
→ Khối lượng MgSO4.6H2O kết tinh: 228.2,7386 ≈ 624 gam.
⟹Điền đáp án : 624
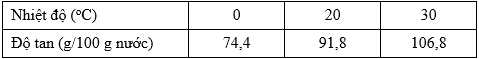
Để tạo ra dung dịch bão hoà của FeCl3 ở 20oC từ 50 g nước thì cần bao nhiêu gam FeCl3.6H2O?
Trong 50g nước độ tan của FeCl3.6H2O là :
91,8 : 2 = 45,9 (g)
Điền đáp án: 45,9
Thí nghiệm 1: Cân 3,92 gam muối Mohr rồi hòa tan vào nước, sau đó định mức trong bình 50mL. Chuẩn độ 5mL dung dịch vừa pha cần dùng 10mL dung dịch KMnO4 0,02M trong môi trường H2SO4 loãng. Xác định công thức phân tử muối Mohr.
Thí nghiệm 2: Làm lạnh 100 gam dung dịch muối Mohr bão hòa ở 30oC đến nhiệt độ ổn định ở 0oC thu được m gam muối Mohr kết tinh. Cho độ tan của muối Mohr trong nước ở các nhiệt độ như sau:

Giá trị của m là bao nhiêu?
10FeSO4 + 2KMnO4 + 8H2SO4 ⟶ 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Số mol của KMnO4 là: nKMnO4 = 0,02 × 0,01 = 2×10-4 mol
Từ phương trình số mol của FeSO4 là: nFeSO4 = 5nKMnO4 = 10-3 mol
Số mol của muối Morh trong 50 mL dung dịch là:
nMorrh = (50 ÷ 5) × 10-3 = 0,01 (mol)
Ta có: MMorh = 3,92 ÷ 10-2 = 152 + 132 + 18n ⟶ n = 6
Công thức của muối Morh là FeSO4.(NH4)2SO4.6H2O
Tại 30 oC độ tan của muối Morh là 45 gam trên 100 gam nước
Tại 30 oC khối lượng lượng muối Morh trong 100 gam dung dịch bão hòa là
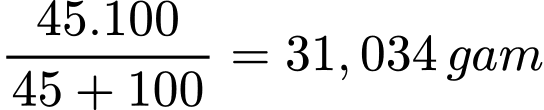
Tại 0 oC giả sử có m gam muối Mohr kết tinh thì khối lượng phần dung dịch bão hòa còn lại là (100 – m) gam.
Cứ 17,2 g muối Morh có thể tan trong 100 g nước tạo thành 117,2 g dung dịch bão hòa.
⟶ Trong (100-m) g dung dịch bão hòa chứa [17,2 × ( 100-m)] ÷ 117,2 g muối Morh.
Bảo toàn khối lượng ta có:
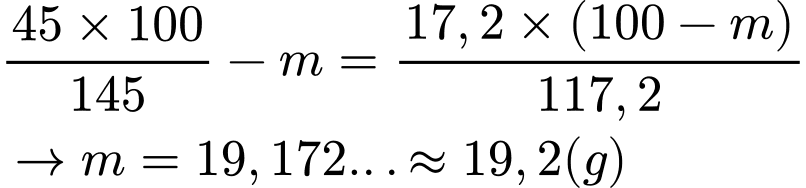
⇒ Điền đáp án: 19,2
Thí nghiệm 2: Thêm dung dịch H2SO4 (loãng, dư) vào 25 ml dung dịch Y, thu được dung dịch Z. Nhỏ từ từ dung dịch KMnO4 0,1M vào Z đến khi phản ứng vừa đủ thì hết 13,5 ml.
Xác định giá trị củaphần trăm Fe bị oxi hóa?
nH2SO4 = 0,0125 mol
nBaSO4 = 0,02 mol = nFeSO4.xH2O + nH2SO4
nFeSO4.xH2O = 0,0075 mol
TN2 : 10 FeSO4 + 2 KMnO4 + 8 H2SO4 ⟶ 5 Fe2(SO4)3 + 2 MnSO4 + K2SO4 + 8H2O
nKMnO4 phản ứng = 13,5 : 1000 × 0,1 = 1,35× 10-3mol
nFeSO4 = 6,75× 10-3 mol
Số mol Fe3+ bị oxi hóa = 0,0075 - 6,75× 10-3 = 7,5 × 10 -4mol
%Fe đã bị oxi hóa = 7,5× 10-4 : 0,0075 × 100 = 10%
⟹ Điền đáp án : 10
Mẫu I: Sơ đồ phản ứng:

Mẫu II: Ba2+ + SO42- ⟶ BaSO4
Số mol của BaSO4 là:
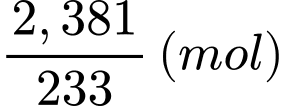
Số mol của M2(SO4)n.aH2O trong 20 mL dung dịch là:
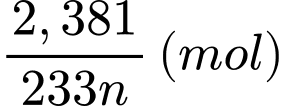
Bảo toàn nguyên tố M, số mol của M2Ox là:
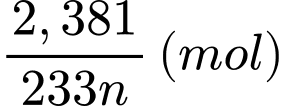
⭐ TH1: M có đa hóa trị hóa trị cố định trong hợp chất → n ≠ x
Khối lượng của M2Ox là:
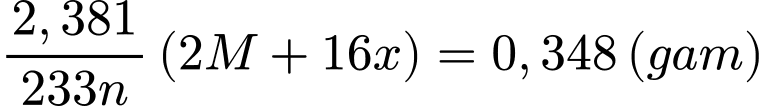
Ta có bảng sau:
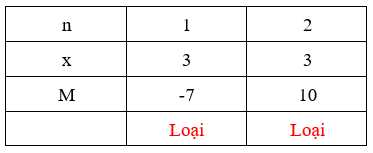
⭐ TH2: M có hóa trị cố định trong hợp chất → n = x
Khối lượng của M2Ox là
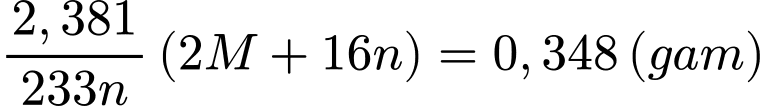
Ta có bảng sau:
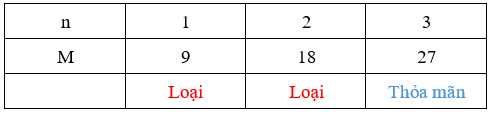
→ M là Al (aluminum)
Khối lượng muối ban đầu là
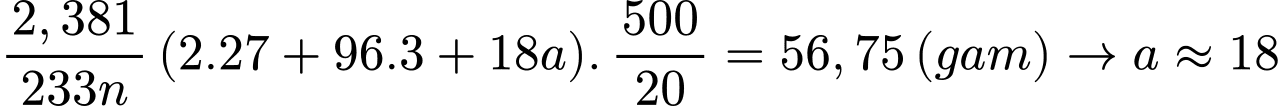
Công thức của muối là Al2(SO4)3.18H2O
Trong công thức muối ngậm nước ban đầu; cứ 1 phân tử muối sulfate kim loại thì ngậm 18 phân tử nước.
⇒ Điền đáp án: 18