Dạng 1. TRẮC NGHIỆM KHÁCH QUAN: mỗi câu hỏi chỉ có một đáp án đúng.
Câu 1 [1009748]: Cho hình vẽ thí nghiệm phân tích định tính hợp chất hữu cơ C6H12O6:
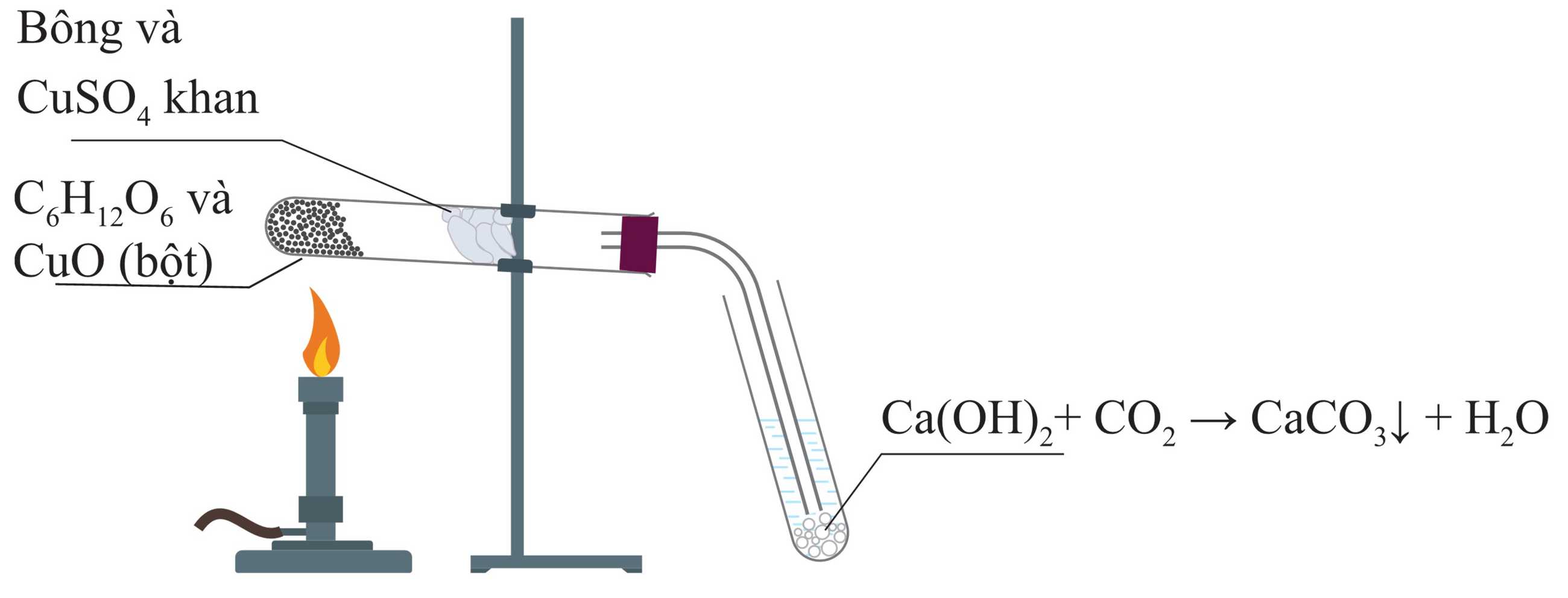
Hãy cho biết vai trò của bông và CuSO4 khan trong thí nghiệm trên?

Hãy cho biết vai trò của bông và CuSO4 khan trong thí nghiệm trên?
A, Xác định sự có mặt của O.
B, Xác định sự có mặt của C và H.
C, Xác định sự có mặt của H.
D, Xác định sự có mặt của C.
Vai trò của bông và CuSO4 khan trong thí nghiệm
⭐Bông: Ngăn hơi nước ngưng tụ chảy ngược làm vỡ ống nghiệm, đồng thời giữ các chất rắn trong ống nghiệm.
⭐CuSO4 khan màu trắng khi hấp thụ H2O sẽ tạo CuSO4.5H2O màu xanh.
⟹ Chọn đáp án C Đáp án: C
⭐Bông: Ngăn hơi nước ngưng tụ chảy ngược làm vỡ ống nghiệm, đồng thời giữ các chất rắn trong ống nghiệm.
⭐CuSO4 khan màu trắng khi hấp thụ H2O sẽ tạo CuSO4.5H2O màu xanh.
⟹ Chọn đáp án C Đáp án: C
Câu 2 [1009749]: Glucose tham gia phản ứng với Cu(OH)2/OH–, đun nóng tạo kết tủa đỏ gạch Cu2O. Trong phản ứng này chứng minh tính chất của nhóm chức nào trong phân tử glucose?
A, Tính chất của polyalcohol.
B, Tính chất của aldehyde.
C, Tính chất ketone.
D, Tính chất nhóm –OH hemiacetal.
Đun nóng dung dịch chứa glucose và Cu(OH)2 trong môi trường kiềm sẽ xuất hiện kết tủa màu đỏ gạch do Cu(OH)2 bị khử thành Cu2O. Đây chính là tính chất của nhóm -CHO trong phân tử glucose (Tính chất của aldehyde).
CH2OH[CHOH]4CHO + 2Cu(OH)2 + NaOH
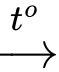
CH2OH[CHOH]4COONa + Cu2O + 3H2O.
⟹ Chọn đáp án B Đáp án: B
CH2OH[CHOH]4CHO + 2Cu(OH)2 + NaOH
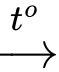
CH2OH[CHOH]4COONa + Cu2O + 3H2O.
⟹ Chọn đáp án B Đáp án: B
Câu 3 [308297]: Cho 5 giọt CuSO4 5% và 1 mL dung dịch NaOH 10% vào ống nghiệm, lắc nhẹ. Gạn bỏ lớp dung dịch, sau đó thêm vào 2 mL glucose 1% lắc nhẹ. Hiện tượng quan sát được là
A, Có kết tủa đỏ gạch.
B, Cu(OH)2 tan tạo dung dịch, màu xanh.
C, Cu(OH)2 bị khử tạo Cu màu đỏ.
D, Cu(OH)2 tan tạo dung dịch trong suốt.
HD: Phân tích thí nghiệm:
• Tạo kết tủa Cu(OH)2 màu xanh lam:
CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4.
2.png)
• Gạn bỏ dung dịch, kết tủa Cu(OH)2 sau đó bị hòa tan bởi glucose thêm vào:
2C6H12O6 (glucose) + Cu(OH)2 → Cu(C6H11O6)2 (phức chất màu xanh) + 2H2O.

⇝ Chọn đáp án B. ♦ Đáp án: B
• Tạo kết tủa Cu(OH)2 màu xanh lam:
CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4.
2.png)
• Gạn bỏ dung dịch, kết tủa Cu(OH)2 sau đó bị hòa tan bởi glucose thêm vào:
2C6H12O6 (glucose) + Cu(OH)2 → Cu(C6H11O6)2 (phức chất màu xanh) + 2H2O.

⇝ Chọn đáp án B. ♦ Đáp án: B
Câu 4 [308298]: Để chứng minh trong phân tử của glucose có nhiều nhóm hydroxy, người ta cho dung dịch glucose phản ứng với
A, Kim loại Na.
B, Cu(OH)2 ở nhiệt độ thường.
C, AgNO3 (hoặc Ag2O) trong dung dịch NH3, đun nóng.
D, Cu(OH)2 trong NaOH, đun nóng.
Phân tích các đáp án:
❌ A. với kim loại Na: chỉ cần 1 nhóm OH + Na → ONa + ½H2↑ nên không chứng minh nó có nhiều nhóm được.
✔️ B. Cu(OH)2 ở nhiệt độ thường tạo dung dịch màu xanh lam đặc trưng thì yêu cầu cần có ít nhất 2 nhóm OH liền kề.
❌ C. AgNO3/NH3: thuốc thử Tollens - chứng minh nhóm chức aldehyde CHO bằng kết tủa Ag trắng bạc.
❌ D. Cu(OH)2 đun nóng tạo kết tủa Cu2O màu đỏ gạch cũng chứng minh nhóm chức CHO.
⟹ Chọn đáp án B Đáp án: B
❌ A. với kim loại Na: chỉ cần 1 nhóm OH + Na → ONa + ½H2↑ nên không chứng minh nó có nhiều nhóm được.
✔️ B. Cu(OH)2 ở nhiệt độ thường tạo dung dịch màu xanh lam đặc trưng thì yêu cầu cần có ít nhất 2 nhóm OH liền kề.
❌ C. AgNO3/NH3: thuốc thử Tollens - chứng minh nhóm chức aldehyde CHO bằng kết tủa Ag trắng bạc.
❌ D. Cu(OH)2 đun nóng tạo kết tủa Cu2O màu đỏ gạch cũng chứng minh nhóm chức CHO.
⟹ Chọn đáp án B Đáp án: B
Câu 5 [1009750]: Thí nghiệm nào sau đây chứng tỏ trong phân tử glucose có 5 nhóm hydroxyl?
A, Khử hoàn toàn glucose thành hexane.
B, Cho glucose tác dụng với Cu(OH)2.
C, Tiến hành phản ứng tạo ester của glucose với anhydride acetic.
D, Thực hiện phản ứng tráng bạc.
Phân tích các phát biểu:
❌A. Khử hoàn toàn gluose thành hexane ⟶ Thí nghiệm chứng tỏ glucose có 6 nguyên tử Carbon tạo thành một mạch không nhánh.
❌B. Cho glucose tác dụng với Cu(OH)2 ⟶ Thí nghiệm chứng tỏ glucose tạo thành phức chất màu xanh lam, tan trong nước chứng tỏ phân tử glucose có nhiều nhóm OH liền kề nhau..
✔️C. Tiến hành phản ứng tạo ester của glucose với anhydride acetic ⟶ Thí nghiệm chứng tỏ trong phân tử glucose có 5 nhóm hydroxyl.
❌D. Thực hiện phản ứng tráng bạc ⟶ Thí nghiệm chứng tỏ phân tử glucose có chứa nhóm chức CH=O.
⟹ Chọn đáp án C Đáp án: C
❌A. Khử hoàn toàn gluose thành hexane ⟶ Thí nghiệm chứng tỏ glucose có 6 nguyên tử Carbon tạo thành một mạch không nhánh.
❌B. Cho glucose tác dụng với Cu(OH)2 ⟶ Thí nghiệm chứng tỏ glucose tạo thành phức chất màu xanh lam, tan trong nước chứng tỏ phân tử glucose có nhiều nhóm OH liền kề nhau..
✔️C. Tiến hành phản ứng tạo ester của glucose với anhydride acetic ⟶ Thí nghiệm chứng tỏ trong phân tử glucose có 5 nhóm hydroxyl.
❌D. Thực hiện phản ứng tráng bạc ⟶ Thí nghiệm chứng tỏ phân tử glucose có chứa nhóm chức CH=O.
⟹ Chọn đáp án C Đáp án: C
Câu 6 [308299]: Tiến hành thí nghiệm theo các bước sau:
Bước 1: Cho 5 giọt dung dịch CuSO4 0,5% vào ống nghiệm sạch.
Bước 2: Thêm 1 mL dung dịch NaOH 10% vào ống nghiệm 1 mL dung dịch NaOH 10% vào ống nghiệm, lắc đều; gạn phần dung dịch, giữ lại kết tủa.
Bước 3: Thêm tiếp 2 mL dung dịch glucose 1% vào ống nghiệm, lắc đều.
Phát biểu nào sau đây sai?
Bước 1: Cho 5 giọt dung dịch CuSO4 0,5% vào ống nghiệm sạch.
Bước 2: Thêm 1 mL dung dịch NaOH 10% vào ống nghiệm 1 mL dung dịch NaOH 10% vào ống nghiệm, lắc đều; gạn phần dung dịch, giữ lại kết tủa.
Bước 3: Thêm tiếp 2 mL dung dịch glucose 1% vào ống nghiệm, lắc đều.
Phát biểu nào sau đây sai?
A, Sau bước 3, kết tủa đã bị hòa tan, thu được dung dịch màu xanh lam.
B, Nếu thay dung dịch NaOH ở bước 2 bằng dung dịch KOH thì hiện tượng ở bước 3 vẫn tương tự.
C, Thí nghiệm trên chứng minh glucose có tính chất của aldehyde.
D, Ở bước 3, nếu thay glucose bằng fructose thì hiện tượng xảy ra vẫn tương tự.
HD: Phân tích thí nghiệm:
• Tạo kết tủa Cu(OH)2 màu xanh lam:
CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4.
2.png)
• Gạn bỏ dung dịch, kết tủa Cu(OH)2 sau đó bị hòa tan bởi glucose thêm vào:
2C6H12O6 (glucose) + Cu(OH)2 → Cu(C6H11O6)2 (phức chất màu xanh) + 2H2O.

⇒ Phân tích các phát biểu:
✔️ A. đúng theo phân tích trên, phức đồng - glucose tan có màu xanh lam.
✔️ B. đúng, vai trò NaOH và KOH là đều cung cấp OH– cho việc tạo Cu(OH)2.
❌ C. sai. thí nghiệm chứng minh nhiều nhóm OH chứ không chứng minh glucose có nhóm chức aldehyde.
✔️ D. đúng vì cấu tạo cùa fructose cũng chứa nhiều nhóm OH (tính chất của polyalcohol). Đáp án: C
• Tạo kết tủa Cu(OH)2 màu xanh lam:
CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4.
2.png)
• Gạn bỏ dung dịch, kết tủa Cu(OH)2 sau đó bị hòa tan bởi glucose thêm vào:
2C6H12O6 (glucose) + Cu(OH)2 → Cu(C6H11O6)2 (phức chất màu xanh) + 2H2O.

⇒ Phân tích các phát biểu:
✔️ A. đúng theo phân tích trên, phức đồng - glucose tan có màu xanh lam.
✔️ B. đúng, vai trò NaOH và KOH là đều cung cấp OH– cho việc tạo Cu(OH)2.
❌ C. sai. thí nghiệm chứng minh nhiều nhóm OH chứ không chứng minh glucose có nhóm chức aldehyde.
✔️ D. đúng vì cấu tạo cùa fructose cũng chứa nhiều nhóm OH (tính chất của polyalcohol). Đáp án: C
Câu 7 [1009751]: Fructose không phản ứng được với chất nào sau đây?
A, Cu(OH)2 ở nhiệt độ thường.
B, Nước bromine.
C, Cu(OH)2 ở nhiệt độ cao.
D, Dung dịch AgNO3/NH3, to.
Phân tích các phát biểu:
✔️A. Fructose tác dụng với Cu(OH)2 ở nhiệt độ thường tạo phức màu xanh làm, tan trong nước.
2C6H12O6 + Cu(OH)2 ⟶ Cu(C6H11O6)2 + 2H2O.
❌B. Fructose không làm mất màu nước bromine.
✔️C. Fructose tác dụng với Cu(OH)2 ở nhiệt độ cao tạo thành kết tủa đỏ gạch Cu2O.
✔️D. Fructose tác dụng với dung dịch AgNO3/NH3, to tạo thành kết tủa bạc kim loại ( phản ứng tráng bạc)
C6H12O6 + 2AgNO3 + 3NH3 + H2O ⟶ CH2OH(CHOH)4COONH4 + 2Ag + 2NH4NO3.
⟹ Chọn đáp án B Đáp án: B
✔️A. Fructose tác dụng với Cu(OH)2 ở nhiệt độ thường tạo phức màu xanh làm, tan trong nước.
2C6H12O6 + Cu(OH)2 ⟶ Cu(C6H11O6)2 + 2H2O.
❌B. Fructose không làm mất màu nước bromine.
✔️C. Fructose tác dụng với Cu(OH)2 ở nhiệt độ cao tạo thành kết tủa đỏ gạch Cu2O.
✔️D. Fructose tác dụng với dung dịch AgNO3/NH3, to tạo thành kết tủa bạc kim loại ( phản ứng tráng bạc)
C6H12O6 + 2AgNO3 + 3NH3 + H2O ⟶ CH2OH(CHOH)4COONH4 + 2Ag + 2NH4NO3.
⟹ Chọn đáp án B Đáp án: B
Câu 8 [308301]: Chất tham gia phản ứng tráng gương là
A, Cellulose.
B, Tinh bột.
C, Saccharose.
D, Fructose.
HD: Phân tích: phản ứng tráng gương có sự tham gia của thuốc thử Tollens: dung dịch của AgNO3 kết hợp với NH3 tạo thành phức chất [Ag(NH3)2]OH. Do môi trường có hoà tan một phần NH3 và NH3 sẽ kết hợp với nước để tạo ra ion OH– ⇝ môi trường lúc này có tính base ⇒ Trong môi trường base, fructose và glucose sẽ có sự chuyển hoá qua lại: fructose ⇄OH–⇄ glucose.
Kết quả là trong ống nghiệm đựng fructose, một phần fructose chuyển thành glucose và sẽ tham gia phản ứng với thuốc thử Tollens cho hiện tượng xuất hiện kết tủa kim loại Ag giống hệt như ống nghiệm đựng glucose ⇒ Fructose có khả năng tham gia phản ứng tráng gương ⇝ Chọn đáp án D. ♠ Đáp án: D
Kết quả là trong ống nghiệm đựng fructose, một phần fructose chuyển thành glucose và sẽ tham gia phản ứng với thuốc thử Tollens cho hiện tượng xuất hiện kết tủa kim loại Ag giống hệt như ống nghiệm đựng glucose ⇒ Fructose có khả năng tham gia phản ứng tráng gương ⇝ Chọn đáp án D. ♠ Đáp án: D
Câu 9 [308303]: Trong chế tạo lớp bạc trong ruột phích người ta thường dùng phương pháp nào sau đây:
A, Cho acetylene tác dụng với dung dịch AgNO3/NH3.
B, Cho formaldehyde tác dụng với dung dịch AgNO3/NH3.
C, Cho formic acid tác dụng với dung dịch AgNO3/NH3.
D, Cho glucose tác dụng với dung dịch AgNO3/NH3.
HD: Phân tích các phương án:
❌ A. không thỏa mãn vì acetylene CH≡CH có phản ứng với AgNO3/NH3 nhưng không tạo ra Ag, không tráng được Ag cho ruột phích:
HC≡CH + 2AgNO3 + 2NH3 → AgC≡CAg↓ (màu vàng nhạt) + 2NH4NO3.
❌ B. formaldehyde: HCHO và ❌ C. formic acid: HCOOH đều có phản ứng tráng bạc với AgNO3/NH3 tuy nhiên các phản ứng này xảy ra với tốc độ cao, lại thêm HCHO và HCOOH độc nên trong chế tạo thực tế, người ta không sử dụng chúng.
✔️ D. thỏa mãn, vì glucose an toàn, tốc độ phản ứng diễn ra chậm nên giúp ta dễ dàng kiểm soát để tráng 1 lớp bạc đều và đẹp. Đáp án: D
❌ A. không thỏa mãn vì acetylene CH≡CH có phản ứng với AgNO3/NH3 nhưng không tạo ra Ag, không tráng được Ag cho ruột phích:
HC≡CH + 2AgNO3 + 2NH3 → AgC≡CAg↓ (màu vàng nhạt) + 2NH4NO3.
❌ B. formaldehyde: HCHO và ❌ C. formic acid: HCOOH đều có phản ứng tráng bạc với AgNO3/NH3 tuy nhiên các phản ứng này xảy ra với tốc độ cao, lại thêm HCHO và HCOOH độc nên trong chế tạo thực tế, người ta không sử dụng chúng.
✔️ D. thỏa mãn, vì glucose an toàn, tốc độ phản ứng diễn ra chậm nên giúp ta dễ dàng kiểm soát để tráng 1 lớp bạc đều và đẹp. Đáp án: D
Câu 10 [308304]: Tiến hành thí nghiệm theo các bước sau:
Bước 1: Cho 1 mL dung dịch AgNO3 1% vào ống nghiệm sạch.
Bước 2: Thêm từ từ từng giọt dung dịch NH3, lắc đều cho đến khi kết tủa tan hết.
Bước 3: Thêm tiếp khoảng 1 mL dung dịch glucose 1% vào ống nghiệm; đun nóng nhẹ.
Phát biểu nào sau đây sai?
Bước 1: Cho 1 mL dung dịch AgNO3 1% vào ống nghiệm sạch.
Bước 2: Thêm từ từ từng giọt dung dịch NH3, lắc đều cho đến khi kết tủa tan hết.
Bước 3: Thêm tiếp khoảng 1 mL dung dịch glucose 1% vào ống nghiệm; đun nóng nhẹ.
Phát biểu nào sau đây sai?
A, Sản phẩm hữu cơ thu được sau bước 3 là ammonium gluconate.
B, Thí nghiệm trên chứng minh glucose có tính chất của polyalcohol.
C, Sau bước 3, có lớp bạc kim loại bám trên thành ống nghiệm.
D, Trong phản ứng ở bước 3, glucose đóng vai trò là chất khử.
HD: Phân tích thí nghiệm:
• Sau bước 2: Ống nghiệm xuất hiện kết tủa AgOH màu trắng.
NH3 + H2O ⇄ NH4+ + OH–.
Ag+ + OH– → AgOH↓.
Tiếp tục nhỏ NH3 vào thì kết tủa tan do tạo thành phức chất [Ag(NH3)2]OH.
AgOH + 2NH3 → [Ag(NH3)2]OH.
• Sau bước 3: Ống nghiệm xuất hiện một lớp kim loại bạc bám trên bề mặt của ống nghiệm.
CH2OH[CHOH]4CHO + [Ag(NH3)2]OH → CH2OH[CHOH]4COONH4 + 2Ag↓ + 3NH3 + H2O.
⇒ Phân tích các phát biểu:
✔️ A. đúng. CH2OH[CHOH]4COONH4 có tên là ammonium gluconate.
❌ B. sai. Thí nghiệm chứng minh tính chất của nhóm chức aldehyde CHO.
✔️ C. đúng theo phân tích trên.
✔️ D. đúng. Mẹo nhỏ: AgNO3 → Ag nên AgNO3 thể hiện tính oxy hóa ⇒ glucose thể hiện tính khử là đúng.
⟹ Chọn đáp án B Đáp án: B
• Sau bước 2: Ống nghiệm xuất hiện kết tủa AgOH màu trắng.
NH3 + H2O ⇄ NH4+ + OH–.
Ag+ + OH– → AgOH↓.
Tiếp tục nhỏ NH3 vào thì kết tủa tan do tạo thành phức chất [Ag(NH3)2]OH.
AgOH + 2NH3 → [Ag(NH3)2]OH.
• Sau bước 3: Ống nghiệm xuất hiện một lớp kim loại bạc bám trên bề mặt của ống nghiệm.
CH2OH[CHOH]4CHO + [Ag(NH3)2]OH → CH2OH[CHOH]4COONH4 + 2Ag↓ + 3NH3 + H2O.
⇒ Phân tích các phát biểu:
✔️ A. đúng. CH2OH[CHOH]4COONH4 có tên là ammonium gluconate.
❌ B. sai. Thí nghiệm chứng minh tính chất của nhóm chức aldehyde CHO.
✔️ C. đúng theo phân tích trên.
✔️ D. đúng. Mẹo nhỏ: AgNO3 → Ag nên AgNO3 thể hiện tính oxy hóa ⇒ glucose thể hiện tính khử là đúng.
⟹ Chọn đáp án B Đáp án: B
Câu 11 [1009752]: Tinh thể chất rắn X không màu, vị ngọt, dễ tan trong nước. X có nhiều trong quả nho chín nên còn gọi là đường nho. Khử chất X bằng H2 thu được chất hữu cơ Y. Tên gọi của X và Y lần lượt là
A, saccharose và fructose.
B, fructose và sobitol.
C, glucose và sobitol.
D, saccharose và glucose.
Tinh thể chất rắn X không màu, vị ngọt, dễ tan trong nước. X có nhiều trong quả nho chín nên còn gọi là đường nho.
⟶ X là glucose
Khử glucose bằng H2 thu được sobitol
C6H12O6 + H2 ⟶ C6H14O6
⟶ Vây Y là sobitol
Tên gọi của X và Y lần lượt là glucose và sobitol.
⟹ Chọn đáp án C
Đáp án: C
⟶ X là glucose
Khử glucose bằng H2 thu được sobitol
C6H12O6 + H2 ⟶ C6H14O6
⟶ Vây Y là sobitol
Tên gọi của X và Y lần lượt là glucose và sobitol.
⟹ Chọn đáp án C
Đáp án: C
Câu 12 [1009753]: Cho phản ứng chuyển hóa như hình bên. Tác nhân (A) thích hợp cho phản ứng đó là (xem như điều kiện phản ứng có đủ)
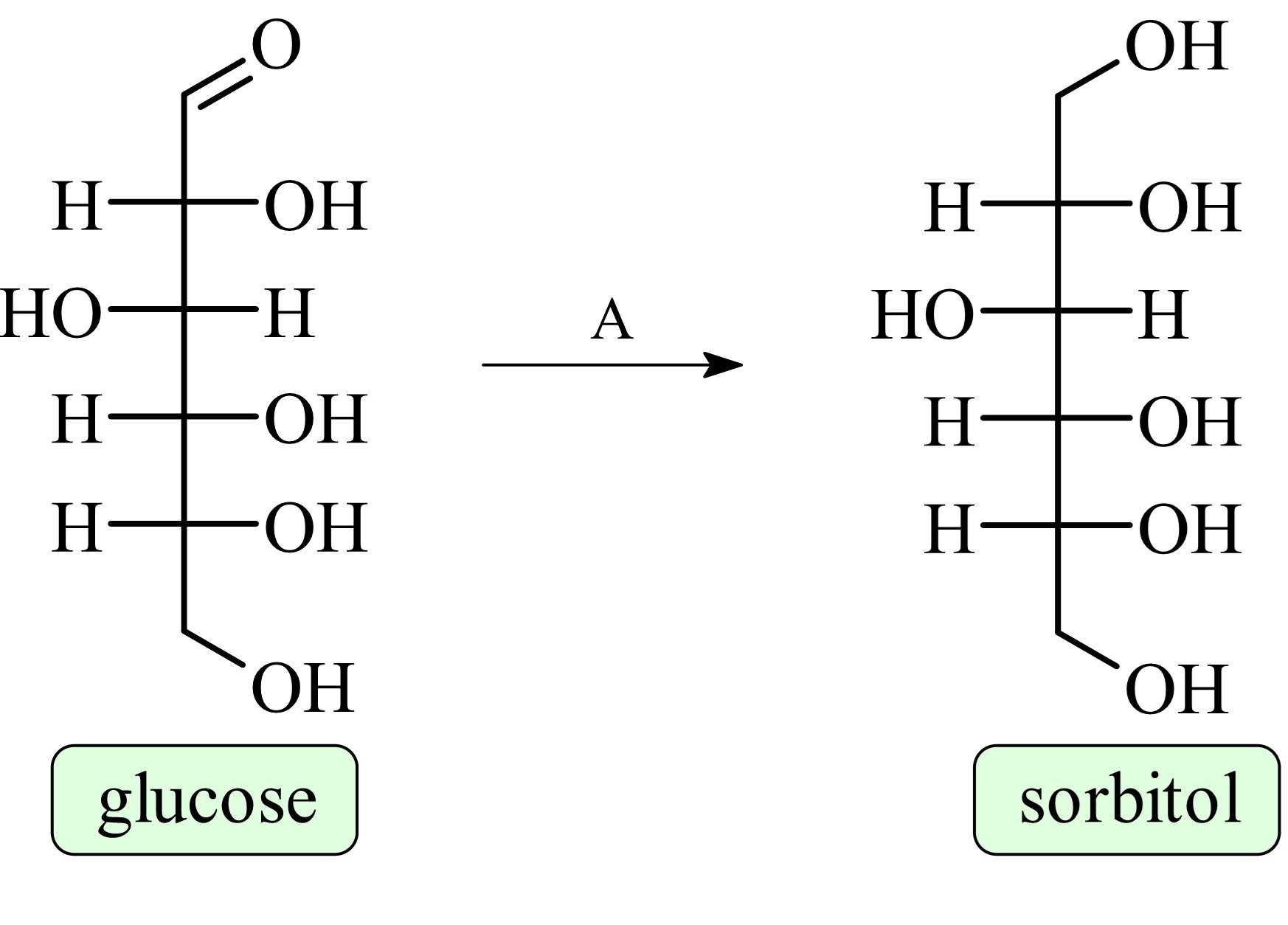

A, H2.
B, Br2.
C, [Ag(NH3)2]OH.
D, HCl.
Khử glucose bằng H2 để tạo thành sobitol.
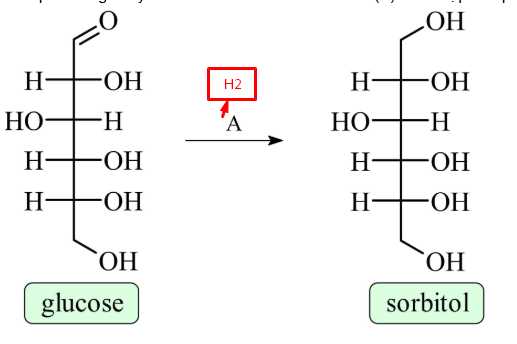

⟹ Chọn đáp án A
Đáp án: A
Câu 13 [1009754]: Fructose không phản ứng được với chất nào sau đây?
A, Cu(OH)2 ở nhiệt độ thường.
B, Nước bromine.
C, Cu(OH)2 ở nhiệt độ cao.
D, Dung dịch AgNO3/NH3, to.
Phân tích các đáp án:
✔️A. Fructose tác dụng với Cu(OH)2 trong môi trường kiềm ở điều kiện thường tạo thành phức chất màu xanh làm, tan trong nước
2C6H12O6 + Cu(OH)2 ⟶ Cu(C6H11O6)2 + 2H2O.
❌B. Fructose không làm mất màu nước Bromine.
✔️C. Fructose tác dụng với Cu(OH)2 ở nhiệt độ cao tạo kết tủa đỏ gạch Cu2O.
✔️D. Fructose đều tham gia phản ứng với thuốc thử Tollens để tạo thành kết tủa bạc kim loại (phản ứng tráng bạc)
CH2OH[CHOH]4CHO + 2[Ag(NH3)2]OH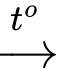 CH2OH[CHOH]4COONH4 + 2Ag↓ + 3NH3 + H2O.
CH2OH[CHOH]4COONH4 + 2Ag↓ + 3NH3 + H2O.
⟹ Chọn đáp án B Đáp án: B
✔️A. Fructose tác dụng với Cu(OH)2 trong môi trường kiềm ở điều kiện thường tạo thành phức chất màu xanh làm, tan trong nước
2C6H12O6 + Cu(OH)2 ⟶ Cu(C6H11O6)2 + 2H2O.
❌B. Fructose không làm mất màu nước Bromine.
✔️C. Fructose tác dụng với Cu(OH)2 ở nhiệt độ cao tạo kết tủa đỏ gạch Cu2O.
✔️D. Fructose đều tham gia phản ứng với thuốc thử Tollens để tạo thành kết tủa bạc kim loại (phản ứng tráng bạc)
CH2OH[CHOH]4CHO + 2[Ag(NH3)2]OH
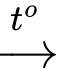 CH2OH[CHOH]4COONH4 + 2Ag↓ + 3NH3 + H2O.
CH2OH[CHOH]4COONH4 + 2Ag↓ + 3NH3 + H2O. ⟹ Chọn đáp án B Đáp án: B
Câu 14 [308305]: Cho 3 dung dịch sau: glucose, acetic acid, glycerol. Hóa chất dùng để phân biệt 3 dung dịch trên là
A, Dung dịch Na2CO3 và kim loại Na.
B, Quỳ tím và dung dịch AgNO3/NH3, đun nóng.
C, Dung dịch NaHCO3 và dung dịch AgNO3.
D, Quỳ tím và kim loại Na.
HD: Phân tích các đáp án:
❌ A. Na2CO3 chỉ phản ứng với acetic acid (tạo khí CO2); tuy nhiên kim loại Na không phân biệt được glucose và glycerol.
❌ C. NaHCO3 giúp nhận biết acetic acid (tạo khí CO2); tuy nhiên thật chú ý AgNO3 không có NH3 nhé nên không phân biệt được glucose và glycerol.
❌ D. Tương tự ý A. sau khi dùng quỳ tím nhận biết được acetic acid; kim loại Na không phân biệt được glucose và glycerol.
✔️ B. Quỳ tím hóa đỏ giúp nhận biết acetic acid (CH3COOH); còn lại AgNO3/NH3 (thuốc thử Tollens) phản ứng với glucose tạo kết tủa Ag↓ giúp nhận biết glucose:
CH2OH[CHOH]4CHO + 2[Ag(NH3)2]OH → CH2OH[CHOH]4COONH4 + 2Ag↓ + 3NH3 + H2O.
Còn lại glycerol không có hiện tượng gì ở cả 2 thí nghiệm. Đáp án: B
❌ A. Na2CO3 chỉ phản ứng với acetic acid (tạo khí CO2); tuy nhiên kim loại Na không phân biệt được glucose và glycerol.
❌ C. NaHCO3 giúp nhận biết acetic acid (tạo khí CO2); tuy nhiên thật chú ý AgNO3 không có NH3 nhé nên không phân biệt được glucose và glycerol.
❌ D. Tương tự ý A. sau khi dùng quỳ tím nhận biết được acetic acid; kim loại Na không phân biệt được glucose và glycerol.
✔️ B. Quỳ tím hóa đỏ giúp nhận biết acetic acid (CH3COOH); còn lại AgNO3/NH3 (thuốc thử Tollens) phản ứng với glucose tạo kết tủa Ag↓ giúp nhận biết glucose:
CH2OH[CHOH]4CHO + 2[Ag(NH3)2]OH → CH2OH[CHOH]4COONH4 + 2Ag↓ + 3NH3 + H2O.
Còn lại glycerol không có hiện tượng gì ở cả 2 thí nghiệm. Đáp án: B
Câu 15 [308307]: Glucose tồn tại ở hai dạng là dạng mạch hở và dạng mạch vòng. Trong đó dạng glucose mạch hở chỉ chiếm một phần nhỏ. Tuy nhiên, khi Cu2+ được sử dụng để oxy hóa dạng mạch hở, gần như toàn bộ glucose trong mẫu đều sẽ tham gia phản ứng. Sử dụng nguyên lý chuyển dịch cân bằng Le Châtelier để giải thích điều này.
A, Glucose dạng mạch hở và dạng vòng đều tham gia phản ứng với Cu2+ nên toàn bộ glucose trong mẫu đều sẽ tham gia phản ứng.
B, Glucose dạng mạch hở phản ứng với Cu2+ nhưng đồng thời cũng sẽ bị phân huỷ nên toàn bộ glucose trong mẫu đều sẽ tham gia phản ứng.
C, Glucose dạng mạch hở phản ứng với Cu2+ nên nồng độ sẽ bị giảm, cân bằng chuyển dịch theo chiều tạo ra thêm glucose dạng mạch hở để tiếp tục phản ứng.
D, Dạng glucose mạch hở phản ứng với Cu2+ nên nồng độ sẽ tăng, cân bằng chuyển dịch theo chiều giảm bớt glucose dạng mạch hở.
HD: Phân tích các đáp án:
❌ A. không thỏa mãn vì nếu dạng mạch vòng tham gia được với Cu2+ thì còn cần gì nguyên lý chuyển dịch cân bằng Le Châtelier để giải thích gì nữa!?
❌ B. không thỏa mãn, glucose mạch hở bị phân hủy là một thông tin nhiễu, không đúng và không có ý nghĩa gì đây cả.
✔️ C. thỏa mãn. phù hợp với nguyên lý chuyển dịch cân bằng Le Châtelier: cân bằng giữa mạch vòng ⇄ mạch hở sẽ chuyển dịch theo chiều làm tăng dạng mạch hở (bởi dạng mạch hở giảm dần do tham gia phản ứng với Cu2+).
❌ D. không thỏa mãn vì dạng hở tham gia phản ứng thì phải giảm đi.
⇒ Chọn đáp án C Đáp án: C
❌ A. không thỏa mãn vì nếu dạng mạch vòng tham gia được với Cu2+ thì còn cần gì nguyên lý chuyển dịch cân bằng Le Châtelier để giải thích gì nữa!?
❌ B. không thỏa mãn, glucose mạch hở bị phân hủy là một thông tin nhiễu, không đúng và không có ý nghĩa gì đây cả.
✔️ C. thỏa mãn. phù hợp với nguyên lý chuyển dịch cân bằng Le Châtelier: cân bằng giữa mạch vòng ⇄ mạch hở sẽ chuyển dịch theo chiều làm tăng dạng mạch hở (bởi dạng mạch hở giảm dần do tham gia phản ứng với Cu2+).
❌ D. không thỏa mãn vì dạng hở tham gia phản ứng thì phải giảm đi.
⇒ Chọn đáp án C Đáp án: C
Câu 16 [308308]: Phản ứng của glucose với chất hay dung dịch nào sau đây chứng tỏ glucose có cấu tạo mạch vòng?
A, Phản ứng với CH3OH/HCl.
B, Phản ứng với Cu(OH)2.
C, Phản ứng với dung dịch AgNO3/NH3.
D, Phản ứng với H2/Ni, to.
HD: Ở dạng mạch hở: 5 nhóm OH có vai trò khá tương đương, chúng đều không phản ứng được với CH3OH/HCl (tạo ether). Ở dạng mạch vòng, nhóm OH trên carbon số 1 (OH hemiacetal) linh động hơn nhiều so với 4 nhóm OH còn lại (C2, C3, C4, C6) nên trong phản ứng với CH3OH/HCl, chỉ một mình nhóm OH hemiacetal này có thể tham gia phản ứng còn 4 nhóm OH còn lại thì không.
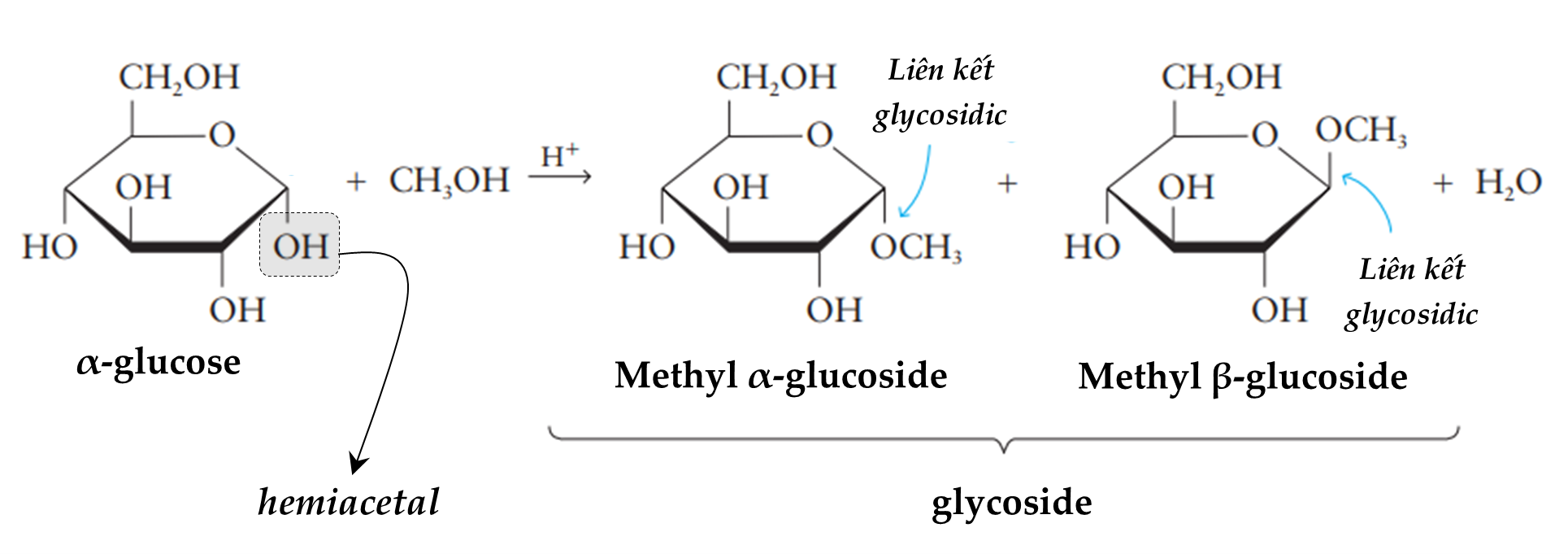 Đáp án: A
Đáp án: A
 Đáp án: A
Đáp án: A
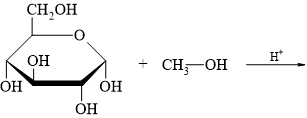
Câu 17 [308310]: Xác định sản phẩm tạo thành của phản ứng sau:

A, 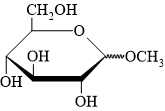

B, 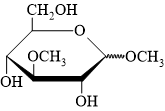

C, 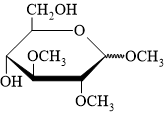

D, 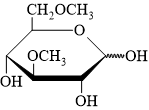

HD: Đánh số carbon glucose (chất phản ứng với CH3OH):

Quan sát cấu tạo của phân tử glucose dạng mạch vòng 6 cạnh có thể thấy glucose có 5 nhóm OH. Nhưng không phải nhóm OH nào cũng có khả năng phản ứng như nhau. Nhóm OH trên carbon số 1 (OH hemiacetal) linh động hơn nhiều so với 4 nhóm OH còn lại (C2, C3, C4, C6) nên trong một số phản ứng nhất định, chỉ một mình nhóm OH hemiacetal này có thể tham gia phản ứng còn 4 nhóm OH còn lại thì không. ► Trong môi trường acid H+, nhóm -OH hemiacetal trong glucose có thể được thay thế bằng nhóm -OR của alcohol. Sản phẩm sinh ra ở dạng hỗn hợp các đồng phân α và đồng phân β ⇒ cách viết sản phẩm ⇝OCH3 biểu diễn chung cho cả 2 dạng này.!
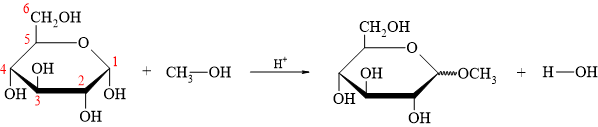
⇝ Chọn đáp án A. ♥ Đáp án: A

Quan sát cấu tạo của phân tử glucose dạng mạch vòng 6 cạnh có thể thấy glucose có 5 nhóm OH. Nhưng không phải nhóm OH nào cũng có khả năng phản ứng như nhau. Nhóm OH trên carbon số 1 (OH hemiacetal) linh động hơn nhiều so với 4 nhóm OH còn lại (C2, C3, C4, C6) nên trong một số phản ứng nhất định, chỉ một mình nhóm OH hemiacetal này có thể tham gia phản ứng còn 4 nhóm OH còn lại thì không. ► Trong môi trường acid H+, nhóm -OH hemiacetal trong glucose có thể được thay thế bằng nhóm -OR của alcohol. Sản phẩm sinh ra ở dạng hỗn hợp các đồng phân α và đồng phân β ⇒ cách viết sản phẩm ⇝OCH3 biểu diễn chung cho cả 2 dạng này.!

⇝ Chọn đáp án A. ♥ Đáp án: A
Câu 18 [308311]: Xác định sản phẩm tạo thành của phản ứng sau:
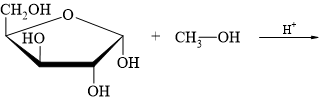

A, 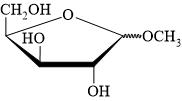

B, 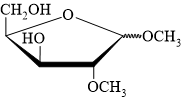

C, 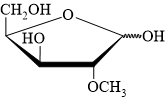

D, 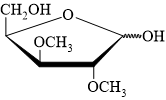

HD: Tính chất phản ứng tương tự câu hỏi có ID = [308310]. Đánh số carbon ⇝ xác định nhóm OH hemiacetal:

⇒ đó là nhóm OH đính vào carbon số 1 ⇒ chỉ có nhóm OH này phản ứng với CH3OH trong môi trường acid tạo ⇝OCH3 (do sản phẩm sinh ra ở dạng hỗn hợp các đồng phân α và đồng phân β nên biểu diễn ⇝OCH3 thể hiện chung cho cả 2 dạng đó).
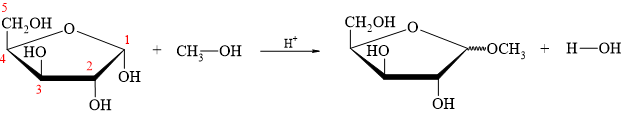
⇝ Chọn đáp án A. ♥ Đáp án: A

⇒ đó là nhóm OH đính vào carbon số 1 ⇒ chỉ có nhóm OH này phản ứng với CH3OH trong môi trường acid tạo ⇝OCH3 (do sản phẩm sinh ra ở dạng hỗn hợp các đồng phân α và đồng phân β nên biểu diễn ⇝OCH3 thể hiện chung cho cả 2 dạng đó).

⇝ Chọn đáp án A. ♥ Đáp án: A
Câu 19 [308312]: Hợp chất sau đây là sản phẩm được tạo thành khi cho glucose phản ứng với alcohol nào?
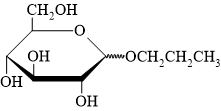

A, CH3OH.
B, CH3CH2OH.
C, CH3CH2CH2OH.
D, (CH3)2CHOH.
HD: Phân tích phản ứng của nhóm chức OH - hemiacetal với alcohol tổng quát dạng ROH trong môi trường acid:

⇒ R ≡ CH3CH2CH2 ⇒ alcohol tương ứng là ROH ≡ CH3CH2CH2OH ⇝ Chọn đáp án C. ♣ Đáp án: C

⇒ R ≡ CH3CH2CH2 ⇒ alcohol tương ứng là ROH ≡ CH3CH2CH2OH ⇝ Chọn đáp án C. ♣ Đáp án: C
Câu 20 [308313]: Chất nào sau đây được dùng làm nguyên liệu điều chế trực tiếp ethanol?
A, Glucose.
B, Methane.
C, Acethylene.
D, Ethane.
HD: Lên men glucose với enzyme xúc tác ở nhiệt độ thích hợp thu được ethanol:
C6H12O6 ––enzyme, to→ 2C2H5OH + 2CO2↑.
⇝ Chọn đáp án A. ♥ Đáp án: A
C6H12O6 ––enzyme, to→ 2C2H5OH + 2CO2↑.
⇝ Chọn đáp án A. ♥ Đáp án: A
Câu 21 [308314]: Trong điều kiện thích hợp glucose lên men tạo thành khí CO2 và
A, HCOOH.
B, CH3CHO.
C, CH3COOH.
D, C2H5OH.
Lên men glucose với enzyme xúc tác ở nhiệt độ thích hợp thu được khí CO2 và ethanol:
C6H12O6 –enzyme, to→ 2C2H5OH + 2CO2↑.
⇒ Chọn đáp án D Đáp án: D
C6H12O6 –enzyme, to→ 2C2H5OH + 2CO2↑.
⇒ Chọn đáp án D Đáp án: D
Câu 22 [1009755]: Glucose có thể lên men tạo lactic acid có trong sữa chua qua phản ứng nào sao đây?
A, CH2OH–[CHOH]4–CHO + Br2 + H2O 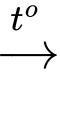 CH2OH–[CHOH]4–COOH + 2HBr.
CH2OH–[CHOH]4–COOH + 2HBr.
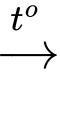 CH2OH–[CHOH]4–COOH + 2HBr.
CH2OH–[CHOH]4–COOH + 2HBr.B, C6H12O6  2CH3CH(OH)COOH.
2CH3CH(OH)COOH.
 2CH3CH(OH)COOH.
2CH3CH(OH)COOH.C, 2C6H12O6 + Cu(OH)2 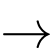 (C6H11O6)2Cu + 2H2O.
(C6H11O6)2Cu + 2H2O.
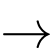 (C6H11O6)2Cu + 2H2O.
(C6H11O6)2Cu + 2H2O.D, C6H12O6  2 C2H5OH + 2 CO2.
2 C2H5OH + 2 CO2.
 2 C2H5OH + 2 CO2.
2 C2H5OH + 2 CO2.
Phân tích các phát biểu:
❌A. Phương trình phản ứng:
CH2OH–[CHOH]4–CHO + Br2 + H2O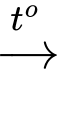 CH2OH–[CHOH]4–COOH + 2HBr.
CH2OH–[CHOH]4–COOH + 2HBr.
⟶ Phản ứng với nước bromine.
✔️B. Phương trình phản ứng:
C6H12O6 2CH3CH(OH)COOH
2CH3CH(OH)COOH
⟶ Phản ứng lên men lactic.
❌C. Phương trình phản ứng:
2C6H12O6 + Cu(OH)2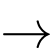 (C6H11O6)2Cu + 2H2O.
(C6H11O6)2Cu + 2H2O.
⟶ Phản ứng với coper(II) hydroxide.
❌D. Phương trình phản ứng:
C6H12O6 2 C2H5OH + 2 CO2.
2 C2H5OH + 2 CO2.
⟶ Phản ứng lên men rượu.
⟹ Chọn đáp án B
Đáp án: B
❌A. Phương trình phản ứng:
CH2OH–[CHOH]4–CHO + Br2 + H2O
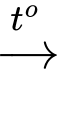 CH2OH–[CHOH]4–COOH + 2HBr.
CH2OH–[CHOH]4–COOH + 2HBr.⟶ Phản ứng với nước bromine.
✔️B. Phương trình phản ứng:
C6H12O6
 2CH3CH(OH)COOH
2CH3CH(OH)COOH⟶ Phản ứng lên men lactic.
❌C. Phương trình phản ứng:
2C6H12O6 + Cu(OH)2
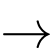 (C6H11O6)2Cu + 2H2O.
(C6H11O6)2Cu + 2H2O.⟶ Phản ứng với coper(II) hydroxide.
❌D. Phương trình phản ứng:
C6H12O6
 2 C2H5OH + 2 CO2.
2 C2H5OH + 2 CO2.⟶ Phản ứng lên men rượu.
⟹ Chọn đáp án B
Đáp án: B
Câu 23 [308315]: Cho lên men 45 gam glucose để điều chế ethanol, hiệu suất phản ứng 80%, thu được V lít CO2 (đkc). Giá trị của V là
A, 7,892.
B, 4,105.
C, 9,916.
D, 4,483.
HD: Lên men glucose với enzyme xúc tác ở nhiệt độ thích hợp thu được khí CO2 và ethanol:
C6H12O6 ––enzyme, to→ 2C2H5OH + 2CO2↑.
Giả thiết sử dụng 45 gam glucose (M = 180) ⇒ nglucose = 45 ÷ 180 = 0,25 mol.
Từ tỉ lệ phản ứng: 1 mol glucose → 2 mol CO2 ⇒ 0,25 mol glucose → 0,5 mol CO2.
► Thật chú ý hiệu suất phản ứng chỉ đạt 80%; nghĩa là đáng nhẽ thu được 0,5 mol CO2 thì thực tế chỉ thu được ít hơn là 0,5 × 0,8 = 0,4 mol CO2 mà thôi.
⇒ Yêu cầu giá trị của V lít khí CO2 (đkc) là V = 0,4 × 24,79 = 9,916 lít ⇝ Chọn đáp án C. ♣ Đáp án: C
C6H12O6 ––enzyme, to→ 2C2H5OH + 2CO2↑.
Giả thiết sử dụng 45 gam glucose (M = 180) ⇒ nglucose = 45 ÷ 180 = 0,25 mol.
Từ tỉ lệ phản ứng: 1 mol glucose → 2 mol CO2 ⇒ 0,25 mol glucose → 0,5 mol CO2.
► Thật chú ý hiệu suất phản ứng chỉ đạt 80%; nghĩa là đáng nhẽ thu được 0,5 mol CO2 thì thực tế chỉ thu được ít hơn là 0,5 × 0,8 = 0,4 mol CO2 mà thôi.
⇒ Yêu cầu giá trị của V lít khí CO2 (đkc) là V = 0,4 × 24,79 = 9,916 lít ⇝ Chọn đáp án C. ♣ Đáp án: C
Câu 24 [705966]: Trong quá trình sản xuất rượu vang, người ta sử dụng nấm men Saccharomyces cerevisiae để lên men glucose và fructose (có trong dịch ép trái nho) tạo thành ethanol. Một học sinh thực hiện thí nghiệm thử tính chất của sản phẩm từ quá trình lên men này trong phòng thí nghiệm bằng dụng cụ như hình dưới:
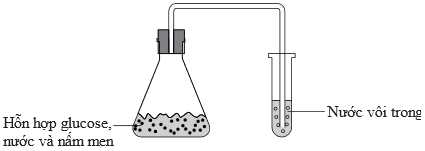
Cho các phát biểu sau về thí nghiệm:
(a) Phản ứng lên men glucose thuộc loại phản ứng phân hủy.
(b) Ethanol bay hơi, không tan trong nước vôi trong tạo bong bóng khí.
(c) Ống nghiệm chứa nước vôi trong bị vẩn đục.
(d) Có thể thay nước vôi trong bằng dung dịch xút.
Các phát biểu đúng là

Cho các phát biểu sau về thí nghiệm:
(a) Phản ứng lên men glucose thuộc loại phản ứng phân hủy.
(b) Ethanol bay hơi, không tan trong nước vôi trong tạo bong bóng khí.
(c) Ống nghiệm chứa nước vôi trong bị vẩn đục.
(d) Có thể thay nước vôi trong bằng dung dịch xút.
Các phát biểu đúng là
A, (a), (c).
B, (b), (c).
C, (a), (b), (c).
D, (b), (c), (d).
Phân tích các phát biểu :
✔️(a) – Đúng. Phản ứng phân hủy: Là phản ứng hóa học trong đó một chất sinh ra hai hay nhiều chất mới. Phản ứng lên men glucose sinh ra nhiều chất mới là CO2 và C2H5OH nên phản ứng lên men là phản ứng phân hủy.
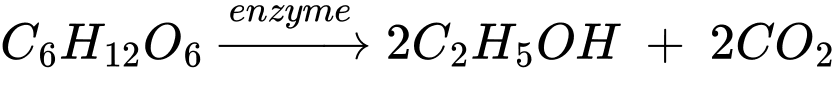
❌(b) – Sai. Ethanol bay hơi, tan vô hạn trong nước.
✔️(c) – Đúng. Ống nghiệm chứa nước vôi trong bị vẩn đục. Nguyên do phản ứng lên men sinh ra CO2 làm vẫn đục nước vôi trong.
CO2 + Ca(OH)2 → CaCO3 + H2O
❌(d) – Sai. Không thể thay nước vôi trong bằng dung dịch xút, khi có khí sinh ra không rõ hiện tượng là khí phản ứng với dung dịch xút hay thoát ra ngoài.
⟹Có 2 phát biểu đúng là (a),(c).
⟹Chọn đáp án A Đáp án: A
✔️(a) – Đúng. Phản ứng phân hủy: Là phản ứng hóa học trong đó một chất sinh ra hai hay nhiều chất mới. Phản ứng lên men glucose sinh ra nhiều chất mới là CO2 và C2H5OH nên phản ứng lên men là phản ứng phân hủy.
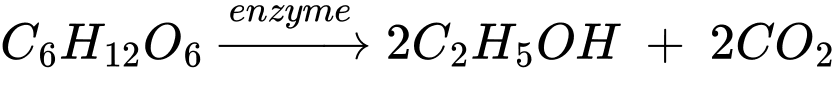
❌(b) – Sai. Ethanol bay hơi, tan vô hạn trong nước.
✔️(c) – Đúng. Ống nghiệm chứa nước vôi trong bị vẩn đục. Nguyên do phản ứng lên men sinh ra CO2 làm vẫn đục nước vôi trong.
CO2 + Ca(OH)2 → CaCO3 + H2O
❌(d) – Sai. Không thể thay nước vôi trong bằng dung dịch xút, khi có khí sinh ra không rõ hiện tượng là khí phản ứng với dung dịch xút hay thoát ra ngoài.
⟹Có 2 phát biểu đúng là (a),(c).
⟹Chọn đáp án A Đáp án: A
Câu 25 [308316]: Phản ứng nào không thể hiện tính khử của glucose?
A, Phản ứng tráng gương.
B, Cho glucose cộng H2 (xúc tác Ni, to).
C, Cho glucose cháy hoàn toàn trong oxygen dư.
D, Cho glucose tác dụng với nước bromine.
HD: Mẹo nhỏ với kinh nghiệm xử lý: "khử cho (electron) - o (oxi hóa) nhận (electron)" ⇒ glucose thể hiện tính khử ⇄ glucose cho electron. Tuy nhiên, nếu phân tích quá trình cho nhận electron của glucose C6h12O6 thì rõ là phức tạp và mất thời gian ⇒ Kinh nghiệm ở đây là gì? Cặp oxi hóa - khử: A + B nếu A là chất khử ⇒ B đối tác là chất oxi hóa thôi.
Phân tích các đáp án:
✔️ A. phản ứng tráng gương: glucose + AgNO3 → Ag↓ + ... || đối tác Ag+ + e → Ag thể hiện tính oxi hóa (nhận e) ⇒ glucose thể hiện tính khử.
❌ B. cộng H2: glucose + H2 ––Ni, to→ sorbitol || đối tác H2 → 2H+ + 2e thể hiện tính khử (cho e) ⇒ glucose thể hiện tính oxi hóa.
✔️ C. glucose + O2 ––to→ CO2 + H2O || đối tác O2 + 4e ⇝ 2O2– thể hiện tính oxi hóa (nhận e) ⇒ glucose thể hiện tính khử.
✔️ D. glucose + Br2 + H2O ––to→ gluconic acid + HBr || đối tác Br2 + 2e → 2Br– thể hiện tính oxi hóa (nhận e) ⇒ glucose thể hiện tính khử. Đáp án: B
Phân tích các đáp án:
✔️ A. phản ứng tráng gương: glucose + AgNO3 → Ag↓ + ... || đối tác Ag+ + e → Ag thể hiện tính oxi hóa (nhận e) ⇒ glucose thể hiện tính khử.
❌ B. cộng H2: glucose + H2 ––Ni, to→ sorbitol || đối tác H2 → 2H+ + 2e thể hiện tính khử (cho e) ⇒ glucose thể hiện tính oxi hóa.
✔️ C. glucose + O2 ––to→ CO2 + H2O || đối tác O2 + 4e ⇝ 2O2– thể hiện tính oxi hóa (nhận e) ⇒ glucose thể hiện tính khử.
✔️ D. glucose + Br2 + H2O ––to→ gluconic acid + HBr || đối tác Br2 + 2e → 2Br– thể hiện tính oxi hóa (nhận e) ⇒ glucose thể hiện tính khử. Đáp án: B
Câu 26 [705748]: Hàm lượng glucose có trong mẫu dược phẩm có thể được xác định bằng phương pháp chuẩn độ với iodine như sau: Cho một thể tích chính xác dung dịch chứa glucose vào một thể tích chính xác và dư nước iodine. Sau đó, thêm vào dung dịch sau phản ứng vài giọt dung dịch X, rồi vừa lắc vừa nhỏ từ từ dung dịch sodium thiosulfate (Na2S2O3) có nồng độ xác định vào dung dịch ở trên đến khi mất màu xanh thì dừng lại. Ghi thể tích dung dịch Na2S2O3 đã tiêu tốn:
I2 + 2Na2S2O3 2NaI + Na2S4O6
2NaI + Na2S4O6
Dung dịch X được sử dụng trong thí nghiệm trên nhằm mục đích chính là
I2 + 2Na2S2O3
 2NaI + Na2S4O6
2NaI + Na2S4O6Dung dịch X được sử dụng trong thí nghiệm trên nhằm mục đích chính là
A, Nhận biết hàm lượng glucose dư trong dung dịch.
B, Nhận biết hàm lượng iodine dư trong dung dịch.
C, Nhận biết hàm lượng sodium thiosulfate dư trong dung dịch.
D, Phản ứng với lượng dư dung dịch sodium thiosulfate.
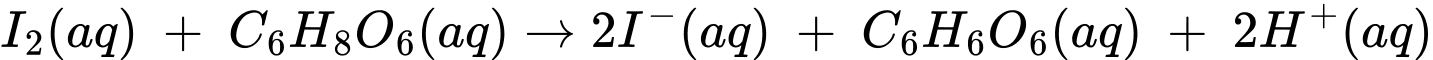
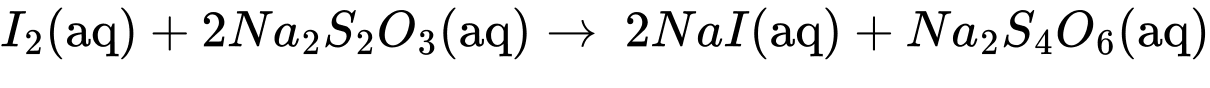
Dung dịch X là hồ tinh bột mục đích nhận biết hàm lượng Iodine dư trong dung dịch sau phản ứng.
⇒ Chọn đáp án B Đáp án: B
Dạng 2: TRẮC NGHIỆM ĐÚNG SAI – mỗi ý a), b), c), d) chọn đúng hoặc sai.
Câu 27 [308318]: Khi hòa tan trong nước, glucose và fructose tồn tại ở trạng thái cân bằng như sau:
fructose ⇄ glucose
Một nhà hóa học đã chuẩn bị dung dịch fructose 0,244 M ở 25°C. Ở trạng thái cân bằng, người ta thấy rằng nồng độ của nó đã giảm xuống còn 0,113 M.
HD: Phân tích các phát biểu:
❌ a. sai. Theo thời gian lượng fructose chuyển hoá thành glucose càng nhiều; tuy nhiên đến điểm cân bằng, lượng fructose và glucose ổn định, không thay đổi nữa ⇒ thời gian dù càng lâu cũng không có biến động.
✔️ b. đúng. A ⇄ B; A mất để tạo B; mất bao nhiêu thì tạo tương ứng bấy nhiêu B.
✔️ c. đúng. Ban đầu [fructose] = 0,244 M; ở cân bằng, [fructose] = 0,113 M ⇒ đã có 0,131 M fructose chuyển hóa thành glucose ⇒ [glucose] = 0,131 M.
Áp vào công thức tính KC = [glucose] ÷ [fructose] = 0,131 ÷ 0,113 = 1,16.
✔️ d. đúng, như phân tích ở ý c. đã có 0,131 M fructose chuyển hóa thành glucose; so với 0,244 M ban đầu là chiếm 0,131 ÷ 0,244 × 100% ≈ 53,69%.
❌ a. sai. Theo thời gian lượng fructose chuyển hoá thành glucose càng nhiều; tuy nhiên đến điểm cân bằng, lượng fructose và glucose ổn định, không thay đổi nữa ⇒ thời gian dù càng lâu cũng không có biến động.
✔️ b. đúng. A ⇄ B; A mất để tạo B; mất bao nhiêu thì tạo tương ứng bấy nhiêu B.
✔️ c. đúng. Ban đầu [fructose] = 0,244 M; ở cân bằng, [fructose] = 0,113 M ⇒ đã có 0,131 M fructose chuyển hóa thành glucose ⇒ [glucose] = 0,131 M.
Áp vào công thức tính KC = [glucose] ÷ [fructose] = 0,131 ÷ 0,113 = 1,16.
✔️ d. đúng, như phân tích ở ý c. đã có 0,131 M fructose chuyển hóa thành glucose; so với 0,244 M ban đầu là chiếm 0,131 ÷ 0,244 × 100% ≈ 53,69%.
Câu 28 [1009756]: Dữ liệu thực nghiệm được sử dụng để chứng minh cấu tạo của glucose bao gồm các phương pháp phân tích hóa học và cấu trúc hóa học. Tổng hợp các dữ liệu thực nghiệm này cung cấp bằng chứng mạnh mẽ về cấu tạo và tính chất của glucose trong hóa học và sinh học. Cho các tính chất (phản ứng) dùng để chứng minh cấu tạo của glucose như sau:
Phân tích các phát biểu:
✔️A. Đúng. Hoà tan Cu(OH)2 ở nhiệt độ thường tạo dung dịch màu xanh lam chứng minh glucose có các nhóm OH liền kề.
2C6H12O6 + Cu(OH)2 ⟶ Cu(C6H11O6)2 + 2H2O.
✔️B. Đúng. Tạo kết tủa đỏ gạch khi đun nóng với Cu(OH)2, chứng minh glucose mang tính khử:
Phương trình hóa học:
CH2OH(CHOH)4CHO + 2Cu(OH)2 + NaOH ⟶ CH2OH(CHOH)4COONa + Cu2O + 3H2O
❌C. Sai. Glucose tác dụng với anhydride acetic tạo 5 nhóm ester ⟶ Chứng minh glucose có 5 nhóm OH, không chứng minh được 5 nhóm OH này liền kề nhau.
❌D. Sai. Glucose lên men tạo thành các sản phẩm khác nhau, tuỳ thuộc vào enzyme có trong men được sử dụng.
Lên men rượu:
C6H12O6 2C2H5OH + 2CO2.
2C2H5OH + 2CO2.
Lên men lactic: C6H12O6 2CH3CH(OH)COOH.
2CH3CH(OH)COOH.
Phản ứng khử glucose thu được hexane chứng minh glucose có chứa 6 nguyên tử carbon mạch không phân nhánh.
✔️A. Đúng. Hoà tan Cu(OH)2 ở nhiệt độ thường tạo dung dịch màu xanh lam chứng minh glucose có các nhóm OH liền kề.
2C6H12O6 + Cu(OH)2 ⟶ Cu(C6H11O6)2 + 2H2O.
✔️B. Đúng. Tạo kết tủa đỏ gạch khi đun nóng với Cu(OH)2, chứng minh glucose mang tính khử:
Phương trình hóa học:
CH2OH(CHOH)4CHO + 2Cu(OH)2 + NaOH ⟶ CH2OH(CHOH)4COONa + Cu2O + 3H2O
❌C. Sai. Glucose tác dụng với anhydride acetic tạo 5 nhóm ester ⟶ Chứng minh glucose có 5 nhóm OH, không chứng minh được 5 nhóm OH này liền kề nhau.
❌D. Sai. Glucose lên men tạo thành các sản phẩm khác nhau, tuỳ thuộc vào enzyme có trong men được sử dụng.
Lên men rượu:
C6H12O6
 2C2H5OH + 2CO2.
2C2H5OH + 2CO2.Lên men lactic: C6H12O6
 2CH3CH(OH)COOH.
2CH3CH(OH)COOH.Phản ứng khử glucose thu được hexane chứng minh glucose có chứa 6 nguyên tử carbon mạch không phân nhánh.
Câu 29 [308319]: Thí nghiệm của thuốc thử Tollens về sự hiện diện của đường có tính khử (chẳng hạn như đường có trong mẫu nước tiểu) liên quan đến việc xử lý mẫu bằng ion bạc trong dung dịch ammonia. Kết quả là sự hình thành kim loại bạc trong bình phản ứng nếu như đường có tính khử. Dùng glucose C6H12O6 để minh họa trong thử nghiệm này, phản ứng oxi hóa khử xảy ra là


CH2OH[CHOH]4CHO + 2[Ag(NH3)2]OH ––to→ CH2OH[CHOH]4COONH4 + 2Ag↓ + 3NH3 + H2O.


Hình II.4.a. Bố trí thí nghiệm của thuốc thử Tollen. b. Ống nghiệm được tráng bạc.
HD: Phân tích các phát biểu:
✔️ a. đúng. Mẹo nhỏ: xác định gián tiếp: chú ý Ag+ + e → Ag nên trong phản ứng với thuốc thử Tollens thì AgNO3 đóng vai trò là chất oxi hóa (nhận electron) ⇒ glucose đóng vai trò là chất khử.
✔️ b. đúng. như phân tích ở ý a. Ag+ nhận electron nên đóng vai trò là chất oxi hóa.
✔️ c. đúng. dạng mạch hở glucose chứa nhóm chức CHO tham gia phản ứng tráng bạc tương tự hợp chất aldehyde được học ở chương trình lớp 11, tổng quát theo sơ đồ:
RCHO + 2[Ag(NH3)2]OH ––to→ RCOONH4 + 2Ag↓ + 3NH3 + H2O.
❌ d. sai. Phân tích: Thuốc thử Tollens: dung dịch của AgNO3 kết hợp với NH3 tạo thành phức chất [Ag(NH3)2]OH. Do môi trường có hoà tan một phần NH3 và NH3 sẽ kết hợp với nước để tạo ra ion OH– ⇝ môi trường lúc này có tính base ⇒ Trong môi trường base, fructose và glucose sẽ có sự chuyển hoá qua lại: fructose ⇄OH–⇄ glucose.
Kết quả là trong ống nghiệm đựng fructose, một phần fructose chuyển thành glucose và sẽ tham gia phản ứng với thuốc thử Tollens cho hiện tượng xuất hiện kết tủa kim loại Ag giống hệt như ống nghiệm đựng glucose.
✔️ a. đúng. Mẹo nhỏ: xác định gián tiếp: chú ý Ag+ + e → Ag nên trong phản ứng với thuốc thử Tollens thì AgNO3 đóng vai trò là chất oxi hóa (nhận electron) ⇒ glucose đóng vai trò là chất khử.
✔️ b. đúng. như phân tích ở ý a. Ag+ nhận electron nên đóng vai trò là chất oxi hóa.
✔️ c. đúng. dạng mạch hở glucose chứa nhóm chức CHO tham gia phản ứng tráng bạc tương tự hợp chất aldehyde được học ở chương trình lớp 11, tổng quát theo sơ đồ:
RCHO + 2[Ag(NH3)2]OH ––to→ RCOONH4 + 2Ag↓ + 3NH3 + H2O.
❌ d. sai. Phân tích: Thuốc thử Tollens: dung dịch của AgNO3 kết hợp với NH3 tạo thành phức chất [Ag(NH3)2]OH. Do môi trường có hoà tan một phần NH3 và NH3 sẽ kết hợp với nước để tạo ra ion OH– ⇝ môi trường lúc này có tính base ⇒ Trong môi trường base, fructose và glucose sẽ có sự chuyển hoá qua lại: fructose ⇄OH–⇄ glucose.
Kết quả là trong ống nghiệm đựng fructose, một phần fructose chuyển thành glucose và sẽ tham gia phản ứng với thuốc thử Tollens cho hiện tượng xuất hiện kết tủa kim loại Ag giống hệt như ống nghiệm đựng glucose.
Câu 30 [308320]: Phân tử glucose tồn ở dạng mạch vòng 6 cạnh, glucose có nhiều nhóm OH. Nhưng không phải nhóm OH nào cũng có khả năng phản ứng như nhau. Có một nhóm OH linh động hơn hẳn (dễ dàng tham gia các phản ứng hơn) các nhóm OH trên các nguyên tử carbon khác.
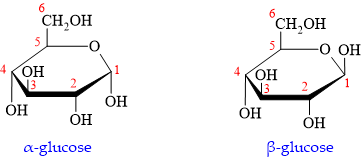

HD: Quan sát lại cấu tạo đề cho và phân tích các phát biểu:

❌a. sai. Kiến thức đã học + thông tin cung cấp cho biết glucose chỉ có 1 nhóm OH hemiacetal; cụ thể đó là nhóm OH đính vào carbon đánh số 1 như trên hình.
✔️ b. đúng. Như phân tích ở ý a. nhóm OH đính vào carbon số 1 chính là nhóm OH hemiacetal linh động hơn hẳn các nhóm OH khác.
❌ c. sai. chỉ có 1 nhóm OH hemiacetal trong glucose có khả năng phản ứng với CH3OH/HCl:

sản phẩm tạo thành là có công thức phân tử C7H14O6 ≠ C7H14O7.
✔️ d. đúng. Nhóm OH hemiacetal linh động và có khả năng mở vòng chuyển thành dạng mạch hở, sau phản ứng với CH3OH/HCl thì tạo thành nhóm OCH3; không còn khả năng này nữa.

❌a. sai. Kiến thức đã học + thông tin cung cấp cho biết glucose chỉ có 1 nhóm OH hemiacetal; cụ thể đó là nhóm OH đính vào carbon đánh số 1 như trên hình.
✔️ b. đúng. Như phân tích ở ý a. nhóm OH đính vào carbon số 1 chính là nhóm OH hemiacetal linh động hơn hẳn các nhóm OH khác.
❌ c. sai. chỉ có 1 nhóm OH hemiacetal trong glucose có khả năng phản ứng với CH3OH/HCl:

sản phẩm tạo thành là có công thức phân tử C7H14O6 ≠ C7H14O7.
✔️ d. đúng. Nhóm OH hemiacetal linh động và có khả năng mở vòng chuyển thành dạng mạch hở, sau phản ứng với CH3OH/HCl thì tạo thành nhóm OCH3; không còn khả năng này nữa.
Dạng 3: TRẮC NGHIỆM YÊU CẦU TRẢ LỜI NGẮN
Câu 31 [1009757]: Cho các phát biểu sau:
(a) Glucose phản ứng với H2 (to, Ni) cho sản phẩm là sobitol.
(b) Trong môi trường acid, glucose và fructose có thể chuyển hóa lẫn nhau.
(c) Có thể phân biệt glucose và fructose bằng phản ứng với dung dịch AgNO3 trong NH3.
(d) Trong dung dịch, glucose và fructose đều hòa tan Cu(OH)2 ở nhiệt độ thường cho dung dịch màu xanh lam.
(e) Fructose là hợp chất đa chức.
(f) Có thể điều chế ethanol từ glucose bằng phương pháp lên men.
Có bao nhiêu phát biểu đúng?
(a) Glucose phản ứng với H2 (to, Ni) cho sản phẩm là sobitol.
(b) Trong môi trường acid, glucose và fructose có thể chuyển hóa lẫn nhau.
(c) Có thể phân biệt glucose và fructose bằng phản ứng với dung dịch AgNO3 trong NH3.
(d) Trong dung dịch, glucose và fructose đều hòa tan Cu(OH)2 ở nhiệt độ thường cho dung dịch màu xanh lam.
(e) Fructose là hợp chất đa chức.
(f) Có thể điều chế ethanol từ glucose bằng phương pháp lên men.
Có bao nhiêu phát biểu đúng?
Phân tích các phát biểu:
✔️A. Đúng. Glucose phản ứng với H2 (to,Ni) cho sản phẩm sobitol.
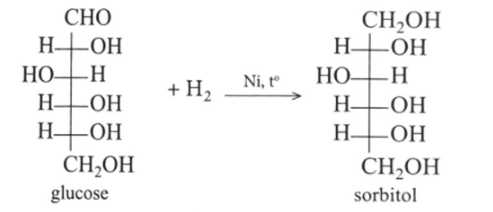 .
.
❌B. Sai. Trong môi trường base, glucose và fructose có thể chuyển hoá lẫn nhau.
❌C. Sai. Glucose và Fructose đều tham gia phản ứng tráng bạc nên không thể dùng đẻ phân biệt hai chất này.
✔️D. Đúng. Trong dung dịch, glucose và fructose đều hoà tan Cu(OH)2 ở nhiệt độ thường tạo phức màu xanh lam, tan trong nước.
2C6H12O6 + Cu(OH)2 ⟶ Cu(C6H11O6)2 + 2H2O.
❌E. Sai. Fructose có 5 nhóm hydroxyl và 1 nhóm carbonyl. Fructose là hợp chất tạp chức.
✔️F. Đúng. Có thể điều chế ethanol tử glucose bằng phương pháp lên men.
C6H12O6 2C2H5OH + 2CO2.
2C2H5OH + 2CO2.
Số phát biểu đúng là 3.
⟹ Điền đáp án 3
✔️A. Đúng. Glucose phản ứng với H2 (to,Ni) cho sản phẩm sobitol.
 .
.❌B. Sai. Trong môi trường base, glucose và fructose có thể chuyển hoá lẫn nhau.
❌C. Sai. Glucose và Fructose đều tham gia phản ứng tráng bạc nên không thể dùng đẻ phân biệt hai chất này.
✔️D. Đúng. Trong dung dịch, glucose và fructose đều hoà tan Cu(OH)2 ở nhiệt độ thường tạo phức màu xanh lam, tan trong nước.
2C6H12O6 + Cu(OH)2 ⟶ Cu(C6H11O6)2 + 2H2O.
❌E. Sai. Fructose có 5 nhóm hydroxyl và 1 nhóm carbonyl. Fructose là hợp chất tạp chức.
✔️F. Đúng. Có thể điều chế ethanol tử glucose bằng phương pháp lên men.
C6H12O6
 2C2H5OH + 2CO2.
2C2H5OH + 2CO2.Số phát biểu đúng là 3.
⟹ Điền đáp án 3
Câu 32 [1009758]: Cho dãy các chất: C2H2, HCHO, HCOOH, CH3CHO, HCOONa, HCOOCH3, C6H12O6 (glucose). Có bao nhiêu chất trong dãy tham gia được phản ứng tráng gương?
Các chất có phản ứng tráng gương khi trong phân tử của chúng có nhóm –CHO hoặc có thể chuyển hóa thành nhóm –CHO trong môi trường kiềm
Có 6 chất trong dãy tham gia phản ứng tráng bạc là: HCHO,HCOOH, CH3CHO, HCOONa, HCOOCH3, C6H12O6.
Phương trình phản ứng:
(1) HCHO + 4AgNO3 + 6NH3 + 2H2O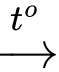 4Ag ↓+ 4NH4NO3 + (NH4)2CO3
4Ag ↓+ 4NH4NO3 + (NH4)2CO3
(2) HCOOH + 2AgNO3 + 4NH3 + H2O → (NH4)2CO3 + 2Ag↓ + 2NH4NO3.
(3) CH3CHO + 2AgNO3 + 3NH3 + H2O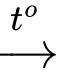 CH3COONH4 + 2NH4NO3 + 2Ag
CH3COONH4 + 2NH4NO3 + 2Ag
(4)18HCOONa + 4AgNO3 + 14NH3 + 6H2O → 4Ag + 9Na2CO3 + 9(NH4)2CO3.
(5)HCOOCH3 + 2AgNO3 + 3NH3 + H2O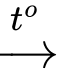 2Ag + 2NH4NO3 + NH4OCOOCH3.
2Ag + 2NH4NO3 + NH4OCOOCH3.
(6) HOCH2[CHOH]4CHO + 2AgNO3 + 3NH3 + H2O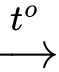 HOCH2[CHOH]4COONH4 + 2Ag + 2NH4NO3
HOCH2[CHOH]4COONH4 + 2Ag + 2NH4NO3
⟹ Điền đáp án 6
Có 6 chất trong dãy tham gia phản ứng tráng bạc là: HCHO,HCOOH, CH3CHO, HCOONa, HCOOCH3, C6H12O6.
Phương trình phản ứng:
(1) HCHO + 4AgNO3 + 6NH3 + 2H2O
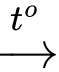 4Ag ↓+ 4NH4NO3 + (NH4)2CO3
4Ag ↓+ 4NH4NO3 + (NH4)2CO3(2) HCOOH + 2AgNO3 + 4NH3 + H2O → (NH4)2CO3 + 2Ag↓ + 2NH4NO3.
(3) CH3CHO + 2AgNO3 + 3NH3 + H2O
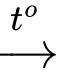 CH3COONH4 + 2NH4NO3 + 2Ag
CH3COONH4 + 2NH4NO3 + 2Ag(4)18HCOONa + 4AgNO3 + 14NH3 + 6H2O → 4Ag + 9Na2CO3 + 9(NH4)2CO3.
(5)HCOOCH3 + 2AgNO3 + 3NH3 + H2O
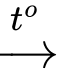 2Ag + 2NH4NO3 + NH4OCOOCH3.
2Ag + 2NH4NO3 + NH4OCOOCH3.(6) HOCH2[CHOH]4CHO + 2AgNO3 + 3NH3 + H2O
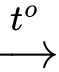 HOCH2[CHOH]4COONH4 + 2Ag + 2NH4NO3
HOCH2[CHOH]4COONH4 + 2Ag + 2NH4NO3⟹ Điền đáp án 6
Câu 33 [705723]: Cho dãy các chất sau: acetic acid, ethyl acetate, isopropylamine, glucose, acetone. Trong số các chất trên, có bao nhiêu tác dụng với Cu(OH)2 ở điều kiện thường?
Các chất tác dụng với Cu(OH)2 ở điều kiện thường là acetic acid, isopropylamine, glucose.
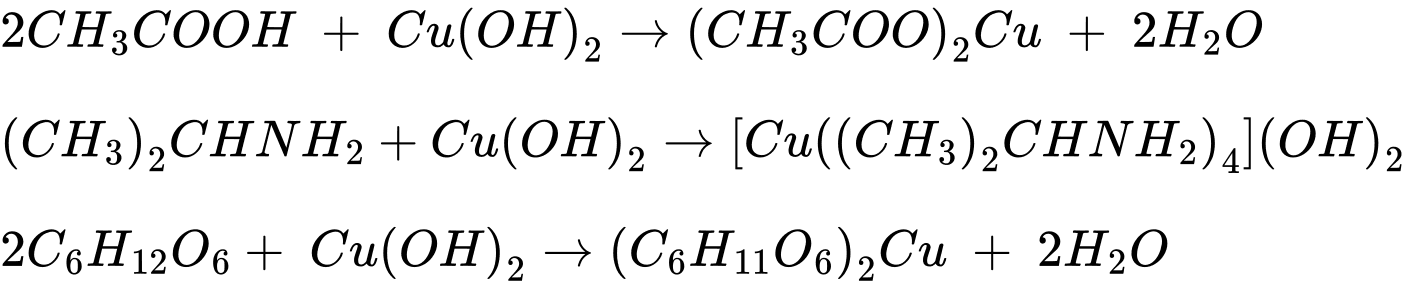
⇒ Điền đáp án: 3
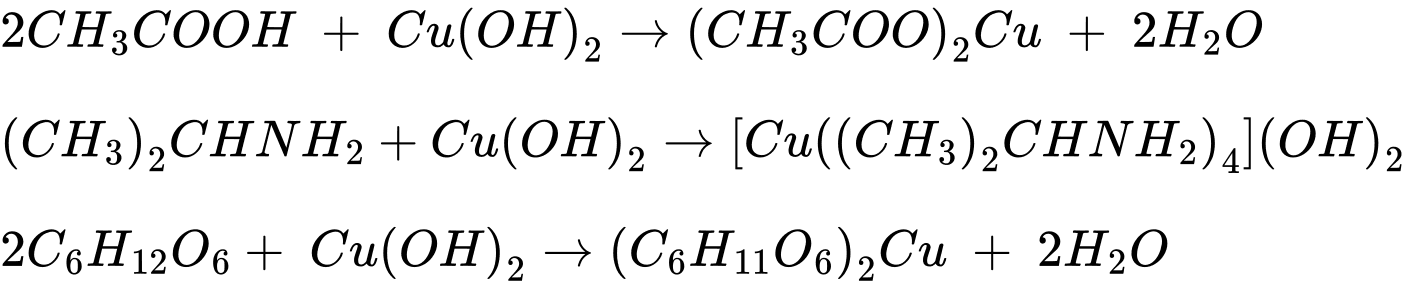
⇒ Điền đáp án: 3
Câu 34 [308325]: Quá trình quang hợp giúp tổng hợp glucose có thể được biểu diễn bằng phương trình sau:
(a) O2 bị loại khỏi hỗn hợp.
(b) C6H12O6 (glucose) bị loại khỏi hỗn hợp.
(c) thêm thêm nước.
(d) thêm chất xúc tác.
(e) giảm nhiệt độ.
Số yếu tố làm cân bằng chuyển dịch theo chiều thuận là
6CO2(g) + 6H2O(l) ⇄ C6H12O6(g) + 6O2(g); ΔHo = 2801 kJ/mol.
Trong các yếu tố sau: (a) O2 bị loại khỏi hỗn hợp.
(b) C6H12O6 (glucose) bị loại khỏi hỗn hợp.
(c) thêm thêm nước.
(d) thêm chất xúc tác.
(e) giảm nhiệt độ.
Số yếu tố làm cân bằng chuyển dịch theo chiều thuận là
HD: The nguyên lí chuyển dịch cân bằng Le Chatelier:
6CO2(g) + 6H2O(l) ⇄ C6H12O6(g) + 6O2(g); ΔHo = 2810 kJ/mol.
Phân tích các yếu tố:
✔️ (a) loại O2 khỏi hỗn hợp ⇝ cần bằng chuyển dịch theo chiều làm tăng O2 chính là chiều thuận.
✔️ (b) loại C6H12O6 cũng giống như ý a, glucose là sản phẩm ⇝ cần bằng chuyển dịch theo chiều làm tăng sản phẩm chính là chiều thuận.
✔️ (c) thêm nước H2O là chất tham gia ⇝ cân bằng chuyển dịch theo chiều làm giảm H2O chính là chiều thuận.
❌ (d) thêm chất xúc tác: chất xúc tác chỉ ảnh hưởng đến tốc độ phản ứng nên cân bằng không chuyển dịch.
❌ (e) ΔH > 0: mẹo nhỏ "âm tỏa - dương thu" ⇝ phản ứng thu nhiệt ⇒ phản ứng là thu nhiệt: cấp nhiệt thì chuyển dịch theo chiều thuận và giảm nhiệt thì chuyển dịch theo chiều nghịch.
⇒ có 3/5 yếu tố thỏa mãn ⇒ điền đáp án: 3.
6CO2(g) + 6H2O(l) ⇄ C6H12O6(g) + 6O2(g); ΔHo = 2810 kJ/mol.
Phân tích các yếu tố:
✔️ (a) loại O2 khỏi hỗn hợp ⇝ cần bằng chuyển dịch theo chiều làm tăng O2 chính là chiều thuận.
✔️ (b) loại C6H12O6 cũng giống như ý a, glucose là sản phẩm ⇝ cần bằng chuyển dịch theo chiều làm tăng sản phẩm chính là chiều thuận.
✔️ (c) thêm nước H2O là chất tham gia ⇝ cân bằng chuyển dịch theo chiều làm giảm H2O chính là chiều thuận.
❌ (d) thêm chất xúc tác: chất xúc tác chỉ ảnh hưởng đến tốc độ phản ứng nên cân bằng không chuyển dịch.
❌ (e) ΔH > 0: mẹo nhỏ "âm tỏa - dương thu" ⇝ phản ứng thu nhiệt ⇒ phản ứng là thu nhiệt: cấp nhiệt thì chuyển dịch theo chiều thuận và giảm nhiệt thì chuyển dịch theo chiều nghịch.
⇒ có 3/5 yếu tố thỏa mãn ⇒ điền đáp án: 3.
Câu 35 [308327]: Lên men là một quá trình sản xuất rượu vang bằng phương pháp hóa học phức tạp, trong đó glucose được chuyển đổi thành ethanol và carbon dioxide:
C6H12O6 ––enzyme→ 2C2H5OH + 2CO2↑.
Giả sử khối lượng riêng của ethanol = 0,789 g/mL. Bắt đầu với 500,4 gam glucose, thể tích ethanol tối đa tính bằng đơn vị mL có thể thu được là bao nhiêu? (làm tròn tới số nguyên gần nhất)
HD: Mglucose = 180 ⇒ nglucose = 500,4 ÷ 180 = 2,78 mol.
Từ tỉ lệ phản ứng 1 mol glucose tạo 2 mol ethanol ⇒ 2,78 mol glucose tạo 5,56 mol ethanol.
ethanol có M = 46 ⇒ methanol = 5,56 × 46 = 255,76 gam.
Giả thiết cho Dethanol = 0,789 g/mL = m ÷ V ⇒ Vethanol = m ÷ D = 255,76 ÷ 0,789 ≈ 324,16 mL.
⇒ số nguyên gần nhất tương ứng là 324 ⇝ điền đáp án: 324.
Từ tỉ lệ phản ứng 1 mol glucose tạo 2 mol ethanol ⇒ 2,78 mol glucose tạo 5,56 mol ethanol.
ethanol có M = 46 ⇒ methanol = 5,56 × 46 = 255,76 gam.
Giả thiết cho Dethanol = 0,789 g/mL = m ÷ V ⇒ Vethanol = m ÷ D = 255,76 ÷ 0,789 ≈ 324,16 mL.
⇒ số nguyên gần nhất tương ứng là 324 ⇝ điền đáp án: 324.
Câu 36 [308328]: Trong quá trình lên men rượu, nấm men chuyển đổi glucose thành ethanol và carbon dioxide:
C6H12O6 ––enzyme→ 2C2H5OH + 2CO2↑
Nếu 5,97 gam glucose phản ứng và thu được 1,44 L khí CO2 ở 293 K và 0,984 atm thì hiệu suất phản ứng là a%. Giá trị của a làm tròn đến hai chữ số thập phân là bao nhiêu?
HD: Phương trình trạng thái: pV = nRT với hằng số R = 0,082
Thay số có nCO2 = 0,984 × 1,44 ÷ 293 ÷ 0,082 = Ans (mol).
Theo lý thuyết từ tỉ lệ phản ứng 1 mol glucose tạo 2 mol CO2
⇒ Để có Ans mol CO2 ⇒ cần dùng Ans ÷ 2 mol glucose
⇒ mglucose lý thuyết = Ans ÷ 2 × 180 = 90Ans (gam).
⇒ Hiệu suất phản ứng H = mglucose lí thuyết ÷ mglucose thực tế dùng × 100% = 90Ans ÷ 5,97 × 100% ≈ 88,91%.
⟹ Điền đáp án : 88,91
Thay số có nCO2 = 0,984 × 1,44 ÷ 293 ÷ 0,082 = Ans (mol).
Theo lý thuyết từ tỉ lệ phản ứng 1 mol glucose tạo 2 mol CO2
⇒ Để có Ans mol CO2 ⇒ cần dùng Ans ÷ 2 mol glucose
⇒ mglucose lý thuyết = Ans ÷ 2 × 180 = 90Ans (gam).
⇒ Hiệu suất phản ứng H = mglucose lí thuyết ÷ mglucose thực tế dùng × 100% = 90Ans ÷ 5,97 × 100% ≈ 88,91%.
⟹ Điền đáp án : 88,91
Câu 37 [308329]: Cho 180 gam dung dịch glucose 1% vào lượng dư dung dịch AgNO3 trong NH3, đun nóng nhẹ đến phản ứng hoàn toàn thu được tối đa m gam Ag. Giá trị m là
HD: mglucose = 180 × 0,01 = 1,8 gam ⇒ nglucose = 0,01 mol.
Phản ứng tráng bạc của glucose xảy ra như sau:
CH2OH[CHOH]4CHO + 2[Ag(NH3)2]OH → CH2OH[CHOH]4COONH4 + 2Ag↓ + 3NH3 + H2O.
Từ tỉ lệ phản ứng ⇒ nAg thu được = 2nglucose = 0,02 mol.
⇒ Yêu cầu m = 0,02 × 108 = 2,16 gam ⇝ điền đáp án: 2,16.
Phản ứng tráng bạc của glucose xảy ra như sau:
CH2OH[CHOH]4CHO + 2[Ag(NH3)2]OH → CH2OH[CHOH]4COONH4 + 2Ag↓ + 3NH3 + H2O.
Từ tỉ lệ phản ứng ⇒ nAg thu được = 2nglucose = 0,02 mol.
⇒ Yêu cầu m = 0,02 × 108 = 2,16 gam ⇝ điền đáp án: 2,16.
Câu 38 [308330]: Cho 7,2 gam hỗn hợp gồm glucose và fructose tác dụng với lượng dư dung dịch AgNO3 trong NH3, đun nóng. Sau khi phản ứng xảy ra hoàn toàn, thu được tối đa m gam Ag. Giá trị m là (Làm tròn đến hai chữ số thập phân).
HD: Chú ý Fructose và glucose có 2 điểm chung:
• một là chung công thức phân tử C6H12O6 có M = 180.
• hai là cùng tráng bạc theo tỉ lệ: 1glucose → 2Ag || 1fructose → 2Ag.
⇒ nglucose + fructose = 7,2 ÷ 180 = 0,04 mol.
Theo tỉ lệ: nAg thu được = 2nglucose + fructose = 0,08 mol.
⇒ yêu cầu mAg thu được = 0,08 × 108 = 8,64 gam.
⇒ Điền đáp án: 8,64.
• một là chung công thức phân tử C6H12O6 có M = 180.
• hai là cùng tráng bạc theo tỉ lệ: 1glucose → 2Ag || 1fructose → 2Ag.
⇒ nglucose + fructose = 7,2 ÷ 180 = 0,04 mol.
Theo tỉ lệ: nAg thu được = 2nglucose + fructose = 0,08 mol.
⇒ yêu cầu mAg thu được = 0,08 × 108 = 8,64 gam.
⇒ Điền đáp án: 8,64.
Câu 39 [706001]: Để tráng một số lượng gương soi có diện tích bề mặt 0,5 m2 với độ dày 0,1 μm người ta đun nóng dung dịch chứa 30,6 gam glucose với một lượng dung dịch silver nitrate trong ammonia. Biết khối lượng riêng của bạc là 10,49 g/cm3, hiệu suất phản ứng tráng gương là 85% (tính theo glucose). Số lượng gương soi tối đa sản xuất được là bao nhiêu (Làm tròn đến hàng đơn vị)?
Thể tích bạc cần cho 1 tấm gương là VAg = 0,5.0,1.10-6 = 5.10-8 m3 = 5.10-2 cm3
Khối lượng Ag cho 1 tấm gương là mAg = 5.10-2. 10,49 = 0,5245 gam
Số mol của glucose là nC6H12O6 = 30,6 : 180 = 0,17 mol
Số mol Ag = 0,17 × 85% × 2 = 0,289 mol
Khối lượng Ag = 31,212 g
Sơ đồ phản ứng: C6H12O6 → 2Ag
Số tấm gương tối đa được sản xuất là
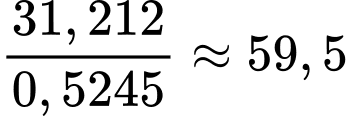
⟹Điền đáp án : 59
Khối lượng Ag cho 1 tấm gương là mAg = 5.10-2. 10,49 = 0,5245 gam
Số mol của glucose là nC6H12O6 = 30,6 : 180 = 0,17 mol
Số mol Ag = 0,17 × 85% × 2 = 0,289 mol
Khối lượng Ag = 31,212 g
Sơ đồ phản ứng: C6H12O6 → 2Ag
Số tấm gương tối đa được sản xuất là
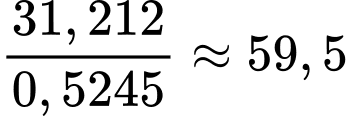
⟹Điền đáp án : 59
Câu 40 [705452]: Một nhóm học sinh tiến hành thí nghiệm thủy phân hoàn toàn tinh bột để điều chế glucose, sau đó thử tính chất của glucose bằng thuốc thử Fehling. Do quá trình không xảy ra các hiện tượng có thể quan sát nên để biết tiến trình của phản ứng thủy phân có thể sử dụng thêm iodine làm chất nhận biết. Các bước trong thí nghiệm này như sau:
(1) Sau khoảng 20 phút, hút lấy 1 – 2 giọt dung dịch trong ống nghiệm (a) nhỏ vào ống nghiệm (b) để kiểm tra tiến trình thủy phân.
(2) Cho vào ống nghiệm (a) dung dịch hồ tinh bột 2% và dung dịch H2SO4 10%, lắc đều rồi đặt ống nghiệm trong nồi nước sôi. Cho vào ống nghiệm (b) dung dịch I2 trong KI.
(3) Thêm tiếp vào ống nghiệm (c) vài giọt dung dịch CuSO4 5%, lắc đều rồi đun nóng ống nghiệm.
(4) Lấy khoảng 1 mL dung dịch đã thuỷ phân hoàn toàn sang ống nghiệm (c), thêm dần từng giọt dung dịch NaOH 10% cho đến môi trường kiềm.
Hãy sắp xếp số thứ tự các bước theo trình tự thành dãy bốn số để thực hiện thí nghiệm trên (ví dụ: 1234, 4213, ...).
(1) Sau khoảng 20 phút, hút lấy 1 – 2 giọt dung dịch trong ống nghiệm (a) nhỏ vào ống nghiệm (b) để kiểm tra tiến trình thủy phân.
(2) Cho vào ống nghiệm (a) dung dịch hồ tinh bột 2% và dung dịch H2SO4 10%, lắc đều rồi đặt ống nghiệm trong nồi nước sôi. Cho vào ống nghiệm (b) dung dịch I2 trong KI.
(3) Thêm tiếp vào ống nghiệm (c) vài giọt dung dịch CuSO4 5%, lắc đều rồi đun nóng ống nghiệm.
(4) Lấy khoảng 1 mL dung dịch đã thuỷ phân hoàn toàn sang ống nghiệm (c), thêm dần từng giọt dung dịch NaOH 10% cho đến môi trường kiềm.
Hãy sắp xếp số thứ tự các bước theo trình tự thành dãy bốn số để thực hiện thí nghiệm trên (ví dụ: 1234, 4213, ...).
Các bước trong thí nghiệm này như sau:
⭐Bước 1: Chuẩn bị dung dịch hồ tinh bột và H2SO4, sau đó đun nóng để thủy phân tinh bột thành glucose. Đây là bước khởi đầu.
⟶ (2) Cho vào ống nghiệm (a) dung dịch hồ tinh bột 2% và dung dịch H2SO4 10%, lắc đều rồi đặt ống nghiệm trong nồi nước sôi. Cho vào ống nghiệm (b) dung dịch I2 trong KI.
⭐Bước 2: Kiểm tra tiến trình thủy phân bằng cách lấy một ít dung dịch và nhỏ vào ống nghiệm chứa iodine. Nếu còn tinh bột, dung dịch sẽ có màu xanh tím; nếu đã thủy phân hoàn toàn, màu sẽ nhạt dần và mất hẳn.
⟶ (1) Sau khoảng 20 phút, hút lấy 1 – 2 giọt dung dịch trong ống nghiệm (a) nhỏ vào ống nghiệm (b) để kiểm tra tiến trình thủy phân.
⭐Bước 3: Khi dung dịch đã thủy phân hoàn toàn, lấy một phần dung dịch và trung hòa bằng NaOH để tạo môi trường kiềm, cần thiết trước khi thực hiện phản ứng với Fehling.
⟶ (4) Lấy khoảng 1 mL dung dịch đã thuỷ phân hoàn toàn sang ống nghiệm (c), thêm dần từng giọt dung dịch NaOH 10% cho đến môi trường kiềm.
⭐Bước 4: Thử tính chất của glucose bằng thuốc thử Fehling (trộn với CuSO4 và đun nóng để quan sát kết tủa đỏ gạch của Cu2O nếu có glucose).
⟶ (3) Thêm tiếp vào ống nghiệm (c) vài giọt dung dịch CuSO4 5%, lắc đều rồi đun nóng ống nghiệm.
Vậy thứ tự tiến hành các bước là: 2143
⇒ Điền đáp án: 2143
⭐Bước 1: Chuẩn bị dung dịch hồ tinh bột và H2SO4, sau đó đun nóng để thủy phân tinh bột thành glucose. Đây là bước khởi đầu.
⟶ (2) Cho vào ống nghiệm (a) dung dịch hồ tinh bột 2% và dung dịch H2SO4 10%, lắc đều rồi đặt ống nghiệm trong nồi nước sôi. Cho vào ống nghiệm (b) dung dịch I2 trong KI.
⭐Bước 2: Kiểm tra tiến trình thủy phân bằng cách lấy một ít dung dịch và nhỏ vào ống nghiệm chứa iodine. Nếu còn tinh bột, dung dịch sẽ có màu xanh tím; nếu đã thủy phân hoàn toàn, màu sẽ nhạt dần và mất hẳn.
⟶ (1) Sau khoảng 20 phút, hút lấy 1 – 2 giọt dung dịch trong ống nghiệm (a) nhỏ vào ống nghiệm (b) để kiểm tra tiến trình thủy phân.
⭐Bước 3: Khi dung dịch đã thủy phân hoàn toàn, lấy một phần dung dịch và trung hòa bằng NaOH để tạo môi trường kiềm, cần thiết trước khi thực hiện phản ứng với Fehling.
⟶ (4) Lấy khoảng 1 mL dung dịch đã thuỷ phân hoàn toàn sang ống nghiệm (c), thêm dần từng giọt dung dịch NaOH 10% cho đến môi trường kiềm.
⭐Bước 4: Thử tính chất của glucose bằng thuốc thử Fehling (trộn với CuSO4 và đun nóng để quan sát kết tủa đỏ gạch của Cu2O nếu có glucose).
⟶ (3) Thêm tiếp vào ống nghiệm (c) vài giọt dung dịch CuSO4 5%, lắc đều rồi đun nóng ống nghiệm.
Vậy thứ tự tiến hành các bước là: 2143
⇒ Điền đáp án: 2143
Câu 41 [704403]: Cho phương trình hóa học của các phản ứng được đánh số thứ tự từ 1 tới 4 dưới đây:
(1) (C6H10O5)n (tinh bột) + nH2O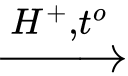 nC6H12O6 (glucose)
nC6H12O6 (glucose)
(2) C6H12O6 (glucose) 2C2H5OH + 2CO2
2C2H5OH + 2CO2
(3) C6H12O6 (glucose) 2CH3CH(OH)COOH
2CH3CH(OH)COOH
(4) C6H12O6 (glucose) + 2[Ag(NH3)2]OH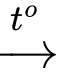 CH2OH(CHOH)4COONH4 + 2Ag + 3NH3 + H2O.
CH2OH(CHOH)4COONH4 + 2Ag + 3NH3 + H2O.
Gán số thứ tự phương trình hoá học của các phản ứng theo tên gọi: lên men rượu, thủy phân, lên men lactic, tráng gương và sắp xếp theo trình tự thành dãy bốn số (ví dụ: 1234, 4321,…).
(1) (C6H10O5)n (tinh bột) + nH2O
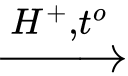 nC6H12O6 (glucose)
nC6H12O6 (glucose)(2) C6H12O6 (glucose)
 2C2H5OH + 2CO2
2C2H5OH + 2CO2(3) C6H12O6 (glucose)
 2CH3CH(OH)COOH
2CH3CH(OH)COOH(4) C6H12O6 (glucose) + 2[Ag(NH3)2]OH
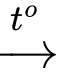 CH2OH(CHOH)4COONH4 + 2Ag + 3NH3 + H2O.
CH2OH(CHOH)4COONH4 + 2Ag + 3NH3 + H2O.Gán số thứ tự phương trình hoá học của các phản ứng theo tên gọi: lên men rượu, thủy phân, lên men lactic, tráng gương và sắp xếp theo trình tự thành dãy bốn số (ví dụ: 1234, 4321,…).
Tên gọi của các phản ứng là:
(1) Phản ứng thủy phân tinh bột: mô tả sự thủy phân tinh bột thành glucose (C6H12O6) với sự có mặt của nước.
Phản ứng: (C6H10O5)n (tinh bột) + nH2O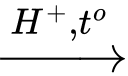 nC6H12O6 (glucose)
nC6H12O6 (glucose)
(2) Phản ứng lên men rượu: mô tả quá trình lên men glucose thành ethanol và CO2 dưới tác dụng của enzyme.
Phản ứng: C6H12O6 (glucose) 2C2H5OH + 2CO2
2C2H5OH + 2CO2
(3) Phản ứng lên men lactic acid: mô tả quá trình lên men glucose thành lactic acid (CH3CH(OH)COOH) dưới tác dụng của enzyme.
Phản ứng: C6H12O6 (glucose) 2CH3CH(OH)COOH
2CH3CH(OH)COOH
(4) Phản ứng tráng gương: là phản ứng giữa glucose và dung dịch Ag(NH3)2OH, trong đó Ag được tạo thành, thể hiện phản ứng tráng gương.
Phản ứng: C6H12O6 (glucose) + 2[Ag(NH3)2]OH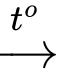 CH2OH(CHOH)4COONH4 + 2Ag + 3NH3 + H2O.
CH2OH(CHOH)4COONH4 + 2Ag + 3NH3 + H2O.
⇒ Thứ tự lần lượt ứng với các tên gọi phản ứng lên men rượu, thủy phân, lên men lactic, tráng gương là: 2134
⇒ Điền đáp án: 2134
(1) Phản ứng thủy phân tinh bột: mô tả sự thủy phân tinh bột thành glucose (C6H12O6) với sự có mặt của nước.
Phản ứng: (C6H10O5)n (tinh bột) + nH2O
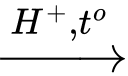 nC6H12O6 (glucose)
nC6H12O6 (glucose)(2) Phản ứng lên men rượu: mô tả quá trình lên men glucose thành ethanol và CO2 dưới tác dụng của enzyme.
Phản ứng: C6H12O6 (glucose)
 2C2H5OH + 2CO2
2C2H5OH + 2CO2(3) Phản ứng lên men lactic acid: mô tả quá trình lên men glucose thành lactic acid (CH3CH(OH)COOH) dưới tác dụng của enzyme.
Phản ứng: C6H12O6 (glucose)
 2CH3CH(OH)COOH
2CH3CH(OH)COOH(4) Phản ứng tráng gương: là phản ứng giữa glucose và dung dịch Ag(NH3)2OH, trong đó Ag được tạo thành, thể hiện phản ứng tráng gương.
Phản ứng: C6H12O6 (glucose) + 2[Ag(NH3)2]OH
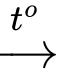 CH2OH(CHOH)4COONH4 + 2Ag + 3NH3 + H2O.
CH2OH(CHOH)4COONH4 + 2Ag + 3NH3 + H2O.⇒ Thứ tự lần lượt ứng với các tên gọi phản ứng lên men rượu, thủy phân, lên men lactic, tráng gương là: 2134
⇒ Điền đáp án: 2134
Câu 42 [705796]: Lactic acid hay acid sữa là hợp trong nhiều quá trình sinh hoá, lần đầu tiên được phân tách vào năm 1780 bởi nhà hoá học Thụy Điển Carl Wilhelm Scheele. Lactic acid có công thức phân tử C3H6O3, công thức cấu tạo CH3–CH(OH)–COOH.
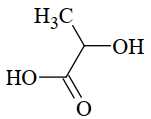
Khi vận động mạnh cơ thể không cung cấp đủ oxygen, thì cơ thể sẽ chuyển hoá glucose thành lactic acid (lactic acid tạo thành từ quá trình này sẽ gây mỏi cơ) theo phương trình sau:C6H12O6(aq) 2C3H6O3(aq);
2C3H6O3(aq); 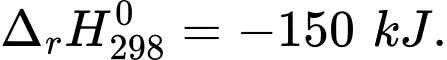 Biết rằng cơ thể chỉ cung cấp 98% năng lượng nhờ oxygen, năng lượng còn lại nhờ vào sự chuyển hoá glucose thành lactic acid. Giả sử một người chạy bộ trong một thời gian tiêu tốn 300 kcal. Tính khối lượng (g) lactic acid tạo ra từ quá trình này (Làm tròn đến hàng phần mười). Biết rằng 1 cal = 4,184 J.
Biết rằng cơ thể chỉ cung cấp 98% năng lượng nhờ oxygen, năng lượng còn lại nhờ vào sự chuyển hoá glucose thành lactic acid. Giả sử một người chạy bộ trong một thời gian tiêu tốn 300 kcal. Tính khối lượng (g) lactic acid tạo ra từ quá trình này (Làm tròn đến hàng phần mười). Biết rằng 1 cal = 4,184 J.

Khi vận động mạnh cơ thể không cung cấp đủ oxygen, thì cơ thể sẽ chuyển hoá glucose thành lactic acid (lactic acid tạo thành từ quá trình này sẽ gây mỏi cơ) theo phương trình sau:C6H12O6(aq)
 2C3H6O3(aq);
2C3H6O3(aq); 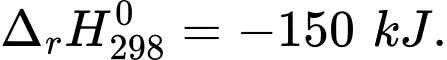 Biết rằng cơ thể chỉ cung cấp 98% năng lượng nhờ oxygen, năng lượng còn lại nhờ vào sự chuyển hoá glucose thành lactic acid. Giả sử một người chạy bộ trong một thời gian tiêu tốn 300 kcal. Tính khối lượng (g) lactic acid tạo ra từ quá trình này (Làm tròn đến hàng phần mười). Biết rằng 1 cal = 4,184 J.
Biết rằng cơ thể chỉ cung cấp 98% năng lượng nhờ oxygen, năng lượng còn lại nhờ vào sự chuyển hoá glucose thành lactic acid. Giả sử một người chạy bộ trong một thời gian tiêu tốn 300 kcal. Tính khối lượng (g) lactic acid tạo ra từ quá trình này (Làm tròn đến hàng phần mười). Biết rằng 1 cal = 4,184 J.
Năng lượng chạy Q = 300 kcal
Q (chuyển hóa G ⇒ Lac) = 2 ÷ 100 × 300 = 6 kcal
6 kcal = 6000 cal = 6000 × 4,184 = 25104 J = 25,104 kJ
Cứ 2 mol C3H6O3 ⇒ -150 kJ
x mol ⇒ 25,104 kJ
⇒ x = 0,33472 mol
⇒ m C3H6O3 = 30,12 (g)
⇒ Điền đáp án: 30,1
Q (chuyển hóa G ⇒ Lac) = 2 ÷ 100 × 300 = 6 kcal
6 kcal = 6000 cal = 6000 × 4,184 = 25104 J = 25,104 kJ
Cứ 2 mol C3H6O3 ⇒ -150 kJ
x mol ⇒ 25,104 kJ
⇒ x = 0,33472 mol
⇒ m C3H6O3 = 30,12 (g)
⇒ Điền đáp án: 30,1
Câu 43 [703021]: Dung dịch glucose ở dạng mạch hở có chứa nhóm aldehyde CHO nên có thể phản ứng oxi hóa khử với Cu(OH)2, các bước tiến hành thí nghiệm như sau:
▪ Bước 1: Chuẩn bị hai ống nghiệm có đánh số (1) và (2); thêm vào mỗi ống nghiệm khoảng 0,5 – 1,0 mL dung dịch CuSO4 5% và 1 mL dung dịch NaOH 10%, lắc nhẹ.
▪ Bước 2: Cho 3 mL dung dịch glucose 2% vào mỗi ống nghiệm, lắc nhẹ.
▪ Bước 3: Đun nhẹ ống (2) đến khi hoá chất trong ống nghiệm đổi màu hoàn toàn.
Cho các phương trình hóa học như sau:
(1) CuSO4 + 2NaOH Cu(OH)2↓ + Na2SO4.
Cu(OH)2↓ + Na2SO4.
(2) Cu(OH)2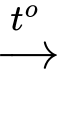 Cu2O.
Cu2O.
(3) 2C6H12O6 + Cu(OH)2 Cu(C6H11O6)2 + 2H2O.
Cu(C6H11O6)2 + 2H2O.
(4) C6H12O6 + 2Cu(OH)2 + NaOH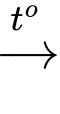 C5H11COONa + Cu2O↓ + 3H2O.
C5H11COONa + Cu2O↓ + 3H2O.
(5) 2C6H12O6 + O2 2C6H12O7.
2C6H12O7.
Hãy sắp xếp các phương trình hóa học dùng để giải thích cho các bước theo đúng thứ tự trong thí nghiệm trên (ví dụ: 123, 135, ...).
▪ Bước 1: Chuẩn bị hai ống nghiệm có đánh số (1) và (2); thêm vào mỗi ống nghiệm khoảng 0,5 – 1,0 mL dung dịch CuSO4 5% và 1 mL dung dịch NaOH 10%, lắc nhẹ.
▪ Bước 2: Cho 3 mL dung dịch glucose 2% vào mỗi ống nghiệm, lắc nhẹ.
▪ Bước 3: Đun nhẹ ống (2) đến khi hoá chất trong ống nghiệm đổi màu hoàn toàn.
Cho các phương trình hóa học như sau:
(1) CuSO4 + 2NaOH
 Cu(OH)2↓ + Na2SO4.
Cu(OH)2↓ + Na2SO4.(2) Cu(OH)2
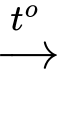 Cu2O.
Cu2O.(3) 2C6H12O6 + Cu(OH)2
 Cu(C6H11O6)2 + 2H2O.
Cu(C6H11O6)2 + 2H2O.(4) C6H12O6 + 2Cu(OH)2 + NaOH
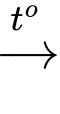 C5H11COONa + Cu2O↓ + 3H2O.
C5H11COONa + Cu2O↓ + 3H2O.(5) 2C6H12O6 + O2
 2C6H12O7.
2C6H12O7.Hãy sắp xếp các phương trình hóa học dùng để giải thích cho các bước theo đúng thứ tự trong thí nghiệm trên (ví dụ: 123, 135, ...).
Các bước tiến hành thí nghiệm phản ứng oxi hóa khử của dung dịch glucose ở dạng mạch hở với Cu(OH)2 như sau:
Bước 1: Phản ứng tạo kết tủa Cu(OH)2
CuSO4 + 2NaOH → Na2SO4 + Cu(OH)2
Bước 2: Tính chất của polyalcohol qua phản ứng của glucose với Cu(OH)2 ở nhiệt độ thường tạo dung dịch màu xanh lam.
Cu(OH)2 + 2C6H12O6 → [C6H11O6]2Cu + 2H2O
Bước 3: Đun nhẹ ống (2) thì xuất hiện kết tủa màu đỏ gạch, tính oxi hóa của glucose.
C6H12O6 + 2Cu(OH)2 + NaOH → C5H11O5COONa + Cu2O + 3H2O
→ Các phương trình hóa học xảy ra theo đúng thức tự các bước thí nghiệm là: 1→3→4.
⇒ Điền đáp án: 134
Bước 1: Phản ứng tạo kết tủa Cu(OH)2
CuSO4 + 2NaOH → Na2SO4 + Cu(OH)2
Bước 2: Tính chất của polyalcohol qua phản ứng của glucose với Cu(OH)2 ở nhiệt độ thường tạo dung dịch màu xanh lam.
Cu(OH)2 + 2C6H12O6 → [C6H11O6]2Cu + 2H2O
Bước 3: Đun nhẹ ống (2) thì xuất hiện kết tủa màu đỏ gạch, tính oxi hóa của glucose.
C6H12O6 + 2Cu(OH)2 + NaOH → C5H11O5COONa + Cu2O + 3H2O
→ Các phương trình hóa học xảy ra theo đúng thức tự các bước thí nghiệm là: 1→3→4.
⇒ Điền đáp án: 134
Câu 44 [703837]: Glucose là một loại monosaccharide với công thức phân tử C6H12O6 được tạo ra bởi thực vật và hầu hết các loại tảo trong quá trình quang hợp từ nước và CO2, sử dụng năng lượng từ ánh sáng mặt trời. Dung dịch glucose 5% (có khối lượng riêng D = 1,1 g/mL) là dung dịch đường tiêm tĩnh mạch, một loại thuốc thiết yếu quan trọng của Tổ chức Y tế Thế giới (WHO) và hệ thống y tế cơ bản. Phương trình nhiệt hóa học của phản ứng oxi hóa glucose:
C6H12O6(s) + 6O2(g) 6CO2(g) + 6H2O(g)
6CO2(g) + 6H2O(g)
Tính năng lượng tối đa mà một bệnh nhân có thể nhận được khi truyền cho bệnh nhân đó một chai 500 mL dung dịch glucose 5% (làm tròn đến hàng đơn vị). Biết các giá trị nhiệt tạo thành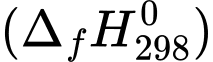 của các chất ở điều kiện chuẩn được cho trong bảng sau:
của các chất ở điều kiện chuẩn được cho trong bảng sau:
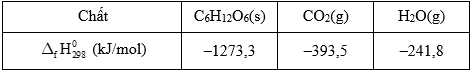
C6H12O6(s) + 6O2(g)
 6CO2(g) + 6H2O(g)
6CO2(g) + 6H2O(g)Tính năng lượng tối đa mà một bệnh nhân có thể nhận được khi truyền cho bệnh nhân đó một chai 500 mL dung dịch glucose 5% (làm tròn đến hàng đơn vị). Biết các giá trị nhiệt tạo thành
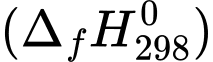 của các chất ở điều kiện chuẩn được cho trong bảng sau:
của các chất ở điều kiện chuẩn được cho trong bảng sau: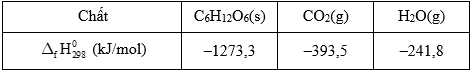
C6H12O6(s) + 6O2 ⟶ 6CO2(g) + 6H2O(g)
Biến thiên enthalpy của phản ứng là: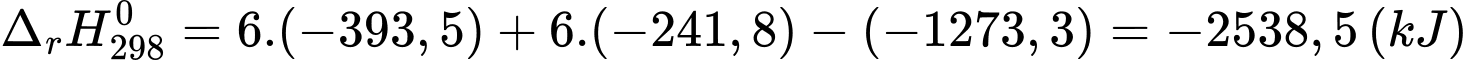
Khối lượng dung dịch glucose 5% là: 500.1,1 = 550 (gam)
Nhiệt lượng mà bệnh nhân nhận được là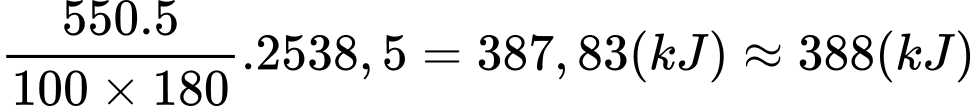
⇒ Điền đáp án: 388
Biến thiên enthalpy của phản ứng là:
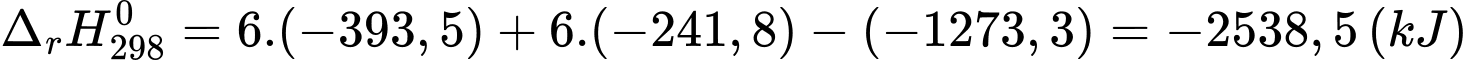
Khối lượng dung dịch glucose 5% là: 500.1,1 = 550 (gam)
Nhiệt lượng mà bệnh nhân nhận được là
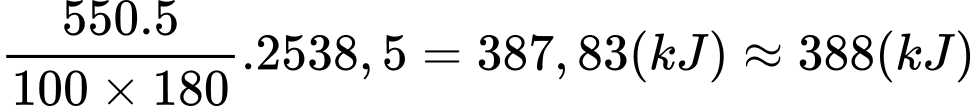
⇒ Điền đáp án: 388
Dạng 4: BÀI TẬP ĐỌC HIỂU – đọc thông tin và trả lời các câu hỏi sau đó
NĂNG LƯỢNG TRONG CƠ THỂ ĐẾN TỪ ĐÂU?
Hầu hết năng lượng cơ thể chúng ta cần đều đến từ carbohydrate và chất béo. Tinh bột thuộc loại carbohydrate, bị phân hủy trong ruột thành glucose, C6H12O6. Glucose hòa tan trong máu và trong cơ thể con người, nó được gọi là đường huyết. Nó được máu vận chuyển đến các tế bào, nơi mà nó phản ứng với O2 theo một loạt các bước, cuối cùng tạo ra CO2(g), H2O(1) và năng lượng: 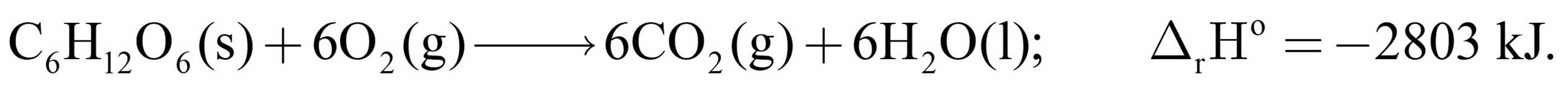
Vì carbohydrate bị phân hủy nhanh nên năng lượng của chúng được cung cấp nhanh chóng cho cơ thể và cơ thể chỉ dự trữ một lượng rất nhỏ carbohydrate. Sản phẩm của phản ứng là CO2 và H2O được đào thải ra bên ngoài bằng cách giải phóng vào trong máu. Sau đó, máu được chuyển đến thận để xử lý, tiếp tục được lưu trữ trong bàng quang và cuối cùng được đào thải ra khỏi cơ thể qua quá trình tiểu tiện.
Câu 45 [308334]: Nếu 1 gam glucose được chuyển hoá sẽ tạo ra bao nhiêu kJ?
A, 15,57 kJ.
B, 18,46 kJ.
C, 20,80 kJ.
D, 40,30 kJ.
HD: Quan sát lại tỉ lệ:
C6H12O6(s) + 6O2(g) → 6CO2(g) + 6H2O(l); ΔrHo = – 2803 kJ.
⇒ 1 mol C6H12O6 chuyển hóa tạo ra 2803 kJ
Tương ứng 180 gam C6H12O6 chuyển hóa tạo ra 2803 kJ
⇒ theo tỉ lệ 1 gam C6H12O6 chuyển hóa tạo ra 2803 ÷ 180 = 15,57 kJ ⇝ Chọn đáp án A. ♥ Đáp án: A
C6H12O6(s) + 6O2(g) → 6CO2(g) + 6H2O(l); ΔrHo = – 2803 kJ.
⇒ 1 mol C6H12O6 chuyển hóa tạo ra 2803 kJ
Tương ứng 180 gam C6H12O6 chuyển hóa tạo ra 2803 kJ
⇒ theo tỉ lệ 1 gam C6H12O6 chuyển hóa tạo ra 2803 ÷ 180 = 15,57 kJ ⇝ Chọn đáp án A. ♥ Đáp án: A
Câu 46 [308335]: Thể tích oxygen cần ở điều kiện chuẩn để oxy hóa hoàn toàn 15,0 g glucose là
A, 17,782 L.
B, 14,230 L.
C, 12,395 L.
D, 15,143 L.
HD: Quan sát lại tỉ lệ phản ứng:
C6H12O6(s) + 6O2(g) → 6CO2(g) + 6H2O(l); ΔrHo = – 2803 kJ.
⇒ Để oxi hóa hoàn toàn 15 gam glucose (tương ứng 15 ÷ 180 mol) thì theo tỉ lệ:
nO2 cần dùng = 6nglucose = 15 × 6 ÷ 180 = 0,5 mol.
⇒ Thể tích khí oxygen cần ở điều kiện chuẩn tương ứng là:
V = 0,5 × 24,79 = 12,395 lít ⇝ Chọn đáp án C. ♣ Đáp án: C
C6H12O6(s) + 6O2(g) → 6CO2(g) + 6H2O(l); ΔrHo = – 2803 kJ.
⇒ Để oxi hóa hoàn toàn 15 gam glucose (tương ứng 15 ÷ 180 mol) thì theo tỉ lệ:
nO2 cần dùng = 6nglucose = 15 × 6 ÷ 180 = 0,5 mol.
⇒ Thể tích khí oxygen cần ở điều kiện chuẩn tương ứng là:
V = 0,5 × 24,79 = 12,395 lít ⇝ Chọn đáp án C. ♣ Đáp án: C
Câu 47 [308336]: Lượng thể tích CO2 thô được tạo ra ở nhiệt độ cơ thể bình thường, 37 °C, và 1 atm khi tiêu thụ 10,0 g glucose trong phản ứng là
A, 8,26 L.
B, 8,47 L.
C, 6,79 L.
D, 10,45 L.
HD: Quan sát lại tỉ lệ phản ứng:
C6H12O6(s) + 6O2(g) → 6CO2(g) + 6H2O(l); ΔrHo = – 2803 kJ.
Ta có tỉ lệ: nCO2 = 6nglucose = 6 × 10 ÷ 180 = 1/3 mol.
Phương trình trạng thái: pV = nRT với hẳng số R = 0,082; p = 1 atm và T = 37 + 273 = 310 K.
⇒ V = 1/3 × 0,082 × 310 ÷ 1 ≈ 8,47 lít ⇝ Chọn đáp án B. ♦ Đáp án: B
C6H12O6(s) + 6O2(g) → 6CO2(g) + 6H2O(l); ΔrHo = – 2803 kJ.
Ta có tỉ lệ: nCO2 = 6nglucose = 6 × 10 ÷ 180 = 1/3 mol.
Phương trình trạng thái: pV = nRT với hẳng số R = 0,082; p = 1 atm và T = 37 + 273 = 310 K.
⇒ V = 1/3 × 0,082 × 310 ÷ 1 ≈ 8,47 lít ⇝ Chọn đáp án B. ♦ Đáp án: B
ĐIỀU HÒA NHIỆT ĐỘ CƠ THỂ
Đối với hầu hết chúng ta, câu hỏi "Bạn có bị sốt không?" là một trong những câu hỏi đầu tiên về chẩn đoán y tế. Thật vậy, sự chênh lệch chỉ một vài độ cho thấy có điều gì đó không ổn đang xảy ra trong cơ thể. Duy trì nhiệt độ gần như không đổi là một trong những chức năng sinh lý cơ bản của cơ thể con người. Để hiểu cơ chế làm nóng và làm mát của cơ thể hoạt động như thế nào, chúng ta có thể xem cơ thể như một hệ thống nhiệt động lực học. Cơ thể làm tăng năng lượng bên trong bằng cách ăn thức ăn từ môi trường xung quanh. Các loại thực phẩm, chẳng hạn như glucose (C6H12O6), được chuyển hóa tạo thành CO2 và H2O: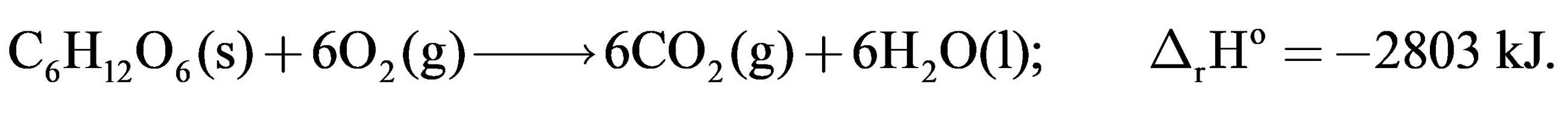
Khoảng 40% năng lượng được tạo ra cuối cùng được sử dụng để thực hiện công việc dưới dạng co cơ và hoạt động của tế bào thần kinh. Phần còn lại được giải phóng dưới dạng nhiệt, một phần được sử dụng để duy trì nhiệt độ cơ thể. Khi cơ thể tạo ra quá nhiều nhiệt, như khi gánh vật nặng, nó sẽ tiêu tán lượng nhiệt dư thừa ra môi trường xung quanh. Nhiệt được truyền từ cơ thể ra môi trường xung quanh chủ yếu bằng bức xạ, đối lưu và bay hơi.
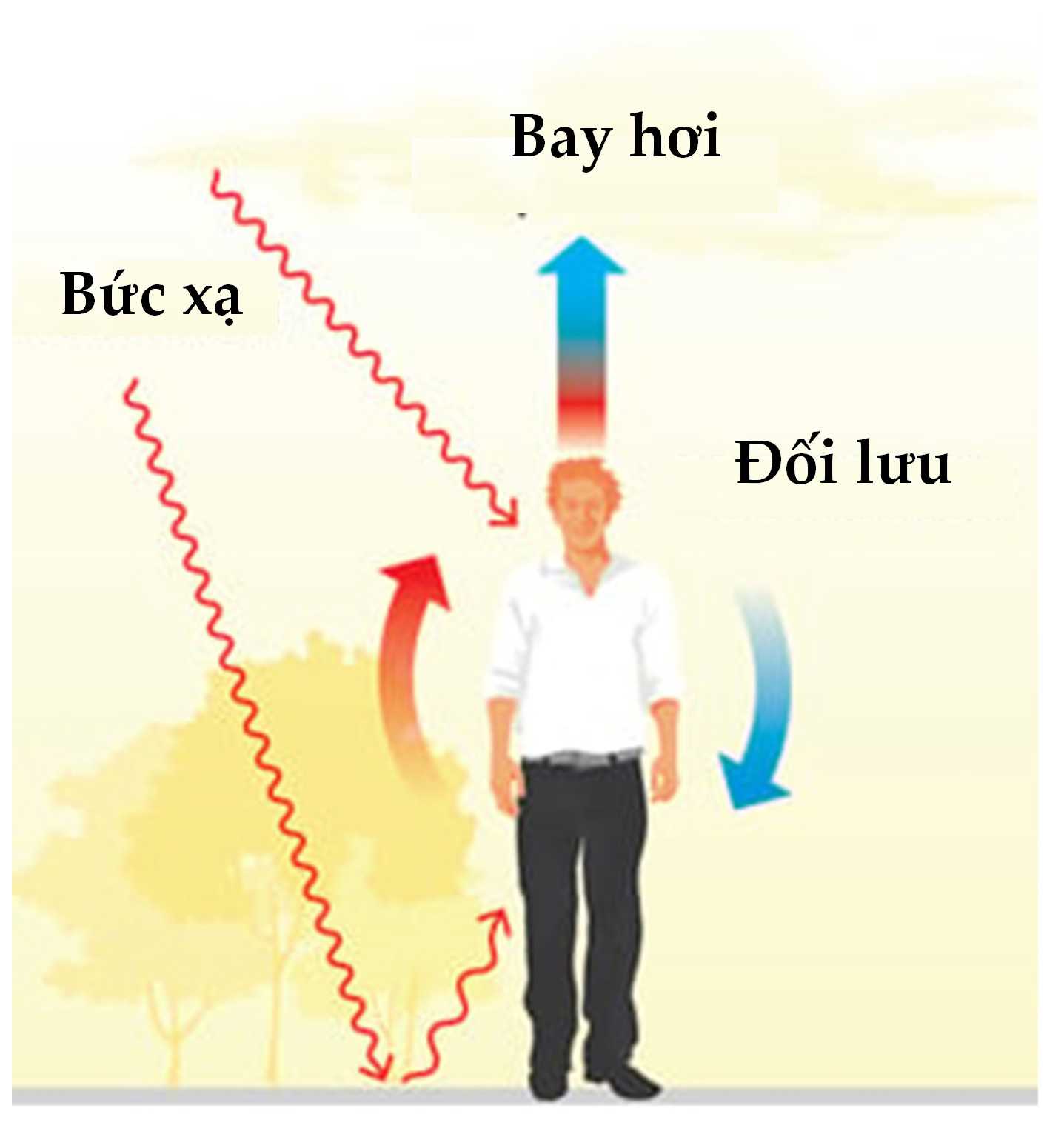
Hình II.5. Nhiệt truyền từ cơ thể ra môi trường xung quanh
▪ Bức xạ là sự mất nhiệt trực tiếp từ cơ thể ra môi trường xung quanh khi môi trường có nhiệt độ thấp hơn cơ thể, giống như một mặt bếp nóng tỏa nhiệt ra môi trường xung quanh.
▪ Đối lưu là sự mất nhiệt do không khí tiếp xúc với cơ thể. Không khí mát tiếp xúc với cơ thể, nhận nhiệt rồi nóng lên và di chuyển ra phía ngoài, luồng không khí mát thế chỗ, di chuyển vào bên trong. Quá trình liên tục được xảy ra một cách tuần hoàn. Quần áo làm giảm sự mất nhiệt đối lưu do đó chúng ta cảm thấy ấm hơn khi mặc quần áo trong thời tiết lạnh.
▪ Làm mát bay hơi xảy ra khi mồ hôi được tạo ra ở bề mặt da bởi tuyến mồ hôi (Hình II.6). Nhiệt được loại bỏ khỏi cơ thể khi mồ hôi bay hơi. Mồ hôi chủ yếu là nước, vì vậy quá trình này là sự chuyển đổi nhiệt của nước lỏng thành hơi nước:

Tốc độ làm mát do bay hơi giảm khi độ ẩm không khí tăng lên, đó là lý do tại sao chúng ta cảm thấy đổ mồ hôi nhiều hơn và khó chịu hơn vào những ngày nóng ẩm.
Khi nhiệt độ cơ thể trở nên quá cao, sự mất nhiệt tăng theo hai cách chính. Đầu tiên, lưu lượng máu gần bề mặt da tăng lên, cho phép tăng cường làm mát bằng bức xạ và đối lưu. Vẻ ngoài đỏ bừng của người nóng là do lưu lượng máu tăng lên. Thứ hai, chúng ta đổ mồ hôi, làm tăng khả năng làm mát bay hơi. Khi hoạt động ở cường độ cao, lượng mồ hôi có thể lên tới 2 đến 4 lít mỗi giờ. Kết quả là phải bổ sung, cung cấp nước cho cơ thể trong những giai đoạn này. Nếu cơ thể mất quá nhiều nước qua mồ hôi, nó sẽ không thể tự làm mát được nữa, điều này có thể dẫn đến kiệt sức vì nóng hoặc say nắng nghiêm trọng hơn. Tuy nhiên, bổ sung nước mà không bổ sung chất điện giải bị mất qua mồ hôi cũng có thể dẫn đến những vấn đề nghiêm trọng. Nếu mức sodium trong máu giảm quá thấp, sẽ xuất hiện chóng mặt, lú lẫn và tình trạng có thể trở nên nguy kịch. Uống đồ uống thể thao có chứa một số chất điện giải giúp ngăn ngừa vấn đề này.

Hình II.6. Đổ mồ hôi do bay hơi nước
Khi nhiệt độ cơ thể xuống quá thấp, lưu lượng máu đến bề mặt da giảm, do đó làm giảm sự mất nhiệt. Nhiệt độ thấp hơn cũng gây ra các cơn co thắt nhỏ không tự chủ của cơ (run rẩy); các phản ứng sinh hóa tạo ra năng lượng để thực hiện công việc này cũng sinh ra nhiệt cho cơ thể. Nếu cơ thể không thể duy trì ở nhiệt độ bình thường, tình trạng rất nguy hiểm được gọi là hạ thân nhiệt có thể xảy ra.
Câu 48 [308337]: Nhiệt được truyền từ cơ thể ra môi trường xung quanh khi nước trên da (mồ hôi) hoặc trong đường hô hấp chuyển thành khí. Nhiệt được giải phóng thông qua quá trình này là
A, Bức xạ.
B, Đối lưu.
C, Bay hơi.
D, Ngưng tụ.
HD: Dựa vào đoạn thông tin: "Làm mát bay hơi xảy ra khi mồ hôi được tạo ra ở bề mặt da bởi tuyến mồ hôi (Hình II.6). Nhiệt được loại bỏ khỏi cơ thể khi mồ hôi bay hơi. Mồ hôi chủ yếu là nước, vì vậy quá trình này là sự chuyển đổi nhiệt của nước lỏng thành hơi nước..."
⇒ Trả lời: Nhiệt được truyền từ cơ thể ra môi trường xung quanh khi nước trên da (mồ hôi) hoặc trong đường hô hấp chuyển thành khí. Nhiệt được giải phóng thông qua quá trình này là bay hơi ⇝ Chọn đáp án C. ♣ Đáp án: C
⇒ Trả lời: Nhiệt được truyền từ cơ thể ra môi trường xung quanh khi nước trên da (mồ hôi) hoặc trong đường hô hấp chuyển thành khí. Nhiệt được giải phóng thông qua quá trình này là bay hơi ⇝ Chọn đáp án C. ♣ Đáp án: C
Câu 49 [308338]: Cho quá trình bay hơi của nước như sau:
H2O(l) → H2O(g); ΔHo = 44,0 kJ/mol.
Trong quá trình đổ mồ hôi, cơ thể mất đi khoảng 3 L nước. Nhiệt lượng mà cơ thể cần cung cấp để chuyển toàn độ 3L nước này thành thể hơi là bao nhiêu? A, 1458,6 kJ.
B, 7333,3 kJ.
C, 4860,4 kJ.
D, 8951,5 kJ.
HD: Quan sát: H2O(l) → H2O(g); ΔHo = 44,0 kJ/mol.
⇒ 1 mol H2O bay hơi cơ thể cần cung cấp 44,0 kJ nhiệt (Δ > 0).
Tương ứng 18 gam H2O bay hơi cần cung cấp 44,0 kJ nhiệt.
► Khối lượng riêng nước cất là 1 gam ⇄ 1 mL ⇒ 18 gam tương ứng 18 mL ⇄ 0,018 L.
⇒ Nhiệt lượng mà cơ thể cần cung cấp để chuyển toàn độ 3 L nước thành thể hơi là:
Q = 3 ÷ 0,018 × 44,0 ≈ 7333,3 kJ ⇝ Chọn đáp án B. ♦ Đáp án: B
⇒ 1 mol H2O bay hơi cơ thể cần cung cấp 44,0 kJ nhiệt (Δ > 0).
Tương ứng 18 gam H2O bay hơi cần cung cấp 44,0 kJ nhiệt.
► Khối lượng riêng nước cất là 1 gam ⇄ 1 mL ⇒ 18 gam tương ứng 18 mL ⇄ 0,018 L.
⇒ Nhiệt lượng mà cơ thể cần cung cấp để chuyển toàn độ 3 L nước thành thể hơi là:
Q = 3 ÷ 0,018 × 44,0 ≈ 7333,3 kJ ⇝ Chọn đáp án B. ♦ Đáp án: B
Câu 50 [308339]: Năng lượng có thể được cung cấp cho cơ thể bằng cách ăn thức ăn. Các loại thực phẩm, chẳng hạn như glucose (C6H12O6), được chuyển hóa tạo thành CO2 và H2O:
C6H12O6(s) + 6O2(g) → 6CO2(g) + 6H2O(l); ΔrHo = – 2803 kJ.
Một loại thực phẩm cung cấp khoảng 5 gam glucose, giả sử toàn bộ lượng năng lượng được cơ thể hấp thụ. Tổng năng lượng mà cơ thể được nhận khi chuyển hoá loại thực phẩm này là bao nhiêu? A, 50,79 kJ.
B, 77,9 kJ.
C, 100,43 kJ.
D, 80,68 kJ.
HD: Quan sát lại quá trình chuyển hóa:
C6H12O6(s) + 6O2(g) → 6CO2(g) + 6H2O(l); ΔrHo = – 2803 kJ.
⇒ Tỉ lệ: cứ 1 mol glucose tương ứng 180 gam glucose chuyển hóa cơ thể nhận được 2803 kJ (Δ < 0).
⇒ chuyển hóa 5 gam glucose thì cơ thể nhận được 5 × 2803 ÷ 180 ≈ 77,9 kJ ⇝ Chọn đáp án B. ♦ Đáp án: B
C6H12O6(s) + 6O2(g) → 6CO2(g) + 6H2O(l); ΔrHo = – 2803 kJ.
⇒ Tỉ lệ: cứ 1 mol glucose tương ứng 180 gam glucose chuyển hóa cơ thể nhận được 2803 kJ (Δ < 0).
⇒ chuyển hóa 5 gam glucose thì cơ thể nhận được 5 × 2803 ÷ 180 ≈ 77,9 kJ ⇝ Chọn đáp án B. ♦ Đáp án: B
Dạng 5. Tự luận
Câu 51 [1010358]: Hoàn thiện thông tin còn thiếu trong bảng sau

Hoàn thiện bảng sau:
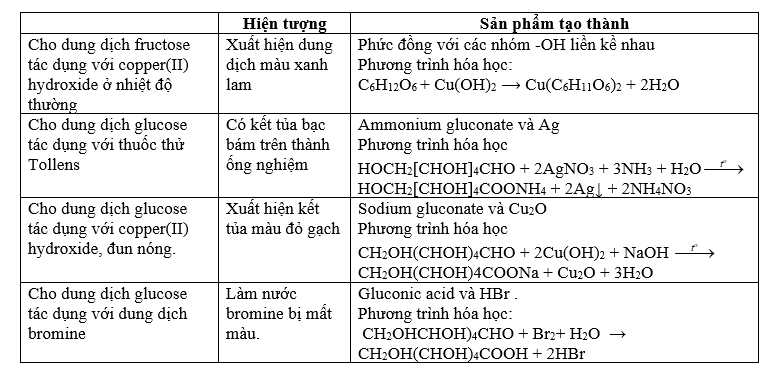

Câu 52 [1026597]: Hàng triệu hợp chất có thể tạo thành chỉ từ 3 nguyên tố carbon, hydrogen, và oxygen. Trong các phân tử đáng chú ý như vậy có đường. Sự đốt cháy các dẫn xuất chứa oxygen của hydrocarbon trong không khí cũng tạo ra CO2 và H2O và năng lượng. Nhiều chất có chức năng là nguồn cung cấp năng lượng trong quá trình trao đổi chất, chẳng hạn như đường glucose C6H12O6, phản ứng với O2 để tạo thành CO2 và H2O. Tuy nhiên, trong cơ thể chúng ta, các phản ứng diễn ra theo một loạt các bước, trải qua nhiều giai đoạn trung gian tại nhiệt độ cơ thể. Những phản ứng này thường được gọi là phản ứng oxy hóa hơn là phản ứng đốt cháy. Cứ mỗi 1 gam glucose được chuyển hóa sẽ tạo ra 16.74 kJ năng lượng.
a) Viết phương trình phản ứng oxy hóa glucose.
b) Nếu một mẫu chứa 5,00 gam C6H12O6 được chuyển hóa thì tạo ra mức năng lượng tối đa tính theo đơn vị kJ là bao nhiêu?
a) Viết phương trình phản ứng oxy hóa glucose.
b) Nếu một mẫu chứa 5,00 gam C6H12O6 được chuyển hóa thì tạo ra mức năng lượng tối đa tính theo đơn vị kJ là bao nhiêu?
a) Phản ứng oxy hóa glucsose là
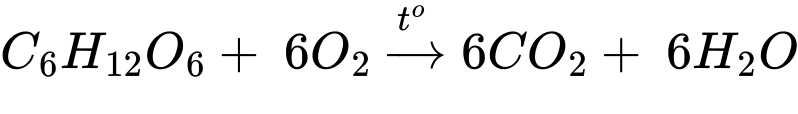
b) Cứ mỗi 1 gam glucose được chuyển hóa sẽ tạo ra 16,74 kJ năng lượng một mẫu chứa 5,00 gam C6H12O6 được chuyển hóa thì tạo ra mức năng lượng tối đa là
Q = 5 × 16,74 = 83,7 kJ
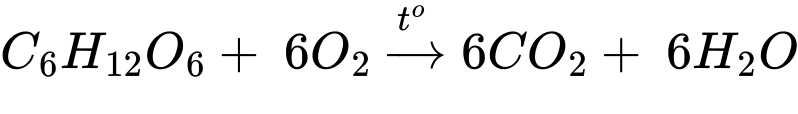
b) Cứ mỗi 1 gam glucose được chuyển hóa sẽ tạo ra 16,74 kJ năng lượng một mẫu chứa 5,00 gam C6H12O6 được chuyển hóa thì tạo ra mức năng lượng tối đa là
Q = 5 × 16,74 = 83,7 kJ
Câu 53 [1010366]: Hàm lượng glucose có trong mẫu dược phẩm có thể được xác định bằng
phương pháp chuẩn độ với iodine như sau:
Bước 1: Cho 20,00 mL một mẫu dung dịch chứa glucose vào 15,00 mL dung dịch iodine
0,10 M dư.
C6H12O6(aq) + I2(aq) + H2O(aq) → C6H12O7(aq) + 2HI(aq)
Bước 2: Sau đó, thêm vào dung dịch sau phản ứng vài giọt dung dịch X, rồi vừa lắc vừa nhỏ
từ từ dung dịch sodium thiosulfate (Na2S2O3) 0,05 M vào dung dịch ở trên đến khi mất màu
xanh thì dừng lại.
I2(aq) + 2Na2S2O3(aq) → 2NaI(aq) + Na2S4O6(aq)
Lặp lại 2 lần, thể tích dung dịch sodium thiosulfate đã dùng được ghi lại.

a) Phương pháp chuẩn độ trên thuộc loại chuẩn độ nào?
b) Nêu vai trò của dung dịch X trong phép chuẩn độ.
c) Xác định nồng độ glucose trong mẫu dung dịch ban đầu.
d) Nếu tăng nồng độ Na2S2O3 lên 2 lần thì thể tích Na2S2O3 cần dùng sẽ là bao nhiêu mL?
phương pháp chuẩn độ với iodine như sau:
Bước 1: Cho 20,00 mL một mẫu dung dịch chứa glucose vào 15,00 mL dung dịch iodine
0,10 M dư.
C6H12O6(aq) + I2(aq) + H2O(aq) → C6H12O7(aq) + 2HI(aq)
Bước 2: Sau đó, thêm vào dung dịch sau phản ứng vài giọt dung dịch X, rồi vừa lắc vừa nhỏ
từ từ dung dịch sodium thiosulfate (Na2S2O3) 0,05 M vào dung dịch ở trên đến khi mất màu
xanh thì dừng lại.
I2(aq) + 2Na2S2O3(aq) → 2NaI(aq) + Na2S4O6(aq)
Lặp lại 2 lần, thể tích dung dịch sodium thiosulfate đã dùng được ghi lại.

a) Phương pháp chuẩn độ trên thuộc loại chuẩn độ nào?
b) Nêu vai trò của dung dịch X trong phép chuẩn độ.
c) Xác định nồng độ glucose trong mẫu dung dịch ban đầu.
d) Nếu tăng nồng độ Na2S2O3 lên 2 lần thì thể tích Na2S2O3 cần dùng sẽ là bao nhiêu mL?
a) Phương pháp chuẩn độ trên thuộc loại chuẩn độ chuẩn độ ngược (back titration) hoặc chuẩn độ oxi hóa - khử (redox titration).
b) Dung dịch X trong phép chuẩn độ này là hồ tinh bột. Vai trò của hồ tinh bột là chất chỉ thị giúp nhận biết điểm cuối chuẩn độ. Khi dung dịch mất màu xanh (màu của phức tinh bột - iot) thì phản ứng đã hoàn tất.
c)
(1) C6H12O6 + I2 + H2O → C6H12O7 + 2HI
(2) I2 + 2Na2S2O3 → 2NaI + Na2S4O6
Thể tích trung bình của Na2S2O3 là
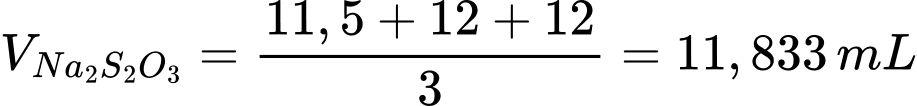
Số mol của Na2S2O3 là nNa2S2O3 = 11,833.10-3.0,05 = 0,0005965 mol
Từ PTHH (2) số mol của I2 là 0,000296 mol
Tổng số mol I2 ban đầu là nI2 = 0,015.0,1 = 0,0015 mol
Số mol I2 tham gia phản ứng (1) là nI2 (1) = 0,0015 – 0,000296 = 0,0001204 mol
Từ PTHH (1) số mol của glucose là 0,0001204 mol
Nồng độ của glucose trong mẫu ban đầu là
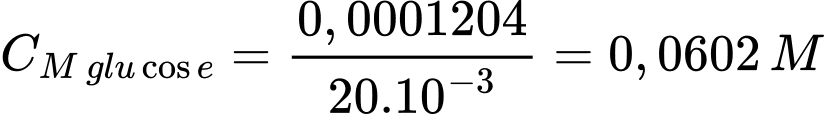
d) Khi tăng nồng độ của Na2S2O3 lên gấp đôi thì thể tích của Na2S2O3 cần dùng chuẩn độ giảm đi một nửa.
Thể tích Na2S2O3 cần dùng trung bình là VNa2S2O3 = 11,833/2 = 5,9165 mL
b) Dung dịch X trong phép chuẩn độ này là hồ tinh bột. Vai trò của hồ tinh bột là chất chỉ thị giúp nhận biết điểm cuối chuẩn độ. Khi dung dịch mất màu xanh (màu của phức tinh bột - iot) thì phản ứng đã hoàn tất.
c)
(1) C6H12O6 + I2 + H2O → C6H12O7 + 2HI
(2) I2 + 2Na2S2O3 → 2NaI + Na2S4O6
Thể tích trung bình của Na2S2O3 là
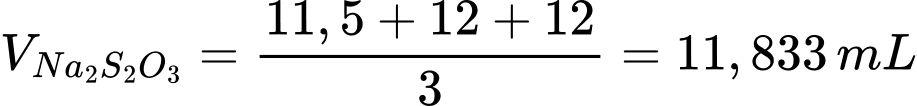
Số mol của Na2S2O3 là nNa2S2O3 = 11,833.10-3.0,05 = 0,0005965 mol
Từ PTHH (2) số mol của I2 là 0,000296 mol
Tổng số mol I2 ban đầu là nI2 = 0,015.0,1 = 0,0015 mol
Số mol I2 tham gia phản ứng (1) là nI2 (1) = 0,0015 – 0,000296 = 0,0001204 mol
Từ PTHH (1) số mol của glucose là 0,0001204 mol
Nồng độ của glucose trong mẫu ban đầu là
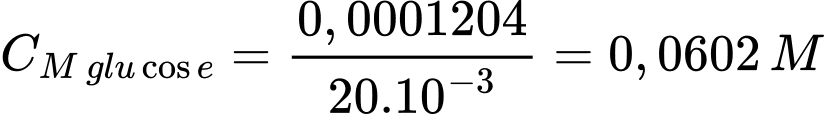
d) Khi tăng nồng độ của Na2S2O3 lên gấp đôi thì thể tích của Na2S2O3 cần dùng chuẩn độ giảm đi một nửa.
Thể tích Na2S2O3 cần dùng trung bình là VNa2S2O3 = 11,833/2 = 5,9165 mL
Câu 54 [1010361]: Nồng độ đường trong máu có thể được xác định bằng phương pháp
Hagedorn – Jensen. Phương pháp này dựa vào phản ứng của Na3[Fe(CN)6] oxi hoá đường
glucose có trong máu thành gluconic acid C5H11O5COOH (C6H12O7).
Quy trình phân tích như sau:
▪ Bước 1: Lấy 0,20 mL mẫu máu cho vào bình tam giác, thêm 5,00 mL dung dịch
Na3[Fe(CN)6] 4,012 mmol/L rồi đun cách thuỷ thu được dung dịch A.
▪ Bước 2: Thêm lần lượt dung dịch KI dư, ZnCl2 dư và CH3COOH vào dung dịch A.
▪ Bước 3: Sau khi các phản ứng xảy ra hoàn toàn, lượng I2 sinh ra tồn tại dưới dạng I3- được chuẩn độ bằng dung dịch Na2S2O3 4,00 mmol/L. Biết rằng phép chuẩn độ cần dùng vừa
đủ 3,28 mL dung dịch Na2S2O3 và pH của máu là 7,4.
Giả thiết các thành phần khác có trong máu không ảnh hưởng đến kết quả thí nghiệm. Các
phương trình xảy ra như sau:
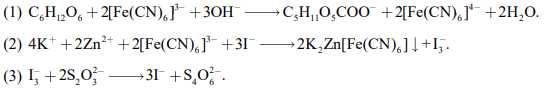
a) Ở bước 1, Na3[Fe(CN)6] đóng vai trò gì? Có thể dùng các muối FeCl3, Fe(NO3)3 thay cho
muối phức Na3[Fe(CN)6] được không? Giải thích.
b) Nêu ý nghĩa của việc thêm CH3COOH ở bước 2.
c) Dấu hiệu nào cho biết điểm kết thúc chuẩn độ ở bước 3?
d) Xác định nồng độ (mg/mL) của glucose có trong mẫu máu.
Hagedorn – Jensen. Phương pháp này dựa vào phản ứng của Na3[Fe(CN)6] oxi hoá đường
glucose có trong máu thành gluconic acid C5H11O5COOH (C6H12O7).
Quy trình phân tích như sau:
▪ Bước 1: Lấy 0,20 mL mẫu máu cho vào bình tam giác, thêm 5,00 mL dung dịch
Na3[Fe(CN)6] 4,012 mmol/L rồi đun cách thuỷ thu được dung dịch A.
▪ Bước 2: Thêm lần lượt dung dịch KI dư, ZnCl2 dư và CH3COOH vào dung dịch A.
▪ Bước 3: Sau khi các phản ứng xảy ra hoàn toàn, lượng I2 sinh ra tồn tại dưới dạng I3- được chuẩn độ bằng dung dịch Na2S2O3 4,00 mmol/L. Biết rằng phép chuẩn độ cần dùng vừa
đủ 3,28 mL dung dịch Na2S2O3 và pH của máu là 7,4.
Giả thiết các thành phần khác có trong máu không ảnh hưởng đến kết quả thí nghiệm. Các
phương trình xảy ra như sau:
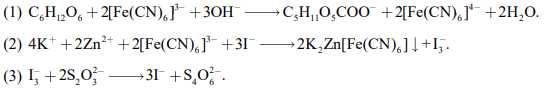
a) Ở bước 1, Na3[Fe(CN)6] đóng vai trò gì? Có thể dùng các muối FeCl3, Fe(NO3)3 thay cho
muối phức Na3[Fe(CN)6] được không? Giải thích.
b) Nêu ý nghĩa của việc thêm CH3COOH ở bước 2.
c) Dấu hiệu nào cho biết điểm kết thúc chuẩn độ ở bước 3?
d) Xác định nồng độ (mg/mL) của glucose có trong mẫu máu.
a) Trong bước 1, Na3[Fe(CN)6] được sử dụng để phản ứng với ion Fe3+ (có thể từ muối FeCl3 hoặc Fe(NO3)3) tạo thành phức chất tan [Fe(CN)6]3- và ion Na+. Phức chất này có màu vàng đặc trưng và tan trong nước, giúp chúng ta dễ dàng quan sát và theo dõi phản ứng.
Nếu thay thế bằng FeCl3 hoặc Fe(NO3)3, phản ứng có thể tạo ra kết tủa của Fe(OH)3 (nếu có mặt nước) hoặc các kết tủa khác, làm mất tính chất đặc trưng của phản ứng và khó quan sát, theo dõi.
FeCl3 và Fe(NO3)3: là các muối của sắt (III) và có thể tan trong nước tạo ra ion Fe3+. Tuy nhiên, khi phản ứng với các chất khác, chúng có thể tạo ra các kết tủa khác nhau do sự kết hợp của Fe3+ với các anion khác có trong dung dịch (như Cl- hoặc NO3-).
b) CH3COOH thêm vào với mục đích tạo môi trường acid và trung hòa lượng OH- còn dư.
c) Trong phương pháp Hagedorn - Jensen phân tích glucose huyết, điểm tương đương được xác định thông qua chuẩn độ iodine bằng sodium thiosulfate với sự có mặt của hồ tinh bột làm chỉ thị. Khi chuẩn độ, dung dịch có màu xanh tím do iodine tạo phức với hồ tinh bột, và điểm tương đương là thời điểm màu xanh tím biến mất hoàn toàn, chứng tỏ iodine đã phản ứng hết — từ đó xác định được lượng glucose trong mẫu.
d)
Ta có số mol của Na2S2O3 đã dùng là nNa2S2O3 =3,28.10−3.4.10−3 = 1,312.10−5 (mol).
Số mol Na3[Fe(CN)6] ban đầu là nNa3[Fe(CN)6] = 4,012.10−3⋅5⋅10−3 = 2,006⋅10−5(mol).
Lượng Na3[Fe(CN)6] tham gia phản ứng (2) là lượng còn dư sau khi tham gia phản ứng (1).
Từ PTHH (2) và (3) số mol Na3[Fe(CN)6] là 1,312.10−5 (mol).
Vậy số mol Na3[Fe(CN)6] đã dùng cho phản ứng (1) là:
2,006⋅10−5 − 1,312⋅10−5 =6,94⋅10−6(mol)
Từ PTHH (1) số mol của C6H12O6 là 3,47.10-6 mol
Nồng độ (mg/mL)mg/mL) của glucose có trong mẫu máu là:
3,47⋅10−6⋅103⋅180/0,2=3,123mg/mL.
b) CH3COOH thêm vào với mục đích tạo môi trường acid và trung hòa lượng OH- còn dư.
c) Trong phương pháp Hagedorn - Jensen phân tích glucose huyết, điểm tương đương được xác định thông qua chuẩn độ iodine bằng sodium thiosulfate với sự có mặt của hồ tinh bột làm chỉ thị. Khi chuẩn độ, dung dịch có màu xanh tím do iodine tạo phức với hồ tinh bột, và điểm tương đương là thời điểm màu xanh tím biến mất hoàn toàn, chứng tỏ iodine đã phản ứng hết — từ đó xác định được lượng glucose trong mẫu.
d)
Ta có số mol của Na2S2O3 đã dùng là nNa2S2O3 =3,28.10−3.4.10−3 = 1,312.10−5 (mol).
Số mol Na3[Fe(CN)6] ban đầu là nNa3[Fe(CN)6] = 4,012.10−3⋅5⋅10−3 = 2,006⋅10−5(mol).
Lượng Na3[Fe(CN)6] tham gia phản ứng (2) là lượng còn dư sau khi tham gia phản ứng (1).
Từ PTHH (2) và (3) số mol Na3[Fe(CN)6] là 1,312.10−5 (mol).
Vậy số mol Na3[Fe(CN)6] đã dùng cho phản ứng (1) là:
2,006⋅10−5 − 1,312⋅10−5 =6,94⋅10−6(mol)
Từ PTHH (1) số mol của C6H12O6 là 3,47.10-6 mol
Nồng độ (mg/mL)mg/mL) của glucose có trong mẫu máu là:
3,47⋅10−6⋅103⋅180/0,2=3,123mg/mL.