Dạng 1: TRẮC NGHIỆM KHÁCH QUAN: mỗi câu hỏi chỉ có một đáp án đúng.
(Áp dụng với amine mạch hở) Đáp án: A
Số electron hóa trị của n nguyên tử C bằng 4, của 1 nguyên tử N bằng 3
Giữa n nguyên tử C và 1 nguyên tử N hình thành n liên kết σ bằng 2n electron hóa trị.
⇒ Tổng số electron hóa trị dùng để tạo liên kết C-C và C-N là 2n
⟹ Chọn đáp án B Đáp án: B
✘ A. Sai. Nguyên tử N trong amine còn cặp electron tự do chưa tham gia vào liên kết hóa học.
✔ B. Đúng. Nguyên tử N trong amine ở trạng thái lai hóa Sp3 nên còn 1 cặp electron tự do chưa tham gia liên kết.
✘ C. Sai. Nguyên tử N trong amine có thể liên kết với hai nguyên tử H, tạo ra amine bậc một; liên kết với một nguyên tử H, tạo ra amine bậc hai hoặc liên kết với ba nguyên tử C, tạo ra amine bậc ba.
✘ D. Sai. Nguyên tử N trong amine còn cặp electron tự do chưa tham gia vào liên kết hóa học. Đáp án: B
⇒ Chọn đáp án D Đáp án: D
+) Methylamine: CH3–NH2
+) Dimethylamine: NH(CH3)2
+) Trimethylamine: N(CH3)3
+) Ethylamine: CH3–CH2–NH2
Aniline (C6H5NH2)là một amine thơm (có nhóm –NH2 gắn vào vòng benzene), tồn tại ở trạng thái lỏng trong điều kiện thường.
⇒ Chọn đáp án A Đáp án: A
Phân tích các đáp án:
❌A. acetone : CH3COCH3 ⟶ ketone
✔️B. methylamine : CH3NH2 ⟶ amine bậc 1
❌C. ethyl formate : HCOOC2H5 ⟶ ester
❌D. ethane : C2H6 ⟶ alkane
⟹ Chọn đáp án B Đáp án: B
Vì vậy ở đây muốn có liên kết Hydrogen thì các amine này phải còn H gắn trực tiếp với N.
(CH3)3N không còn H gắn vào N nên amine này không tạo được liên kết hydrogen với nhau.
⟹ Chọn đáp án D
Dẫn xuất halide < Aldehyde, ketone, ester <Amine < Alcohol < Carboxylic acid
Ester không có khả năng tạo liên kết hydrogen nên liên kết giữa các phân tử kém bền, dễ bay hơi
⇒ Nhiệt độ sôi thấp
Phân tích các đáp án:
❌A.CH3COOH.⟶ Carboxylic acid
❌B.C6H5NH2.⟶ Amine
❌C.C2H5OH.⟶ Alcohol
✔️D.HCOOCH3.⟶ Ester
⟹ Chọn đáp án D
Đáp án: D
Amine < Alcohol < Acid (Do lực liên kết hydrogen liên phân tử tăng dần)
Trong dãy đồng đẳng của amine, nhiệt độ sôi tăng dần theo chiều tăng phân tử khối nên nhiệt độ sôi của methylamine < ethylamine.
⇒ (3) methylamine < (2) ethylamine < (1) ethyl alcohol < (4) acetic acid Đáp án: B
- Độ tan của C4H9OH < C3H7OH do mạch C càng lớn thì độ tan càng giảm
Độ tan của C3H7OH < C3H5(OH)3 do số lượng nhóm -OH
- Phenol (C6H5OH) và aniline (C6H5NH2) ít tan trong nước do phân lớp, chúng chỉ tan trong nước nóng.
⟹ Chọn đáp án B Đáp án: B
❌ B. Methyl formate (HCOOCH3) là một ester, thường có mùi thơm dễ chịu, không có mùi khai.
❌ C. Aniline (C6H5NH2) là một amine thơm, có mùi đặc trưng (hắc và khó chịu), nhưng không phải mùi khai.
❌ D. Glycine (H2NCH2COOH) là một amino acid không có mùi khai, mà có mùi nhẹ hoặc không mùi.
⇒ Chọn đáp án A Đáp án: A
- Barium hydroxide là chất điện li mạnh
⇒ Dimethylamine là chất điện li yếu Đáp án: C
⟹ Chọn đáp án A Đáp án: A
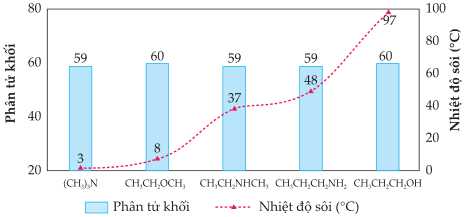
Dựa vào biểu đồ trên, cho biết chất nào có nhiệt độ sôi thấp nhất?
(CH3)3N là amin bậc ba: Không có nguyên tử H liên kết với N, nên không tạo được liên kết hydrogen nội phân tử hay với nước. Chỉ có lực Vander Waals yếu → dễ bay hơi, → nhiệt độ sôi thấp nhất.
Các chất khác có thể tạo liên kết hydrogen hoặc có lực tương tác phân tử mạnh hơn.
⟹ Chọn đáp án D Đáp án: D
Dạng 2: TRẮC NGHIỆM ĐÚNG SAI – mỗi ý a), b), c), d) chọn đúng hoặc sai.
✔ a. Đúng. Dimethylamine có tên thay thế là N-methylmethanamine.
✘ b. Sai. Dimethylamine có CTCT là CH3-NH-CH3 → CTPT là C2H7N.
✘ c. Sai. Dimethylamine có nhóm -NH- nên nó thuộc amine bậc hai.
✘ d. Sai. Methylamine có CTPT là CH5N → 2 chất này không phải đồng phân.
✔ a. Đúng. CTCT của trimethylamine là CH3-N(CH3)-CH3 → CTPT là C3H9N
✔ b. Đúng. Trimethylamine là amine bậc ba vì thấy trong phân tử, nhóm chức amine không còn H.
✔ c. Đúng. Trimethylamine có tên thay thế là N,N-dimethylmethanamine.
✘ d. Sai. Ở điều kiện thường trimethylamine là chất khí.
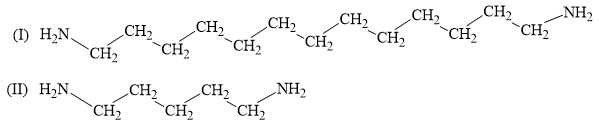
Biết rằng alkane có 13 nguyên tử carbon mạch thẳng có tên là tridecane.
Phân tích các đáp án:
✔️A. Đúng. Tên thay thế của amine (I) là tridecane-1,13-diamine.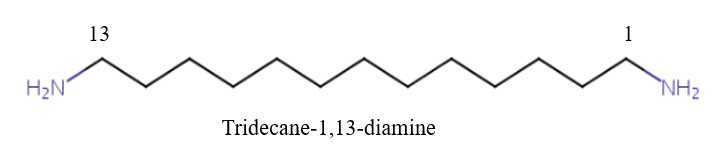
✔️B. Đúng. Đồng đẳng là những chất có cùng nhóm chức, tính chất hóa học tương tự nhau, nhưng khác nhau về số nhóm –CH2– trong mạch carbon.
Hai amine (I) và (II) đều thuộc cùng một dãy đồng đẳng.
❌C. Sai. Công thức phân tử của amine (I) là C13H30N2; amine (II) là C5H14N2. Không có cùng công thức đơn giản nhất.
❌D. Sai. Nhiệt độ sôi của amine (I) cao hơn amine (II) do amine (I) có phân tử khối lớn hơn amine (II), có tương tác Val deer Waals lớn hơn nên có nhiệt độ sôi lớn hơn.
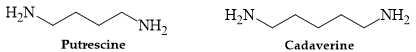
Phân tích các đáp án:
✔️(a) – Đúng. Trimethylamine có công thức cấu tạo: (CH3)3N; công thức phân tử là C3H9N.
✔️(b) – Đúng. Alkylamine là các hợp chất hữu cơ trong đó nhóm amine (–NH2, –NHR hoặc –NR2) gắn trực tiếp vào một nhóm alkyl (mạch hydrocarbon no).
Trimethylamine, putrescine và cadaverine đều là alkylamine.
✔️(c) – Đúng. Tên thay thế của cadaverine là pentane -1,5-diamine.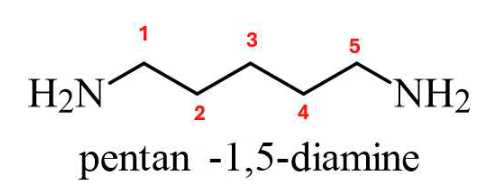
❌(d) – Sai. Chỉ có putrescine và cadaverine tạo được liên kết hydrogen liên phân tử. Putrescine và cadaverine đều là diamine, chứa hai nhóm –NH2 có liên kết N–H, nên có thể tạo liên kết hydrogen giữa các phân tử với nhau.
Trong khi đó, trimethylamine là amin bậc ba, không có liên kết N–H mà chỉ có cặp electron tự do trên nguyên tử nitrogen, nên không thể hình thành liên kết hydrogen liên phân tử với chính nó.
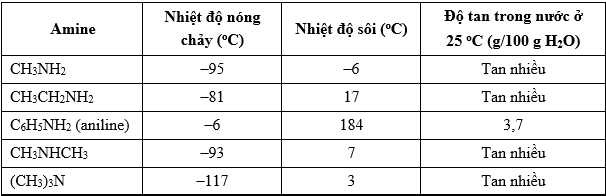
❌(a) – Sai. Từ bảng số liệu, Ở điều kiện thường (to = 25 oC) có CH3NH2, CH3CH2NH2, CH3NHCH3, (CH3)3N là chất khí ở điều kiện thường. Aniline có nhiệt độ sôi 184 oC, nên là chất lỏng ở nhiệt độ thường.
❌(b) – Sai. Trong bảng trên, nhiệt độ nóng chảy của aniline là lớn nhất (-6 oC), trimethylamine là nhỏ nhất (-117 oC).
✔️(c) – Đúng. Khi số nguyên tử carbon trong gốc hydrocarbon tăng, độ tan trong nước của các amine giảm. Nguyên nhân là do phần hydrocarbon không phân cực trong phân tử ngày càng lớn, làm giảm khả năng tạo liên kết hydrogen với nước. Điều này khiến phân tử amine trở nên kị nước hơn, dẫn đến giảm độ tan trong dung môi phân cực như nước.
✔️(d) – Đúng. Khi so sánh các amine với các hydrocarbon có cùng số nguyên tử carbon hoặc phân tử khối tương đương, nhiệt độ sôi của amine thường cao hơn. Nguyên nhân là do amine, đặc biệt là amine bậc một và hai, có thể tạo liên kết hydrogen giữa các phân tử, trong khi hydrocarbon chỉ có lực hút phân tử yếu kiểu Van der Waals. Liên kết hydrogen làm tăng năng lượng cần thiết để các phân tử tách khỏi nhau, từ đó làm tăng nhiệt độ sôi.
Dạng 3: TRẮC NGHIỆM YÊU CẦU TRẢ LỜI NGẮN
Với số nguyên tử carbon n = 5 → Công thức phân tử là C5H13N
Số nguyên tử hydrogen là 13.
⟹ Điền đáp án: 13
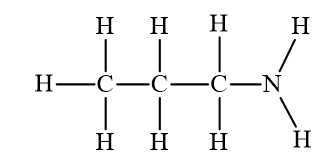
Số liên kết σ trong phân tử C3H9N là 12.
⟹ Điền đáp án: 12
(3) Methylamine (CH3NH2): amine bậc một, có khả năng tạo liên kết hydrogen yếu hơn alcohol và acid.
(2) Ethylamine (CH3CH2NH2): amine bậc một, mạch dài hơn methylamine
→ phân tử lớn hơn → nhiệt độ sôi cao hơn methylamine.
(1) Ethyl alcohol (ethanol, CH3CH2OH): tạo được liên kết hydrogen mạnh
→ nhiệt độ sôi cao hơn các amine cùng khối lượng.
(4) Acetic acid (CH3COOH): tạo liên kết hydrogen kép (dimer hóa trong pha lỏng)
→ nhiệt độ sôi rất cao.
Thứ tự của các chất theo chiều tăng dần nhiệt độ sôi là:
(3) methylamine; (2) ethylamine; (1) ethyl alcohol; (4) acetic acid.
⟹ Điền đáp án: 3214
(1) ở điều kiện thường là chất khí, mùi khai, (2) dễ tan trong nước,
(3) là amine bậc một, (4) thuộc dãy đồng đẳng amine no, đơn chức, mạch hở.
Số nhận định đúng với cả methylamine và ethylamine là
(1) Đúng. Ở điều kiện thường, CH3NH2 và C2H5NH2 là chất khí, có mùi khai.
(2) Đúng. Cả 2 amine đều dễ tan trong nước vì hình thành được liên kết hydrogen với nước.
(3) Đúng. 2 amine đều là amine bậc một.
(4) Đúng. CH3NH2 và C2H5NH2 cùng thuộc dãy đồng đẳng amine no, đơn chức, mạch hở vì cùng là amine bậc một và hơn kém nhau 1 nhóm -CH2
⇒ Điền đáp án: 4
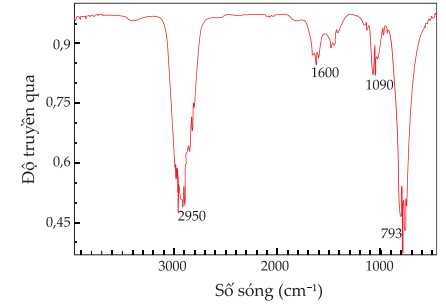
⇒ Điền đáp án: 2950
Dạng 4. Tự luận
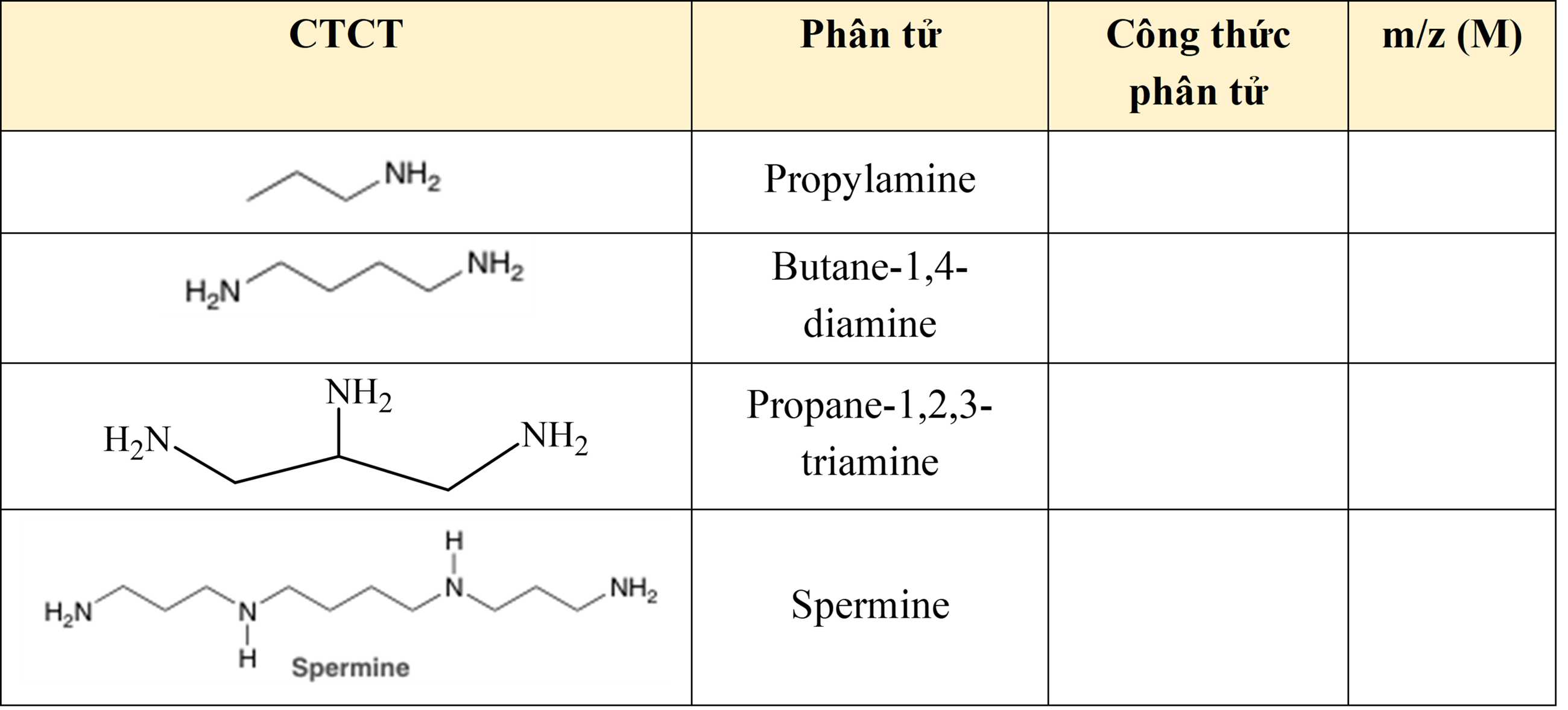
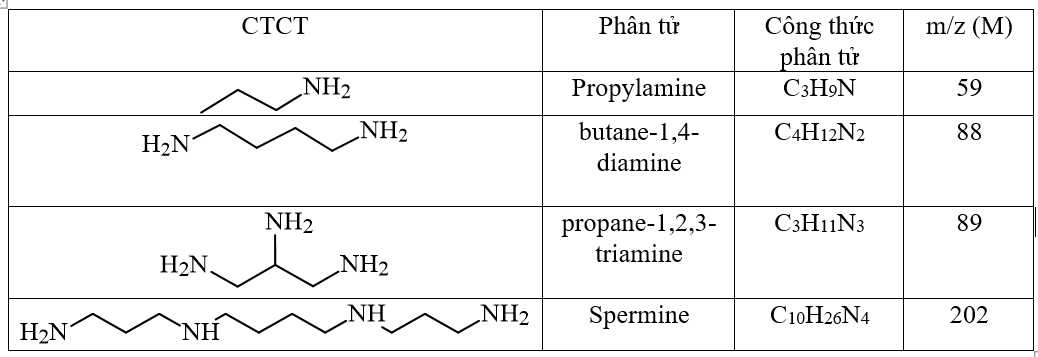
Nhận xét về số nguyên tử H khi số nitrogen:
+ Số N chẵn ⟶ m/z chẵn
+ Số N lẻ ⟶ m/z lẻ
b) Vì sao các amine có nhiệt độ sôi cao hơn hydrocarbon có cùng số nguyên tử carbon hoặc có phân tử khối tương đương?
- Amine có số nguyên tử carbon nhỏ tan tốt trong nước vì chúng có thể tạo liên kết hydrogen với nước nhờ cặp electron tự do trên nguyên tử nitrogen. Trong khi đó, dẫn xuất halogen không tạo được liên kết hydrogen hiệu quả nên tan kém hơn trong nước.
- Amine là hợp chất phân cực, có khả năng tương tác mạnh với dung môi phân cực như nước. Dẫn xuất halogen tuy cũng phân cực, nhưng mức độ tương tác với nước yếu hơn do không có khả năng hình thành liên kết hydrogen bền vững như amine.
b) Amine có nhiệt độ sôi cao hơn hydrocarbon có cùng số nguyên tử carbon hoặc phân tử khối tương đương vì chúng có khả năng tạo liên kết hydrogen liên phân tử nhờ nguyên tử nitrogen mang cặp electron tự do. Liên kết hydrogen làm tăng lực hút giữa các phân tử, khiến chúng khó bay hơi hơn và cần nhiều năng lượng hơn để chuyển sang pha khí. Trong khi đó, hydrocarbon là các hợp chất không phân cực, chỉ có lực Van der Waals yếu nên dễ bay hơi và có nhiệt độ sôi thấp hơn.
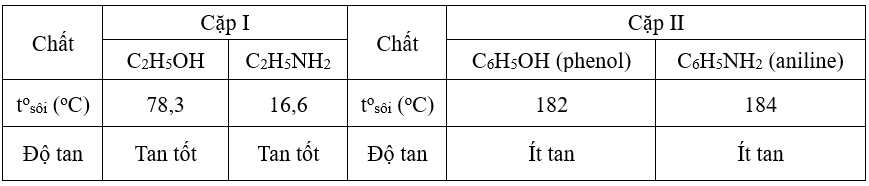
Cặp II gồm phenol (C6H5OH) và aniline (C6H5NH2) đều có chứa vòng benzene, làm giảm đáng kể độ tan trong nước so với cặp I. Dù vẫn có nhóm –OH hoặc –NH2 tạo được liên kết hydrogen, nhưng ảnh hưởng kị nước của vòng benzene làm cho chúng tan kém. Cả phenol và aniline đều có khối lượng phân tử lớn hơn nên có nhiệt độ sôi cao hơn so với các chất trong cặp I.
So sánh chung, cặp I tan tốt hơn trong nước và dễ bay hơi hơn do có mạch ngắn và phân cực cao.
Cặp II ít tan hơn và có nhiệt độ sôi cao hơn vì chứa vòng benzene, làm tăng khối lượng phân tử và giảm khả năng tương tác với nước.
Một nhà sản xuất vì tham lợi nhuận đã pha loãng và cho melamine vào sữa. Với 500 lít sữa loại có nồng độ đạm là 17% (khối lượng riêng của loại sữa này là 1,1 gam/mL), họ đã pha thêm 10 lít nước để được hỗn hợp có thể tích 510 lít. Cho khối lượng riêng của nước là 1,0 gam/ml.
a) Tại sao melamine được sử dụng để tăng độ đạm trong các loại thực phẩm.
b) Tính khối lượng melamine nhà sản xuất đã cho vào 510 lít sữa để đạt tiêu chuẩn (có độ đạm 17%).
b) Gọi số mol C3H6N6 đã thêm vào là x mol ⟹ nN = 6x mol ⟹ mN = 6x .14 = 84x (g) = 0,084x (kg)
- m sữa = 500 .1,1 = 550 (kg) ⟹ mNitrogen = 550 . 17% = 93,5 (kg)
- m H2O = 10 . 1 = 10 (kg)
- m melamine = 126x (gam) = 0,126x (kg)
⟹ mdd = 550 + 10 + 0,126x = 560 + 0,126x (kg), mNitrogen = 93,5 + 0,084x (kg)
⟹ %mNitrogen = (93,5 + 0,084x) / (560 + 0,126x) = 17% ⟹ x = 27,16 (mol)
⟹ mN = 27,165 . 126 = 3422,16 (gam)
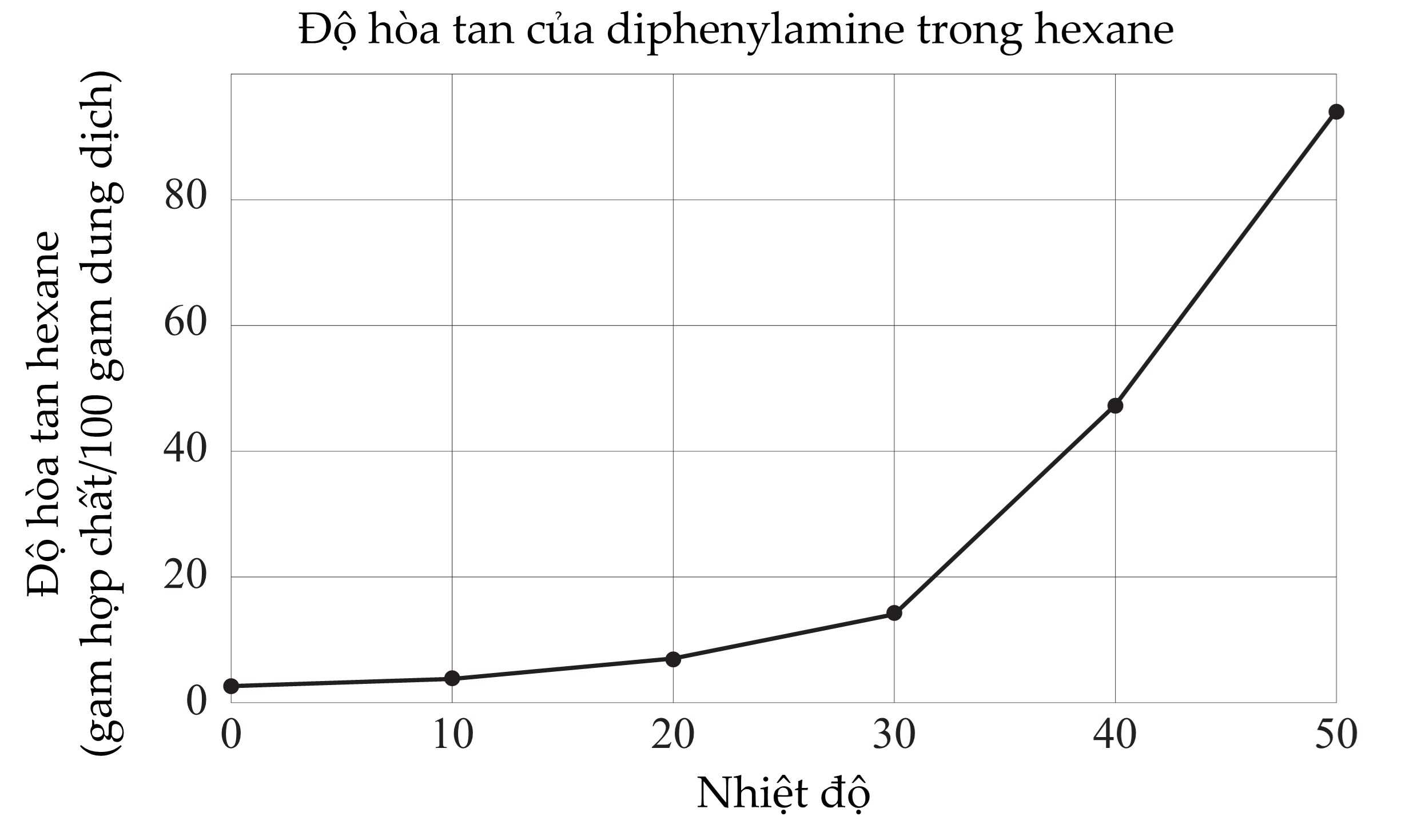
a) Độ tan của diphenylamine phụ thuộc vào các yếu tố nào?
b) Nhận xét độ tan của diphenylamine tạo khoảng nhiệt độ thấp và nhiệt độ cao. Từ đó kết luận rằng diphenylamine có thể được kết tinh tốt hay không?
b) Nhận xét độ tan của diphenylamine ở nhiệt độ thấp và cao:
- Ở nhiệt độ thấp, độ tan của diphenylamine rất kém, chỉ tan được rất ít trong dung môi.
- Ở nhiệt độ cao, độ tan của diphenylamine tăng mạnh, dễ dàng hoà tan hoàn toàn trong dung môi thích hợp như ethanol, ether, hay acetone.
Kết luận: Do diphenylamine tan kém ở nhiệt độ thấp và tan tốt ở nhiệt độ cao, nên khi làm nguội dung dịch bão hoà nóng, chất này sẽ kết tinh lại dễ dàng và hiệu quả.
→ Diphenylamine là chất có thể được kết tinh tốt bằng phương pháp kết tinh lại từ dung môi phù hợp.