Dạng 1. TRẮC NGHIỆM KHÁCH QUAN: mỗi câu hỏi chỉ có một đáp án đúng.
Câu 1 [1016549]: Trong nguồn điện hoá học (pin, acquy) có sự chuyển hoá chủ yếu từ
A, cơ năng thành điện năng.
B, nhiệt năng thành điện năng.
C, hoá năng thành điện năng.
D, quang năng thành điện năng.
Trong các nguồn điện hoá học như pin và ắc quy, năng lượng điện được sinh ra từ phản ứng oxi hóa - khử, trong đó có sự chuyển hóa năng lượng hoá học (hoá năng) thành điện năng.
Pin hoạt động dựa trên phản ứng giữa các chất có tính khử – oxi hoá khác nhau.
Ắc quy cũng hoạt động theo nguyên lý tương tự, nhưng có thể nạp lại bằng cách cung cấp điện năng để đảo ngược phản ứng hoá học.
⟹ Chọn đáp án C Đáp án: C
Pin hoạt động dựa trên phản ứng giữa các chất có tính khử – oxi hoá khác nhau.
Ắc quy cũng hoạt động theo nguyên lý tương tự, nhưng có thể nạp lại bằng cách cung cấp điện năng để đảo ngược phản ứng hoá học.
⟹ Chọn đáp án C Đáp án: C
Câu 2 [560490]: Ưu điểm của pin Li-ion (acquy Li-ion) là
A, Có thể nạp lại được nhiều lần.
B, Vòng đời pin ngắn.
C, Chi phí rẻ.
D, Nguồn năng lượng vô tận.
Pin Li-ion (acquy Li-ion) là một loại pin có thể tái sử dụng nhiều lần bằng cách sạc điện. Acquy thường được phân loại dựa theo bản chất vật liệu làm điện cực.
⟹ Chọn đáp án A Đáp án: A
⟹ Chọn đáp án A Đáp án: A
Câu 3 [560491]: Nhược điểm của acquy chì là
A, Chi phí cao do phải có bộ phận lưu trữ nhiên liệu đặc biệt là hydrogen.
B, Chỉ sinh ra dòng điện khi có ánh sáng mặt trời.
C, Không xử lí đúng cách sẽ gây hại môi trường.
D, Vòng đời pin ngắn.
* Ưu điểm:
Vòng đời sử dụng được kéo dài do có thể nạp lại để tái sử dụng mà không cần phải thay thế viên pin.
* Nhược điểm:
Chi phí sản xuất acquy thường lớn hơn so với pin thông thường; acquy cũ, hỏng không được thu gom và xử lí đúng cách sẽ gây ô nhiễm môi trường bởi các thành phần kim loại, hoá chất cũng như lớp vỏ của acquy (làm bằng nhựa khó phân huỷ).
⟹ Chọn đáp án C Đáp án: C
Vòng đời sử dụng được kéo dài do có thể nạp lại để tái sử dụng mà không cần phải thay thế viên pin.
* Nhược điểm:
Chi phí sản xuất acquy thường lớn hơn so với pin thông thường; acquy cũ, hỏng không được thu gom và xử lí đúng cách sẽ gây ô nhiễm môi trường bởi các thành phần kim loại, hoá chất cũng như lớp vỏ của acquy (làm bằng nhựa khó phân huỷ).
⟹ Chọn đáp án C Đáp án: C
Câu 4 [1016550]: Acquy chì là một loại acquy đơn giản, gồm bản cực dương bằng PbO2, bản cực âm bằng Pb, cả hai điện cực được đặt vào dung dịch H2SO4 loãng. Loại acquy này có thể sạc lại nhiều lần. Đây cũng là loại acquy được sử dụng phổ biến trên các dòng xe máy hiện nay với nhiều ưu điểm vượt trội. Acquy chì có các đặc điểm sau:
(1) dễ sản xuất, giá thành thấp;
(2) gây ô nhiễm môi trường;
(3) có khả năng trữ một lượng điện lớn trong bình ắc quy;
(4) hoạt động ổn định.
Những ưu điểm của acquy chì là
(1) dễ sản xuất, giá thành thấp;
(2) gây ô nhiễm môi trường;
(3) có khả năng trữ một lượng điện lớn trong bình ắc quy;
(4) hoạt động ổn định.
Những ưu điểm của acquy chì là
A, (1), (2), (3).
B, (1), (3), (4).
C, (1), (2), (4).
D, (2), (3), (4).
Acquy chì có các ưu điểm sau:
(1) dễ sản xuất, giá thành thấp;
3) có khả năng trữ một lượng điện lớn trong bình ắc quy;
(4) hoạt động ổn định.
Nhược điểm: (2) là nhược điểm của acquy chì. Acquy chì chứa chì (Pb), H2SO4 và những vỏ nhựa bền chắc là những rác thải khó xử lý, độc hại và gây ô nhiễm môi trường nếu không được xử lý đúng cách.
⟹ Chọn đáp án B Đáp án: B
(1) dễ sản xuất, giá thành thấp;
3) có khả năng trữ một lượng điện lớn trong bình ắc quy;
(4) hoạt động ổn định.
Nhược điểm: (2) là nhược điểm của acquy chì. Acquy chì chứa chì (Pb), H2SO4 và những vỏ nhựa bền chắc là những rác thải khó xử lý, độc hại và gây ô nhiễm môi trường nếu không được xử lý đúng cách.
⟹ Chọn đáp án B Đáp án: B
Câu 5 [560492]: Pin nhiên liệu là loại pin biến đổi trực tiếp năng lượng hoá học (hoá năng) thành điện năng nhờ quá trình oxi hoá gián tiếp các loại nhiên liệu như là
A, Hydrogen.
B, Than chì.
C, Oxygen.
D, Lipid.
Pin nhiên liệu là loại pin biến đổi trực tiếp năng lượng hoá học (hoá năng) thành điện năng nhờ quá trình oxi hoá gián tiếp nhiên liệu (hydrogen, alcohol,...) diễn ra trong pin. Chất oxi hoá thường dùng trong pin nhiên liệu là hydrogen.
⟹ Chọn đáp án A Đáp án: A
⟹ Chọn đáp án A Đáp án: A
Câu 6 [560493]: Ưu điểm nào sau đây không phải của pin nhiên liệu?
A, Hiệu suất chuyển hoá từ nhiên liệu sang điện năng cao.
B, Pin nhiên liệu hydrogen không tạo ra các sản phẩm gây ô nhiễm môi trường.
C, Giá thành pin nhiên liệu thấp.
D, Nguồn năng lượng vô tận.
* Ưu điểm của pin nhiên liệu:
- Tạo điện năng trực tiếp từ phản ứng hoá học nên có hiệu suất chuyển hoá từ nhiên liệu sang điện năng cao.
- Pin nhiên liệu hydrogen không tạo ra các sản phẩm gây ô nhiễm môi trường.
*Nhược điểm:
Giá thành pin nhiên liệu cao vì cấu tạo
phức tạp của pin (gồm các điện cực phủ xúc
tác, lớp màng đặc biệt giữa hai điện cực, dung
dịch trong pin,...) cũng như phải có bộ phận
lưu trữ nhiên liệu đặc biệt là hydrogen.
⟹ Chọn đáp án C Đáp án: C
- Tạo điện năng trực tiếp từ phản ứng hoá học nên có hiệu suất chuyển hoá từ nhiên liệu sang điện năng cao.
- Pin nhiên liệu hydrogen không tạo ra các sản phẩm gây ô nhiễm môi trường.
*Nhược điểm:
Giá thành pin nhiên liệu cao vì cấu tạo
phức tạp của pin (gồm các điện cực phủ xúc
tác, lớp màng đặc biệt giữa hai điện cực, dung
dịch trong pin,...) cũng như phải có bộ phận
lưu trữ nhiên liệu đặc biệt là hydrogen.
⟹ Chọn đáp án C Đáp án: C
Câu 7 [1016551]: Pin nhiên liệu được nghiên cứu rộng rãi nhằm thay thế nguồn nhiên liệu hóa thạch ngày càng cạn kiệt. Trong pin nhiên liệu, dòng điện được tạo ra do phản ứng oxi hóa nhiên liệu (hyđrogen, carbon monooxide, methanol, ethanol, propane,…) bằng oxi không khí. Pin nhiên liệu phổ biến hiện nay là pin hydrogen. Pin nhiên liệu có các ưu, nhược điểm sau:
(1) nhiên liệu được bổ sung liên tục.
(2) thời gian hoạt động của pin không bị hạn chế.
(3) không tạo ra các sản phẩm gây ô nhiễm môi trường.
(4) giá thành cao.
Những ưu điểm của pin nhiên liệu là
(1) nhiên liệu được bổ sung liên tục.
(2) thời gian hoạt động của pin không bị hạn chế.
(3) không tạo ra các sản phẩm gây ô nhiễm môi trường.
(4) giá thành cao.
Những ưu điểm của pin nhiên liệu là
A, (1), (2), (3).
B, (1), (3), (4).
C, (1), (2), (4).
D, (2), (3), (4).
Ưu điểm:
(1) Nhiên liệu được bổ sung liên tục:
→ Đúng. Khác với pin thông thường (có dung lượng giới hạn), pin nhiên liệu hoạt động liên tục khi được cung cấp nhiên liệu như hydro và oxi.
(2) Thời gian hoạt động của pin không bị hạn chế:
→ Đúng. Vì nhiên liệu được cung cấp liên tục, nên thời gian hoạt động chỉ phụ thuộc vào nguồn cung nhiên liệu, chứ không phụ thuộc vào dung lượng pin như ắc quy truyền thống.
(3) Không tạo ra các sản phẩm gây ô nhiễm môi trường:
→ Phần lớn đúng. Với pin nhiên liệu hydrogen, sản phẩm chính là nước (H2O), nên rất thân thiện với môi trường. Tuy nhiên, nếu sử dụng nhiên liệu khác như methanol hoặc propane, vẫn có thể phát sinh một số khí phụ như CO2, nhưng vẫn ít ô nhiễm hơn nhiều so với việc đốt cháy nhiên liệu hóa thạch.
Những ưu điểm của pin nhiên liệu là: (1), (2), (3).
Nhược điểm:
(4) Giá thành cao:
→ Đúng. Đây là nhược điểm lớn hiện nay của pin nhiên liệu do chi phí sản xuất cao, công nghệ còn phức tạp và sử dụng các kim loại quý như bạch kim làm xúc tác.
⟹ Chọn đáp án A Đáp án: A
(1) Nhiên liệu được bổ sung liên tục:
→ Đúng. Khác với pin thông thường (có dung lượng giới hạn), pin nhiên liệu hoạt động liên tục khi được cung cấp nhiên liệu như hydro và oxi.
(2) Thời gian hoạt động của pin không bị hạn chế:
→ Đúng. Vì nhiên liệu được cung cấp liên tục, nên thời gian hoạt động chỉ phụ thuộc vào nguồn cung nhiên liệu, chứ không phụ thuộc vào dung lượng pin như ắc quy truyền thống.
(3) Không tạo ra các sản phẩm gây ô nhiễm môi trường:
→ Phần lớn đúng. Với pin nhiên liệu hydrogen, sản phẩm chính là nước (H2O), nên rất thân thiện với môi trường. Tuy nhiên, nếu sử dụng nhiên liệu khác như methanol hoặc propane, vẫn có thể phát sinh một số khí phụ như CO2, nhưng vẫn ít ô nhiễm hơn nhiều so với việc đốt cháy nhiên liệu hóa thạch.
Những ưu điểm của pin nhiên liệu là: (1), (2), (3).
Nhược điểm:
(4) Giá thành cao:
→ Đúng. Đây là nhược điểm lớn hiện nay của pin nhiên liệu do chi phí sản xuất cao, công nghệ còn phức tạp và sử dụng các kim loại quý như bạch kim làm xúc tác.
⟹ Chọn đáp án A Đáp án: A
Câu 8 [1016552]: Pin mặt trời là loại pin biến đổi trực tiếp
A, cơ năng thành điện năng.
B, nội năng thành điện năng.
C, hoá năng thành điện năng.
D, quang năng thành điện năng.
Pin mặt trời (hay còn gọi là pin quang điện, solar cell) hoạt động dựa trên hiện tượng quang điện. Khi ánh sáng mặt trời (chứa quang năng) chiếu vào chất bán dẫn (thường là silicon), sẽ giải phóng các electron và tạo ra dòng điện. Vì vậy, pin mặt trời chuyển đổi trực tiếp quang năng thành điện năng.
⟹ Chọn đáp án D
Các phát biểu khác:
A. Cơ năng thành điện năng. Các thiết bị như máy phát điện mới biến đổi chứ không phải pin mặt trời.
B. Nội năng thành điện năng. Các thiết bị như pin nhiệt điện biến đổi chứ không phải pin mặt trời.
C. Hoá năng thành điện năng. Đây là dạng chuyển đổi trong pin hoá học như pin điện hoá phản ứng xảy ra tạo ra dòng điện. Đáp án: D
⟹ Chọn đáp án D
Các phát biểu khác:
A. Cơ năng thành điện năng. Các thiết bị như máy phát điện mới biến đổi chứ không phải pin mặt trời.
B. Nội năng thành điện năng. Các thiết bị như pin nhiệt điện biến đổi chứ không phải pin mặt trời.
C. Hoá năng thành điện năng. Đây là dạng chuyển đổi trong pin hoá học như pin điện hoá phản ứng xảy ra tạo ra dòng điện. Đáp án: D
Câu 9 [560494]: Nhược điểm nào sau đây không phải của pin mặt trời?
A, Chỉ sinh ra dòng điện khi có ánh sáng mặt trời.
B, Chi phí sản xuất cần nguồn nguyên liệu giá thành đắt.
C, Không tạo ra bất cứ sản phẩm hoá học nào nên không thân thiện với môi trường.
D, Khi pin hết hạn sử dụng, việc xử lí không đúng cách sẽ gây ô nhiễm môi trường đất.
* Ưu điểm của pin mặt trời:
Sử dụng nguồn năng lượng vô tận là
ánh sáng mặt trời, không tạo ra bất cứ sản
phẩm hoá học nào trong quá trình hoạt
động nên thân thiện với môi trường.
*Nhược điểm:
Chỉ sinh ra dòng điện khi có ánh sáng mặt trời,
công suất dòng điện tỉ lệ với cường độ ánh sáng.
Khi pin hết hạn sử dụng, việc xử lí không đúng
cách sẽ gây ô nhiễm môi trường đất.
⟹ Chọn đáp án C Đáp án: C
Sử dụng nguồn năng lượng vô tận là
ánh sáng mặt trời, không tạo ra bất cứ sản
phẩm hoá học nào trong quá trình hoạt
động nên thân thiện với môi trường.
*Nhược điểm:
Chỉ sinh ra dòng điện khi có ánh sáng mặt trời,
công suất dòng điện tỉ lệ với cường độ ánh sáng.
Khi pin hết hạn sử dụng, việc xử lí không đúng
cách sẽ gây ô nhiễm môi trường đất.
⟹ Chọn đáp án C Đáp án: C
Câu 10 [1016553]: Pin mặt trời (pin quang điện) bao gồm nhiều tế bào quang điện làm biến đổi năng lượng ánh sáng thành năng lượng điện. Pin mặt trời mang đến rất nhiều lợi ích, nó được ứng dụng khá rộng rãi trong đời sống hiện nay.
Có các phát biểu sau về lợi ích của việc sử dụng pin mặt trời.
(a) Tạo ra được nguồn năng lượng xanh.
(b) Thân thiện với môi trường.
(c) Chi phí trang bị không quá cao.
(d) Thời gian sử dụng ngắn.
Số phát biểu đúng là
Có các phát biểu sau về lợi ích của việc sử dụng pin mặt trời.
(a) Tạo ra được nguồn năng lượng xanh.
(b) Thân thiện với môi trường.
(c) Chi phí trang bị không quá cao.
(d) Thời gian sử dụng ngắn.
Số phát biểu đúng là
A, 1.
B, 3.
C, 2.
D, 4.
Phân tích các phát biểu:
✔️(a) – Đúng. Tạo ra được nguồn năng lượng xanh Pin mặt trời sử dụng ánh sáng mặt trời – nguồn năng lượng tái tạo và không gây ô nhiễm, nên được coi là năng lượng xanh.
✔️b) – Đúng. Thân thiện với môi trường Trong quá trình hoạt động, pin mặt trời không thải ra khí CO₂ hay chất độc hại, nên rất thân thiện với môi trường.
❌(c) – Sai. Chi phí trang bị không quá cao → Sai. Chi phí lắp đặt ban đầu của hệ thống pin mặt trời vẫn còn khá cao, dù về lâu dài có thể tiết kiệm chi phí sử dụng điện.
❌(d) – Sai. Thời gian sử dụng ngắn Pin mặt trời có tuổi thọ dài, thường trên 20 năm, nên không thể xem là “thời gian sử dụng ngắn”.
Số phát biểu đúng là: 2
⟹ Chọn đáp án C Đáp án: C
✔️(a) – Đúng. Tạo ra được nguồn năng lượng xanh Pin mặt trời sử dụng ánh sáng mặt trời – nguồn năng lượng tái tạo và không gây ô nhiễm, nên được coi là năng lượng xanh.
✔️b) – Đúng. Thân thiện với môi trường Trong quá trình hoạt động, pin mặt trời không thải ra khí CO₂ hay chất độc hại, nên rất thân thiện với môi trường.
❌(c) – Sai. Chi phí trang bị không quá cao → Sai. Chi phí lắp đặt ban đầu của hệ thống pin mặt trời vẫn còn khá cao, dù về lâu dài có thể tiết kiệm chi phí sử dụng điện.
❌(d) – Sai. Thời gian sử dụng ngắn Pin mặt trời có tuổi thọ dài, thường trên 20 năm, nên không thể xem là “thời gian sử dụng ngắn”.
Số phát biểu đúng là: 2
⟹ Chọn đáp án C Đáp án: C
Câu 11 [1016554]: Một học sinh thiết lập một pin điện hóa gồm hai mảnh kẽm (Zn) và đồng (Cu) cắm vào một quả chanh và sau đó nối với đầu bên ngoài một ampe kế, thấy kim chỉ thị lệch khỏi vạch 0 (hình vẽ). Quá trình nào có thể xảy ra tại điện cực đồng?
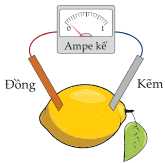

A, Khử H+ thành khí H2.
B, Khử Cu2+ thành Cu.
C, Khử Zn2+ thành Zn.
D, Oxi hóa H2O thành O2.
Zn có tính khử mạnh hơn Cu nên Zn là anode, Cu là cathode.
Trong quả chanh có acid
Tại điện cực Cu xảy ra quá trình khử H+ thành khí H2 (H+ do acid hữu cơ có trong chanh phân ly ra).
Quá trình xảy ra trong pin
Anode (-) Zn → Zn2+ + 2e
Cathdoe (+) 2H+ + 2e → H2
⟹ Chọn đáp án A Đáp án: A
Trong quả chanh có acid
Tại điện cực Cu xảy ra quá trình khử H+ thành khí H2 (H+ do acid hữu cơ có trong chanh phân ly ra).
Quá trình xảy ra trong pin
Anode (-) Zn → Zn2+ + 2e
Cathdoe (+) 2H+ + 2e → H2
⟹ Chọn đáp án A Đáp án: A
Sử dụng đoạn thông tin dưới đây để trả lời câu 17 và câu 18:
Lưu huỳnh (sulfur) là phi kim đa hóa trị phổ biến, hiện diện trong một số amino acid và là tiền chất của nhiều hóa chất công nghiệp quan trọng, bao gồm H2SO4. H2SO4 là acid khoáng phổ biến với nhiều ứng dụng, một trong số đó là làm chất điện li trong pin.
Trong pin chì-acid của xe hơi, các phản ứng sau xảy ra:
∎ Anode: Pb(s) → Pb2+(aq) + 2e;
∎ Cathode: PbO2(s) + 4H+(aq) + 2e → Pb2+(aq) + 2H2O(l).
Trong pin chì-acid của xe hơi, các phản ứng sau xảy ra:
∎ Anode: Pb(s) → Pb2+(aq) + 2e;
∎ Cathode: PbO2(s) + 4H+(aq) + 2e → Pb2+(aq) + 2H2O(l).
Câu 12 [705787]: Khi pin hoạt động giải phóng năng lượng,
A, nồng độ H+ giảm dần.
B, nồng độ Pb2+ giảm dần.
C, khối lượng Pb rắn giảm.
D, khối lượng PbO2 rắn giảm.
Phản ứng tại mỗi điện cực:
Anode (cực âm - nơi oxi hóa xảy ra): Pb(s) ⟶ Pb2+(aq) + 2e
→ Chì kim loại bị oxi hóa thành ion Pb2+, làm nồng độ Pb²⁺ tăng.
Cathode (cực dương - nơi khử xảy ra): PbO2(s) + 4H+(aq) + 2e ⟶ Pb2+(aq) + 2H2O(l)
→ PbO2 rắn bị tiêu hao để tạo ra Pb2+.
→ H+ bị tiêu hao, làm nồng độ H+ giảm.
Phân tích các đáp án:
❌ A. Sai. Ở cathode, ion H+ bị tiêu hao trong phản ứng với PbO2 nên nồng độ H+ giảm chứ không tăng.
✔️ B. Đúng. Cả hai điện cực đều tạo ra Pb2+ trong dung dịch, làm nồng độ Pb2+ tăng.
❌ C. Đúng. Pb ở anode bị oxi hóa thành Pb2+, tức là Pb bị ăn mòn, khối lượng giảm chứ không tăng.
❌ D. Sai. PbO2 rắn ở cathode bị tiêu hao để tạo Pb2+, nên khối lượng giảm.
⇒ Chọn đáp án B Đáp án: B
Anode (cực âm - nơi oxi hóa xảy ra): Pb(s) ⟶ Pb2+(aq) + 2e
→ Chì kim loại bị oxi hóa thành ion Pb2+, làm nồng độ Pb²⁺ tăng.
Cathode (cực dương - nơi khử xảy ra): PbO2(s) + 4H+(aq) + 2e ⟶ Pb2+(aq) + 2H2O(l)
→ PbO2 rắn bị tiêu hao để tạo ra Pb2+.
→ H+ bị tiêu hao, làm nồng độ H+ giảm.
Phân tích các đáp án:
❌ A. Sai. Ở cathode, ion H+ bị tiêu hao trong phản ứng với PbO2 nên nồng độ H+ giảm chứ không tăng.
✔️ B. Đúng. Cả hai điện cực đều tạo ra Pb2+ trong dung dịch, làm nồng độ Pb2+ tăng.
❌ C. Đúng. Pb ở anode bị oxi hóa thành Pb2+, tức là Pb bị ăn mòn, khối lượng giảm chứ không tăng.
❌ D. Sai. PbO2 rắn ở cathode bị tiêu hao để tạo Pb2+, nên khối lượng giảm.
⇒ Chọn đáp án B Đáp án: B
Câu 13 [705788]: Cho 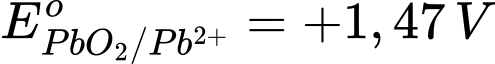 và
và 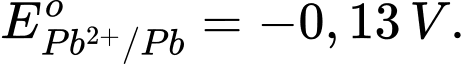 Tính giá trị Eo của pin.
Tính giá trị Eo của pin.
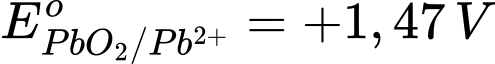 và
và 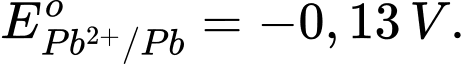 Tính giá trị Eo của pin.
Tính giá trị Eo của pin. A, 0,48 V.
B, 0,85 V.
C, 1,34 V.
D, 1,60 V.
Eopin = Eocathode – Eoanode = 1,47 – (–0,13) = 1,60 V
⇒ Chọn đáp án D Đáp án: D
⇒ Chọn đáp án D Đáp án: D
Dạng 2: TRẮC NGHIỆM ĐÚNG SAI – mỗi ý a), b), c), d) chọn đúng hoặc sai.
Câu 14 [1016555]: Pin AA là loại pin phổ biến nhờ kích thước tiêu chuẩn, dễ thay thế, tương thích với nhiều thiết bị điện tử và có nhiều loại như pin kiềm, pin sạc, pin lithium. Với giá thành hợp lý và dễ tiếp cận, pin AA là giải pháp năng lượng tiện lợi và hiệu quả cho cả nhu cầu cá nhân lẫn chuyên dụng.
Phân tích các phát biểu:
✔️(a) – Đúng. Pin AA (đặc biệt là loại pin kiềm hoặc pin lithium) có độ ổn định cao, ít rò rỉ, ít cháy nổ nếu sử dụng đúng cách. Chúng được thiết kế an toàn cho người sử dụng và có tuổi thọ khá tốt (tùy loại pin).
✔️(b) – Đúng. Pin AA cung cấp điện áp 1,5V (đối với pin không sạc) – đây là mức điện áp thấp, không gây nguy hiểm cho người bình thường khi sử dụng.
❌(c) – Sai. Chỉ đúng với pin dùng 1 lần (như pin kiềm, pin than kẽm), còn pin sạc AA (như pin NiMH, pin lithium AA) có thể sạc lại và tái sử dụng nhiều lần.
❌(d) – Sai. Nếu không được thu gom và xử lý đúng cách, pin AA có thể gây ô nhiễm môi trường vì chứa kim loại nặng (như kẽm, mangan, lithium...). Do đó, cần phân loại và tái chế đúng quy định.
✔️(a) – Đúng. Pin AA (đặc biệt là loại pin kiềm hoặc pin lithium) có độ ổn định cao, ít rò rỉ, ít cháy nổ nếu sử dụng đúng cách. Chúng được thiết kế an toàn cho người sử dụng và có tuổi thọ khá tốt (tùy loại pin).
✔️(b) – Đúng. Pin AA cung cấp điện áp 1,5V (đối với pin không sạc) – đây là mức điện áp thấp, không gây nguy hiểm cho người bình thường khi sử dụng.
❌(c) – Sai. Chỉ đúng với pin dùng 1 lần (như pin kiềm, pin than kẽm), còn pin sạc AA (như pin NiMH, pin lithium AA) có thể sạc lại và tái sử dụng nhiều lần.
❌(d) – Sai. Nếu không được thu gom và xử lý đúng cách, pin AA có thể gây ô nhiễm môi trường vì chứa kim loại nặng (như kẽm, mangan, lithium...). Do đó, cần phân loại và tái chế đúng quy định.
Câu 15 [829921]: Acquy chì có cấu tạo như hình vẽ dưới đây:
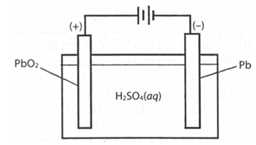
Cực dương là thanh than chì (C) được phủ PbO2 và cực âm là tấm chì (Pb), cùng nhúng vào dung dịch H2SO4 nồng độ 28%. Phản ứng xảy ra khi acquy xả điện là:
Pb(s) + PbO2(s) + 2H2SO4(aq)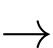 2PbSO4(s) + 2H2O(l)
2PbSO4(s) + 2H2O(l)
Biết rằng PbSO4 sinh ra từ điện cực nào đều bám hết vào điện cực đó.

Cực dương là thanh than chì (C) được phủ PbO2 và cực âm là tấm chì (Pb), cùng nhúng vào dung dịch H2SO4 nồng độ 28%. Phản ứng xảy ra khi acquy xả điện là:
Pb(s) + PbO2(s) + 2H2SO4(aq)
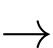 2PbSO4(s) + 2H2O(l)
2PbSO4(s) + 2H2O(l)Biết rằng PbSO4 sinh ra từ điện cực nào đều bám hết vào điện cực đó.
Pb(s) + PbO2(s) + 2H2SO4(aq) → 2PbSO4(s) + 2H2O(l)
Quá trình trong pin điện hóa
Anode (-): Pb → Pb2+ + 2e
Cathode (+): PbO2 + 4H+ + 4e → Pb2+ + 2H2O
Phân tích các đáp án
❌(a) – Sai. Tại anode, Pb bị oxi hoá và tạo thành PbSO4.
❌(b) – Sai. Tại cathode, PbO2 bị khử và tạo thành PbSO4.
❌(c) – Sai. Khi ắc quy xả điện, các điện cực bị biến đổi hóa học thành PbSO4.
Khối lượng vật liệu hoạt động giảm, nhưng tổng khối lượng có thể không thay đổi đáng kể do PbSO4 vẫn bám trên bản cực.
✔️(d) – Đúng. Ắc quy chì có dung dịch điện ly là sulfuric acid loãng (H2SO4).Khi xả điện: Cả hai điện cực (Pb và PbO2) phản ứng với ion SO42- từ H2SO4 để tạo thành PbSO4: Do đó, ion SO42- trong dung dịch bị tiêu hao → nồng độ H2SO4 giảm.
Quá trình trong pin điện hóa
Anode (-): Pb → Pb2+ + 2e
Cathode (+): PbO2 + 4H+ + 4e → Pb2+ + 2H2O
Phân tích các đáp án
❌(a) – Sai. Tại anode, Pb bị oxi hoá và tạo thành PbSO4.
❌(b) – Sai. Tại cathode, PbO2 bị khử và tạo thành PbSO4.
❌(c) – Sai. Khi ắc quy xả điện, các điện cực bị biến đổi hóa học thành PbSO4.
Khối lượng vật liệu hoạt động giảm, nhưng tổng khối lượng có thể không thay đổi đáng kể do PbSO4 vẫn bám trên bản cực.
✔️(d) – Đúng. Ắc quy chì có dung dịch điện ly là sulfuric acid loãng (H2SO4).Khi xả điện: Cả hai điện cực (Pb và PbO2) phản ứng với ion SO42- từ H2SO4 để tạo thành PbSO4: Do đó, ion SO42- trong dung dịch bị tiêu hao → nồng độ H2SO4 giảm.
Câu 16 [1016556]: Pin kẽm-mangan (Zn-MnO2) là loại pin phổ biến trong các thiết bị điện tử do giá thành thấp và an toàn. Tuy nhiên, loại pin này thường có tuổi thọ ngắn do phản ứng phụ làm giảm hiệu suất hoạt động. Một nhóm học sinh nghiên cứu ảnh hưởng của nồng độ KOH đến hiệu suất và tuổi thọ của pin Zn-MnO2. Thí nghiệm được tiến hành như sau:
∎ Bước 1: Pha các dung dịch KOH với nồng độ 2 M, 6 M, 10 M.
∎ Bước 2: Lắp ráp pin Zn-MnO2.
- Điện cực cực âm (anode): Dùng tấm kẽm (Zn).
- Điện cực cực dương (cathode): Dùng MnO2 trộn với than hoạt tính và chất kết dính để tạo thành điện cực.
- Nhúng điện cực vào dung dịch KOH tương ứng.
∎ Bước 3:
- Đo hiệu suất ban đầu, ghi nhận các giá trị vào bảng số liệu.
- Sử dụng máy đo dung lượng pin để tiến hành sạc-xả 50 chu kỳ.Ghi lại dung lượng sau mỗi 10 chu kỳ.
- So sánh dung lượng ban đầu và dung lượng sau 50 chu kỳ.
- Xác định hiệu suất Coulombic (%) của từng mẫu.
- Kiểm tra sự suy giảm hiệu suất do ăn mòn kẽm hoặc hòa tan MnO2.
∎ Bước 1: Pha các dung dịch KOH với nồng độ 2 M, 6 M, 10 M.
∎ Bước 2: Lắp ráp pin Zn-MnO2.
- Điện cực cực âm (anode): Dùng tấm kẽm (Zn).
- Điện cực cực dương (cathode): Dùng MnO2 trộn với than hoạt tính và chất kết dính để tạo thành điện cực.
- Nhúng điện cực vào dung dịch KOH tương ứng.
∎ Bước 3:
- Đo hiệu suất ban đầu, ghi nhận các giá trị vào bảng số liệu.
- Sử dụng máy đo dung lượng pin để tiến hành sạc-xả 50 chu kỳ.Ghi lại dung lượng sau mỗi 10 chu kỳ.
- So sánh dung lượng ban đầu và dung lượng sau 50 chu kỳ.
- Xác định hiệu suất Coulombic (%) của từng mẫu.
- Kiểm tra sự suy giảm hiệu suất do ăn mòn kẽm hoặc hòa tan MnO2.

Phân tích các phát biểu:
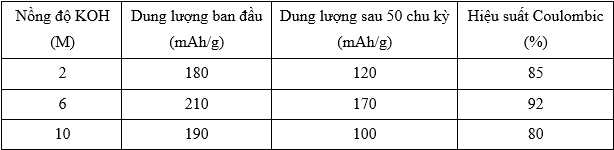
✔️(a) – Đúng. Pin với KOH 6M có hiệu suất cao nhất (92%), dung lượng duy trì tốt sau 50 chu kỳ (giảm 40 mAh, so với mức giảm 60 và 90 mAh ở nồng độ 2M và 10M).
❌(b) – Sai. Cực âm xảy ra quá trình oxi hóa Zn và cực dương xảy ra quá trình khử Mn2+.
Anode (-) Zn + 2OH → Zn(OH)2 + 2e
Cathode (+) MnO2 + H2O + e → MnO(OH) + OH-
✔️(c) – Đúng. Phản ứng phụ (ăn mòn kẽm khi nồng độ KOH quá cao):
Zn + 2H2O + 2OH- → [Zn(OH)4]2- + H2
✔️(d) – Đúng. Trong 3 nồng độ KOH ở trên thì nồng độ 6M là tối ưu nhất, thể hiện qua 2 thông số là dung lượng ban đầu lớn và dung lượng bị hao hụt sau 50 lần sạc – xả nhỏ, hiệu suất Coulombic cao.
Hiệu suất Coulombic = Tổng lượng điện tích do pin sản sinh khi xả / Tổng lượng điện tích đưa vào pin khi sạc (trong cùng 1 chu kỳ sạc – xả).
✔️(a) – Đúng. Pin với KOH 6M có hiệu suất cao nhất (92%), dung lượng duy trì tốt sau 50 chu kỳ (giảm 40 mAh, so với mức giảm 60 và 90 mAh ở nồng độ 2M và 10M).
❌(b) – Sai. Cực âm xảy ra quá trình oxi hóa Zn và cực dương xảy ra quá trình khử Mn2+.
Anode (-) Zn + 2OH → Zn(OH)2 + 2e
Cathode (+) MnO2 + H2O + e → MnO(OH) + OH-
✔️(c) – Đúng. Phản ứng phụ (ăn mòn kẽm khi nồng độ KOH quá cao):
Zn + 2H2O + 2OH- → [Zn(OH)4]2- + H2
✔️(d) – Đúng. Trong 3 nồng độ KOH ở trên thì nồng độ 6M là tối ưu nhất, thể hiện qua 2 thông số là dung lượng ban đầu lớn và dung lượng bị hao hụt sau 50 lần sạc – xả nhỏ, hiệu suất Coulombic cao.
Hiệu suất Coulombic = Tổng lượng điện tích do pin sản sinh khi xả / Tổng lượng điện tích đưa vào pin khi sạc (trong cùng 1 chu kỳ sạc – xả).
Dạng 3: TRẮC NGHIỆM YÊU CẦU TRẢ LỜI NGẮN
Câu 17 [704017]: Acquy chứa chì thường được sử dụng trong ô tô. Để giảm lượng chì và các hợp chất nguy hiểm thải ra bãi chôn lấp khi những bình acquy này bị vứt bỏ, người ta đã đề xuất thay thế chì bằng carbon monoxide. Phản ứng xảy ra trong pin khi hoạt động như sau:
PbO2(s) + CO(g) + H2SO4(aq) → PbSO4(s) + CO2(g) + H2O.
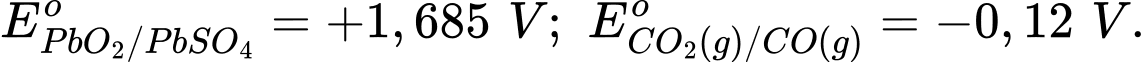
Nếu khối lượng riêng của dung dịch sulfuric acid trong acquy giảm từ 1,3 g/mL (40% H2SO4 theo khối lượng) xuống 1,2 g/mL (20% H2SO4 theo khối lượng) trong quá trình sử dụng, hãy xác định điện lượng của acquy đã tạo ra theo đơn vị ampere.giờ. Biết thể tích của acquy là 3,0 lít và thể tích thay đổi không đáng kể. (Làm tròn kết quả đến phần nguyên)
PbO2(s) + CO(g) + H2SO4(aq) → PbSO4(s) + CO2(g) + H2O.
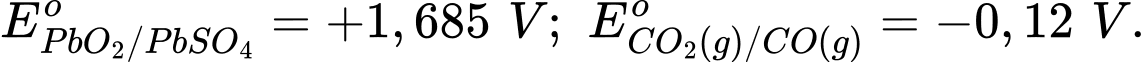
Nếu khối lượng riêng của dung dịch sulfuric acid trong acquy giảm từ 1,3 g/mL (40% H2SO4 theo khối lượng) xuống 1,2 g/mL (20% H2SO4 theo khối lượng) trong quá trình sử dụng, hãy xác định điện lượng của acquy đã tạo ra theo đơn vị ampere.giờ. Biết thể tích của acquy là 3,0 lít và thể tích thay đổi không đáng kể. (Làm tròn kết quả đến phần nguyên)
mH2SO4 ban đầu = V.D.C%= 3000. 1,3.40% = 1560
mH2SO4 sau phản ứng=V.D.C%=3000. 1,2. 20%= 720
⇒ ∆m = 1560 - 720= 840 g
⇒ nH2SO4= 8,57
⇒ ne trao đổi= 2.nH2SO4= 17,14 mol
mH2SO4 sau phản ứng=V.D.C%=3000. 1,2. 20%= 720
⇒ ∆m = 1560 - 720= 840 g
⇒ nH2SO4= 8,57
⇒ ne trao đổi= 2.nH2SO4= 17,14 mol
Q = ne . F = 17,14 . 96500 = 1654810 A.s
⇒ Đổi: 1654810/3600 = 460 A.h
⇒ Điền đáp án: 460
⇒ Điền đáp án: 460
Câu 18 [705509]: Pin nhiên liệu được nghiên cứu rộng rãi nhằm thay thế nguồn nhiên liệu hóa thạch ngày càng cạn kiệt. Trong pin nhiên liệu, dòng điện được tạo ra do phản ứng oxi hóa nhiên liệu (hydrogen, carbon monoxide, methanol, ethanol, propane, ...) bằng oxygen không khí. Pin nhiên liệu sử dụng tế bào nhiên liệu với nguyên liệu là khí hydrogen để chuyển hoá năng lượng thành điện năng:
Anode (+): 2H2 + 4OH– 4H2O + 4e
4H2O + 4e
Cathode (–): O2 + 4e + 2H2O 4OH–
4OH–
Một máy điện sử dụng các pin nhiên liệu để phát điện với nguyên liệu là khí hydrogen và có hiệu suất là 60% (nghĩa là có 60% năng lượng của phản ứng chuyển hoá thành điện năng). Mỗi ngày nhà máy sản xuất được 480 kWh. Tính khối lượng (theo kg) khí hydrogen tiêu thụ trong một ngày (Làm tròn đến hàng phần mười)? Cho biết: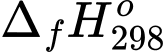 (H2O(l)) = –285,84 kJ/mol, 1 kWh = 3,6.106 J.
(H2O(l)) = –285,84 kJ/mol, 1 kWh = 3,6.106 J.
Anode (+): 2H2 + 4OH–
 4H2O + 4e
4H2O + 4eCathode (–): O2 + 4e + 2H2O
 4OH–
4OH–Một máy điện sử dụng các pin nhiên liệu để phát điện với nguyên liệu là khí hydrogen và có hiệu suất là 60% (nghĩa là có 60% năng lượng của phản ứng chuyển hoá thành điện năng). Mỗi ngày nhà máy sản xuất được 480 kWh. Tính khối lượng (theo kg) khí hydrogen tiêu thụ trong một ngày (Làm tròn đến hàng phần mười)? Cho biết:
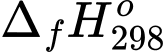 (H2O(l)) = –285,84 kJ/mol, 1 kWh = 3,6.106 J.
(H2O(l)) = –285,84 kJ/mol, 1 kWh = 3,6.106 J. 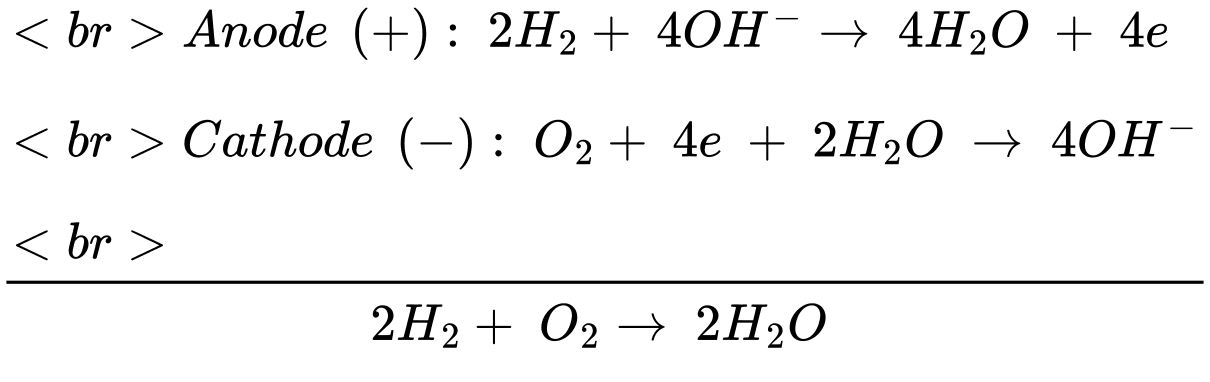
Biến thiên enthalpy của phản ứng là:
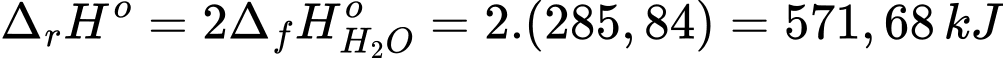
Hiệu suất chuyển hóa điện năng là 60%
2 mol H2 sẽ tạo ra năng lượng thực tế là 571,68 × 60% = 343,008 kJ
4 gam H2 sẽ tạo ra năng lượng thực tế là 343,008 kJ
x gam H2 sẽ tạo ra năng lượng thực tế là 480 × 3,6 × 103 kJ
→
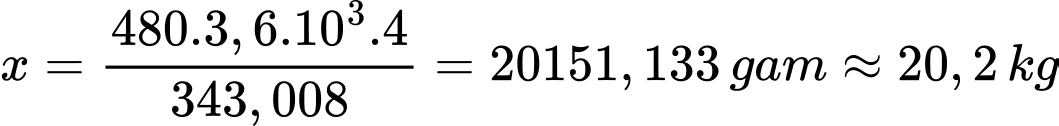
⇒ Điền đáp án: 20,2
Câu 19 [705724]: Pin nhiên liệu được nghiên cứu rộng rãi nhằm thay thế nguồn nhiên liệu hóa thạch ngày càng cạn kiệt. Trong pin nhiên liệu, dòng điện được tạo ra do phản ứng oxi hóa nhiên liệu (hydrogen, carbon monoxide, methanol, ethanol, propane, ...) bằng oxygen không khí. Pin nhiên liệu sử dụng tế bào nhiên liệu với nguyên liệu là khí hydrogen để chuyển hoá năng lượng thành điện năng:
Anode (-): O2 + 4e + 2H2O → 4OH–
Cathode (+): 2H2 + 4OH– → 4H2O + 4e
Một máy điện sử dụng các pin nhiên liệu để phát điện với nguyên liệu là khí hydrogen và có hiệu suất là 60% (nghĩa là có 60% năng lượng của phản ứng chuyển hoá thành điện năng).
Lượng khí hydrogen được điều chế từ khí thiên nhiên theo các quy trình sau: CH4 + H2O → CO + 3H2
CO + H2O → CO2 + H2
Mỗi ngày nhà máy sản xuất được 500 kWh. Tính khối lượng (theo kg) khí thiên nhiên tiêu thụ mỗi ngày? Cho biết: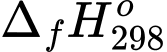 H2O(l) = –285,84 kJ/mol, 1kWh = 3,6.106 J. Khí thiên nhiên đã sử dụng chứa 100% CH4 và hiệu suất điều chế hydrogen là 90%.
H2O(l) = –285,84 kJ/mol, 1kWh = 3,6.106 J. Khí thiên nhiên đã sử dụng chứa 100% CH4 và hiệu suất điều chế hydrogen là 90%.
Anode (-): O2 + 4e + 2H2O → 4OH–
Cathode (+): 2H2 + 4OH– → 4H2O + 4e
Một máy điện sử dụng các pin nhiên liệu để phát điện với nguyên liệu là khí hydrogen và có hiệu suất là 60% (nghĩa là có 60% năng lượng của phản ứng chuyển hoá thành điện năng).
Lượng khí hydrogen được điều chế từ khí thiên nhiên theo các quy trình sau: CH4 + H2O → CO + 3H2
CO + H2O → CO2 + H2
Mỗi ngày nhà máy sản xuất được 500 kWh. Tính khối lượng (theo kg) khí thiên nhiên tiêu thụ mỗi ngày? Cho biết:
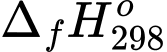 H2O(l) = –285,84 kJ/mol, 1kWh = 3,6.106 J. Khí thiên nhiên đã sử dụng chứa 100% CH4 và hiệu suất điều chế hydrogen là 90%.
H2O(l) = –285,84 kJ/mol, 1kWh = 3,6.106 J. Khí thiên nhiên đã sử dụng chứa 100% CH4 và hiệu suất điều chế hydrogen là 90%.
Nhà máy sản xuất 500 kWh điện mỗi ngày:
1 kWh = 3,6 × 106 J nên tổng năng lượng cần thiết là: 500 × 3,6 × 106 = 1,8 × 109 J
Vì hiệu suất chuyển hóa là 60%, năng lượng do phản ứng cung cấp thực tế là: (1,8 × 109) ÷ 0,6 = 3,0 × 109 J
Phương trình phản ứng ở pin nhiên liệu:
2H2 + 4OH− → 4H2O + 4e
O2 + 4e + 2H2O → 4OH−
Tổng phản ứng: H2 + 1/2O2 → H2O
Mỗi mol H2 sinh ra năng lượng: ∆H = −285,84 kJ/mol H2 = −285,84 × 103 J/mol H2
Số mol H2 cần thiết là: (3,0 × 109) ÷ (285,84 × 103) ≈ 10495,6 mol
Quá trình điều chế H2 từ CH4:
CH4 + H2O → CO + 3H2
CO + H2O → CO2 + H2
1 mol CH4 tạo ra 4 mol H2 nên số mol CH4 lý thuyết cần thiết để tạo 10495,6 mol H2 là: [10495,6 × 4a × 90% × 60% × 1000 ] : 3,6×106 = 500
→ a = 2915,4 mol
→ Khối lượng CH4 tiêu thụ mỗi ngày là: 2915,4 × 16 = 46646,4 g = 46,6 kg.
⇒ Điền đáp án: 46,6
1 kWh = 3,6 × 106 J nên tổng năng lượng cần thiết là: 500 × 3,6 × 106 = 1,8 × 109 J
Vì hiệu suất chuyển hóa là 60%, năng lượng do phản ứng cung cấp thực tế là: (1,8 × 109) ÷ 0,6 = 3,0 × 109 J
Phương trình phản ứng ở pin nhiên liệu:
2H2 + 4OH− → 4H2O + 4e
O2 + 4e + 2H2O → 4OH−
Tổng phản ứng: H2 + 1/2O2 → H2O
Mỗi mol H2 sinh ra năng lượng: ∆H = −285,84 kJ/mol H2 = −285,84 × 103 J/mol H2
Số mol H2 cần thiết là: (3,0 × 109) ÷ (285,84 × 103) ≈ 10495,6 mol
Quá trình điều chế H2 từ CH4:
CH4 + H2O → CO + 3H2
CO + H2O → CO2 + H2
1 mol CH4 tạo ra 4 mol H2 nên số mol CH4 lý thuyết cần thiết để tạo 10495,6 mol H2 là: [10495,6 × 4a × 90% × 60% × 1000 ] : 3,6×106 = 500
→ a = 2915,4 mol
→ Khối lượng CH4 tiêu thụ mỗi ngày là: 2915,4 × 16 = 46646,4 g = 46,6 kg.
⇒ Điền đáp án: 46,6