Dạng 1. TRẮC NGHIỆM KHÁCH QUAN: mỗi câu hỏi chỉ có một đáp án đúng.
Câu 1 [703920]: “Điện phân là quá trình ...(1)... xảy ra trên bề mặt các điện cực khi có dòng điện ...(2)... đi qua chất điện li nóng chảy hoặc dung dịch chất điện li”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, khử, một chiều.
B, oxi hoá, một chiều.
C, oxi hoá – khử, xoay chiều.
D, oxi hoá – khử, một chiều.
- Điện phân là một quá trình hóa học trong đó xảy ra sự oxi hóa (mất electron) tại anode (cực dương) và khử (nhận electron) tại cathode (cực âm).
- Để xảy ra điện phân, cần có dòng điện một chiều làm cho các ion dương (cation) di chuyển về cathode và các ion âm (anion) di chuyển về anode.
⇒ Điện phân là quá trình oxi hoá – khử xảy ra trên bề mặt các điện cực khi có dòng điện một chiều đi qua chất điện li nóng chảy hoặc dung dịch chất điện li.
⇒ Chọn đáp án D Đáp án: D
- Để xảy ra điện phân, cần có dòng điện một chiều làm cho các ion dương (cation) di chuyển về cathode và các ion âm (anion) di chuyển về anode.
⇒ Điện phân là quá trình oxi hoá – khử xảy ra trên bề mặt các điện cực khi có dòng điện một chiều đi qua chất điện li nóng chảy hoặc dung dịch chất điện li.
⇒ Chọn đáp án D Đáp án: D
Câu 2 [560525]: Trong bình điện phân, sự oxi hoá
A, chỉ xảy ra ở cực dương (anode).
B, chỉ xảy ra ở cực âm (cathode).
C, xảy ra ở cực dương (anode) và cực âm (cathode).
D, không xảy ra ở cực dương (anode) và cực âm (cathode).
Anode là nơi xảy ra sự oxi hóa. Cathode là nơi xảy ra sự khử. Đáp án: A
Câu 3 [560526]: Cho một bình điện phân chứa dung dịch FeCl2. Tiến hành điện phân thì ở anode xảy ra quá trình
A, Fe(s)  Fe2+(aq) +2e.
Fe2+(aq) +2e.
 Fe2+(aq) +2e.
Fe2+(aq) +2e.B, Fe2+(aq) + 2e  Fe(s).
Fe(s).
 Fe(s).
Fe(s).C, 2Cl–(aq)  Cl2(g) + 2e.
Cl2(g) + 2e.
 Cl2(g) + 2e.
Cl2(g) + 2e.D, Cl2(g) + 2e  2Cl–(aq).
2Cl–(aq).
 2Cl–(aq).
2Cl–(aq).Trong bình điện phân FeCl2, anode là cực dương (+) là nơi các ion âm (Cl-) tiến về.
Tại đây xảy ra quá trình oxi hóa ion Cl- :
2Cl- ➝ Cl2 + 2e
Đáp án: C
Câu 4 [560527]: Cathode trong bình điện phân là điện cực nơi xảy ra
A, quá trình nhường electron.
B, quá trình oxi hóa.
C, quá trình khử.
D, quá trình các chất tăng số oxi hóa.
Cathode là điện cực xảy ra quá trình khử.
Anode là điện cực xảy ra quá trình oxi hóa.
⟹ Chọn đáp án C Đáp án: C
Anode là điện cực xảy ra quá trình oxi hóa.
⟹ Chọn đáp án C Đáp án: C
Câu 5 [1016557]: Trong các quá trình điện phân, các anion di chuyển về
A, cathode, ở đây chúng bị oxi hóa.
B, cực dương, ở đây chúng bị khử.
C, anode, ở đây chúng bị oxi hóa.
D, cathode, ở đây chúng bị khử.
Trong quá trình điện phân, xảy ra trong một bình điện phân có hai điện cực được nối với nguồn điện ngoài:
Anion (ion âm) sẽ bị hút về cực dương (anode) → vì trái dấu với nó.
Tại anode (cực dương), anion bị nhường electron → bị oxi hóa.
⟹ Chọn đáp án C Đáp án: C
Anion (ion âm) sẽ bị hút về cực dương (anode) → vì trái dấu với nó.
Tại anode (cực dương), anion bị nhường electron → bị oxi hóa.
⟹ Chọn đáp án C Đáp án: C
Câu 6 [1016558]: Trong quá trình điện phân, dung dịch Pb(NO3)2 với điện cực trơ, ion Pb2+ di chuyển về
A, cực dương và bị oxi hóa.
B, cực dương và bị khử.
C, cực âm và bị oxi hóa.
D, cực âm và bị khử.
Pb(NO3)2 trong dung dịch phân li thành Pb(NO3)2 → Pb2+ + 2NO3-
Các quá trình xảy trên các điện cực
Anode (+) H2O → 4H+ + 4e + O2
Cathode (-) Pb2+ + 2e → Pb
⟹ Chọn đáp án D Đáp án: D
Các quá trình xảy trên các điện cực
Anode (+) H2O → 4H+ + 4e + O2
Cathode (-) Pb2+ + 2e → Pb
⟹ Chọn đáp án D Đáp án: D
Câu 7 [560528]: Tiến hành điện phân dung dịch SnCl2(aq) như hình:
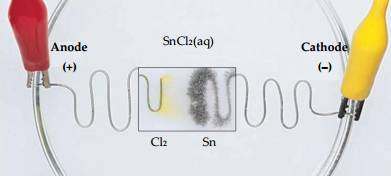
Ở anode xảy ra quá trình

Ở anode xảy ra quá trình
A, oxi hóa ion Cl–.
B, khử ion Cl–.
C, oxi hóa ion Sn2+.
D, khử ion Sn2+.
Tại anode xảy ra quá trình oxi hóa Cl-:
2Cl- ➝ Cl2 + 2e.
⟹ Chọn đáp án A Đáp án: A
2Cl- ➝ Cl2 + 2e.
⟹ Chọn đáp án A Đáp án: A
Câu 8 [560540]: Tiến hành điện phân LiCl nóng chảy. Điện áp tối thiểu cần thiết để quá trình điện phân bắt đầu xảy ra là bao nhiêu? Biết EoLi+/Li = - 3,05 V; EoCl2/2Cl- = 1,36 V.
A, 4,41 V.
B, 1,69 V.
C, 1,56 V.
D, 2,76 V.
Điện phân nóng chảy LiCl:
(-) Cathode: Li+ + 1e ➝ Li (Eo Li+/Li= - 3,05 V)
(+) Anode: 2Cl- ➝ Cl2 + 2e (EoCl2/2Cl-= 1,36 V)
=> U = Eo (+) - Eo (-) = 1,36 - (-0,35) = 4,41 V
(-) Cathode: Li+ + 1e ➝ Li (Eo Li+/Li= - 3,05 V)
(+) Anode: 2Cl- ➝ Cl2 + 2e (EoCl2/2Cl-= 1,36 V)
=> U = Eo (+) - Eo (-) = 1,36 - (-0,35) = 4,41 V
⟹ Chọn đáp án A
Đáp án: A
Câu 9 [560541]: Tiến hành điện phân dung dịch CuBr2. Điện áp tối thiểu cần thiết để quá trình điện phân bắt đầu xảy ra là bao nhiêu? Biết Eo Cu2+/Cu= 0,34 V; EoBr2/2Br-= 1,07 V.
A, 2,70 V.
B, 1,41 V.
C, 0,73 V.
D, 3,15 V.
Điện phân nóng chảy CuBr2:
(-) Cathode: Cu2+ + 2e ➝ Cu (Eo Cu2+/Cu= 0,34 V)
(+) Anode: 2Br- ➝ Br2 + 2e (EoBr2/2Br-= 1,07 V)
=> U = Eo (+) - Eo (-) = 1,07 - 0,34 = 0,73 V
(-) Cathode: Cu2+ + 2e ➝ Cu (Eo Cu2+/Cu= 0,34 V)
(+) Anode: 2Br- ➝ Br2 + 2e (EoBr2/2Br-= 1,07 V)
=> U = Eo (+) - Eo (-) = 1,07 - 0,34 = 0,73 V
⟹ Chọn đáp án C
Đáp án: C
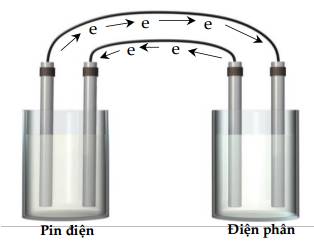
Câu 10 [560562]: Sơ đồ cho thấy một bình điện phân được cung cấp năng lượng bởi một pin điện. Xác định từng điện cực từ trái sang phải là cathode hay anode?

A, Cathode, anode, anode, cathode.
B, Cathode, anode, cathode, anode.
C, Anode, cathode, anode, cathode.
D, Anode, anode, cathode, cathode.
Trong bình điện phân và pin điện, anode là nơi xảy ra quá trình oxi hóa (nhường e), cathode là nơi xảy ra quá trình khử (nhận e).
Dựa vào sơ đồ ta nhận thấy điện cực thứ nhất (từ trái sang phải) nhường electron ⇒ Anode.
Tương tự thế, ta có thứ tự điện cực: Anode, cathode, anode, cathode.
⇒ Chọn đáp án C Đáp án: C
Dựa vào sơ đồ ta nhận thấy điện cực thứ nhất (từ trái sang phải) nhường electron ⇒ Anode.
Tương tự thế, ta có thứ tự điện cực: Anode, cathode, anode, cathode.
⇒ Chọn đáp án C Đáp án: C
Dạng 2: TRẮC NGHIỆM ĐÚNG SAI – mỗi ý a), b), c), d) chọn đúng hoặc sai.
Câu 11 [560563]: Sơ đồ dưới đây cho thấy bố trí thí nghiệm để điện phân nóng chảy lead bromide với hai điện cực trơ:
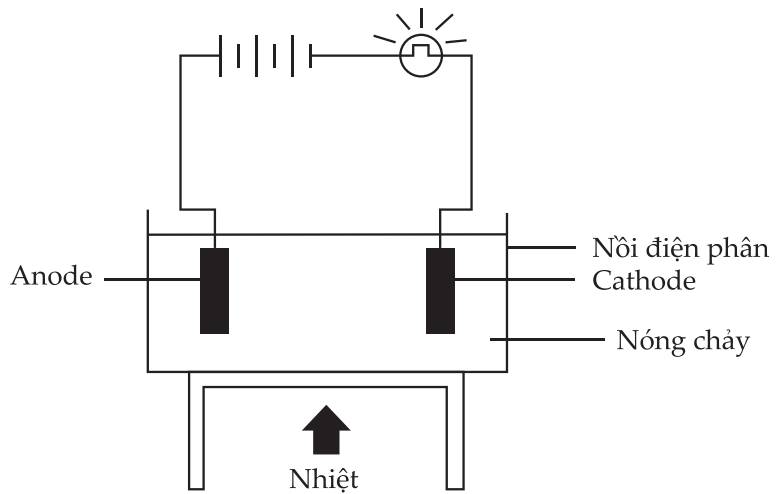

Phân tích các phát biểu sau:
✔️a. Đúng. Lead bromide ở trạng thái rắn nên dòng điện chưa truyền qua được.
❌ b. Sai. Cực âm (cathode) xảy ra quá trình khử Pb2+ thành các hạt Pb bám lên trên điện cực.
✔️ c. Đúng. Tại anode(+) 2Br- ➝ Br2 + 2e => Có khí Br2 thoát ra.
❌ b. Sai. Cực dương bằng than chì giữ nguyên theo thời gian điện phân.
✔️a. Đúng. Lead bromide ở trạng thái rắn nên dòng điện chưa truyền qua được.
❌ b. Sai. Cực âm (cathode) xảy ra quá trình khử Pb2+ thành các hạt Pb bám lên trên điện cực.
✔️ c. Đúng. Tại anode(+) 2Br- ➝ Br2 + 2e => Có khí Br2 thoát ra.
❌ b. Sai. Cực dương bằng than chì giữ nguyên theo thời gian điện phân.
Câu 12 [560564]:
Hình dưới đây mô phỏng quá trình điện phân nóng chảy lead bromide.
Phân tích các phát biểu sau:
✔️ a. Đúng. Ở trạng thái nóng chảy, ion Br- di chuyển về điện cực anode(+) và ion Pb2+ di chuyển về điện cực cathode(-).
❌ b. Sai. Vì 2Br- ➝ Br2 + 2e => ion Br- nhường 2 electron.
✔️ c. Đúng. Tại cathode(-) xảy ra phản ứng: Pb2+ + 2e ➝ Pb.
✔️ d. Đúng. Phản ứng oxi hóa khử vì tại anode xảy ra quá trình oxi hóa, tại cathode xảy ra quá trình khử.
✔️ a. Đúng. Ở trạng thái nóng chảy, ion Br- di chuyển về điện cực anode(+) và ion Pb2+ di chuyển về điện cực cathode(-).
❌ b. Sai. Vì 2Br- ➝ Br2 + 2e => ion Br- nhường 2 electron.
✔️ c. Đúng. Tại cathode(-) xảy ra phản ứng: Pb2+ + 2e ➝ Pb.
✔️ d. Đúng. Phản ứng oxi hóa khử vì tại anode xảy ra quá trình oxi hóa, tại cathode xảy ra quá trình khử.
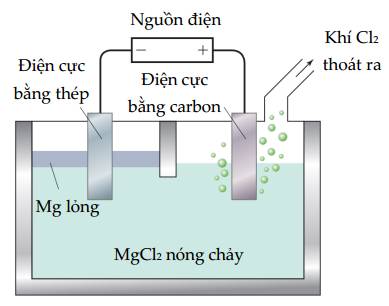
Câu 13 [560565]: Nguyên tố magnesium, được sản xuất thương mại bằng phương pháp điện phân từ muối MgCl2 nóng chảy như bình điện phân được hiển thị dưới đây:
Cho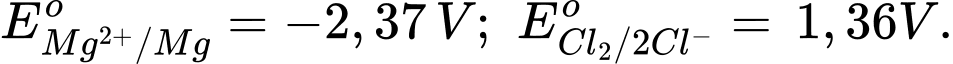

Cho
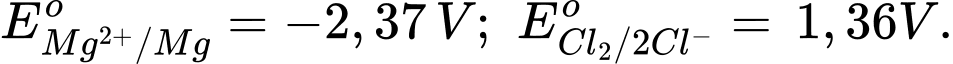
Phân tích các phát biểu sau:
✔️ a. Đúng. Điện áp tối thiểu đặt vào pin U=│Eo cathode - Eo anode│=│-2,37 - 1,36│= 3,73 (V)
✔️ b. Đúng. Tại anode(+): 2Cl- ➝ Cl2 + 2e
✔️ c. Đúng. Tại cathode(-): Mg2+ + 2e ➝ Mg
❌ d. Sai. Phản ứng trong bình điện phân không phải là phản ứng tự diễn biến mà cần có sự can thiệp của dòng điện.
✔️ a. Đúng. Điện áp tối thiểu đặt vào pin U=│Eo cathode - Eo anode│=│-2,37 - 1,36│= 3,73 (V)
✔️ b. Đúng. Tại anode(+): 2Cl- ➝ Cl2 + 2e
✔️ c. Đúng. Tại cathode(-): Mg2+ + 2e ➝ Mg
❌ d. Sai. Phản ứng trong bình điện phân không phải là phản ứng tự diễn biến mà cần có sự can thiệp của dòng điện.
Dạng 3: BÀI TẬP ĐỌC HIỂU – đọc thông tin và trả lời các câu hỏi sau đó
ĐIỆN PHÂN NÓNG CHẢY HF LỎNG
Vì fluorine (F2) chất oxi hóa mạnh nên nó phải được điều chế bằng phương pháp điện phân thay vì chỉ sử dụng các phản ứng oxi hóa ion fluoride (F–) như bình thường. Tuy nhiên, quá trình điện phân không hiệu quả đối với dung dịch nước chứa ion fluoride vì fluoride là chất oxi hóa mạnh hơn cả oxygen (O2). Chúng ta thấy rằng: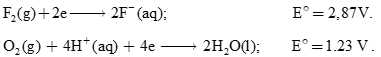
Nếu F2 được hình thành bằng cách điện phân dung dịch fluoride trong nước, nó cũng sẽ ngay lập tức quay trở lại oxi hóa nước thành oxygen.

Vì lý do này, fluorine được điều chế bằng cách điện phân hydrogen fluoride (HF) lỏng có chứa potassium fluoride (KF) để tăng độ dẫn điện của nó, ở khoảng 70°C (Hình a):
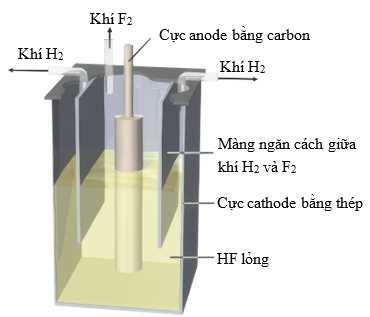
Hình a. Bình điện phân để điều chế khí fluorine.
Lưu ý rằng vì H2 và F2 tạo thành hỗn hợp dễ nổ nên các khí này phải được tách ra khỏi nhau. Tại cathode và anode sẽ xảy ra các quá trình như sau:
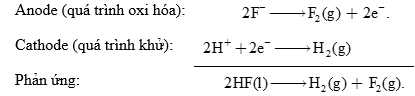
Câu 14 [560586]: Khí F2 có thể được điều chế bằng phương pháp
A, điện phân dung dịch HF.
B, điện phân HF lỏng.
C, nhiệt phân HF.
D, thủy phân HF.
Khí fluorine được điều chế bằng cách điện phân hydrogen fluoride (HF) lóng có chứa potassium fluoride (KF) để tăng độ dẫn điện của nó, ở khoảng 70°C
⇒ Chọn đáp án B Đáp án: B
⇒ Chọn đáp án B Đáp án: B
Câu 15 [560587]: Trong quá trình điện phân HF lỏng, phát biểu nào sau đây sai?
A, Ở anode thu được khí F2.
B, KF đóng vai trò làm tăng khả năng dẫn điện.
C, Màng ngăn để tránh khí H2 tiếp xúc với khí F2.
D, Ở cathode xảy ra quá trình oxi hóa.
Trong quá trình điện phân HF lỏng.
Anode (quá trình oxi hóa): 2F- ⟶ F2 + 2e
Cathode (quá trình khử): 2HF ⟶ H2 + F2
→ Phản ứng: 2HF ⟶ H2 + F2
Fluorine được điều chế bằng cách điện phân hydrogen fluoride (HF) lỏng có chứa potassium fluoride (KF) để tăng độ dẫn điện.
→ D sai vì ở cathode xảy ra quá trình khử.
⇒ Chọn đáp án D
Đáp án: D
Anode (quá trình oxi hóa): 2F- ⟶ F2 + 2e
Cathode (quá trình khử): 2HF ⟶ H2 + F2
→ Phản ứng: 2HF ⟶ H2 + F2
Fluorine được điều chế bằng cách điện phân hydrogen fluoride (HF) lỏng có chứa potassium fluoride (KF) để tăng độ dẫn điện.
→ D sai vì ở cathode xảy ra quá trình khử.
⇒ Chọn đáp án D
Đáp án: D
Câu 16 [560588]: Để điều chế khí F2, đầu tiên sẽ HF phải được được điều chế bằng phản ứng giữa CaF2 với H2SO4: CaF2(s) + H2SO4(l) → 2HF(g) + CaSO4(s). Sau khi có HF, nó có thể bị điện phân: 2HF(l) → F2(g) + H2(g). Fluorine phản ứng cực kì mãnh liệt, vì vậy nó thường được bán dưới dạng hỗn hợp 5% theo thể tích trong khí trơ helium. Cần bao nhiêu gam CaF2 để tạo ra 500,0L khí hỗn hợp 5% F2 trong helium? Giả sử khối lượng riêng của khí F2 là 1,70g/L?
A, 87,2 g.
B, 48,3 g.
C, 60,4 g.
D, 52,0 g.
Số mol F2 trong 500,0L khí hỗn hợp 5% F2 trong helium cần tạo ra là:
n = (500 x 1,7 x 5) / (19 x2 x 100) = 1,1179 (mol)
Quá trình điều chế F2:
CaF2(s) + H2SO4(l) → 2HF(g) + CaSO4(s)
2HF(l) → F2(g) + H2(g)
→ nF2 = nCaF2 = 1,1179 (mol)
→ mCaF2 = 1,1179 x 78 = 87,2 g
⇒ Chọn đáp án A Đáp án: A
n = (500 x 1,7 x 5) / (19 x2 x 100) = 1,1179 (mol)
Quá trình điều chế F2:
CaF2(s) + H2SO4(l) → 2HF(g) + CaSO4(s)
2HF(l) → F2(g) + H2(g)
→ nF2 = nCaF2 = 1,1179 (mol)
→ mCaF2 = 1,1179 x 78 = 87,2 g
⇒ Chọn đáp án A Đáp án: A