Dạng 1. TRẮC NGHIỆM KHÁCH QUAN: mỗi câu hỏi chỉ có một đáp án đúng.
Câu 1 [705569]: Ion kim loại ứng với thế điện cực chuẩn …(1)… hơn sẽ được điện phân trước ở …(2)… Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, dương, cực dương.
B, dương, cực âm.
C, âm, cực âm.
D, âm, cực dương.
Ion kim loại ứng với thế điện cực chuẩn dương hơn sẽ được điện phân trước ở cực âm.
Giải thích:
- Thế điện cực chuẩn của một cặp oxi hoá - khử thể hiện khả năng nhận electron (bị khử) nên:
+ Ion có thế điện cực chuẩn (Eo) dương hơn sẽ dễ bị khử (dễ nhận e hơn) để hình thành kim loại tự do.
+ Ion có thế điện cực chuẩn (Eo) âm hơn sẽ khó bị khử hơn (thường ít tham gia vào quá trình điện phân nếu có mặt của các ion có Eo dương hơn)
⟶ Ưu tiên điện phân ion có thế điện cực chuẩn dương hơn trước.
- Quá trình nhận electron là quá trình khử, xảy ra ở cathode (cực âm).
⇒ Chọn đáp án B Đáp án: B
Giải thích:
- Thế điện cực chuẩn của một cặp oxi hoá - khử thể hiện khả năng nhận electron (bị khử) nên:
+ Ion có thế điện cực chuẩn (Eo) dương hơn sẽ dễ bị khử (dễ nhận e hơn) để hình thành kim loại tự do.
+ Ion có thế điện cực chuẩn (Eo) âm hơn sẽ khó bị khử hơn (thường ít tham gia vào quá trình điện phân nếu có mặt của các ion có Eo dương hơn)
⟶ Ưu tiên điện phân ion có thế điện cực chuẩn dương hơn trước.
- Quá trình nhận electron là quá trình khử, xảy ra ở cathode (cực âm).
⇒ Chọn đáp án B Đáp án: B
Câu 2 [560529]: Quá trình điện phân dung dịch NaCl bão hòa (điện cực trơ, có màng ngăn xốp) thu được đồng thời NaOH và hai đơn chất là
A, O2 và Cl2.
B, H2 và Cl2.
C, H2 và O2.
D, Na và Cl2.
Quá trình điện phân dung dịch NaCl bão hòa (điện cực trơ, có màng ngăn xốp) thu được đồng thời NaOH và hai đơn chất H2 và Cl2.
Phương trình điện phân: 2NaCl + 2H2O ➝ 2NaOH + H2 + Cl2.
⟹ Chọn đáp án B
Đáp án: B
Phương trình điện phân: 2NaCl + 2H2O ➝ 2NaOH + H2 + Cl2.
⟹ Chọn đáp án B
Câu 3 [560530]: Ở cathode (cực âm) của bình điện phân sẽ thu được kim loại khi điện phân dung dịch nào sau đây?
A, HCl.
B, NaCl.
C, CuCl2.
D, KNO3.
Tại cathode (-) của 4 bình điện phân: HCl, NaCl, CuCl2, KNO3
★ Cation không bị điện phân: Na+; K+ (nước sẽ bị điện phân)
★ Cation bị điện phân: Cu2+; H+
Cu2+ + 2e ➝ Cu
H+ + 2e ➝ H2
⟹ Dung dịch CuCl2 sẽ thu được kim loại ở cathode.
⟹ Chọn đáp án C Đáp án: C
★ Cation không bị điện phân: Na+; K+ (nước sẽ bị điện phân)
★ Cation bị điện phân: Cu2+; H+
Cu2+ + 2e ➝ Cu
H+ + 2e ➝ H2
⟹ Dung dịch CuCl2 sẽ thu được kim loại ở cathode.
⟹ Chọn đáp án C Đáp án: C
Câu 4 [560531]: Kim loại nào sau đây được tạo thành khi điện phân (với điện cực trơ) dung dịch muối sulfate tương ứng?
A, Na.
B, Al.
C, Mg.
D, Cu.
Các cation: Na+, K+, Ba2+, Mg2+, Al3+ KHÔNG bị điện phân mà nước sẽ bị điện phân.
Cation Cu2+ bị điện phân: Cu2+ + 2e ➝ Cu.
⇒ Chọn đáp án D Đáp án: D
Cation Cu2+ bị điện phân: Cu2+ + 2e ➝ Cu.
⇒ Chọn đáp án D Đáp án: D
Câu 5 [560532]: Trong công nghiệp, để điều chế NaOH người ta điện phân dung dịch chất X (có màng ngăn). Chất X là
A, Na2SO4.
B, NaNO3.
C, Na2CO3.
D, NaCl.
Trong công nghiệp, để điều chế NaOH người ta điện phân dung dịch NaCl (có màng ngăn)
Phương trình điện phân: 2NaCl + 2H2O ➝ 2NaOH + H2 + Cl2.
⟹ Chọn đáp án D Đáp án: D
Phương trình điện phân: 2NaCl + 2H2O ➝ 2NaOH + H2 + Cl2.
⟹ Chọn đáp án D Đáp án: D
Câu 6 [560533]: Điện phân dung dịch chất T (với điện cực trơ, màng ngăn xốp), thu được dung dịch có chứa chất tan là base. Chất nào sau đây thỏa mãn tính chất của T?
A, CuSO4.
B, AgNO3.
C, FeCl3.
D, NaCl.
Phương trình điện phân:
➝ Dựa vào sản phẩm thì dung dịch NaCl có chứa chất tan là base.
⟹ Chọn đáp án D Đáp án: D
⋆ 2CuSO4 + H2O ➝ 2Cu + 2O2 + H2SO4
⋆ 4AgNO3 + 2H2O ➝ 4Ag + O2 + 4HNO3
⋆ 2FeCl3 + 6H2O ➝ 2Fe(OH)3 + 3Cl2 + 3H2
⋆ 2NaCl + 2H2O ➝ 2NaOH + H2 + Cl2
⟹ Chọn đáp án D Đáp án: D
Câu 7 [560534]: Điện phân dung dịch chất E (với điện cực trơ), thu được dung dịch có chứa chất tan là acid. Chất nào sau đây thỏa mãn tính chất của E?
A, K2SO4.
B, CuSO4.
C, NaCl.
D, KNO3.
Phương trình điện phân
⋆ 2CuSO4 + H2O ➝ 2Cu + 2O2 + H2SO4
⋆ 2NaCl + 2H2O ➝ 2NaOH + H2 + Cl2
⋆ Điện phân K2SO4, KNO3 thực chất là điện phân H2O : H2O ➝ H2 + O2
⟹ Chọn đáp án B
Đáp án: B
⋆ 2CuSO4 + H2O ➝ 2Cu + 2O2 + H2SO4
⋆ 2NaCl + 2H2O ➝ 2NaOH + H2 + Cl2
⋆ Điện phân K2SO4, KNO3 thực chất là điện phân H2O : H2O ➝ H2 + O2
⟹ Chọn đáp án B
Câu 8 [560535]: Điện phân dung dịch nào sau đây thì có khí thoát ra ở cả 2 điện cực (ngay từ lúc mới đầu bắt đầu điện phân)?
A, Cu(NO3)2.
B, FeCl2.
C, K2SO4.
D, FeSO4.
Vì cation K+ và anion SO42- không bị điện phân trong dung dịch nên thực tế điện phân K2SO4 là điện phân H2O:
⋆ H2O ➝ H2 + O2 ➝ Ở cả 2 điện cực có khí thoát ra ngay lúc mới bắt đầu điện phân.
⟹ Chọn đáp án C
Đáp án: C
⋆ H2O ➝ H2 + O2 ➝ Ở cả 2 điện cực có khí thoát ra ngay lúc mới bắt đầu điện phân.
⟹ Chọn đáp án C
Câu 9 [1016559]: Cho dung dịch chứa các ion: Na+, Al3+, Cu2+, Cl-, SO42-, NO3-. Các ion không bị điện phân khi ở trạng thái dung dịch là
A, Na+, Al3+, SO42-, NO3-.
B, Na+, SO42-, Cl-, Al3+.
C, Na+, Al3+, Cl-, NO3-.
D, Al3+, Cu2+, Cl-, NO3-.
Các ion không bị điện phân trong dung dịch là Na+; Al3+; SO42-, NO3-
Trong điện phân dung dịch (với điện cực trơ như than chì hoặc platinum), chỉ một số ion bị điện phân, tùy thuộc vào thế oxi hóa - khử chuẩn và tính chất ưu tiên phóng điện.
Cation: Na+: Không bị điện phân trong dung dịch nước, vì nước ưu tiên bị khử hơn → tạo H2 (khử nước dễ hơn Na+). → Không bị điện phân.
Al3+: cũng như Na+, không bị điện phân trong dung dịch, vì khó khử hơn nước. → Không bị điện phân.
Cu2+: Bị khử dễ dàng hơn nước → bị điện phân tại cathode.
Anion: Cl-: Có thể bị oxi hóa tạo Cl2 nếu nồng độ Cl⁻ đủ cao.
Nhưng trong điều kiện bình thường, có thể xảy ra hoặc không, nhưng vẫn là ion có khả năng bị điện phân.
SO42-: Không bị oxi hóa được trong dung dịch → nước bị oxi hóa thành O2. → Không bị điện phân.
NO3-: Giống SO42-, không bị oxi hóa được, nên không bị điện phân. → Nước bị oxi hóa thay thế.
⟹ Chọn đáp án A Đáp án: A
Trong điện phân dung dịch (với điện cực trơ như than chì hoặc platinum), chỉ một số ion bị điện phân, tùy thuộc vào thế oxi hóa - khử chuẩn và tính chất ưu tiên phóng điện.
Cation: Na+: Không bị điện phân trong dung dịch nước, vì nước ưu tiên bị khử hơn → tạo H2 (khử nước dễ hơn Na+). → Không bị điện phân.
Al3+: cũng như Na+, không bị điện phân trong dung dịch, vì khó khử hơn nước. → Không bị điện phân.
Cu2+: Bị khử dễ dàng hơn nước → bị điện phân tại cathode.
Anion: Cl-: Có thể bị oxi hóa tạo Cl2 nếu nồng độ Cl⁻ đủ cao.
Nhưng trong điều kiện bình thường, có thể xảy ra hoặc không, nhưng vẫn là ion có khả năng bị điện phân.
SO42-: Không bị oxi hóa được trong dung dịch → nước bị oxi hóa thành O2. → Không bị điện phân.
NO3-: Giống SO42-, không bị oxi hóa được, nên không bị điện phân. → Nước bị oxi hóa thay thế.
⟹ Chọn đáp án A Đáp án: A
Câu 10 [1016560]: Khi điện phân dung dịch chứa các ion sau: Cu²⁺, Na⁺, Cl⁻, SO₄²⁻ với điện cực trơ, ion nào sẽ bị khử trước tại cathode?
A, Na⁺.
B, Cu²⁺.
C, H⁺.
D, Không có phản ứng xảy ra.
Tại cathode – cực âm, sẽ xảy ra quá trình điện phân các ion dương.
Trong các ion dương, Cu2+ sẽ bị khử trước, vì có thế khử cao nhất (dễ bị khử nhất).
Quá trình khử xảy ra trên điện cực cathode.
Cu2+ + 2e → Cu
⟹ Chọn đáp án B Đáp án: B
Trong các ion dương, Cu2+ sẽ bị khử trước, vì có thế khử cao nhất (dễ bị khử nhất).
Quá trình khử xảy ra trên điện cực cathode.
Cu2+ + 2e → Cu
⟹ Chọn đáp án B Đáp án: B
Câu 11 [1016561]: Thứ tự điện phân đúng khi có các ion: Al³⁺, Zn²⁺, Fe²⁺, Cu²⁺ là
A, Cu²⁺ → Fe²⁺ → Zn²⁺ → Al³⁺.
B, Zn²⁺ → Fe²⁺ → Cu²⁺ → Al³⁺.
C, Al³⁺ → Zn²⁺ → Fe²⁺ → Cu²⁺.
D, Fe²⁺ → Cu²⁺ → Zn²⁺ → Al³⁺.
Trong quá trình điện phân dung dịch với điện cực trơ, các ion dương (cation) bị khử tại cathode theo thứ tự ưu tiên nhất định.
Các ion kim loại quý như Ag+, Cu2+ dễ bị khử hơn nên sẽ bị điện phân trước, tạo thành kim loại rắn.
Sau đó đến ion H+ trong nước, bị khử thành khí hydrogen.
Những ion của kim loại hoạt động mạnh như Al3+, Na+, K+, Ca2+ rất khó bị khử nên thường không tham gia điện phân trong dung dịch; thay vào đó, nước sẽ bị khử để tạo khí hydrogen.
Thứ tự điện phân đúng các ion trên là
Cu2+ → Fe2+ → Zn2+ → Al3+
⟹ Chọn đáp án A Đáp án: A
Các ion kim loại quý như Ag+, Cu2+ dễ bị khử hơn nên sẽ bị điện phân trước, tạo thành kim loại rắn.
Sau đó đến ion H+ trong nước, bị khử thành khí hydrogen.
Những ion của kim loại hoạt động mạnh như Al3+, Na+, K+, Ca2+ rất khó bị khử nên thường không tham gia điện phân trong dung dịch; thay vào đó, nước sẽ bị khử để tạo khí hydrogen.
Thứ tự điện phân đúng các ion trên là
Cu2+ → Fe2+ → Zn2+ → Al3+
⟹ Chọn đáp án A Đáp án: A
Câu 12 [1016562]: Cho các quá trình oxi hóa – khử sau:
(1) Cu2+ + 2e → Cu;
(2) 2Cl– → Cl2 + 2e;
(3) Fe3+ + 1e → Fe2+.
(4) Fe2+ + 2e → Fe;
(5) 2H+ + 2e → H2.
Khi điện phân hỗn hợp gồm các dung dịch: FeCl3, CuCl2, HCl. Quá trình xảy ra ở cathode và thứ tự xảy ra là
(1) Cu2+ + 2e → Cu;
(2) 2Cl– → Cl2 + 2e;
(3) Fe3+ + 1e → Fe2+.
(4) Fe2+ + 2e → Fe;
(5) 2H+ + 2e → H2.
Khi điện phân hỗn hợp gồm các dung dịch: FeCl3, CuCl2, HCl. Quá trình xảy ra ở cathode và thứ tự xảy ra là
A, (3) → (1) → (5) → (4).
B, (4) → (5) → (1) → (3).
C, (2) → (1) → (5) → (3).
D, (1) → (3) → (5) → (4).
Trong quá trình điện phân dung dịch với điện cực trơ, các ion dương (cation) bị khử tại cathode theo thứ tự ưu tiên nhất định.
Các quá trình tham gia tại cathode là (1); (3); (4); (5).
Tại cathode, chất oxi hoá mạnh hơn sẽ bị khử trước.
Thứ tự điện phân các quá trình tại cathode là
(3) → (1) → (5) → (4)
⟹ Chọn đáp án A Đáp án: A
Các quá trình tham gia tại cathode là (1); (3); (4); (5).
Tại cathode, chất oxi hoá mạnh hơn sẽ bị khử trước.
Thứ tự điện phân các quá trình tại cathode là
(3) → (1) → (5) → (4)
⟹ Chọn đáp án A Đáp án: A
Câu 13 [1016563]: Khi điện phân dung dịch hỗn hợp FeCl2 và CuCl2 tại cathode, ion nào bị điện phân trước?
A, Fe2+.
B, Cu2+.
C, H+(H2O).
D, Cl–.
Tại cathode, chất oxi hoá mạnh hơn sẽ bị khử trước.
Trong dung dịch FeCl2 và CuCl2, có ion Fe2+ và Cu2+
Ion kim loại bị điện phân trước tại cathode là Cu2+ do có tính oxi hóa mạnh hơn Fe2+.
⟹ Chọn đáp án B Đáp án: B
Trong dung dịch FeCl2 và CuCl2, có ion Fe2+ và Cu2+
Ion kim loại bị điện phân trước tại cathode là Cu2+ do có tính oxi hóa mạnh hơn Fe2+.
⟹ Chọn đáp án B Đáp án: B
Câu 14 [1016564]: Trong quá trình mạ vàng (mạ vàng) một vật bằng đồng, người ta dùng cathode là vật bằng đồng, anode làm bằng vàng, dung dịch điện li là dung dịch muối vàng (ví dụ AuCl3). Phương trình hóa học của phản ứng xảy ra ở điện cực âm là
A, Au → Au3+ + 3e.
B, Cu2+ + 2e → Cu.
C, Au3+ + 3e → Au.
D, Cu → Cu2+ + 2e.
Mạ điện là quá trình phủ một lớp kim loại lên bề mặt kim loại khác bằng phương pháp điện phân. Trong quá trình mạ điện, vật cần mạ được gắn với cực âm của nguồn điện, còn kim loại mạ được gắn với cực dương và cùng nhúng trong dung dịch chứa ion kim loại cần mạ. Khi có dòng điện chạy qua, các ion kim loại sẽ di chuyển về cực âm, bị khử thành kim loại và phủ lên bề mặt vật cần mạ.
Các quá trình xảy ra khi mạ Au lên thanh đồng là:
Anode (+) Au → Au3+ + 3e
Cathode (-) Au3+ + 3e → Au.
⟹ Chọn đáp án C Đáp án: C
Các quá trình xảy ra khi mạ Au lên thanh đồng là:
Anode (+) Au → Au3+ + 3e
Cathode (-) Au3+ + 3e → Au.
⟹ Chọn đáp án C Đáp án: C
Câu 15 [560536]: Khi điện phân dung dịch NaCl (cực âm bằng sắt, cực dương bằng than chì, có màng ngăn xốp) thì
A, ở cực âm xảy ra quá trình khử H2O và ở cực dương xảy ra quá trình oxi hóa ion Cl–.
B, ở cực âm xảy ra quá trình oxi hóa H2O và ở cực dương xảy ra quá trình khử ion Cl–.
C, ở cực âm xẩy ra quá trình khử ion Na+ và ở cực dương xảy ra quá trình oxi hóa ion Cl–.
D, ở cực dương xảy ra quá trình oxi hóa ion Na+ và ở cực âm xảy ra quá trình khử ion Cl–.
Trong điện phân:
+ Cathode (cực âm) là nơi xảy ra quá trình khử
+ Anode (cực dương) là nơi xảy ra quá trình oxi hóa
Phản ứng điện cực:
Cathode (-): Na+ không bị điện phân => H2O bị khử 2H2O + 2e ➝ H2 + 2OH-
Anode (+): Cl- bị oxi hóa => 2Cl- ➝ Cl2 + 2e.
⟹ Chọn đáp án A Đáp án: A
+ Cathode (cực âm) là nơi xảy ra quá trình khử
+ Anode (cực dương) là nơi xảy ra quá trình oxi hóa
Phản ứng điện cực:
Cathode (-): Na+ không bị điện phân => H2O bị khử 2H2O + 2e ➝ H2 + 2OH-
Anode (+): Cl- bị oxi hóa => 2Cl- ➝ Cl2 + 2e.
⟹ Chọn đáp án A Đáp án: A
Câu 16 [560537]: Trong quá trình điện phân nóng chảy NaCl, ở anode (cực dương) thu được chất nào?
A, Cl2.
B, Na.
C, NaOH.
D, H2.
Dưới tác dụng của điện trường, ion Cl- chạy về cực dương. Tại đây xảy ra quá trình oxi hóa Cl-
2Cl- ➝ Cl2 + 2e
⟹ Chọn đáp án A Đáp án: A
2Cl- ➝ Cl2 + 2e
⟹ Chọn đáp án A Đáp án: A
Câu 17 [560538]: Khi điện phân NaCl nóng chảy (với điện cực trơ), tại cathode xảy ra
A, sự oxi hóa ion Cl–.
B, sự oxi hóa ion Na+.
C, sự khử ion Cl–.
D, sự khử ion Na+.
Cathode là cực âm nên hút các ion dương (Na+), và tại đây xảy ra quá trình khử Na+:
Na+ + 1e ➝ Na
⟹ Chọn đáp án D Đáp án: D
Na+ + 1e ➝ Na
⟹ Chọn đáp án D Đáp án: D
Câu 18 [560542]: Kim loại nào có thể điều chế được bằng phương pháp điện phân dung dịch?
A, Cu.
B, K.
C, Al.
D, Mg.
★ Điều chế Cu bằng phương pháp điện phân dung dịch vì ion Cu2+ bị khử thành kim loại Cu.
★ Các ion K+, Al3+, Mg2+ không bị điện phân trong dung dịch. Có thể điều chế K, Al, Mg bằng điện phân nóng chảy.
⇒ Chọn đáp án A Đáp án: A
★ Các ion K+, Al3+, Mg2+ không bị điện phân trong dung dịch. Có thể điều chế K, Al, Mg bằng điện phân nóng chảy.
⇒ Chọn đáp án A Đáp án: A
Câu 19 [560543]: Dãy các kim loại đều có thể được điều chế bằng phương pháp điện phân dung dịch muối (với điện cực trơ) là
A, Ni, Cu, Ag.
B, Li, Ag, Sn.
C, Ca, Zn, Cu.
D, Al, Fe, Cr.
Các ion kim loại kiềm (Li+, Na+, K+); kiềm thổ (Ca2+, Ba2+); nhôm (Al3+) không bị khử trong dung dịch nên không thể điều chế kim loại bằng phương pháp điện phân dung dịch muối (với điện cực trơ).
=> Loại đáp án B, C, D vì có chứa Li, Ca, Al.
⇒ Chọn đáp án A Đáp án: A
=> Loại đáp án B, C, D vì có chứa Li, Ca, Al.
⇒ Chọn đáp án A Đáp án: A
Câu 20 [560544]: Trong công nghiệp, kim loại nào sau đây được điều chế bằng phương pháp điện phân nóng chảy?
A, Na.
B, Cu.
C, Ag.
D, Fe.
⭐ Cu, Ag, Fe sử dụng phương pháp điện phân dung dịch.
⭐ Điều chế Na bằng phương pháp điện phân nóng chảy.
⇒ Chọn đáp án A Đáp án: A
⭐ Điều chế Na bằng phương pháp điện phân nóng chảy.
⇒ Chọn đáp án A Đáp án: A
Câu 21 [560545]: Dãy gồm các kim loại thường điều chế bằng phương pháp điện phân nóng chảy là
A, Na, Ca, Al.
B, Mg, Fe, Cu.
C, Cr, Fe, Cu.
D, Cu, Au, Ag.
Phương pháp điện phân nóng chảy có thể điều chế được kim loạt hoạt động mạnh (kim loại kiềm, kiềm thổ, nhôm)
⇒ Chọn đáp án A Đáp án: A
⇒ Chọn đáp án A Đáp án: A
Câu 22 [1016565]: Điện phân dung dịch copper(II) sulfate bằng cặp điện cực copper với cường độ dòng điện không đổi. Đồ thị nào sau đây biểu diễn sự thay đổi khối lượng anode và cathode theo thời gian?
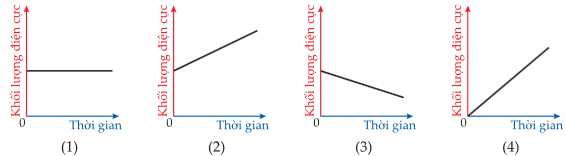

A, (3) và (2).
B, (3) và (4).
C, (2) và (3).
D, (1) và (3).
Điện phân dung dịch copper(II) sulfate bằng cặp điện cực copper với cường độ dòng điện không đổi.
Quá trình xảy ra trên các điện cực
Anode (+) Cu → Cu2+ + 2e
Cathode (-) Cu2+ + 2e → Cu
Trong quá trình điện phân xảy ra hiện tượng dương cực tan, Cu trên Anode tan dần nên khối lượng điện cực anode sẽ giảm đi
Trên điện cực cathode có Cu sinh ra bám lên, nên khối lượng sẽ tăng lên.
Sơ đồ (3) biểu diễn cho anode
Sơ đồ (2) biểu diễn cho cathode.
⟹ Chọn đáp án A Đáp án: A
Quá trình xảy ra trên các điện cực
Anode (+) Cu → Cu2+ + 2e
Cathode (-) Cu2+ + 2e → Cu
Trong quá trình điện phân xảy ra hiện tượng dương cực tan, Cu trên Anode tan dần nên khối lượng điện cực anode sẽ giảm đi
Trên điện cực cathode có Cu sinh ra bám lên, nên khối lượng sẽ tăng lên.
Sơ đồ (3) biểu diễn cho anode
Sơ đồ (2) biểu diễn cho cathode.
⟹ Chọn đáp án A Đáp án: A
Dạng 2: TRẮC NGHIỆM ĐÚNG SAI – mỗi ý a), b), c), d) chọn đúng hoặc sai.
Câu 23 [560567]: Điện phân dung dịch NaCl là một phương pháp thu được những sản phẩm có tính ứng dụng rất cao trong ngành công nghiệp sản xuất. Tuy nhiên, thực tế phương pháp này được vận dụng phần lớn vào việc xử lý nước hồ bơi do tạo ra ion ClO– có tính oxi hóa mạnh.
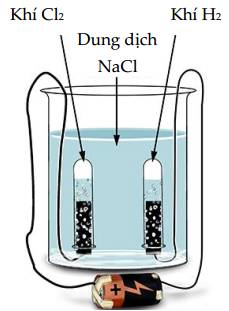

Phân tích các phát biểu sau:
✔️ a. Đúng. Ở cathode (-): ion Na+ không bị điện phân, H2O bị điện phân (Phương trình phản ứng: 2H2O + 2e ➝ H2 + 2OH-)
✔️ b. Đúng. Không có màng ngăn, NaOH sinh ra ở cathode sẽ phản ứng với khí Cl2 sinh ra ở anode => sinh ra dung dịch (NaOCl, NaCl) gọi là nước Javel.
❌ c. Sai. Ion Na+ không bị điện phân nên nồng độ không đổi.
✔️ d. Đúng. Phản ứng trong điện phân là quá trình không tự diễn biến mà cần có sự can thiệp của dòng điện.
✔️ a. Đúng. Ở cathode (-): ion Na+ không bị điện phân, H2O bị điện phân (Phương trình phản ứng: 2H2O + 2e ➝ H2 + 2OH-)
✔️ b. Đúng. Không có màng ngăn, NaOH sinh ra ở cathode sẽ phản ứng với khí Cl2 sinh ra ở anode => sinh ra dung dịch (NaOCl, NaCl) gọi là nước Javel.
❌ c. Sai. Ion Na+ không bị điện phân nên nồng độ không đổi.
✔️ d. Đúng. Phản ứng trong điện phân là quá trình không tự diễn biến mà cần có sự can thiệp của dòng điện.
Câu 24 [560568]: Quá trình điện phân dung dịch NaCl đặc thu được hai khí A và B như sơ đồ dưới đây:
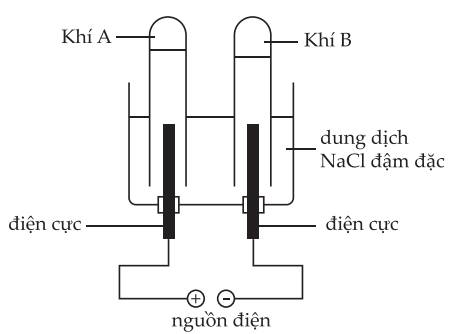

Phân tích các phát biểu sau:
❌ a. Sai. Quá trình điện phân NaCl tạo ra 2 khí là H2 và Cl2. Trong đó, H2 nhẹ hơn không khí và Cl2 nặng hơn không khí
✔️ b. Đúng. Điện cực carbon có đặc tính trơ và ổn định => có thể dùng để điện phân dung dịch NaCl.
❌ c. Sai. Lúc bắt đầu điện phân, ở anode điện phân ion Cl-, cathode điện phân H2O. Đến khi ion Cl- hết thì cả 2 điện cực mới xảy ra điện phân H2O.
❌ d. Sai. Điện cực dương (anode) sinh ra khí Cl2 (khí A màu vàng nhạt); Điện cực âm (cathode) sinh ra khí H2 (khí B không màu).
❌ a. Sai. Quá trình điện phân NaCl tạo ra 2 khí là H2 và Cl2. Trong đó, H2 nhẹ hơn không khí và Cl2 nặng hơn không khí
✔️ b. Đúng. Điện cực carbon có đặc tính trơ và ổn định => có thể dùng để điện phân dung dịch NaCl.
❌ c. Sai. Lúc bắt đầu điện phân, ở anode điện phân ion Cl-, cathode điện phân H2O. Đến khi ion Cl- hết thì cả 2 điện cực mới xảy ra điện phân H2O.
❌ d. Sai. Điện cực dương (anode) sinh ra khí Cl2 (khí A màu vàng nhạt); Điện cực âm (cathode) sinh ra khí H2 (khí B không màu).
Câu 25 [560570]: Có 6 hóa chất từ A đến F được hòa tan trong nước và lần lượt nối vào mạch điện bên dưới. A đại diện cho một ampe kế, được sử dụng để đo dòng điện. Bảng hiển thị kết quả.
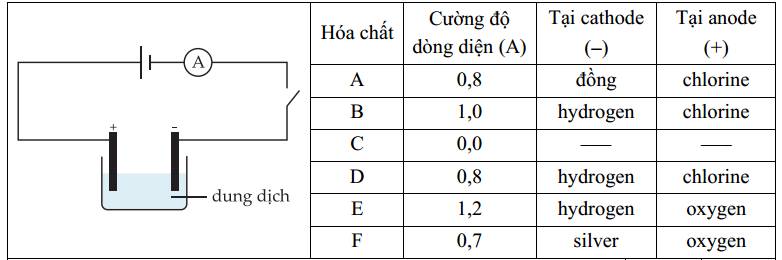

Phân tích các phát biểu sau:
✔️a. Đúng. Tại cathode thu được kim loại Cu, anode thu được khí chlorine => hóa chất A có thể là CuCl2.
Cathode ( - ) : Cu2+ + 2e ⟶ Cu
Anode ( + ) : 2Cl- ⟶ Cl2 + 2e
✔️ b. Đúng. Vì cường độ dòng điện bằng 0 nên chất C không dẫn diện, không có khả năng phân li thành ion trong dung dịch => Saccharose là đúng.
❌ c. Sai. Tại anode (+) thu được khí oxygen (nước bị điện phân) nên anion trong dung dịch không bị điện phân. Tuy nhiên có nhiều loại anion không bị điện phân như SO42-, NO3-, ClO4-,... => Dung dịch E và F có thể chứa khác loại anion.
Anode (+) 2H2O ⟶ 4H+ + O2 + 4e
❌d. Sai. Điện phân dung dịch B, D, E tại cathode có thể là điện phân nước và H+ để tạo H2
✔️a. Đúng. Tại cathode thu được kim loại Cu, anode thu được khí chlorine => hóa chất A có thể là CuCl2.
Cathode ( - ) : Cu2+ + 2e ⟶ Cu
Anode ( + ) : 2Cl- ⟶ Cl2 + 2e
✔️ b. Đúng. Vì cường độ dòng điện bằng 0 nên chất C không dẫn diện, không có khả năng phân li thành ion trong dung dịch => Saccharose là đúng.
❌ c. Sai. Tại anode (+) thu được khí oxygen (nước bị điện phân) nên anion trong dung dịch không bị điện phân. Tuy nhiên có nhiều loại anion không bị điện phân như SO42-, NO3-, ClO4-,... => Dung dịch E và F có thể chứa khác loại anion.
Anode (+) 2H2O ⟶ 4H+ + O2 + 4e
❌d. Sai. Điện phân dung dịch B, D, E tại cathode có thể là điện phân nước và H+ để tạo H2
Câu 26 [560569]: Tiến hành điện phân dung dịch Na2SO4(aq). Nhỏ thêm chất chỉ thị phenolphthalein vào mỗi điện cực.
Phân tích các phát biểu sau:
✔️ a. Đúng. Ion Na+ và ion SO42- không bị điện phân nên H2O ở 2 điện cực bị điện phân sinh ra khí ở cả 2 điện cực.
❌ b. Sai. Tại anode(+): 2H2O ➝ O2 + 4H+ + 4e. Tại cathode(-): 2H2O + 2e ➝ H2 + 2OH- => Cathode (tạo ion OH-) làm đổi màu dung dịch phenolphtalein.
❌ c. Sai. Trộn dung dịch 2 nửa pin thì mất màu hồng vì ion H+ trung hòa hết lượng ion OH-.
❌ d. Sai. Na2SO4 phân li ra các ion dẫn điện => làm giảm điện trở của bình điện phân ⇒ tăng hiệu suất quá trình điện phân.
✔️ a. Đúng. Ion Na+ và ion SO42- không bị điện phân nên H2O ở 2 điện cực bị điện phân sinh ra khí ở cả 2 điện cực.
❌ b. Sai. Tại anode(+): 2H2O ➝ O2 + 4H+ + 4e. Tại cathode(-): 2H2O + 2e ➝ H2 + 2OH- => Cathode (tạo ion OH-) làm đổi màu dung dịch phenolphtalein.
❌ c. Sai. Trộn dung dịch 2 nửa pin thì mất màu hồng vì ion H+ trung hòa hết lượng ion OH-.
❌ d. Sai. Na2SO4 phân li ra các ion dẫn điện => làm giảm điện trở của bình điện phân ⇒ tăng hiệu suất quá trình điện phân.
Dạng 3: TRẮC NGHIỆM YÊU CẦU TRẢ LỜI NGẮN
Câu 27 [1016566]: Cho các ion sau: Ca2+, K+, SO42–, Br–, Cu2+, NO3–. Trong dung dịch, có bao nhiêu ion không bị điện phân?
Điện phân dung dịch là quá trình xảy ra ở điện cực, trong đó:
Ion dương (cation) sẽ bị khử ở cathode (–).
Ion âm (anion) sẽ bị oxi hóa ở anode (+).
Tuy nhiên, không phải ion nào có mặt trong dung dịch cũng bị điện phân – việc một ion có tham gia phản ứng điện phân hay không còn phụ thuộc vào thế điện cực chuẩn (Eo), tức là khả năng oxi hóa/khử của ion đó so với nước.
Các ion không bị điện phân là Ca2+; K+; SO42–; NO3–.
⟹ Điền đáp án 4
Ion dương (cation) sẽ bị khử ở cathode (–).
Ion âm (anion) sẽ bị oxi hóa ở anode (+).
Tuy nhiên, không phải ion nào có mặt trong dung dịch cũng bị điện phân – việc một ion có tham gia phản ứng điện phân hay không còn phụ thuộc vào thế điện cực chuẩn (Eo), tức là khả năng oxi hóa/khử của ion đó so với nước.
Các ion không bị điện phân là Ca2+; K+; SO42–; NO3–.
⟹ Điền đáp án 4
Câu 28 [1016567]: Cho các trường hợp sau:
(1) Điện phân nóng chảy CaCl2;
(2) Điện phân nóng chảy MgBr2;
(3) Điện phân dung dịch FeSO4;
(4) Điện phân dung dịch NaCl.
Số trường hợp ion kim loại bị khử thành kim loại là bao nhiêu?
(1) Điện phân nóng chảy CaCl2;
(2) Điện phân nóng chảy MgBr2;
(3) Điện phân dung dịch FeSO4;
(4) Điện phân dung dịch NaCl.
Số trường hợp ion kim loại bị khử thành kim loại là bao nhiêu?
(1) Điện phân nóng chảy CaCl2:
Quá trình xảy ra trên các điện cực
Anode (+) 2Cl‒ ⟶ Cl2 + 2e
Cathode (‒) Ca2+ + 2e ⟶ Ca
Phản ứng điện phân
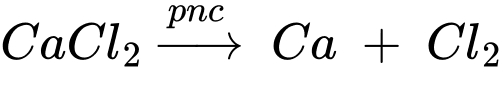
(2) Điện phân nóng chảy MgBr2;
Quá trình xảy ra trên các điện cực
Anode (+) 2Br‒ ⟶ Br2 + 2e
Cathode (‒) Mg2+ + 2e ⟶ Mg
Phản ứng điện phân
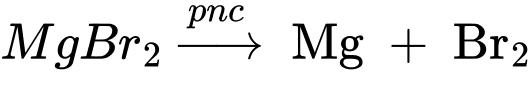
(3) Điện phân dung dịch FeSO4;
Quá trình xảy ra trên các điện cực
Anode (+) H2O ⟶ 4H+ + 4e + O2
Cathode (‒) Fe2+ + 2e ⟶ Fe
Phản ứng điện phân
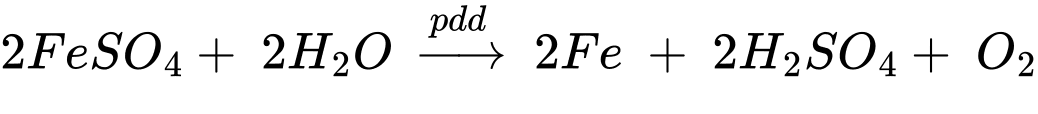
(4) Điện phân dung dịch NaCl.
Quá trình xảy ra trên các điện cực
Anode (+) 2Cl‒ ⟶ Cl2 + 2e
Cathode (‒) 2H2O + 2e ⟶ 2OH‒+ H2
Phản ứng điện phân
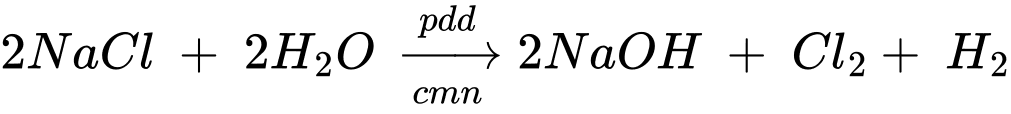
Số trường hợp ion kim loại bị khử thành kim loại là: 3
⟹ Điền đáp án 3
Quá trình xảy ra trên các điện cực
Anode (+) 2Cl‒ ⟶ Cl2 + 2e
Cathode (‒) Ca2+ + 2e ⟶ Ca
Phản ứng điện phân
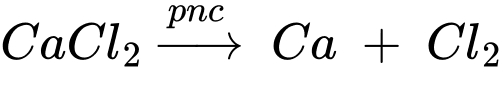
(2) Điện phân nóng chảy MgBr2;
Quá trình xảy ra trên các điện cực
Anode (+) 2Br‒ ⟶ Br2 + 2e
Cathode (‒) Mg2+ + 2e ⟶ Mg
Phản ứng điện phân
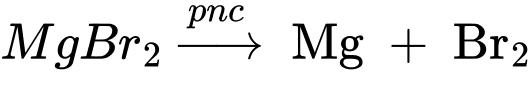
(3) Điện phân dung dịch FeSO4;
Quá trình xảy ra trên các điện cực
Anode (+) H2O ⟶ 4H+ + 4e + O2
Cathode (‒) Fe2+ + 2e ⟶ Fe
Phản ứng điện phân
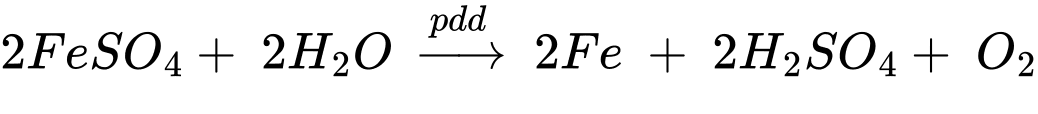
(4) Điện phân dung dịch NaCl.
Quá trình xảy ra trên các điện cực
Anode (+) 2Cl‒ ⟶ Cl2 + 2e
Cathode (‒) 2H2O + 2e ⟶ 2OH‒+ H2
Phản ứng điện phân
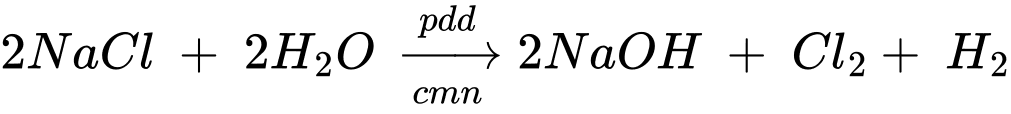
Số trường hợp ion kim loại bị khử thành kim loại là: 3
⟹ Điền đáp án 3
Câu 29 [1016568]: Có các bán phản ứng sau:
(1) Cu2+ +2e → Cu;
(2) Cu → Cu2+ + 2e;
(3) 2H2O + 2e → H2 + 2OH–;
(4) 2H2O → 4H+ + O2 + 4e;
(5) 2Br–→ Br2+2e;
(6) 2H+ + 2e → H2;
Có bao nhiêu bán phản ứng xảy ra ở cathode trong quá trình điện phân dung dịch?
(1) Cu2+ +2e → Cu;
(2) Cu → Cu2+ + 2e;
(3) 2H2O + 2e → H2 + 2OH–;
(4) 2H2O → 4H+ + O2 + 4e;
(5) 2Br–→ Br2+2e;
(6) 2H+ + 2e → H2;
Có bao nhiêu bán phản ứng xảy ra ở cathode trong quá trình điện phân dung dịch?
Quá trình xảy ra trên cathode là quá trình khử
Các bán phản ứng xảy ra trên cathode là
(1) Cu2+ +2e → Cu
(3) 2H2O + 2e → H2 + 2OH¯
(6) 2H+ + 2e → H2
⟹ Điền đáp án 3
Các bán phản ứng xảy ra trên cathode là
(1) Cu2+ +2e → Cu
(3) 2H2O + 2e → H2 + 2OH¯
(6) 2H+ + 2e → H2
⟹ Điền đáp án 3
Câu 30 [1016569]: Lithium (Li) là kim loại quan trọng trong các ngành công nghiệp như pin điện, chế tạo các hợp kim,… Kim loại Li được điều chế bằng phương pháp điện phân nóng chảy hỗn hợp LiCl – KCl với tỷ lệ khối lượng tương ứng 3 : 2, ở nhiệt độ 425 – 500 °C. Hiệu suất điện phân đạt 75%. Khối lượng kim loại Li (kg) thu được từ 1 tấn hỗn hợp LiCl – KCl ban đầu là bao nhiêu (làm tròn kết quả đến hàng phần mười)?
Vì LiCl chiếm tỉ lệ khối lượng 3:2 ( ứng với 60%) nên:
Khối lượng của LiCl trong 1 tấn hỗn hợp là mLiCl = 1000 × 60% = 600 kg
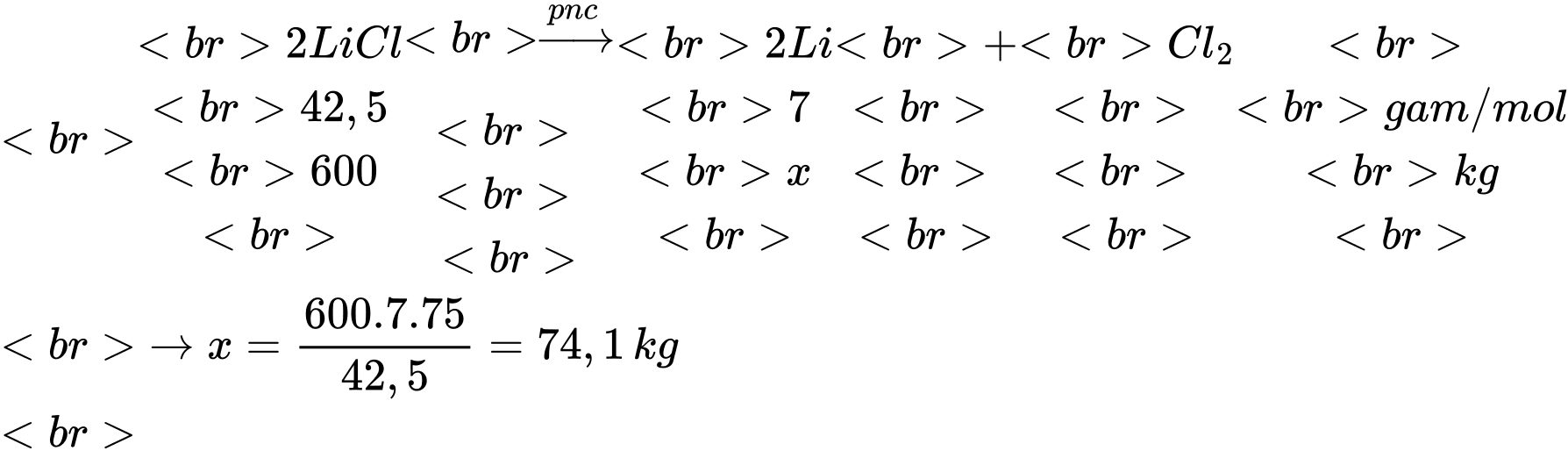
⟹ Điền đáp án: 74,1
Khối lượng của LiCl trong 1 tấn hỗn hợp là mLiCl = 1000 × 60% = 600 kg
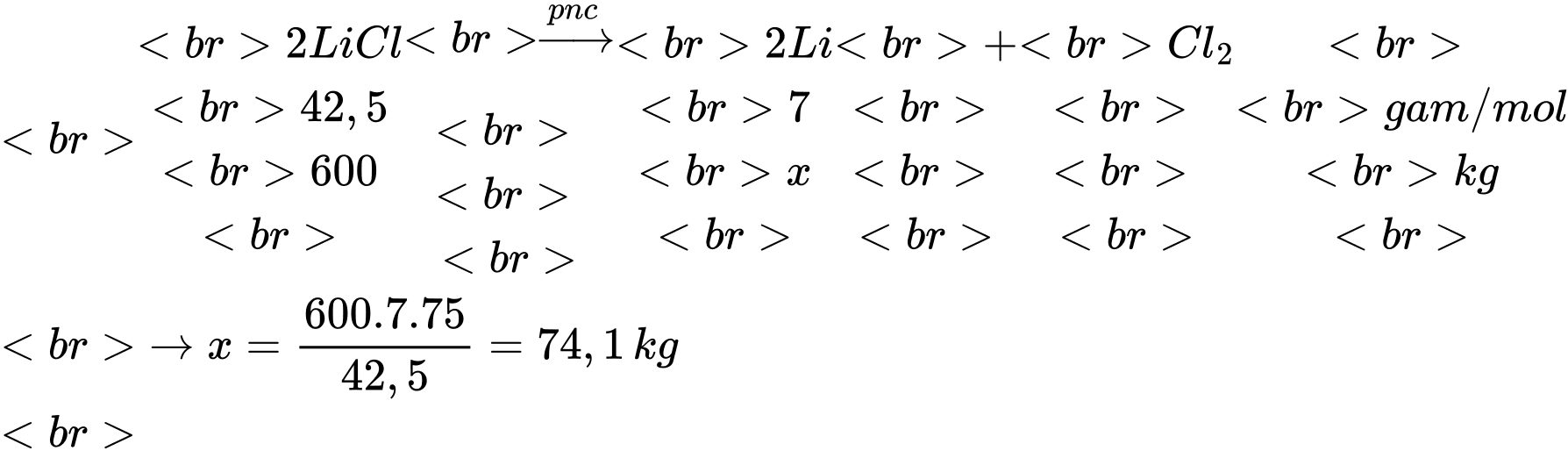
⟹ Điền đáp án: 74,1
Câu 31 [1016570]: Trong công nghiệp, phương pháp điện phân dung dịch sodium chloride có màng ngăn xốp được dùng để sản xuất xút (NaOH), khí chlorine và khí hydrogen. Khí chlorine và khí hydrogen được dùng để tổng hợp hydrochloric acid. Một nhà máy với quy mô sản xuất 160 tấn xút mỗi ngày thì đồng thời sản xuất được V m3 dung dịch HCl 37% (D = 1,19 g/mL). Biết rằng 65% lượng khí chlorine từ quá trình điện phân được dùng để sản xuất hydrochloric acid (hiệu suất 90%). Tính giá trị của V (làm tròn đến hàng đơn vị).
Đổi 1,19 g/mL = 1,19 tấn/m3
Ta có phương trình:
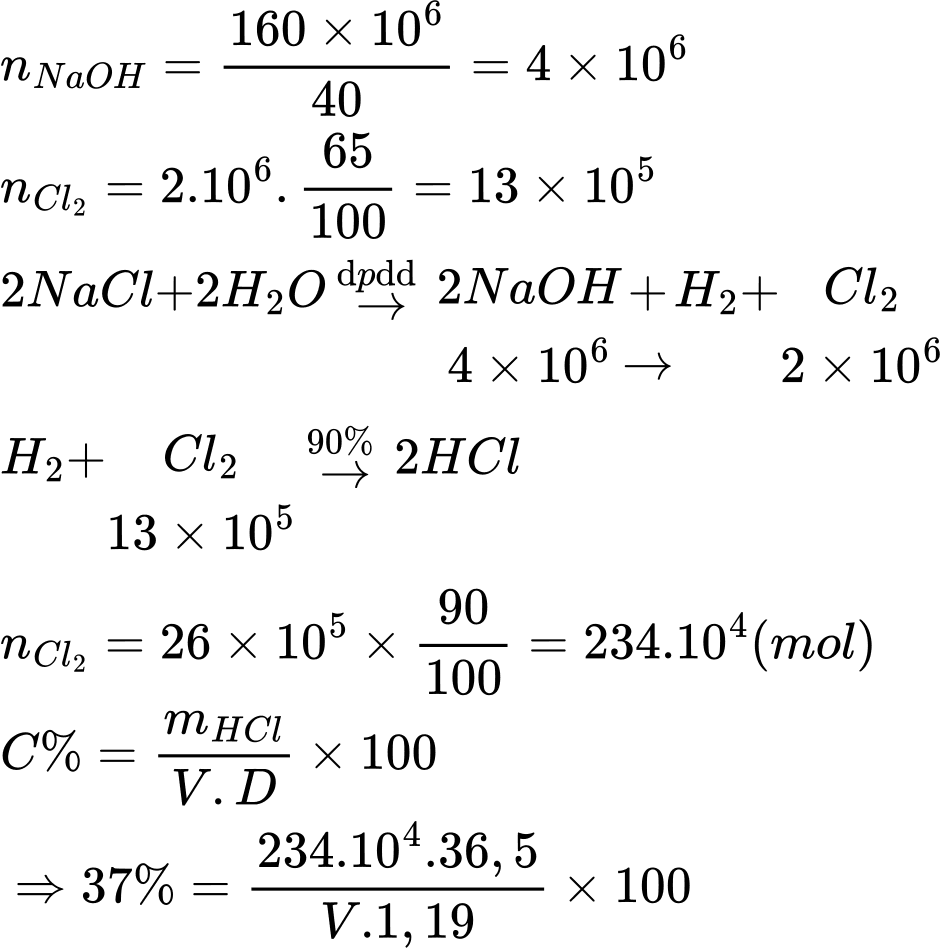
⟶ V = 193,98 (m3)
⟹ Điền đáp án 194
Ta có phương trình:
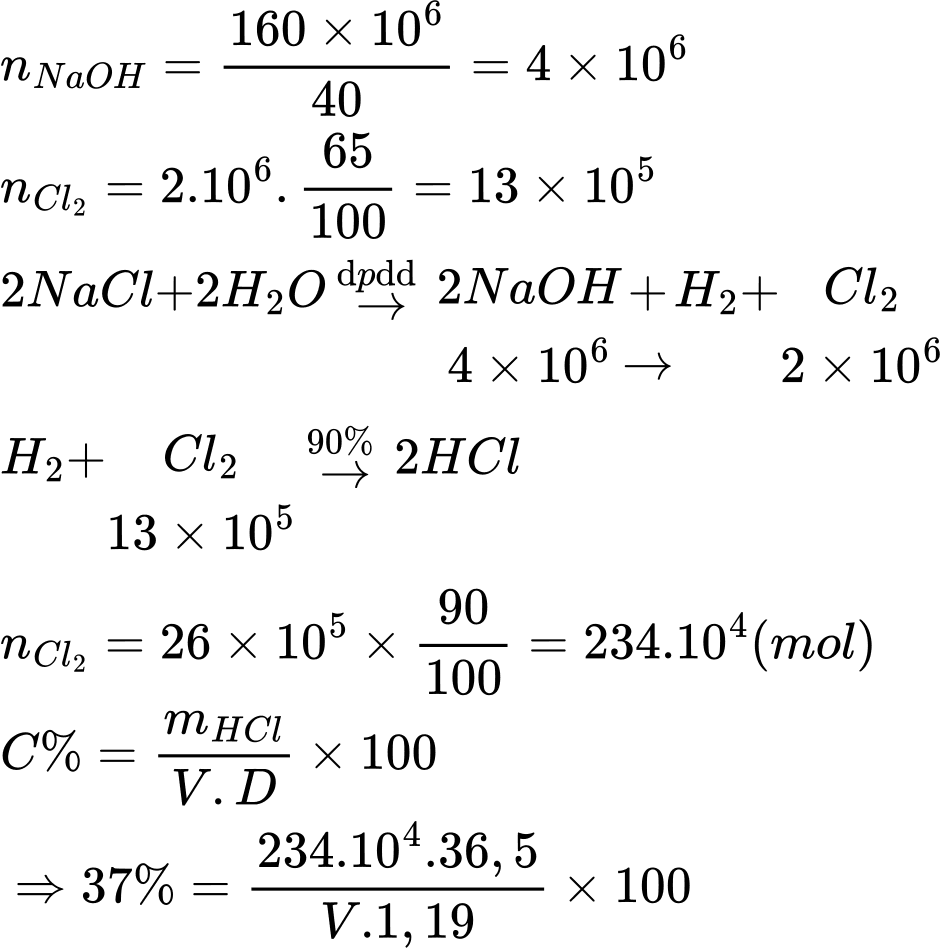
⟶ V = 193,98 (m3)
⟹ Điền đáp án 194
Câu 32 [706144]: Trong công nghiệp chlorine-kiềm, dung dịch sodium chloride (NaCl) bão hoà có nồng độ khoảng 300 g.L–1 chỉ được điện phân một phần thành “nước muối nghèo” có nồng độ 220 g.L–1. “Nước muối nghèo" sau đó được dẫn ra khỏi bể điện phân, trong khi nước muối bão hoà mới được bơm vào. Từ x lít dung dịch NaCl bão hoà điện phân thành “nước muối nghèo” sẽ sản xuất được một thùng 10 lít xút 50% thương phẩm có khối lượng riêng là 1,52 g.mL–1. Biết lượng xút trong quá trình điều chế thất thoát 20% và trong quá trình điện phân, thể tích dung dịch thay đổi không đáng kể. Tính giá trị của x (làm tròn đến hàng đơn vị).
Đổi 10 L = 10000 mL
Khối lượng dung dịch NaOH là mdd NaOH = 10000 × 1,52 = 15200 gam
Khối lượng NaOH là mNaOH = 15200 × 50% = 7600 gam
Số mol của NaOH là nNaOH = 7600 ÷ 40 = 190 mol
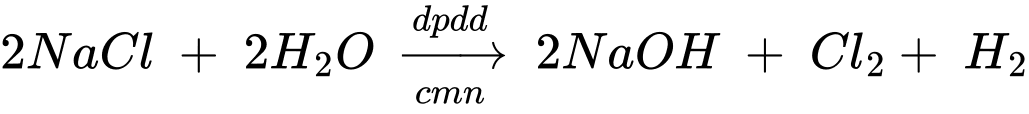
Theo phương trình số mol của NaCl là 190 mol
Khối lượng của NaCl là: x.(300 – 220) = 190 × 58,5 : 80% → x ≈ 173,67
⟹ Điền đáp án: 174
Khối lượng dung dịch NaOH là mdd NaOH = 10000 × 1,52 = 15200 gam
Khối lượng NaOH là mNaOH = 15200 × 50% = 7600 gam
Số mol của NaOH là nNaOH = 7600 ÷ 40 = 190 mol
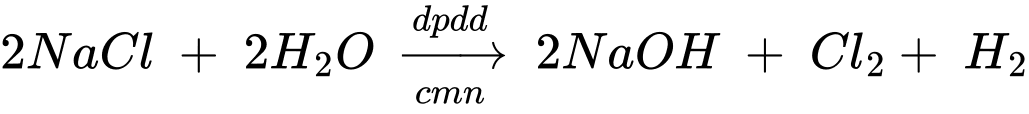
Theo phương trình số mol của NaCl là 190 mol
Khối lượng của NaCl là: x.(300 – 220) = 190 × 58,5 : 80% → x ≈ 173,67
⟹ Điền đáp án: 174
Dạng 4: BÀI TẬP ĐỌC HIỂU – đọc thông tin và trả lời các câu hỏi sau đó
ĐIỀU CHẾ KHÍ CHLORINE
Khí chlorine (Cl2) được điều chế trong công nghiệp bằng phương pháp điện phân nóng chảy NaCl hoặc bằng quá trình chlor–alkali, điện phân dung dịch NaCl đậm đặc (chlor biểu thị cho chlorine và alkali biểu thị cho kim loại kiềm, chẳng hạn như sodium Na). Hai trong số các quy trình điện phân phổ biến được sử dụng trong quá trình chlor–alkali là điện phân thủy ngân và điện phân có màng ngăn. Ở cả hai quy trình điện phân, phản ứng tổng quát đều là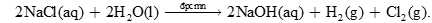
Như bạn có thể thấy, phản ứng này tạo ra hai sản phẩm phụ hữu ích là NaOH và H2. Các bình điện phân được thiết kế để tách khí chlorine ra khỏi dung dịch sodium hydroxide và khí hydrogen để ngăn chặn các phản ứng phụ như:
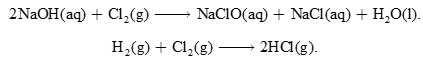
Những phản ứng này phải được ngăn chặn vì chúng sẽ làm tiêu hao đi các sản phẩm mà chúng ta mong muốn và cũng rất nguy hiểm vì hỗn hợp H2 và Cl2 dễ gây nổ. Hình vẽ dưới đây cho thấy quy trình điện phân thủy ngân. Cathode là bể thủy ngân lỏng ở đáy bình điện phân và anode được làm bằng than chì hoặc titanium phủ platinum. Nước muối (NaCl) liên tục được đưa vào bình điện phân như thể hiện trong sơ đồ:
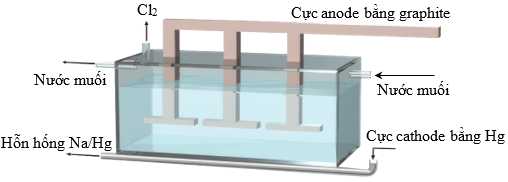
Các phản ứng tương ứng ở điện cực như sau:
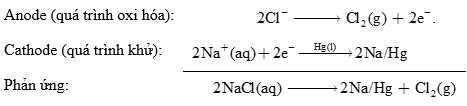
Trong đó Na/Hg biểu thị sự hình thành hỗn hống của sodium với thủy ngân. Khí chlorine được tạo ra theo cách này rất tinh khiết. Hỗn hống sodium không phản ứng với dung dịch nước muối mà bị phân hủy khi xử lý bằng nước tinh khiết bên ngoài bình điện phân:
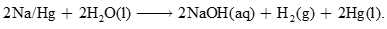
Sản phẩm phụ là sodium hydroxide và khí hydrogen. Mặc dù thủy ngân được tuần hoàn trở lại bình điện phân để tái sử dụng, tuy nhiên một phần thủy ngân cũng sẽ bị rò rỉ ra bên ngoài môi trường cùng với các dung dịch thải, dẫn đến ô nhiễm thủy ngân. Đây là một nhược điểm lớn của quy trình điện phân thủy ngân.
Đối với quy trình điện phân có màng ngăn (Hình vẽ dưới). Tấm màng amiăng cho phép các ion có thể thấm qua nhưng không cho phép các khí hydrogen và chlorine đi qua và do đó ngăn không cho các khí trộn lẫn vào với nhau. Định kỳ, dung dịch nước muối NaCl mới được thêm vào bình điện phân và dung dịch sodium hydroxide sẽ được xả ra bên ngoài như hình minh họa. Quy trình điện phân có màng ngăn không gây ra vấn đề ô nhiễm.
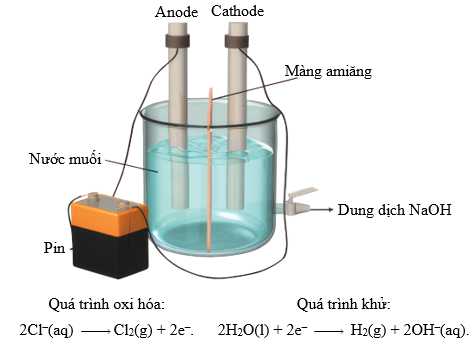
Trong phòng thí nghiệm, chlorine có thể được điều chế bằng cách đun nóng NaCl trong sulfuric acid đậm đặc với sự có mặt của manganese(IV) oxide. Phản ứng xảy ra như sau:
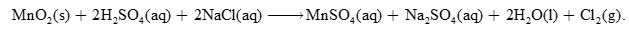
Câu 33 [560589]: Khí Cl2 có thể được điều chế bằng phương pháp
A, điện phân nóng chảy và điện phân dung dịch có màng ngăn.
B, điện phân nóng chảy và điện phân dung dịch không màng ngăn.
C, nhiệt phân nóng chảy và điện phân dung dịch có màng ngăn.
D, thủy phân và điện phân dung dịch không màng ngăn.
Khí Cl2 có thể được điều chế bằng phương pháp điện phân nóng chảy và điện phân dung dịch có màng ngăn. Đáp án: A
Câu 34 [560590]: Khi điện phân dung dịch NaCl có màng ngăn, trong các phát biểu sau:
(a) Cathode thu được khí H2 và dung dịch NaOH.
(b) Anode thu được khí Cl2.
(c) Màng ngăn cho phép ion Cl– di chuyển qua.
(d) Theo thời gian, nồng độ ion Na+ giảm dần.
(e) Điện phân không có màng ngăn thì ở anode thu được khí Cl2.
Số phát biểu đúng là
(a) Cathode thu được khí H2 và dung dịch NaOH.
(b) Anode thu được khí Cl2.
(c) Màng ngăn cho phép ion Cl– di chuyển qua.
(d) Theo thời gian, nồng độ ion Na+ giảm dần.
(e) Điện phân không có màng ngăn thì ở anode thu được khí Cl2.
Số phát biểu đúng là
A, 1.
B, 2.
C, 3.
D, 4.
Phân tích các phát biểu:
✔️(a) Cathode thu được khí H2 và dung dịch NaOH.
Tại cathode, cation H+ bị khử trước ( từ nước ) tạo H2. Nồng độ OH- tăng, Na+ không bị điện phân ⟶ NaOH.
✔️(b) Anode thu được khí Cl2.
Tại anode, anion bị oxi hóa : 2Cl - ⟶ Cl2 + 2e
❌(c) Màng ngăn không cho phép ion Cl– di chuyển qua.
Màng ngăn trong quá trình điện phân dung dịch NaCl có vai trò ngăn không cho khí Cl2 sinh ra ở anode tác dụng với ion OH- và khí H2 sinh ra ở cathode, tránh tạo thành các sản phẩm không mong muốn như nước Javel (NaClO). Màng ngăn thường là màng xốp hoặc màng trao đổi ion, chỉ cho phép các ion Na+ và H2O di chuyển qua, còn ion Cl- và OH- thì không.
❌(d) Theo thời gian, nồng độ ion Na+ tăng dần.
Trong quá trình điện phân dung dịch NaCl có màng ngăn, ion Na+ di chuyển từ anode sang cathode qua màng ngăn để cân bằng điện tích. Tuy nhiên, ion Na+ không tham gia trực tiếp vào phản ứng điện cực. Nước bị điện phân ở cathode tạo ra ion OH-, kết hợp với ion Na+ tạo thành NaOH. Do đó, nồng độ ion Na+ thực tế không giảm mà có thể tăng lên trong dung dịch ở vùng cathode do sự tích tụ NaOH.
❌(e) Điện phân không có màng ngăn thì ở anode thu được khí Cl2.
Anode thu được Cl2 tuy nhiên sau đó sẽ phản ứng luôn với NaOH sinh ra nước Javel. Đáp án: B
✔️(a) Cathode thu được khí H2 và dung dịch NaOH.
Tại cathode, cation H+ bị khử trước ( từ nước ) tạo H2. Nồng độ OH- tăng, Na+ không bị điện phân ⟶ NaOH.
✔️(b) Anode thu được khí Cl2.
Tại anode, anion bị oxi hóa : 2Cl - ⟶ Cl2 + 2e
❌(c) Màng ngăn không cho phép ion Cl– di chuyển qua.
Màng ngăn trong quá trình điện phân dung dịch NaCl có vai trò ngăn không cho khí Cl2 sinh ra ở anode tác dụng với ion OH- và khí H2 sinh ra ở cathode, tránh tạo thành các sản phẩm không mong muốn như nước Javel (NaClO). Màng ngăn thường là màng xốp hoặc màng trao đổi ion, chỉ cho phép các ion Na+ và H2O di chuyển qua, còn ion Cl- và OH- thì không.
❌(d) Theo thời gian, nồng độ ion Na+ tăng dần.
Trong quá trình điện phân dung dịch NaCl có màng ngăn, ion Na+ di chuyển từ anode sang cathode qua màng ngăn để cân bằng điện tích. Tuy nhiên, ion Na+ không tham gia trực tiếp vào phản ứng điện cực. Nước bị điện phân ở cathode tạo ra ion OH-, kết hợp với ion Na+ tạo thành NaOH. Do đó, nồng độ ion Na+ thực tế không giảm mà có thể tăng lên trong dung dịch ở vùng cathode do sự tích tụ NaOH.
❌(e) Điện phân không có màng ngăn thì ở anode thu được khí Cl2.
Anode thu được Cl2 tuy nhiên sau đó sẽ phản ứng luôn với NaOH sinh ra nước Javel. Đáp án: B
Câu 35 [560591]: Mùi hôi của nước chứa hydrogen sulfide H2S có thể được loại bỏ nhờ tác dụng của chlorine. Phản ứng xảy ra:
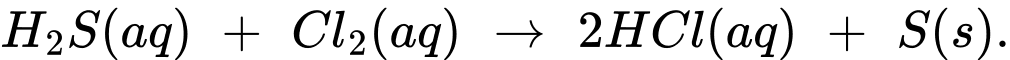
Nếu hàm lượng hydrogen sulfide trong nước bị ô nhiễm là 22 ppm theo khối lượng. Tính lượng Cl2 (theo đơn vị gam) cần thiết để loại bỏ tất cả lượng hydrogen sulfide ra khỏi 757,00 lít nước.
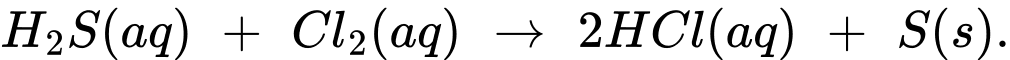
Nếu hàm lượng hydrogen sulfide trong nước bị ô nhiễm là 22 ppm theo khối lượng. Tính lượng Cl2 (theo đơn vị gam) cần thiết để loại bỏ tất cả lượng hydrogen sulfide ra khỏi 757,00 lít nước.
A, 34,78 g.
B, 69,55 g.
C, 25,48 g.
D, 50,34 g.
HƯỚNG DẪN GIẢI:
(Đơn vị ppm: một phần triệu)
- Thể tích của nước nhiễm H2S là 757 lít, vậy khối lượng của 757 lít nước này là 757kg
⟹ Khối lượng của H2S là: 757. (22/1 000 000) = 0,016654 (kg) = 16,654 (g)
- nH2S = 0,4898 (mol) = nCl2 cần dùng.
⟹ mCl2 = 0,4898 . 71 = 34,78 (g)
⟹ Chọn đáp án: A Đáp án: A
(Đơn vị ppm: một phần triệu)
- Thể tích của nước nhiễm H2S là 757 lít, vậy khối lượng của 757 lít nước này là 757kg
⟹ Khối lượng của H2S là: 757. (22/1 000 000) = 0,016654 (kg) = 16,654 (g)
- nH2S = 0,4898 (mol) = nCl2 cần dùng.
⟹ mCl2 = 0,4898 . 71 = 34,78 (g)
⟹ Chọn đáp án: A Đáp án: A