Dạng 1. TRẮC NGHIỆM KHÁCH QUAN: mỗi câu hỏi chỉ có một đáp án đúng.
2C + O2 ➝ 2CO
C + O2 ➝ CO2
⟹Ngoài O2 thì hỗn hợp khí thoát ra ở anode có thêm CO và CO2.
⟹ Chọn đáp án C Đáp án: C
⇒ Chọn đáp án A Đáp án: A
⭒ Al2O3 bền nhiệt hơn rất nhiều nên có thể tồn tại ở dạng nóng chảy
❌A sai: Nhiệt độ nóng chảy của AlCl3 thấp hơn Al2O3.
❌C sai: Điện phân AlCl3 nóng chảy vẫn tạo ra Cl2, nhưng đây không phải là lý do chính khiến người ta không sử dụng nó để điều chế Al.
❌D sai: Điện phân Al2O3 nóng chảy tạo ra Al có độ tinh khiết cao, nhưng đây không phải là yếu tố quyết định duy nhất. Tính chất thăng hoa của AlCl3 mới là lý do chính.
⟹ Chọn đáp án B Đáp án: B
⭐ Làm giảm nhiệt độ nóng chảy của hỗn hợp (từ 2072oC xuống khoảng 1000o)
⭐Làm tăng độ dẫn điện của hỗn hợp nóng chảy ➝ Làm tăng hiệu suất điện phân.
⭐ Tạo một lớp xỉ ngăn nhôm sinh ra không tiếp xúc với về mặt và không bị oxi hóa bởi O2 trong không khí. Đáp án: D
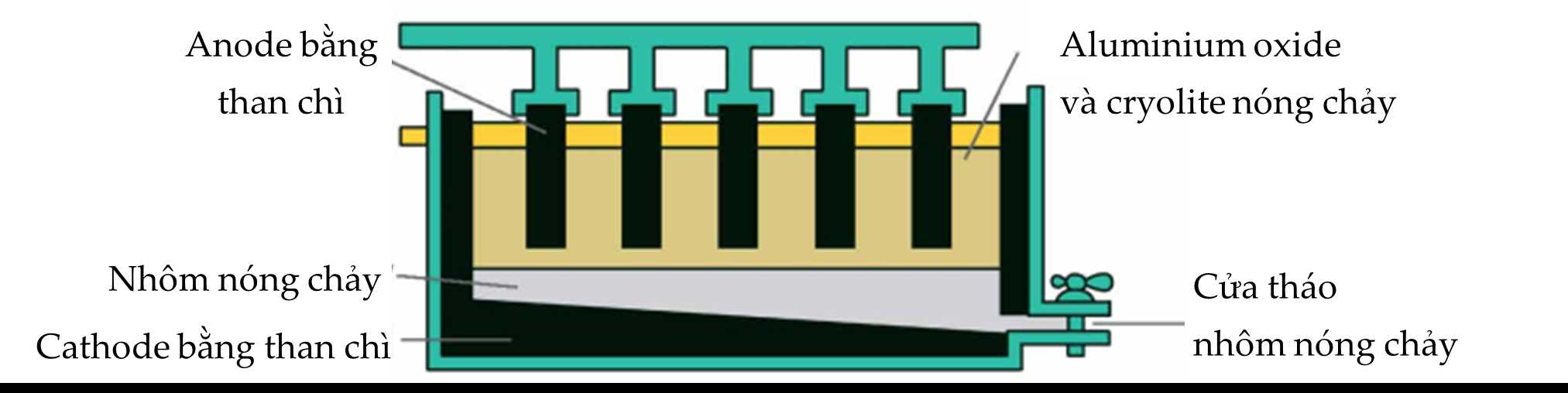
Cho các phát biểu sau:
(a) Cathode xảy ra quá trình khử Al3+ thành kim loại Al nóng chảy.
(b) Ở anode xuất hiện hỗn hợp khí O2, CO và CO2.
(c) Na3AlF6 được thêm vào sẽ nổi lên trên, bảo vệ nhôm nóng chảy khỏi bị oxi hóa bởi O2 không khí.
(d) Trong quá trình điện phân, cực âm luôn phải được thay mới do điện cực làm bằng than chì.Số phát biểu đúng là
✔️ (a) – Đúng. Cathode xảy ra quá trình khử Al3+ thành kim loại Al nóng chảy.
Điện phân nóng chảy:
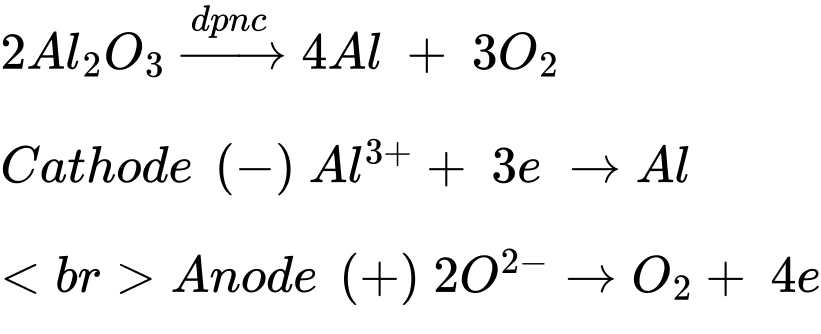
✔️ (b) – Đúng. Ở anode xuất hiện hỗn hợp khí O2, CO và CO2 nguyên do điện cực làm bằng than chì nên sẽ phản ứng với O2 sinh ra.
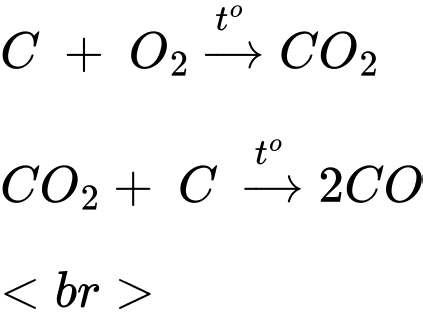
✔️ (c) – Đúng.
Cryolite (Na3AlF6) là nguyên liệu được dùng để sản xuất nhôm với mục đích:
- Làm giảm nhiệt độ nóng chảy của Al2O3.
- Tiết kiệm được năng lượng, tạo được chất lỏng có tính dẫn điện tốt hơn Al2O3.
- Tạo chất lỏng có tỉ khối nhỏ hơn nhôm, nổi lên bề mặt ngăn nhôm nóng chảy bị oxi hoá.
❌ (d) – Sai. Trong quá trình điện phân, cực dương (anode) luôn phải được thay mới do điện cực làm bằng than chì sẽ phản ứng với O2 sinh ra trong quá trình sản xuất nhôm.
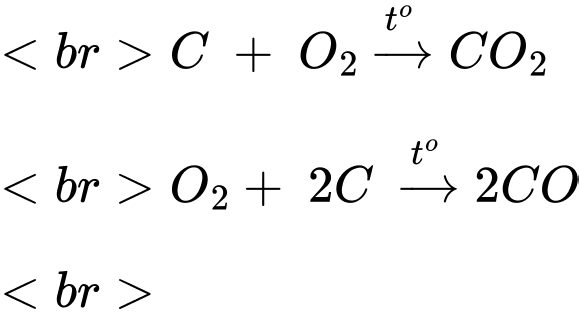
Các phát biểu đúng là (a) (b) (c)
⇒ Chọn đáp án C Đáp án: C
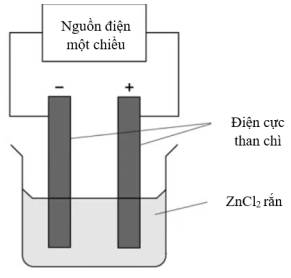
Lý do nào làm quá trình điện phân không xảy ra?
=> Chọn đáp án A Đáp án: A
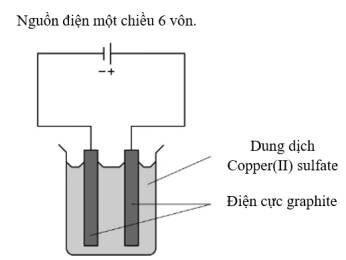
Những chất nào được tạo thành ở điện cực âm (cathode) và điện cực dương (anode)?
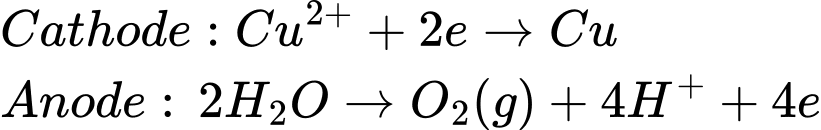
=> Chọn đáp án B Đáp án: B
✔ B. Anode (cực dương) gắn với kim loại. Cu ➝ Cu2+ + 2e => Hiện tượng dương cực tan.
✔ C. Hai điện cực được ngâm trong dung dịch CuSO4.
✖ D. Nồng độ Cu2+ không đổi nhờ 2 quá trình xảy ra đồng thời tại anode và cathode. Đáp án: D
(-) Cathode: làm bằng tấm sắt có độ tinh khiết thấp. Tại đây ion Fe2+ bị điện phân bám lên tấm sắt tạo lớp sắt tinh khiết.
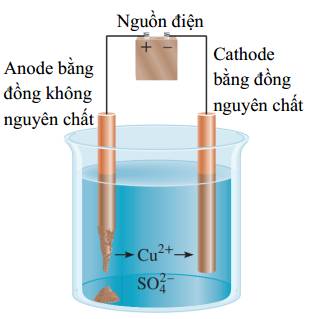
Giải thích cho hiện tượng này là
t= 3 (h) = 10 800 (s)
ne trao đổi của Ca = 2
Áp dụng định luật Faraday:
mCa = (MCa x I x t) / (F x ne trao đổi) = (40 x 1,12 x 10 800) / (96 500 x 2) = 2,51 (gam)
=> Đáp án A Đáp án: A
Tại anode (+): 2H2O ➝ O2 + 4H++ 4e => Số e trao đổi để tạo ra O2 là 4e.
Áp dụng định luật Faraday:
nO2 = (I x t) / (F x ne trao đổi) = (0,995 x t) / (96 500 x 4)
=> t ≈ 21595(s) ≈ 6 (h) Đáp án: A
I = 1,93A
Theo định luật Faraday, khối lượng Na thu được là:
mNa = (M x I x t) / (F x ne trao đổi)= (23 x 1,93 x 400) / (96 500 x 1) = 0,184 gam
Trong khi đó khối lượng Na thực tế thu được là 0,1472 gam
=> H% = (mthực tế / mlý thuyết) x 100%
= (0,1472/ 0,184) x 100% = 80%
=> Đáp án B Đáp án: B
Tính toán theo phương trình hóa học: nCl2= 1/71 => n NaCl = 2/71
=> mNaCl phản ứng= n x M = (2/71) x 58,5 = 1,648 (tấn)
=> H% = (mNaCl phản ứng / mNaCl cần dùng) x 100%
= (1,648 / 1,735) x 100% = 94,99%
=> Đáp án D Đáp án: D
I= 200 000 A
Al2O3 ⟶ 2Al + 1,5O2
Ta có: 3nAl = It / 96500
⟶ nAl = 0,06×106 mol
⟶ mAl = n×27 = 1,62×106 g = 1620kg
⟶ Chọn đáp án C Đáp án: C
Khí O2 sinh ra đốt cháy điện cực anode làm bằng than chì thành CO và CO2.
Xét 24,79 lít khí X (đkc) : O2 x (mol)
CO y (mol)
CO2 z (mol)
(1) x + y + z = 1
(2) 32x + 28y + 44z = mX= MX . nx = 32,4
Khi cho X vào nước vôi trong dư, chỉ có CO2 bị hấp thụ
=> nCO2 = nkết tủa = nCaCO3 = 4/100 = 0,04 (mol)
Thay z = 0,04 vào 2 phương trình trên, suy ra: x= 0,94; y= 0,02 (mol).
Trong X: nO= 2nO2 + 2nCO2 + nCO = 1,98 (mol)
=> nAl = 2/3 nO = 1,32 (mol)
mAl = 1,32 x 27 = 35,64 (gam) là khối lượng Al sinh ra trong 1,32 giây.
=> Trong 24 giờ (86400 giây): mAl= 35,64 x (86 400/1,32) = 2 332 800 gam= 2332,8 kg
nCuSO4= 0,3. 0,1 = 0,03 (mol)
Dung dịch mất màu xanh chứng tỏ đã điện phân hết Cu2+ trong dung dịch => nCu= 0,03 (mol)
Áp dụng định luật Faraday ta có:
nCu = (I x t) / (F x ne trao đổi )
<=> 0,03 = (1,93 x t) / (96500 x 2)
Tính được t = 3 000 giây = 50 phút => Đáp án D
Đáp án: DSau t phút, ở cathode(-) chưa có bọt khí => chỉ có Cu2+ bị khử
=> Áp dụng định luật Faraday ta có:
t = (mCu x F x n) / (MCu x I) = (1,92 x 96500 x 2) / (64 x 1,93) = 3 000 (s) = 50 phút
Đáp án: ADạng 2: TRẮC NGHIỆM ĐÚNG SAI – mỗi ý a), b), c), d) chọn đúng hoặc sai.
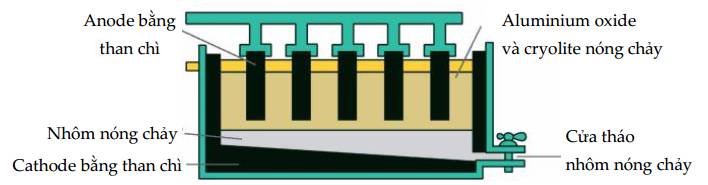
✔️ a. Đúng. Tại cathode (-) xảy ra quá trình khử: Al3+ + 3e ➝ Al.
✔️ b. Đúng. Do điện cực anode làm bằng than chì, khí O2 sinh ra đốt cháy dần carbon thành CO và CO2
✔️ c. Đúng. Na3AlF6 tạo một lớp xỉ ngăn nhôm sinh ra không tiếp xúc với bề mặt và không bị oxi hóa trong không khí.
❌ d. Sai. Sau một thời gian điện phân thì điện cực anode than chì bị mòn- lúc này mới phải thay thế bằng điện cực mới.
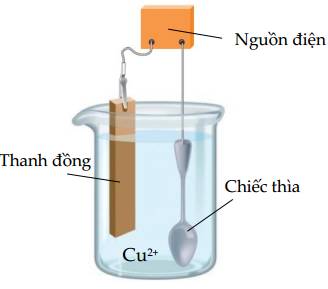
❌ a. Sai. Vật cần mạ (chiếc thìa) được gắn vào cực âm nguồn điện (cathode).
❌ b. Sai. Anode (cực dương) gắn với miếng kim loại đồng dùng để mạ.
✔️ c. Đúng. Điện cực Cu (anode) bị tan ra do Cu chuyển thành ion Cu2+ hay còn gọi là hiện tượng dương cực tan.
✔️ d. Đúng. Nồng độ ion Cu2+ trong dung dịch không đổi.
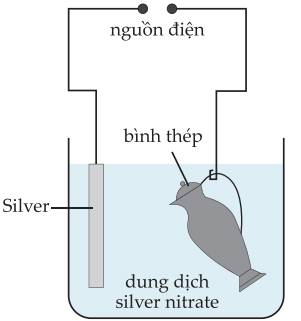
Mạ điện là một công nghệ điện phân. Quá trình tổng quát là:
– Trên anode xảy ra quá trình hòa tan kim loại:
M – ne ⟶ Mn+
– Trên cathode xảy ra quá trình cation phóng điện trở thành kim loại mạ:
Mn+ + ne → M
Phân tích các phát biểu:
✔️a) Đúng. Trong quá trình mạ điện, vật cần mạ (bình thép) được gắn với cực âm cathode, kim loại mạ (silver) gắn với cực dương anode của nguồn điện trong dung dịch điện phân.
❌b) Sai. Trên anode xảy ra quá trình hòa tan kim loại: Ag(s) – e ⟶ Ag+(aq)
✔️c) Đúng. Trên anode xảy ra quá trình hòa tan kim loại
❌d) Sai. Ion Ag+ di chuyển về cathode (cực âm), bị khử thành kim loại Ag và phủ lên bề mặt của bình thép.

✔️a. Đúng. Cực dương (anode) làm bằng tấm đồng có độ tinh khiết thấp. Tại đây xảy ra quá trình oxi hóa Cu tạo thành ion Cu2+ tan vào trong dung dịch.
✔️ b. Đúng. Cu bị oxi hóa tại anode nên khối lượng giảm dần: Cu ➝ Cu2+ + 2e
✔️ c. Đúng. Tại cực âm (cathode) ion Cu2+ bị điện phân, Cu bám lên điện cực tạo lớp đồng tinh khiết đến 99,95%.
✔️ d. Đúng. Các tạp chất không bị oxi hóa sẽ rơi xuống đáy bình tạo thành bùn dương cực.
Dạng 3: TRẮC NGHIỆM YÊU CẦU TRẢ LỜI NGẮN
MgCl2(l)
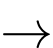 Mg(l) + Cl2(g)
Mg(l) + Cl2(g)Nếu sử dụng cường độ dòng điện 500 A thì cần bao nhiêu giờ để chuyển toàn bộ 1000 kg MgCl2 thành Mg kim loại?
nMg = nMgCl2 = 10526,3 (mol)
Quá trình khử: Mg2+ + 2e ➝ Mg => Số e trao đổi bằng 2e.
Áp dụng định luật Faraday:
Tính ra t= 4 063 151 giây= 1129 giờ
=> Điền đáp án: 1129
Đổi t = 8h = 28 800s ; I= 25 mA = 0,025A
→ Ion H+ trong HCl bị khử thành khí hydrogen, nên nồng độ H+ giảm → dung dịch bớt acid → đến khi hết H⁺ → dung dịch chuyển sang màu tím (do quỳ tím chuyển màu (đỏ) khi có H+, chuyển sang màu tím khi pH = 7)
→ Số mol H⁺ đã bị khử = số mol HCl ban đầu.
Số mol là:
n = It / F = 0,025 × 28800 : 96500 = 0,00746 mol
→ 2 mol H+ cần 2 mol e⁻ → tỉ lệ 1:1
→ Số mol H+ đã bị khử cũng là 0,00746 mol = nHCl
Nồng độ HCl = n : V = 0,00746 : 0,01 = 0,746 M
Điền đáp án: 0,75
Đổi: I = 20 kA = 20 000A
Vì tạo thành monobromo phenol nên tỉ lệ phản ứng là 1 Br2 : 1 phenol
➝ nBr2 thoát ra= nphenol =
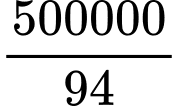 = 5319,15 (mol)
= 5319,15 (mol)Áp dụng định luật Faraday:
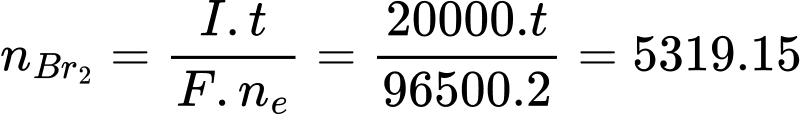
=> t= 51330 giây = 855,496 phút
=> Điền đáp án: 855
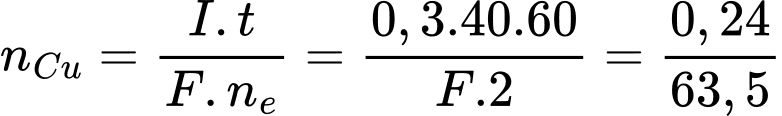
=> F= 95250 (C/mol) = 9,53. 101=> a= 9,53
=> Điền đáp án: 9525
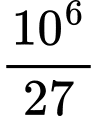
Phương trình phản ứng: 2Al2O3 ➝ 4Al + 3O2 => nO2 =
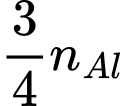 =
= 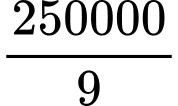
Điện cực than chì phản ứng với O2 theo 2 phương trình:
=> Số mol O2 phản ứng= 0,5x + x = 1,5x = 250000/9
=> x= 500000/27
=> nC phản ứng = 2.x= 1000000/27 => mC= 0,44 tấn
=> Điền đáp án: 0,44
Theo định luật Faraday, tại bình chứa dung dịch AgNO3:
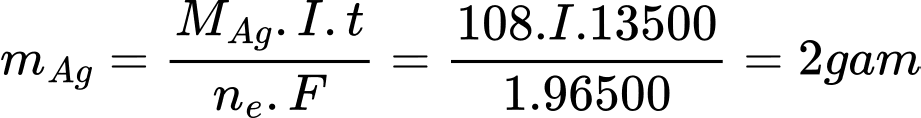
=> I = 0,132 A
Vì hai bình điện phân mắc nối tiếp nên cường độ dòng điện ở 2 bình bằng nhau (I= 0,132A)
=> Khối lượng đồng trong bình điện phân 2 là:
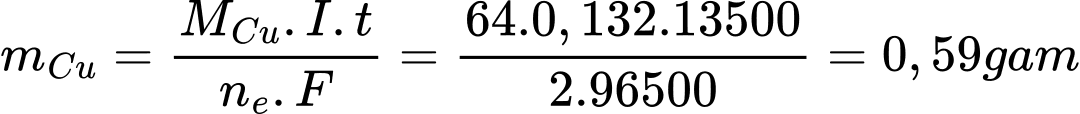
=> Điền đáp án: 0,59
(làm tròn đến hai chữ số thập phân)
Áp dụng định luật Faraday, khối lượng khí chlorine lý thuyết thu được là:
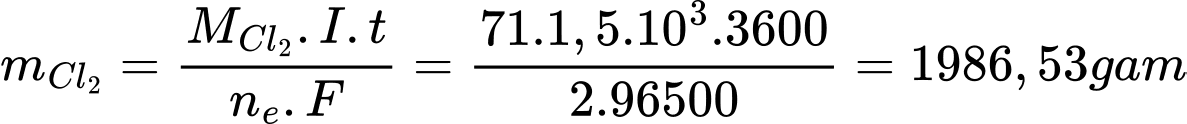
Biết Hpứ = 93% => Khí Cl2 thực tế thu được là 1986,53 . 93% = 1847,5 gam = 1,85 kg
=> Điền đáp án: 1,85
(làm tròn đến hai chữ số thập phân)
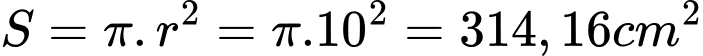
=> Thể tích lớp Ag cần mạ là V= 314,16. 0,01 . 10-1 = 0,314 cm-3
Khối lượng Ag: 10,5. 0,314 =
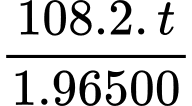
=> t= 1473 giây = 0,41 giờ
=> Điền đáp án: 0,41
Cr2O72−(aq) + 12e + 14H+(aq)
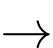 2Cr(s) + 7H2O(l)
2Cr(s) + 7H2O(l)Để mạ được lớp chromium dày 1,0×10−2 mm cho thanh cản ô tô có diện tích bề mặt 0,25 m2 trong một bình điện phân có cường độ dòng điện 25,0 A thì cần bao nhiêu thời gian (tính bằng giờ) biết khối lượng riêng của chromium là 7,19 g/cm3
(làm tròn đến hai chữ số thập phân)
V lớp mạ Cr = 10-3.2500 = 2,5 cm3
=> Khối lượng Cr:
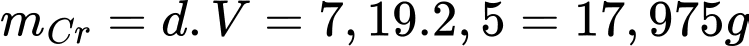
Từ phương trình phản ứng ta xác định được ne trao đổi = 6e
Áp dụng định luật Faraday:
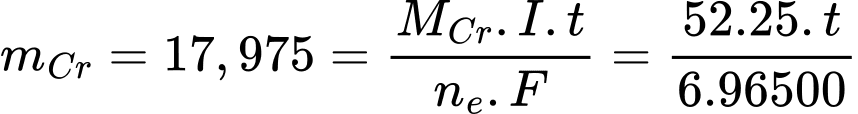
=> t= 8006 giây = 2,22 giờ
=> Điền đáp án: 2,22
(làm tròn đến số nguyên)
=> Diện tích toàn phần của miếng đồng = (5+ 1).2.0,1 + 2.5.1 = 11,2 cm2
Vì tất cả các mặt đều được mạ bằng bạc đến độ dày 1 micrometer (10-4 cm) => Thể tích lớp Ag: V= 11,2.10-4= 1,12.10-3 cm3
=> Khối lượng Ag cần mạ là m = D.V= 10,5. 1,12.10-3 =0,01176 gam
Áp dụng định luật Faraday:
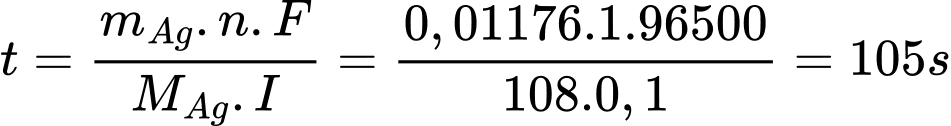
=> Điền đáp án: 105
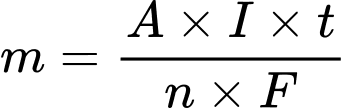
Trong đó m : Khối lượng chất thu được ở điện cực, tính bằng gam.
A : Khối lượng mol nguyên tử của chất thu được ở điện cực.
n: Số electron mà nguyên tử hoặc ion đã cho hoặc nhận.
1 : Cường độ dòng điện, tính bằng ampe (A).
t : Thời gian điện phân, tính bằng giây (s).
F : Hằng số Faraday (F = 96500 culông/mol).
(làm tròn đến hàng đơn vị)
Với hiệu suất điện phân là 90% thì khối lượng aluminium thực thế cần điện phân ra là 120.100/90 = 133.33 gam
Từ định luật Faraday, ta có:
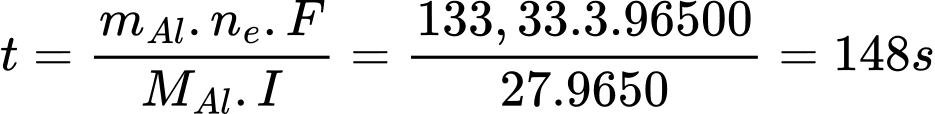
=> Điền đáp án: 148
Cho biết: MLi = 7 g/mol; hằng số Faraday là 96500 C/mol; I là cường độ dòng điện (A), t là thời gian (s), 1 năm = 365 ngày.
Nếu pin hoạt động ở cường độ dòng điện ổn định là 2,5.10-5 A thì một pin được chế tạo bởi 0,6 gam lithium có thể hoạt động tối đa trong thời gian bao nhiêu năm (Làm tròn đến hàng phần mười)?
Quá trình xảy ra trong pin:
Anode (-):
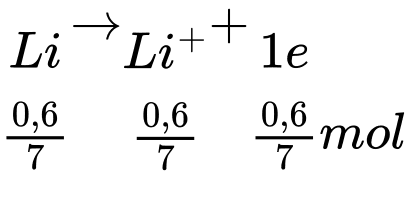
Số năm pin lithium có thể hoạt động tối đa là:
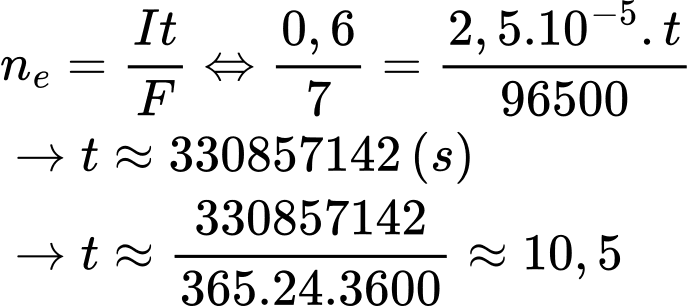
⇒ Điền đáp án: 10,5
Dạng 4: BÀI TẬP ĐỌC HIỂU – đọc thông tin và trả lời các câu hỏi sau đó
=> Chọn đáp án B Đáp án: B
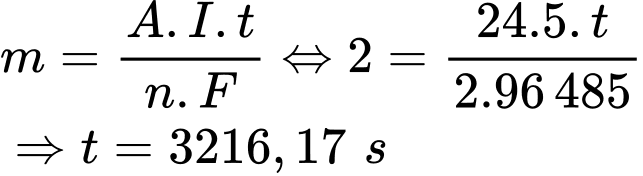 Đáp án: D
Đáp án: D Dạng 5: CÂU HỎI TỰ LUẬN
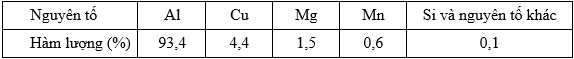
Cần điện phân nóng chảy m kg MgCl2 với hiệu suất điện phân 95% để thu được Mg phục vụ cho quá trình sản xuất 1000 kg duralumin trên. Tính giá trị của m.
mMg = 1000 × 1,5% = 15 kg
Ta có:
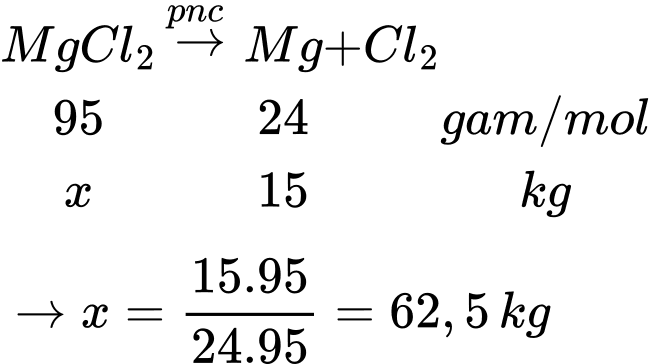
⟹ Điền đáp án 62,5
∎ Giai đoạn 1: Tinh chế quặng bauxite.
∎ Giai đoạn 2: Điện phân alumium oxide (Al2O3) nóng chảy (Al2O3 được trộn cùng với cryolite Na3AlF6).
Cấu tạo bể điện phân như hình sau:
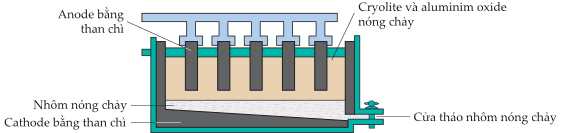
Hình. Sơ đồ mô phỏng bể điện phân sản xuất nhômMột mẫu quặng bauxite có chứa 60 % alumium oxide còn lại là các tạp chất khác. Giả thiết trong quá trình sản xuất chỉ có 85 % lượng alumium trong quặng chuyển hoá thành kim loại.
a) Viết phương trình phản ứng ở cathode và ở anode.
b) Biết rằng khối lượng Al trong 1 km dây cáp là 1080 kg. Để sản xuất 500 km một loại dây cáp hạ thế từ m tấn quặng bauxite. Xác định giá trị của m.
Anode (+) 2O2‒ → O2 + 4e
Cathode (‒ ) Al3+ + 3e → Al
Phản ứng điện phân
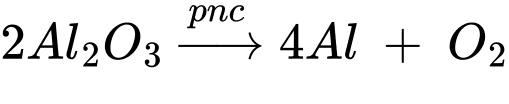
b) Khối lượng Al có trong 500 km dây cáp là mAl = 500 × 1080 = 540000 kg.
Ta có:
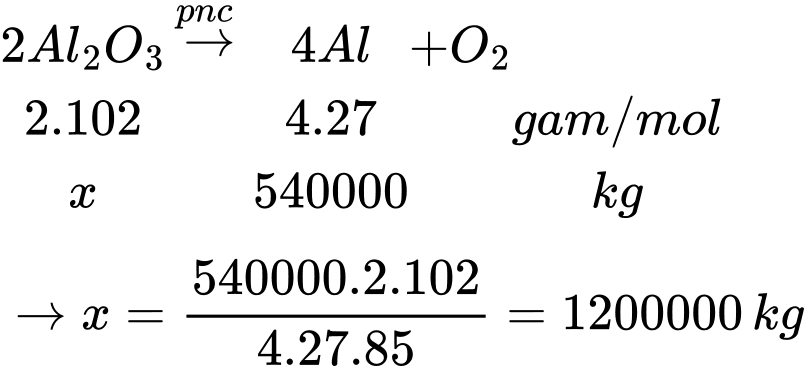
Khối lượng quặng bauxite là
mquặng = 1200000/60% = 2000000 kg = 2000 tấn
⟹ Điền đáp án 2000
a) Viết quá trình xảy ra trên các điện cực.
b) Tính giá trị của x.
Anode (+) Cu → Cu2+ + 2e
Cathode (‒ ) Cu2+ + 2e → Cu
b) Đổi 0,18 mm = 0,018 cm; 2h40m50s = 9650 s
Khối lượng Cu sinh ra trong quá trình điện phân là
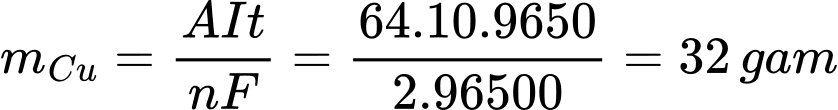
Diện tích bề mặt tấm sắt là
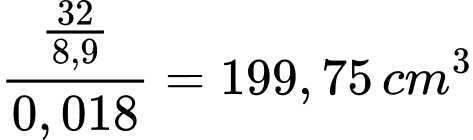
Giả sử, một thanh kim loại hình trụ có bán kính 20 mm và chiều cao 0,5 m cần được phủ lên bề mặt một lớp kim loại nickel có bề dày 200 μm bằng phương pháp điện phân. Bình điện phân được thiết kế cho thí nghiệm này chứa 5,4 kg NiSO4.7H2O và 7,2 L nước với cathode là kim loại cần mạ và anode là điện cực graphite. Cường độ dòng điện là 2,2 A.
a) Viết các phương trình phản ứng xảy ra trên các điện cực.
b) Xác định nồng độ % của NiSO4 tại thời điểm ban đầu và sau khi kết thúc điện phân.
c) Tính thời gian cần thiết để kết thúc quá trình điện phân, giả sử hiệu suất của quá trình điện phân là 90%. Cho biết khối lượng riêng của Ni là 8,9 g/cm3, của nước là 1,0 g/cm3.
a) Các phương trình xảy ra tại hai điện cực như sau:
+) Cathode (-): Ni2+ + 2e ⟶ Ni
+) Anode (+): 2H2O ⟶ 4H+ + O2 + 4e
b) 5,4kg = 5400 g NiSO4.7H2O
⟶ nNiSO4.7H2O = 5400 / (59 + 32 + 16.4 + 7.18) = 5400/281 (mol)
⟶ nNiSO4 = 5400/281 (mol)
⟶ mNiSO4 = (5400/281) . (59 + 32 + 16.4) = 2978,65 (g)
+) 7,2L = 7,2kg H2O = 7200g H2O
⟶ m dung dịch = 7200 + 5400 = 12600 (g)
⟶ C% NiSO4 trước phản ứng = 2978,65 / 12600 = 23,64%
+) 20mm = 2cm. 0,5m = 50cm. 200 μm = 0,02 cm.
- Thể tích thanh kim loại trước phản ứng là: V hình trụ = S đáy . h = πR2 .h = π. 22.50 = 200π (cm3)
- Bán kính mới của đáy là: 2 + 0,02 = 2,02 (cm)
- Chiều cao mới của thanh thép là: 50 + 0,02 . 2 = 50,04 (cm) (do chiều cao được tăng lên ở cả hai đầu của thanh nên ta nhân đôi)
⟶ Thể tích thanh kim loại sau phản ứng là: V = πR2 .h = π.2,022.50,04 = 641,46 (cm3)
⟶ Thể tích Nickel bám lên thanh kim loại là: 641,46 - 200π = 13,142 (cm3)
⟶ Khối lượng Nickel bám lên thanh là: m = d.V = 8,9 . 13,142 = 116,96 (g)
⟶ nNi phản ứng = 116,96 / 59 = 1,9824 (mol)
⟶ nNi phản ứng = nNiSO4 mất đi = 1,9824 mol. ⟶ mNiSO4 mất đi = 307,28 (g) ⟶ mNiSO4 còn lại = 2978,65 - 307,28 = 2671,37314 (gam)
- Khối lượng dung dịch sau khi phản ứng bằng khối lượng dung dịch ban đầu trừ đi lượng kim loại Ni thoát ra (bám lên thanh kim loại) và khối lượng khí O2 bay lên.
- nNi phản ứng = 1,9824 mol ⟶ ne trao đổi = 2. 1,9824 = 3,9648 mol ⟶ nO2 = 3,9648 / 4 = 0,9912 (mol) ⟶ mO2 = 0,9912 . 32 = 31,7184 (g)
⟶ mdung dịch sau = 12600 - 31,7184 - 116,96 = 12451,32 (g)
⟶ C% NiSO4 sau = 2671,37314 / 12451,32 = 21,45%
c) ne trao đổi = 3,9648 mol.
- Giả sử hiệu suất điện phân là 100%.
- Ta có I.t = n.F với:
+) I là cường độ dòng điện (Ampe)
+) t là thời gian điện phân (giây)
+) n là số mol electron trao đổi.
+) F là hằng số Faraday (96500)
→ t = n.F / I = 3,9648 . 96500 / 2,2 = 173911 (giây)
- Do hiệu suất thực tế là 90% nên thời gian cần là: 173911 / 90% = 193234 (giây) = 53,7 giờ.