Sử dụng thông tin ở bảng dưới đây để trả lời các câu 1 – 2:
Cho các cặp oxi hoá – khử và thể điện cực chuẩn tương ứng:
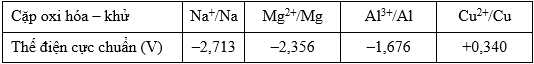
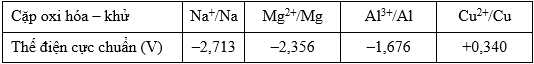
Câu 1 [829769]: Ion kim loại nào sau đây bị khử tại cathode khi điện phân (với điện graphite) dung dịch muối sulfate tương ứng?
A, Mg2+.
B, Na+.
C, Cu2+.
D, Al3+.
Các kim loại mạnh có thế khử chuẩn càng âm thì sẽ được điều chế bằng phương pháp điện phân nóng chảy như Na, Mg, Al.
Ion kim loại bị khử tại cathode khi điện phân (với điện cực graphite) dung dịch muối sulfate tương ứng là Cu.
Điện phân dung dịch CuSO4
Cathode (-) Cu2+ + 2e → Cu
Anode (+) 2H2O → 4H+ + O2 + 4e
Phương trình điện phân: 2CuSO4 + 2H2O → 2Cu + 2H2SO4 + O2.
⟹ Chọn đáp án C Đáp án: C
Ion kim loại bị khử tại cathode khi điện phân (với điện cực graphite) dung dịch muối sulfate tương ứng là Cu.
Điện phân dung dịch CuSO4
Cathode (-) Cu2+ + 2e → Cu
Anode (+) 2H2O → 4H+ + O2 + 4e
Phương trình điện phân: 2CuSO4 + 2H2O → 2Cu + 2H2SO4 + O2.
⟹ Chọn đáp án C Đáp án: C
Câu 2 [829772]: Thí nghiệm điện phân nóng chảy riêng biệt 3 ion kim loại Na+, Mg2+ và Al3+. Nếu ở thí nghiệm điện phân ion Na+ thu được 3,45 gam kim loại thì ở các thí nghiệm còn lại khối lượng kim loại lớn nhất có thể thu được tại một điện cực là bao nhiêu? Giả sử các thí nghiệm được thiết lập ở cùng điều kiện.
A, 3,45 gam.
B, 1,80 gam.
C, 1,35 gam.
D, 1,00 gam.
Nếu ở thí nghiệm điện phân ion Na+ thu được 3,45 gam kim loại
→ Số mol electron trao đổi đối với các thí nghiệm điện phân các kim loại là như nhau
Số mol của Na là nNa = 3,45 ÷ 23 = 0,15 mol
Cathode (-) Na+ + 1e → Na
Số mol electron trao đổi là ne = 0,15 mol
Xét điện phân Mg2+
Cathode (-) Mg2+ + 2e → Mg
Số mol của Mg là nMg = 0,075 mol
→ Khối lượng của kim loại Mg là mMg = 0,075.24 = 1,8 gam
Xét điện phân Al3+
Cathode (-) Al3+ + 3e → Al
Số mol của Al là nAl = 0,05 mol
→ Khối lượng của kim loại Al là mMg = 0,05 × 27 = 1,35 gam
→ Khối lượng kim loại lớn nhất có thể thu được tại một điện cực là 1,8 gam.
⟹ Chọn đáp án B Đáp án: B
→ Số mol electron trao đổi đối với các thí nghiệm điện phân các kim loại là như nhau
Số mol của Na là nNa = 3,45 ÷ 23 = 0,15 mol
Cathode (-) Na+ + 1e → Na
Số mol electron trao đổi là ne = 0,15 mol
Xét điện phân Mg2+
Cathode (-) Mg2+ + 2e → Mg
Số mol của Mg là nMg = 0,075 mol
→ Khối lượng của kim loại Mg là mMg = 0,075.24 = 1,8 gam
Xét điện phân Al3+
Cathode (-) Al3+ + 3e → Al
Số mol của Al là nAl = 0,05 mol
→ Khối lượng của kim loại Al là mMg = 0,05 × 27 = 1,35 gam
→ Khối lượng kim loại lớn nhất có thể thu được tại một điện cực là 1,8 gam.
⟹ Chọn đáp án B Đáp án: B
Sử dụng thông tin dưới đây để trả lời các câu 3 – 4:
Ở 25°C, nhúng một thanh Zn vào cốc đựng dung dịch ZnSO4 1 M (cốc 1), nhúng một thanh Cu vào cốc đựng dung dịch CuSO4 1 M (cốc 2). Nối thanh Zn và thanh Cu bằng dây dẫn, lắp một vôn kế để đo hiệu điện thế. Đóng kín mạch bằng cầu muối chứa dung dịch bão hoà KNO3.
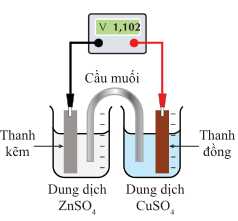

Câu 3 [829773]: Khi pin hoạt động, sự di chuyển ion nào sau đây là đúng?
A, Ion K+ di chuyển từ cầu muối về cốc 1.
B, Ion NO3– di chuyển từ cầu muối về cốc 1.
C, Ion Zn2+ di chuyển cốc 1 sang cốc 2.
D, Ion Cu2+ di chuyển cốc 2 sang cốc 1.
Quá trình xảy ra trong pin
Cathode (+) Cu2+ + 2e → Cu
Anode (-) Zn → Zn2+ + 2e
→ Phản ứng trong pin: Cu2+ + Zn → Cu + Zn2+
Khi pin hoạt động, sự di chuyển ion NO3- từ cầu muối di chuyển vào dung dịch ZnSO4; K+ di chuyển từ cầu muối vào dung dịch CuSO4.
⟹ Chọn đáp án B Đáp án: B
Cathode (+) Cu2+ + 2e → Cu
Anode (-) Zn → Zn2+ + 2e
→ Phản ứng trong pin: Cu2+ + Zn → Cu + Zn2+
Khi pin hoạt động, sự di chuyển ion NO3- từ cầu muối di chuyển vào dung dịch ZnSO4; K+ di chuyển từ cầu muối vào dung dịch CuSO4.
⟹ Chọn đáp án B Đáp án: B
Câu 4 [829774]: Dựa vào sức điện động của pin và biết 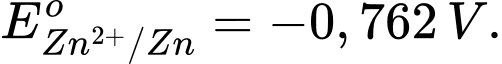 Thế điện cực chuẩn của Cu2+/Cu là bao nhiêu?
Thế điện cực chuẩn của Cu2+/Cu là bao nhiêu?
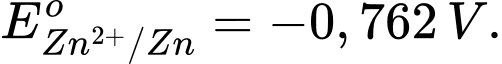 Thế điện cực chuẩn của Cu2+/Cu là bao nhiêu?
Thế điện cực chuẩn của Cu2+/Cu là bao nhiêu? A, 0,340 V.
B, 0,762 V.
C, 1,124 V.
D, 1,864 V.
Quá trình xảy ra trong pin
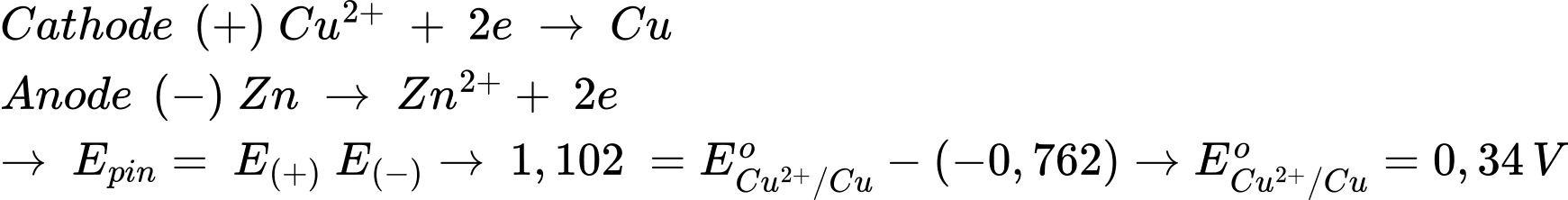
⟹ Chọn đáp án A Đáp án: A
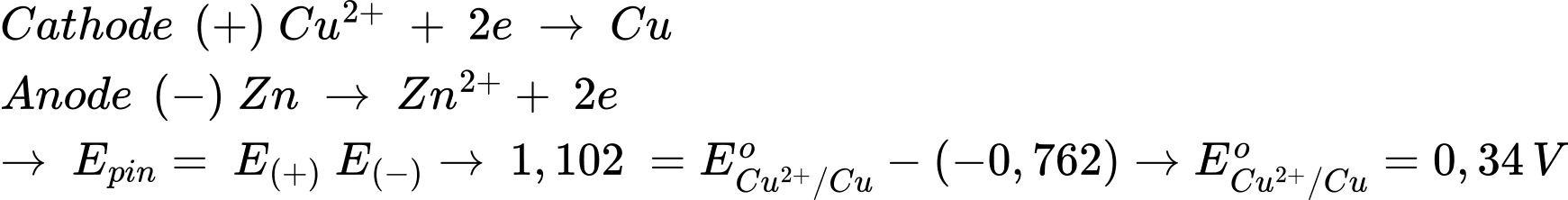
⟹ Chọn đáp án A Đáp án: A
Sử dụng thông tin dưới đây để trả lời các câu 5 – 6:
Một pin điện hoá Zn – H2 được thiết lập ở các điều kiện như hình vẽ sau:
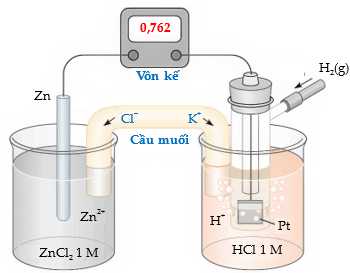

Câu 5 [829775]: Mô tả nào sau đây không chính xác những gì đang xảy ra trong điện cực Zn2+/Zn?
A, Điện cực mất khối lượng.
B, Nồng độ ion Zn2+ tăng.
C, Điện cực xảy ra quá trình nhường e.
D, Thế điện cực chuẩn mang giá trị dương.
Quá trình xảy ra trong pin
Cathode (+) 2H+ + 2e → H2
Anode (-) Zn → Zn2+ + 2e
→ Phản ứng trong pin: 2H+ + Zn → H2 + Zn2+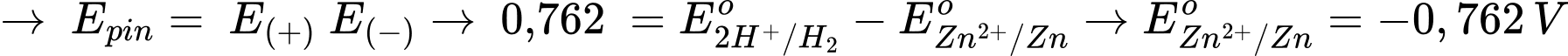
Phân tích các đáp án:
✔️A - Đúng. Điện cực mất khối lượng.
✔️B – Đúng. Nồng độ ion Zn2+ tăng.
✔️C – Đúng. Điện cực xảy ra quá trình nhường e.
❌D – Sai. Thế điện cực chuẩn mang giá trị âm.
⟹ Chọn đáp án D Đáp án: D
Cathode (+) 2H+ + 2e → H2
Anode (-) Zn → Zn2+ + 2e
→ Phản ứng trong pin: 2H+ + Zn → H2 + Zn2+
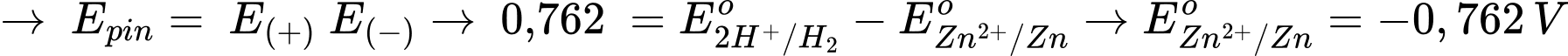
Phân tích các đáp án:
✔️A - Đúng. Điện cực mất khối lượng.
✔️B – Đúng. Nồng độ ion Zn2+ tăng.
✔️C – Đúng. Điện cực xảy ra quá trình nhường e.
❌D – Sai. Thế điện cực chuẩn mang giá trị âm.
⟹ Chọn đáp án D Đáp án: D
Câu 6 [829778]: Giả sử có x ion Zn2+ bị điện phân, để bảo toàn điện tích thì tổng số lượng ion âm và ion dương di chuyển từ cầu muối về cathode và anode là bao nhiêu?
A, 1x+1.
B, 2x+2.
C, 3x–1.
D, 4x.
Khi điện phân dung dịch chứa Zn2+
Quá trình xảy ra trong quá trình điện phân
Cathode (+) Zn2+ + 2e → Zn
Anode (-) H2O → 4H+ + 4e + O2
→ Khi dung dịch có x mol Zn2+ bị điện phân
→ Từ quá trình điện phân bị mất đi x mol Zn2+ và tạo ra 2x mol H+
→ Để bảo toàn điện tích thì tổng số lượng ion âm và ion dương di chuyển từ cầu muối về cathode và anode là 2x + 2x = 4x mol.
⟹ Chọn đáp án D Đáp án: D
Quá trình xảy ra trong quá trình điện phân
Cathode (+) Zn2+ + 2e → Zn
Anode (-) H2O → 4H+ + 4e + O2
→ Khi dung dịch có x mol Zn2+ bị điện phân
→ Từ quá trình điện phân bị mất đi x mol Zn2+ và tạo ra 2x mol H+
→ Để bảo toàn điện tích thì tổng số lượng ion âm và ion dương di chuyển từ cầu muối về cathode và anode là 2x + 2x = 4x mol.
⟹ Chọn đáp án D Đáp án: D
Sử dụng thông tin trong bảng dưới đây để trả lời các câu 7 – 8:
Cho biết sức điện động chuẩn của các pin sau:
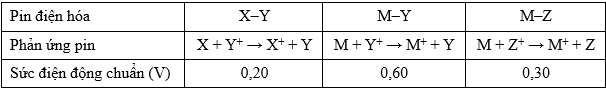
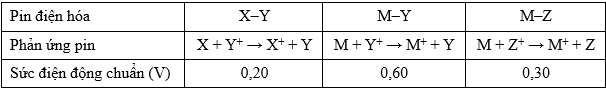
Câu 7 [829780]: Sự sắp xếp nào đúng với tính khử của các kim loại X, Y, Z, M?
A, M < Z < Y < X.
B, Y < X < Z < M.
C, X < Y < M < Z.
D, X < Y < Z < M.
Pin X-Y: X + Y+ → X+ + Y
→ X mạnh hơn Y
→ EX-Y = EY – EX = 0,2 V (1)
Pin M–Y: M + Y+ → M+ + Y
→ M mạnh hơn Y
→ EM-Y = EY – EM = 0,6 V (2)
Pin M-Z: M + Z+ → M+ + Z
→ M mạnh hơn Z
→ EM-Z = EZ – EM = 0,3 V (3)
Ta có:
EM-Y > EM-Z → nên tính khử của Y < Z.
EM-Y > EX-Y → nên tính khử của X < M.
→ Sự sắp xếp nào đúng với tính khử của các kim loại X, Y, Z, M là M > Z > X > Y.
⟹ Chọn đáp án B
Đáp án: B
→ X mạnh hơn Y
→ EX-Y = EY – EX = 0,2 V (1)
Pin M–Y: M + Y+ → M+ + Y
→ M mạnh hơn Y
→ EM-Y = EY – EM = 0,6 V (2)
Pin M-Z: M + Z+ → M+ + Z
→ M mạnh hơn Z
→ EM-Z = EZ – EM = 0,3 V (3)
Ta có:
EM-Y > EM-Z → nên tính khử của Y < Z.
EM-Y > EX-Y → nên tính khử của X < M.
→ Sự sắp xếp nào đúng với tính khử của các kim loại X, Y, Z, M là M > Z > X > Y.
⟹ Chọn đáp án B
Đáp án: B
Câu 8 [829782]: Sức điện động chuẩn của pin điện hóa M–X có giá trị là bao nhiêu V?
A, 0,2 V.
B, 0,4 V.
C, 0,8 V.
D, 1,0 V.
Khi tạo pin M-X từ pin (2) và pin (1)
→ EM-X = Epin(2) - Epin(1) = (EY - EM) – (EY - EX) = 0,6 – 0,2 = 0,4 V (5).
⟹ Chọn đáp án B Đáp án: B
Sử dụng thông tin trong bảng dưới đây để trả lời các câu 9 – 10:
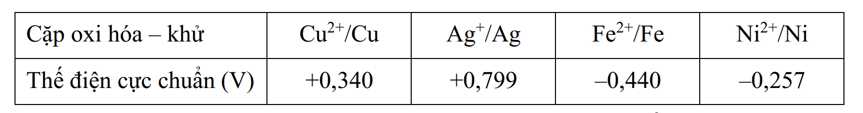
Cho bảng giá trị thế điện cực chuẩn của các cặp oxi hóa - khử như sau:
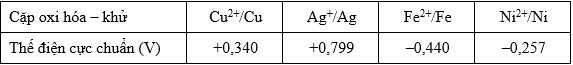

Câu 9 [829783]: Khả năng nhường electron của kim loại nào trong số các cặp oxi hóa – khử trên là lớn nhất?
A, Cu.
B, Ag.
C, Fe.
D, Ni.
Giá trị thế điện cực càng nhỏ → Tính khử của kim loại càng mạnh → Khả năng nhường electron càng tốt
→ Kim loại có khả năng nhường electron tốt nhất là Fe.
⟹ Chọn đáp án C
⟹ Chọn đáp án C
Câu 10 [829785]: Sức điện động chuẩn lớn nhất của pin Galvani thiết lập từ hai cặp oxi hóa - khử trong số các cặp trên là bao nhiêu?
A, 1,239V.
B, 1,560V.
C, 0,183V.
D, 0,780V.
Sức điện động chuẩn lớn nhất của pin Galvani thiết lập từ hai cặp oxi hóa - khử trong số các cặp trên là cặp Fe-Ag
Quá trình xảy ra trong pin
Anode (-) Fe → Fe2+ + 2e
Cathode (+) Ag+ + 1e → Ag
→ Epin = E(+) – E(-) = 0,799 – (-0,44) = 1,239 V.
⟹ Chọn đáp án A Đáp án: A
Quá trình xảy ra trong pin
Anode (-) Fe → Fe2+ + 2e
Cathode (+) Ag+ + 1e → Ag
→ Epin = E(+) – E(-) = 0,799 – (-0,44) = 1,239 V.
⟹ Chọn đáp án A Đáp án: A
Sử dụng thông tin dưới đây để trả lời các câu 11 – 12:
Pin Galvani được coi là nguồn điện hoá học đầu tiên mà con người phát minh ra. Pin Galvani Zn – Cu được biểu diễn ở hình sau:
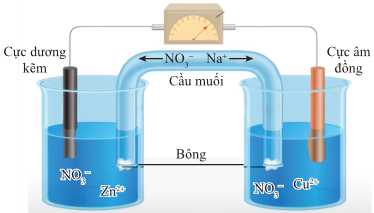
Biết thế điện cực chuẩn của cặp oxi hoá – khử Zn2+/Zn là –0,76 V và Cu2+/Cu là +0,340 V.

Biết thế điện cực chuẩn của cặp oxi hoá – khử Zn2+/Zn là –0,76 V và Cu2+/Cu là +0,340 V.
Câu 11 [829795]: Phát biểu nào sau đây không đúng?
A, Khi pin hoạt động, khối lượng thanh Zn giảm dần.
B, Electron chuyển từ thanh Zn qua dây dẫn đến thanh Cu.
C, Cầu muối đóng vai trò khép kín mạch và trung hoà điện tích của dung dịch ở hai điện cực.
D, Điện cực âm xảy ra quá trình khử Zn, điện cực dương xảy ra quá trình oxi hóa ion Cu2+.
Ta có: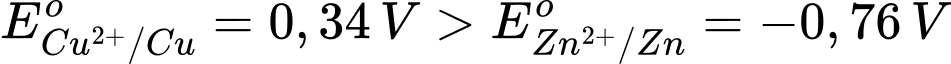
Quá trình xảy ra trong pin
Anode (-) Zn → Zn2+ + 2e
Cathode (+) Cu2+ + 2e → Cu
→ Epin = E(+) – E(-) = 0,34 – (-0,76) = 1,1 V
Phân tích các đáp án:
✔️A – Đúng. Khi pin hoạt động, khối lượng thanh Zn giảm dần.
✔️B – Đúng. Electron chuyển từ thanh Zn qua dây dẫn đến thanh Cu.
✔️C - Đúng. Cầu muối là bộ phận giúp khép kín mạch điện và duy trì sự trung hòa điện tích tại các điện cực trong quá trình điện phân hoặc hoạt động của pin. Nó cho phép các ion dương và âm di chuyển đến điện cực tương ứng để cân bằng sự thay đổi điện tích do phản ứng oxi hóa - khử gây ra.
❌D – Sai. Điện cực âm xảy ra quá trình oxi hóa Zn, điện cực dương xảy ra quá trình khử ion Cu2+.
⟹ Chọn đáp án D Đáp án: D
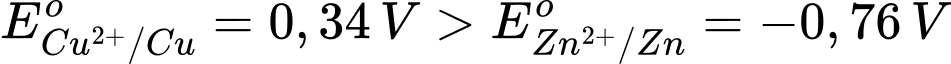
Quá trình xảy ra trong pin
Anode (-) Zn → Zn2+ + 2e
Cathode (+) Cu2+ + 2e → Cu
→ Epin = E(+) – E(-) = 0,34 – (-0,76) = 1,1 V
Phân tích các đáp án:
✔️A – Đúng. Khi pin hoạt động, khối lượng thanh Zn giảm dần.
✔️B – Đúng. Electron chuyển từ thanh Zn qua dây dẫn đến thanh Cu.
✔️C - Đúng. Cầu muối là bộ phận giúp khép kín mạch điện và duy trì sự trung hòa điện tích tại các điện cực trong quá trình điện phân hoặc hoạt động của pin. Nó cho phép các ion dương và âm di chuyển đến điện cực tương ứng để cân bằng sự thay đổi điện tích do phản ứng oxi hóa - khử gây ra.
❌D – Sai. Điện cực âm xảy ra quá trình oxi hóa Zn, điện cực dương xảy ra quá trình khử ion Cu2+.
⟹ Chọn đáp án D Đáp án: D
Câu 12 [829797]: Nếu thay điện cực của cặp oxi hóa khử Zn2+/Zn bằng Fe2+/Fe, cả hai trường hợp đều được thiết lập ở điều kiện chuẩn thì sức điện động chuẩn của pin chêch lệch so với trước khi thay là bao nhiêu? Biết thế điện cực chuẩn của cặp oxi hoá – khử Fe2+/Fe là –0,44 V.
A, 0,10 V.
B, 0,32 V.
C, 0,78 V.
D, 1,20 V.
Ta có:
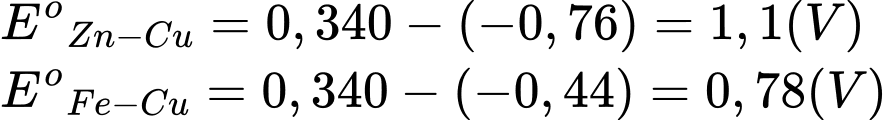
Suất điện động của pin chệnh lệch trước khi thay là: Epin = 1,1 - 0,78 = 0,32V
Chọn đáp án B Đáp án: B
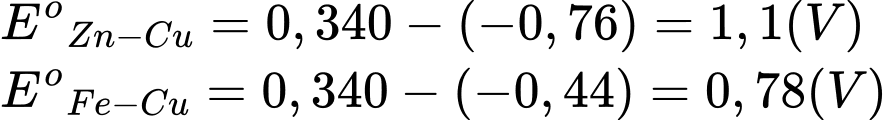
Suất điện động của pin chệnh lệch trước khi thay là: Epin = 1,1 - 0,78 = 0,32V
Chọn đáp án B Đáp án: B
Sử dụng thông tin trong bảng dưới đây để trả lời các câu 13 – 14:
Cho bảng giá trị thế điện cực chuẩn của các cặp oxi hóa - khử như sau:
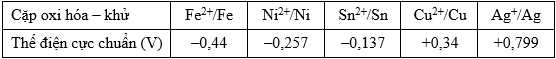
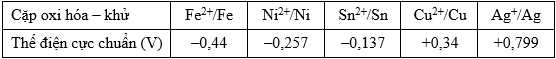
Câu 13 [829790]: Kim loại Cu có thể khử được bao nhiêu ion kim loại thuộc các cặp oxi hóa – khử trên?
A, 1.
B, 2.
C, 3.
D, 4.
Thế điện cực chuẩn của cặp oxi hóa – khử càng lớn thì tính khử của dạng khử càng yếu, tính oxi hóa của dạng oxi hóa càng mạnh và ngược lại.
Nếu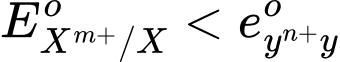 ="" thì="" tính="" khử:="" x=""> Y; tính oxi hóa: Xm+ < Yn+.
="" thì="" tính="" khử:="" x=""> Y; tính oxi hóa: Xm+ < Yn+.
→ Kim loại Cu có thể khử được Ag.
⟹ Chọn đáp án A
Đáp án: A
Nếu
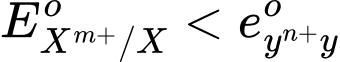 ="" thì="" tính="" khử:="" x=""> Y; tính oxi hóa: Xm+ < Yn+.
="" thì="" tính="" khử:="" x=""> Y; tính oxi hóa: Xm+ < Yn+.→ Kim loại Cu có thể khử được Ag.
⟹ Chọn đáp án A
Đáp án: A
Câu 14 [829794]: Sức điện động chuẩn của pin điện hoá gồm hai điện cực M2+/M và Ag+/Ag bằng 0,936 V. Kim loại M là kim loại nào sau đây?
A, Cu.
B, Fe.
C, Ni.
D, Sn.
Từ bảng số liệu ta nhận thấy Ag+/Ag có thế điện cực chuẩn lớn nhất
Quá trình xảy ra trong pin
Anode (-) M → M2+ + 2e
Cathode (+) Ag+ + 1e → Ag
→ Epin = E(+) – E(-) = 0,799 – E(-) = 0,936 V
→ E(-) = –0,137 V
→ Kim loại M tương ứng là Sn.
⟹ Chọn đáp án D Đáp án: D
Quá trình xảy ra trong pin
Anode (-) M → M2+ + 2e
Cathode (+) Ag+ + 1e → Ag
→ Epin = E(+) – E(-) = 0,799 – E(-) = 0,936 V
→ E(-) = –0,137 V
→ Kim loại M tương ứng là Sn.
⟹ Chọn đáp án D Đáp án: D
Sử dụng đoạn thông tin dưới đây để trả lời câu 15 – 16:
Cho bảng thế điện cực chuẩn của các cặp oxi hóa – khử như sau:

Thiết lập một pin Galvani nối với bóng đèn hình vẽ dưới đây:
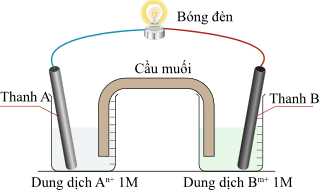
Trong đó 2 điện cực A và B là hai trong số các cặp oxi hóa – khử bên trên. Giả sử một bóng đèn cần tối thiểu 1,5 V để hoạt động.

Thiết lập một pin Galvani nối với bóng đèn hình vẽ dưới đây:

Trong đó 2 điện cực A và B là hai trong số các cặp oxi hóa – khử bên trên. Giả sử một bóng đèn cần tối thiểu 1,5 V để hoạt động.
Câu 15 [702618]: Nếu dung dịch A và B được thiết lập từ các cặp oxi hoá khử là Fe2+/Fe và Ag+/Ag ở điều kiện chuẩn thì quá trình xảy ra ở cực âm là
A, Fe(s)  Fe2+(aq) +2e.
Fe2+(aq) +2e.
 Fe2+(aq) +2e.
Fe2+(aq) +2e.B, Fe2+(aq) + 2e  Fe(s).
Fe(s).
 Fe(s).
Fe(s).C, Ag+(aq) + 1e  Ag(s).
Ag(s).
 Ag(s).
Ag(s).D, Ag(s)  Ag+(aq) + 1e.
Ag+(aq) + 1e.
 Ag+(aq) + 1e.
Ag+(aq) + 1e.
Pin Galvani gồm hai điện cực được nối với nhau bằng cầu muối. Khi pin hoạt động, ở điện cực âm (anode) xảy ra quá trình oxi hoá kim loại và ở điện cực dương (cathode) xảy ra quá trình khử cation.
Cực dương là kim loại có thế điện cực lớn hơn, cực âm là kim loại có thế điện cực nhỏ hơn.
Vì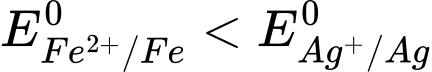 nên cực âm là Fe.
nên cực âm là Fe.
Cực dương là kim loại có thế điện cực lớn hơn, cực âm là kim loại có thế điện cực nhỏ hơn.
Vì
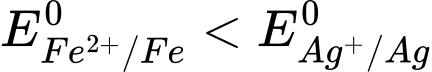 nên cực âm là Fe.
nên cực âm là Fe.Khi pin hoạt động, ở điện cực âm (anode) xảy ra quá trình oxi hoá kim loại: Fe(s) → Fe2+(aq)+ 2e.
⇒ Chọn đáp án A
⇒ Chọn đáp án A
Câu 16 [702619]: Có bao nhiêu cách tạo ra pin Galvani được thiết lập từ hai cặp oxi hóa – khử trong số các cặp trong bảng trên để bóng đèn hoạt động?
A, 1.
B, 2.
C, 3.
D, 4.
Để bóng đèn hoạt động thì cần tối thiểu 1,5 V. Ta xét bảng hiệu điện thế của các cặp oxi hoá - khử như sau:
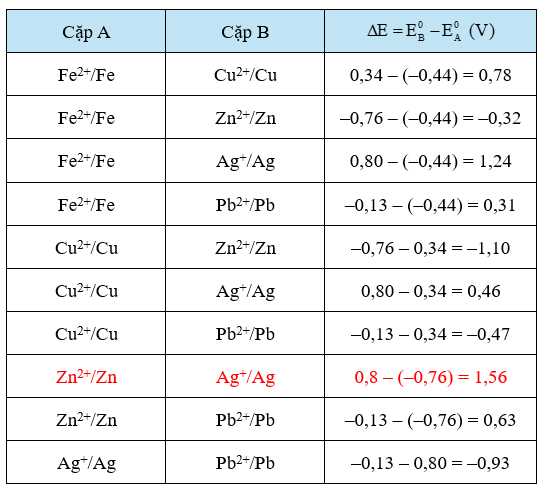
Vậy chỉ có 1 cặp oxi hóa – khử có hiệu điện thế lớn hơn 1,5: Ag được tạo ra ở cực dương, Zn2+ được tạo ra ở cực âm.
⇒ Chọn đáp án A Đáp án: A

Vậy chỉ có 1 cặp oxi hóa – khử có hiệu điện thế lớn hơn 1,5: Ag được tạo ra ở cực dương, Zn2+ được tạo ra ở cực âm.
⇒ Chọn đáp án A Đáp án: A
Câu 17 [702815]: Trong các ion kim loại có trong bảng trên, ở điều kiện chuẩn ion nào có tính oxi hóa mạnh nhất?
A, Ag+.
B, Cu2+.
C, Fe2+.
D, Ni2+.
Kim loại có thế điện cực chuẩn càng âm thì càng có tính khử mạnh, càng dương thì tính tính oxi hoá càng mạnh.
Thấy giá trị thế điện cực chuẩn của cặp oxi hoá - khử Ag+/Ag là dương nhất nên Ag+ có tính oxi hoá mạnh nhất.
⇒ Chọn đáp án A Đáp án: A
Thấy giá trị thế điện cực chuẩn của cặp oxi hoá - khử Ag+/Ag là dương nhất nên Ag+ có tính oxi hoá mạnh nhất.
⇒ Chọn đáp án A Đáp án: A
Câu 18 [702816]: Biết sức điện động chuẩn của pin điện hoá gồm hai điện cực M2+/M và Ag+/Ag bằng 1,056 V. Kim loại nào sau đây phù hợp với M?
A, Fe.
B, Sn.
C, Ni.
D, Cu.
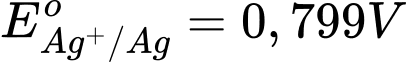 giá trị thế điện cực dương nhất → Ag+/Ag là cực dương, cathode
giá trị thế điện cực dương nhất → Ag+/Ag là cực dương, cathodeSức điện động của pin trên.
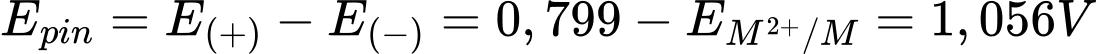
→
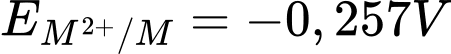 → Cặp oxi hóa khử phù hợp Ni2+/Ni
→ Cặp oxi hóa khử phù hợp Ni2+/Ni → Kim loại phù hợp là Ni
⇒ Chọn đáp án C Đáp án: C
Sử dụng đoạn thông tin dưới đây để trả lời câu 19 – 20:
MgCl2 nóng chảy có thể bị phân hủy thành các nguyên tố nếu như đặt một điện áp đủ lớn vào hai điện cực trơ. Sản phẩm của phản ứng là Mg nóng chảy (ở cực âm) và khí Cl2 (ở cực dương). Cho bảng thế điện cực chuẩn của các bán phản ứng như sau:


Câu 19 [703013]: Giả sử các chất ở điều kiện chuẩn. Hiệu điện thế tối thiểu cần đặt vào để phản ứng điện phân xảy ra là
A, 3,73 V.
B, 1,01 V.
C, 2,16 V.
D, 3,43 V.
MgCl2 –(đpnc)→ Mg + Cl2
Cathode (–): Mg2+ + 2e → Mg
Anode (+): 2Cl– → Cl2 + 2e
→ E = –2,37 – 1,26 = –3,73 V
→ Hiệu điện thế tối thiểu cần đặt vào để phản ứng điện phân là 3,73 V
⇒ Chọn đáp án A Đáp án: A
Cathode (–): Mg2+ + 2e → Mg
Anode (+): 2Cl– → Cl2 + 2e
→ E = –2,37 – 1,26 = –3,73 V
→ Hiệu điện thế tối thiểu cần đặt vào để phản ứng điện phân là 3,73 V
⇒ Chọn đáp án A Đáp án: A
Câu 20 [703014]: Nếu dòng điện trong bình được giữ ở mức không đổi 5 A, giả sử hằng số Faraday bằng 96485 C thì mất bao nhiêu giây để tạo ra 2,00 gam Mg(l) ở cực âm?
A, 2160.
B, 4190.
C, 3180.
D, 3216.
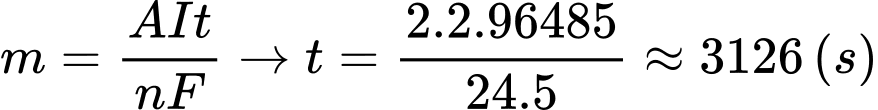
⇒ Chọn đáp án D Đáp án: D
[TK 2025]: Sử dụng thông tin ở bảng dưới đây để trả lời các câu 21 - 22:
Cho bảng giá trị thế điện cực chuẩn của các cặp oxi hóa - khử như sau:
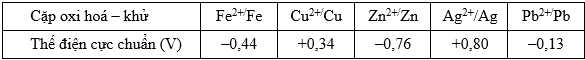

Câu 21 [680869]: Trong số các ion kim loại gồm Fe2+, Cu2+ và Zn2+, ở điều kiện chuẩn ion nào có tính oxi hóa yếu hơn Ag2+, nhưng mạnh hơn Pb2+?
A,
Fe2+, Cu2+, Zn2+.
B, Fe2+, Cu2+.
C, Zn2+.
D, Cu2+.
Ta có
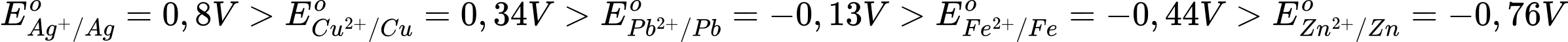
→ Thấy rằng chỉ có Cu2+/Cu có thế điện cực chuẩn nhỏ hơn Ag+/Ag và lớn hơn Pb2+/Pb
→ Cu2+ có tính oxi hóa mạnh hơn Pb2+/Pb và yếu hơn Ag+/Ag.
⇒ Chọn đáp án D
Đáp án: D
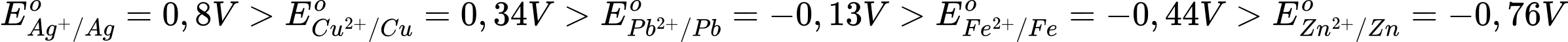
→ Thấy rằng chỉ có Cu2+/Cu có thế điện cực chuẩn nhỏ hơn Ag+/Ag và lớn hơn Pb2+/Pb
→ Cu2+ có tính oxi hóa mạnh hơn Pb2+/Pb và yếu hơn Ag+/Ag.
⇒ Chọn đáp án D
Đáp án: D
Câu 22 [680870]: Sức điện động chuẩn lớn nhất của pin Galvani thiết lập từ hai cặp oxi hóa - khử trong số các cặp trên là
A, 1,24 V.
B, 1,56 V.
C, 1,60 V.
D, 0,93 V.
Sức điện động lớn nhất của pin galvani thiết lặp từ cặp Zn2+/Zn và Ag+/Ag
Với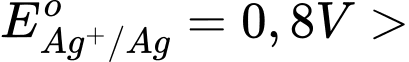
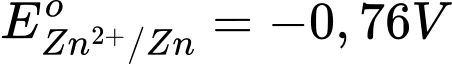 → Zn đóng vai trò là anode (-) và Ag đóng vai trò là cathode (+)
→ Zn đóng vai trò là anode (-) và Ag đóng vai trò là cathode (+)
Zn + 2Ag+ → Zn2+ + 2Ag
Phản ứng trong pin:
Cathode (+): Ag+ +1e → Ag
Anode (-): Zn → Zn2+ + 2e
Sức điện của pin là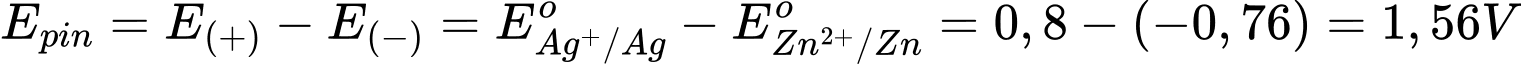
⇒ Chọn đáp án B Đáp án: B
Với
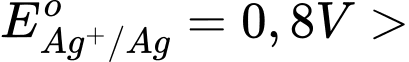
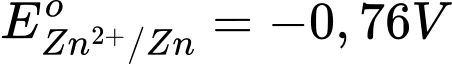 → Zn đóng vai trò là anode (-) và Ag đóng vai trò là cathode (+)
→ Zn đóng vai trò là anode (-) và Ag đóng vai trò là cathode (+)Zn + 2Ag+ → Zn2+ + 2Ag
Phản ứng trong pin:
Cathode (+): Ag+ +1e → Ag
Anode (-): Zn → Zn2+ + 2e
Sức điện của pin là
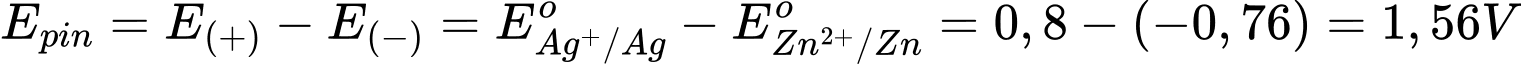
⇒ Chọn đáp án B Đáp án: B
Sử dụng thông tin ở bảng dưới đây để trả lời câu 23 – 24:
Cho giá trị thế điện cực chuẩn của một số cặp oxi hóa – khử trong bảng sau:
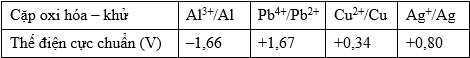

Câu 23 [703828]: Phản ứng hóa học nào sau đây không xảy ra?
A, 2Al(s) + 3Cu2+(aq)  2Al3+(aq) + 3Cu(s).
2Al3+(aq) + 3Cu(s).
 2Al3+(aq) + 3Cu(s).
2Al3+(aq) + 3Cu(s).B, Cu(s) + 2Ag+(aq)  Cu2+(aq) + 2Ag(s).
Cu2+(aq) + 2Ag(s).
 Cu2+(aq) + 2Ag(s).
Cu2+(aq) + 2Ag(s).C, 2Ag+(aq) + Pb2+(aq)  Pb4+(aq) + 2Ag(s).
Pb4+(aq) + 2Ag(s).
 Pb4+(aq) + 2Ag(s).
Pb4+(aq) + 2Ag(s).D, Cu(s) + Pb4+(aq)  Cu2+(aq) + Pb2+(aq).
Cu2+(aq) + Pb2+(aq).
 Cu2+(aq) + Pb2+(aq).
Cu2+(aq) + Pb2+(aq).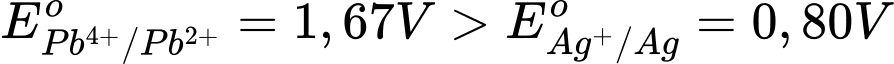
→ Theo quy tắc 𝞪, dạng oxi hóa mạnh sẽ phản ứng với dạng khử mạnh.
2Ag(s) + Pb4+(aq) ⟶ Pb2+(aq) + 2Ag+(aq).
⟹ Chọn đáp án C Đáp án: C
Câu 24 [703829]: Sức điện động chuẩn lớn nhất của pin Galvani thiết lập từ hai cặp oxi hóa – khử trong số các cặp trên là
A, 1,67 V.
B, 4,05 V.
C, 2,46 V.
D, 3,33 V.
Cặp oxi hóa - khử tạo pin galvani có sức điện động lớn nhất là Al3+/Al và Pb4+/Pb2+.
Phản ứng trong pin galvani:
2Al(s) + 3Pb4+(aq) ⟶ 2Al3+(aq) + 3Pb2+(aq)
Cathode (-): Pb4+(aq) + 2e ⟶ Pb2+(aq)
Anode (+): Al(s) ⟶ Al3+ + 3e
→ Epin = E(+) – E(-) = 1,67 – (–1,66) = 3,33 V
⇒ Chọn đáp án D Đáp án: D
Phản ứng trong pin galvani:
2Al(s) + 3Pb4+(aq) ⟶ 2Al3+(aq) + 3Pb2+(aq)
Cathode (-): Pb4+(aq) + 2e ⟶ Pb2+(aq)
Anode (+): Al(s) ⟶ Al3+ + 3e
→ Epin = E(+) – E(-) = 1,67 – (–1,66) = 3,33 V
⇒ Chọn đáp án D Đáp án: D
Sử dụng đoạn thông tin dưới đây để trả lời câu 25 – 26:
Cho thế điện cực chuẩn của các cặp oxi hóa – khử như sau:
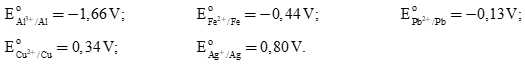
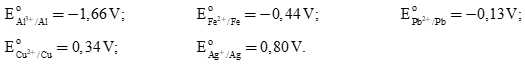
Câu 25 [704182]: Trong số các kim loại: Fe, Pb, Ag và Al, kim loại nào hoạt động mạnh hơn kim loại Cu?
A, Fe, Pb.
B, Al, Ag.
C, Fe, Pb, Al.
D, Fe.
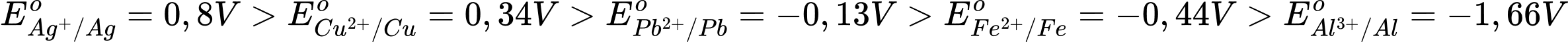
Kim loại có độ hoạt động mạnh hơn Cu là những kim loại có thế điện cực chuẩn nhỏ hơn Cu
→ Pb, Fe, Al hoạt động mạnh hơn Cu.
⇒ Chọn đáp án C Đáp án: C
Câu 26 [704183]: Sức điện động chuẩn nhỏ nhất của pin Galvani được thiết lập từ hai cặp oxi hóa khử trong số các cặp trên có giá trị là
A, 0,46 V.
B, 0,21 V.
C, 0,31 V.
D, 0,47 V.
Sức điện động nhỏ nhất của pin galvani thiết lặp từ cặp Fe2+/Fe và Pb2+/Pb
Với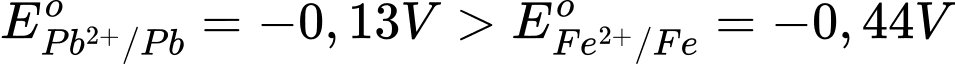 → Fe đóng vai trò là anode (-) và Pb đóng vai trò là cathode (+)
→ Fe đóng vai trò là anode (-) và Pb đóng vai trò là cathode (+)
Fe + Pb+ Fe2+ + Pb
Fe2+ + Pb
Phản ứng trong pin:
Cathode (+) Pb2+ + 2e Pb
Pb
Anode (-) Fe Fe2+ + 2e
Fe2+ + 2e
Sức điện của pin là: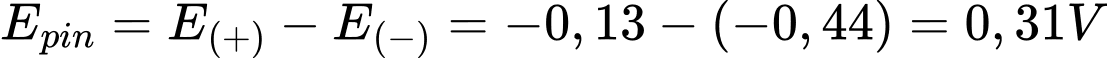
⇒ Chọn đáp án C Đáp án: C
Với
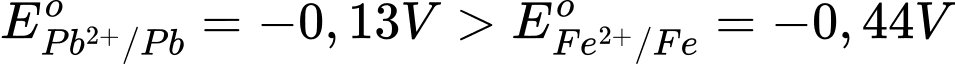 → Fe đóng vai trò là anode (-) và Pb đóng vai trò là cathode (+)
→ Fe đóng vai trò là anode (-) và Pb đóng vai trò là cathode (+)Fe + Pb+
 Fe2+ + Pb
Fe2+ + PbPhản ứng trong pin:
Cathode (+) Pb2+ + 2e
 Pb
Pb Anode (-) Fe
 Fe2+ + 2e
Fe2+ + 2eSức điện của pin là:
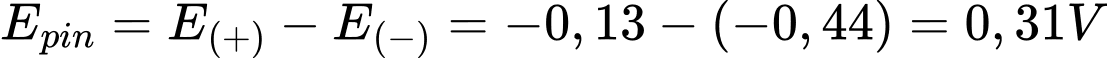
⇒ Chọn đáp án C Đáp án: C
Sử dụng thông tin ở bảng dưới đây để trả lời các câu 27 – 28:
Cho bảng giá trị thế điện cực chuẩn 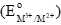 của các cặp oxi hóa – khử như sau:
của các cặp oxi hóa – khử như sau:
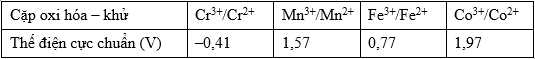
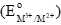 của các cặp oxi hóa – khử như sau:
của các cặp oxi hóa – khử như sau:
Câu 27 [705693]: Kim loại nào thay đổi trạng thái oxi hoá từ +2 lên +3 dễ nhất?
A, Cr.
B, Mn.
C, Fe.
D, Co.
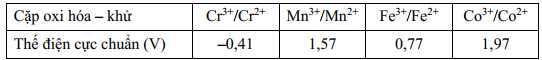
Nguyên tắc: Thế điện cực chuẩn càng lớn → chất càng có xu hướng nhận e dễ hơn (bị khử), còn quá trình oxi hóa sẽ khó xảy ra hơn.Ngược lại, thế điện cực chuẩn càng nhỏ → chất càng dễ bị oxi hóa (mất e) từ +2 lên +3.
Từ bảng giá trị thế điện cực chuẩn ta thấy được cặp Cr3+/Cr2+ có giá trị thế điện cực nhỏ nhất nên có tính khử mạnh nhất nên sẽ dễ dàng mất electron thay đổi trạng thái số oxi hóa từ +2 lên +3.
⇒ Chọn đáp án A Đáp án: A
Câu 28 [705694]: Giá trị thế điện cực chuẩn của các cặp oxi hóa – khử có được là do điện cực của mỗi cặp oxi hóa – khử được ghép với điện cực hydrogen chuẩn và quy ước thế điện cực chuẩn của 2H+/H2 bằng 0,00 V. Nếu quy ước thế điện cực chuẩn của 2H+/H2 bằng 0,50 V thì thế điện cực chuẩn lớn nhất trong các cặp oxi hóa – khử trên là
A, 2,07 V.
B, 2,47 V.
C, 3,05 V.
D, 4,84 V.
Khi pin được thiết lập, sức điện động của pin luôn dương.
Nếu quy ước thế điện cực chuẩn của 2H+/H2 bằng 0,50 V thì giá trị thế điện cực của các cặp oxi – khử sẽ tăng đi 0,50 V
Ta có bảng giá trị thế điện cực mới:
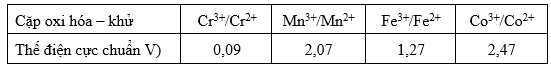
Giá trị thế điện cực chuẩn lớn nhất là 2,47 V của Co3+/Co2+.
⇒ Chọn đáp án B Đáp án: B
Nếu quy ước thế điện cực chuẩn của 2H+/H2 bằng 0,50 V thì giá trị thế điện cực của các cặp oxi – khử sẽ tăng đi 0,50 V
Ta có bảng giá trị thế điện cực mới:

Giá trị thế điện cực chuẩn lớn nhất là 2,47 V của Co3+/Co2+.
⇒ Chọn đáp án B Đáp án: B
Sử dụng đoạn thông tin dưới đây để trả lời câu 29 – 30:
Bộ phận quan trọng nhất của máy tạo nhịp tim là một hệ pin điện hoá lithium - iodine (gồm hai cặp oxi hoá khử Li+/Li và I2/2I–). Hai điện cực được đặt vào tim, phát sinh dòng điện nhỏ kích thích tim đập ổn định. Khi pin hoạt động, lithium bị oxi hoá và iodine bị khử. Biết 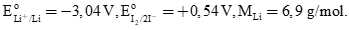 Điện tích của 1 mol electron là 96500 C/mol; q = I.t, trong đó q là điện tích (C), I là cường độ dòng điện (A), t là thời gian (s).
Điện tích của 1 mol electron là 96500 C/mol; q = I.t, trong đó q là điện tích (C), I là cường độ dòng điện (A), t là thời gian (s).
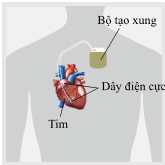
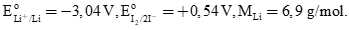 Điện tích của 1 mol electron là 96500 C/mol; q = I.t, trong đó q là điện tích (C), I là cường độ dòng điện (A), t là thời gian (s).
Điện tích của 1 mol electron là 96500 C/mol; q = I.t, trong đó q là điện tích (C), I là cường độ dòng điện (A), t là thời gian (s).
Câu 29 [705446]: Cho các nhận định sau, nhận định nào không đúng?
A, Iodine là cathode, lithium là anode.
B, Phản ứng tổng cộng xảy ra trong pin khi pin hoạt động là 2Li + I2 → 2Li+ + 2I-
C, Sức điện động chuẩn của pin là 3,58 V.
D, Cực dương xảy ra quá trình: Li → Li+ + 1e, cực âm xảy ra quá trình: I2 + 2e →2I-.
Ta có: 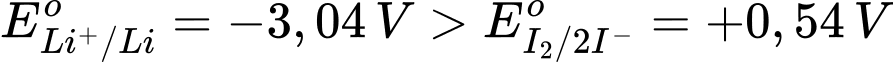 → Li+/Li vai trò điện cực anode (–), I2/2I– vai trò làm điện cực cathode (+)
→ Li+/Li vai trò điện cực anode (–), I2/2I– vai trò làm điện cực cathode (+)
Quá trình xảy ra trong pin:
Cathode (+): I2 + 2e ⟶ 2I–
Anode (–): Li ⟶ Li+ + 1e
Phản ứng trong pin: 2Li + I2 ⟶ 2Li+ + 2I–
⟶ Epin = E(+) – E(–) = 0,54 – (–3,04) = 3,58 V
Phân tích các nhận định:
✔️ A. Đúng. Iodine là cathode, lithium là anode.
✔️ B. Đúng. Phản ứng tổng cộng xảy ra trong pin khi pin hoạt động là 2Li + I2 → 2Li+ + 2I-.
✔️ C. Đúng. Sức điện động chuẩn của pin là 3,58 V.
❌ D. Sai. Cực dương xảy ra quá trình: I2 + 2e →2I-, cực âm xảy ra quá trình: Li → Li+ + 1e.
⇒ Chọn đáp án D Đáp án: D
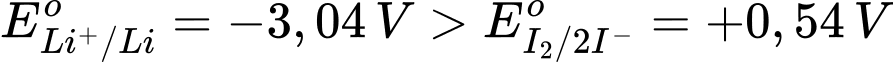 → Li+/Li vai trò điện cực anode (–), I2/2I– vai trò làm điện cực cathode (+)
→ Li+/Li vai trò điện cực anode (–), I2/2I– vai trò làm điện cực cathode (+)Quá trình xảy ra trong pin:
Cathode (+): I2 + 2e ⟶ 2I–
Anode (–): Li ⟶ Li+ + 1e
Phản ứng trong pin: 2Li + I2 ⟶ 2Li+ + 2I–
⟶ Epin = E(+) – E(–) = 0,54 – (–3,04) = 3,58 V
Phân tích các nhận định:
✔️ A. Đúng. Iodine là cathode, lithium là anode.
✔️ B. Đúng. Phản ứng tổng cộng xảy ra trong pin khi pin hoạt động là 2Li + I2 → 2Li+ + 2I-.
✔️ C. Đúng. Sức điện động chuẩn của pin là 3,58 V.
❌ D. Sai. Cực dương xảy ra quá trình: I2 + 2e →2I-, cực âm xảy ra quá trình: Li → Li+ + 1e.
⇒ Chọn đáp án D Đáp án: D
Câu 30 [705447]: Nếu pin tạo ra một dòng điện ổn định bằng 2,5×10-5 thì một pin được chế tạo bởi 0,1 gam lithium có thể hoạt động tối đa trong bao nhiêu ngày?
A, 648 ngày.
B, 1554 ngày.
C, 378 ngày.
D, 965 ngày.
Với t (thời gian, đơn vị: giây). Gọi a là số ngày cần tìm, đổi sang giây ta được: a × 24 × 3600 = t (giây)
Áp dụng định luật Faraday, ta có:
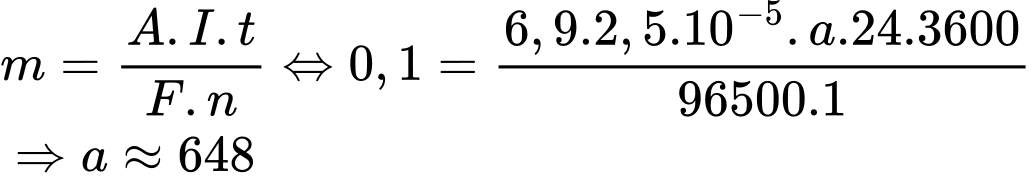
Vậy nếu pin tạo ra một dòng điện ổn định bằng 2,5×10-5 thì một pin được chế tạo bởi 0,1 gam lithium có thể hoạt động tối đa trong 648 ngày.
⇒ Chọn đáp án A Đáp án: A
Áp dụng định luật Faraday, ta có:
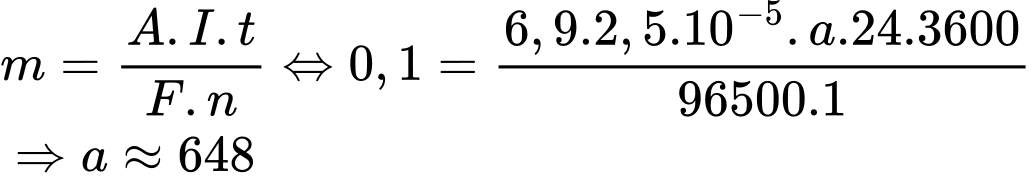
Vậy nếu pin tạo ra một dòng điện ổn định bằng 2,5×10-5 thì một pin được chế tạo bởi 0,1 gam lithium có thể hoạt động tối đa trong 648 ngày.
⇒ Chọn đáp án A Đáp án: A