Dạng 1. TRẮC NGHIỆM KHÁCH QUAN: mỗi câu hỏi chỉ có một đáp án đúng.
Câu 1 [1016533]: Sự chênh lệch điện thế tại một điều kiện bất kì gọi là
A, điện cực.
B, cầu muối.
C, thế điện cực.
D, thế điện cực chuẩn.
Sự chênh lệch điện thế tại một điều kiện bất kì gọi là thế điện cực.
Thế điện cực là giá trị điện thế (hiệu điện thế) giữa một điện cực và dung dịch chất điện ly của nó tại một điều kiện bất kỳ (có thể khác điều kiện chuẩn).
Thế điện cực chuẩn là thế điện cực được đo khi các ion có nồng độ 1M, áp suất khí (nếu có) là 1 bar, và nhiệt độ thường là 25oC (298K).
⟹ Chọn đáp án C Đáp án: C
Thế điện cực là giá trị điện thế (hiệu điện thế) giữa một điện cực và dung dịch chất điện ly của nó tại một điều kiện bất kỳ (có thể khác điều kiện chuẩn).
Thế điện cực chuẩn là thế điện cực được đo khi các ion có nồng độ 1M, áp suất khí (nếu có) là 1 bar, và nhiệt độ thường là 25oC (298K).
⟹ Chọn đáp án C Đáp án: C
Câu 2 [1016534]: Nếu thế điện cực di chuyển từ điện cực đồng sang điện cực kẽm thì
A, điện thế bên cặp cực đồng cao hơn bên cặp cực kẽm.
B, điện thế bên cặp cực đồng thấp hơn bên cặp cực kẽm.
C, điện thế bên cặp cực đồng và bên cặp cực kẽm bằng nhau.
D, không thể so sánh được điện thế giữa cặp cực đồng và cặp cực kẽm.
Khi di chuyển từ điện cực đồng sang điện cực kẽm, điện thế giảm vì điện cực đồng có thế điện cực cao hơn điện cực kẽm. Cụ thể, thế điện cực chuẩn của cặp Cu2+/Cu là +0,34V, trong khi của cặp Zn2+/Zn là –0,76V.
Do đó, có thể kết luận rằng điện thế bên cặp cực đồng cao hơn bên cặp cực kẽm.
⟹ Chọn đáp án A Đáp án: A
Do đó, có thể kết luận rằng điện thế bên cặp cực đồng cao hơn bên cặp cực kẽm.
⟹ Chọn đáp án A Đáp án: A
Câu 3 [560412]: Thế điện cực chuẩn là thế điện cực được đo trong điều kiện nồng độ ion kim loại trong dung dịch là 1 M và nhiệt độ
A, 0oC.
B, 20oC.
C, 25oC.
D, 100oC.
Điều kiện chuẩn là điều kiện trong đó nồng độ của ion kim loại trong dung dịch là 1 M và nhiệt độ là 25 oC (nhiệt độ phòng)
⟹ Chọn đáp án C Đáp án: C
⟹ Chọn đáp án C Đáp án: C
Câu 4 [560413]: Hai cặp oxi hóa khử Zn2+/Zn và Cu2+/Cu đều được thiết lập ở điều kiện chuẩn thì nồng độ mol của 2 ion Zn2+ và Cu2+ trong dung dịch của từng điện cực như thế nào so với nhau?
A, 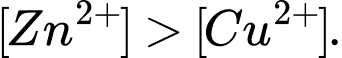
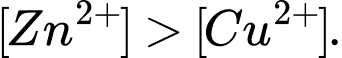
B, 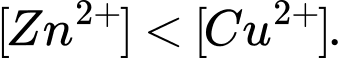
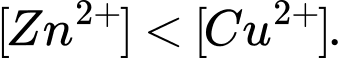
C, 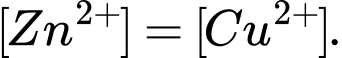
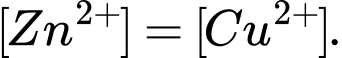
D, Chưa đủ thông tin để xác định.
Ở điều kiện chuẩn, cả hai cặp oxi hóa khử Zn2+/Zn và Cu2+/Cu đều có nồng độ mol chuẩn của ion là 1 M
→ nồng độ mol của Zn2+ và Cu2+ trong dung dịch của từng điện cực đều bằng 1 M vì điều kiện chuẩn trong điện hóa học được định nghĩa là nồng độ 1 M cho các ion trong dung dịch.
→ Nồng độ mol của Zn2+ và Cu2+ trong dung dịch của từng điện cực là bằng nhau và đều là 1 M trong điều kiện chuẩn.
⟹ Chọn đáp án C Đáp án: C
→ nồng độ mol của Zn2+ và Cu2+ trong dung dịch của từng điện cực đều bằng 1 M vì điều kiện chuẩn trong điện hóa học được định nghĩa là nồng độ 1 M cho các ion trong dung dịch.
→ Nồng độ mol của Zn2+ và Cu2+ trong dung dịch của từng điện cực là bằng nhau và đều là 1 M trong điều kiện chuẩn.
⟹ Chọn đáp án C Đáp án: C
Câu 5 [560414]: Yếu tố nào sau đây không ảnh hưởng đến thế điện cực của điện cực?
A, Bản chất của điện cực (kim loại).
B, Nhiệt độ.
C, Nồng độ mol của dung dịch.
D, Kích thước của điện cực.
Kích thước của điện cực không ảnh hưởng đến thế điện cực, vì thế điện cực phụ thuộc vào bản chất của điện cực (kim loại) và nồng độ ion, chứ không phải vào kích thước của điện cực đó.
⟹ Chọn đáp án D Đáp án: D
⟹ Chọn đáp án D Đáp án: D
Câu 6 [1016535]: Sử dụng bảng thế điện cực chuẩn của kim loại, cho biết cặp oxi hóa – khử nào sau đây có giá trị thế điện cực chuẩn lớn hơn 0?
A, K+/K.
B, Li+/Li.
C, Ba2+/Ba.
D, Cu2+/Cu.
Dựa vào bảng thế điện cực chuẩn của kim loại, cặp oxi hóa – khử Cu2+/Cu có giá trị thế điện cực chuẩn là +0,34V, lớn hơn 0. Trong khi đó, các cặp K+/K, Li+/Li, và Ba2+/Ba có giá trị thế điện cực chuẩn lần lượt là -2,93V, -3,05V và -2,90V đều có giá trị âm vì các kim loại này dễ nhường electron hơn. Do đó, trong các lựa chọn, chỉ có cặp Cu2+/Cu có thế điện cực chuẩn lớn hơn 0.
⟹ Chọn đáp án D
⟹ Chọn đáp án D
Câu 7 [824892]: Giá trị thế điện cực chuẩn của cặp oxi hóa – khử nào được quy ước bằng 0 V?
A, Na+/Na.
B, 2H+/H2.
C, Cl2/2Cl–.
D, Hg2+/Hg.
Phân tích các đáp án:
❌A. Giá trị thế điện cực chuẩn của Na+/Na Eo = -2,71V.
✔️B. Giá trị thế điện cực chuẩn của 2H+/H2 Eo = 0V.
❌C. Giá trị thế điện cực chuẩn của Cl2/2Cl- Eo = 1,36V.
❌D. Giá trị thế điện cực chuẩn của Hg2+/Hg Eo = 0,85V.
⟹ Chọn đáp án B Đáp án: B
❌A. Giá trị thế điện cực chuẩn của Na+/Na Eo = -2,71V.
✔️B. Giá trị thế điện cực chuẩn của 2H+/H2 Eo = 0V.
❌C. Giá trị thế điện cực chuẩn của Cl2/2Cl- Eo = 1,36V.
❌D. Giá trị thế điện cực chuẩn của Hg2+/Hg Eo = 0,85V.
⟹ Chọn đáp án B Đáp án: B
Câu 8 [824894]: Cặp oxi hóa - khử nào sau đây có giá trị thế điện cực chuẩn nhỏ hơn 0?
A, Ag+/Ag.
B, Na+/Na.
C, Cu2+/Cu.
D, Au3+/Au.
Phân tích các đáp án:
❌A. Giá trị thế điện cực của Ag+/Ag Eo = 0,80V.
✔️B. Giá trị thế điện cực của Na+/Na Eo = -2,71V.
❌C. Giá trị thế điện cực của Cu2+/Cu Eo = 0,34V.
❌D. Giá trị thế điện cực của Au3+/Au Eo = 1,50V.
⟹ Cặp oxi hóa - khử Na+/Na có giá trị thế điện cực Eo < 0.
⟹ Chọn đáp án B Đáp án: B
❌A. Giá trị thế điện cực của Ag+/Ag Eo = 0,80V.
✔️B. Giá trị thế điện cực của Na+/Na Eo = -2,71V.
❌C. Giá trị thế điện cực của Cu2+/Cu Eo = 0,34V.
❌D. Giá trị thế điện cực của Au3+/Au Eo = 1,50V.
⟹ Cặp oxi hóa - khử Na+/Na có giá trị thế điện cực Eo < 0.
⟹ Chọn đáp án B Đáp án: B
Câu 9 [824895]: Cặp oxi hóa - khử nào sau đây có giá trị thế điện cực chuẩn lớn hơn 0?
A, Ni2+/Ni.
B, Pb2+/Pb.
C, Al3+/Al.
D, Hg2+/Hg.
Phân tích các đáp án:
❌A. Giá trị thế điện cực chuẩn của Ni2+/Ni Eo = -0,25V.
❌B. Giá trị thế điện cực chuẩn của Pb2+/Pb Eo = -0,13V.
❌C. Giá trị thế điện cực chuẩn của Al3+/Al Eo = -1,66V.
✔️D. Giá trị thế điện cực chuẩn của Hg2+/Hg Eo = 0,85V.
⟹ Cặp oxi hóa - khử Hg2+/Hg có giá trị thế điện cực chuẩn lớn hơn 0.
⟹ Chọn đáp án D Đáp án: D
❌A. Giá trị thế điện cực chuẩn của Ni2+/Ni Eo = -0,25V.
❌B. Giá trị thế điện cực chuẩn của Pb2+/Pb Eo = -0,13V.
❌C. Giá trị thế điện cực chuẩn của Al3+/Al Eo = -1,66V.
✔️D. Giá trị thế điện cực chuẩn của Hg2+/Hg Eo = 0,85V.
⟹ Cặp oxi hóa - khử Hg2+/Hg có giá trị thế điện cực chuẩn lớn hơn 0.
⟹ Chọn đáp án D Đáp án: D
Dạng 2: TRẮC NGHIỆM ĐÚNG SAI – mỗi ý a), b), c), d) chọn đúng hoặc sai.
Câu 10 [560430]: Tiến hành lặp đặt bộ dụng cụ như minh hoạ ở hình dưới đây:
• Điện cực Cu: Cốc thuỷ tinh chứa thanh đồng Cu nhúng trong dung dịch CuSO4 1 M (cốc ❶).
• Điện cực Zn: Cốc thuỷ tinh chứa thanh kẽm Zn nhúng trong dung dịch ZnSO4 1 M (cốc ❷).
• Cầu muối: Ống thuỷ tinh chữ U đựng dung dịch NaNO3 bão hoà kết nối hai cốc thuỷ tinh.

Nối hai thanh kim loại bằng dây dẫn điện qua một vôn kế, giá trị của vôn kế hiển thị là 1,10 V.
• Điện cực Cu: Cốc thuỷ tinh chứa thanh đồng Cu nhúng trong dung dịch CuSO4 1 M (cốc ❶).
• Điện cực Zn: Cốc thuỷ tinh chứa thanh kẽm Zn nhúng trong dung dịch ZnSO4 1 M (cốc ❷).
• Cầu muối: Ống thuỷ tinh chữ U đựng dung dịch NaNO3 bão hoà kết nối hai cốc thuỷ tinh.

Nối hai thanh kim loại bằng dây dẫn điện qua một vôn kế, giá trị của vôn kế hiển thị là 1,10 V.
Phân tích các phát biểu:
✔️ a. Đúng. Có dòng điện chạy qua dây dẫn do vôn kế hiển thị giá trị là 1,10V.
❌ b. Sai. Sự chênh lệch điện thế giữa hai điện cực là nguyên nhân tạo ra dòng điện và giá trị điện thế đo được là 1,10 V.
❌ c. Sai. Hai điện cực hình thành là Cu2+/Cu và Zn2+/Zn.
❌ d. Sai. Yếu tố nồng độ của ion kim loại ảnh hưởng đến thế điện cực nên khi thay nồng độ của CuSO4 thành 2 M thì vôn kế hiển thị sẽ thay đổi.
✔️ a. Đúng. Có dòng điện chạy qua dây dẫn do vôn kế hiển thị giá trị là 1,10V.
❌ b. Sai. Sự chênh lệch điện thế giữa hai điện cực là nguyên nhân tạo ra dòng điện và giá trị điện thế đo được là 1,10 V.
❌ c. Sai. Hai điện cực hình thành là Cu2+/Cu và Zn2+/Zn.
❌ d. Sai. Yếu tố nồng độ của ion kim loại ảnh hưởng đến thế điện cực nên khi thay nồng độ của CuSO4 thành 2 M thì vôn kế hiển thị sẽ thay đổi.
Câu 11 [560431]: Nhúng một thanh kẽm vào cốc đựng dung dịch copper(II) sulfate, sau một thời gian nhấc thanh kẽm ra thì thấy xuất hiện một lớp đồng màu nâu đỏ bám vào thanh kẽm.
Phân tích các phát biểu:
❌ a. Sai. Zn khử ion Cu2+.
✔️ b. Đúng. Zn đóng vai trò là chất khử vì có số oxi hoá tăng từ 0 lên +2.
❌ c. Sai. SO42– không tham gia trực tiếp vào phản ứng oxi hóa - khử, nên không phải chất oxi hóa.
✔️ d. Đúng. Nồng độ ion Cu2+ trong dung dịch giảm do chuyển thành kim loại Cu.
❌ a. Sai. Zn khử ion Cu2+.
✔️ b. Đúng. Zn đóng vai trò là chất khử vì có số oxi hoá tăng từ 0 lên +2.
❌ c. Sai. SO42– không tham gia trực tiếp vào phản ứng oxi hóa - khử, nên không phải chất oxi hóa.
✔️ d. Đúng. Nồng độ ion Cu2+ trong dung dịch giảm do chuyển thành kim loại Cu.
Câu 12 [560433]: Hình vẽ dưới đây cho thấy điện cực kẽm chuẩn được nối với điện cực hydrogen chuẩn.
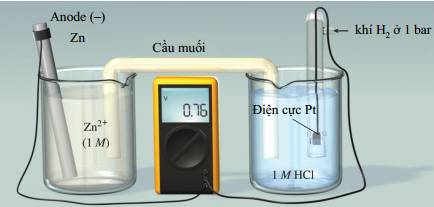
Sự chênh lệch thế điện cực chuẩn đo được là 0,76 V và dòng điện di chuyển từ điện cực kẽm về điện cực hydrogen chuẩn.

Sự chênh lệch thế điện cực chuẩn đo được là 0,76 V và dòng điện di chuyển từ điện cực kẽm về điện cực hydrogen chuẩn.
Sự chênh lệch thế điện cực đo được là 0,76 V và dòng electron mang điện tích âm di chuyển từ điện cực kẽm về điện cực hydrogen chuẩn ⇝ Điện cực kẽm chứa nhiều electron và thế điện cực sẽ âm hơn.
Phân tích các phát biểu:
❌ a. Sai. Thế điện cực chuẩn của 2H+/H2 là 0,00 V.
✔️ b. Đúng. Dòng electron chạy từ điện cực kẽm về điện cực hydrogen.
❌ c. Sai. Thế điện cực chuẩn phụ thuộc vào nồng độ H+ thông qua phương trình Nernst. Khi nồng độ H+ tăng, thế điện cực của cặp H+/H2 sẽ thay đổi, và do đó sự chênh lệch thế điện cực sẽ không còn là 0,76 V.
❌ d. Sai. Nếu coi thế điện cực chuẩn của 2H+/H2 là 1 V thì thế điện cực chuẩn của Zn2+/Zn là 1 - 0,76 V = 0,24V
Phân tích các phát biểu:
❌ a. Sai. Thế điện cực chuẩn của 2H+/H2 là 0,00 V.
✔️ b. Đúng. Dòng electron chạy từ điện cực kẽm về điện cực hydrogen.
❌ c. Sai. Thế điện cực chuẩn phụ thuộc vào nồng độ H+ thông qua phương trình Nernst. Khi nồng độ H+ tăng, thế điện cực của cặp H+/H2 sẽ thay đổi, và do đó sự chênh lệch thế điện cực sẽ không còn là 0,76 V.
❌ d. Sai. Nếu coi thế điện cực chuẩn của 2H+/H2 là 1 V thì thế điện cực chuẩn của Zn2+/Zn là 1 - 0,76 V = 0,24V
Câu 13 [560435]: Sơ đồ sau được thiết kế để tìm thế điện cực chuẩn của kẽm:
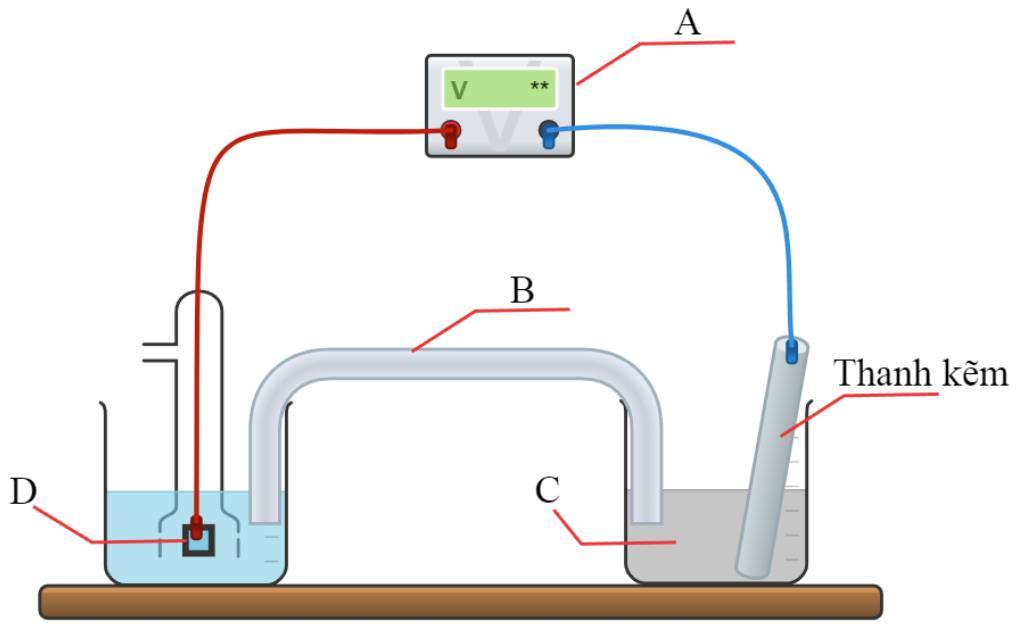

Phân tích các phát biểu:
❌ a. Sai. Dụng cụ A là Volt kế để đo hiệu điện thế. (đơn vị volt).
✔️ b. Đúng. Dụng cụ B là cầu muối, ví dụ NaNO3.
✔️ c. Đúng. Dung dịch C bắt buộc phải là dung dịch muối của kim loại kẽm.
✔️ d. Đúng. D là điện cực trơ, có thể làm bằng Pt.
❌ a. Sai. Dụng cụ A là Volt kế để đo hiệu điện thế. (đơn vị volt).
✔️ b. Đúng. Dụng cụ B là cầu muối, ví dụ NaNO3.
✔️ c. Đúng. Dung dịch C bắt buộc phải là dung dịch muối của kim loại kẽm.
✔️ d. Đúng. D là điện cực trơ, có thể làm bằng Pt.
Dạng 3: TRẮC NGHIỆM YÊU CẦU TRẢ LỜI NGẮN
Câu 14 [560440]: Điện cực nhôm Al3+/Al chuẩn được nối với điện cực hydrogen chuẩn 2H+/H2 thì vôn kế hiển thị giá trị là 1,66 V và dòng electron di chuyển từ điện cực nhôm về điện cực hydrogen. Thế điện cực chuẩn của Al3+/Al bằng bao nhiêu volt (V)?
Sự chênh lệch thế điện cực đo được là 1,66 V dòng electron mang điện tích âm di chuyển từ điện cực nhôm về điện cực hydrogen chuẩn ⇝ Điện cực nhôm chứa nhiều electron, thế điện cực sẽ âm hơn và bằng -1,66 V
⇒ Điền đáp án: -1,66
⇒ Điền đáp án: -1,66
Câu 15 [560441]: Điện cực đồng Cu2+/Cu chuẩn được nối với điện cực hydrogen chuẩn 2H+/H2 thì vôn kế hiển thị giá trị là 0,34 V và dòng electron di chuyển từ điện cực hydrogen về điện cực đồng. Thế điện cực chuẩn của Cu2+/Cu bằng bao nhiêu volt (V)?
Sự chênh lệch thế điện cực đo được là 0,34 V và dòng electron di chuyển từ điện cực hydrogen
chuẩn về điện cực đồng ⇝ Điện cực đồng chứa ít electron, thế điện cực sẽ dương hơn và bằng +0,34 V
⇒ Điền đáp án: 0,34
chuẩn về điện cực đồng ⇝ Điện cực đồng chứa ít electron, thế điện cực sẽ dương hơn và bằng +0,34 V
⇒ Điền đáp án: 0,34
Dạng 4: BÀI TẬP ĐỌC HIỂU – đọc thông tin và trả lời các câu hỏi sau đó
ĐIỆN CỰC HYDROGEN TIÊU CHUẨN (SHE)
Điện cực hydrogen tiêu chuẩn (standard hydrogen electrode – SHE) bao gồm một dây bạch kim (Platinum - Pt) được nối với một tấm bạch kim, trên tấm bạch kim có phủ một lớp bạch kim mịn, dùng làm bề mặt trơ cho phản ứng: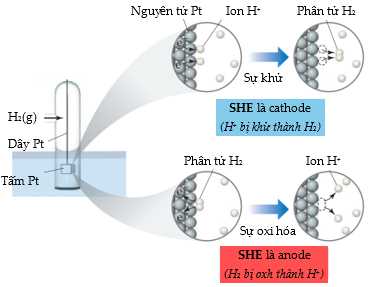
SHE cho phép bạch kim tiếp xúc với cả ion H+ (aq) 1 M và dòng khí hydrogen ở áp suất 1 bar. SHE có thể hoạt động như cực dương xảy ra quá trình H+ tạo H2 hoặc cực âm H2 tạo H+, tùy thuộc vào bản chất của điện cực kia. Khi nối điện cực Zn2+/Zn chuẩn với SHE thì quá trình xảy ra như sau:
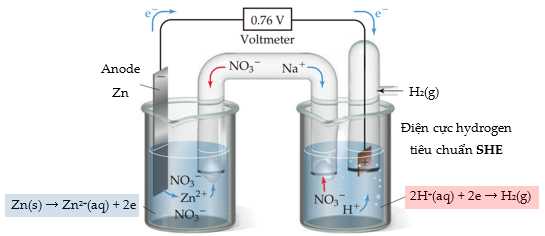
Câu 16 [560444]: Dây bạch kim Pt có vai trò
A, chất khử.
B, chất oxi hoá.
C, chất dẫn điện.
D, chất bị khử.
- Pt là kim loại trơ, không bị oxy hóa hay tham gia phản ứng trong quá trình điện phân, nên thường dùng làm điện cực trơ (cực dương hoặc cực âm).
- Pt được dùng làm điện cực trơ trong nhiều ứng dụng điện phân quan trọng nhờ tính bền vững và dẫn điện tốt.
Chọn đáp án C Đáp án: C
- Pt được dùng làm điện cực trơ trong nhiều ứng dụng điện phân quan trọng nhờ tính bền vững và dẫn điện tốt.
Chọn đáp án C Đáp án: C
Câu 17 [560445]: Thế điện cực chuẩn của Zn2+/Zn là
A, 0,00 V.
B, –0,76 V.
C, +0,76 V.
D, –1,76 V.
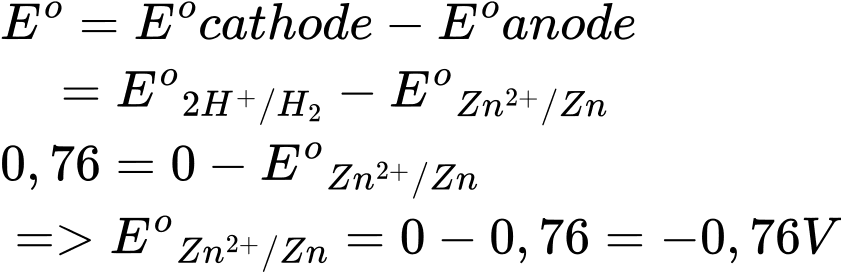
Chọn đáp án B Đáp án: B
Câu 18 [560446]: Nếu nối một điện cực chuẩn Xn+/X với SHE, trên SHE xảy ra quá trình:H2 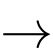 2H+ + 2e thì điện cực Xn+/X có thế điện cực chuẩn như thế nào?
2H+ + 2e thì điện cực Xn+/X có thế điện cực chuẩn như thế nào?
 2H+ + 2e thì điện cực Xn+/X có thế điện cực chuẩn như thế nào?
2H+ + 2e thì điện cực Xn+/X có thế điện cực chuẩn như thế nào? A, 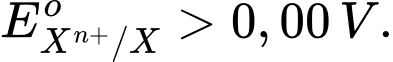
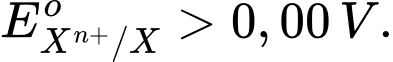
B, 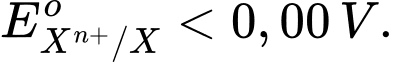
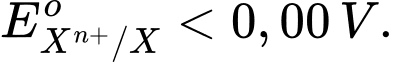
C, 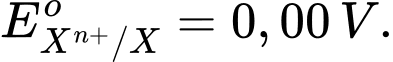
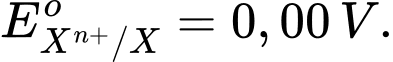
D, 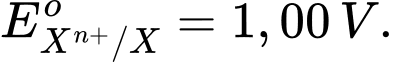
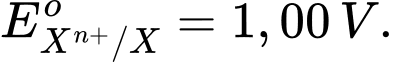
H2 → 2H++2e
Đây là phản ứng oxi hóa H2 thành ion H+ tức là SHE đóng vai trò là anot (+) => Zn đóng vai trò cathode
Vì SHE đóng vai trò anot, nên thế điện cực chuẩn của Xn+ phải lớn hơn thế điện cực chuẩn của SHE (0,00V), tức là:EoXn+/X > 0,00V.
Chọn đáp án A Đáp án: A
Đây là phản ứng oxi hóa H2 thành ion H+ tức là SHE đóng vai trò là anot (+) => Zn đóng vai trò cathode
Vì SHE đóng vai trò anot, nên thế điện cực chuẩn của Xn+ phải lớn hơn thế điện cực chuẩn của SHE (0,00V), tức là:EoXn+/X > 0,00V.
Chọn đáp án A Đáp án: A