Dạng 1. TRẮC NGHIỆM KHÁCH QUAN: mỗi câu hỏi chỉ có một đáp án đúng.
Câu 1 [560415]: Cho thế điện cực chuẩn của các cặp oxi hóa – khử như sau:
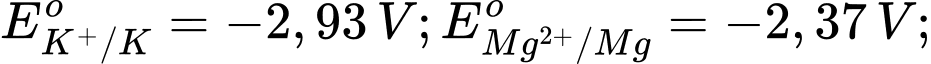
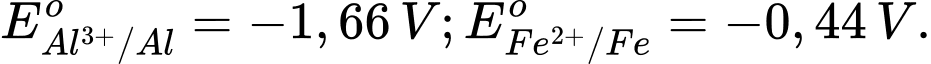
Trong các kim loại sau đây, kim loại nào sau đây có tính khử mạnh nhất?
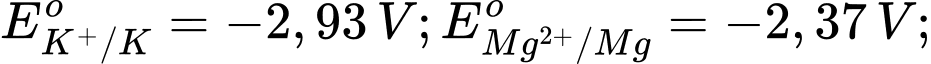
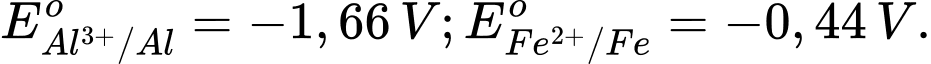
Trong các kim loại sau đây, kim loại nào sau đây có tính khử mạnh nhất?
A, Fe.
B, K.
C, Al.
D, Mg.
Kim loại có tính khử mạnh nhất trong số các kim loại được liệt kê là Potassium (K), vì nó có thế điện cực chuẩn âm nhất.
⟹ Chọn đáp án B Đáp án: B
⟹ Chọn đáp án B Đáp án: B
Câu 2 [560416]: Cho thế điện cực chuẩn của các cặp oxi hóa – khử như sau:
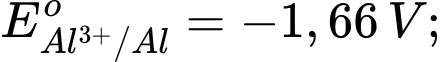
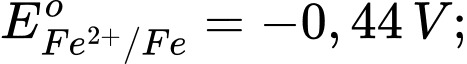
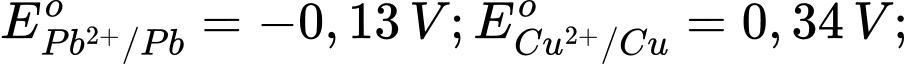
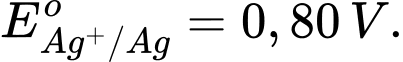
Kim loại nào sau đây có tính khử mạnh hơn Fe?
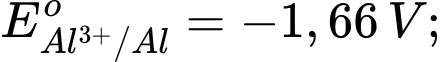
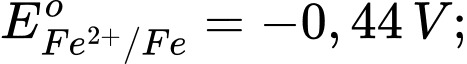
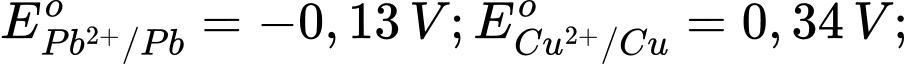
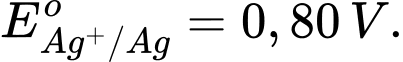
Kim loại nào sau đây có tính khử mạnh hơn Fe?
A, Ag.
B, Cu.
C, Pb.
D, Al.
Kim loại có tính khử mạnh hơn Fe là Al vì có thế điện cực chuẩn của cặp oxi hoá khử nhỏ hơn của Fe.
Kim loại có tính khử càng mạnh thì thế điện cực chuẩn càng nhỏ.
⟹ Chọn đáp án D Đáp án: D
Kim loại có tính khử càng mạnh thì thế điện cực chuẩn càng nhỏ.
⟹ Chọn đáp án D Đáp án: D
Câu 3 [560417]: Cho thế điện cực chuẩn của các cặp oxi hóa – khử như sau:
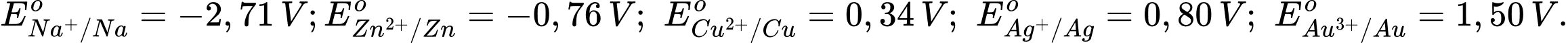
Kim loại nào sau đây có tính khử mạnh hơn kim loại Zn?
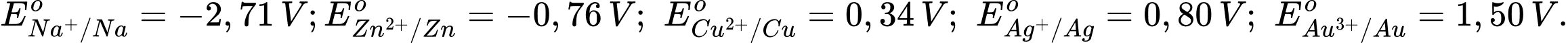
Kim loại nào sau đây có tính khử mạnh hơn kim loại Zn?
A, Ag.
B, Na.
C, Cu.
D, Au.
Kim loại có tính khử mạnh hơn Zn là Na vì có thế điện cực chuẩn của cặp oxi hoá khử nhỏ hơn của Zn.
Kim loại có tính khử càng mạnh thì thế điện cực chuẩn càng nhỏ.
⟹ Chọn đáp án B Đáp án: B
Kim loại có tính khử càng mạnh thì thế điện cực chuẩn càng nhỏ.
⟹ Chọn đáp án B Đáp án: B
Câu 4 [560418]: Cho thế điện cực chuẩn của các cặp oxi hóa – khử như sau:
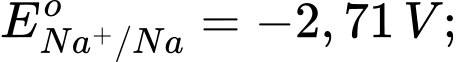
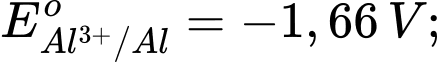
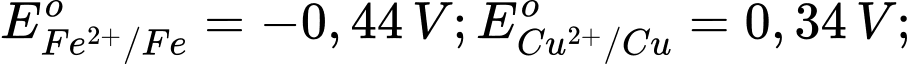
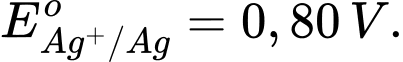
Kim loại nào sau đây có tính khử yếu nhất?
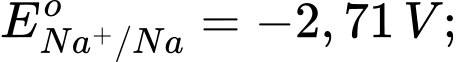
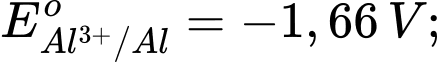
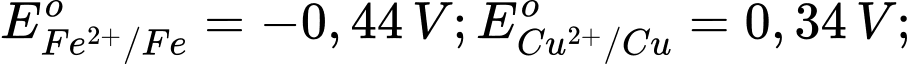
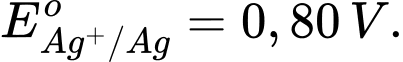
Kim loại nào sau đây có tính khử yếu nhất?
A, Ag.
B, Na.
C, Al.
D, Fe.
Tính khử của một kim loại được thể hiện qua khả năng nhường electron của nó. Kim loại có thế điện cực chuẩn Eo của cặp oxi hóa-khử Mn+/M càng lớn thì tính khử càng yếu, vì kim loại đó khó bị oxi hóa thành ion Mn+.
Phân tích các giá trị thế điện cực chuẩn:
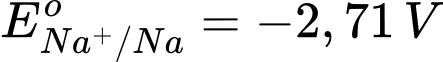 : Kim loại NaNa có tính khử mạnh nhất.
: Kim loại NaNa có tính khử mạnh nhất.
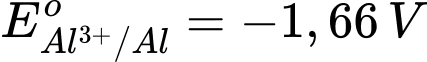 : Kim loại Al có tính khử mạnh, nhưng yếu hơn Na.
: Kim loại Al có tính khử mạnh, nhưng yếu hơn Na.
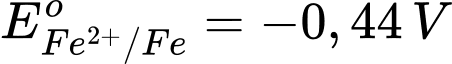 : Kim loại Fe có tính khử yếu hơn Al.
: Kim loại Fe có tính khử yếu hơn Al.
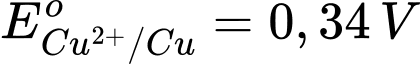 : Kim loại Cu có tính khử yếu hơn Fe.
: Kim loại Cu có tính khử yếu hơn Fe.
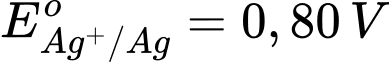 : Kim loại Ag có tính khử yếu nhất trong các kim loại này.
: Kim loại Ag có tính khử yếu nhất trong các kim loại này.
⇒ Chọn đáp án A Đáp án: A
Phân tích các giá trị thế điện cực chuẩn:
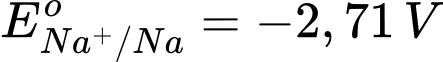 : Kim loại NaNa có tính khử mạnh nhất.
: Kim loại NaNa có tính khử mạnh nhất.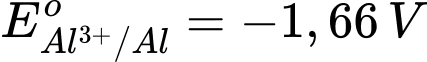 : Kim loại Al có tính khử mạnh, nhưng yếu hơn Na.
: Kim loại Al có tính khử mạnh, nhưng yếu hơn Na.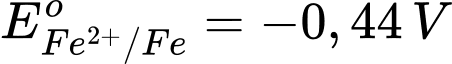 : Kim loại Fe có tính khử yếu hơn Al.
: Kim loại Fe có tính khử yếu hơn Al. 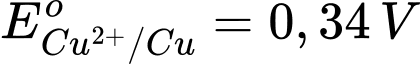 : Kim loại Cu có tính khử yếu hơn Fe.
: Kim loại Cu có tính khử yếu hơn Fe.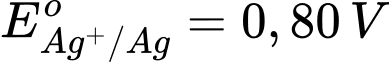 : Kim loại Ag có tính khử yếu nhất trong các kim loại này.
: Kim loại Ag có tính khử yếu nhất trong các kim loại này.⇒ Chọn đáp án A Đáp án: A
Câu 5 [560419]: Ion kim loại nào sau đây có tính oxi hóa mạnh nhất?
A, Cu2+.
B, Mg2+.
C, Pb2+.
D, Ag+.
Tính oxi hóa tăng dần như sau: Mg2+ < Pb2+ < Cu2+ < Ag+.
Vậy ion kim loại có tính oxi hóa mạnh nhất là Ag+.
⟹ Chọn đáp án D Đáp án: D
Vậy ion kim loại có tính oxi hóa mạnh nhất là Ag+.
⟹ Chọn đáp án D Đáp án: D
Câu 6 [560420]: Cho dãy các ion: Fe2+, Ni2+, Cu2+, Sn2+. Trong cùng điều kiện, ion có tính oxi hóa mạnh nhất trong dãy là
A, Sn2+.
B, Ni2+.
C, Cu2+.
D, Fe2+.
Trong cùng điều kiện, tính oxi hóa mạnh nhất trong dãy có xu hướng tăng dần như sau: Fe2+ < Ni2+ < Sn2+ < Cu2+
→ Ion có tính oxi hóa mạnh nhất trong dãy là Cu2+
⟹ Chọn đáp án C Đáp án: C
→ Ion có tính oxi hóa mạnh nhất trong dãy là Cu2+
⟹ Chọn đáp án C Đáp án: C
Câu 7 [706100]: Cho các thế điện cực chuẩn: 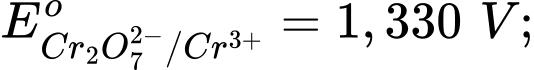
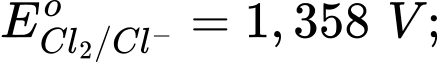
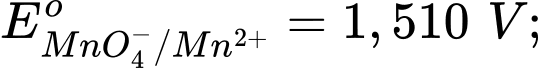
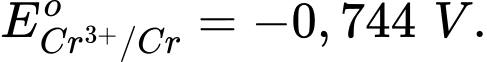 Chọn cách sắp xếp các ion và kim loại theo thứ tự tăng dần tính khử.
Chọn cách sắp xếp các ion và kim loại theo thứ tự tăng dần tính khử.
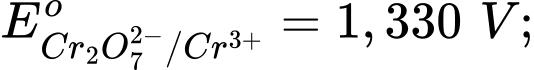
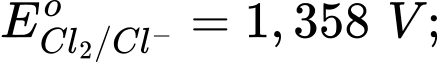
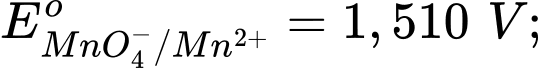
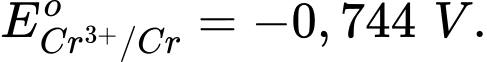 Chọn cách sắp xếp các ion và kim loại theo thứ tự tăng dần tính khử.
Chọn cách sắp xếp các ion và kim loại theo thứ tự tăng dần tính khử. A, Cr3+, Cl–, Mn2+, Cr.
B, Mn2+, Cl–, Cr3+, Cr.
C, Cr3+, Cl–, Cr2O72–, MnO4–.
D, Mn2+, Cr3+, Cl–, Cr.
Thế điện cực chuẩn của cặp oxi hóa – khử càng lớn thì tính khử của dạng khử càng yếu, tính oxi hóa của dạng oxi hóa càng mạnh và ngược lại.
Thứ tự tăng dần thế điện cực chuẩn là :
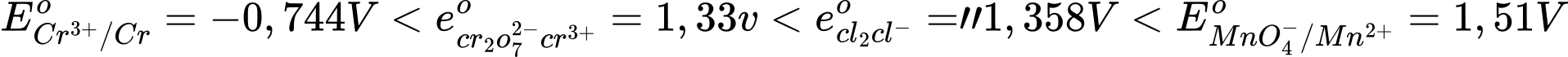 ""
"" Thứ tự tăng dần tính khử là: Mn2+ < Cl- < Cr3+ < Cr.
⟹Chọn đáp án B Đáp án: B
Thứ tự tăng dần thế điện cực chuẩn là :
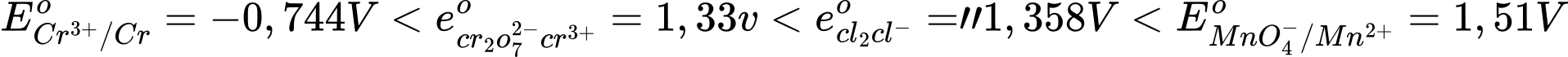 ""
"" ⟹Chọn đáp án B Đáp án: B
Câu 8 [705885]: Trong các phản ứng oxi hóa – khử, việc chọn tác nhân oxi hóa để phù hợp với các điều kiện của phản ứng là quan trọng. Một phản ứng cần chọn tác nhân oxi hóa rất mạnh, trong các tác nhân sau, tác nhân oxi hóa mạnh nhất là? Cho các thế điện cực chuẩn: 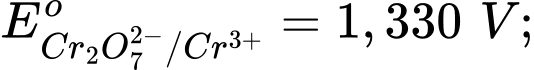
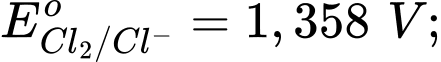
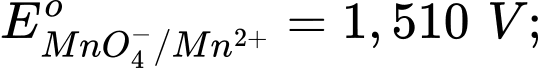
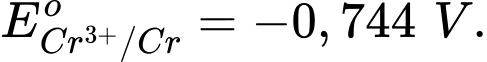
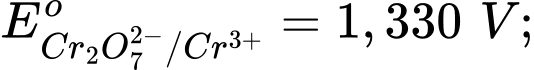
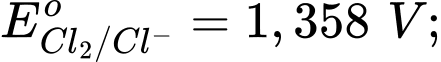
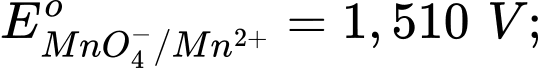
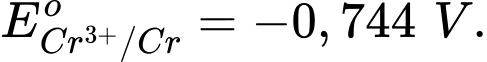
A, Cl–.
B, Mn2+.
C, MnO4–.
D, Cr3+.
-Thế điện cực của cặp oxi hóa – khử của kim loại (đơn vị là Volt – V) trong điều kiện chuẩn (nồng độ ion kim loại trong dung dịch là 1M, nhiệt độ 25oC) được gọi là thế điện cực chuẩn của kim loại (hay thế khử chuẩn của kim loại, kí hiệu là .
-Thế điện cực chuẩn của cặp oxi hóa – khử càng lớn thì tính khử của dạng khử càng yếu, tính oxi hóa của dạng oxi hóa càng mạnh và ngược lại.
Chọn đáp án C Đáp án: C
-Thế điện cực chuẩn của cặp oxi hóa – khử càng lớn thì tính khử của dạng khử càng yếu, tính oxi hóa của dạng oxi hóa càng mạnh và ngược lại.
Chọn đáp án C Đáp án: C
Câu 9 [705396]: Thế điện cực chuẩn của cặp oxi hóa – khử càng lớn thì tính oxi hóa của dạng oxi hóa càng …(1)… và tính khử của dạng khử càng …(2)… Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, mạnh, yếu.
B, yếu, mạnh.
C, mạnh, mạnh.
D, yếu, yếu.
Thế điện cực chuẩn của cặp oxi hóa – khử càng lớn thì tính oxi hóa của dạng oxi hóa càng mạnh và tính khử của dạng khử càng yếu.
Giải thích:
Dựa vào đặc điểm của thế điện cực chuẩn, thế điện cực chuẩn càng lớn:
+) Dạng oxi hóa (chất nhận electron) có tính oxi hóa mạnh hơn, vì dễ dàng nhận electron.
+) Dạng khử (chất cho electron) có tính khử yếu hơn, vì khó nhường electron.
⇒ Chọn đáp án A Đáp án: A
Giải thích:
Dựa vào đặc điểm của thế điện cực chuẩn, thế điện cực chuẩn càng lớn:
+) Dạng oxi hóa (chất nhận electron) có tính oxi hóa mạnh hơn, vì dễ dàng nhận electron.
+) Dạng khử (chất cho electron) có tính khử yếu hơn, vì khó nhường electron.
⇒ Chọn đáp án A Đáp án: A
Câu 10 [706008]: Kim loại M hoạt động hóa học càng mạnh thì giá trị thế điện cực chuẩn của cặp oxi hoá – khử Mn+/M
A, càng âm.
B, càng dương.
C, bằng 0.
D, càng biến đổi không có xu hướng.
Bảng thế điện cực chuẩn của kim loại có thể được sắp xếp thành một dãy như sau (còn được gọi là dãy điện hóa của kim loại):
Thế điện cực chuẩn của cặp oxi hóa – khử càng lớn thì tính khử của dạng khử càng yếu, tính oxi hóa của dạng oxi hóa càng mạnh và ngược lại.
⟹ Chọn đáp án A
Câu 11 [1016536]: Cho các cặp oxi hóa – khử của kim loại và thế điện cực chuẩn tương ứng:
Trong các kim loại trên, số kim loại tác dụng được với dung dịch HCl ở điều kiện chuẩn, giải phóng khí H2 là

Trong các kim loại trên, số kim loại tác dụng được với dung dịch HCl ở điều kiện chuẩn, giải phóng khí H2 là
A, 1.
B, 2.
C, 3.
D, 4.
Thế điện cực chuẩn của 2H+/H2 là 0.
Điều kiện là kim loại phải có thế điện cực chuẩn nhỏ hơn 0V, nghĩa là nằm trước H+/H2 trong dãy điện hóa.
Các kim loại phản ứng với HCl là Na, Ca, Ni.
⟹ Chọn đáp án C Đáp án: C
Điều kiện là kim loại phải có thế điện cực chuẩn nhỏ hơn 0V, nghĩa là nằm trước H+/H2 trong dãy điện hóa.
Các kim loại phản ứng với HCl là Na, Ca, Ni.
⟹ Chọn đáp án C Đáp án: C
Câu 12 [560421]: Kim loại M tan được trong dung dịch HCl 1M ở 25oC tạo muối MCln và H2. Giá trị thế điện cực chuẩn của cặp Mn+/M như thế nào so với 2H+/H2?
A, Lớn hơn.
B, Nhỏ hơn.
C, Bằng nhau.
D, Không xác định.
2M + 2nH+ ⟶ 2Mn+ + nH2
Dựa vào phản ứng ta thấy H+ có tính oxi hóa mạnh hơn Mn+, M có tính khử mạnh hơn H2 ⟹ Giá trị thế điện cực chuẩn của cặp Mn+/M nhỏ hơn so với 2H+/H2 Đáp án: B
Câu 13 [706240]: Ở điều kiện chuẩn, những kim loại tan trong hydrochloric acid hoặc sulfuric acid loãng thường có thế điện cực chuẩn
A, lớn hơn 0 V.
B, nhỏ hơn 0 V.
C, lớn hơn –0,413 V.
D, nhỏ hơn –0,413 V.
Phân tích các đáp án:
❌A. SAI. Kim loại có thế điện cực chuẩn lớn hơn 0 V (ví dụ: Cu, Ag, Au) không phản ứng với acid HCl hoặc H2SO4 loãng.
✔️B. ĐÚNG. Kim loại có thế điện cực chuẩn nhỏ hơn 0 V (ví dụ: Zn, Fe, Al) phản ứng với acid HCl hoặc H2SO4 loãng.
❌C,D. SAI. Giá trị -0,413 V không phải là một mốc quan trọng trong phản ứng của kim loại với acid.
⟹ Chọn đáp án B Đáp án: B
❌A. SAI. Kim loại có thế điện cực chuẩn lớn hơn 0 V (ví dụ: Cu, Ag, Au) không phản ứng với acid HCl hoặc H2SO4 loãng.
✔️B. ĐÚNG. Kim loại có thế điện cực chuẩn nhỏ hơn 0 V (ví dụ: Zn, Fe, Al) phản ứng với acid HCl hoặc H2SO4 loãng.
❌C,D. SAI. Giá trị -0,413 V không phải là một mốc quan trọng trong phản ứng của kim loại với acid.
⟹ Chọn đáp án B Đáp án: B
Câu 14 [706201]: Magnesium tác dụng với nước ở nhiệt độ thường (dù chậm) tạo ra hydroxide và khí hydrogen. Tính chất này phù hợp với dữ kiện là cặp oxi hoá – khử Mg2+/Mg có giá trị thế điện cực chuẩn
A, lớn hơn –0,413 V.
B, nhỏ hơn –0,413 V.
C, lớn hơn 0 V.
D, nhỏ hơn 0 V.
Magnesium (Mg) phản ứng với nước ở nhiệt độ thường tạo ra hydroxide Mg(OH)2 và khí hydrogen H2.
Phản ứng này xảy ra được vì Mg là kim loại có tính khử mạnh, có thế điện cực chuẩn Eo nhỏ hơn thế điện cực chuẩn của cặp 2H2O/H2,OH- (-0,413V).
Khi Eo (Mg2+/Mg) < -0.413V, Mg có khả năng khử H2O thành H2.
⟹ Chọn đáp án B
Đáp án: B ⟹ Chọn đáp án B
Câu 15 [560422]: Cho các cặp oxi hoá - khử sau: Zn2+/Zn và Fe2+/Fe. Phương trình hoá học của phản ứng theo chiều tự diễn biến từ các cặp oxi hoá - khử tương ứng đã cho là
A, Zn2+ + Fe  Zn + Fe2+.
Zn + Fe2+.
 Zn + Fe2+.
Zn + Fe2+.B, Zn + Fe2+  Zn2+ + Fe.
Zn2+ + Fe.
 Zn2+ + Fe.
Zn2+ + Fe.C, Fe2+ + Zn2+  Zn + Fe.
Zn + Fe.
 Zn + Fe.
Zn + Fe.D, Zn + Fe  Fe2+ + Zn2+.
Fe2+ + Zn2+.
 Fe2+ + Zn2+.
Fe2+ + Zn2+.
Phương trình hoá học của phản ứng theo chiều tự diễn biến từ các cặp oxi hoá - khử tương ứng đã cho là: Zn + Fe2+  Zn2+ + Fe. Đáp án: B
Zn2+ + Fe. Đáp án: B
 Zn2+ + Fe. Đáp án: B
Zn2+ + Fe. Đáp án: B
Câu 16 [560423]: Cho các cặp oxi hoá - khử sau: Ag+/Ag và Au3+/Au. Phương trình hoá học của phản ứng theo chiều tự diễn biến từ các cặp oxi hoá - khử tương ứng đã cho là
A, Ag+ + Au  Ag + Au3+.
Ag + Au3+.
 Ag + Au3+.
Ag + Au3+.B, Ag + Au3+  Ag+ + Au.
Ag+ + Au.
 Ag+ + Au.
Ag+ + Au.C, Au3+ + Ag+  Ag + Au.
Ag + Au.
 Ag + Au.
Ag + Au.D, Ag + Au  Au3+ + Ag+.
Au3+ + Ag+.
 Au3+ + Ag+.
Au3+ + Ag+.Phương trình hoá học của phản ứng theo chiều tự diễn biến từ các cặp oxi hoá - khử tương ứng đã cho là: Ag + Au3+  Ag+ + Au.
Ag+ + Au.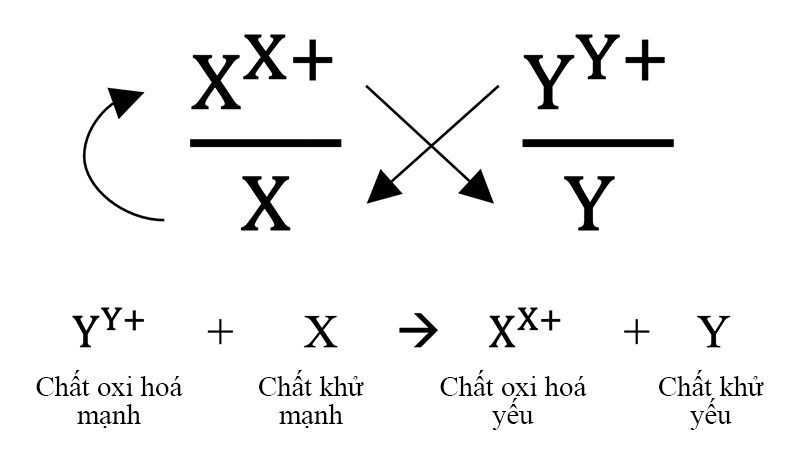
Câu 17 [1016537]: Kim loại nào sau đây không khử được ion Fe2+ thành Fe trong dung dịch? Biết Eo của cặp oxi hóa khử Fe2+/Fe là −0,44 V.
A, Zn (Eo = −0,76 V).
B, Cu (Eo = +0,34 V).
C, Al (Eo = −1,66 V).
D, Mg (Eo = −2,37 V).
Thế điện cực chuẩn của cặp oxi hóa – khử càng lớn thì tính khử của dạng khử càng yếu, tính oxi hóa của dạng oxi hóa càng mạnh và ngược lại.
Nguyên tắc chung: Chất oxi hóa mạnh hơn + Chất khử mạnh hơn Chất khử yếu hơn + Chất oxi hóa yếu hơn
→ Chất không khử được Fe2+ thành Fe là Cu.
⟹ Chọn đáp án B Đáp án: B
Nguyên tắc chung: Chất oxi hóa mạnh hơn + Chất khử mạnh hơn Chất khử yếu hơn + Chất oxi hóa yếu hơn
→ Chất không khử được Fe2+ thành Fe là Cu.
⟹ Chọn đáp án B Đáp án: B
Câu 18 [1016538]: Kim loại M có thế điện cực chuẩn là −0,20 V. Có thể dùng M để điều chế kim loại nào sau đây từ dung dịch muối chứa ion kim loại tương ứng?
A, Ni (Eo = -0,26V).
B, Fe (Eo = −0,44 V).
C, Zn (Eo = −0,76 V).
D, Ag (Eo = +0,80 V).
Kim loại M có Eo = –0,20 V
M sẽ khử được ion kim loại nào có Eo cao hơn M, vì khi đó phản ứng khử xảy ra tự phát.
Kim loại Ag có Eo = +0,80 cao hơn kim loại M có thể điều chế ion kim loại tương ứng.
⟹Chọn đáp án D Đáp án: D
M sẽ khử được ion kim loại nào có Eo cao hơn M, vì khi đó phản ứng khử xảy ra tự phát.
Kim loại Ag có Eo = +0,80 cao hơn kim loại M có thể điều chế ion kim loại tương ứng.
⟹Chọn đáp án D Đáp án: D
Câu 19 [824901]: Thế điện cực chuẩn 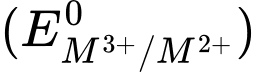 của các kim loại Cr, Mn, Fe và Co lần lượt là –0,408 V; 1,57 V; 0,771 V và 1,97 V. Kim loại nào thay đổi trạng thái oxi hóa từ +2 lên +3 dễ nhất?
của các kim loại Cr, Mn, Fe và Co lần lượt là –0,408 V; 1,57 V; 0,771 V và 1,97 V. Kim loại nào thay đổi trạng thái oxi hóa từ +2 lên +3 dễ nhất?
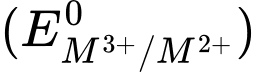 của các kim loại Cr, Mn, Fe và Co lần lượt là –0,408 V; 1,57 V; 0,771 V và 1,97 V. Kim loại nào thay đổi trạng thái oxi hóa từ +2 lên +3 dễ nhất?
của các kim loại Cr, Mn, Fe và Co lần lượt là –0,408 V; 1,57 V; 0,771 V và 1,97 V. Kim loại nào thay đổi trạng thái oxi hóa từ +2 lên +3 dễ nhất? A, Cr.
B, Mn.
C, Fe.
D, Co.
So sánh các giá trị thế điện cực chuẩn, ta thấy Cr có thế điện cực chuẩn thấp nhất (-0,408 V).
Điều này có nghĩa là Cr2+ dễ dàng nhường electron nhất để trở thành Cr3+.
Vậy, kim loại dễ thay đổi trạng thái oxi hóa từ +2 lên +3 nhất là Cr.
⟹ Chọn đáp án A Đáp án: A
Điều này có nghĩa là Cr2+ dễ dàng nhường electron nhất để trở thành Cr3+.
Vậy, kim loại dễ thay đổi trạng thái oxi hóa từ +2 lên +3 nhất là Cr.
⟹ Chọn đáp án A Đáp án: A
Câu 20 [824902]: Phản ứng X + Y2+ → X2+ + Y sẽ tự xảy ra nếu X và Y lần lượt là các chất nào sau đây?
A, Sn và Fe.
B, Mg và Zn.
C, Fe và Mg.
D, Sn và Zn.
Để phản ứng X + Y2+ → X2+ + Y xảy ra tự phát, X phải là chất khử mạnh hơn Y2+. Điều này có nghĩa là thế điện cực chuẩn của cặp X2+/X phải nhỏ hơn thế điện cực chuẩn của cặp Y2+/Y.
Thế điện cực chuẩn của các cặp oxi hóa - khử
Eo Sn2+/Sn = -0,14V
Eo Mg2+/Mg = -2,37V
Eo Fe2+/Fe = -0,44V
Eo Zn2+/Zn = -0,76V
Phân tích các đáp án:
❌A. Sn và Fe. Ta có Eo Sn2+/Sn > Eo Fe2+/Fe (-0,14 > -0,44) . Phản ứng không tự xảy ra theo chiều tự phát.
✔️B. Mg và Zn. Ta có Eo Mg2+/Mg > Eo Zn2+/Zn (-2,37 < -0,76). Phản ứng tự xảy ra theo chiều tự phát.
❌C. Fe và Mg. Ta có Eo Fe2+/Fe > Eo Mg2+/Mg ( -0,44 > -2,37). Phản ứng không tự xảy ra theo chiều tự phát.
❌D. Sn và Zn. Ta có Eo Sn2+/Sn > Eo Zn2+/Zn (-0,14 > -0,76). Phản ứng không tự xảy ra theo chiều tự phát.
⟹ Chọn đáp án B Đáp án: B
Thế điện cực chuẩn của các cặp oxi hóa - khử
Eo Sn2+/Sn = -0,14V
Eo Mg2+/Mg = -2,37V
Eo Fe2+/Fe = -0,44V
Eo Zn2+/Zn = -0,76V
Phân tích các đáp án:
❌A. Sn và Fe. Ta có Eo Sn2+/Sn > Eo Fe2+/Fe (-0,14 > -0,44) . Phản ứng không tự xảy ra theo chiều tự phát.
✔️B. Mg và Zn. Ta có Eo Mg2+/Mg > Eo Zn2+/Zn (-2,37 < -0,76). Phản ứng tự xảy ra theo chiều tự phát.
❌C. Fe và Mg. Ta có Eo Fe2+/Fe > Eo Mg2+/Mg ( -0,44 > -2,37). Phản ứng không tự xảy ra theo chiều tự phát.
❌D. Sn và Zn. Ta có Eo Sn2+/Sn > Eo Zn2+/Zn (-0,14 > -0,76). Phản ứng không tự xảy ra theo chiều tự phát.
⟹ Chọn đáp án B Đáp án: B
Câu 21 [560424]: Cho phương trình hóa học phản ứng: Fe + 3Ag+  Fe3+ + 3Ag.
Fe3+ + 3Ag.
Nhận xét nào sau đây về phản ứng trên là đúng?
 Fe3+ + 3Ag.
Fe3+ + 3Ag. Nhận xét nào sau đây về phản ứng trên là đúng?
A, Fe3+ là chất khử, Ag+ là chất oxi hóa.
B, Ag+ là chất khử, Fe3+ là chất oxi hóa.
C, Fe là chất khử, Ag+ là chất oxi hóa.
D, Fe là chất oxi hóa, Ag+ là chất khử.
Fe là chất khử vì số oxi hoá tăng (từ 0 lên +3)
Ag+ là chất oxi hoá vì số oxi hoá giảm (từ +1 xuống 0) Đáp án: C
Ag+ là chất oxi hoá vì số oxi hoá giảm (từ +1 xuống 0) Đáp án: C
Câu 22 [560425]: Cho phương trình hóa học phản ứng: 2Cr + 3Sn2+  2Cr3+ + 3Sn.
2Cr3+ + 3Sn.
Nhận xét nào sau đây về phản ứng trên là đúng?
 2Cr3+ + 3Sn.
2Cr3+ + 3Sn. Nhận xét nào sau đây về phản ứng trên là đúng?
A, Cr3+ là chất khử, Sn2+ là chất oxi hóa.
B, Sn2+ là chất khử, Cr3+ là chất oxi hóa.
C, Cr là chất khử, Sn2+ là chất oxi hóa.
D, Cr là chất oxi hóa, Sn2+ là chất khử.
Cr là chất khử vì số oxi hoá tăng (từ 0 lên +3)
Sn2+ là chất oxi hoá vì số oxi hoá giảm (từ +2 xuống 0) Đáp án: C
Sn2+ là chất oxi hoá vì số oxi hoá giảm (từ +2 xuống 0) Đáp án: C
Câu 23 [560426]: Cho các cặp oxi hoá - khử được sắp xếp theo chiều tăng dần tính oxi hoá của dạng oxi hóa như sau: Fe2+/Fe, Cu2+/Cu, Fe3+/Fe2+. Phát biểu nào sau đây là đúng?
A, Fe2+ oxi hóa được Cu thành Cu2+.
B, Cu2+ oxi hoá được Fe2+ thành Fe3+.
C, Fe3+ oxi hóa được Cu thành Cu2+.
D, Cu khử được Fe3+ thành Fe.
A. Sai. Fe2+ không oxi hóa được Cu thành Cu2+
B. Sai. Cu2+ không oxi hóa được Fe2+ thành Fe3+ do có tính oxi hóa yếu hơn Fe3+
C. Đúng. Fe3+ oxi hóa được Cu thành Cu2+
D. Sai. Cu chỉ khử được Fe3+ xuống Fe2+
Đáp án: C
B. Sai. Cu2+ không oxi hóa được Fe2+ thành Fe3+ do có tính oxi hóa yếu hơn Fe3+
C. Đúng. Fe3+ oxi hóa được Cu thành Cu2+
D. Sai. Cu chỉ khử được Fe3+ xuống Fe2+
Đáp án: C
Câu 24 [560427]: Chromium (Cr) thường được sử dụng để mạ lên kim loại do Cr tạo được lớp phủ sáng bóng. Hãy cho biết thiết bị kim loại được mạ Cr có không bền trong môi trường dung dịch chất nào sau đây? Cho biết thế điện cực chuẩn của cặp Cr2+/Cr là –0,910 V và các cặp Fe2+/Fe; Mg2+/Mg; Na+/Na; Al3+/Al tương ứng là –0,44 V; –2,37 V; –2,71 V; –1,66 V.
A, Fe(NO3)2.
B, Mg(NO3)2.
C, NaNO3.
D, Al(NO3)2.
Thế điện cực của cặp Fe2+/Fe lớn hơn cặp Cr2+/Cr nên Fe sẽ đứng sau Cr trong dãy hoạt động hóa học của kim loại
⇒ Có phản ứng Cr + Fe(NO3)2 → Cr(NO3)2 + Fe Đáp án: A
⇒ Có phản ứng Cr + Fe(NO3)2 → Cr(NO3)2 + Fe Đáp án: A
Câu 25 [560428]: Cho bán phản ứng và giá trị thế điện cực chuẩn như sau:
Chất nào có tính oxi hóa mạnh nhất trong bảng trên?
Chất nào có tính oxi hóa mạnh nhất trong bảng trên?
A, Co3+.
B, Cr3+.
C, Fe3+.
D, S2O82–.
Chất có tính oxi hoá mạnh nhất trong bảng trên là S2O82– vì nó có thế điện cực chuẩn lớn nhất. Đáp án: D
Câu 26 [1016539]: Một học sinh tiến hành thí nghiệm: Nhúng một thanh đồng vào dung dịch AgNO3, sau một lúc nhúng tiếp một thanh sắt vào dung dịch này đến phản ứng hoàn toàn. Sau khi thí nghiệm kết thúc, học sinh đó rút ra các kết luận sau:
(a) Dung dịch thu được sau phản ứng có màu xanh nhạt.
(b) Khối lượng thanh đồng bị giảm sau phản ứng.
(c) Khối lượng thanh sắt tăng lên sau phản ứng.
Số nhận định không đúng là
(a) Dung dịch thu được sau phản ứng có màu xanh nhạt.
(b) Khối lượng thanh đồng bị giảm sau phản ứng.
(c) Khối lượng thanh sắt tăng lên sau phản ứng.
Số nhận định không đúng là
A, 0.
B, 1.
C, 2.
D, 3.
Nhúng một thanh đồng vào dung dịch AgNO3
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
sau một lúc nhúng tiếp một thanh sắt vào dung dịch này đến phản ứng hoàn toàn.
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu
Phân tích các nhận định:
✔️(a) – Đúng. Dung dịch thu được sau phản ứng có màu xanh nhạt, trong dung dịch có muối Fe(NO3)2 nên có màu xanh nhạt.
❌(b) – Sai. Sau phản ứng có Ag (M = 108 amu) bám vào thanh đồng Cu (M = 64 amu) nên khối lượng của thanh đồng tăng lên.
✔️(c) – Đúng. Khối lượng thanh sắt tăng lên sau phản ứng nguyên do Cu và Ag bám lên lên thanh Fe.
Số nhận định không đúng là: 1
⟹ Chọn đáp án B
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
sau một lúc nhúng tiếp một thanh sắt vào dung dịch này đến phản ứng hoàn toàn.
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu
Phân tích các nhận định:
✔️(a) – Đúng. Dung dịch thu được sau phản ứng có màu xanh nhạt, trong dung dịch có muối Fe(NO3)2 nên có màu xanh nhạt.
❌(b) – Sai. Sau phản ứng có Ag (M = 108 amu) bám vào thanh đồng Cu (M = 64 amu) nên khối lượng của thanh đồng tăng lên.
✔️(c) – Đúng. Khối lượng thanh sắt tăng lên sau phản ứng nguyên do Cu và Ag bám lên lên thanh Fe.
Số nhận định không đúng là: 1
⟹ Chọn đáp án B
Câu 27 [1016540]: Cho hỗn hợp Zn và Fe vào dung dịch hỗn hợp Cu(NO3)2 và AgNO3, sau khi các phản ứng xảy ra hoàn toàn thu được hỗn hợp hai kim loại. Hai kim loại đó là
A, Fe, Cu.
B, Cu, Ag.
C, Zn, Ag.
D, Fe, Ag.
Cho hỗn hợp Zn và Fe vào dung dịch hỗn hợp Cu(NO3)2 và AgNO3, sau khi các phản ứng xảy ra hoàn toàn thu được hỗn hợp hai kim loại.
Fe và Zn đều mạnh hơn Cu và Ag mà sau phản ứng thu được 2 kim loại.
→ Hai kim loại thu được là Cu, Ag.
Fe và Zn đều mạnh hơn Cu và Ag mà sau phản ứng thu được 2 kim loại.
→ Hai kim loại thu được là Cu, Ag.
⟹ Chọn đáp án B
Đáp án: B
Câu 28 [705733]: Thế điện cực chuẩn của các cặp Cu2+/Cu, Zn2+/Zn, Sn2+/Sn và Ag+/Ag lần lượt là 0,340 V; –0,763 V; –0,138 V và 0,799 V. Phát biểu nào sau đây là đúng?
A, Thùng bằng kẽm có thể dùng để chứa dung dịch CuSO4.
B, Thùng bằng kẽm có thể dùng để chứa dung dịch AgNO3.
C, Thùng bằng thiếc (Sn) có thể dùng để chứa dung dịch AgNO3.
D, Thùng bằng bạc có thể dùng để chứa dung dịch CuSO4.
Phân tích các đáp án:
❌A – Sai. Thùng bằng kẽm không thể dùng để chứa dung dịch CuSO4. Do Zn có tính khử mạnh hơn Cu nên sẽ có phản ứng hóa học làm thùng kẽm bị ăn mòn dần.
Zn + CuSO4 → ZnSO4 + Cu
❌B – Sai. Thùng bằng kẽm không thể dùng để chứa dung dịch AgNO3. Do Zn có tính khử mạnh hơn Ag nên sẽ có phản ứng hóa học làm thùng kẽm bị ăn mòn dần.
Zn + 2AgNO3 → Zn(NO3)2 + 2Ag
❌C – Sai. Thùng bằng thiếc (Sn) không thể dùng để chứa dung dịch AgNO3. Do Sn có tính khử mạnh hơn Ag nên sẽ có phản ứng hóa học làm thùng thiếc bị ăn mòn dần.
Sn + 2AgNO3 → Sn(NO3)2 + 2Ag
✔️D – Đúng. Thùng bằng bạc (Ag) có thể dùng để chứa dung dịch CuSO4. Do Ag có tính khử yếu hơn Cu nên không có phản ứng hóa học với dung dịch CuSO4
⟹Chọn đáp án D Đáp án: D
❌A – Sai. Thùng bằng kẽm không thể dùng để chứa dung dịch CuSO4. Do Zn có tính khử mạnh hơn Cu nên sẽ có phản ứng hóa học làm thùng kẽm bị ăn mòn dần.
Zn + CuSO4 → ZnSO4 + Cu
❌B – Sai. Thùng bằng kẽm không thể dùng để chứa dung dịch AgNO3. Do Zn có tính khử mạnh hơn Ag nên sẽ có phản ứng hóa học làm thùng kẽm bị ăn mòn dần.
Zn + 2AgNO3 → Zn(NO3)2 + 2Ag
❌C – Sai. Thùng bằng thiếc (Sn) không thể dùng để chứa dung dịch AgNO3. Do Sn có tính khử mạnh hơn Ag nên sẽ có phản ứng hóa học làm thùng thiếc bị ăn mòn dần.
Sn + 2AgNO3 → Sn(NO3)2 + 2Ag
✔️D – Đúng. Thùng bằng bạc (Ag) có thể dùng để chứa dung dịch CuSO4. Do Ag có tính khử yếu hơn Cu nên không có phản ứng hóa học với dung dịch CuSO4
⟹Chọn đáp án D Đáp án: D
Câu 29 [706204]: Một kim loại X được nhúng qua một dung dịch chứa ion Ym+ 1 M ở 25 °C. Nếu giá trị thế điện cực chuẩn của các cặp oxi hoá – khử: Xn+/X > Ym+/Y. Phát biểu nào sau đây đúng?
A, Kim loại X khử được ion Ym+.
B, Kim loại X oxi hóa được ion Ym+.
C, Ion Xn+ khử được kim loại Y.
D, Ion Xn+ oxi hóa được kim loại Y.
Phân tích các đáp án:
Vì Xn+/X có thế điện cực chuẩn lớn hơn, nên Y có tính khử mạnh hơn X.
⟶ ion Xn+ dễ bị khử hơn ion Ym+
❌ A. Sai. Kim loại X không khử được ion Ym+
❌ B. Sai. Kim loại X có tính khử, không có tính oxi hóa.
❌ C. Sai. Ion Xn+ có tính oxi hóa, không có tính khử.
✔️ D. Đúng. Xn+ là chất oxi hóa, Ym+/Y có thế điện cực chuẩn nhỏ hơn, nên Y bị oxi hóa bởi Xn+.
⟹ Chọn đáp án D Đáp án: D
Vì Xn+/X có thế điện cực chuẩn lớn hơn, nên Y có tính khử mạnh hơn X.
⟶ ion Xn+ dễ bị khử hơn ion Ym+
❌ A. Sai. Kim loại X không khử được ion Ym+
❌ B. Sai. Kim loại X có tính khử, không có tính oxi hóa.
❌ C. Sai. Ion Xn+ có tính oxi hóa, không có tính khử.
✔️ D. Đúng. Xn+ là chất oxi hóa, Ym+/Y có thế điện cực chuẩn nhỏ hơn, nên Y bị oxi hóa bởi Xn+.
⟹ Chọn đáp án D Đáp án: D
Câu 30 [706255]: Một khí X ở 1 atm được sục qua một dung dịch chứa hỗn hợp Ym– 1 M và Zk– 1 M ở 25 °C. Nếu giá trị thế điện cực chuẩn của các cặp oxi hoá – khử X/Xn–, Y/Ym– và Z/Zk– xếp theo trật tự Z/Zk– > X/Xn– >Y/Ym–. Cho các phát biểu sau:
(a) X sẽ oxi hoá được Ym– nhưng không oxi hoá được Zk–.
(b) X sẽ oxi hoá được cả Ym– và Zk–.
(c) X sẽ oxi hoá được Zk– nhưng không oxi hoá được Ym–.
(d) X sẽ khử được cả Ym– và Zk–.
(e) Phản ứng giữa X và Ym– là phản ứng tự diễn biến.
Số phát biểu không đúng là
(a) X sẽ oxi hoá được Ym– nhưng không oxi hoá được Zk–.
(b) X sẽ oxi hoá được cả Ym– và Zk–.
(c) X sẽ oxi hoá được Zk– nhưng không oxi hoá được Ym–.
(d) X sẽ khử được cả Ym– và Zk–.
(e) Phản ứng giữa X và Ym– là phản ứng tự diễn biến.
Số phát biểu không đúng là
A, 1.
B, 2.
C, 3.
D, 4.
Ta có: Z/Zk– > X/Xn– >Y/Ym–
⟶Tính khử : Y > X > Z
⟶Tính oxi hóa : Zk– > Xn– > Ym–
Phân tích các phát biểu:
✔️(a) ĐÚNG. Vì X/Xn- > Y/Ym-, X có thể oxi hóa Ym-. Vì Z/Zk- > X/Xn-, X không thể oxi hóa Zk-.
⟶Tính khử : Y > X > Z
⟶Tính oxi hóa : Zk– > Xn– > Ym–
Phân tích các phát biểu:
✔️(a) ĐÚNG. Vì X/Xn- > Y/Ym-, X có thể oxi hóa Ym-. Vì Z/Zk- > X/Xn-, X không thể oxi hóa Zk-.
❌(b) SAI. Như đã phân tích ở trên, X không thể oxi hóa Zk-.
❌(c) SAI. X không oxi hóa được Zk-.
❌(d) SAI. X khử được Z nhưng không
✔️(e) ĐÚNG. Vì X có thể oxi hóa Ym-, phản ứng này tự diễn biến.
Các phát biểu (b), (c), (d) là các phát biểu không đúng.
⟹ Chọn đáp án C
Dạng 2: TRẮC NGHIỆM ĐÚNG SAI – mỗi ý a), b), c), d) chọn đúng hoặc sai.
Câu 31 [1016541]: Thế điện cực chuẩn của hai cặp oxi hóa Cu2+/Cu là 0,34 V và Al3+/Al là −1,66 V. Một học sinh tiến hành thí nghiệm cho một chiếc thìa làm bằng đồng khuấy vào cốc chứa dung dịch aluminium nitrate.
Thế điện cực chuẩn của hai cặp oxi hóa Cu2+/Cu là 0,34 V và Al3+/Al là −1,66 V.
Tiến hành thí nghiệm cho một chiếc thìa làm bằng đồng khuấy vào cốc chứa dung dịch aluminium nitrate.
→ Cu không phản ứng với Al3+.
Phân tích các phát biểu:
❌(a) – Sai. Chiếc thìa bằng đồng vẫn giữ nguyên.
❌(b) – Sai. Không xảy ra phản ứng, nên dưới đáy cốc không xuất hiện kim loại màu nâu.
❌(c) – Sai. Không xảy ra phản ứng, nên dung dịch aluminium nitrate không chuyển sang màu xanh.
✔️(d) – Đúng. Không có hiện tượng hóa học xảy ra.
Tiến hành thí nghiệm cho một chiếc thìa làm bằng đồng khuấy vào cốc chứa dung dịch aluminium nitrate.
→ Cu không phản ứng với Al3+.
Phân tích các phát biểu:
❌(a) – Sai. Chiếc thìa bằng đồng vẫn giữ nguyên.
❌(b) – Sai. Không xảy ra phản ứng, nên dưới đáy cốc không xuất hiện kim loại màu nâu.
❌(c) – Sai. Không xảy ra phản ứng, nên dung dịch aluminium nitrate không chuyển sang màu xanh.
✔️(d) – Đúng. Không có hiện tượng hóa học xảy ra.
Câu 32 [704305]: Khả năng hoạt động hóa học của hai kim loại có thể được so sánh thông quá thí nghiệm như sau:
Bước 1: Chuẩn bị một đinh sắt đã được đánh sạch bề mặt, một dung dịch copper(II) sulfate 1 M được đựng trong cốc thuỷ tinh.
Bước 2: Cho đinh sắt vào cốc thuỷ tinh chứa dung dịch copper(II) sulfate 1 M. Sau khoảng 10 phút thì quan sát hiện tượng.
Bước 1: Chuẩn bị một đinh sắt đã được đánh sạch bề mặt, một dung dịch copper(II) sulfate 1 M được đựng trong cốc thuỷ tinh.
Bước 2: Cho đinh sắt vào cốc thuỷ tinh chứa dung dịch copper(II) sulfate 1 M. Sau khoảng 10 phút thì quan sát hiện tượng.
Fe + CuSO4 → FeSO4 + Cu
Quá trình oxi hóa Fe → Fe2+ + 2e
Quá trình khử Cu2+ + 2e → Cu
Phân tích các phát biểu:
✔️ (a) Đúng. Sau phản ứng sinh ra kim loại Cu màu nâu bám trên đinh sắt.
❌ (b) Sai. Sau phản ứng sinh ra kim loại Cu nên nồng độ của Cu2+ giảm dần.
❌ (c) Sai. Thế khử chuẩn của Fe2+/Fe nhỏ hơn thế khử chuẩn của Cu2+/Cu, Eo Mn+/M càng lớn thì tính oxi hóa của Mn+ càng mạnh; tính khử của M càng yếu
✔️ (d) Đúng. Từ hiện tượng ta thấy được Fe đã chiếm vị trí của Cu trong muối, Fe có độ hoạt động mạnh hơn Cu.
Quá trình oxi hóa Fe → Fe2+ + 2e
Quá trình khử Cu2+ + 2e → Cu
Phân tích các phát biểu:
✔️ (a) Đúng. Sau phản ứng sinh ra kim loại Cu màu nâu bám trên đinh sắt.
❌ (b) Sai. Sau phản ứng sinh ra kim loại Cu nên nồng độ của Cu2+ giảm dần.
❌ (c) Sai. Thế khử chuẩn của Fe2+/Fe nhỏ hơn thế khử chuẩn của Cu2+/Cu, Eo Mn+/M càng lớn thì tính oxi hóa của Mn+ càng mạnh; tính khử của M càng yếu
✔️ (d) Đúng. Từ hiện tượng ta thấy được Fe đã chiếm vị trí của Cu trong muối, Fe có độ hoạt động mạnh hơn Cu.
Câu 33 [560432]: Hãy xem xét bảng thế điện cực chuẩn sau đây:


Nếu thế điện cực chuẩn càng lớn thì:
- Tính oxi hoá của ion Mn+ càng mạnh.
- Tính khử của kim loại M càng yếu.
Phân tích các phát biểu:
✔️ a. Đúng. Ion có tính oxi hóa mạnh nhất là A+(aq) do có thế điện cực chuẩn lớn nhất.
❌ b. Sai. Ion có tính oxi hóa yếu nhất là D3+(aq) do có thế điện cực chuẩn nhỏ nhất.
❌ c. Sai. Chất có tính khử mạnh nhất là D(s) do có thế điện cực chuẩn nhỏ nhất.
❌ d. Sai. D3+(aq) không thể oxi hoá C2+(aq) do có thế điện cực nhỏ hơn nên tính oxi hoá yếu hơn.
- Tính oxi hoá của ion Mn+ càng mạnh.
- Tính khử của kim loại M càng yếu.
Phân tích các phát biểu:
✔️ a. Đúng. Ion có tính oxi hóa mạnh nhất là A+(aq) do có thế điện cực chuẩn lớn nhất.
❌ b. Sai. Ion có tính oxi hóa yếu nhất là D3+(aq) do có thế điện cực chuẩn nhỏ nhất.
❌ c. Sai. Chất có tính khử mạnh nhất là D(s) do có thế điện cực chuẩn nhỏ nhất.
❌ d. Sai. D3+(aq) không thể oxi hoá C2+(aq) do có thế điện cực nhỏ hơn nên tính oxi hoá yếu hơn.
Câu 34 [560434]: Cho danh sách thế điện chuẩn cực sau:
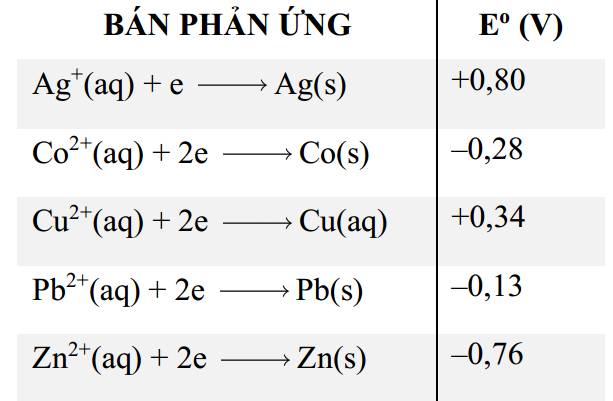

Nếu thế điện cực chuẩn càng lớn thì:
- Tính oxi hoá của ion Mn+ càng mạnh.
- Tính khử của kim loại M càng yếu.
Phân tích các phát biểu:
❌ a. Sai. Kim loại có tính khử mạnh nhất là Zn.
❌ b. Sai. Zn 2+ không dễ bị oxi hóa, mà kim loại Zn dễ bị oxi hóa (do E thấp nhất). Vì vậy, câu này sai.
✔️ c. Đúng. Kim loại Ag khó bị oxi hóa nhất do có tính khử yếu nhất.
❌ d. Sai. Có 4 kim loại trong dãy phản ứng được với ion Ag+ do cả 4 kim loại đều có thế điện cực nhỏ hơn Ag.
- Tính oxi hoá của ion Mn+ càng mạnh.
- Tính khử của kim loại M càng yếu.
Phân tích các phát biểu:
❌ a. Sai. Kim loại có tính khử mạnh nhất là Zn.
❌ b. Sai. Zn 2+ không dễ bị oxi hóa, mà kim loại Zn dễ bị oxi hóa (do E thấp nhất). Vì vậy, câu này sai.
✔️ c. Đúng. Kim loại Ag khó bị oxi hóa nhất do có tính khử yếu nhất.
❌ d. Sai. Có 4 kim loại trong dãy phản ứng được với ion Ag+ do cả 4 kim loại đều có thế điện cực nhỏ hơn Ag.
Câu 35 [560436]: Danh sách dưới đây cho biết thế điện cực chuẩn của năm bán phản ứng:
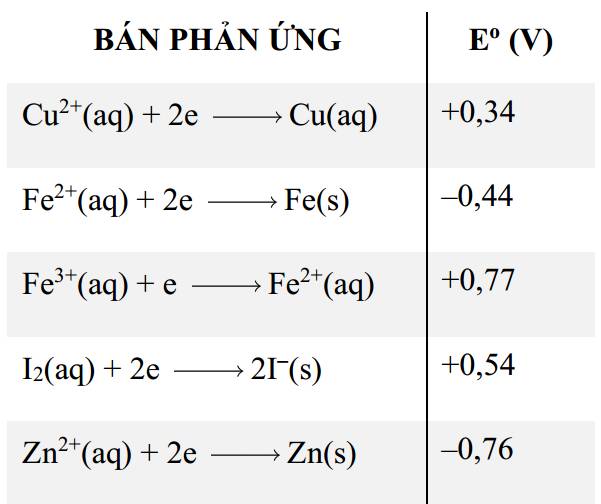

Phân tích các phát biểu:
❌ a. Sai. Ion kim loại có tính oxi hóa mạnh nhất danh sách là Fe3+ do có thế điện cực chuẩn lớn nhất.
✔️ b. Đúng. Kẽm (Zn) dễ bị oxi hóa nhất trong danh sách các chất.
✔️ c. Đúng. I2 có thể phản ứng được với tất cả các kim loại có trong danh sách.
✔️ d. Đúng. Một phản ứng theo chiều tự diễn biến từ các cặp oxi hóa - khử trên là 2Fe3+ + 2I– ⟶ 2Fe2+ + I2.
❌ a. Sai. Ion kim loại có tính oxi hóa mạnh nhất danh sách là Fe3+ do có thế điện cực chuẩn lớn nhất.
✔️ b. Đúng. Kẽm (Zn) dễ bị oxi hóa nhất trong danh sách các chất.
✔️ c. Đúng. I2 có thể phản ứng được với tất cả các kim loại có trong danh sách.
✔️ d. Đúng. Một phản ứng theo chiều tự diễn biến từ các cặp oxi hóa - khử trên là 2Fe3+ + 2I– ⟶ 2Fe2+ + I2.
Câu 36 [560437]: Cho giá trị thế điện cực chuẩn của các cặp oxi hóa khử như bằng sau:
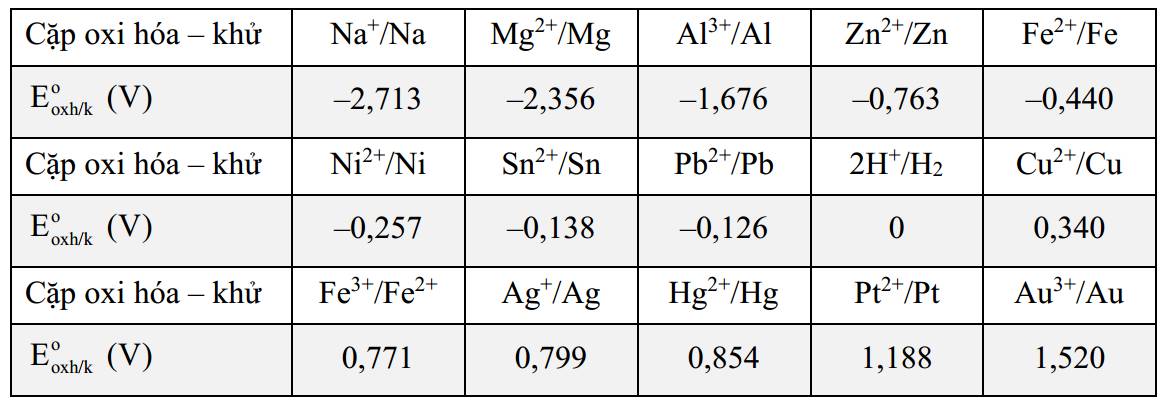

Phân tích các phát biểu:
❌ a. Sai. Cu2+ có tính oxi hoá yếu hơn Fe3+ và Cu có tính khử mạnh hơn Fe2+.
✔️ b. Đúng. Zn có tính khử mạnh hơn Pb và Zn2+ có tính oxi hoá yếu hơn Pb2+.
✔️ c. Đúng. Những kim loại có thế điện cực chuẩn âm đều khử được H+ thành H2 và phản ứng được trong dung dịch HCl.
✔️ d. Đúng. Kẽm có thể khử các ion Fe2+ và Ni2+ về kim loại Fe và Ni nhưng không thể khử ion Al3+ về kim loại Al.
❌ a. Sai. Cu2+ có tính oxi hoá yếu hơn Fe3+ và Cu có tính khử mạnh hơn Fe2+.
✔️ b. Đúng. Zn có tính khử mạnh hơn Pb và Zn2+ có tính oxi hoá yếu hơn Pb2+.
✔️ c. Đúng. Những kim loại có thế điện cực chuẩn âm đều khử được H+ thành H2 và phản ứng được trong dung dịch HCl.
✔️ d. Đúng. Kẽm có thể khử các ion Fe2+ và Ni2+ về kim loại Fe và Ni nhưng không thể khử ion Al3+ về kim loại Al.
Câu 37 [560438]: Cho các cặp oxi hoá - khử: Al3+/Al; Cr3+/Cr; Co2+/Co; Sn4+/Sn2+; Sn2+/Sn và Cl2(g)/2Cl– với các thế khử chuẩn lần lượt là –1,676 V; –0,740 V; –0,280 V; 0,150 V; –0,14 V và 1,360 V.
Phân tích các phát biểu:
❌ a. Sai. Al, Cr và Sn đều có thế điện cực chuẩn nhỏ hơn 0 nên sẽ tham gia phản ứng với dung dịch HCl, khử H+ (trong HCl) thành H2.
✔️ b. Đúng. Chất có tính oxi hoá mạnh nhất là Cl2.
❌ c. Sai. Chất có khả năng khử Cr3+(aq) thành Cr(s) ở điều kiện chuẩn là Al.
✔️ d. Đúng. Chất có khả năng khử Sn4+(aq) thành Sn2+(aq) nhưng không khử được Cr2+(aq) thành Cr(s) ở điều kiện chuẩn là Co.
❌ a. Sai. Al, Cr và Sn đều có thế điện cực chuẩn nhỏ hơn 0 nên sẽ tham gia phản ứng với dung dịch HCl, khử H+ (trong HCl) thành H2.
✔️ b. Đúng. Chất có tính oxi hoá mạnh nhất là Cl2.
❌ c. Sai. Chất có khả năng khử Cr3+(aq) thành Cr(s) ở điều kiện chuẩn là Al.
✔️ d. Đúng. Chất có khả năng khử Sn4+(aq) thành Sn2+(aq) nhưng không khử được Cr2+(aq) thành Cr(s) ở điều kiện chuẩn là Co.
Dạng 3: TRẮC NGHIỆM YÊU CẦU TRẢ LỜI NGẮN
Câu 38 [560439]: Cho từng kim loại: Na, Ba, Fe, Mg, Cu vào dung dịch Fe2(SO4)3. Có bao nhiêu kim loại tham gia phản ứng khử ion Fe3+?
Để kim loại khử được Fe3+ thì thế điện cực chuẩn Eo của phản ứng oxi hóa kim loại đó phải nhỏ hơn Eo của Fe3+/Fe2+.
Các kim loại có thể khử ion Fe3+ trong dung dịch Fe2(SO4)3 là Cu, Fe và Mg.
Các kim loại mạnh như K, Ba, Ca, Na khi trong dung dịch đầu tiên sẽ hản ứng với H2O tạo dung dịch kiềm trước, sau đó dung dịch kiềm mới phản ứng với dung dịch muối, đây chỉ là phản ứng trao đổi chứ không phải phản oxi hóa-khử nên ko có quá trình oxi hoá-khử.
⇒ Điền đáp án: 3
Các kim loại có thể khử ion Fe3+ trong dung dịch Fe2(SO4)3 là Cu, Fe và Mg.
Các kim loại mạnh như K, Ba, Ca, Na khi trong dung dịch đầu tiên sẽ hản ứng với H2O tạo dung dịch kiềm trước, sau đó dung dịch kiềm mới phản ứng với dung dịch muối, đây chỉ là phản ứng trao đổi chứ không phải phản oxi hóa-khử nên ko có quá trình oxi hoá-khử.
⇒ Điền đáp án: 3
Câu 39 [704000]: Kim loại không tan trong nước và có giá trị thế điện cực chuẩn nhỏ hơn thường tác dụng được với dung dịch muối của kim loại có giá trị thế điện cực chuẩn lớn hơn ở điều kiện chuẩn.  Kim loại Fe có thể phản ứng với dung dịch muối CuSO4. Để kiểm tra tính chất này, một nhóm học sinh đã tiến hành các bước thí nghiệm kiểm chứng như sau:
Kim loại Fe có thể phản ứng với dung dịch muối CuSO4. Để kiểm tra tính chất này, một nhóm học sinh đã tiến hành các bước thí nghiệm kiểm chứng như sau:
(1) Sau đó, làm sạch một chiếc đinh sắt.
(2) Cho lượng muối CuSO4. 5H2O thích hợp vào nước để tạo thành dung dịch CuSO4 1 M.
(3) Cho đinh sắt vào cốc thuỷ tinh chứa dung dịch CuSO4 1 M.
(4) Sau một thời gian, kim loại Cu sinh ra sẽ hình thành một lớp kim loại màu nâu bám trên đinh sắt.
Hãy gắn số thứ tự các bước theo trình tự dãy bốn số để thực hiện thí nghiệm trên (ví dụ: 1234, 4321, ...).
 Kim loại Fe có thể phản ứng với dung dịch muối CuSO4. Để kiểm tra tính chất này, một nhóm học sinh đã tiến hành các bước thí nghiệm kiểm chứng như sau:
Kim loại Fe có thể phản ứng với dung dịch muối CuSO4. Để kiểm tra tính chất này, một nhóm học sinh đã tiến hành các bước thí nghiệm kiểm chứng như sau:(1) Sau đó, làm sạch một chiếc đinh sắt.
(2) Cho lượng muối CuSO4. 5H2O thích hợp vào nước để tạo thành dung dịch CuSO4 1 M.
(3) Cho đinh sắt vào cốc thuỷ tinh chứa dung dịch CuSO4 1 M.
(4) Sau một thời gian, kim loại Cu sinh ra sẽ hình thành một lớp kim loại màu nâu bám trên đinh sắt.
Hãy gắn số thứ tự các bước theo trình tự dãy bốn số để thực hiện thí nghiệm trên (ví dụ: 1234, 4321, ...).
Các bước tiến hành thí nghiệm diễn ra như sau:
Bước 1: Cho lượng muối CuSO4.5H2O thích hợp vào nước tạo thành dung dịch CuSO4 1M → ứng với (2)
Bước 2: Sau đó, làm sạch 1 chiếc đinh sắt. → ứng với (1)
Bước 3: Cho đinh sắt vào cốc thủy tinh chứa dung dịch CuSO4 1M → ứng với (3)
Bước 4: Sau một thời gian, kim loại Cu sinh ra sẽ hình thành một lớp kim loại màu nâu bám trên đinh sắt → ứng với (4)
Bước 1: Cho lượng muối CuSO4.5H2O thích hợp vào nước tạo thành dung dịch CuSO4 1M → ứng với (2)
Bước 2: Sau đó, làm sạch 1 chiếc đinh sắt. → ứng với (1)
Bước 3: Cho đinh sắt vào cốc thủy tinh chứa dung dịch CuSO4 1M → ứng với (3)
Bước 4: Sau một thời gian, kim loại Cu sinh ra sẽ hình thành một lớp kim loại màu nâu bám trên đinh sắt → ứng với (4)
Fe + CuSO4 ⟶ FeSO4 + Cu
⇒ Điền đáp án: 2134
Sử dụng thông tin ở bảng dưới đây để trả lời các câu 40 và câu 41
Cho bảng thế điện cực chuẩn của một số cặp oxi hóa – khử sau:
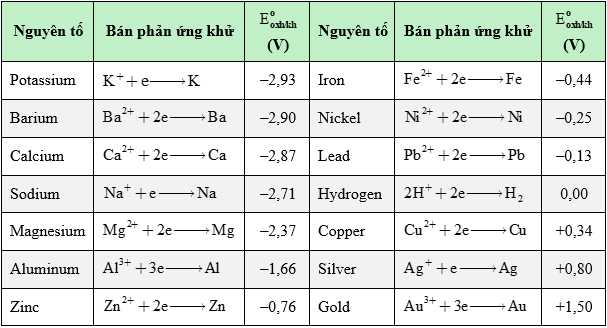

Câu 40 [1016542]: Có bao nhiêu kim loại trong bảng phản ứng được với dung dịch AgNO3 tạo thành kim loại Ag?
Thế điện cực chuẩn của cặp oxi hóa – khử càng lớn thì tính khử của dạng khử càng yếu, tính oxi hóa của dạng oxi hóa càng mạnh và ngược lại.
Nguyên tắc chung:
Chất oxi hóa mạnh hơn + Chất khử mạnh hơn ⟶ Chất khử yếu hơn + Chất oxi hóa yếu hơn
Các kim loại phản ứng với dung dịch AgNO3 tạo thành Ag là Mg; Al; Zn; Fe; Ni; Pb; Cu.
⟹ Điền đáp án 7
Nguyên tắc chung:
Chất oxi hóa mạnh hơn + Chất khử mạnh hơn ⟶ Chất khử yếu hơn + Chất oxi hóa yếu hơn
Các kim loại phản ứng với dung dịch AgNO3 tạo thành Ag là Mg; Al; Zn; Fe; Ni; Pb; Cu.
⟹ Điền đáp án 7
Câu 41 [1016543]: Có bao nhiêu kim loại trong bảng phản ứng được với dung dịch acid HCl tạo thành khí H2?
Thế điện cực chuẩn của cặp oxi hóa – khử càng lớn thì tính khử của dạng khử càng yếu, tính oxi hóa của dạng oxi hóa càng mạnh và ngược lại.
Nguyên tắc chung:
Chất oxi hóa mạnh hơn + Chất khử mạnh hơn ⟶ Chất khử yếu hơn + Chất oxi hóa yếu hơn
Các kim loại phản ứng với dung dịch HCl thu được khí H2 là K; Ba; Na; Ca; Mg; Al; Zn; Fe; Ni; Pb.
⟹ Điền đáp án 10
Nguyên tắc chung:
Chất oxi hóa mạnh hơn + Chất khử mạnh hơn ⟶ Chất khử yếu hơn + Chất oxi hóa yếu hơn
Các kim loại phản ứng với dung dịch HCl thu được khí H2 là K; Ba; Na; Ca; Mg; Al; Zn; Fe; Ni; Pb.
⟹ Điền đáp án 10
Dạng 4: BÀI TẬP ĐỌC HIỂU – đọc thông tin và trả lời các câu hỏi sau đó
PHẢN ỨNG OXI HÓA KHỬ
Phản ứng oxi hóa khử là phản ứng hóa học trong đó các electron được chuyển từ chất phản ứng này sang chất phản ứng khác. Ví dụ: nếu ta cho một miếng kim loại zinc (kẽm – Zn) vào dung dịch chứa ion copper (đồng – Cu) thì phản ứng sau sẽ xảy ra:Zn(s) + Cu2+(aq) → Zn2+(aq) + Cu(s).
Phản ứng này được thể hiện trên hình bên. Trong quá trình này, các nguyên tử kẽm bị oxi hóa (chúng mất electron) và các ion đồng bị khử (chúng thu được electron). Mỗi nguyên tử kẽm mất đi hai electron để trở thành ion kẽm,
Zn(s) → Zn2+(aq) + 2e.
và mỗi ion đồng nhận thêm hai electron để trở thành nguyên tử đồng.
Cu2+(aq) + 2e → Cu(s).
Tổng của hai nửa phương trình phản ứng là phương trình tổng thể của phản ứng oxi hóa khử:
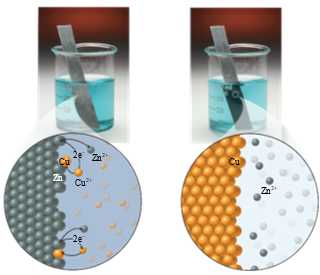
Quá trình oxi hóa kẽm trong dung dịch copper(II) sulfate.

Để một quá trình nhận được electron thì quá trình khác phải mất đi electron. Quá trình oxi hóa là quá trình mất đi electron. Quá trình ngược lại, quá trình nhận electron, được gọi là quá trình khử. Trong phản ứng của Zn với Cu2+, Zn được gọi là chất khử vì nó cho electron làm Cu2+ bị khử. Cu2+ được gọi là chất oxi hóa vì nó nhận electron nên Zn bị oxi hóa.
Câu 42 [382309]: Quá trình oxy hóa là quá trình
A, mất đi electron.
B, nhận lại electron.
C, chất phản ứng có số oxi hóa không đổi.
D, chất phản ứng có số oxi hóa giảm.
Quá trình oxi hóa là quá trình mất electron của một nguyên tử, ion hoặc phân tử, làm tăng số oxi hóa của nó.
Chọn đáp án A Đáp án: A
Chọn đáp án A Đáp án: A
Câu 43 [382310]: Trong phản ứng trên, nếu thay tấm kim loại kẽm (Zn) bằng tấm kim loại sắt (Fe) thì
A, Fe đóng vai trò là chất oxi hóa.
B, Cu2+ đóng vai trò là chất oxi hóa.
C, Fe sẽ nhường đi electron để hình thành Fe3+.
D, Cu sẽ nhường electron để hình thành Cu2+.
Zn + Cu2+ ⟶ Zn2+ + Cu
Cu có sự giảm số oxi hóa từ +2 xuống 0 ⟶ Cu2+ đóng vai trò là chất oxi hóa.
Chọn đáp án B Đáp án: B
Cu có sự giảm số oxi hóa từ +2 xuống 0 ⟶ Cu2+ đóng vai trò là chất oxi hóa.
Chọn đáp án B Đáp án: B
Câu 44 [382311]: Nhúng thanh kẽm vào dung dịch 100 mL CuSO4 aM. Sau khi phản ứng xảy ra hoàn toàn, lấy từ từ thanh kẽm ra bên ngoài, sấy khô và cân lại cẩn thận thanh kẽm. Các thông tin được ghi lại trong bảng sau:

Giả sử toàn bộ lượng kim loại sinh ra sẽ bám hoàn toàn trên thanh kẽm. Giá trị của a là

Giả sử toàn bộ lượng kim loại sinh ra sẽ bám hoàn toàn trên thanh kẽm. Giá trị của a là
A, 0,2 M.
B, 0,15 M.
C, 0,1 M.
D, 0,3 M.
Khối lượng thanh Zn thay đổi:
m sau - m trước = 0,778 - 0,793 = - 0,015g
⟶ Zn giảm do Zn tan vào dung dịch, Cu bám vào.
Zn + Cu2+ ⟶ Zn2+ + Cu
n Zn tan = n Cu bám
ta có: m ( Zn sau) = m (Zn trước) - m(Zn tan ) + m(Cu bám vào)
0,778 = 0,793 - 65n + 64n
⟶ n = 0,015 mol
⟶ a = n : V = 0,015 : 0,1 = 0,15M
Chọn đáp án B Đáp án: B
m sau - m trước = 0,778 - 0,793 = - 0,015g
⟶ Zn giảm do Zn tan vào dung dịch, Cu bám vào.
Zn + Cu2+ ⟶ Zn2+ + Cu
n Zn tan = n Cu bám
ta có: m ( Zn sau) = m (Zn trước) - m(Zn tan ) + m(Cu bám vào)
0,778 = 0,793 - 65n + 64n
⟶ n = 0,015 mol
⟶ a = n : V = 0,015 : 0,1 = 0,15M
Chọn đáp án B Đáp án: B
KHẢ NĂNG HOẠT ĐỘNG HÓA HỌC CỦA KIM LOẠI
Khi thực hiện phản ứng cho kim loại sắt (Fe) vào dung dịch copper(II) chloride (CuCl2) thì xảy ra phản ứng hóa học được biểu diễn bằng phương trình sau:
Đây là một ví dụ về phản ứng oxi hóa khử. Sắt thay thế đồng trong dung dịch muối bằng cách oxi hóa từ Fe thành Fe2+. Đồng bị đẩy khỏi muối (và bị loại khỏi dung dịch) bằng cách khử từ Cu2+ thành Cu. Cloride (Cl−), chất không bị oxi hóa cũng không bị khử, đóng vai trò như là một ion quan sát trong phản ứng này.
Vậy điều gì sẽ xảy ra nếu cho kim loại đồng vào dung dịch chứa iron(II) chloride (FeCl2)? Liệu Cu(s) có bị oxi hóa thành Cu2+(aq) bởi Fe2+(aq) giống như cách Fe(s) bị oxi hóa thành Fe2+(aq) bởi Cu2+(aq) không? Câu trả lời là không. Trên thực tế, sẽ không có phản ứng nào xảy ra nếu chúng ta nhúng kim loại đồng vào dung dịch FeCl2.
Cu(s) + Fe2+(aq) → không phản ứng

Một số kim loại như đồng kém phản ứng đến mức chúng tồn tại trong tự nhiên ở đơn chất.
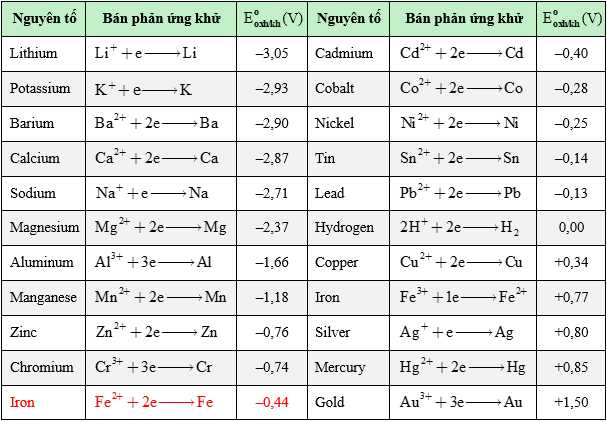
Dãy hoạt động hóa học của kim loại (bảng bên dưới) là danh sách các kim loại (và hydrogen) được sắp xếp từ trên xuống dưới theo chiều dễ bị oxi hóa giảm dần. Cột thứ hai và thứ năm hiển thị bán phản ứng khử tương ứng với từng nguyên tố trong cột đầu tiên. Lưu ý vị trí của sắt và đồng trong bảng. Sắt xuất hiện ở vị trí cao hơn trong bảng và do đó dễ bị oxi hóa hơn. Trên thực tế, một nguyên tố trong dãy sẽ bị oxi hóa bởi các ion của bất kỳ nguyên tố nào xuất hiện bên dưới nó. Do đó, theo kết quả của bảng, kim loại sắt sẽ bị oxi hóa bởi dung dịch chứa bất kỳ ion nào sau đây: Cr3+, Fe2+, Cd2+, Co2+, Ni2+, Sn2+, H+, Cu2+, Ag+, Hg2+, Pt2+, hoặc Au3+. Ngược lại, sắt sẽ không bị oxi hóa bởi dung dịch chứa các ion Mn2+, Al3+, Mg2+, Na+, Ca2+, Ba2+, K+, Li+.
Câu 45 [382315]: Trong phản ứng giữa kim loại Fe dung dịch CuCl2 ,
A, Fe đóng vai trò chất oxi hóa.
B, ion Cl– đóng vai trò là chất khử.
C, Cu đóng vai trò là ion quan sát.
D, ion Cu2+ đóng vai trò là chất oxi hóa.
Fe + Cu2+ ⟶ Fe2+ + Cu
Sắt (Fe) từ trạng thái 0 lên +2 (mất electron), nên bị oxi hóa → Fe là chất khử.
Ion Cu2+ từ +2 xuống 0 (nhận electron), nên bị khử → Cu 2+là chất oxi hóa.
⇒ Chọn đáp án D Đáp án: D
Sắt (Fe) từ trạng thái 0 lên +2 (mất electron), nên bị oxi hóa → Fe là chất khử.
Ion Cu2+ từ +2 xuống 0 (nhận electron), nên bị khử → Cu 2+là chất oxi hóa.
⇒ Chọn đáp án D Đáp án: D
Câu 46 [382316]: Dựa vào bảng trên, hãy cho biết kim loại thiếc Sn không phản ứng được với dung dịch chứa ion nào dưới đây?
A, Pb2+.
B, H+.
C, Ag+.
D, Co2+.
Vì Eo Co2+/Co < Eo Sn2+/Sn nên Co có tính khử mạnh hơn Sn.
⇒ Sn không phản ứng được với dung dịch chứa ion Co2+
⇒ Chọn đáp án D Đáp án: D
⇒ Sn không phản ứng được với dung dịch chứa ion Co2+
⇒ Chọn đáp án D Đáp án: D
Câu 47 [382317]: Dữ liệu cho thấy kết quả của sự kết hợp giữa kim loại và ion kim loại như sau:
Thí nghiệm 1: A(s) + D+(aq) →A+(aq) + D(s).
Thí nghiệm 2: C(s) + B+(aq) → C+(aq) + B(s).
Thí nghiệm 3: D(s) + B+(aq) → không phản ứng.
Thí nghiệm 4: C(s) + A+(aq) → không phản ứng.
Thí nghiệm 5: B(s) + E+(aq) → B+(aq) + E(s).
Thí nghiệm 6: D(s) + E+ (aq) → không có phản ứng.
Khả năng hoạt động hóa học đối với năm kim loại: A, B, C, D và E theo thứ tự giảm dần là
Thí nghiệm 1: A(s) + D+(aq) →A+(aq) + D(s).
Thí nghiệm 2: C(s) + B+(aq) → C+(aq) + B(s).
Thí nghiệm 3: D(s) + B+(aq) → không phản ứng.
Thí nghiệm 4: C(s) + A+(aq) → không phản ứng.
Thí nghiệm 5: B(s) + E+(aq) → B+(aq) + E(s).
Thí nghiệm 6: D(s) + E+ (aq) → không có phản ứng.
Khả năng hoạt động hóa học đối với năm kim loại: A, B, C, D và E theo thứ tự giảm dần là
A, A > C > B > E > D.
B, A > B > C > E > D.
C, D > C > B > E > A.
D, B > C > A > D > E.
Thí nghiệm 1: A(s) + D+(aq) → A+(aq) + D(s)
⟹ A có tính khử mạnh hơn D ⇒ A > D
Thí nghiệm 2: C(s) + B+(aq) → C+(aq) + B(s)
⟹ C có tính khử mạnh hơn B ⇒ C > B
Thí nghiệm 5: B(s) + E+(aq) → B+(aq) + E(s)
⟹ B có tính khử mạnh hơn E ⇒ B > E
Thí nghiệm 4: C(s) + A+(aq) → không phản ứng
⟹ C < A
⟹ A > C > B > E
Thí nghiệm 6: D(s) + E+ (aq) → không có phản ứng
⟹ E > D
⟹ A > C > B > E > D
⇒ Chọn đáp án A
Đáp án: A
⟹ A có tính khử mạnh hơn D ⇒ A > D
Thí nghiệm 2: C(s) + B+(aq) → C+(aq) + B(s)
⟹ C có tính khử mạnh hơn B ⇒ C > B
Thí nghiệm 5: B(s) + E+(aq) → B+(aq) + E(s)
⟹ B có tính khử mạnh hơn E ⇒ B > E
Thí nghiệm 4: C(s) + A+(aq) → không phản ứng
⟹ C < A
⟹ A > C > B > E
Thí nghiệm 6: D(s) + E+ (aq) → không có phản ứng
⟹ E > D
⟹ A > C > B > E > D
⇒ Chọn đáp án A
Đáp án: A
Dạng 5: CÂU HỎI TỰ LUẬN
Câu 48 [1016544]: Cho biết dãy thế điện cực chuẩn của các cặp oxi hóa - khử sau:
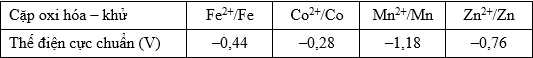
Ở điều kiện chuẩn, hãy sắp xếp các ion trên theo chiều tăng dần tính oxi hóa?

Ở điều kiện chuẩn, hãy sắp xếp các ion trên theo chiều tăng dần tính oxi hóa?
Thế điện cực chuẩn của cặp oxi hóa – khử càng lớn thì tính khử của dạng khử càng yếu, tính oxi hóa của dạng oxi hóa càng mạnh và ngược lại.
Các ion theo chiều tăng dần tính oxi hóa là Mn2+; Zn2+; Fe2+; Co2+.
Các ion theo chiều tăng dần tính oxi hóa là Mn2+; Zn2+; Fe2+; Co2+.
Câu 49 [1016545]: Cho bảng số liệu và các phản ứng sau đây:
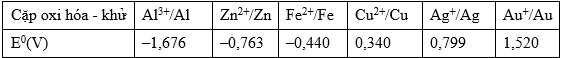
(1) Cu + Fe2+ →
(2) Cu + 2Ag+ →
(3) Zn + Cu2+ →
(4) Al3+ + Zn →
(5) Zn + Fe2+ →
Sử dụng bảng số liệu và hoàn thành các phương trình hóa học trên.

(1) Cu + Fe2+ →
(2) Cu + 2Ag+ →
(3) Zn + Cu2+ →
(4) Al3+ + Zn →
(5) Zn + Fe2+ →
Sử dụng bảng số liệu và hoàn thành các phương trình hóa học trên.
Nguyên tắc chung:
Chất oxi hóa mạnh hơn + Chất khử mạnh hơn Chất khử yếu hơn + Chất oxi hóa yếu hơn
(1) Cu + Fe2+ → không xảy ra phản ứng
(2) Cu + 2Ag+ → Cu2+ + 2Ag
(3) Zn + Cu2+ → Cu + Zn2+
(4) Al3+ + Zn → không xảy ra phản ứng
(5) Zn + Fe2+ → Fe + Zn2+
Chất oxi hóa mạnh hơn + Chất khử mạnh hơn Chất khử yếu hơn + Chất oxi hóa yếu hơn
(1) Cu + Fe2+ → không xảy ra phản ứng
(2) Cu + 2Ag+ → Cu2+ + 2Ag
(3) Zn + Cu2+ → Cu + Zn2+
(4) Al3+ + Zn → không xảy ra phản ứng
(5) Zn + Fe2+ → Fe + Zn2+
Câu 50 [1016546]: Ngâm đinh sắt sạch trong 200 mL dung dịch CuSO4. Sau phản ứng kết thúc lấy đinh sắt ra rửa nhẹ và làm khô thấy khối lượng đinh sắt tăng 8 gam. Xác định nồng độ ban đầu của CuSO4.
Đổi 200 mL = 0,2 L
Gọi số mol của Fe phản ứng là a mol
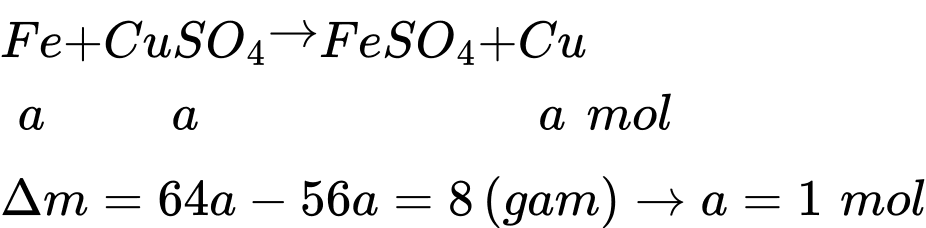
Nồng độ của dung dịch CuSO4 là CM CuSO4 = 1 ÷ 0,2 = 5 M.
Gọi số mol của Fe phản ứng là a mol
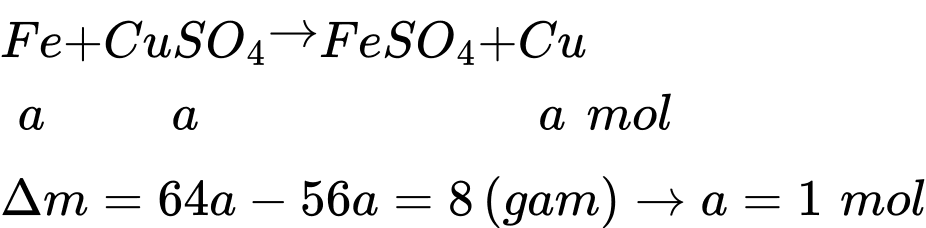
Nồng độ của dung dịch CuSO4 là CM CuSO4 = 1 ÷ 0,2 = 5 M.