Dạng 1: TRẮC NGHIỆM KHÁCH QUAN: mỗi câu hỏi chỉ có một đáp án đúng.
Câu 1 [703962]: “...(1)... là vật liệu kim loại chứa một kim loại cơ bản và một số kim loại khác hoặc …(2)…”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, vật liệu tổng hợp, polymer.
B, hợp kim, khí hiếm.
C, hợp kim, phi kim.
D, chất dẻo, khí hiếm.
Để tăng độ cứng, chống ăn mòn hoặc tăng cường khả năng chịu nhiệt hoặc điện của vật liệu, người ta thường trộn một kim loại cơ bản (như sắt, đồng, hoặc nhôm) với một hoặc nhiều nguyên tố khác. Các nguyên tố bổ sung có thể là kim loại (như chromium, nickel) hoặc phi kim (như carbon, silicon)... được gọi là họp kim.
⇒ Hợp kim là vật liệu kim loại chứa một kim loại cơ bản và một số kim loại khác hoặc phi kim.
⇒ Chọn đáp án C Đáp án: C
⇒ Hợp kim là vật liệu kim loại chứa một kim loại cơ bản và một số kim loại khác hoặc phi kim.
⇒ Chọn đáp án C Đáp án: C
Câu 2 [705924]: “Tính chất hoá học của ..(1).. thường tương tự tính chất hoá học của các ..(2).. thành phần tham gia tạo hợp kim”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, phi kim, đơn chất.
B, kim loại, hợp chất.
C, hợp kim, đơn chất.
D, khí hiếm, phi kim.
Hợp kim là vật liệu được tạo từ kim loại và một số nguyên tố khác.
Tính chất hóa học của hợp kim thường tương tự với các đơn chất kim loại vì hợp kim chủ yếu được tạo từ kim loại.
“Tính chất hoá học của hợp kim thường tương tự tính chất hoá học của các đơn chất thành phần tham gia tạo hợp kim”.
Chọn đáp án C Đáp án: C
Tính chất hóa học của hợp kim thường tương tự với các đơn chất kim loại vì hợp kim chủ yếu được tạo từ kim loại.
“Tính chất hoá học của hợp kim thường tương tự tính chất hoá học của các đơn chất thành phần tham gia tạo hợp kim”.
Chọn đáp án C Đáp án: C
Câu 3 [560735]: Nhờ có hàm lượng lớn trong vỏ Trái Đất nên một số kim loại được sử dụng làm kim loại cơ bản trong các hợp kim, đó là
A, iron, aluminium và magnesium.
B, iron, zinc và calcium.
C, aluminium, magnesium và sodium.
D, iron, aluminium và tin.
Nhờ có hàm lượng lớn trong vỏ Trái Đất nên một số kim loại được sử dụng làm kim loại cơ bản trong các hợp kim, đó là: iron, aluminium và magnesium. Đáp án: A
Câu 4 [560736]: Vật liệu nào trong số các vật liệu này là hợp kim?


A, Iron.
B, Copper.
C, Aluminium.
D, Thép.
Thép là hợp kim của sắt và các nguyên tố kim loại, phi kim khác. Đáp án: D
Câu 5 [560737]: Hợp kim là gì?
A, Hỗn hợp của hai hoặc nhiều nguyên tố, trong đó ít nhất một nguyên tố là kim loại.
B, Hỗn hợp của ba hoặc nhiều nguyên tố, trong đó ít nhất một nguyên tố là kim loại.
C, Hợp chất của hai hoặc nhiều nguyên tố, trong đó ít nhất một nguyên tố là kim loại.
D, Hợp chất của ba hoặc nhiều nguyên tố, trong đó ít nhất một nguyên tố là kim loại.

Hợp kim là hỗn hợp của ba hoặc nhiều nguyên tố, trong đó ít nhất một nguyên tố là kim loại.
=> Chọn đáp án B Đáp án: B
Câu 6 [560738]: Cấu trúc nào dưới đây minh họa cấu tạo của một hợp kim?
A, 

B, 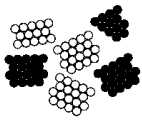

C, 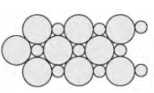

D, 

B,D sai vì có cấu trúc dạng đơn chất.
C sai vì có cấu trúc đồng nhất, theo 1 cấu trúc nhất định => có khả năng là ion.
A. Đúng. Do có cấu trúc dạng hợp chất.=> Chọn đáp án A
Đáp án: A
C sai vì có cấu trúc đồng nhất, theo 1 cấu trúc nhất định => có khả năng là ion.
A. Đúng. Do có cấu trúc dạng hợp chất.=> Chọn đáp án A
Đáp án: A
Câu 7 [560739]: Phát biểu nào sau đây về hợp kim là đúng? Hầu hết các hợp kim
A, ít hữu ích hơn các nguyên tố riêng lẻ tạo ra hợp kim.
B, mềm hơn các nguyên tố riêng lẻ tạo ra hợp kim.
C, đều cứng hơn các nguyên tố riêng lẻ tạo ra hợp kim.
D, đều không tạo đặc tính mới so với các nguyên tố riêng lẻ tạo ra hợp kim.
A sai vì hợp kim thường hữu ích
hơn so với các nguyên tố riêng lẻ.
B sai vì hợp kim thường cứng hơn,
không mềm hơn.
D sai vì hợp kim thường có các đặc
tính mới (ví dụ: chống ăn mòn, độ cứng, độ bền cao hơn).
=> Chọn đáp án C
Câu 8 [560740]: Hợp kim nào sau đây siêu nhẹ, được dùng trong vật liệu hàng không?


A, Fe – C.
B, Fe – Cr.
C, Cu – Zn.
D, Li – Al.
Hợp kim aluminium–lithium (Li–Al) là một trong những vật liệu siêu nhẹ, có độ bền cao và chịu nhiệt tốt, rất phù hợp để sử dụng trong ngành hàng không và vũ trụ. Các hợp kim khác trong các lựa chọn không đáp ứng các yêu cầu tương tự về trọng lượng và tính năng cần thiết trong lĩnh vực này.
⇒ Chọn đáp án D Đáp án: D
⇒ Chọn đáp án D Đáp án: D
Câu 9 [560741]: Tại sao hợp kim được sử dụng phổ biến và rộng rãi?
A, Hợp kim cải thiện các thuộc tính còn hạn chế của kim loại.
B, Hợp kim làm cho kim loại phản ứng mạnh hơn.
C, Hợp kim làm cho kim loại ít độc hơn.
D, Hợp kim có giá thành rẻ hơn kim loại nguyên chất.
Hợp kim có nhiều tính chất hoá học tương tự kim loại thành phần nhưng tính chất vật lí thường khác nhau nhiều do đó hợp kim được sử dụng phổ biến trong đời sống và sản xuất.
+ Hợp kim có những tính chất vật lí chung như tính ánh kim, dẫn điện, dẫn nhiệt …
+ Độ cứng của hợp kim thường cứng hơn độ cứng của kim loại thành phần trong hợp kim và độ dẻo thường kém hơn.
+ Nhiệt độ nóng chảy của hợp kim tuỳ thuộc vào thành phần và cấu tạo tinh thể của hợp kim, nhưng khác so với kim loại thành phần trong hợp kim.
⇒ Hợp kim cải thiện các thuộc tính còn hạn chế của kim loại.
⇒ Chọn đáp án A Đáp án: A
+ Hợp kim có những tính chất vật lí chung như tính ánh kim, dẫn điện, dẫn nhiệt …
+ Độ cứng của hợp kim thường cứng hơn độ cứng của kim loại thành phần trong hợp kim và độ dẻo thường kém hơn.
+ Nhiệt độ nóng chảy của hợp kim tuỳ thuộc vào thành phần và cấu tạo tinh thể của hợp kim, nhưng khác so với kim loại thành phần trong hợp kim.
⇒ Hợp kim cải thiện các thuộc tính còn hạn chế của kim loại.
⇒ Chọn đáp án A Đáp án: A
Câu 10 [560742]: Bảng dưới đây cho thấy phần trăm khối lượng của carbon có trong một số hợp kim của sắt và độ bền kéo thay đổi khi phần trăm carbon thay đổi.
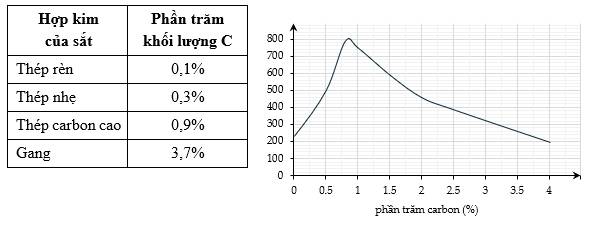
Một loại thép có độ bền kéo cao sẽ được sử dụng để xây dựng khung cho mái nhà. Sử dụng thông tin trong bảng và biểu đồ để cho biết hợp kim có độ bền kéo cao nhất là

Một loại thép có độ bền kéo cao sẽ được sử dụng để xây dựng khung cho mái nhà. Sử dụng thông tin trong bảng và biểu đồ để cho biết hợp kim có độ bền kéo cao nhất là
A, Thép rèn.
B, Thép nhẹ.
C, Thép carbon cao.
D, Gang.
Từ đồ thị ta thấy được thép với hàm lượng C là 0,9% cho độ bền kéo cao nhất là khoảng 800 nên loại thép này là thép carbon cao.
⇒ Chọn đáp án C Đáp án: C
⇒ Chọn đáp án C Đáp án: C
Câu 11 [560743]: Câu phát biểu nào dưới đây là đúng?
A, Thép là hợp kim của Fe không có C và có một ít S, Mn, P, Si.
B, Thép là hợp kim của Fe có từ 0,01-2% C và một ít Si, Mn, Cr, Ni.
C, Thép là hợp kim của Fe có từ 2-5% C và một ít S, Mn, p, Si.
D, Thép là hợp kim của Fe có từ 5-10% C và một lượng rất ít Si, Mn, Cr, Ni.
Thép là hợp kim của Fe có từ 0,01-2% C và một ít Si, Mn, Cr, Ni. Đáp án: B
Câu 12 [560744]: Bảng sau cho thông tin về một số tính chất của các loại thép (hợp kim của sắt).
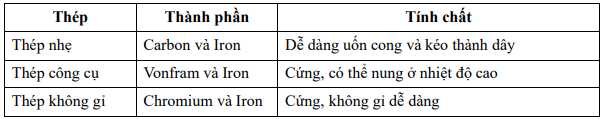
Thép là hợp kim của sắt nhưng cứng hơn sắt nguyên chất, điều nào lí giải đúng cho hiện tượng này?


Thép là hợp kim của sắt nhưng cứng hơn sắt nguyên chất, điều nào lí giải đúng cho hiện tượng này?

A, Do các nguyên tố được thêm vào sắt có độ cứng cao.
B, Do sắt tạo liên kết bền vững với các nguyên tố được thêm vào.
C, Do khi này thép có lớp màng oxide trơ bên ngoài bảo vệ.
D, Do các nguyên tử được sắp xếp chặt khít hơn thay cho cấu trúc ban đầu của nguyên tử kim loại.
A.Sai vì không phải tất cả các nguyên tố thêm vào thép đều có độ cứng cao.
C: Sai, vì lớp màng oxit không liên quan đến độ cứng mà chủ yếu bảo vệ thép khỏi ăn mòn.
D. Sai vì trong hợp kim, cấu trúc mạng tinh thể của sắt bị biến đổi do các nguyên tố khác xen vào, làm cản trở sự dịch chuyển của các lớp nguyên tử trong mạng tinh thể khi chịu lực.
=> Chọn đáp án B Đáp án: B
C: Sai, vì lớp màng oxit không liên quan đến độ cứng mà chủ yếu bảo vệ thép khỏi ăn mòn.
D. Sai vì trong hợp kim, cấu trúc mạng tinh thể của sắt bị biến đổi do các nguyên tố khác xen vào, làm cản trở sự dịch chuyển của các lớp nguyên tử trong mạng tinh thể khi chịu lực.
=> Chọn đáp án B Đáp án: B
Câu 13 [560745]: Cấu trúc của một hợp kim được hiển thị như hình bên. Hợp kim là hỗn hợp của kim loại với một kim loại khác hoặc phi kim khác. Chúng thường mạnh hơn và cứng hơn nhiều so với kim loại nguyên chất. Phát biểu nào dưới đây giải thích cho những đặc điểm này?


A, Trong hợp kim, các nguyên tử có kích thước không đều đặn nên cần một lực lớn hơn để làm biến dạng.
B, Trong hợp kim, các nguyên tử có kích thước đều đặn nên cần một lực lớn hơn để làm biến dạng.
C, Trong hợp kim, các nguyên tử di chuyển hỗn loạn nên nên cần một lực lớn hơn để làm biến dạng.
D, Trong hợp kim, các nguyên tử kim loại khác hoặc phi kim sẽ xếp bao quanh các nguyên tử kim loại chính nên cần một lực lớn để làm biến dạng.
Trong hợp kim, các nguyên tử có kích thước không đều đặn nên các lớp rất khó trượt lên nhau, cần một lực lớn hơn để làm biến dạng. Đáp án: A
Câu 14 [560746]: Hình dưới cho thấy cấu trúc của một hợp kim.
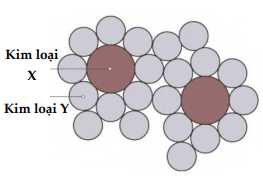
Ý nào sau đây giải thích đúng lí do khiến hợp kim này cứng hơn kim loại Y nguyên chất?

Ý nào sau đây giải thích đúng lí do khiến hợp kim này cứng hơn kim loại Y nguyên chất?
A, Do các nguyên tử của kim loại X và Y có kích thước khác nhau do đó không có lớp nào trượt lên nhau.
B, Do kim loại X có kích thước lớn hơn kim loại Y, tạo ra độ cứng lớn hơn.
C, Do kim loại X có kích thước lớn hơn kim loại Y, tạo liến kết với các nguyên tử Y bền vững hơn.
D, Do kim loại X và Y có khả năng liên kết bền vững với nhau.
Những nguyên tử được thêm vào kim loại có kích thước khác với nguyên tử kim loại, vì vậy chúng làm biến dạng các lớp nguyên tử. Điều này có nghĩa là cần một lực lớn hơn để các lớp trượt lên nhau. Do đó hợp kim cứng hơn kim loại Y nguyên chất. Đáp án: A
Câu 15 [706239]: Kim loại cơ bản trong dural và thép 304 lần lượt là
A, nhôm và magnesium.
B, nhôm và sắt.
C, magnesium và sắt.
D, kẽm và sắt.
Phân tích các đáp án:
❌A. SAI. Mặc dù magnesium có trong duralumin, nhưng kim loại cơ bản của thép 304 là sắt, không phải magnesium.
✔️B. ĐÚNG. Nhôm là kim loại cơ bản trong duralumin và sắt là kim loại cơ bản trong thép 304.
❌C. SAI. Magnesium không phải là kim loại cơ bản trong duralumin.
❌D. SAI. Kẽm không phải là kim loại cơ bản trong duralumin.
⟹ Chọn đáp án B Đáp án: B
❌A. SAI. Mặc dù magnesium có trong duralumin, nhưng kim loại cơ bản của thép 304 là sắt, không phải magnesium.
✔️B. ĐÚNG. Nhôm là kim loại cơ bản trong duralumin và sắt là kim loại cơ bản trong thép 304.
❌C. SAI. Magnesium không phải là kim loại cơ bản trong duralumin.
❌D. SAI. Kẽm không phải là kim loại cơ bản trong duralumin.
⟹ Chọn đáp án B Đáp án: B
Câu 16 [560747]: Cần lựa chọn hợp kim có tính chất đặc trưng nào sau đây để làm các tấm khiên trang bị cho lực lượng cảnh sát?
A, Độ cứng cao.
B, Nhiệt độ nóng chảy lớn.
C, Độ dẻo cao.
D, Có tính ánh kim.
A. Độ cứng cao: Đây là một tính chất quan trọng, vì khiên cần có khả năng chống chịu va đập hoặc tác động mạnh
B. Nhiệt độ nóng chảy lớn: Điều này không liên quan trực tiếp đến việc làm khiên, vì nhiệt độ nóng chảy không ảnh hưởng nhiều trong trường hợp sử dụng thực tế.
C. Độ dẻo cao: Độ dẻo cao giúp vật liệu dễ uốn, nhưng đối với khiên, đây không phải yếu tố chính vì độ cứng và bền quan trọng hơn.
D. Có tính ánh kim: Đây chỉ là tính chất thẩm mỹ, không quan trọng cho chức năng của khiên.
=> Chọn đáp án A
Câu 17 [560748]: Thép không gỉ 304 là loại thép không gỉ phổ biến nhất. Nó là hợp kim của sắt, carbon, chromium và nickel. Tại sao thép 304 được sử dụng rất phổ biến trong đời sống?
A, Dẫn điện kém.
B, Dẫn nhiệt kém.
C, Chống ăn mòn trong môi trường acid.
D, Chống ăn mòn trong môi trường khí quyển.
Thép không gỉ 304 được sử dụng rộng rãi vì khả năng chống ăn mòn tuyệt vời, đặc biệt là trong điều kiện khí quyển. Crom trong hợp kim tạo thành lớp oxit crom bảo vệ trên bề mặt thép, giúp thép không bị rỉ sét hoặc ăn mòn. Điều này làm cho nó lý tưởng để sử dụng trong nhiều ứng dụng khác nhau, chẳng hạn như đồ dùng nhà bếp, bồn rửa và đồ nội thất ngoài trời.
=> Chọn đáp án D Đáp án: D
=> Chọn đáp án D Đáp án: D
Dạng 2: TRẮC NGHIỆM ĐÚNG SAI – mỗi ý a), b), c), d) chọn đúng hoặc sai.
Câu 18 [560749]: Hợp kim là vật liệu kim loại chứa một kim loại cơ bản và một số kim loại khác hoặc phi kim. Nhìn chung, hợp kim có nhiều tính chất hoá học tương tự kim loại thành phần nhưng tính chất vật lí thường khác nhau nhiều.
a. Hợp kim được sử dụng trong đời sống và sản xuất phổ biến hơn so với kim loại.
b. Kim loại A có nhiệt độ nóng chảy cao hơn kim loại B, nhiệt độ nóng chảy của hợp kim A-B luôn cao hơn nhiệt độ nóng chảy của B.
c. Hợp kim có thể cứng hơn rất nhiều các kim loại tạo nên nó.
d. Hợp kim thường khó bị oxi hoá hơn các đơn kim loại thành phần.
a. Hợp kim được sử dụng trong đời sống và sản xuất phổ biến hơn so với kim loại.
b. Kim loại A có nhiệt độ nóng chảy cao hơn kim loại B, nhiệt độ nóng chảy của hợp kim A-B luôn cao hơn nhiệt độ nóng chảy của B.
c. Hợp kim có thể cứng hơn rất nhiều các kim loại tạo nên nó.
d. Hợp kim thường khó bị oxi hoá hơn các đơn kim loại thành phần.
Phân tích các phát biểu sau:
✔️ a. Đúng. Nhờ cải thiện được các thuộc tính còn hạn chế của kim loại mà hợp kim được sử dụng trong đời sống và sản xuất phổ biến hơn kim loại.
❌ b. Sai. Tùy thuộc vào kim loại và hợp kim khác nhau sẽ có nhiệt độ nóng chảy riêng, không phải hợp kim nào cũng luôn có nhiệt độ nóng chảy cao hơn kim loại tạo nên nó.
✔️ c. Đúng. Hợp kim có thể cứng hơn rất nhiều các kim loại tạo nên nó.
✔️ d. Đúng. Hợp kim thường khó bị oxi hóa hơn các đơn kim loại thành phần.
✔️ a. Đúng. Nhờ cải thiện được các thuộc tính còn hạn chế của kim loại mà hợp kim được sử dụng trong đời sống và sản xuất phổ biến hơn kim loại.
❌ b. Sai. Tùy thuộc vào kim loại và hợp kim khác nhau sẽ có nhiệt độ nóng chảy riêng, không phải hợp kim nào cũng luôn có nhiệt độ nóng chảy cao hơn kim loại tạo nên nó.
✔️ c. Đúng. Hợp kim có thể cứng hơn rất nhiều các kim loại tạo nên nó.
✔️ d. Đúng. Hợp kim thường khó bị oxi hóa hơn các đơn kim loại thành phần.
Câu 19 [560751]: Hình ảnh dưới đây mô tả về sự ăn mòn của gang, thép trong không khí ẩm?
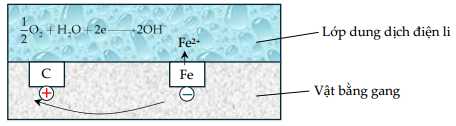
a. Dạng ăn mòn hoá học là chủ yếu, do sắt dễ dàng phản ứng với oxygen trong không khí.
b. Carbon đóng vai trò là cực âm (anode), sắt là cực dương (cathode) khi sự ăn mòn điện hóa xảy ra.
c. Oxygen đóng vai trò là chất oxi hoá.
d. Carbon bị khử tại cathode, Fe bị oxi hoá tại anode thành Fe2+.

a. Dạng ăn mòn hoá học là chủ yếu, do sắt dễ dàng phản ứng với oxygen trong không khí.
b. Carbon đóng vai trò là cực âm (anode), sắt là cực dương (cathode) khi sự ăn mòn điện hóa xảy ra.
c. Oxygen đóng vai trò là chất oxi hoá.
d. Carbon bị khử tại cathode, Fe bị oxi hoá tại anode thành Fe2+.
Phân tích các phát biểu sau:
❌ a. Sai. Sắt bị ăn mòn điện hóa. Do trong không khí ẩm, trên bề mặt gang có lớp nước tạo thành dung dịch chất điện li. Sắt và các thành phần khác (chủ yếu là carbon) thành phần của gang tiếp xúc với dung dịch điện li, tạo nên pin điện hoá.
❌ b. Sai. Khi sự ăn mòn điện hóa xảy ra, carbon đóng vai trò là cực dương (cathode), sắt là cực âm (anode).
✔️ c. Đúng. Oxygen đóng vai trò là chất oxi hóa: O2 + 4e + 2H2O ➝ 4OH-
❌ d. Sai. Carbon không bị khử vì nó không tham gia vào phản ứng hóa học mà chỉ đóng vai trò cực dương (cathode). Quá trình khử xảy ra với oxygen (O2).
❌ a. Sai. Sắt bị ăn mòn điện hóa. Do trong không khí ẩm, trên bề mặt gang có lớp nước tạo thành dung dịch chất điện li. Sắt và các thành phần khác (chủ yếu là carbon) thành phần của gang tiếp xúc với dung dịch điện li, tạo nên pin điện hoá.
❌ b. Sai. Khi sự ăn mòn điện hóa xảy ra, carbon đóng vai trò là cực dương (cathode), sắt là cực âm (anode).
✔️ c. Đúng. Oxygen đóng vai trò là chất oxi hóa: O2 + 4e + 2H2O ➝ 4OH-
❌ d. Sai. Carbon không bị khử vì nó không tham gia vào phản ứng hóa học mà chỉ đóng vai trò cực dương (cathode). Quá trình khử xảy ra với oxygen (O2).
Câu 20 [560750]: Để lợp nhà, các tấm tôn (thép mạ một lớp kẽm mỏng) được gắn với nhau bởi các đinh thép. Theo thời gian, các tấm tôn bị ăn mòn.
a. Vị trí đóng đinh thép dễ xảy ra ăn mòn hơn các vị trí khác.
b. Tấm tôn bị ăn mòn từ trong ra ngoài do thép bị ăn mòn trước kẽm.
c. Sắt trong tấm tôn không bị ăn mòn theo thời gian.
d. Nước mưa càng có tính acid thì tấm tôn bị ăn mòn càng nhanh.
a. Vị trí đóng đinh thép dễ xảy ra ăn mòn hơn các vị trí khác.
b. Tấm tôn bị ăn mòn từ trong ra ngoài do thép bị ăn mòn trước kẽm.
c. Sắt trong tấm tôn không bị ăn mòn theo thời gian.
d. Nước mưa càng có tính acid thì tấm tôn bị ăn mòn càng nhanh.
Phân tích các phát biểu sau:
✔️ a. Đúng. Vị trí đóng đinh thép bị ăn mòn trước là do việc đóng đinh tạo ra lỗ thủng trên tấm tôn làm cho lõi thép và lớp tráng kẽm cùng tiếp xúc với nước. Trong điều kiện này, vị trí đóng đinh thép sẽ xuất hiện một pin điện hoá và sự ăn mòn điện hoá diễn ra nhanh hơn so với các vị trí khác trên tấm tôn.
❌ b. Sai. Tấm tôn bị ăn mòn từ ngoài, lớp kẽm bị ăn mòn trước thép.
❌ c. Sai. Vì ngoài sắt trong thép còn có carbon, khi hai thành phần này cùng tiếp xúc nước mưa (tại vị trí không có kẽm hoặc khi lớp kẽm đã bị ăn mòn), sắt đóng vai trò là anode và vẫn bị ăn mòn.
✔️ d. Đúng. Nước mưa càng có tính acid thì kẽm bị ăn mòn càng nhanh thì tấm tôn cũng bị ăn mòn nhanh hơn.
✔️ a. Đúng. Vị trí đóng đinh thép bị ăn mòn trước là do việc đóng đinh tạo ra lỗ thủng trên tấm tôn làm cho lõi thép và lớp tráng kẽm cùng tiếp xúc với nước. Trong điều kiện này, vị trí đóng đinh thép sẽ xuất hiện một pin điện hoá và sự ăn mòn điện hoá diễn ra nhanh hơn so với các vị trí khác trên tấm tôn.
❌ b. Sai. Tấm tôn bị ăn mòn từ ngoài, lớp kẽm bị ăn mòn trước thép.
❌ c. Sai. Vì ngoài sắt trong thép còn có carbon, khi hai thành phần này cùng tiếp xúc nước mưa (tại vị trí không có kẽm hoặc khi lớp kẽm đã bị ăn mòn), sắt đóng vai trò là anode và vẫn bị ăn mòn.
✔️ d. Đúng. Nước mưa càng có tính acid thì kẽm bị ăn mòn càng nhanh thì tấm tôn cũng bị ăn mòn nhanh hơn.
Câu 21 [560752]: Thực hiện thí nghiệm sau:
Bước 1: Cho dung dịch NaCl 5% vào ống thuỷ tinh hình chữ U như hình bên.
Bước 2: Nhúng một thanh đồng và một thanh kẽm đã làm sạch vào hai đầu của ống chữ U.
Bước 3: Nối hai thanh kim loại bằng dây dẫn.
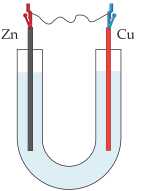
a. Sau bước 2, kim loại Zn bị ăn mòn.
b. Sau bước 3, kẽm bị oxi hoá và đóng vai trò là anode.
c. Cu2+ bị khử thành Cu bám vào thanh đồng, làm khối lượng thanh đồng
tăng dần.
d. Khoảng vài phút sau bước 3, nhỏ vài giọt phenolphthalein vào dung
dịch gần thanh copper và quan sát thấy dung dịch dần chuyển sang màu
hồng.
Bước 1: Cho dung dịch NaCl 5% vào ống thuỷ tinh hình chữ U như hình bên.
Bước 2: Nhúng một thanh đồng và một thanh kẽm đã làm sạch vào hai đầu của ống chữ U.
Bước 3: Nối hai thanh kim loại bằng dây dẫn.

a. Sau bước 2, kim loại Zn bị ăn mòn.
b. Sau bước 3, kẽm bị oxi hoá và đóng vai trò là anode.
c. Cu2+ bị khử thành Cu bám vào thanh đồng, làm khối lượng thanh đồng
tăng dần.
d. Khoảng vài phút sau bước 3, nhỏ vài giọt phenolphthalein vào dung
dịch gần thanh copper và quan sát thấy dung dịch dần chuyển sang màu
hồng.
Phân tích các phát biểu sau:
❌ a. Sai. Hai kim loại chưa tiếp xúc với nhau nên chưa xảy ra sự ăn mòn.
✔️ b. Đúng. Sau bước 3, kẽm bị oxi hóa và đóng vai trò là anode.
❌ c. Sai. Trong dung dịch không chứa Cu2+. Thanh đồng (điện cực cathode) xảy ra quá trình khử H+ thành H2
✔️ d. Đúng. Tại cathode xảy ra quá trình khử nước tạo ion OH- nên khi nhỏ dung dịch phenolphtalein vào thì dung dịch dần chuyển sang màu hồng.
❌ a. Sai. Hai kim loại chưa tiếp xúc với nhau nên chưa xảy ra sự ăn mòn.
✔️ b. Đúng. Sau bước 3, kẽm bị oxi hóa và đóng vai trò là anode.
❌ c. Sai. Trong dung dịch không chứa Cu2+. Thanh đồng (điện cực cathode) xảy ra quá trình khử H+ thành H2
✔️ d. Đúng. Tại cathode xảy ra quá trình khử nước tạo ion OH- nên khi nhỏ dung dịch phenolphtalein vào thì dung dịch dần chuyển sang màu hồng.
2H2O + 2e ➝ H2 + 2OH-
Câu 22 [560753]: Thép là hợp kim, trong đó kim loại cơ bản là sắt, phi kim là carbon (chiếm 0,02% - 2,14%) và một số kim loại như chromium, nickel,... (chiếm phần trăm tương đối nhỏ). Gang là hợp kim của sắt và carbon, trong đó có hàm lượng C lớn hơn so với thép. Gang có độ cứng cao nhưng giòn nên khó gia công hơn thép.
a. Gang và thép đều cứng hơn sắt.
b. Gang cứng hơn thép do có hàm lượng carbon cao hơn.
c. Trong thực tế, thép có nhiều ứng dụng và được sản xuất nhiều hơn gang.
d. Thép khó bị ăn mòn điện hóa hơn gang trong cùng điều kiện.
a. Gang và thép đều cứng hơn sắt.
b. Gang cứng hơn thép do có hàm lượng carbon cao hơn.
c. Trong thực tế, thép có nhiều ứng dụng và được sản xuất nhiều hơn gang.
d. Thép khó bị ăn mòn điện hóa hơn gang trong cùng điều kiện.
Phân tích các phát biểu sau:
✔️ a. Đúng. Gang và thép đều cứng hơn sắt.
✔️ b. Đúng. Gang cứng hơn thép do có hàm lượng carbon cao hơn.
✔️ c. Đúng.Trong thực tế, thép có nhiều ứng dụng và được sản xuất nhiều hơn gang. Vì thép chống ăn mòn tốt hơn.
✔️ d. Đúng. Thép khó bị ăn mòn điện hóa hơn gang trong cùng điều kiện.
✔️ a. Đúng. Gang và thép đều cứng hơn sắt.
✔️ b. Đúng. Gang cứng hơn thép do có hàm lượng carbon cao hơn.
✔️ c. Đúng.Trong thực tế, thép có nhiều ứng dụng và được sản xuất nhiều hơn gang. Vì thép chống ăn mòn tốt hơn.
✔️ d. Đúng. Thép khó bị ăn mòn điện hóa hơn gang trong cùng điều kiện.
Dạng 3: TRẮC NGHIỆM YÊU CẦU TRẢ LỜI NGẮN
Câu 23 [560754]: Cho 12 gam hợp kim của bạc vào dung dịch HNO3 loãng (dư), đun nóng đến phản ứng hoàn toàn, thu được dung dịch có 8,5 gam AgNO3. Giả sử các thành phần khác không tham gia phản ứng. Phần trăm khối lượng của bạc trong mẫu hợp kim là
Điền đáp án: ..........
Điền đáp án: ..........
nAgNO3 = 8,5/170 = 0,05 mol
Bảo toàn số mol nguyên tử nguyên tố Ag: nAg = nAgNO3 = 0,05 mol
=> m Ag = 0,05.108 = 5,4 gam
=> Phần trăm khối lượng của bạc là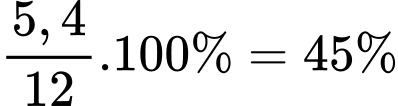
=> Điền đáp án: 45
Bảo toàn số mol nguyên tử nguyên tố Ag: nAg = nAgNO3 = 0,05 mol
=> m Ag = 0,05.108 = 5,4 gam
=> Phần trăm khối lượng của bạc là
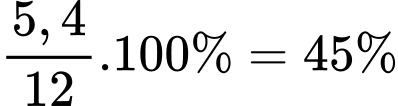
=> Điền đáp án: 45
Câu 24 [560755]: Cho 9,6 gam hợp kim gồm Mg-Fe vào dung dịch H2SO4 dư thấy thoát ra 0,3 mol khí H2. Mặt khác cũng 9,6 gam hợp kim trên cho vào 500 mL dung dịch AgNO3 1,5M thì thu được m gam chất rắn. Giá trị của m là
Gọi số mol của Mg và Fe lần lượt là x và y.
Dựa trên khối lượng hợp kim và số mol H2 tạo ra sau phản ứng ta có hệ phương trình:
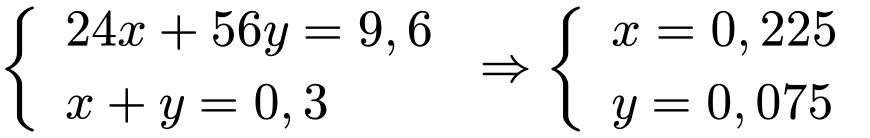
Ta có: nAgNO3= 0,75 mol
Mg + 2Ag+ ⟶ Mg2+ + 2Ag
Fe + 2Ag+ ⟶ Fe2+ + 2Ag
Vì Ag+ trong dung dịch vẫn còn dư nên xảy ra phản ứng
Ag+ + Fe2+ ⟶ Fe3+ + Ag
=> n Ag= 2 . 0,225 + 2. 0,075 + 0,075 = 0,675 mol
=> Khối lượng chất rắn: mAg= 0,675.108 = 72,9 gam
=> Điền đáp án: 72,9
Dựa trên khối lượng hợp kim và số mol H2 tạo ra sau phản ứng ta có hệ phương trình:
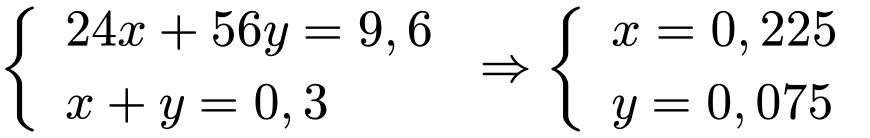
Ta có: nAgNO3= 0,75 mol
Mg + 2Ag+ ⟶ Mg2+ + 2Ag
Fe + 2Ag+ ⟶ Fe2+ + 2Ag
Vì Ag+ trong dung dịch vẫn còn dư nên xảy ra phản ứng
Ag+ + Fe2+ ⟶ Fe3+ + Ag
=> n Ag= 2 . 0,225 + 2. 0,075 + 0,075 = 0,675 mol
=> Khối lượng chất rắn: mAg= 0,675.108 = 72,9 gam
=> Điền đáp án: 72,9
Câu 25 [560756]: Vàng được sử dụng làm đồ trang sức là vàng hợp kim với các kim loại khác, thường là bạc, đồng và kẽm. Điều này làm cho đồ trang sức bền hơn nhiều trong khi vẫn giữ được khả năng sáng bóng. Tỷ lệ vàng trong hợp kim được đo bằng Karat, với vàng 24 Karat là vàng nguyên chất. Tỷ lệ vàng (theo khối lượng) trong các hợp kim vàng khác nhau được tóm tắt trong bảng sau:
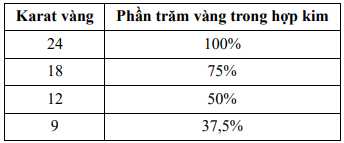
Một món đồ trang sức bằng vàng được làm từ vàng 14 Karat. Tính phần trăm khối lượng vàng trong hợp kim này (làm tròn kết quả đến hàng phần mười).

Một món đồ trang sức bằng vàng được làm từ vàng 14 Karat. Tính phần trăm khối lượng vàng trong hợp kim này (làm tròn kết quả đến hàng phần mười).
Phần trăm khối lượng vàng trong vàng 14 Karat là 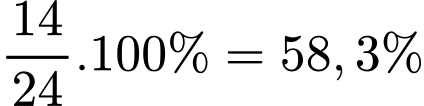
=> Điền đáp án: 58,3
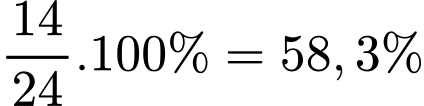
=> Điền đáp án: 58,3
Câu 26 [560757]: Một số loại thuốc hàn là hợp kim của Tin và Lead. Một loại chất hàn được tạo ra bằng cách trộn 22,5 gam lead với 15,0 gam tin. Phần trăm khối lượng tin trong loại thuốc hàn trên là bao nhiêu?

Điền đáp án: ..........

Điền đáp án: ..........
Phần trăm khối lượng tin trong loại thuốc hàn trên là: 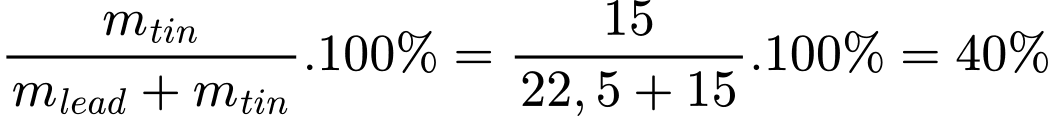
=> Điền đáp án: 40
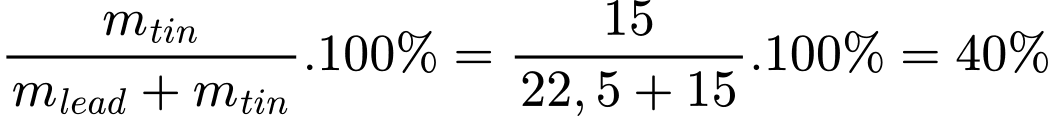
=> Điền đáp án: 40
Câu 27 [560758]: Gỉ sét có thể được mô hình hóa bằng cách sử dụng phương trình:
4Fe(s) + 6H2O(l) + 3O2(g) 2Fe2O3.6H2O(s)
2Fe2O3.6H2O(s)
Một thanh sắt khối lượng 750 gam để ngoài trời mưa. Giả sử toàn bộ sắt bị chuyển sang gỉ sét. Biết gỉ sét hình thành với tốc độ 50 gam mỗi ngày. Sau bao nhiêu ngày thanh sắt sẽ hoàn toàn bị chuyển thành gỉ sét?
Điền đáp án: ..........
4Fe(s) + 6H2O(l) + 3O2(g)
 2Fe2O3.6H2O(s)
2Fe2O3.6H2O(s)Một thanh sắt khối lượng 750 gam để ngoài trời mưa. Giả sử toàn bộ sắt bị chuyển sang gỉ sét. Biết gỉ sét hình thành với tốc độ 50 gam mỗi ngày. Sau bao nhiêu ngày thanh sắt sẽ hoàn toàn bị chuyển thành gỉ sét?
Điền đáp án: ..........
- Thanh sắt 750 gam có thể tạo ra được khối lượng gỉ sét:
nFe= 750/56 = 13,393 mol => nFe2O3.6H2O = 2/4 . nFe = 6,6965 mol
=> Khối lượng gỉ tạo thành là 6,6965 . 268 = 1794,662 gam
- Mỗi ngày gỉ tạo ra 50 gam, số ngày thanh sắt chuyển hoàn toàn thành gỉ là: 1794,662 / 50 ≈ 36 ngày
=> Điền đáp án: 36
nFe= 750/56 = 13,393 mol => nFe2O3.6H2O = 2/4 . nFe = 6,6965 mol
=> Khối lượng gỉ tạo thành là 6,6965 . 268 = 1794,662 gam
- Mỗi ngày gỉ tạo ra 50 gam, số ngày thanh sắt chuyển hoàn toàn thành gỉ là: 1794,662 / 50 ≈ 36 ngày
=> Điền đáp án: 36
Câu 28 [560759]: Coi gỉ sét là iron(III) oxide Fe2O3. Nó được hình thành khi sắt tiếp xúc với nước và oxygen. Một số đinh sắt đã được cân trước và sau khi tiếp xúc với nước và oxygen trong một tuần. Khối lượng trước khi tiếp xúc là 28 gam và sau một tuần khối lượng là 40 gam. Phần trăm lượng oxygen có trên đinh sắt sau một tuần là bao nhiêu?
Sau một tuần, đinh sắt tiếp xúc với không khí đã chuyển một phần thành gỉ sắt => khối lượng tăng lên là khối lượng oxygen trong gỉ sắt => mO=40 - 28 = 12 gam
=> Phần trăm oxygen: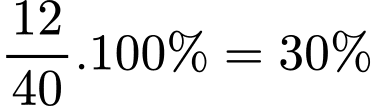
=> Điền đáp án: 30
=> Phần trăm oxygen:
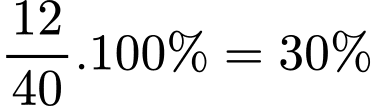
=> Điền đáp án: 30
Câu 29 [560760]: Nhiều quặng kim loại có chứa sulfur. Chalcocite là một loại quặng đồng quan trọng với thành phần Cu2S. Đồng có thể thu được từ quặng bằng cách nung nóng trong không khí. Phương trình phản ứng xảy ra như sau:
Cu2S(s) + O2(g)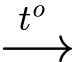 2Cu(s) + SO2(g)
2Cu(s) + SO2(g)
Khối lượng đồng tối đa sinh ra khi nung 20,5 tấn Cu2S với một lượng dư oxygen là bao nhiêu?
Điền đáp án: ..........
Cu2S(s) + O2(g)
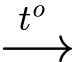 2Cu(s) + SO2(g)
2Cu(s) + SO2(g)Khối lượng đồng tối đa sinh ra khi nung 20,5 tấn Cu2S với một lượng dư oxygen là bao nhiêu?
Điền đáp án: ..........
Phương trình phản ứng: Cu2S + O2 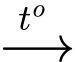 2Cu + SO2
2Cu + SO2
nCu2S = 20,5 ÷ 160 =0,128125 (mol)
=> nCu= 2 × nCu2S = 0,25625 mol
=> Khối lượng đống tối đa sinh ra là 0,25625 × 64 = 16,4 tấn
=> Điền đáp án: 16,4
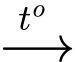 2Cu + SO2
2Cu + SO2nCu2S = 20,5 ÷ 160 =0,128125 (mol)
=> nCu= 2 × nCu2S = 0,25625 mol
=> Khối lượng đống tối đa sinh ra là 0,25625 × 64 = 16,4 tấn
=> Điền đáp án: 16,4
Câu 30 [560761]: Khi quá trình khai thác được thực hiện với 20,5 tấn chalcocite (thành phần chính là Cu2S), có tối đa 12,3 tấn đồng được tạo thành. Phần trăm tạp chất có trong quặng này là bao nhiêu?
Điền đáp án: ..........
Điền đáp án: ..........
Bảo toàn nguyên tố Cu: nCu= 2.nCu2S = 12,3 / 64
=> nCu2S = 12,3 / 128 mol.tấn
=> Khối lượng Cu2S có trong quặng chalcocite là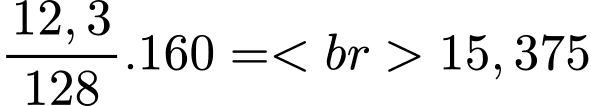
=> Khối lượng tạp chất trong quặng là 20,5 - 15,375 =5,125 tấn
Phần trăm tạp chất:
=> Điền đáp án: 25
=> nCu2S = 12,3 / 128 mol.tấn
=> Khối lượng Cu2S có trong quặng chalcocite là
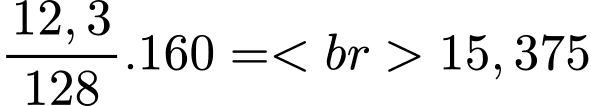
=> Khối lượng tạp chất trong quặng là 20,5 - 15,375 =5,125 tấn
Phần trăm tạp chất:

=> Điền đáp án: 25
Câu 31 [560762]: Để xác định hàm lượng bạc trong hợp kim người ta hoà tan 0,5 gam hợp kim đó vào nitric acid. Khi cho thêm hydrochloric acid vào dung dịch đó thu được 0,398 gam kết tủa. Hàm lượng của bạc có trong hợp kim là bao nhiêu?
Điền đáp án: ..........
Điền đáp án: ..........
Tóm tắt quy trình: Ag ⟶ AgNO3 ⟶ AgCl
=> nAgCl = n Ag= 0,398 / 143,5
=> Khối lượng bạc trong hợp kim là 0,398/143,5 × 108
=> Hàm lượng của bạc: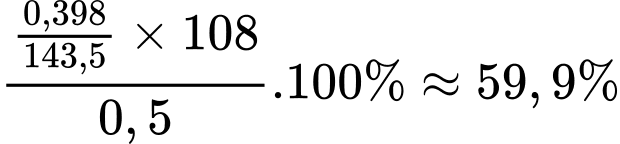
⟹Điền đáp án: 59,9
=> nAgCl = n Ag= 0,398 / 143,5
=> Khối lượng bạc trong hợp kim là 0,398/143,5 × 108
=> Hàm lượng của bạc:
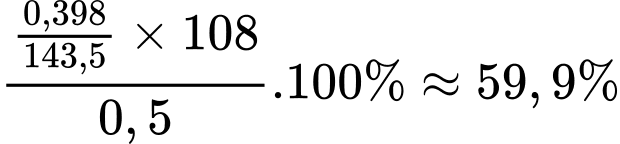
⟹Điền đáp án: 59,9
Câu 32 [704407]: C60600 là hợp kim của đồng và nhôm. Phản ứng sau đây có thể được sử dụng để xác định hàm lượng Cu trong C60600.
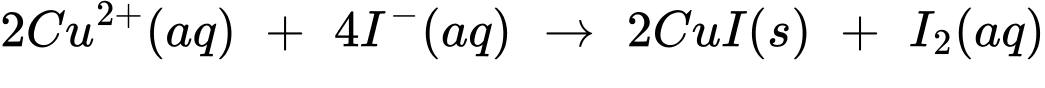
Quy trình được thực hiện như sau:
Bước 1. Hoà tan 0,5 g mẫu hợp kim C60600 trong sulfuric acid đặc, rồi pha loãng bằng nước;
Bước 2. Thêm dung dịch I- đến dư.
Bước 3. Thêm dần dung dịch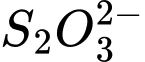 0,50 M để phản ứng với iodine theo phản ứng sau:
0,50 M để phản ứng với iodine theo phản ứng sau:
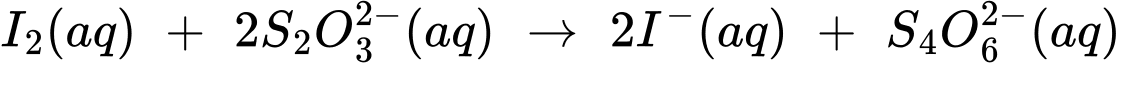
Thể tích dung dịch cần dùng để phản ứng trên xảy ra vừa đủ là 14,85 mL. Hàm lượng phần trăm khối lượng Cu trong mẫu hợp kim C60600 là bao nhiêu? (làm tròn kết quả đến phần chục).
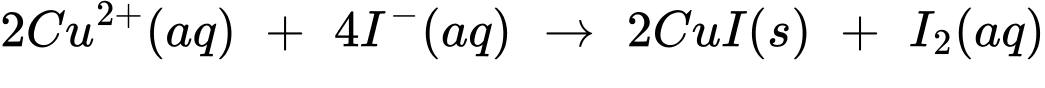
Quy trình được thực hiện như sau:
Bước 1. Hoà tan 0,5 g mẫu hợp kim C60600 trong sulfuric acid đặc, rồi pha loãng bằng nước;
Bước 2. Thêm dung dịch I- đến dư.
Bước 3. Thêm dần dung dịch
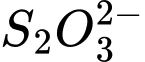 0,50 M để phản ứng với iodine theo phản ứng sau:
0,50 M để phản ứng với iodine theo phản ứng sau: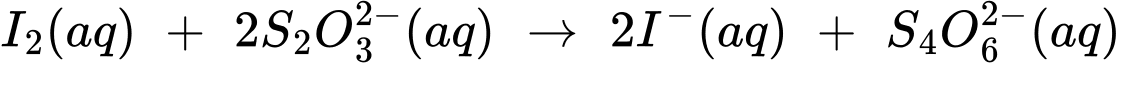
Thể tích dung dịch cần dùng để phản ứng trên xảy ra vừa đủ là 14,85 mL. Hàm lượng phần trăm khối lượng Cu trong mẫu hợp kim C60600 là bao nhiêu? (làm tròn kết quả đến phần chục).
(1) 2Cu2+(aq) + 4I–(aq) ⟶ 2CuI(s) + I2(aq)
(2) I2(aq) + 2S2O32–(aq) ⟶ 2I– + S4O62–(aq)
Đổi 14,85 mL = 0,01485 L
Số mol của Na2S2O3 là: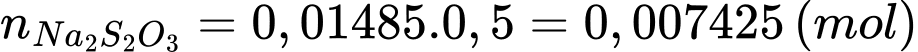
Từ phương trình (1) và (2) số mol của Cu là: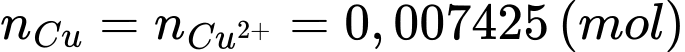
Phần trăm của Cu trong mẫu hợp kim C60600 là:
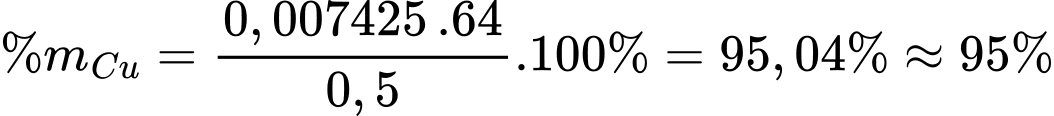
⇒ Điền đáp án: 95,0
(2) I2(aq) + 2S2O32–(aq) ⟶ 2I– + S4O62–(aq)
Đổi 14,85 mL = 0,01485 L
Số mol của Na2S2O3 là:
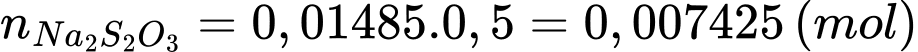
Từ phương trình (1) và (2) số mol của Cu là:
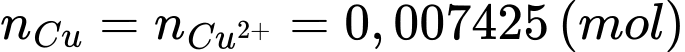
Phần trăm của Cu trong mẫu hợp kim C60600 là:
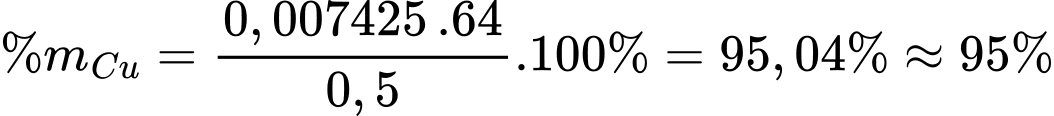
⇒ Điền đáp án: 95,0
Dạng 4: BÀI TẬP ĐỌC HIỂU – đọc thông tin và trả lời các câu hỏi sau đó
GANG
Sắt (Fe) tồn tại trong lớp vỏ Trái Đất ở nhiều loại khoáng chất khác nhau như sắt pyrite (FeS2), siderite (FeCO3), hematite (Fe2O3) và magnetite (Fe3O4, thường được ký hiệu là FeO. Fe2O3). Trong số này, hematite và magnetite đặc biệt thích hợp cho việc điều chế sắt. Quá trình luyện kim sắt liên quan đến việc khử các khoáng chất của sắt bằng carbon (thành phần chủ yếu của than cốc) trong lò cao (Hình vẽ dưới).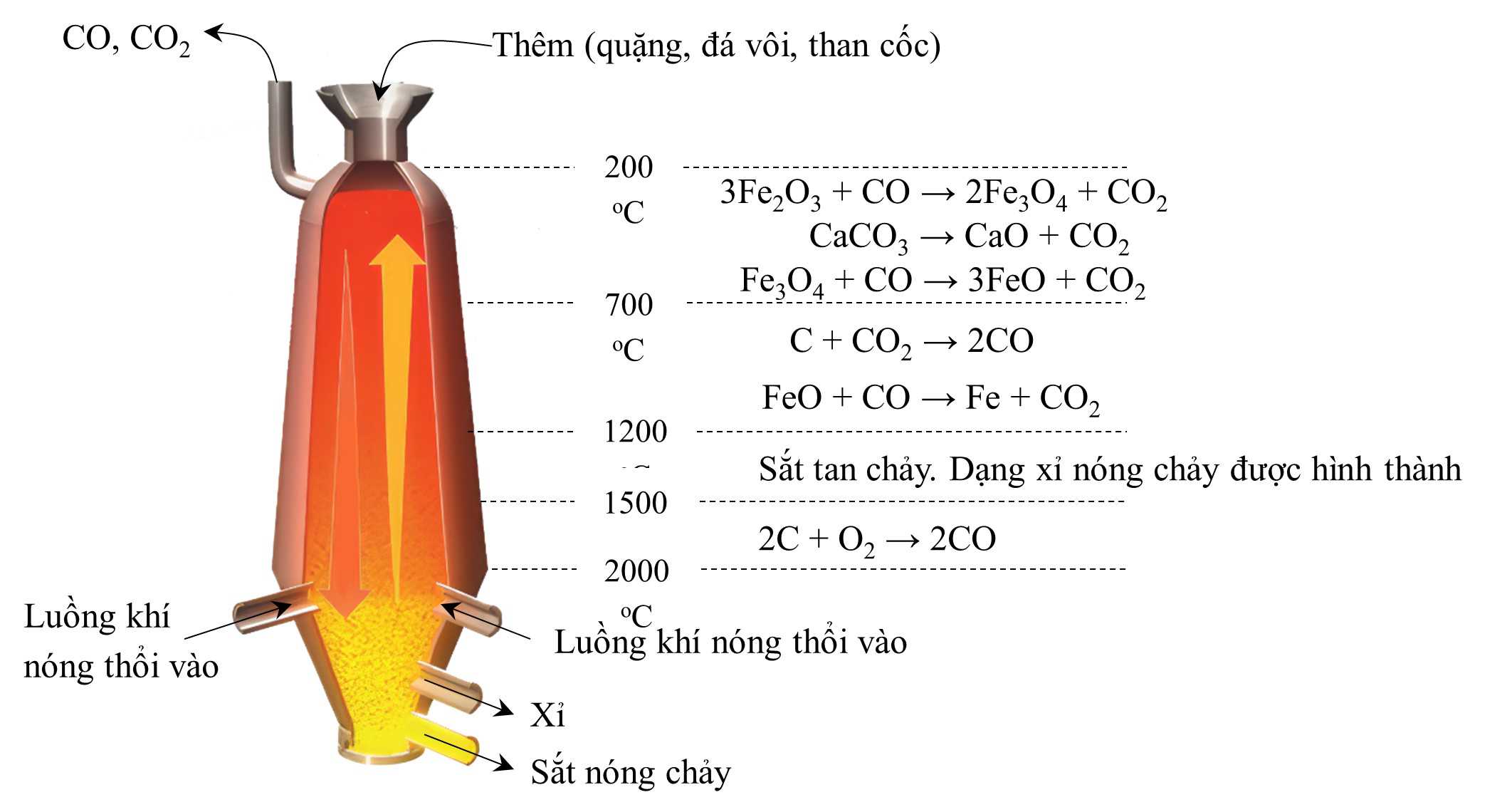
3Fe2O3(s) + CO(g) → 2Fe3O4(s) + CO2(g)
Fe3O4(s) + CO(g) → 3FeO(s) + CO2(g)
FeO(s) + CO(g) → Fe(l) + CO2(g)
Đá vôi phân hủy trong lò như sau:
CaCO3(s) → CaO(s) + CO2(g)
Calcium oxide (CaO) được sinh ra sẽ phản ứng với các tạp chất có trong quặng sắt, chủ yếu là cát (SiO2) và aluminium oxide (Al2O3):
CaO(s) + SiO2(s) → CaSiO3(l)
CaO(s) + Al2O3(s) → Ca(AlO2)2(l)
Hỗn hợp calcium silicate (CaSiO3) và calcium aluminate (Ca(AlO2)2) nóng chảy tại nhiệt độ trong lò được gọi là xỉ.
Vào thời điểm quặng đi xuống đáy lò, phần lớn quặng đã bị biến thành sắt. Nhiệt độ của phần dưới của lò cao hơn nhiệt độ nóng chảy của sắt, và do đó sắt sẽ nóng chảy và có thể chảy xuống thiết bị thu nằm ở phía bên dưới. Lớp xỉ ít đậm đặc hơn, nổi ở trên bề mặt tạo thành lớp trên cùng, phía trên sắt nóng chảy và có thể chảy ra ở lỗ thoát phía trên, như trong hình vẽ trên.
Sắt được chiết xuất theo cách này chứa nhiều tạp chất nên được gọi là gang; nó có thể chứa tới 5% carbon và một số nguyên tố khác như silicon, phosphorus, manganese và lưu huỳnh. Các tạp chất này có nguồn gốc từ khoáng chất silicate và phosphate, trong khi carbon và lưu huỳnh thì đến từ than cốc.
Gang có dạng hạt và giòn. Nó có điểm nóng chảy tương đối thấp (khoảng 1180°C), vì vậy nó có thể được đúc ở nhiều dạng khác nhau.
Câu 33 [560763]: Một loại hợp kim của sắt trong đó có nguyên tố C (5%) và một lượng rất ít các nguyên tố Si, Mn, S, P. Hợp kim đó là
A, gang.
B, thép.
C, canxi silicat.
D, xỉ.
Hợp kim của sắt với thành phần chính là C (carbon) khoảng 5% cùng một lượng rất ít các nguyên tố như Si (silic), Mn (mangan), S (lưu huỳnh), và P (phốt pho) được gọi là gang.
=> Chọn đáp án A Đáp án: A
=> Chọn đáp án A Đáp án: A
Câu 34 [560764]: Trong các phát biểu sau:
(i) CO đóng vai trò là chất khử.
(ii) Các tạp chất như cát (SiO2) và nhôm oxide (Al2O3) có trong than cốc.
(iii) Đá vôi được thêm vào để loại bỏ các tạp chất SiO2 và Al2O3.
(iv) Lớp xỉ lỏng nặng hơn lớp sắt lỏng nên chìm xuống phía dưới.
(v) Gang có nhiệt độ nóng chảy tương đối thấp khoảng 1180°C.
Số phát biểu đúng là
(i) CO đóng vai trò là chất khử.
(ii) Các tạp chất như cát (SiO2) và nhôm oxide (Al2O3) có trong than cốc.
(iii) Đá vôi được thêm vào để loại bỏ các tạp chất SiO2 và Al2O3.
(iv) Lớp xỉ lỏng nặng hơn lớp sắt lỏng nên chìm xuống phía dưới.
(v) Gang có nhiệt độ nóng chảy tương đối thấp khoảng 1180°C.
Số phát biểu đúng là
A, 1.
B, 2.
C, 3.
D, 4.
Các phát biểu đúng là (i); (iii); (v) Đáp án: C
Câu 35 [560765]: Tiến hành xác định hàm lượng carbon có trong một mẫu gang X. Cho 1,75 gam mẫu gang X phản ứng với khí O2 dư thu được 0,1568 lít khí CO2 (đktc). Thành phần phần trăm theo khối lượng của carbon trong mẫu gang đó là
A, 3,2 %.
B, 1,8 %.
C, 4,8 %.
D, 2,5 %.
nCO2= 0,1568/ 22,4 = 7.10-3 mol
=> Khối lượng C cần để xảy ra phản ứng tạo CO2 là 7.10-3. 12 =0,084 gam
=> %C = 0,084/1,75 .100% = 4,8%
=> Đáp án C Đáp án: C
=> Khối lượng C cần để xảy ra phản ứng tạo CO2 là 7.10-3. 12 =0,084 gam
=> %C = 0,084/1,75 .100% = 4,8%
=> Đáp án C Đáp án: C
THÉP
Sản xuất thép là một trong những ngành công nghiệp kim loại quan trọng nhất. Tại Hoa Kỳ, lượng tiêu thụ thép hàng năm vượt trên 100 triệu tấn. Thép là một hợp kim sắt có chứa từ 0,03 đến 1,4% carbon và nhiều nguyên tố khác.Trong khi sản xuất gang về cơ bản là một quá trình khử (chuyển sắt oxide thành sắt kim loại), thì việc chuyển hóa sắt thành thép về cơ bản là một quá trình oxi hóa trong đó các tạp chất không mong muốn được loại bỏ khỏi sắt bằng phản ứng với khí oxygen.
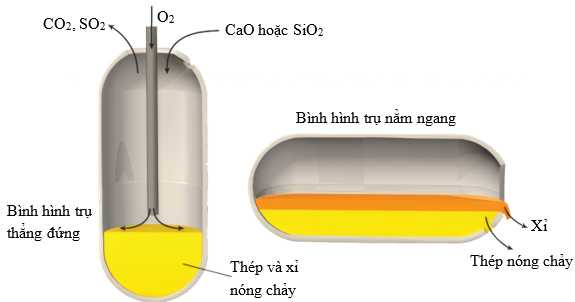
Hình 1. Quá trình oxi hóa cơ bản.
Sắt nóng chảy từ lò cao được đổ vào một bình hình trụ thẳng đứng. Khí oxygen được đưa vào bình thông qua một ống làm mát bằng nước phía trên lớp kim loại nóng chảy. Trong điều kiện này, manganese, phosphorus và silicon cũng như lượng carbon dư thừa sẽ phản ứng với oxygen để tạo thành oxide. Sau đó, các oxide này được phản ứng với các chất hỗ trợ thích hợp (ví dụ CaO) để tạo thành xỉ.SiO2(s) + CaO(s) → CaSiO3(l)
P4O10(l) + 6CaO(s) → 2Ca3(PO4)2(l)
Mặt khác, nếu manganese là tạp chất chính thì cần có chất hỗ trợ là SiO2 để tạo thành xỉ:
MnO(s) + SiO2(s) → MnSiO3(l)
Thép nóng chảy được lấy mẫu định kỳ. Khi đạt được sự pha trộn mong muốn giữa carbon và các tạp chất khác, bình được quay sang vị trí nằm ngang để có thể tách thép nóng chảy ra (Hình 2).
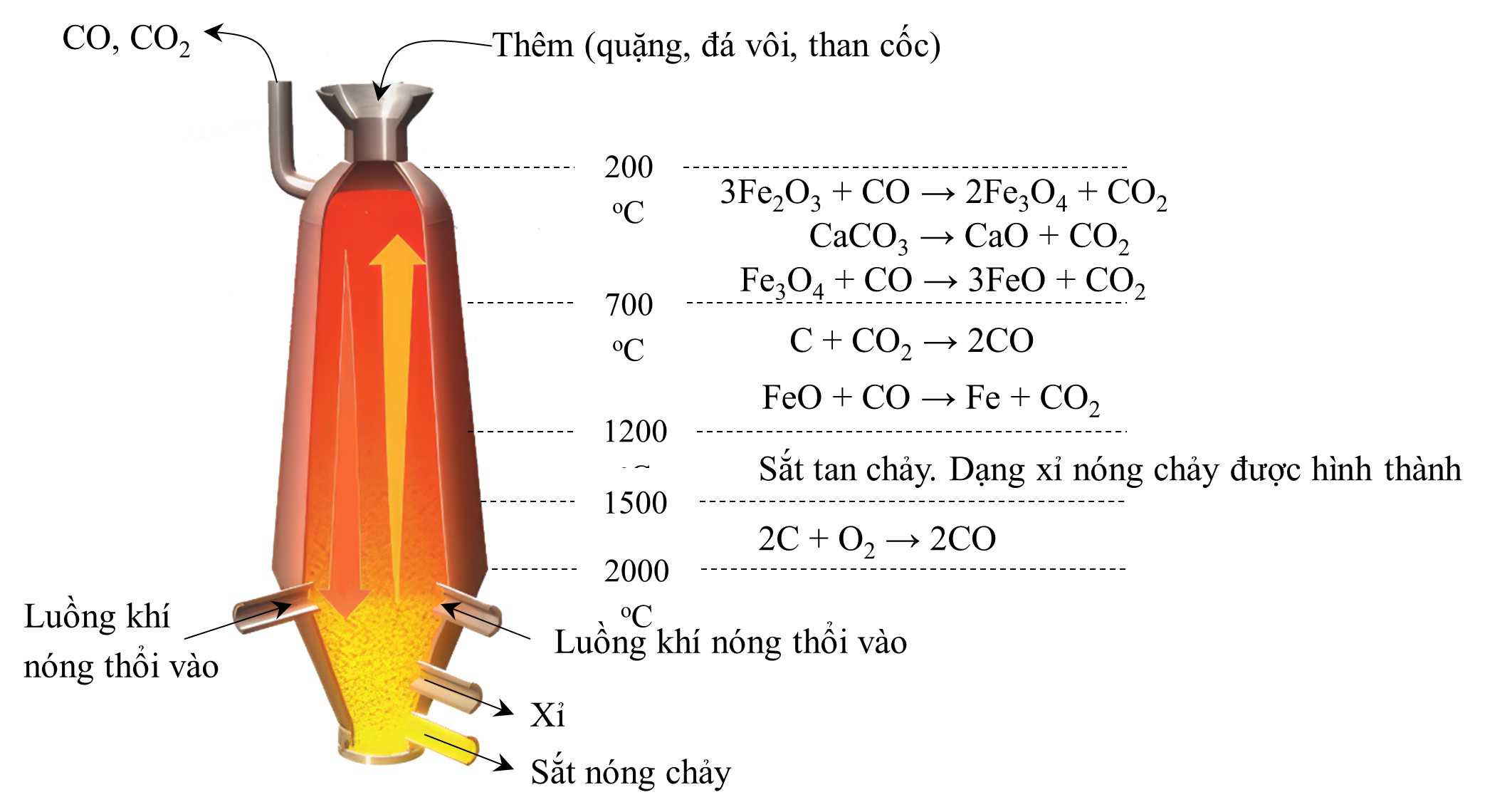
Hình 2.
Các tính chất của thép không chỉ phụ thuộc vào thành phần hóa học mà còn phụ thuộc vào quá trình xử lý nhiệt. Bảng 3 liệt kê thành phần, tính chất và công dụng của các loại thép.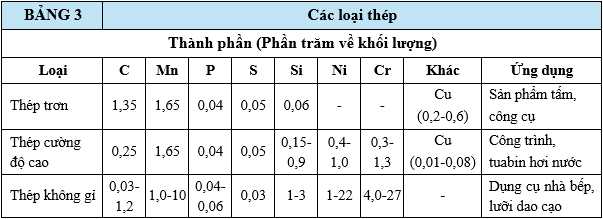
Câu 36 [560766]: Thép là hợp kim của sắt với carbon và một số nguyên tố khác trong đó hàm lượng carbon chiếm
A, trên 2%.
B, dưới 2%.
C, từ 2% đến 5%.
D, trên 5%.
Thép là hợp kim của Fe với carbon (C) và một số nguyên tố khác. Trong thép, hàm lượng carbon thường chiếm từ 0,02% đến 2,14% khối lượng, tùy thuộc vào loại thép. Hàm lượng carbon thấp hơn hoặc cao hơn phạm vi này sẽ tạo ra các vật liệu khác như sắt rèn (hàm lượng carbon thấp hơn 0,02%) hoặc gang (hàm lượng carbon lớn hơn 2,14%).
=> Chọn đáp án B Đáp án: B
=> Chọn đáp án B Đáp án: B
Câu 37 [560767]: Trong các phát biểu dưới đây:
(i) Khí oxygen có vai trò loại bỏ các tạp chất như manganese, phosphorus và silicon cũng như lượng carbon dư thừa.
(ii) Nếu manganese là tạp chất chính thì cần có chất hỗ trợ là CaO.
(iii) Tùy thuộc vào hàm lượng C mong muốn mà có thể tạo ra các loại thép khác nhau.
(iv) Xỉ có chứa các chất như CaSiO3, Ca3(PO4)2, MnSiO3.
Số phát biểu đúng là
(i) Khí oxygen có vai trò loại bỏ các tạp chất như manganese, phosphorus và silicon cũng như lượng carbon dư thừa.
(ii) Nếu manganese là tạp chất chính thì cần có chất hỗ trợ là CaO.
(iii) Tùy thuộc vào hàm lượng C mong muốn mà có thể tạo ra các loại thép khác nhau.
(iv) Xỉ có chứa các chất như CaSiO3, Ca3(PO4)2, MnSiO3.
Số phát biểu đúng là
A, 1.
B, 2.
C, 3.
D, 4.
Phát biểu đúng là (i); (iii) và (iv). Đáp án: C
Câu 38 [560768]: Nung một mẫu thép có khối lượng 20 gam trong O2 dư thu được 0,3136 lít khí CO2 (đktc). Thành phần phần trăm theo khối lượng của carbon trong mẫu thép đó là
A, 0,82%.
B, 0,84%.
C, 0,85%.
D, 0,86%.
nCO2= 0,3136/ 22,4 = 0,014 mol
=> Khối lượng C cần để xảy ra phản ứng tạo CO2 là 0,014 . 12 = 0,168 gam
=> %C = 0,168/20 .100% = 0,84%
=> Đáp án B Đáp án: B
=> Khối lượng C cần để xảy ra phản ứng tạo CO2 là 0,014 . 12 = 0,168 gam
=> %C = 0,168/20 .100% = 0,84%
=> Đáp án B Đáp án: B
ĐỒNG THAU
Đồng thau là hợp kim của đồng và kẽm. Tỉ lệ pha chế giữa đồng và kẽm cho ta một loạt các đồng thau đa dạng khác nhau có tính chất cơ học và điện khác nhau. Để phân tích Cu trong mẫu đồng thau, sinh viên thực hiện theo quy trình sau: hòa tan 2,8 gam hợp kim đồng thau trong dung dịch HNO3 đặc, nóng. Chuyển dung dịch thu được vào bình định mức 250,0 mL và định mức bằng nước cất đến vạch. Lấy 25,0 mL dung dịch, thêm Na2CO3 để trung hòa acid dư đến thoáng xuất hiện kết tủa, hòa tan kết tủa bằng dung dịch CH3COOH vừa đủ. Thêm KI dư và chuẩn độ I2 sinh ra bằng dung dịch Na2S2O3 0,100 M thấy hết 29,8 mL.Biết các phản ứng xảy ra như sau:
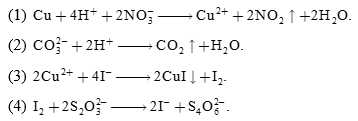
Câu 39 [560769]: Nếu mẫu đồng thau có lẫn kim loại nào sau đây thì sẽ ảnh hưởng đến quá trình chuẩn độ?
A, Fe.
B, Ag.
C, Al.
D, Sn.
- Ag+ phản ứng với I- tạo thành kết tủa AgI màu vàng nhạt, không tan trong nước và các axit loãng.
- Kết tủa AgI rất bền, khó hòa tan trong các dung dịch thông thường, do đó không thể khôi phục lượng I- đã bị kết tủa.
- Các kim loại khác như Hg, Pb cũng tạo kết tủa với I- nhưng mức độ ảnh hưởng có thể ít hơn Ag do độ tan của các kết tủa này có thể khác nhau.
=> Chọn đáp án B Đáp án: B
- Kết tủa AgI rất bền, khó hòa tan trong các dung dịch thông thường, do đó không thể khôi phục lượng I- đã bị kết tủa.
- Các kim loại khác như Hg, Pb cũng tạo kết tủa với I- nhưng mức độ ảnh hưởng có thể ít hơn Ag do độ tan của các kết tủa này có thể khác nhau.
=> Chọn đáp án B Đáp án: B
Câu 40 [560770]: Phát biểu nào sau đây không đúng?
A, Có thể sử dụng acid H2SO4 đặc để thay thế HNO3.
B, Có thể thay thế Na2CO3 bằng NH3 để trung hòa acid dư.
C, Tinh bột sử dụng làm chất chỉ thị phản ứng giữa I2 và Na2S2O3 được thêm vào khi dung dịch đã nguội.
D, Cần trung hòa acid dư vì trong môi trường acid mạnh: 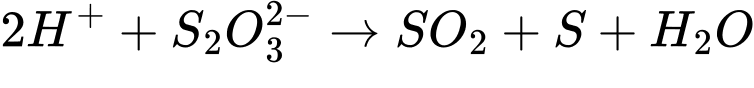 sẽ ảnh hưởng đến quá trình chuẩn độ.
sẽ ảnh hưởng đến quá trình chuẩn độ.
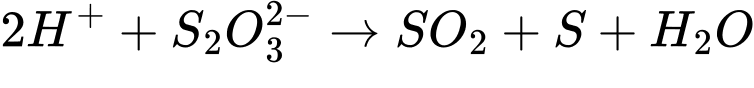 sẽ ảnh hưởng đến quá trình chuẩn độ.
sẽ ảnh hưởng đến quá trình chuẩn độ.
NH3 sẽ tạo phức và phức chất có thể có phản ứng oxi hóa khử với Na2S2O3 làm lệch kết quả của quá trình chuẩn độ.
Cu(NH3)4(OH)2 + Na2S2O3 ⟶ Na2SO4 + CuS + H2O + 4 NH3
Chọn đáp án B
Đáp án: B
Chọn đáp án B
Đáp án: B
Câu 41 [560771]: Phần trăm khối lượng Cu trong hợp kim đồng thau là (biết MCu = 63,45)
A, 57,8%.
B, 61,7%.
C, 63,5%.
D, 67,5%.
Chuẩn độ hết 29,8 mL Na2S2O3 0,1 M => nS2O32- = 2,98.10-3
Từ phương trình (4) => nI2 = 1,49.10-3
Từ phương trình (3) => nCu2+= 2,98.10-3
Vì chỉ lấy 25 ml dung dịch đem đi chuẩn độ nên nCu2+ trong 250mL dung dịch là 2,98.10-2
=> nCu =2,98.10-2
=> Khối lượng Cu là 2,98.10-2.63,45= 1,891 gam
=> Phần trăm Cu trong hợp kim là 1,891 / 2,8 .100% = 67,5% Đáp án: D
Từ phương trình (4) => nI2 = 1,49.10-3
Từ phương trình (3) => nCu2+= 2,98.10-3
Vì chỉ lấy 25 ml dung dịch đem đi chuẩn độ nên nCu2+ trong 250mL dung dịch là 2,98.10-2
=> nCu =2,98.10-2
=> Khối lượng Cu là 2,98.10-2.63,45= 1,891 gam
=> Phần trăm Cu trong hợp kim là 1,891 / 2,8 .100% = 67,5% Đáp án: D
HỢP KIM CỦA VÀNG
Vàng từ lâu đã là kim loại được lựa chọn làm đồ trang trí, đồ trang sức và tiền xu. Sự phổ biến của vàng là bởi màu sắc khác thường của nó, khả năng chống lại nhiều phản ứng hóa học và thực tế là nó có thể dễ dàng gia công. Tuy nhiên, vàng nguyên chất quá mềm đối với nhiều ứng dụng, kể cả đồ trang sức. Để tăng độ bền và độ cứng cũng như để thay đổi màu sắc, vàng thường được tạo hợp kim với các kim loại khác. Trong buôn bán đồ trang sức, vàng nguyên chất được gọi là 24 Karat. Số Karat giảm khi phần trăm khối lượng của vàng giảm. Các hợp kim phổ biến nhất được sử dụng trong đồ trang sức là 14 Karat, tức là (14/24) × 100 = 58% vàng và 18 Karat, tức là (18/24) × 100 = 75% vàng. Màu sắc của vàng thay đổi tùy thuộc vào kim loại đi cùng để tạo thành hợp kim với nó. Vàng thường được kết hợp với bạc hoặc đồng. Cả ba nguyên tố đều kết tinh với cấu trúc lập phương tâm mặt. Thực tế là cả ba nguyên tố đều có bán kính tương tự nhau (Au và Ag có kích thước gần như nhau; Cu nhỏ hơn khoảng 11%) và kết tinh với cùng loại cấu trúc nên có thể dễ dàng kết hợp với nhau theo mọi tỉ lệ. Sự thay đổi màu sắc của các hợp kim này theo thành phần được thể hiện trong Hình 12.18.
Vàng được kết hợp với bạc và đồng (chấm màu xanh) có màu vàng sáng mà chúng ta liên tưởng đến đồ trang sức bằng vàng 18 Karat. Vàng hồng (14 Karat) là hợp kim giàu đồng (chấm màu đỏ). Các hợp kim giàu bạc có màu xanh lục, cuối cùng dần chuyển sang màu trắng bạc vì bạc trở thành thành phần chính.
Mặc dù các loại vàng này thường được sử dụng tên thương mại giống nhau như vàng hồng, vàng đỏ, tuy nhiên chúng khác nhau về thành phần phần trăm nguyên tố: hàm lượng đồng càng cao thì màu đỏ càng đậm. Vàng hồng sử dụng ít đồng nhất, còn vàng đỏ có hàm lượng đồng cao nhất.
▪ Vàng đỏ 18K: 75% vàng, 25% đồng.
▪ Vàng hồng 18K: 75% vàng, 22,25% đồng, 2,75% bạc.
▪ Vàng hồng 18K: 75% vàng, 20% đồng, 5% bạc.
▪ Vàng đỏ 12K: 50% vàng và 50% đồng.
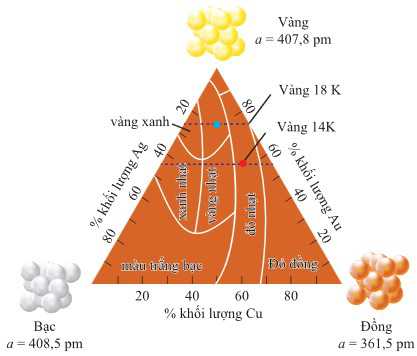
Hình vẽ. Màu sắc của hợp kim Au–Ag–Cu theo thành phần.
Câu 42 [560772]: Trong các loại vàng dưới đây, loại vàng nào chứa hàm lượng Au là lớn nhất?
A, 18K.
B, 14K.
C, 10K.
D, 9K.
Trong buôn bán đồ trang sức, vàng nguyên chất được gọi là 24 Karat (24K)
Loại vàng chứa hàm lượng Au lớn nhất trong 4 đáp án là 18K
Vàng 18K có chứa hàm lượng Au lớn nhất (75% Au).
⇒ Chọn đáp án A Đáp án: A
Loại vàng chứa hàm lượng Au lớn nhất trong 4 đáp án là 18K
Vàng 18K có chứa hàm lượng Au lớn nhất (75% Au).
⇒ Chọn đáp án A Đáp án: A
Câu 43 [560773]: Một loại nhẫn được chế tác từ hợp kim vàng 14K.

Xác định thành phần phần trăm khối lượng Au trong loại hợp kim trên.

Xác định thành phần phần trăm khối lượng Au trong loại hợp kim trên.
A, 58,33 %.
B, 41,67 %.
C, 75,00 %.
D, 83,33 %.
Vàng nguyên chất được gọi là 24 Karat
⇒ Vàng 14 Karat có chứa hàm lượng Au là: 14 ÷ 24 × 100% = 58,33%
⇒ Chọn đáp án A Đáp án: A
⇒ Vàng 14 Karat có chứa hàm lượng Au là: 14 ÷ 24 × 100% = 58,33%
⇒ Chọn đáp án A Đáp án: A
Câu 44 [560774]: Tiến hành trộn 10 gam vàng, 5 gam bạc và 5 gam đồng để chế tạo hợp kim. Giả sử trong quá trình chế tác không có sự thất thoát, loại hợp kim tạo ra có giá trị Karat bằng bao nhiêu?
A, 50K.
B, 20K.
C, 12K.
D, 8K.
Hàm lượng Au trong hợp kim trên là:
%mAu = 5 ÷ (5 + 5) × 100% = 50%
Trong buôn bán đồ trang sức, vàng nguyên chất được gọi là 24K
Loại hợp kim tạo ra có giá trị Karat là: 50% × 24 = 12K.
⇒ Chọn đáp án C Đáp án: C
%mAu = 5 ÷ (5 + 5) × 100% = 50%
Trong buôn bán đồ trang sức, vàng nguyên chất được gọi là 24K
Loại hợp kim tạo ra có giá trị Karat là: 50% × 24 = 12K.
⇒ Chọn đáp án C Đáp án: C
Dạng 5: CÂU HỎI TỰ LUẬN
Câu 45 [1016811]: Trong nhiều thế kỷ, các kim loại cơ bản Fe, Cu, Ni, Zn, Al, Sn và Pb đã được sử dụng làm thành phần hợp kim trong tiền xu. Nhìn chung, kim loại phải có độ bền tương đối để đảm bảo tuổi thọ của đồng xu, phải giữ được vẻ ngoài trong điều kiện khí quyển và không được quá đắt. Là một kim loại mềm và đắt tiền, vàng (gold) thường được kết hợp với đồng để tạo thành hợp kim bền. Đồng tiền vàng sovereign của Anh, hiện vẫn đang được đúc, được làm từ khoảng 91 % Au và 8,3 % Cu. Một đồng vàng sovereign được phân tích bằng quy trình hóa học sau:
▪ Bước 1: Cho đồng vàng sovereign phản ứng với nitric acid đậm đặc dư trong tủ hút.
Cu(s) + 4H+(aq) + 2NO3–(aq) → Cu2+(aq) + 2NO2(g) + 2H2O(1)
▪ Bước 2: Hỗn hợp sau phản ứng được lọc để loại bỏ vàng không phản ứng.
▪ Bước 3: Dung dịch sau lọc được pha loãng với nước cất đến thể tích 250 mL.
▪ Bước 4: Hút 25 mL dung dịch này vào bình tam giác và thêm lượng dư 50 mL dung dịch KI 1 M. Dung dịch thu được ngay lập tức chuyển sang màu cam nâu.
2Cu2+(aq) + 4I–(aq) → 2CuI(s) + I2(aq)
▪ Bước 5: Sau đó chuẩn độ dung dịch này bằng dung dịch Na2S2O3 0,05 M cho đến khi dung dịch chuyển sang màu vàng rơm.
2S2O32–(aq) + I2(aq) → 2I–(aq) + S4O62–(aq)
▪ Bước 6: Sau đó thêm chất chỉ thị tinh bột để tạo màu xanh đen.
▪ Bước 7: Thêm tiếp dung dịch Na2S2O3 cho đến khi dung dịch không màu. Ghi lại sự thay đổi thể tích dung dịch Na2S2O3 ở bảng dưới. Lặp lại chuẩn độ 3 lần và ghi lại kết quả chính xác đến 0,05 mL.
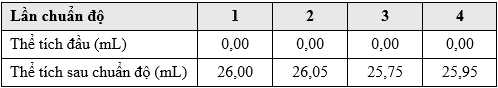
a) Tại sao phải thực hiện thí nghiệm trong tủ hút?
b) Trong số các thí nghiệm, kết quả của thí nghiệm nào không đáng tin cậy?
c) Nêu ý nghĩa của việc sử dụng tinh bột làm chất chỉ thị.
d) Từ các kết quả đáng tin cậy, xác định khối lượng Cu có trong đồng vàng sovereign.
▪ Bước 1: Cho đồng vàng sovereign phản ứng với nitric acid đậm đặc dư trong tủ hút.
Cu(s) + 4H+(aq) + 2NO3–(aq) → Cu2+(aq) + 2NO2(g) + 2H2O(1)
▪ Bước 2: Hỗn hợp sau phản ứng được lọc để loại bỏ vàng không phản ứng.
▪ Bước 3: Dung dịch sau lọc được pha loãng với nước cất đến thể tích 250 mL.
▪ Bước 4: Hút 25 mL dung dịch này vào bình tam giác và thêm lượng dư 50 mL dung dịch KI 1 M. Dung dịch thu được ngay lập tức chuyển sang màu cam nâu.
2Cu2+(aq) + 4I–(aq) → 2CuI(s) + I2(aq)
▪ Bước 5: Sau đó chuẩn độ dung dịch này bằng dung dịch Na2S2O3 0,05 M cho đến khi dung dịch chuyển sang màu vàng rơm.
2S2O32–(aq) + I2(aq) → 2I–(aq) + S4O62–(aq)
▪ Bước 6: Sau đó thêm chất chỉ thị tinh bột để tạo màu xanh đen.
▪ Bước 7: Thêm tiếp dung dịch Na2S2O3 cho đến khi dung dịch không màu. Ghi lại sự thay đổi thể tích dung dịch Na2S2O3 ở bảng dưới. Lặp lại chuẩn độ 3 lần và ghi lại kết quả chính xác đến 0,05 mL.

a) Tại sao phải thực hiện thí nghiệm trong tủ hút?
b) Trong số các thí nghiệm, kết quả của thí nghiệm nào không đáng tin cậy?
c) Nêu ý nghĩa của việc sử dụng tinh bột làm chất chỉ thị.
d) Từ các kết quả đáng tin cậy, xác định khối lượng Cu có trong đồng vàng sovereign.
a) Trong quá trình thực hiện thí nghiệm có sinh ra khí NO2 (khí độc, Gây kích ứng mạnh hệ hô hấp: ho, khó thở, đau ngực; đặc biệt nguy hiểm với trẻ em, người già và người có bệnh hen suyễn, phổi). Tủ hút giúp ngăn khí độc lan ra không khí, bảo vệ hệ hô hấp và sức khỏe.
b) Trong các thí nghiệm trên, kết quả thí nghiệm lần 3 không đáng tin cậy nhất nguyên do kết quả thu được thể tích Na2S2O3 là 25,75 mL lệch rất nhiều so với các kết quả khác nên độ tin cậy không cao.
c) Hồ tinh bột được sử dụng làm chỉ thị chủ yếu trong các phản ứng có mặt iodine (I2) nhờ khả năng tạo màu đặc trưng. Trong thí nghiệm trên dùng để nhận biết I2, khi dung dịch từ màu xanh sang không màu tức là toàn bọ I2 đã phản ứng hết với Na2S2O3.
d) Thể tích trung bình của Na2S2O3 là
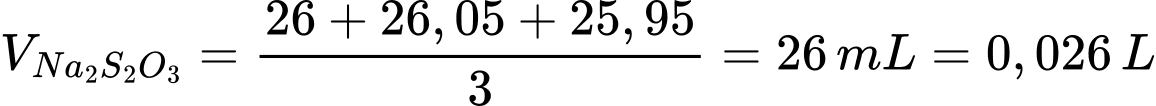
Số mol của Na2S2O3 là nNa2S2O3 = 0,026 × 0,05 = 0,0013 mol
Từ phương trình hoá học số mol của Cu là nCu = 0,0013 mol
Khối lượng của Cu trong đồng vàng trên là:
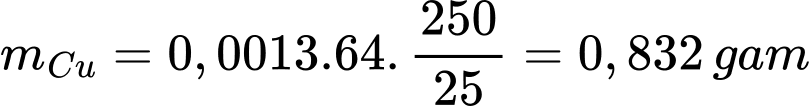
b) Trong các thí nghiệm trên, kết quả thí nghiệm lần 3 không đáng tin cậy nhất nguyên do kết quả thu được thể tích Na2S2O3 là 25,75 mL lệch rất nhiều so với các kết quả khác nên độ tin cậy không cao.
c) Hồ tinh bột được sử dụng làm chỉ thị chủ yếu trong các phản ứng có mặt iodine (I2) nhờ khả năng tạo màu đặc trưng. Trong thí nghiệm trên dùng để nhận biết I2, khi dung dịch từ màu xanh sang không màu tức là toàn bọ I2 đã phản ứng hết với Na2S2O3.
d) Thể tích trung bình của Na2S2O3 là
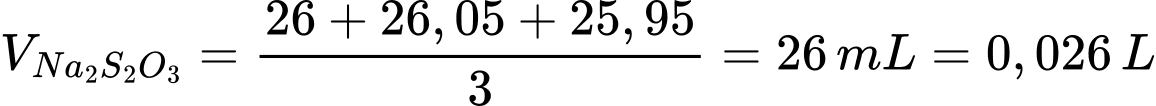
Số mol của Na2S2O3 là nNa2S2O3 = 0,026 × 0,05 = 0,0013 mol
Từ phương trình hoá học số mol của Cu là nCu = 0,0013 mol
Khối lượng của Cu trong đồng vàng trên là:
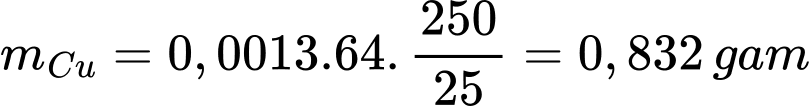
Câu 46 [1016812]: Phương pháp Volhard là phép chuẩn độ Ag(I) bởi dung dịch chuẩn potassium thiocyanate (KSCN), thường được tiến hành trong môi trường acid. Khi bạc(I) đã được kết tủa ở dạng kết tủa trắng AgSCN thì SCN– sẽ ngay lập tức phản ứng với chất chỉ thị sắt(III), tạo thành phức chất màu đỏ máu [FeSCN]2+. Có thể xác định hàm lượng bạc trong một hợp kim Ag–Cu bằng phương pháp Volhard, với quy trình như sau:
▪ Bước 1: Hòa tan hoàn toàn 0,3 gam hợp kim vào 5 mL dung dịch nitric acid đậm đặc, nồng độ 63%.
▪ Bước 2: Dung dịch tạo thành được pha loãng 4 – 5 lần và rồi nhỏ vào vài giọt dung dịch Fe(NO3)3 đậm đặc làm chất chỉ thị.
▪ Bước 3: Tiến hành chuẩn độ với dung dịch KSCN 0,100 M từ burette cho đến khi xuất hiện màu đỏ máu trên kết tủa trắng AgSCN trong bình tam giác. Thể tích dung dịch KSCN 0,100 M đã dùng là 20 mL.
Cho biết Cu(II) không phản ứng với ion thiocyanate SCN–.
a) Dấu hiệu tại điểm kết thúc chuẩn độ là gì?
b) Phần trăm khối lượng của Ag trong hợp kim là bao nhiêu?
c) So sánh độ bền của hai hợp chất AgSCN và [FeSCN]2+.
▪ Bước 1: Hòa tan hoàn toàn 0,3 gam hợp kim vào 5 mL dung dịch nitric acid đậm đặc, nồng độ 63%.
▪ Bước 2: Dung dịch tạo thành được pha loãng 4 – 5 lần và rồi nhỏ vào vài giọt dung dịch Fe(NO3)3 đậm đặc làm chất chỉ thị.
▪ Bước 3: Tiến hành chuẩn độ với dung dịch KSCN 0,100 M từ burette cho đến khi xuất hiện màu đỏ máu trên kết tủa trắng AgSCN trong bình tam giác. Thể tích dung dịch KSCN 0,100 M đã dùng là 20 mL.
Cho biết Cu(II) không phản ứng với ion thiocyanate SCN–.
a) Dấu hiệu tại điểm kết thúc chuẩn độ là gì?
b) Phần trăm khối lượng của Ag trong hợp kim là bao nhiêu?
c) So sánh độ bền của hai hợp chất AgSCN và [FeSCN]2+.
a) Trong phương pháp Volhard, điểm tương đương là khi toàn bộ Ag+ dư đã phản ứng hết với SCN-, và ngay sau đó, SCN⁻ dư phản ứng với Fe3+ tạo màu đỏ máu đặc trưng, dùng làm dấu hiệu xác định điểm kết thúc chuẩn độ.
b)
Đổi 20 mL = 0,02 L
Phản ứng chuẩn độ: Ag+ + SCN- → AgSCN
Số mol của KSCN là nKSCN = 0,02 × 0,1 = 0,002 mol
Từ phương trình hoá học số mol của Ag+ là 0,002 mol
Phần trăm khối lượng của Ag là: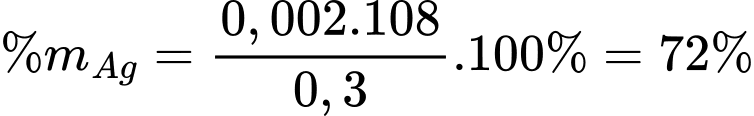
c) AgSCN là một muối kết tủa rất bền, có hằng số tan (Kₛₚ) rất nhỏ nên gần như không phân ly trong dung dịch. Trong khi đó, [FeSCN]2+ là một phức chất tan, có hằng số bền (Kf) khá lớn nhưng vẫn kém bền hơn AgSCN. Vì vậy, khi cùng tồn tại Ag+ và Fe3+, ion SCN⁻ sẽ ưu tiên tạo kết tủa AgSCN trước rồi mới tạo phức [FeSCN]2+. Do đó, AgSCN có độ bền cao hơn [FeSCN]2+.
b)
Đổi 20 mL = 0,02 L
Phản ứng chuẩn độ: Ag+ + SCN- → AgSCN
Số mol của KSCN là nKSCN = 0,02 × 0,1 = 0,002 mol
Từ phương trình hoá học số mol của Ag+ là 0,002 mol
Phần trăm khối lượng của Ag là:
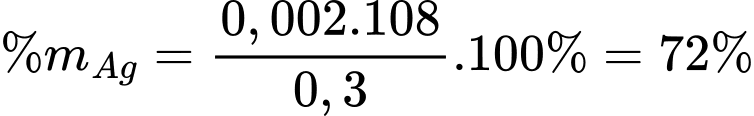
c) AgSCN là một muối kết tủa rất bền, có hằng số tan (Kₛₚ) rất nhỏ nên gần như không phân ly trong dung dịch. Trong khi đó, [FeSCN]2+ là một phức chất tan, có hằng số bền (Kf) khá lớn nhưng vẫn kém bền hơn AgSCN. Vì vậy, khi cùng tồn tại Ag+ và Fe3+, ion SCN⁻ sẽ ưu tiên tạo kết tủa AgSCN trước rồi mới tạo phức [FeSCN]2+. Do đó, AgSCN có độ bền cao hơn [FeSCN]2+.
Câu 47 [1016813]: Vận động viên Trần Lê Quốc Toàn đã giành tấm huy chương Đồng ở bộ môn cử tạ hạng 56 kg - Nam tại Thế vận hội mùa hè (Olympics) ở London năm 2012. Đây cũng là huy chương duy nhất của đoàn Việt Nam năm đó. Các huy chương Đồng được làm bằng hợp kim chứa đồng, kẽm và thiếc. Tiến hành quy trình phân tích định lượng sau:
▪ Bước 1: Hòa tan 0,800 g mẫu huy chương đồng vào dung dịch nitric acid đậm đặc, nóng.
▪ Bước 2: Sau khi làm nguội và pha loãng, thêm một lượng dư dung dịch potassium iodide vào rồi tiếp tục pha loãng dung dịch đến 250,0 mL.
2Cu2+(aq) + 4I–(aq) → 2CuI(s) + I2(aq)
▪ Bước 3: Chuẩn độ 25,00 mL mẫu dung dịch này bằng 12,20 mL dung dịch sodium thiosulfate (không màu) 0,100 M.
I2(aq) + 2S2O32–(aq) → 2I–(aq) + S4O62–(aq).
a) Nêu hiện tượng tại điểm kết thúc chuẩn độ.
b) Hàm lượng đồng trong chiếc huy chương là bao nhiêu?
c) Tại sao không xác định được hàm lượng đồng trong huy chương từ khối lượng của kết tủa CuI. Giải thích.
d) Sự có mặt của kẽm và thiếc trong huy chương có làm ảnh hưởng đến kết quả chuẩn độ ở bước 3 không? Giải thích.
▪ Bước 1: Hòa tan 0,800 g mẫu huy chương đồng vào dung dịch nitric acid đậm đặc, nóng.
▪ Bước 2: Sau khi làm nguội và pha loãng, thêm một lượng dư dung dịch potassium iodide vào rồi tiếp tục pha loãng dung dịch đến 250,0 mL.
2Cu2+(aq) + 4I–(aq) → 2CuI(s) + I2(aq)
▪ Bước 3: Chuẩn độ 25,00 mL mẫu dung dịch này bằng 12,20 mL dung dịch sodium thiosulfate (không màu) 0,100 M.
I2(aq) + 2S2O32–(aq) → 2I–(aq) + S4O62–(aq).
a) Nêu hiện tượng tại điểm kết thúc chuẩn độ.
b) Hàm lượng đồng trong chiếc huy chương là bao nhiêu?
c) Tại sao không xác định được hàm lượng đồng trong huy chương từ khối lượng của kết tủa CuI. Giải thích.
d) Sự có mặt của kẽm và thiếc trong huy chương có làm ảnh hưởng đến kết quả chuẩn độ ở bước 3 không? Giải thích.
a) Ban đầu: dung dịch có màu vàng nâu (do I2).
Khi thêm Na2S2O3, màu vàng nhạt dần.
Trước điểm kết thúc, có thể thêm vài giọt hồ tinh bột, dung dịch chuyển xanh tím đậm.
Tại điểm kết thúc: màu xanh tím biến mất, dung dịch trở lại không màu → chứng tỏ I2 đã bị khử hoàn toàn.
b) Đổi 12,2 mL = 0,0122 L
Số mol của Na2S2O3 là nNa2S2O3 = 0,0122 × 0,1 = 0,00122 mol
(1) 2Cu2+ + 4I- → 2CuI + I2
(2) I2 + 2S2O32- → 2I- + S4O62-
Từ phương trình hoá học số mol của Cu2+ là nCu = 0,00122 mol
Hàm lượng Cu trong mẫu huy chương đồng là
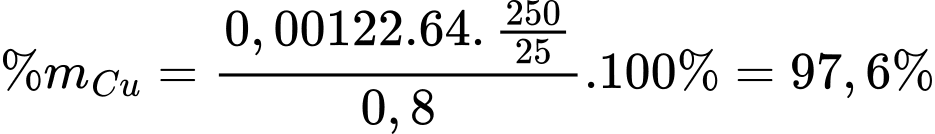
c) Không thể xác định hàm lượng đồng trong huy chương dựa vào khối lượng kết tủa CuI vì kết tủa này có thể lẫn tạp chất như iod tự do hoặc ion kim loại khác, đồng thời quá trình lọc, rửa và sấy kết tủa dễ gây sai số, làm sai lệch kết quả.
d) Sự có mặt của kẽm và thiếc trong huy chương không ảnh hưởng đến kết quả chuẩn độ ở bước 3, vì các ion Zn2+ và Sn2+ không phản ứng với ion iodua (I⁻) để tạo ra iod tự do (I2), nên không làm thay đổi lượng I₂ sinh ra cũng như không ảnh hưởng đến kết quả chuẩn độ bằng dung dịch sodium thiosulfate.
Khi thêm Na2S2O3, màu vàng nhạt dần.
Trước điểm kết thúc, có thể thêm vài giọt hồ tinh bột, dung dịch chuyển xanh tím đậm.
Tại điểm kết thúc: màu xanh tím biến mất, dung dịch trở lại không màu → chứng tỏ I2 đã bị khử hoàn toàn.
b) Đổi 12,2 mL = 0,0122 L
Số mol của Na2S2O3 là nNa2S2O3 = 0,0122 × 0,1 = 0,00122 mol
(1) 2Cu2+ + 4I- → 2CuI + I2
(2) I2 + 2S2O32- → 2I- + S4O62-
Từ phương trình hoá học số mol của Cu2+ là nCu = 0,00122 mol
Hàm lượng Cu trong mẫu huy chương đồng là
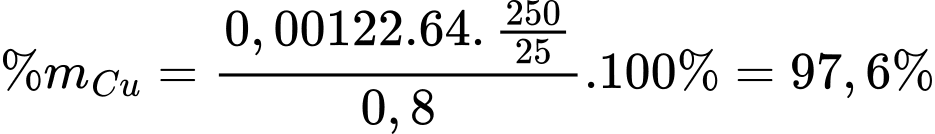
c) Không thể xác định hàm lượng đồng trong huy chương dựa vào khối lượng kết tủa CuI vì kết tủa này có thể lẫn tạp chất như iod tự do hoặc ion kim loại khác, đồng thời quá trình lọc, rửa và sấy kết tủa dễ gây sai số, làm sai lệch kết quả.
d) Sự có mặt của kẽm và thiếc trong huy chương không ảnh hưởng đến kết quả chuẩn độ ở bước 3, vì các ion Zn2+ và Sn2+ không phản ứng với ion iodua (I⁻) để tạo ra iod tự do (I2), nên không làm thay đổi lượng I₂ sinh ra cũng như không ảnh hưởng đến kết quả chuẩn độ bằng dung dịch sodium thiosulfate.