Dạng 1: TRẮC NGHIỆM KHÁCH QUAN: mỗi câu hỏi chỉ có một đáp án đúng.
Câu 1 [1016771]: Ở trạng thái cơ bản, cấu hình electron của nguyên tử Mg (Z = 12) là
A, 1s22s22p63s1.
B, 1s22s22p63s2.
C, 1s22s32p63s2.
D, 1s22s22p73s1.
Ở trạng thái cơ bản, cấu hình electron của nguyên tử Mg (Z = 12) là: 1s22s22p63s2.
Chọn đáp án B Đáp án: B
Chọn đáp án B Đáp án: B
Câu 2 [560595]: Nhôm là kim loại phổ biến nhất trong vỏ Trái Đất và có trong thành phần của đất sét, khoáng vật criolit, quặng boxide. Trong bảng tuần hoàn, nhôm thuộc chu kì 3, nhóm IIIA. Cấu hình electron lớp ngoài cùng của nguyên tử nhôm ở trạng thái cơ bản là
A, 3s23p3.
B, 3s23p1.
C, 3s23p4.
D, 3s23p5.
Nhôm thuộc chu kì 3, nhóm IIIA => nhôm chứa 3 lớp e và có 3 electron lớp ngoài cùng => cấu hình lớp e ngoài cùng là 3s23p1. Đáp án: B
Câu 3 [560596]: Sắt là kim loại được con người sử dụng với khối lượng lớn nhất, chiếm trên 90% tổng khối lượng các kim loại. Dựa vào cấu hình electron của nguyên tử Fe (ở trạng thái cơ bản) là [Ar]3d64s2 thì nguyên tố này được xếp vào bảng tuần hoàn ở nhóm
A, VIB.
B, VIIIA.
C, VIIIB.
D, VIIB.
Cấu hình electron phân lớp ngoài cùng và sát lớp ngoài cùng của Fe là 3d64s2
=> Fe là nguyên tố nhóm B.
Tổng electron của 2 phân lớp (n-1)d và ns là 6 + 2 = 8
=> Fe được xếp vào nhóm VIIIB Đáp án: C
=> Fe là nguyên tố nhóm B.
Tổng electron của 2 phân lớp (n-1)d và ns là 6 + 2 = 8
=> Fe được xếp vào nhóm VIIIB Đáp án: C
Câu 4 [1016772]: Nguyên tử X có cấu hình electron 1s22s22p63s1. Vị trí của nguyên tố X trong bảng tuần hoàn các nguyên tố hóa học là
A, chu kì 4, nhóm IIIA.
B, chu kì 3, nhóm IIA.
C, chu kì 3, nhóm IA.
D, chu kì 4, nhóm VIIA.
Cấu hình của nguyên tố X là 1s2 2s2 2p6 3s1
Có 3 lớp electron → Nguyên tố X thuộc chu kì 3
Có 1 electron lớp ngoài → Nguyên tố X thuộc nhóm IA
⟹ Chọn đáp án C Đáp án: C
Có 3 lớp electron → Nguyên tố X thuộc chu kì 3
Có 1 electron lớp ngoài → Nguyên tố X thuộc nhóm IA
⟹ Chọn đáp án C Đáp án: C
Câu 5 [1016773]: Vị trí kim loại nhóm IA trong bảng tuần hoàn các nguyên tố hóa học thường
A, ở đầu nhóm.
B, ở cuối nhóm.
C, ở đầu chu kì.
D, ở cuối chu kì.
Kim loại nhóm IA (kim loại kiềm) nằm ở nhóm 1, khối s, phía ngoài cùng bên trái của bảng tuần hoàn, từ chu kỳ 2 đến chu kỳ 7. Chúng gồm các nguyên tố: Li, Na, K, Rb, Cs và Fr, đều có một electron ở lớp ngoài cùng (cấu hình ns1). Đây là những kim loại mềm, có tính khử mạnh, dễ bị oxi hóa, phản ứng mạnh với nước tạo dung dịch kiềm và khí hydrogen.
⟹ Chọn đáp án C Đáp án: C
⟹ Chọn đáp án C Đáp án: C
Câu 6 [1016774]: Cấu hình electron nào sau đây là của nguyên tử kim loại?
A, 1s22s22p6.
B, 1s22s22p63s23p4.
C, 1s22s22p63s23p5.
D, 1s22s22p63s1.
Nguyên tử kim loại thường có số electron lớp ngoài cùng là 1; 2; 3 electron lớp ngoài cùng.
Câu hình 1s2 2s2 2p6 3s1 là nguyên tố kim loại nguyên do có 1 electron ở lớp thứ 3.
⟹ Chọn đáp án D Đáp án: D
Câu hình 1s2 2s2 2p6 3s1 là nguyên tố kim loại nguyên do có 1 electron ở lớp thứ 3.
⟹ Chọn đáp án D Đáp án: D
Câu 7 [1016775]: Trong bảng tuần hoàn các nguyên tố kim loại thường có
A, 4 electron ở lớp ngoài cùng.
B, 1, 2, 3 electron ở lớp ngoài cùng.
C, 5, 6, 7 electron ở lớp ngoài cùng.
D, 8 electron ở lớp ngoài cùng.
Trong bảng tuần hoàn, các nguyên tố kim loại thường có 1, 2 hoặc 3 electron ở lớp ngoài cùng. Điều này giúp chúng dễ mất electron để tạo thành ion dương (cation), thể hiện tính kim loại mạnh. Cụ thể:
- Kim loại nhóm IA có 1 electron lớp ngoài (ns1),
- Nhóm IIA có 2 electron (ns2),
- Nhóm IIIA (như Al) có 3 electron (ns2np1). Số electron lớp ngoài quyết định hóa trị và tính chất hóa học đặc trưng của các kim loại này.
⟹ Chọn đáp án B Đáp án: B
- Kim loại nhóm IA có 1 electron lớp ngoài (ns1),
- Nhóm IIA có 2 electron (ns2),
- Nhóm IIIA (như Al) có 3 electron (ns2np1). Số electron lớp ngoài quyết định hóa trị và tính chất hóa học đặc trưng của các kim loại này.
⟹ Chọn đáp án B Đáp án: B
Câu 8 [560598]: Dãy gồm các kim loại có cùng kiểu mạng tinh thể lập phương tâm khối là
A, Na, K, Ba.
B, Mg, Ca, Ba.
C, Na, K , Ca.
D, Li , Na, Mg.
★ Mạng tinh thể lập phương tâm khối (Li, Na, K, Ba,...)
★ Mạng tinh thể lập phương tâm diện (Cu, Al, Ag, Ca...)
★ Mạng tinh thể lục phương (Be, Mg, Zn,...)
=> Chọn đáp án A
Đáp án: A
★ Mạng tinh thể lập phương tâm diện (Cu, Al, Ag, Ca...)
★ Mạng tinh thể lục phương (Be, Mg, Zn,...)
=> Chọn đáp án A
Đáp án: A
Câu 9 [703815]: “Trong tinh thể kim loại, liên kết kim loại được hình thành do ...(1)... giữa các electron hoá trị tự do với các ...(2)... kim loại ở các nút mạng”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, lực hút tĩnh điện, ion dương.
B, lực hút tĩnh điện, ion âm.
C, lực hạt nhân, ion dương.
D, lực đẩy tĩnh điện, ion âm.
Trong tinh thể kim loại, các nguyên tử kim loại giải phóng electron hóa trị (electron ở lớp ngoài cùng) để trở thành ion dương. Lực hút tĩnh điện giữa các electron tự do và ion dương kim loại là yếu tố chính giữ các ion dương ở vị trí cố định trong mạng tinh thể. Do đó, lực hút tĩnh điện là đặc trưng cơ bản của liên kết kim loại.
⇒ Trong tinh thể kim loại, liên kết kim loại được hình thành do lực hút tĩnh điện giữa các electron hoá trị tự do với các ion dương kim loại ở các nút mạng.
Chọn đáp án A Đáp án: A
⇒ Trong tinh thể kim loại, liên kết kim loại được hình thành do lực hút tĩnh điện giữa các electron hoá trị tự do với các ion dương kim loại ở các nút mạng.
Chọn đáp án A Đáp án: A
Câu 10 [702828]: Tinh thể kim loại chứa các …(1)… sắp xếp theo trật tự nhất định cùng với các …(2)… chuyển động tự do. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, hạt kim loại, hạt nhân nguyên tử.
B, hạt nhân nguyên tử, hạt kim loại.
C, electron tự do, cation kim loại.
D, cation kim loại, electron tự do.
- Trong kim loại, khi các nguyên tử mất đi electron ở lớp vỏ ngoài cùng sẽ trở thành các ion dương (cation). Những ion này chiếm các vị trí cố định trong mạng tinh thể kim loại, tạo nên cấu trúc trật tự.
- Các electron bị mất không bị giữ cố định bởi bất kỳ ion dương nào mà chuyển động tự do trong tinh thể kim loại.
⇒ Tinh thể kim loại chứa các cation kim loại sắp xếp theo trật tự nhất định cùng với các electron tự do chuyển động tự do.
Chọn đáp án D Đáp án: D
- Các electron bị mất không bị giữ cố định bởi bất kỳ ion dương nào mà chuyển động tự do trong tinh thể kim loại.
⇒ Tinh thể kim loại chứa các cation kim loại sắp xếp theo trật tự nhất định cùng với các electron tự do chuyển động tự do.
Chọn đáp án D Đáp án: D
Câu 11 [1016776]: Liên kết trong mạng tinh thể kim loại là loại liên kết nào sau đây?
A, Liên kết ion.
B, Liên kết cộng hoá trị.
C, Liên kết hydrogen.
D, Liên kết kim loại.
Liên kết kim loại được hình thành do lực hút tĩnh điện giữa các electron hóa trị tự do và các ion dương kim loại trong mạng tinh thể. Các electron này không thuộc về riêng nguyên tử nào mà di chuyển tự do trong toàn bộ mạng tinh thể, tạo thành "biển electron" liên kết các ion kim loại lại với nhau.
⟹ Chọn đáp án D Đáp án: D
⟹ Chọn đáp án D Đáp án: D
Câu 12 [706006]: Tinh thể kim loại M
A, mang điện tích dương.
B, mang điện tích âm.
C, trung hòa về điện.
D, không xác định.
Phân tích các đáp án :
❌A. Mang điện tích dương: Trong kim loại, các nguyên tử kim loại liên kết với nhau bằng liên kết kim loại. Các ion dương (cation) nằm trong "biển electron" tự do, nhưng tổng thể tinh thể kim loại không mang điện tích dương vì số lượng electron vẫn đủ để cân bằng với ion dương.
❌B. Mang điện tích âm: Dù có các electron tự do di chuyển, tinh thể kim loại không bị thừa electron đến mức mang điện tích âm.
✔️C. Trung hòa về điện: Trong trạng thái tự nhiên, tinh thể kim loại có tổng điện tích bằng 0 do số proton trong hạt nhân cân bằng với số electron trong hệ thống.
❌D. Không xác định: Điện tích của tinh thể kim loại đã được xác định rõ ràng là trung hòa về điện, nên đáp án này không chính xác.
⟹ Chọn đáp án C Đáp án: C
❌A. Mang điện tích dương: Trong kim loại, các nguyên tử kim loại liên kết với nhau bằng liên kết kim loại. Các ion dương (cation) nằm trong "biển electron" tự do, nhưng tổng thể tinh thể kim loại không mang điện tích dương vì số lượng electron vẫn đủ để cân bằng với ion dương.
❌B. Mang điện tích âm: Dù có các electron tự do di chuyển, tinh thể kim loại không bị thừa electron đến mức mang điện tích âm.
✔️C. Trung hòa về điện: Trong trạng thái tự nhiên, tinh thể kim loại có tổng điện tích bằng 0 do số proton trong hạt nhân cân bằng với số electron trong hệ thống.
❌D. Không xác định: Điện tích của tinh thể kim loại đã được xác định rõ ràng là trung hòa về điện, nên đáp án này không chính xác.
⟹ Chọn đáp án C Đáp án: C
Câu 13 [560597]: Một cấu trúc mạng tinh thể kim loại được thể hiện trong sơ đồ. Nội dung nào là phù hợp để điền vào vị trí của X, Y.
A, A: Cation kim loại, B: các ion tích điện âm.
B, A: proton tích điện dương, B: Anion phi kim.
C, A: Cation kim loại, B: Các electron tự do.
D, A: proton tích điện dương, B: Các electron tự do.
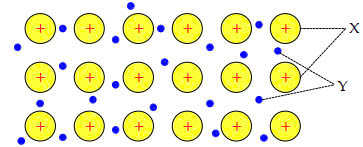
=> X là cation kim loại, Y là các electron tự do.
=> Chọn đáp án C
Câu 14 [560601]: Sự giống nhau giữa liên kết kim loại và liên kết ion là đều có
A, các cation kim loại.
B, các anion.
C, các electron.
D, tương tác tĩnh điện.
So sánh liên kết ion và liên kết kim loại:
★ Giống nhau: đều có tương tác tĩnh điện hình thành giữa điện tích âm và điện tích dương.
★ Khác nhau:
+ Liên kết ion: do lực hút tĩnh điện giữa hai ion mang điện tích trái dấu: anion(-) và phần dương do cation kim loại hoặc NH4+ tạo thành.
+ Liên kết kim loại: do các electron tự do trong kim loại và cation kim loại.
⇒ Chọn đáp án D Đáp án: D
★ Giống nhau: đều có tương tác tĩnh điện hình thành giữa điện tích âm và điện tích dương.
★ Khác nhau:
+ Liên kết ion: do lực hút tĩnh điện giữa hai ion mang điện tích trái dấu: anion(-) và phần dương do cation kim loại hoặc NH4+ tạo thành.
+ Liên kết kim loại: do các electron tự do trong kim loại và cation kim loại.
⇒ Chọn đáp án D Đáp án: D
Câu 15 [1016777]: Trong mạng tinh thể kim loại chứa các cation kim loại được sắp xếp theo một trật tự nhất định cùng với các electron chuyển động
A, theo một quỹ đạo xác định.
B, xung quanh một vị trí xác định.
C, tự do trong toàn bộ mạng tinh thể.
D, trong một khu vực không gian nhất định.
Trong mạng tinh thể kim loại, các cation kim loại (là phần còn lại sau khi nguyên tử kim loại mất electron hóa trị) được sắp xếp theo trật tự nhất định tạo thành mạng tinh thể.
Các electron hóa trị không gắn chặt với một nguyên tử nào mà chuyển động tự do trong toàn bộ mạng tinh thể, tạo thành "mây electron" hay "gas electron tự do".
Chính sự chuyển động tự do này giúp kim loại: Dẫn điện tốt; Dẫn nhiệt tốt; Có tính dẻo, dễ dát mỏng.
⟹ Chọn đáp án C Đáp án: C
Các electron hóa trị không gắn chặt với một nguyên tử nào mà chuyển động tự do trong toàn bộ mạng tinh thể, tạo thành "mây electron" hay "gas electron tự do".
Chính sự chuyển động tự do này giúp kim loại: Dẫn điện tốt; Dẫn nhiệt tốt; Có tính dẻo, dễ dát mỏng.
⟹ Chọn đáp án C Đáp án: C
Câu 16 [560599]: Liên kết kim loại được hình thành bởi
A, Lực hút tĩnh điện giữa các nguyên tử.
B, Lực hút tĩnh điện giữa các hạt tích điện dương và các electron hóa trị tự do.
C, Lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
D, Lực hút tĩnh điện giữa hạt nhân hai nguyên tử và cặp electron dùng chung.
Liên kết kim loại là liên kết hình thành từ lực hút tĩnh điện giữa các cation kim loại và các electron hóa trị tự do trong tinh thể kim loại. Đáp án: B
Câu 17 [560600]: Phát biểu nào sau đây về liên kết kim loại là đúng?
A, Liên kết kim loại là liên kết được hình thành từ lực hút tĩnh điện giữa các cation kim loại và các electron hoá trị tự do. Vì vậy, liên kết kim loại cũng chính là liên kết ion.
B, Liên kết kim loại được hình thành do giữa các nguyên tử kim loại có sự dùng chung các electron hoá trị tự do. Vì vậy, liên kết kim loại cũng chính là liên kết cộng hoá trị.
C, Liên kết kim loại là liên kết được hình thành từ lực hút tĩnh điện giữa các cation kim loại và các electron hoá trị tự do trong tinh thể kim loại.
D, Liên kết kim loại là liên kết được hình thành do sự xen phủ các orbital chứa electron hoá trị tự do của các nguyên tử kim loại.
Liên kết kim loại là liên kết hình thành từ lực hút tĩnh điện giữa các cation kim loại và các electron hóa trị tự do trong tinh thể kim loại. Đáp án: C
Câu 18 [1016778]: Hình vẽ nào sau đây có thể được dùng để mô tả cấu trúc tinh thể kim loại?
A, 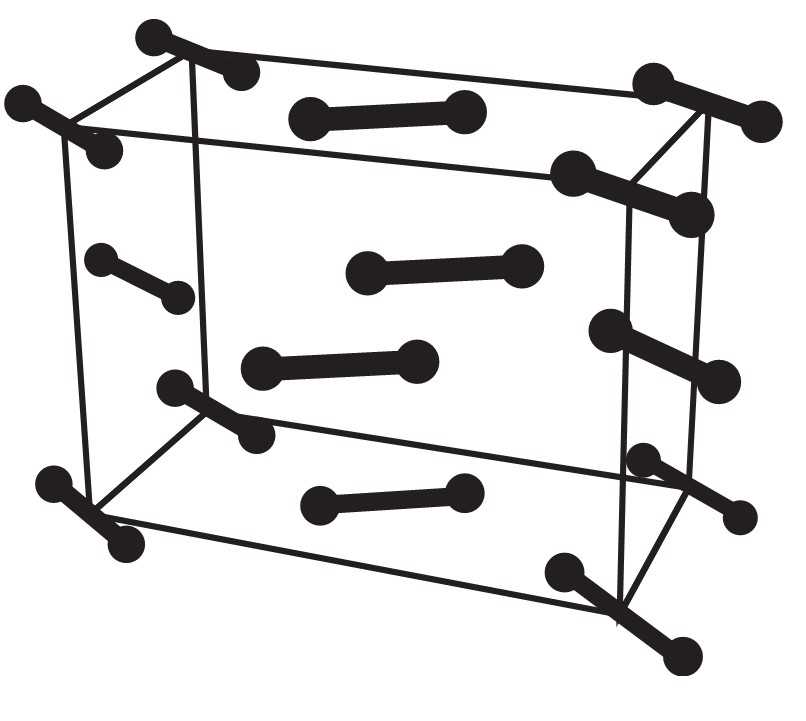

B, 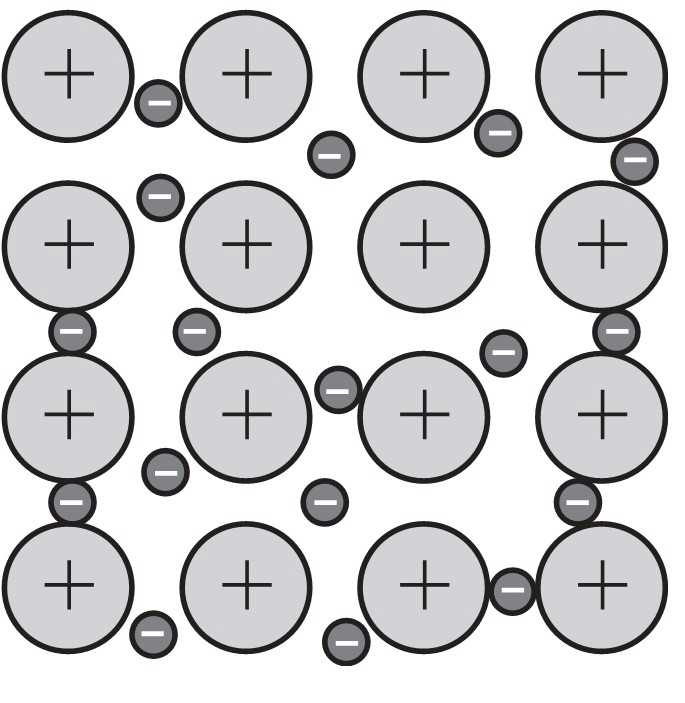

C, 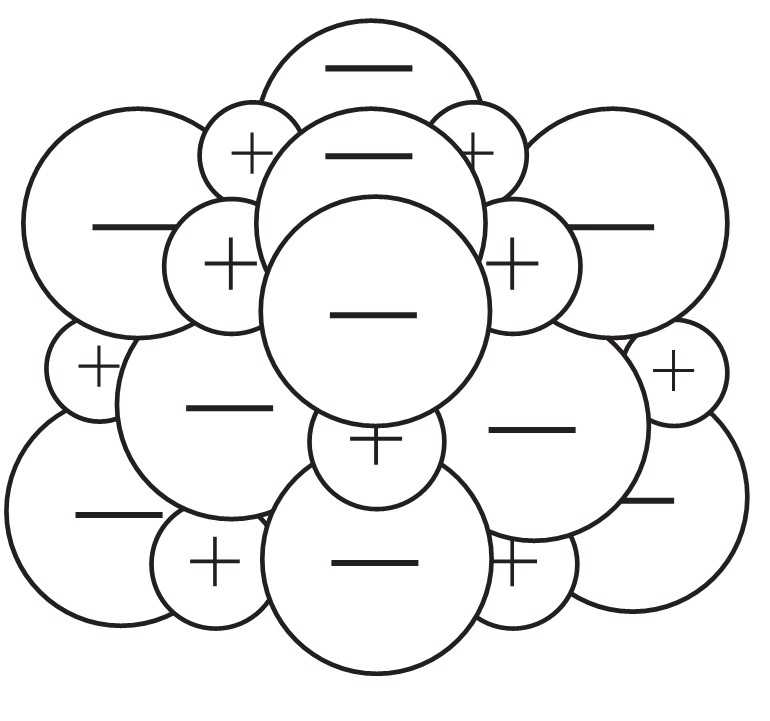

D, 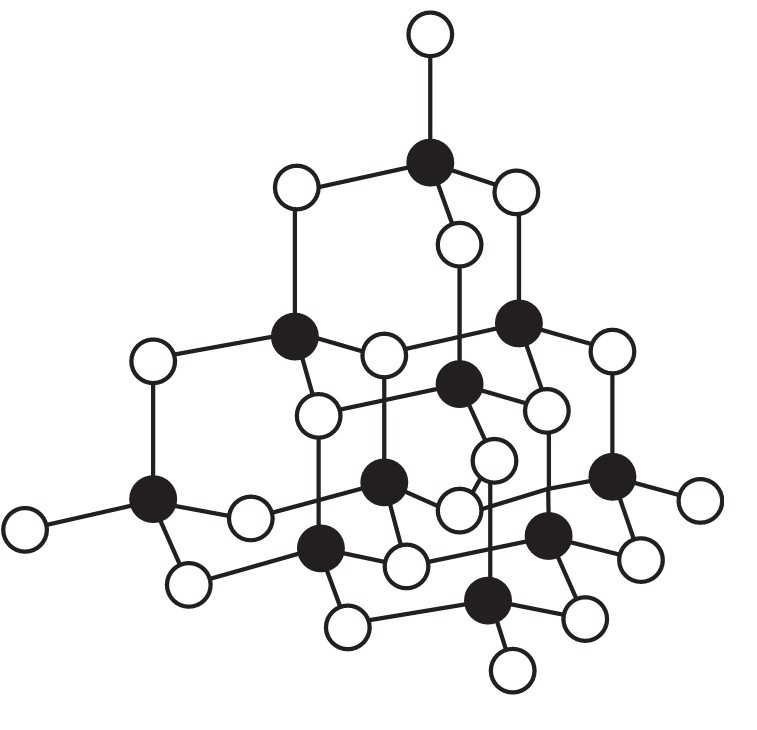

Trong mạng tinh thể kim loại, các cation kim loại (là phần còn lại sau khi nguyên tử kim loại mất electron hóa trị) được sắp xếp theo trật tự nhất định tạo thành mạng tinh thể.
Các electron hóa trị không gắn chặt với một nguyên tử nào mà chuyển động tự do trong toàn bộ mạng tinh thể, tạo thành "mây electron" hay "gas electron tự do".
Các electron hóa trị không gắn chặt với một nguyên tử nào mà chuyển động tự do trong toàn bộ mạng tinh thể, tạo thành "mây electron" hay "gas electron tự do".
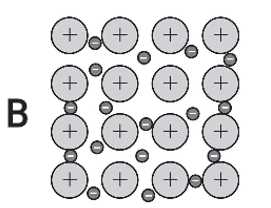
⟹ Chọn đáp án B
Câu 19 [706040]: Phát biểu nào sau đây là không đúng?
A, Ở điều kiện thường, tất cả các kim loại đều tồn tại ở thể rắn và có cấu tạo tinh thể.
B, Các cation kim loại và nguyên tử kim loại được sắp xếp trật tự trong tinh thể kim loại.
C, Electron hoá trị của nguyên tử kim loại chịu lực hút yếu của hạt nhân nguyên tử.
D, Giống như liên kết ion, liên kết kim loại cũng được hình thành từ tương tác tĩnh điện.
Phân tích các đáp án :
❌A – Sai. Ở điều kiện thường, hầu như các kim loại đều tồn tại ở thể rắn và có cấu tạo tinh thể ngoại trừ Hg ở trạng thái lỏng ở dk thường.
✔️B – Đúng. Các cation kim loại và nguyên tử kim loại được sắp xếp trật tự trong tinh thể kim loại.
✔️(c) – Đúng. Electron hoá trị của nguyên tử kim loại chịu lực hút yếu của hạt nhân nguyên tử, vì ở lớp ngoài cùng cách xa hạt nhân nhất nên ít chịu ảnh hưởng bởi hạt nhân.
✔️(d) – Đúng. Giống như liên kết ion, liên kết kim loại cũng được hình thành từ tương tác tĩnh điện.
So sánh liên kết kim loại với liên kết ion.
- Giống nhau: đều là liên kết sinh ra bởi lực hút tĩnh điện.
- Khác nhau:
+ Liên kết ion: do lực hút tĩnh điện giữa hai ion mang điện tích trái dấu.
+ Liên kết kim loại: lực hút tĩnh điện sinh ra do các electron tự do trong kim loại và ion dương kim loại.
⟹ Chọn đáp án A Đáp án: A
❌A – Sai. Ở điều kiện thường, hầu như các kim loại đều tồn tại ở thể rắn và có cấu tạo tinh thể ngoại trừ Hg ở trạng thái lỏng ở dk thường.
✔️B – Đúng. Các cation kim loại và nguyên tử kim loại được sắp xếp trật tự trong tinh thể kim loại.
✔️(c) – Đúng. Electron hoá trị của nguyên tử kim loại chịu lực hút yếu của hạt nhân nguyên tử, vì ở lớp ngoài cùng cách xa hạt nhân nhất nên ít chịu ảnh hưởng bởi hạt nhân.
✔️(d) – Đúng. Giống như liên kết ion, liên kết kim loại cũng được hình thành từ tương tác tĩnh điện.
So sánh liên kết kim loại với liên kết ion.
- Giống nhau: đều là liên kết sinh ra bởi lực hút tĩnh điện.
- Khác nhau:
+ Liên kết ion: do lực hút tĩnh điện giữa hai ion mang điện tích trái dấu.
+ Liên kết kim loại: lực hút tĩnh điện sinh ra do các electron tự do trong kim loại và ion dương kim loại.
⟹ Chọn đáp án A Đáp án: A
Câu 20 [706200]: Cho các phát biểu sau về tinh thể kim loại M:
(1) Tinh thể kim loại M trung hoà về điện.
(2) Trong tinh thể kim loại M có các cation Mn⁺ và các electron hoá trị tự do.
(3) Trong tinh thể kim loại M có các electron hoá trị tự do chuyển động.
(4) Trong tinh thể kim loại M, các cation Mn+ và electron hoá trị tự do được phân bố theo trật tự nhất định.
Số phát biểu đúng là
(1) Tinh thể kim loại M trung hoà về điện.
(2) Trong tinh thể kim loại M có các cation Mn⁺ và các electron hoá trị tự do.
(3) Trong tinh thể kim loại M có các electron hoá trị tự do chuyển động.
(4) Trong tinh thể kim loại M, các cation Mn+ và electron hoá trị tự do được phân bố theo trật tự nhất định.
Số phát biểu đúng là
A, 2.
B, 3.
C, 4.
D, 1.
Phân tích các phát biểu:
✔️Đúng. (1) Tinh thể kim loại M trung hòa về điện:
✔️Đúng. (1) Tinh thể kim loại M trung hòa về điện:
Tinh thể kim loại được tạo thành từ các ion kim loại dương (cation) và electron tự do, tổng điện tích của chúng cân bằng.
✔️ Đúng. (2) Trong tinh thể kim loại M có các cation Mn+ và các electron hóa trị tự do
Các nguyên tử kim loại mất electron hóa trị để tạo thành cation, các electron này di chuyển tự do trong mạng tinh thể.
✔️Đúng. (3) Trong tinh thể kim loại M có các electron hóa trị tự do chuyển động.
Đây là đặc điểm quan trọng của kim loại, giúp chúng dẫn điện và dẫn nhiệt tốt.
❌Sai. (4) Trong tinh thể kim loại M, các cation Mn+ và electron hóa trị tự do được phân bố theo trật tự nhất định.Các electron tự do không được sắp xếp theo trật tự nhất định, chúng chuyển động hỗn loạn.
Số phát biểu đúng: (1), (2), (3)
Số phát biểu đúng: (1), (2), (3)
⟹ Chọn đáp án B
Dạng 2: TRẮC NGHIỆM ĐÚNG SAI – mỗi ý a), b), c), d) chọn đúng hoặc sai.
Câu 21 [560629]: Do số lượng electron hóa trị ít và bán kính nguyên tử lớn nên các electron này dễ dàng tách ra khỏi các nguyên tử kim loại, hình thành nên tính khử của kim loại.
Phân tích các phát biểu sau:
✔️a. Đúng. Trong cùng một chu kì, kim loại thường nằm ở phía bên trái bảng tuần hoàn, có bán kính nguyên tử lớn hơn phi kim nằm ở bên phải do số proton và lực hút hạt nhân yếu hơn
❌ b. Sai. Điện tích hạt nhân lớn làm lực hút giữa hạt nhân và electron lớp ngoài cùng mạnh hơn, khiến electron khó bị tách ra, làm giảm tính khử. Tính khử mạnh hơn ở những nguyên tố có bán kính lớn và lực hút hạt nhân yếu (như ở các kim loại kiềm hoặc kiềm thổ).
✔️ c. Đúng. Kim loại thường có 1, 2, 3 electron lớp ngoài cùng.
✔️ d. Đúng. Trong cùng một nhóm, khi đi từ trên xuống, bán kính nguyên tử tăng, lực hút giữa hạt nhân và electron lớp ngoài cùng giảm, làm electron dễ bị mất hơn, tính khử tăng.
✔️a. Đúng. Trong cùng một chu kì, kim loại thường nằm ở phía bên trái bảng tuần hoàn, có bán kính nguyên tử lớn hơn phi kim nằm ở bên phải do số proton và lực hút hạt nhân yếu hơn
❌ b. Sai. Điện tích hạt nhân lớn làm lực hút giữa hạt nhân và electron lớp ngoài cùng mạnh hơn, khiến electron khó bị tách ra, làm giảm tính khử. Tính khử mạnh hơn ở những nguyên tố có bán kính lớn và lực hút hạt nhân yếu (như ở các kim loại kiềm hoặc kiềm thổ).
✔️ c. Đúng. Kim loại thường có 1, 2, 3 electron lớp ngoài cùng.
✔️ d. Đúng. Trong cùng một nhóm, khi đi từ trên xuống, bán kính nguyên tử tăng, lực hút giữa hạt nhân và electron lớp ngoài cùng giảm, làm electron dễ bị mất hơn, tính khử tăng.
Câu 22 [560630]: Mô hình mô tả khái quát cation kim loại và các electron hoá trị tự do trong tinh thể kim loại
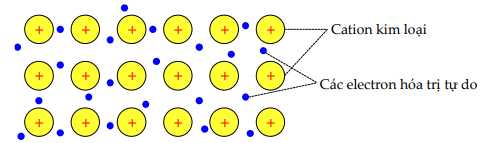

Phân tích các phát biểu sau:
✔️a. Đúng. Tinh thể kim loại gồm các cation kim loại và electron hóa trị tự do.
❌ b. Sai. Các electron chuyển động tự do trong tinh thể kim loại từ nguyên tử kim loại này đến nguyên tử kim loại khác, không theo một hướng nhất định.
✔️ c. Đúng. Các cation kim loại được sắp xếp theo một trật tự nhất định.
❌ d. Sai. Liên kết kim loại tạo thành từ lực hút tĩnh điện. Liên kết cộng hóa trị được hình thành tự sự dùng chung electron giữa 2 nguyên tử tham gia liên kết.
✔️a. Đúng. Tinh thể kim loại gồm các cation kim loại và electron hóa trị tự do.
❌ b. Sai. Các electron chuyển động tự do trong tinh thể kim loại từ nguyên tử kim loại này đến nguyên tử kim loại khác, không theo một hướng nhất định.
✔️ c. Đúng. Các cation kim loại được sắp xếp theo một trật tự nhất định.
❌ d. Sai. Liên kết kim loại tạo thành từ lực hút tĩnh điện. Liên kết cộng hóa trị được hình thành tự sự dùng chung electron giữa 2 nguyên tử tham gia liên kết.
Câu 23 [560631]: Ở điều kiện thường, trừ thủy ngân ở thể lỏng, các kim loại khác đều tồn tại ở thể rắn và có cấu tạo tinh thể được thể hiện dưới dạng mô hình khái quát như hình dưới đây.
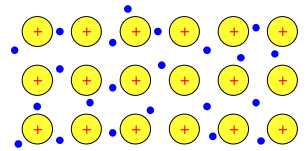

Phân tích các phát biểu sau:
✔️a. Đúng. Trong tinh thể kim loại M có các cation Mn+ và các electron hóa trị tự do.
❌ b. Sai. Các cation Mn+ được sắp xếp theo trật tự nhất định.
❌ c. Sai. Lực hút giữa Mn+ và electron hóa trị tự do trong liên kết kim loại không phụ thuộc vào độ âm điện, mà chủ yếu dựa vào bán kính cation, điện tích ion, và mật độ electron tự do.
❌ d. Sai. Trong tinh thể kim loại M, các cation Mn+ phân bố theo trật tự nhất định cùng với electron chuyển động tự do.
✔️a. Đúng. Trong tinh thể kim loại M có các cation Mn+ và các electron hóa trị tự do.
❌ b. Sai. Các cation Mn+ được sắp xếp theo trật tự nhất định.
❌ c. Sai. Lực hút giữa Mn+ và electron hóa trị tự do trong liên kết kim loại không phụ thuộc vào độ âm điện, mà chủ yếu dựa vào bán kính cation, điện tích ion, và mật độ electron tự do.
❌ d. Sai. Trong tinh thể kim loại M, các cation Mn+ phân bố theo trật tự nhất định cùng với electron chuyển động tự do.
Dạng 3: TRẮC NGHIỆM YÊU CẦU TRẢ LỜI NGẮN
Câu 24 [560634]: Cấu hình electron nguyên tử nguyên tố X là 1s22s22p63s23p1. Số hiệu nguyên tử của X là
Số hiệu nguyên tử của X là 2 + 2 + 6 + 2 + 1 = 13
⟹ Điền đáp án: 13
⟹ Điền đáp án: 13
Câu 25 [1016779]: Nguyên tử của nguyên tố Mg (Z = 12) có bao nhiêu electron ở lớp ngoài cùng?
Magnesium có số hiệu nguyên tử là 12 → nguyên tử Mg có 12 electron.
Cấu hình electron nguyên tử magie là 1s2 2s2 2p6 3s2 → Nguyên tử Mg có 2 electron lớp ngoài cùng.
Magnesium có số hiệu nguyên tử là 12 → nguyên tử Mg có 12 electron.
⟹ Điền đáp án 2
Cấu hình electron nguyên tử magie là 1s2 2s2 2p6 3s2 → Nguyên tử Mg có 2 electron lớp ngoài cùng.
Magnesium có số hiệu nguyên tử là 12 → nguyên tử Mg có 12 electron.
⟹ Điền đáp án 2
Câu 26 [1016780]: Nguyên tử của nguyên tố K (Z = 19) có bao nhiêu electron ở lớp ngoài cùng?
Potassium có kí hiệu hóa học là K.
Potassium có số hiệu nguyên tử là 19 → nguyên tử K có 19 electron.
Cấu hình electron nguyên tử K là 1s22s22p63s23p64s1 → Nguyên tử K có 1 electron lớp ngoài cùng.
⟹ Điền đáp án 1
Potassium có số hiệu nguyên tử là 19 → nguyên tử K có 19 electron.
Cấu hình electron nguyên tử K là 1s22s22p63s23p64s1 → Nguyên tử K có 1 electron lớp ngoài cùng.
⟹ Điền đáp án 1
Câu 27 [1016781]: Calcium là một loại khoáng chất cực kỳ quan trọng đối với sự phát triển của cơ thể, chiếm khoảng 1 - 2% trọng lượng cơ thể ở một người trưởng thành. Số hiệu nguyên tử của calcium là 20, hãy cho biết số electron lớp ngoài cùng trong cấu hình electron nguyên tử của calcium.
Calcium có kí hiệu hóa học là Ca.
Calcium có số hiệu nguyên tử là 20 → nguyên tử Ca có 20 electron.
Cấu hình electron nguyên tử K là 1s22s22p63s23p64s2 → Nguyên tử Ca có 2 electron lớp ngoài cùng.
⟹ Điền đáp án 2
Calcium có số hiệu nguyên tử là 20 → nguyên tử Ca có 20 electron.
Cấu hình electron nguyên tử K là 1s22s22p63s23p64s2 → Nguyên tử Ca có 2 electron lớp ngoài cùng.
⟹ Điền đáp án 2
Câu 28 [1016782]: Đồng (Copper - Cu) được dùng làm lõi dây dẫn điện, que hàn đồng, đúc tượng, nam châm điện từ, các động cơ máy móc,… Cấu hình electron 2 phân lớp ngoài cùng trong nguyên tử đồng là 3d104s1. Hãy cho biết số hiệu nguyên tử của đồng là bao nhiêu?
Cấu hình electron của 2 phân lớp ngoài cùng là 3d10 4s1
Cấu hình elctron của Cu là 1s22s22p63s23p63d104s1 → nguyên tử Cu có số hiệu nguyên tử là 29 electron.
⟹ Điền đáp án 29
Cấu hình elctron của Cu là 1s22s22p63s23p63d104s1 → nguyên tử Cu có số hiệu nguyên tử là 29 electron.
⟹ Điền đáp án 29
Câu 29 [1016783]: Cho cấu hình electron của một số nguyên tử sau:
(a) 1s22s22p63s23p64s1
(b) 1s22s22p63s23p5
(c) 1s22s22p63s1
(d) 1s2
(e) 1s22s22p1
(g) 1s22s22p63s23p63d64s2
Có bao nhiêu cấu hình electron là của nguyên tử kim loại?
(a) 1s22s22p63s23p64s1
(b) 1s22s22p63s23p5
(c) 1s22s22p63s1
(d) 1s2
(e) 1s22s22p1
(g) 1s22s22p63s23p63d64s2
Có bao nhiêu cấu hình electron là của nguyên tử kim loại?
Nguyên tử kim loại thường có số electron lớp ngoài cùng là 1; 2; 3 electron lớp ngoài cùng.
Các cấu hình electron là của nguyên tử kim loại là
(a) 1s22s22p63s23p64s1
(c) 1s22s22p63s1
(g) 1s22s22p63s23p63d64s2
Cấu hình (d) 1s2 là của khí hiếm; (b) 1s22s22p63s23p5 là của phi kim; (e) 1s22s22p1 cấu hình của B là nguyên tố phi kim
⟹ Điền đáp án 3
Các cấu hình electron là của nguyên tử kim loại là
(a) 1s22s22p63s23p64s1
(c) 1s22s22p63s1
(g) 1s22s22p63s23p63d64s2
Cấu hình (d) 1s2 là của khí hiếm; (b) 1s22s22p63s23p5 là của phi kim; (e) 1s22s22p1 cấu hình của B là nguyên tố phi kim
⟹ Điền đáp án 3
Câu 30 [1016784]: Cho các nhận định sau:
(a) Các kim loại thuộc nhóm IA, IIA bao gồm các nguyên tố s;
(b) Nguyên tử của hầu hết các kim loại có từ 1 đến 3 electron ở lớp ngoài cùng;
(c) Nguyên tử kim loại dễ nhường electron hơn so với các nguyên tử phi kim;
(d) Trong mạng tinh thể kim loại các electron chuyển động tự do theo nhiều hướng.
Có bao nhiêu nhận định đúng?
(a) Các kim loại thuộc nhóm IA, IIA bao gồm các nguyên tố s;
(b) Nguyên tử của hầu hết các kim loại có từ 1 đến 3 electron ở lớp ngoài cùng;
(c) Nguyên tử kim loại dễ nhường electron hơn so với các nguyên tử phi kim;
(d) Trong mạng tinh thể kim loại các electron chuyển động tự do theo nhiều hướng.
Có bao nhiêu nhận định đúng?
Phân tích các phát biểu:
✔️(a) – Đúng. Vì các nguyên tố nhóm IA (cấu hình ns1) và IIA (ns2) đều có electron cuối cùng điền vào phân lớp s → thuộc khối s.
✔️(b) – Đúng. Kim loại nhóm IA có 1e, IIA có 2e, IIIA (như Al) có 3e lớp ngoài → phần lớn kim loại có 1–3 e lớp ngoài cùng.
✔️(c) – Đúng. Tính kim loại là dễ nhường e, còn tính phi kim là dễ nhận e → đây là đặc trưng cơ bản của kim loại.
✔️(d) – Đúng. Các electron tự do không bị gắn cố định, chuyển động hỗn loạn theo nhiều hướng trong mạng tinh thể → chính điều này giúp kim loại dẫn điện, dẫn nhiệt.
Số phát biểu đúng là 4
⟹ Điền đáp án 4
✔️(a) – Đúng. Vì các nguyên tố nhóm IA (cấu hình ns1) và IIA (ns2) đều có electron cuối cùng điền vào phân lớp s → thuộc khối s.
✔️(b) – Đúng. Kim loại nhóm IA có 1e, IIA có 2e, IIIA (như Al) có 3e lớp ngoài → phần lớn kim loại có 1–3 e lớp ngoài cùng.
✔️(c) – Đúng. Tính kim loại là dễ nhường e, còn tính phi kim là dễ nhận e → đây là đặc trưng cơ bản của kim loại.
✔️(d) – Đúng. Các electron tự do không bị gắn cố định, chuyển động hỗn loạn theo nhiều hướng trong mạng tinh thể → chính điều này giúp kim loại dẫn điện, dẫn nhiệt.
Số phát biểu đúng là 4
⟹ Điền đáp án 4
Dạng 4: CÂU HỎI TỰ LUẬN
Câu 31 [1016785]: Viết cấu hình electron của nguyên tử Sc (Z = 21) và Ti (Z = 22). Cho biết số electron ở lớp ngoài cùng và trên phân lớp d sát lớp ngoài cùng.
Cấu hình electron của scandium (Sc) được viết là 1s2 2s2 2p6 3s2 3p6 3d1 4s2
Cấu hình electron của Titanium (Ti) được viết là 1s2 2s2 2p6 3s2 3p6 3d2 4s2
Cả 2 nguyên tử Sc và Ti đều có 2 e lớp ngoài cùng
Nguyên tử Sc có 1 electron thuộc phân lớp d, nguyên tử Ti có 2 e thuộc phân lớp d.
Cấu hình electron của Titanium (Ti) được viết là 1s2 2s2 2p6 3s2 3p6 3d2 4s2
Cả 2 nguyên tử Sc và Ti đều có 2 e lớp ngoài cùng
Nguyên tử Sc có 1 electron thuộc phân lớp d, nguyên tử Ti có 2 e thuộc phân lớp d.
Câu 32 [1016786]: Electron “cuối cùng” (electron có năng lượng cao nhất) của các nguyên tố X, Y, Z phân bố vào các phân lớp 3p1, 3d6, 4s2.
a) Dựa vào cấu hình electron, dự đoán vị trí của các nguyên tố (ô nguyên tố, số thứ tự chu kì, nhóm nguyên tố, khối nguyên tố) trong bảng tuần hoàn.
b) Các nguyên tố này là kim loại hay phi kim?
a) Dựa vào cấu hình electron, dự đoán vị trí của các nguyên tố (ô nguyên tố, số thứ tự chu kì, nhóm nguyên tố, khối nguyên tố) trong bảng tuần hoàn.
b) Các nguyên tố này là kim loại hay phi kim?
a) Electron “cuối cùng” (electron có năng lượng cao nhất) của các nguyên tố X, Y, Z phân bố vào các phân lớp 3p1, 3d6, 4s2.
→ Cấu hình electron của các nguyên tố X, Y, Z là
(X) 1s2 2s2 2p6 3s2 3p1
(Y) 1s2 2s2 2p6 3s2 3p6 3d6 4s2
(Z) 1s2 2s2 2p6 3s2 3p6 4s2
Nguyên tố X: electron cuối cùng phân bố vào 3p1
• Cấu hình e đầy đủ: 1s2 2s2 2p6 3s2 3p1
• Tổng số electron = 13 → Z = 13
• Ô nguyên tố: số 13
• Chu kỳ: 3 (vì electron ngoài cùng ở phân lớp 3p)
• Có 3 elctron hóa trị → Nhóm: IIIA
Nguyên tố Y: electron cuối cùng phân bố vào 3d6
• Trước 3d là 4s2 → Cấu hình e: 1s2 2s2 2p6 3s2 3p6 4s2 3d6
• Tổng số electron = 26 → Z = 26
• Ô nguyên tố: số 26
• Chu kỳ: 4 (vì lớp ngoài cùng là n = 4)
• Có 8 elctron hóa trị → Nhóm VIIIB
Nguyên tố Z: electron cuối cùng phân bố vào 4s2
• Cấu hình e: 1s2 2s2 2p6 3s2 3p6 4s2
• Tổng số electron = 20 → Z = 20
• Ô nguyên tố: số 20
• Chu kỳ: 4
• Có 2 elctron hóa trị → Nhóm: IIA
b) Nguyên tố X có 3 electron lớp ngoài cùng, Y có 2 electron lớp ngoài cùng, Z có 2 electron lớp ngoài cùng đều là kim loại.
→ Cấu hình electron của các nguyên tố X, Y, Z là
(X) 1s2 2s2 2p6 3s2 3p1
(Y) 1s2 2s2 2p6 3s2 3p6 3d6 4s2
(Z) 1s2 2s2 2p6 3s2 3p6 4s2
Nguyên tố X: electron cuối cùng phân bố vào 3p1
• Cấu hình e đầy đủ: 1s2 2s2 2p6 3s2 3p1
• Tổng số electron = 13 → Z = 13
• Ô nguyên tố: số 13
• Chu kỳ: 3 (vì electron ngoài cùng ở phân lớp 3p)
• Có 3 elctron hóa trị → Nhóm: IIIA
Nguyên tố Y: electron cuối cùng phân bố vào 3d6
• Trước 3d là 4s2 → Cấu hình e: 1s2 2s2 2p6 3s2 3p6 4s2 3d6
• Tổng số electron = 26 → Z = 26
• Ô nguyên tố: số 26
• Chu kỳ: 4 (vì lớp ngoài cùng là n = 4)
• Có 8 elctron hóa trị → Nhóm VIIIB
Nguyên tố Z: electron cuối cùng phân bố vào 4s2
• Cấu hình e: 1s2 2s2 2p6 3s2 3p6 4s2
• Tổng số electron = 20 → Z = 20
• Ô nguyên tố: số 20
• Chu kỳ: 4
• Có 2 elctron hóa trị → Nhóm: IIA
b) Nguyên tố X có 3 electron lớp ngoài cùng, Y có 2 electron lớp ngoài cùng, Z có 2 electron lớp ngoài cùng đều là kim loại.
Câu 33 [1016787]: So sánh liên kết kim loại với liên kết ion và liên kết cộng hoá trị.
Liên kết kim loại, liên kết ion, và liên kết cộng hóa trị là ba loại liên kết hóa học chính, mỗi loại có những đặc điểm và tính chất riêng biệt.
⭐Liên kết kim loại:
Định nghĩa: Liên kết kim loại là lực hút tĩnh điện giữa các cation kim loại và các electron tự do (biển electron) trong mạng tinh thể kim loại.
Đặc điểm: Tính dẫn điện tốt: Các electron tự do dễ dàng di chuyển dưới tác dụng của điện trường, mang điện tích. Tính dẫn nhiệt tốt: Các electron tự do truyền năng lượng nhiệt dễ dàng. Tính dẻo: Các lớp nguyên tử kim loại có thể trượt lên nhau dễ dàng mà không làm gãy liên kết.
⭐Liên kết ion:
Định nghĩa: Liên kết ion hình thành do sự chuyển electron từ nguyên tử kim loại sang phi kim, tạo ra các ion mang điện tích trái dấu (cation và anion) hút nhau bằng lực hút tĩnh điện.
Đặc điểm: Thường gặp trong hợp chất muối; Tính giòn: Các ion mang điện tích cùng dấu đẩy nhau khi bị xê dịch, làm gãy tinh thể; Dẫn điện khi nóng chảy hoặc hòa tan trong nước: Các ion có thể di chuyển tự do.
⭐Liên kết cộng hóa trị:
Định nghĩa: Liên kết cộng hóa trị hình thành khi hai nguyên tử phi kim chia sẻ electron để tạo thành cặp electron dùng chung.
Đặc điểm: Thường gặp trong phân tử của các phi kim; Không dẫn điện (trừ một số trường hợp đặc biệt như graphit); Tính chất của chất phụ thuộc vào cấu trúc phân tử.
⭐Liên kết kim loại:
Định nghĩa: Liên kết kim loại là lực hút tĩnh điện giữa các cation kim loại và các electron tự do (biển electron) trong mạng tinh thể kim loại.
Đặc điểm: Tính dẫn điện tốt: Các electron tự do dễ dàng di chuyển dưới tác dụng của điện trường, mang điện tích. Tính dẫn nhiệt tốt: Các electron tự do truyền năng lượng nhiệt dễ dàng. Tính dẻo: Các lớp nguyên tử kim loại có thể trượt lên nhau dễ dàng mà không làm gãy liên kết.
⭐Liên kết ion:
Định nghĩa: Liên kết ion hình thành do sự chuyển electron từ nguyên tử kim loại sang phi kim, tạo ra các ion mang điện tích trái dấu (cation và anion) hút nhau bằng lực hút tĩnh điện.
Đặc điểm: Thường gặp trong hợp chất muối; Tính giòn: Các ion mang điện tích cùng dấu đẩy nhau khi bị xê dịch, làm gãy tinh thể; Dẫn điện khi nóng chảy hoặc hòa tan trong nước: Các ion có thể di chuyển tự do.
⭐Liên kết cộng hóa trị:
Định nghĩa: Liên kết cộng hóa trị hình thành khi hai nguyên tử phi kim chia sẻ electron để tạo thành cặp electron dùng chung.
Đặc điểm: Thường gặp trong phân tử của các phi kim; Không dẫn điện (trừ một số trường hợp đặc biệt như graphit); Tính chất của chất phụ thuộc vào cấu trúc phân tử.