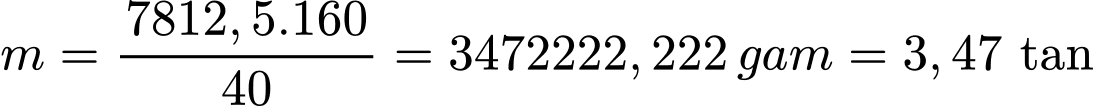Dạng 1: TRẮC NGHIỆM KHÁCH QUAN: mỗi câu hỏi chỉ có một đáp án đúng.
Câu 1 [1016800]: Một loại đồng thau có chứa 59,63% Cu và 40,37% Zn. Hợp kim này có cấu tạo tinh thể của hợp chất hoá học giữa đồng và kẽm. Công thức hoá học của hợp chất là
A, Cu3Zn2.
B, Cu2Zn.
C, Cu2Zn3.
D, CuZn2.
Gọi công thức của đồng thau có dạng CuaZnb
Ta có: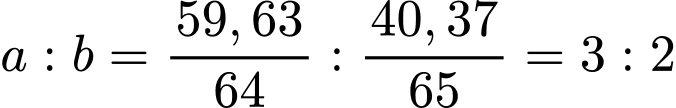
Công thức của đồng thau là Cu3Zn2.
➔ Chọn đáp án A. Cu3Zn2 Đáp án: A
Ta có:
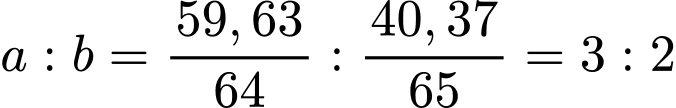
Công thức của đồng thau là Cu3Zn2.
➔ Chọn đáp án A. Cu3Zn2 Đáp án: A
Câu 2 [1016801]: Trong hợp kim Al–Mg, cứ có 9 mol Al thì có 1 mol Mg. Thành phần phần trăm khối lượng của từng kim loại trong hợp kim là
A, 80% Al và 20% Mg.
B, 91% Al và 9% Mg.
C, 81% Al và 19% Mg.
D, 83% Al và 17% Mg.
HD:
Phần trăm khối lượng của các kim loại trong hợp kim là:
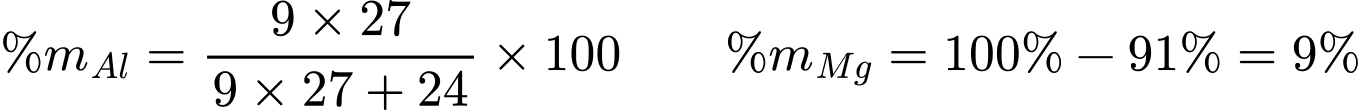 Đáp án: B
Đáp án: B
Phần trăm khối lượng của các kim loại trong hợp kim là:
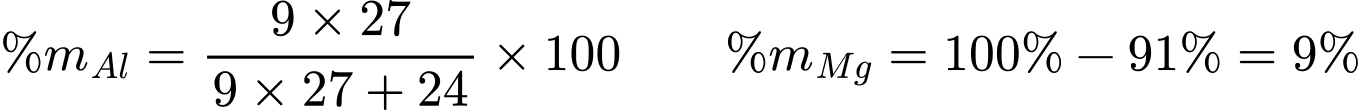 Đáp án: B
Đáp án: B
Câu 3 [273490]: Một khoáng chất chứa 31,3% silicon; 53,6% oxygen còn lại là nhôm và berillium. Phần trăm khối lượng của nhôm trong khoáng chất là
A, 2,5%.
B, 5,0%.
C, 10,1%.
D, 15,1%.
Ta có: % Al và Be còn lại: 15,1%
Gọi % Be = a ⟶ %Al = 15,1 - a
Do hóa trị của Al = 3, Be = 2, Si = 4 và O = 2
nên ta có: [(15 ×1 - a) / 27] × 3 + [(a / 9) × 2] + [(31 × 3 / 28) × 4] - [(53 × 6 / 16) × 2] = 0
=> Giải phương trình cho a = % Be = 4,96
Phần trăm khối lượng của nhôm trong khoáng chất là: %Al = 15.1 - a = 10,14%.
⟹Chọn đáp án C
Gọi % Be = a ⟶ %Al = 15,1 - a
Do hóa trị của Al = 3, Be = 2, Si = 4 và O = 2
nên ta có: [(15 ×1 - a) / 27] × 3 + [(a / 9) × 2] + [(31 × 3 / 28) × 4] - [(53 × 6 / 16) × 2] = 0
=> Giải phương trình cho a = % Be = 4,96
Phần trăm khối lượng của nhôm trong khoáng chất là: %Al = 15.1 - a = 10,14%.
⟹Chọn đáp án C
Câu 4 [273491]: Một khoáng chất có thành phần về khối lượng là: 14,81% Mg; 47,41% O; 0,25% H còn lại là Ca và Si. Phần trăm khối lượng của Ca trong khoáng chất là
A, 9,90%.
B, 17,78%.
C, 27,63%.
D, 37,53%.
Giả sử ta có 100 gam quặng loại này.
Tính lần lượt số mol các chất đã biết:
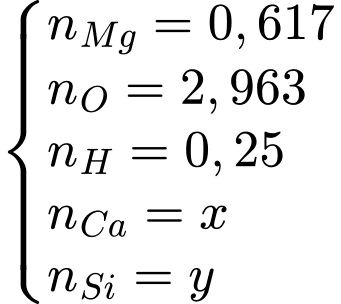
Trong quặng, thì các nguyên tố sẽ có các số oxi hóa tương ứng Ca2+, Mg2+, O2-, H+, Si4+. Ngoài ra, các số oxi hóa này phải đảm bảo cân bằng giữa tổng số oxi hóa âm và dương.
Tóm lại, ta có hệ:
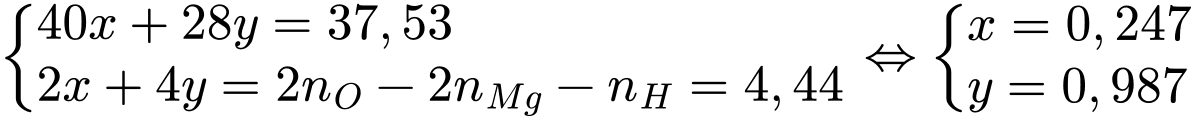
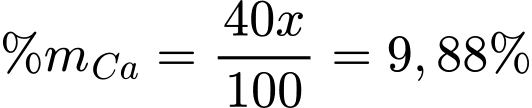
⟹ Chọn đáp án A Đáp án: A
Tính lần lượt số mol các chất đã biết:
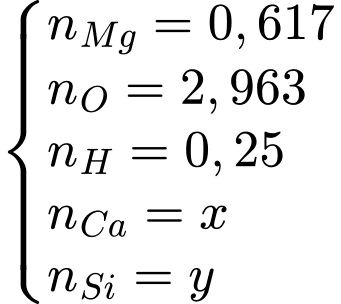
Trong quặng, thì các nguyên tố sẽ có các số oxi hóa tương ứng Ca2+, Mg2+, O2-, H+, Si4+. Ngoài ra, các số oxi hóa này phải đảm bảo cân bằng giữa tổng số oxi hóa âm và dương.
Tóm lại, ta có hệ:
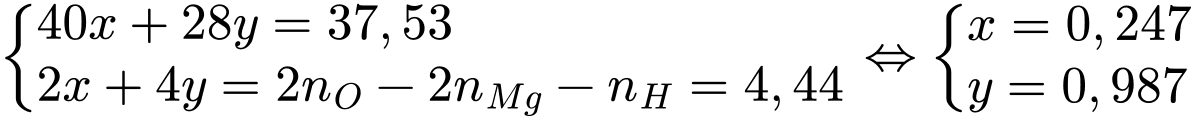
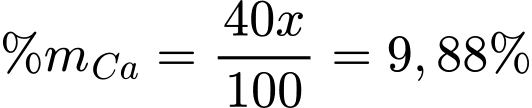
⟹ Chọn đáp án A Đáp án: A
Câu 5 [273492]: Một khoáng chất có chứa a% nhôm, 21,7% silicon, 1,55% hydrogen (theo khối lượng), còn lại là oxygen. Giá trị của a là
A, 12,86%.
B, 52,94%.
C, 20,94%.
D, 39,13%.
Gọi công thức của khoáng chất : AlxSiyOzHt .
%mAl = a; %mO =b .
Ta có : a+ b= 100% - ( 21,7% + 1,55 % ) = 76,75% (1).
Áp dụng định luật bảo toàn điện tích ta có : 3x + 4y + t = 2z
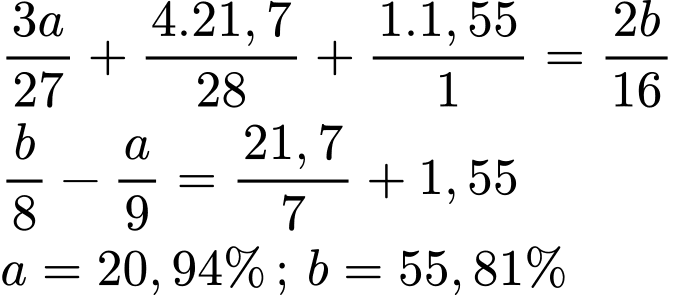
Vậy Al chiếm 20,94%
⟹ Chọn đáp án C Đáp án: C
%mAl = a; %mO =b .
Ta có : a+ b= 100% - ( 21,7% + 1,55 % ) = 76,75% (1).
Áp dụng định luật bảo toàn điện tích ta có : 3x + 4y + t = 2z
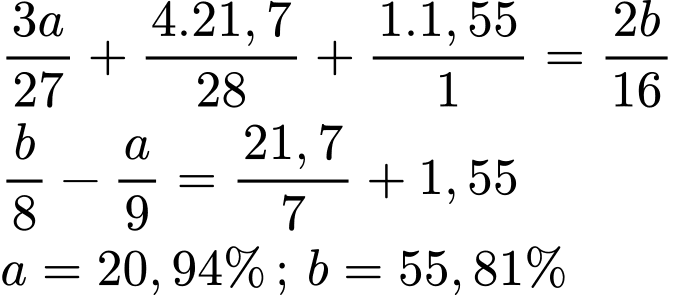
Vậy Al chiếm 20,94%
⟹ Chọn đáp án C Đáp án: C
Câu 6 [273493]: Một khoáng chất có thành phần về khối lượng là: 39,68% Ca; 18,45% P; 38,10% O và còn lại là một nguyên tố X. Nguyên tố X là
A, N.
B, F.
C, S.
D, C.
Giả sử khối lượng X là 100 gam: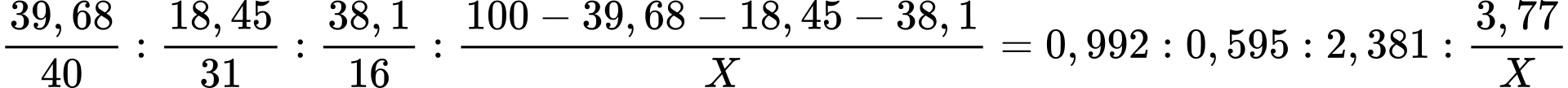
nx = 3,77: Mx
=> BT điện tích: 0,992. 2 + 0,5952. 5 + x. 3,77 : M(X) = 2. 2,381
=> M = 19nx
( Cân bằng điện tích có hóa trị của Ca là +2; P là +5; O là -2. Giả sử X có hóa trị là âm => thỏa mãn )
Biện luận nx=1, 2, 3, 4
Thấy có giá trị nx=1; M=19 thỏa mãn.
=> X là flourine.
⟹ Chọn đáp án B Đáp án: B
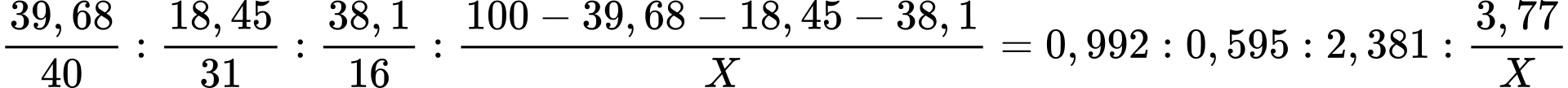
nx = 3,77: Mx
=> BT điện tích: 0,992. 2 + 0,5952. 5 + x. 3,77 : M(X) = 2. 2,381
=> M = 19nx
( Cân bằng điện tích có hóa trị của Ca là +2; P là +5; O là -2. Giả sử X có hóa trị là âm => thỏa mãn )
Biện luận nx=1, 2, 3, 4
Thấy có giá trị nx=1; M=19 thỏa mãn.
=> X là flourine.
⟹ Chọn đáp án B Đáp án: B
Câu 7 [273494]: Một loại khoáng có chứa 13,77% Na; 7,18% Mg; 57,48% O; 2,39% H và X về khối lượng. X là nguyên tố nào?
A, Lưu huỳnh.
B, Cacbon.
C, Nitơ.
D, Flo.
%X = 100% - 13.77% - 7.18% - 57.48% - 2.39% = 19.18%
Tỉ lệ nguyên tố:
Na : Mg : O : H : X =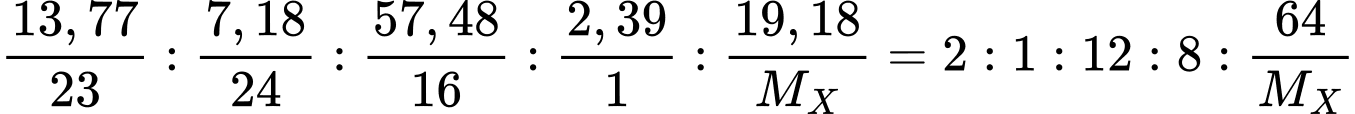
=> Biện luận tỉ lệ 64/MX là các giá trị nguyên như 1, 2, 3, 4, 5
=> MX lần lượt là 64 (Cu); 32 (Sulfur); 21,3 (Loại); 16 (Oxygen, trùng nên loại); 12,8 (Loại)
⟹ Chọn đáp án A Đáp án: A
Tỉ lệ nguyên tố:
Na : Mg : O : H : X =
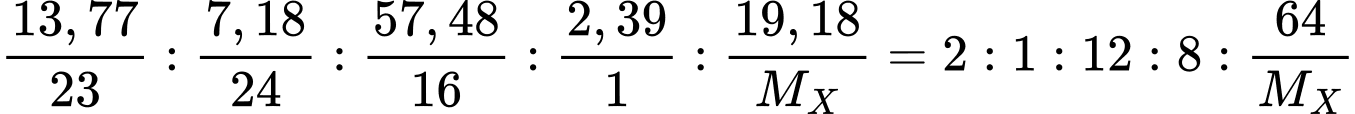
=> Biện luận tỉ lệ 64/MX là các giá trị nguyên như 1, 2, 3, 4, 5
=> MX lần lượt là 64 (Cu); 32 (Sulfur); 21,3 (Loại); 16 (Oxygen, trùng nên loại); 12,8 (Loại)
⟹ Chọn đáp án A Đáp án: A
Câu 8 [273495]: Một khoáng chất có thành phần về khối lượng là: 14,05% K; 8,65% Mg; 34,6% O; 4,32% H và còn lại là một nguyên tố X. Nguyên tố X là
A, S.
B, Cl.
C, P.
D, Si.
Giả sử m(khoáng chất) = 100 (g)
→ m(K) = 14,05; m(Mg) = 8,65; m(O) = 34,6; m(H) = 4,32 và m(X) = 38,388
→ n(K) = 0,36; n(Mg) = 0,36; n(O) = 2,1625; n(H) = 4,32
Gọi x là hóa trị của X
→ BT điện tích: x. n(X) = n(K) + 2n(Mg) + n(H) – 2n(O) = 1,08
→ M(X) = 35,5. x → X: Cl
⟹ Chọn đáp án B Đáp án: B
→ m(K) = 14,05; m(Mg) = 8,65; m(O) = 34,6; m(H) = 4,32 và m(X) = 38,388
→ n(K) = 0,36; n(Mg) = 0,36; n(O) = 2,1625; n(H) = 4,32
Gọi x là hóa trị của X
→ BT điện tích: x. n(X) = n(K) + 2n(Mg) + n(H) – 2n(O) = 1,08
→ M(X) = 35,5. x → X: Cl
⟹ Chọn đáp án B Đáp án: B
Câu 9 [560679]: Dựa vào giá trị thế điện cực chuẩn của cặp oxi hóa khử Au3+/Au, lí do nào sau đây giải thích vàng có thể tồn tại ở dạng đơn chất trong tự nhiên?
A, Do có thể khử chuẩn lớn nên Au cực kì kém hoạt động hóa học.
B, Do có thể khử chuẩn nhỏ nên Au3+ cực kì kém hoạt động hóa học.
C, Do có thể khử chuẩn lớn nên nên Au hoạt động hóa học mạnh.
D, Do có thể khử chuẩn nhỏ nên Au3+ hoạt động hóa học mạnh.
Thế điện cực chuẩn càng nhỏ thì dạng khử có tính khử càng mạnh và ngược lại. Do đó vì giá trị thế điện cực chuẩn lớn nên Au kém hoạt động hóa học.
⟹ Chọn đáp án A
Đáp án: A ⟹ Chọn đáp án A
Câu 10 [560680]: Nước tự nhiên ở khu vực có khoáng vật calcite (CaCO3) thường chứa cation kim loại nào?
A, Cu2+.
B, Ca2+.
C, NH4+.
D, CO32–.
Calcite là dạng khoáng vật chính của calcium carbonate, do đó nước trong khu vực này thường chứa ion calciumtừ quá trình hòa tan calcite.
 => Chứa cation Ca2+
=> Chứa cation Ca2+
⇒ Chọn đáp án B Đáp án: B
 => Chứa cation Ca2+
=> Chứa cation Ca2+⇒ Chọn đáp án B Đáp án: B
Câu 11 [560681]: Trong vỏ Trái Đất, những kim loại nào sau tồn tại chủ yếu dưới dạng đơn chất?
A, Ag, Au.
B, Zn, Fe.
C, Mg, Al.
D, Na, Ba.
Vì Ag và Au cực kì kém hoạt động hóa học nên tồn tại chủ yếu ở dạng đơn chất.
⇒ Chọn đáp án A Đáp án: A
⇒ Chọn đáp án A Đáp án: A
Câu 12 [560682]: Một số kim loại, chẳng hạn như aluminium có thể được tách ra khỏi quặng bằng phương pháp điện phân nóng chảy. Giải thích tại sao lại chọn sử dụng phương pháp này?
A, Do các kim loại này có tính khử mạnh.
B, Do nhiệt độ nóng chảy của các kim loại thấp.
C, Do các kim loại có khả năng dẫn điện.
D, Do chi phí điện phân thấp hơn các phương pháp tách khác, dễ thực hiện.
Do các kim loại (kiềm, kiềm thổ, alunimium) có tính khử mạnh nên các phương pháp nhiệt luyện, thủy luyện không thể sử dụng được.
⟹ Chọn đáp án A Đáp án: A
⟹ Chọn đáp án A Đáp án: A
Câu 13 [560683]: Trong tự nhiên, nguyên tố kim loại có thể được tìm thấy chủ yếu ở đâu trong các nguồn dưới đây?
(a) Nước ngầm.
(b) Nước biển.
(c) Đất đá.
(d) Cây xanh có hoa.
(a) Nước ngầm.
(b) Nước biển.
(c) Đất đá.
(d) Cây xanh có hoa.
A, (a), (b) và (c).
B, (b) và (c).
C, (a) và (c).
D, (a), (b), (c) và (d).
(a) Nước ngầm: Nước ngầm hòa tan nhiều khoáng chất từ đất và đá, bao gồm cả các hợp chất kim loại. Do đó, nước ngầm là một nguồn chứa các nguyên tố kim loại.
(b) Nước biển: Nước biển chứa một lượng lớn các ion hòa tan, trong đó có nhiều ion kim loại như Na, Mg, Ca, K,..và nhiều kim loại khác với hàm lượng nhỏ hơn. Việc khai thác một số kim loại từ nước biển đã được thực hiện.
(c) Đất đá: Vỏ trái đất cấu tạo chủ yếu từ các loại đất và đá, chúng chứa đựng hầu hết các nguyên tố kim loại trong các hợp chất khác nhau (oxide, silicate,...). Đây là nguồn cung cấp chính các kim loại để con người khai thác.
(d) Cây xanh có hoa: Cây xanh hấp thụ các chất dinh dưỡng từ đất, bao gồm cả các ion kim loại cần thiết cho sự phát triển của chúng với một hàm lượng nhất định. Tuy nhiên, hàm lượng kim loại trong cây xanh thường rất nhỏ so với các nguồn khoáng sản trong đất đá hoặc các ion hòa tan trong nước. Cây xanh không phải là nguồn chính để tìm thấy các nguyên tố kim loại ở quy mô lớn.
Kim loại có thể tìm thấy ở 3 nguồn nước ngầm, nước biển và đất đá.
⟹ Chọn đáp án A Đáp án: A
(b) Nước biển: Nước biển chứa một lượng lớn các ion hòa tan, trong đó có nhiều ion kim loại như Na, Mg, Ca, K,..và nhiều kim loại khác với hàm lượng nhỏ hơn. Việc khai thác một số kim loại từ nước biển đã được thực hiện.
(c) Đất đá: Vỏ trái đất cấu tạo chủ yếu từ các loại đất và đá, chúng chứa đựng hầu hết các nguyên tố kim loại trong các hợp chất khác nhau (oxide, silicate,...). Đây là nguồn cung cấp chính các kim loại để con người khai thác.
(d) Cây xanh có hoa: Cây xanh hấp thụ các chất dinh dưỡng từ đất, bao gồm cả các ion kim loại cần thiết cho sự phát triển của chúng với một hàm lượng nhất định. Tuy nhiên, hàm lượng kim loại trong cây xanh thường rất nhỏ so với các nguồn khoáng sản trong đất đá hoặc các ion hòa tan trong nước. Cây xanh không phải là nguồn chính để tìm thấy các nguyên tố kim loại ở quy mô lớn.
Kim loại có thể tìm thấy ở 3 nguồn nước ngầm, nước biển và đất đá.
⟹ Chọn đáp án A Đáp án: A
Câu 14 [560684]: Nguyên tắc tách kim loại ra khỏi hợp chất của chúng là
A, Khử ion kim loại trong hợp chất thành nguyên tử.
B, Oxi hoá ion kim loại trong hợp chất thành nguyên tử.
C, Hoà tan các khoáng vật có trong quặng để thu được kim loại.
D, Dựa trên tính chất của kim loại như từ tính, khối lượng riêng lớn để tách chúng ra khỏi quặng.
Trong hợp chất, nguyên tố kim loại tồn tại dạng cation kim loại (Mn+) nên nguyên tắc chung để tách được nguyên tố kim loại ra khỏi hợp chất cần thực hiện phản ứng khử cation kim loại thành nguyên tử.
Đáp án: A
Mn+ + ne ⟶ M
⇒ Chọn đáp án A
Câu 15 [982771]: [TN THPT 2020 - ĐII]: Kim loại nào sau đây điều chế được bằng phương pháp nhiệt luyện với chất khử H2?
A, Mg.
B, Na.
C, Al.
D, Fe.
HD: H2 khử được các oxit sắt để thu được kim loại tương ứng:
Fe3O4 + 4H2 –––to–→ 3Fe + 4H2O.
⇒ Chọn đáp án D Đáp án: D
Fe3O4 + 4H2 –––to–→ 3Fe + 4H2O.
⇒ Chọn đáp án D Đáp án: D
Câu 16 [981796]: [TN THPT 2020 - ĐII]: Kim loại nào sau đây điều chế được bằng phương pháp nhiệt luyện với chất khử CO?
A, Ba.
B, Fe.
C, Mg.
D, K.
HD: CO không khử được các oxit kim loại từ Zn trở lên.
⇒ Các đáp án Ba, Mg, K không thoả mãn. Còn lại:
3CO + Fe2O3 –––to–→ 3CO2 + 2Fe.
⇒ Chọn đáp án B Đáp án: B
⇒ Các đáp án Ba, Mg, K không thoả mãn. Còn lại:
3CO + Fe2O3 –––to–→ 3CO2 + 2Fe.
⇒ Chọn đáp án B Đáp án: B
Câu 17 [233843]: [TN THPT 2022]: Ở nhiệt độ cao, chất nào sau đây không khử được Fe2O3?
A, H2.
B, CO.
C, Al.
D, CO2.
HD: Bài học phương pháp nhiệt luyện điều chế kim loại:
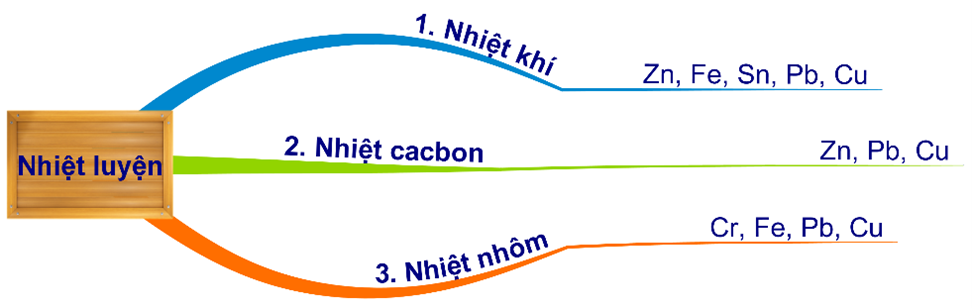
⇝ CO, H2 (nhiệt khí) và Al (nhiệt nhôm) khử được Fe.
► CO2 không thể nhận thêm e, làm sao mà "khử được" Fe2O3 nên cũng có thể chọn nhanh D.
☆ các phản ứng xảy ra:
✔️ 3CO + Fe2O3 ––to→ 2Fe + 3CO2.
✔️ 3H2 + Fe2O3 ––to→ 2Fe + 3H2O.
✔️ 2Al + Fe2O3 ––to→ 2Fe + Al2O3. Đáp án: D

⇝ CO, H2 (nhiệt khí) và Al (nhiệt nhôm) khử được Fe.
► CO2 không thể nhận thêm e, làm sao mà "khử được" Fe2O3 nên cũng có thể chọn nhanh D.
☆ các phản ứng xảy ra:
✔️ 3CO + Fe2O3 ––to→ 2Fe + 3CO2.
✔️ 3H2 + Fe2O3 ––to→ 2Fe + 3H2O.
✔️ 2Al + Fe2O3 ––to→ 2Fe + Al2O3. Đáp án: D
Câu 18 [59338]: Trong công nghiệp, crom được điều chế bằng phương pháp nhiệt luyện. Kim loại nào sau đây được dùng để khử Cr2O3 thành Cr?
A, Ag.
B, Cu.
C, Al.
D, Fe.
HD:
Trong công nghiệp, crom được điều chế bằng cách cho Al khử Cr2O3 thành Cr:
2Al + Cr2O3 to→ 2Cr + Al2O3.
⇒ Chọn đáp án C
Đáp án: C
Trong công nghiệp, crom được điều chế bằng cách cho Al khử Cr2O3 thành Cr:
2Al + Cr2O3 to→ 2Cr + Al2O3.
⇒ Chọn đáp án C
Đáp án: C
Câu 19 [12650]: [THPT QG 2017]: Dẫn khí CO dư đi qua hỗn hợp bột gồm MgO, CuO, Al2O3 và FeO, nung nóng. Sau khi các phản ứng xảy ra hoàn toàn, thu được hỗn hợp chất rắn Y. Số oxit kim loại có trong Y là
A, 3.
B, 1.
C, 4.
D, 2.
HD: CO khử các oxit kim loại trung bình yếu: CuO, Feo thành kim loại:
![596549[LG].png](https://asset.moon.vn/img/ai/Teachers/rongden_167/ProS2018/TAPIII/596549[LG].png)
CO không khử được MgO và Al2O3. Có 2 oxit thỏa mãn yêu cầu
→ Chọn đáp án D. ♠.
Đáp án: D
![596549[LG].png](https://asset.moon.vn/img/ai/Teachers/rongden_167/ProS2018/TAPIII/596549[LG].png)
CO không khử được MgO và Al2O3. Có 2 oxit thỏa mãn yêu cầu
→ Chọn đáp án D. ♠.
Đáp án: D
Câu 20 [560685]: Tách Fe bằng cách khử Fe2O3 bởi CO theo phương trình hoá học:
Fe2O3(s) + 3CO(g) 2Fe(l) + 3CO2(g).
2Fe(l) + 3CO2(g).
Chất khử được sử dụng trong phản ứng là
Fe2O3(s) + 3CO(g)
 2Fe(l) + 3CO2(g).
2Fe(l) + 3CO2(g).Chất khử được sử dụng trong phản ứng là
A, Fe2O3.
B, CO.
C, Fe.
D, CO2.
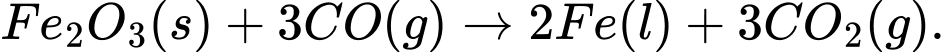
Khử tăng – oxi hóa giảm.
Chất khử được sử dụng trong phản ứng là CO (do số oxi hóa tăng từ +2 lên +4).
⟹ Chọn đáp án B Đáp án: B
Câu 21 [560686]: Tách Zn bằng cách khử ZnO bởi C theo phương trình hoá học:
ZnO(s) + C(s) Zn(g) + CO(g).
Zn(g) + CO(g).
Sau phản ứng, làm nguội, hơi kẽm ngưng tụ thành kẽm ở thể lỏng hoặc rắn. Chất khử được sử dụng trong phản ứng là
ZnO(s) + C(s)
 Zn(g) + CO(g).
Zn(g) + CO(g).Sau phản ứng, làm nguội, hơi kẽm ngưng tụ thành kẽm ở thể lỏng hoặc rắn. Chất khử được sử dụng trong phản ứng là
A, ZnO.
B, C.
C, Zn.
D, CO.
Quá trình oxi hóa (nhường e): C0 ⟶ C+2 + 2e nên chất khử được sử dụng trong phản ứng là C.
⟹ Chọn đáp án B Đáp án: B
⟹ Chọn đáp án B Đáp án: B
Câu 22 [560687]: Tách iron từ quặng hematite theo phương trình:
Fe2O3(s) + 3CO(g) 2Fe(l) + 3CO2(g).
2Fe(l) + 3CO2(g).
Trong phương trình này, Fe2O3 đóng vai trò là
Fe2O3(s) + 3CO(g)
 2Fe(l) + 3CO2(g).
2Fe(l) + 3CO2(g).Trong phương trình này, Fe2O3 đóng vai trò là
A, Chất bị khử.
B, Chất bị oxi hóa.
C, Chất trung tính.
D, Chất nhường electron.
Fe3+ + 3e ⟶ Fe là quá trình nhận electron nên Fe2O3 là chất oxi hóa (bị khử).
⟹ Chọn đáp án A Đáp án: A
⟹ Chọn đáp án A Đáp án: A
Câu 23 [560688]: Nhiều kim loại có thể được điều chế từ quặng của chúng bằng cách nung oxide kim loại với carbon (phương pháp nhiệt carbon). Kim loại nào sau đây không thể được điều chế bằng phương pháp nhiệt carbon?
A, Zinc.
B, Copper.
C, Aluminium.
D, Iron.
- Nhôm là mộtkim loại có tính khử rất mạnh (nằm cao trong dãy điện hóa). Nó có khả năng khửcác oxide kim loại khác nhưng bản thân oxide của nórất bền
⟹ Chọn đáp án C Đáp án: C
Câu 24 [212583]: [TK 2022]: Kim loại nào sau đây điều chế được bằng phương pháp thủy luyện?
A, Au.
B, Ca.
C, Na.
D, Mg.
HD: ☆ Bài học về điều chế kim loại:
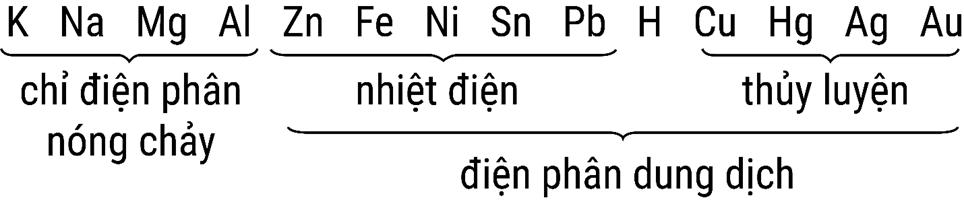
⇒ Au được điều chế bằng phương pháp thủy luyện (Na, Ca, Mg phản ứng được với nước nên không điều chế được) ⇝ Chọn đáp án A. ♥ Đáp án: A

⇒ Au được điều chế bằng phương pháp thủy luyện (Na, Ca, Mg phản ứng được với nước nên không điều chế được) ⇝ Chọn đáp án A. ♥ Đáp án: A
Câu 25 [59356]: Để thu được kim loại Cu từ dung dịch CuSO4 bằng phương pháp thủy luyện, ta không thể dùng kim loại nào sau đây?
A, Mg.
B, Ca.
C, Fe.
D, Zn.
HD: Thứ tự dãy điện hóa các kim loại: Ca > Mg > Zn > Fe > Cu.
⇝ các kim loại đều đứng trước Cu trong dãy điện hóa.
Tuy nhiên, trường hợp các kim loại kiềm, kiềm thổ như Na, K, Ca, Ba
phản ứng mãnh liệt với H2O tạo dung dịch bazơ trước:
Ca + 2H2O → Ca(OH)2 + H2↑.
Sau đó: Ca(OH)2 + CuSO4 → Cu(OH)2↓ + CaSO4.
⇒ không dùng được Ca để đẩy Cu2+ ra khỏi dung dịch bằng phương pháp thủy luyện. ❒
⇒ Chọn đáp án B Đáp án: B
⇝ các kim loại đều đứng trước Cu trong dãy điện hóa.
Tuy nhiên, trường hợp các kim loại kiềm, kiềm thổ như Na, K, Ca, Ba
phản ứng mãnh liệt với H2O tạo dung dịch bazơ trước:
Ca + 2H2O → Ca(OH)2 + H2↑.
Sau đó: Ca(OH)2 + CuSO4 → Cu(OH)2↓ + CaSO4.
⇒ không dùng được Ca để đẩy Cu2+ ra khỏi dung dịch bằng phương pháp thủy luyện. ❒
⇒ Chọn đáp án B Đáp án: B
Câu 26 [59367]: Trong các kim loại Cu; Ag; Na; K và Ba, số kim loại điều chế được bằng phương pháp thủy luyện là
- Phương pháp thủy luyện áp dụng điều chế các kim loại có mức độ hoạt động thấp như Cu, Hg, Au, Ag...
- Điều chế kim loại bằng phương pháp thủy luyện thường được sử dụng trong phòng thí nghiệm với mục đích điều chế những kim loại yếu đứng sau Mg.
Kim loại được điều chế bằng phương pháp thủy luyện gồm Cu và Ag
⇒ Có 2 kim loại.
⟹ Điền đáp án 2
- Điều chế kim loại bằng phương pháp thủy luyện thường được sử dụng trong phòng thí nghiệm với mục đích điều chế những kim loại yếu đứng sau Mg.
Kim loại được điều chế bằng phương pháp thủy luyện gồm Cu và Ag
⇒ Có 2 kim loại.
⟹ Điền đáp án 2
Câu 27 [560689]: Aluminium có thể được sản xuất bằng phương pháp điện phân.

Phát biểu nào sau đây không đúng về quá trình điện phân aluminium oxide?

Phát biểu nào sau đây không đúng về quá trình điện phân aluminium oxide?
A, Cực âm phải được thay thế thường xuyên vì nó bị cháy đi.
B, Aluminium nhận electron trong quá trình điện phân và bị khử.
C, Cực dương và cực âm được làm bằng than chì.
D, Cryolite được thêm vào đề làm giảm điêm nóng chảy của aluminium oxide.
Cực dương (anode) cần được thay thế sau một thời gian sử dụng vì khí O2 sinh ra phản ứng với điện cực ở nhiệt độ cao tạo khí CO và CO2
⟹ Chọn đáp án A Đáp án: A
⟹ Chọn đáp án A Đáp án: A
Câu 28 [560690]: Với quá trình tách sodium bằng phương pháp điện phân sodium chloride nóng chảy, phát biểu nào sau đây là đúng?
A, Tại anode xảy ra quá trình khử ion Na+.
B, Tại cathode xảy ra quá trình khử ion Cl–.
C, Tại cathode xảy ra quá trình khử ion Na+.
D, Tại anode xảy ra quá trình khử ion Cl–.
Khi điện phân nóng chảy NaCl:
Anode (+) xảy ra quá trình oxi hóa: 2Cl- ⟶ Cl2 + 2e
Cathode (-) xảy ra quá trình khử: Na+ + 1e ⟶ Na
⇒ Chọn đáp án C Đáp án: C
Anode (+) xảy ra quá trình oxi hóa: 2Cl- ⟶ Cl2 + 2e
Cathode (-) xảy ra quá trình khử: Na+ + 1e ⟶ Na
⇒ Chọn đáp án C Đáp án: C
Câu 29 [560693]: Ba phát biểu về aluminium dưới đây đều chính xác.
(i) Aluminium phản ứng dễ dàng tạo thành aluminium oxide.
(ii) Aluminium được tách ra khỏi quặng bằng phương pháp điện phân nóng chảy do không thể điều chế bằng phương pháp nhiệt luyện.
(iii) Aluminium được dùng làm lõi dây điện vì khả năng dẫn điện tốt.
Khi thay aluminium bằng copper thì những phát biểu vẫn đúng là
(i) Aluminium phản ứng dễ dàng tạo thành aluminium oxide.
(ii) Aluminium được tách ra khỏi quặng bằng phương pháp điện phân nóng chảy do không thể điều chế bằng phương pháp nhiệt luyện.
(iii) Aluminium được dùng làm lõi dây điện vì khả năng dẫn điện tốt.
Khi thay aluminium bằng copper thì những phát biểu vẫn đúng là
A, Cả (i), (ii), (iii).
B, Chỉ (ii).
C, (i) và (iii).
D, Chỉ (iii).
✔️ (i) – Đúng. Aluminium phản ứng dễ dàng tạo thành aluminium oxide.
❌ (ii) – Sai.
Làm giàu quặng: Do hàm lượng đồng trong quặng thấp (dưới 1%) vì vậy làm giàu bằng phương pháp tuyển nổi.
- Chuyển hóa quặng đồng thành đồng
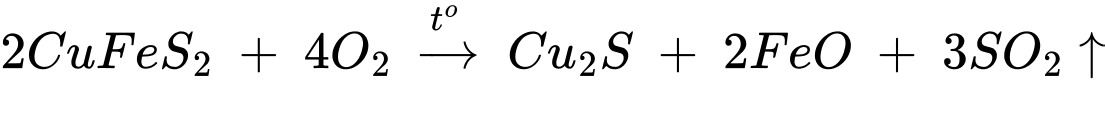
- Nung Cu2S trong không khí sao cho một phần Cu2S chuyển thành Cu2O
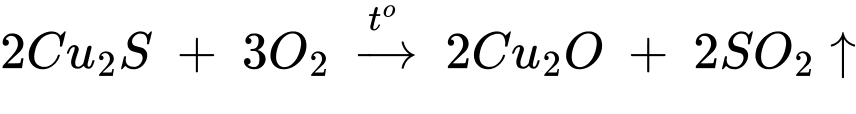
- Sau đó ngừng cung cấp oxi để xảy ra phản ứng:
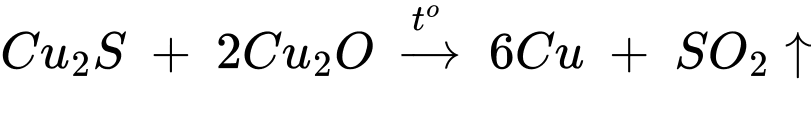
✔️ (iii) – Đúng. Copper được dùng làm lõi dây điện vì khả năng dẫn điện tốt.
⇒ Chọn đáp án C Đáp án: C
❌ (ii) – Sai.
Làm giàu quặng: Do hàm lượng đồng trong quặng thấp (dưới 1%) vì vậy làm giàu bằng phương pháp tuyển nổi.
- Chuyển hóa quặng đồng thành đồng
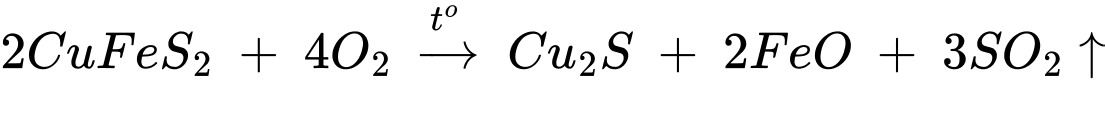
- Nung Cu2S trong không khí sao cho một phần Cu2S chuyển thành Cu2O
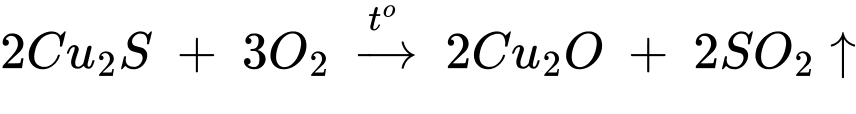
- Sau đó ngừng cung cấp oxi để xảy ra phản ứng:
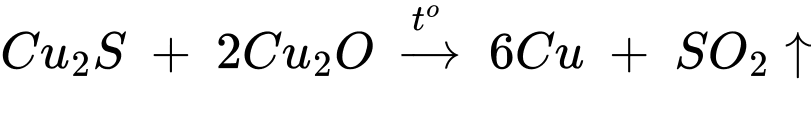
✔️ (iii) – Đúng. Copper được dùng làm lõi dây điện vì khả năng dẫn điện tốt.
⇒ Chọn đáp án C Đáp án: C
Câu 30 [560694]: Một số tính chất của các phân tử X, L, M và Z được đưa ra như sau:
(i) X đóng vai trò là chất xúc tác và oxide của nó phản ứng với hydrochloric acid.
(ii) L là chất rắn màu xám đen xỉn, dẫn điện và có nhiệt độ nóng chảy 3600°C.
(ii) M dễ dàng được rèn thành hình và có khối lượng riêng lớn.
(iv) Z có nhiệt độ nóng chảy là 113° C và tạo thành acidic oxide khi tác dụng với oxygen.
Nguyên tố nào có thể là kim loại?
(i) X đóng vai trò là chất xúc tác và oxide của nó phản ứng với hydrochloric acid.
(ii) L là chất rắn màu xám đen xỉn, dẫn điện và có nhiệt độ nóng chảy 3600°C.
(ii) M dễ dàng được rèn thành hình và có khối lượng riêng lớn.
(iv) Z có nhiệt độ nóng chảy là 113° C và tạo thành acidic oxide khi tác dụng với oxygen.
Nguyên tố nào có thể là kim loại?
A, X và M.
B, L, M và Z.
C, L, M.
D, L và Z.
+ X, M là kim loại
+ L là carbon
+ N là phi kim
⟹ Chọn đáp án A Đáp án: A
+ L là carbon
+ N là phi kim
⟹ Chọn đáp án A Đáp án: A
Câu 31 [705705]: Thực hiện các thí nghiệm sau:
(a) Nhiệt phân muối silver nitrate.
(b) Điện phân dung dịch sodium chloride có màng ngăn xốp.
(c) Dẫn khí hydrogen qua bột copper(II) oxide đun nóng.
(d) Cho dung dịch iron(II) nitrate vào dung dịch silver nitrate.
Sau khi các phản ứng xảy ra hoàn toàn, những thí nghiệm thu được kim loại là
(a) Nhiệt phân muối silver nitrate.
(b) Điện phân dung dịch sodium chloride có màng ngăn xốp.
(c) Dẫn khí hydrogen qua bột copper(II) oxide đun nóng.
(d) Cho dung dịch iron(II) nitrate vào dung dịch silver nitrate.
Sau khi các phản ứng xảy ra hoàn toàn, những thí nghiệm thu được kim loại là
A, (a), (b), (c).
B, (a), (c), (d).
C, (b), (c), (d).
D, (a), (b), (d).
Các phản ứng xảy ra như sau:
(a) Nhiệt phân muối silver nitrate
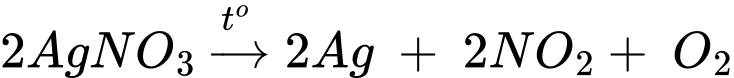
(b) Điện phân dung dịch sodium chloride có màng ngăn xốp
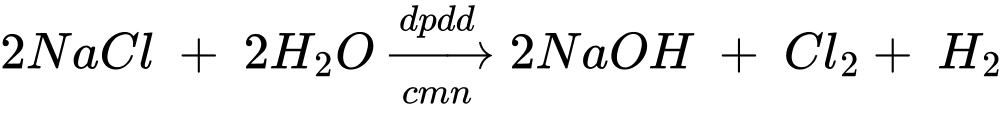
(c) Dẫn khí hydrogen qua bột copper(II) oxide đun nóng
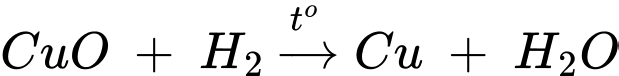
(d) Cho dung dịch iron(II) nitrate vào dung dịch silver nitrate
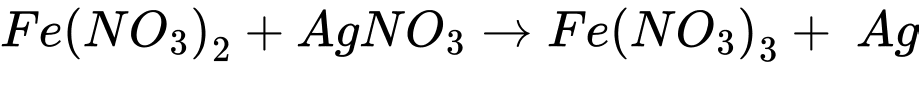
Sau phản ứng, các thí nghiệm thu được kim loại là (a) (c) và (d)
⇒ Chọn đáp án B Đáp án: B
(a) Nhiệt phân muối silver nitrate
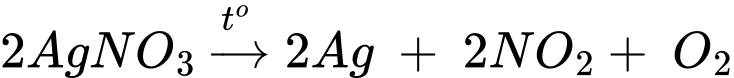
(b) Điện phân dung dịch sodium chloride có màng ngăn xốp
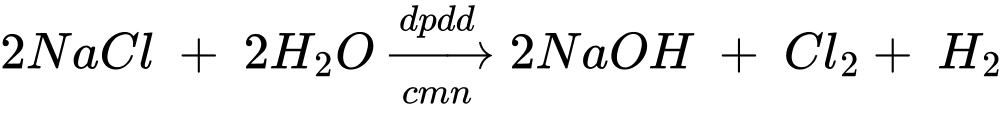
(c) Dẫn khí hydrogen qua bột copper(II) oxide đun nóng
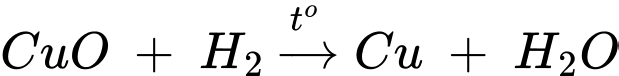
(d) Cho dung dịch iron(II) nitrate vào dung dịch silver nitrate
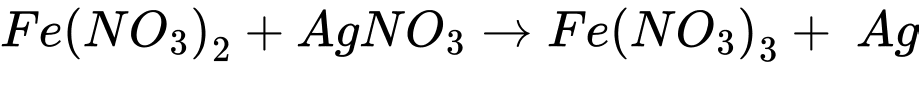
Sau phản ứng, các thí nghiệm thu được kim loại là (a) (c) và (d)
⇒ Chọn đáp án B Đáp án: B
Câu 32 [704021]: Tiến hành các thí nghiệm sau:
Thí nghiệm 1: Cho kim loại sodium vào dung dịch zinc sulfate dư.
Thí nghiệm 2: Cho dung dịch iron(II) nitrate vào dung dịch silver nitrate dư.
Thí nghiệm 3: Nhiệt phân hoàn toàn calcium carbonate ở nhiệt độ cao.
Thí nghiệm 4: Dẫn khí hydrogen dư đi qua bột copper(II) oxide nung nóng.
Sau khi các phản ứng kết thúc, các thí nghiệm thu được kim loại là
Thí nghiệm 1: Cho kim loại sodium vào dung dịch zinc sulfate dư.
Thí nghiệm 2: Cho dung dịch iron(II) nitrate vào dung dịch silver nitrate dư.
Thí nghiệm 3: Nhiệt phân hoàn toàn calcium carbonate ở nhiệt độ cao.
Thí nghiệm 4: Dẫn khí hydrogen dư đi qua bột copper(II) oxide nung nóng.
Sau khi các phản ứng kết thúc, các thí nghiệm thu được kim loại là
A, thí nghiệm 1 và 2.
B, thí nghiệm 3 và 4.
C, thí nghiệm 2 và 4.
D, thí nghiệm 1 và 3.
Các phản ứng xảy ra như sau:
⍟ Thí nghiệm 1: 2Na + 2H2O 2NaOH + H2
2NaOH + H2
2NaOH + ZnSO4 Na2SO4 + Zn(OH)2
Na2SO4 + Zn(OH)2
2NaOH + Zn(OH)2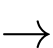 Na2ZnO2 + 2H2O
Na2ZnO2 + 2H2O
⍟ Thí nghiệm 2: Fe(NO3)2 + AgNO3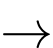 Fe(NO3)3 + Ag
Fe(NO3)3 + Ag
⍟ Thí nghiệm 3: CaCO3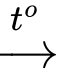 CaO + CO2
CaO + CO2
⍟ Thí nghiệm 4: CuO + H2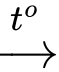 Cu + H2O
Cu + H2O
⟶ Chỉ có thí nghiệm 2 và thí nghiệm 4 thu được kim loại sau phản ứng.
⇒ Chọn đáp án C Đáp án: C
⍟ Thí nghiệm 1: 2Na + 2H2O
 2NaOH + H2
2NaOH + H22NaOH + ZnSO4
 Na2SO4 + Zn(OH)2
Na2SO4 + Zn(OH)22NaOH + Zn(OH)2
 Na2ZnO2 + 2H2O
Na2ZnO2 + 2H2O⍟ Thí nghiệm 2: Fe(NO3)2 + AgNO3
 Fe(NO3)3 + Ag
Fe(NO3)3 + Ag⍟ Thí nghiệm 3: CaCO3
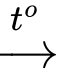 CaO + CO2
CaO + CO2⍟ Thí nghiệm 4: CuO + H2
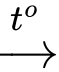 Cu + H2O
Cu + H2O⟶ Chỉ có thí nghiệm 2 và thí nghiệm 4 thu được kim loại sau phản ứng.
⇒ Chọn đáp án C Đáp án: C
Sử dụng đoạn thông tin dưới đây để trả lời câu 33 và câu 34:
Hàm lượng Au trong quặng hoặc trong đất thường rất thấp vì vậy rất khó tách Au bằng phương pháp cơ học. Trong công nghiệp, người ta tách vàng từ quặng theo phương trình
Vàng bị hoà tan tạo thành phức chất:
4Au(s) + 8KCN(aq) + O2(g) + 2H2O(l) → 4K[Au(CN)2](aq) + 4KOH(aq) (1)
và sau đó kết tủa vàng bằng kẽm (Zn):
Zn(s) + 2K[Au(CN)2] (aq) → K2[Zn(CN)4](aq) + 2Au(s) (2)
Vàng bị hoà tan tạo thành phức chất:
4Au(s) + 8KCN(aq) + O2(g) + 2H2O(l) → 4K[Au(CN)2](aq) + 4KOH(aq) (1)
và sau đó kết tủa vàng bằng kẽm (Zn):
Zn(s) + 2K[Au(CN)2] (aq) → K2[Zn(CN)4](aq) + 2Au(s) (2)
Câu 33 [705428]: Phương pháp điều chế kim loại nào đã được sử dụng trong quá tình sản xuất vàng theo sơ đồ trên?
A, Thủy luyện.
B, Nhiệt luyện.
C, Điện phân.
D, Chiết.
Phản ứng thủy luyện là dùng kim loại mạnh đẩy kim loại yếu hơn ra khỏi dung dịch muối của chúng.
Trong quy trình điều chế Au thì đã dùng Zn mạnh hơn Au để đẩy Au ra khỏi dung dịch muối → Đây là phương pháp thủy luyện.
⇒ Chọn đáp án A Đáp án: A
Trong quy trình điều chế Au thì đã dùng Zn mạnh hơn Au để đẩy Au ra khỏi dung dịch muối → Đây là phương pháp thủy luyện.
⇒ Chọn đáp án A Đáp án: A
Câu 34 [705429]: Nếu dùng 19,5 kg KCN thì có thể tách được bao nhiêu kg vàng từ quặng theo chuỗi phản ứng trên? Giả thiết các chất khác trong quặng không phản ứng với KCN.
A, 29,55 kg.
B, 9,75 kg.
C, 29,25 kg.
D, 39,0 kg.
4Au + 8KCN + O2 + 2H2O → 4K[Au(CN)2] + 4KOH
Zn + 2K[Au(CN)2] → K2[Zn(CN)4] + 2Au
Số mol của KCN là: nKCN = 19,5 ÷ 65 = 0,3 (kmol)
Từ phương trình hóa học số mol của vàng (Au) là:
nAu = nKCN ÷ 2 = 0,3 ÷ 2 = 0,15 (kmol)
Khối lượng vàng (Au) thu được là: mAu = 197.0,15 = 29,55 (kg)
⇒ Chọn đáp án A Đáp án: A
Zn + 2K[Au(CN)2] → K2[Zn(CN)4] + 2Au
Số mol của KCN là: nKCN = 19,5 ÷ 65 = 0,3 (kmol)
Từ phương trình hóa học số mol của vàng (Au) là:
nAu = nKCN ÷ 2 = 0,3 ÷ 2 = 0,15 (kmol)
Khối lượng vàng (Au) thu được là: mAu = 197.0,15 = 29,55 (kg)
⇒ Chọn đáp án A Đáp án: A
Sử dụng đoạn thông tin dưới đây để trả lời câu 35 và câu 36:
Hình sau mô tả thí nghiệm khử 50 gam copper(II) oxide thành đồng kim loại. Sau thí nghiệm, tắt đèn khí, nhưng vẫn duy trì dòng khí hydrogen cho đến khi ống nghiệm nguội.
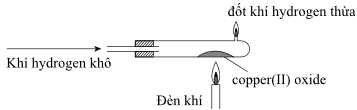

Câu 35 [704396]: Mục đích chính của việc duy trì dòng khí hydrogen là
A, tránh ống nghiệm bị nổ khi đang nóng.
B, để phản ứng xảy ra hoàn toàn.
C, ngăn đồng kim loại phản ứng với không khí.
D, đuổi hơi nước khỏi ống nghiệm.
⭐ Phản ứng trong thí nghiệm:
+) Khí hydrogen (H2) được sử dụng để khử copper(II) oxide (CuO) thành đồng kim loại (Cu):
CuO + H2 –to⟶ Cu + H2O
+) Sau phản ứng, nước được tạo thành dưới dạng hơi và đồng kim loại là sản phẩm rắn.
⭐ Lý do duy trì dòng khí hydrogen:
+) Sau khi tắt đèn khí (tức là ngừng nung nóng), ống nghiệm vẫn còn nóng.
+) Nếu không duy trì dòng khí hydrogen, đồng kim loại có thể phản ứng với oxygen trong không khí ở nhiệt độ cao, dẫn đến sự tái tạo lại CuO:
2Cu + O2 –to⟶ 2CuO
→ Duy trì dòng khí hydrogen tạo ra môi trường khử (không chứa
oxygen) bên trong ống nghiệm, ngăn đồng bị oxi hóa trở lại.
Phân tích các đáp án:
❌ A. Sai. Nổ ống nghiệm thường do áp suất tăng hoặc phản ứng mạnh, không liên quan trực tiếp đến việc duy trì hydrogen.
❌ B. Sai. Phản ứng khử đã hoàn thành trước đó.
✔️ C. Đúng. Duy trì dòng khí hydrogen tạo ra môi trường khử (không chứa
oxygen) bên trong ống nghiệm, ngăn đồng bị oxi hóa trở lại
❌ D. Sai. Dòng khí hydrogen không có tác dụng trực tiếp với việc đuổi hơi nước, vì hơi nước không ảnh hưởng đến sản phẩm đồng.
⇒ Chọn đáp án C Đáp án: C
+) Khí hydrogen (H2) được sử dụng để khử copper(II) oxide (CuO) thành đồng kim loại (Cu):
CuO + H2 –to⟶ Cu + H2O
+) Sau phản ứng, nước được tạo thành dưới dạng hơi và đồng kim loại là sản phẩm rắn.
⭐ Lý do duy trì dòng khí hydrogen:
+) Sau khi tắt đèn khí (tức là ngừng nung nóng), ống nghiệm vẫn còn nóng.
+) Nếu không duy trì dòng khí hydrogen, đồng kim loại có thể phản ứng với oxygen trong không khí ở nhiệt độ cao, dẫn đến sự tái tạo lại CuO:
2Cu + O2 –to⟶ 2CuO
→ Duy trì dòng khí hydrogen tạo ra môi trường khử (không chứa
oxygen) bên trong ống nghiệm, ngăn đồng bị oxi hóa trở lại.
Phân tích các đáp án:
❌ A. Sai. Nổ ống nghiệm thường do áp suất tăng hoặc phản ứng mạnh, không liên quan trực tiếp đến việc duy trì hydrogen.
❌ B. Sai. Phản ứng khử đã hoàn thành trước đó.
✔️ C. Đúng. Duy trì dòng khí hydrogen tạo ra môi trường khử (không chứa
oxygen) bên trong ống nghiệm, ngăn đồng bị oxi hóa trở lại
❌ D. Sai. Dòng khí hydrogen không có tác dụng trực tiếp với việc đuổi hơi nước, vì hơi nước không ảnh hưởng đến sản phẩm đồng.
⇒ Chọn đáp án C Đáp án: C
Câu 36 [704397]: Sau khi tiến hành thí nghiệm, đem cân thấy khối lượng chất rắn thu được là 42 gam. Hiệu suất của phản ứng trên là bao nhiêu?
A, 60%.
B, 80%.
C, 90%.
D, 70%.
Phản ứng hoá học: CuO + H2 –to⟶ Cu + H2O
Chất rắn trong ống chuyển từ màu đen sang màu nâu đỏ của đồng.
Khối lượng chất rắn giảm là khối lượng nguyên tố O mất đi trong CuO:
mO = 50 - 42 = 8 (gam)
Số mol của CuO đã tham gia phản ứng là:
nCuO = nO = 8 ÷ 16 = 0,5 (mol)
Hiệu suất phản ứng là: H = (0,5 × 80 ÷ 50) × 100% = 80%
⇒ Chọn đáp án B Đáp án: B
Chất rắn trong ống chuyển từ màu đen sang màu nâu đỏ của đồng.
Khối lượng chất rắn giảm là khối lượng nguyên tố O mất đi trong CuO:
mO = 50 - 42 = 8 (gam)
Số mol của CuO đã tham gia phản ứng là:
nCuO = nO = 8 ÷ 16 = 0,5 (mol)
Hiệu suất phản ứng là: H = (0,5 × 80 ÷ 50) × 100% = 80%
⇒ Chọn đáp án B Đáp án: B

Câu 37 [705713]: Phương pháp điều chế kim loại nào đã được sử dụng trong quá tình sản xuất Zn theo sơ đồ trên?
A, Thủy luyện.
B, Nhiệt luyện.
C, Điện phân.
D, Chiết.
Phản ứng 1: Đốt quặng zinc blende (ZnS) để chuyển thành ZnO.
Phản ứng 2: Khử ZnO bằng than cốc (C) ở nhiệt độ cao để thu được Zn kim loại.
👉 Đây là phương pháp nhiệt luyện (dùng nhiệt và chất khử C để khử oxide kim loại thành kim loại).
⇒ Chọn đáp án B Đáp án: B
Phản ứng 2: Khử ZnO bằng than cốc (C) ở nhiệt độ cao để thu được Zn kim loại.
👉 Đây là phương pháp nhiệt luyện (dùng nhiệt và chất khử C để khử oxide kim loại thành kim loại).
⇒ Chọn đáp án B Đáp án: B
Câu 38 [705714]: Phát biểu nào sau đây đúng?
A, ZnO đóng vai trò là chất khử trong phản ứng hoá học trên.
B, Phản ứng xảy ra ở nhiệt độ rất cao, tạo ra kẽm ở dạng hơi.
C, O2 được thêm vào để làm giảm nồng độ CO giúp cân bằng dịch chuyển sang chiều thuận.
D, Phương pháp này còn được dùng để tách kim loại Al khỏi hợp chất Al2O3.
Phân tích các phát biểu:
❌ A. Sai, ZnO bị khử thành Zn, nên nó là chất bị khử, còn C là chất khử (C bị oxi hóa thành CO).
✅ B. Đúng, kẽm có nhiệt độ sôi 907 oC, còn phản ứng khử ZnO bằng C thường xảy ra ở trên 1000 oC, khiến kẽm bay hơi và phải ngưng tụ lại để thu hồi.
❌ C. Sai,O2 không tham gia vào phản ứng khử ZnO bằng C. Thêm O2 có thể gây phản ứng cháy với C tạo CO2, không có lợi cho quá trình điều chế Zn.
❌ D. Sai. Phương pháp trên không thể điều chế kim loại nhôm từ hợp chất Al2O3. Nhôm được điều chế từ aluminium oxide bằng phương pháp điện nóng chảy.
⇒ Chọn đáp án B Đáp án: B
❌ A. Sai, ZnO bị khử thành Zn, nên nó là chất bị khử, còn C là chất khử (C bị oxi hóa thành CO).
✅ B. Đúng, kẽm có nhiệt độ sôi 907 oC, còn phản ứng khử ZnO bằng C thường xảy ra ở trên 1000 oC, khiến kẽm bay hơi và phải ngưng tụ lại để thu hồi.
❌ C. Sai,O2 không tham gia vào phản ứng khử ZnO bằng C. Thêm O2 có thể gây phản ứng cháy với C tạo CO2, không có lợi cho quá trình điều chế Zn.
❌ D. Sai. Phương pháp trên không thể điều chế kim loại nhôm từ hợp chất Al2O3. Nhôm được điều chế từ aluminium oxide bằng phương pháp điện nóng chảy.
⇒ Chọn đáp án B Đáp án: B
Câu 39 [704194]: “Tái chế là quá trình xử lí để tái sử dụng ...(1)... không cần thiết thành ...(2)... mang lại lợi ích cho đời sống và sản xuất”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, tài nguyên thiên nhiên, năng lượng mới.
B, rác thải, sản phẩm mới .
C, rác thải hoặc vật liệu, vật liệu mới.
D, kim loại, kim loại mới.
Tái chế là quá trình xử lí để tái sử dụng rác thải hoặc vật liệu không cần thiết thành vật liệu mới mang lại lợi ích cho đời sống và sản xuất.
Giải thích:
- Các vật liệu hoặc đồ dùng đã qua sử dụng, không còn giá trị sử dụng ban đầu hoặc bị bỏ đi, như chai nhựa, giấy cũ, kim loại phế liệu, v.v sẽ được thu gom, phân loại và làm sạch, xử lý để sản xuất ra vật liệu mới.
- Đây là một trong những phương pháp quản lý rác thải hiệu quả, góp phần bảo vệ môi trường, tiết kiệm tài nguyên và giảm thiểu ô nhiễm.
⇒ Chọn đáp án C
Đáp án: C
Giải thích:
- Các vật liệu hoặc đồ dùng đã qua sử dụng, không còn giá trị sử dụng ban đầu hoặc bị bỏ đi, như chai nhựa, giấy cũ, kim loại phế liệu, v.v sẽ được thu gom, phân loại và làm sạch, xử lý để sản xuất ra vật liệu mới.
- Đây là một trong những phương pháp quản lý rác thải hiệu quả, góp phần bảo vệ môi trường, tiết kiệm tài nguyên và giảm thiểu ô nhiễm.
⇒ Chọn đáp án C
Đáp án: C
Câu 40 [706166]: Trong quá trình tái chế kim loại, ở công đoạn phân loại phế liệu, có thể dùng nam châm lớn để tách riêng phế liệu
A, nhôm.
B, thép.
C, đồng.
D, kẽm.
Nam châm có khả năng hút các vật liệu từ tính, trong đó thép là một ví dụ điển hình.
Các kim loại khác như nhôm, đồng và kẽm không có tính từ tính, do đó không bị nam châm hút.
Vì vậy, trong quá trình tái chế kim loại, nam châm lớn có thể được sử dụng để tách riêng phế liệu thép ra khỏi hỗn hợp các kim loại khác.
⟹ Chọn đáp án B Đáp án: B
Các kim loại khác như nhôm, đồng và kẽm không có tính từ tính, do đó không bị nam châm hút.
Vì vậy, trong quá trình tái chế kim loại, nam châm lớn có thể được sử dụng để tách riêng phế liệu thép ra khỏi hỗn hợp các kim loại khác.
⟹ Chọn đáp án B Đáp án: B
Câu 41 [560691]: Hình vẽ bên liên quan đến công đoạn nào trong quá trình tái chế kim loại?


A, Thu gom, phân loại.
B, Nghiền, băm nhỏ.
C, Luyện kim.
D, Tạo vật liệu.

Quá trình tinh luyện để cho các kim loại đạt được độ sạch cao nhất, sau đó pha trộn giữa các kim loại đó lại để có các hợp kim đáp ứng được những yêu cầu mong như mong muốn. Và sau đó tạo hình dáng cho chúng để phù hợp với các nhu cầu sử dụng của các chủ đầu tư. Đây là quá trình được gọi là công nghệ luyện kim.
=> Chọn đáp án C Đáp án: C
Câu 42 [560692]: Lý do nào không đúng khi nói về sự cần thiết của tái chế kim loại?
A, Trữ lượng các mỏ quặng kim loại ngày càng cạn kiệt.
B, Do lượng phế thải kim loại tạo ra ngày càng nhiều.
C, Đảm bảo nguồn cung, tăng giá trị kinh tế.
D, Kim loại thu được từ tái chế tinh khiết hơn kim loại sản xuất từ quặng.
✔️A. Việc khai thác quặng kim loại làm cạn kiệt tài nguyên tự nhiên.
✔️B. Tái chế giúp giảm lượng phế thải, bảo vệ môi trường.
✔️C. Tái chế kim loại giúp duy trì nguồn cung và giảm chi phí khai thác.
❌D. Sai vì kim loại tái chế thường chứa tạp chất, không thể tinh khiết hơn so với kim loại nguyên khai sản xuất từ quặng.
=> Chọn đáp án D Đáp án: D
✔️B. Tái chế giúp giảm lượng phế thải, bảo vệ môi trường.
✔️C. Tái chế kim loại giúp duy trì nguồn cung và giảm chi phí khai thác.
❌D. Sai vì kim loại tái chế thường chứa tạp chất, không thể tinh khiết hơn so với kim loại nguyên khai sản xuất từ quặng.
=> Chọn đáp án D Đáp án: D
Câu 43 [706199]: Xỉ xuất hiện trong quá trình tách kim loại, luyện kim và tinh luyện để tái chế kim loại. Xỉ là hỗn hợp nhiều chất, hỗn hợp này thường
A, dễ bay hơi.
B, dễ chảy lỏng.
C, có nhiều độc tính nên cần phải được chôn lấp sau khi được tháo ra khỏi lò.
D, có khối lượng riêng nhỏ hơn so với kim loại cần tách hoặc cần tái chế.
Xỉ là sản phẩm phụ trong quá trình luyện kim, thường là hỗn hợp các oxit kim loại và tạp chất khác. Xỉ là hỗn hợp nhiều chất, hỗn hợp này thường có khối lượng riêng nhỏ hơn so với kim loại cần tách hoặc cần tái chế. Điều này giải thích tại sao trong quá trình luyện kim, xỉ thường nổi lên trên bề mặt kim loại nóng chảy. Nhờ đó, người ta dễ dàng loại bỏ xỉ khỏi kim loại tinh khiết bên dưới bằng cách gạn hoặc vớt.
⟹ Chọn đáp án D Đáp án: D
⟹ Chọn đáp án D Đáp án: D
Câu 44 [703945]: Quy trình tái chế một kim loại thông dụng để đựng đồ uống được thực hiện như sau:
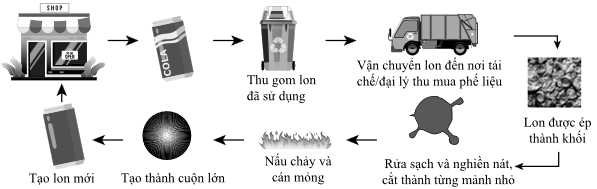
Phát biểu nào sau đây về quy trình trên đúng?

Phát biểu nào sau đây về quy trình trên đúng?
A, Kim loại được tái chế trong quy trình có thể là nhôm (aluminium).
B, Rửa sạch nguyên liệu trước khi nóng chảy giúp loại lớp sơn trên vỏ, lon.
C, Trong quá trình tái chế có sử dụng phương pháp nhiệt luyện.
D, Các giai đoạn của quy trình không làm phát thải khí gây hiệu ứng nhà kính.
Phân tích các phát biểu:
✔️ A. Đúng. Nhôm là một trong những kim loại phổ biến được dùng để sản xuất lon đồ uống nhờ nhẹ, bền và khả năng tái chế cao. Trong thực tế, nhôm từ vỏ lon đồ uống thường được tái chế để sản xuất lon mới.
❌ B. Sai. Rửa sạch trước khi nóng chảy thường chỉ nhằm loại bỏ bụi bẩn, dầu mỡ, hoặc tạp chất bề mặt. Lớp sơn hoặc lớp phủ trên lon nhôm thường được loại bỏ thông qua quá trình đốt cháy hoặc nhiệt phân trong lò nung, không phải trong bước rửa.
❌ C. Sai. Quá trình tái chế nhôm là nóng chảy nhôm phế liệu ở nhiệt độ cao và đúc lại chứ không phải nhiệt luyện.
❌ D. Sai. Quá trình tái chế nhôm, đặc biệt là giai đoạn nóng chảy, tiêu tốn năng lượng và có thể phát thải khí nhà kính như C gây hiệu ứng nhà kính.
⇒ Chọn đáp án A Đáp án: A
✔️ A. Đúng. Nhôm là một trong những kim loại phổ biến được dùng để sản xuất lon đồ uống nhờ nhẹ, bền và khả năng tái chế cao. Trong thực tế, nhôm từ vỏ lon đồ uống thường được tái chế để sản xuất lon mới.
❌ B. Sai. Rửa sạch trước khi nóng chảy thường chỉ nhằm loại bỏ bụi bẩn, dầu mỡ, hoặc tạp chất bề mặt. Lớp sơn hoặc lớp phủ trên lon nhôm thường được loại bỏ thông qua quá trình đốt cháy hoặc nhiệt phân trong lò nung, không phải trong bước rửa.
❌ C. Sai. Quá trình tái chế nhôm là nóng chảy nhôm phế liệu ở nhiệt độ cao và đúc lại chứ không phải nhiệt luyện.
❌ D. Sai. Quá trình tái chế nhôm, đặc biệt là giai đoạn nóng chảy, tiêu tốn năng lượng và có thể phát thải khí nhà kính như C gây hiệu ứng nhà kính.
⇒ Chọn đáp án A Đáp án: A
Dạng 2: TRẮC NGHIỆM ĐÚNG SAI – mỗi ý a), b), c), d) chọn đúng hoặc sai.
Câu 45 [560695]: Kim loại kẽm được tách từ hợp chất zinc sulfide trong khoáng vật sphalerite.
Bước 1: Đốt zinc sulfide trong khí oxygen dư để tạo zinc oxide và sulfur dioxide.
Bước 2: Để thu được zinc, có thể khử zinc oxide bằng carbon.
Bước 1: Đốt zinc sulfide trong khí oxygen dư để tạo zinc oxide và sulfur dioxide.
Bước 2: Để thu được zinc, có thể khử zinc oxide bằng carbon.
Phân tích các phát biểu:
❌a. Sai. Zinc sulfide có công thức hóa học là ZnS, không phải ZnSO3
✔️b. Đúng. Trong hợp chất ZnS, (S) có số oxi hóa -2. Vì hợp chất trung hòa điện tích, nên (Zn) phải có số oxi hóa +2.
❌c. Sai. Phản ứng trong bước 1 là: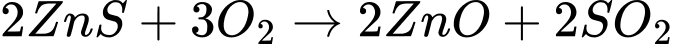
Số oxi hóa của Zn vẫn là +2 trong cả ZnS và ZnO.Tuy nhiên, (S) trong ZnS bị oxi hóa từ -2 (trong ZnS) thành +4 (trong SO2).
✔️d. Đúng. Zinc (Zn) trong ZnO có số oxi hóa +2 và bị khử thành số oxi hóa 0 trong Zn.
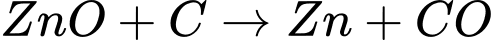
❌a. Sai. Zinc sulfide có công thức hóa học là ZnS, không phải ZnSO3
✔️b. Đúng. Trong hợp chất ZnS, (S) có số oxi hóa -2. Vì hợp chất trung hòa điện tích, nên (Zn) phải có số oxi hóa +2.
❌c. Sai. Phản ứng trong bước 1 là:
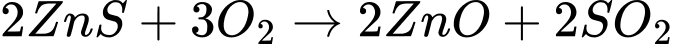
Số oxi hóa của Zn vẫn là +2 trong cả ZnS và ZnO.Tuy nhiên, (S) trong ZnS bị oxi hóa từ -2 (trong ZnS) thành +4 (trong SO2).
✔️d. Đúng. Zinc (Zn) trong ZnO có số oxi hóa +2 và bị khử thành số oxi hóa 0 trong Zn.
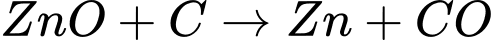
Câu 46 [560696]: Để tái chế nhôm, người ta có thể sử dụng phế liệu kim loại như vỏ của các lon, hộp chứa nước giải khát hay thực phẩm. Phế liệu này còn lẫn các tạp chất là các hợp chất hữu cơ và vô cơ (có trong nhãn, mác in hoặc sơn trên vỏ lon, hộp). Phế liệu được cắt, băm nhỏ rồi cho vào lò nung đến khi chảy lỏng. Phần lớn các tạp chất biến thành xỉ lỏng, nổi lên trên, được vớt ra khỏi lò. Phần tạp chất còn lại vẫn bị lẫn trong trong nhôm ở trạng thái nóng chảy.
Phân tích các phát biểu:
✔️ a. Đúng. Việc cắt, băm nhỏ phế liệu nhôm trước khi nung chảy để tăng diện tích tiếp xúc với nhiệt.
✔️b. Đúng. Nhôm tái chế có thể chứa các tạp chất như kim loại nặng (chì, cadmium…) hoặc hợp chất không mong muốn, ảnh hưởng đến an toàn thực phẩm. Không nên dùng nhôm tái chế để chế tạo xoong, chảo.
✔️ c. Đúng. Vỏ của các lon, hộp chứa nước giải khát chứa lượng nhôm lớn.
✔️ d. Đúng. Lớp xỉ lỏng bên trên đóng vai trò tạo lớp bảo vệ, ngăn không cho Al tiếp xúc với không khí.
✔️ a. Đúng. Việc cắt, băm nhỏ phế liệu nhôm trước khi nung chảy để tăng diện tích tiếp xúc với nhiệt.
✔️b. Đúng. Nhôm tái chế có thể chứa các tạp chất như kim loại nặng (chì, cadmium…) hoặc hợp chất không mong muốn, ảnh hưởng đến an toàn thực phẩm. Không nên dùng nhôm tái chế để chế tạo xoong, chảo.
✔️ c. Đúng. Vỏ của các lon, hộp chứa nước giải khát chứa lượng nhôm lớn.
✔️ d. Đúng. Lớp xỉ lỏng bên trên đóng vai trò tạo lớp bảo vệ, ngăn không cho Al tiếp xúc với không khí.
Câu 47 [560697]: Hầu hết các kim loại đều được điều chế từ quặng tìm thấy trong lớp vỏ Trái đất. Phương pháp được sử dụng để tách kim loại ra khỏi quặng có liên quan đến khả năng phản ứng của kim loại. Mức độ phản ứng của một số kim loại được hiển thị dưới đây:
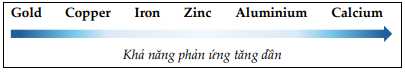

Phân tích các phát biểu:
✔️ a. Đúng. Trong tự nhiên có thể tìm thấy gold ở dạng đơn chất.
✔️ b. Đúng. Aluminium khả năng hoạt động hóa học mạnh hơn iron, copper nên dễ nhường electron hơn.
❌ c. Sai. Tách Al bằng phương pháp điện phân nóng chảy.
❌ d. Sai. Cả 4 phương pháp đều có thể sử dụng để điều chế copper, tuy nhiên điện phân nóng chảy không phổ biến vì hiệu quả kinh tế không cao.
✔️ a. Đúng. Trong tự nhiên có thể tìm thấy gold ở dạng đơn chất.
✔️ b. Đúng. Aluminium khả năng hoạt động hóa học mạnh hơn iron, copper nên dễ nhường electron hơn.
❌ c. Sai. Tách Al bằng phương pháp điện phân nóng chảy.
❌ d. Sai. Cả 4 phương pháp đều có thể sử dụng để điều chế copper, tuy nhiên điện phân nóng chảy không phổ biến vì hiệu quả kinh tế không cao.
Câu 48 [560699]: Trong công nghiệp, aluminium (nhôm) được sản xuất từ quặng bauxite theo hai giai đoạn chính:
Giai đoạn 1: Tinh chế quặng bauxite.
Giai đoạn 2: Điện phân Al2O3 nóng chảy.
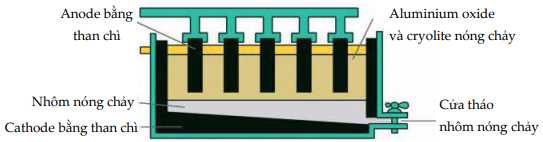
Giai đoạn 1: Tinh chế quặng bauxite.
Giai đoạn 2: Điện phân Al2O3 nóng chảy.

Phân tích các phát biểu:
❌ a. Sai. Aluminium được tạo ra ở cathode (cực âm).
❌ b. Sai. Khí O2 sinh ra ở nhiệt độ cao phản ứng với điện cực than chì (C) tạo hỗn hợp khí CO và khí CO2.
✔️ c. Đúng. Cực dương (anode) làm bằng than chì bị mòn dầy theo thời gian vì phản ứng với oxygen và cần được thay thế thường xuyên.
❌ d. Sai. PTHH: 2Al2O3 ⟶ 4Al + 3O2 => nO2= 3/4. nAl = 1/36 (mol).
Vì lượng CO và CO2 sinh ra là như nhau => nCO= nCO2= a (mol) => nO2 phản ứng= a/2 + a= 1/36
=> a=1/54 => Khối lượng carbon phản ứng là 2. a . 12 = 0,44 tấn.
❌ a. Sai. Aluminium được tạo ra ở cathode (cực âm).
❌ b. Sai. Khí O2 sinh ra ở nhiệt độ cao phản ứng với điện cực than chì (C) tạo hỗn hợp khí CO và khí CO2.
✔️ c. Đúng. Cực dương (anode) làm bằng than chì bị mòn dầy theo thời gian vì phản ứng với oxygen và cần được thay thế thường xuyên.
❌ d. Sai. PTHH: 2Al2O3 ⟶ 4Al + 3O2 => nO2= 3/4. nAl = 1/36 (mol).
Vì lượng CO và CO2 sinh ra là như nhau => nCO= nCO2= a (mol) => nO2 phản ứng= a/2 + a= 1/36
=> a=1/54 => Khối lượng carbon phản ứng là 2. a . 12 = 0,44 tấn.
Câu 49 [560698]: Mức độ phản ứng của một số kim loại được hiển thị dưới đây:


Phân tích các phát biểu:
❌ a. Sai. Kim loại luôn tìm thấy ở dạng quặng trong vỏ Trái đất là nhôm và sắt.
✔️ b. Đúng. Điều chế aluminium từ quặng bauxite có thể dùng phương pháp điện phân nóng chảy.
❌ c. Sai. Trong phản ứng thì iron oxide đóng vai trò là chất nhận electron để tạo thành kim loại iron.
❌ d. Sai. Từ 240 tấn Fe2O3 => nFe2O3 = 240/160 = 1,5 => nFe = 1,5 .2 = 3 mol. Vậy khối lượng Fe thu được là 168 tấn.
❌ a. Sai. Kim loại luôn tìm thấy ở dạng quặng trong vỏ Trái đất là nhôm và sắt.
✔️ b. Đúng. Điều chế aluminium từ quặng bauxite có thể dùng phương pháp điện phân nóng chảy.
❌ c. Sai. Trong phản ứng thì iron oxide đóng vai trò là chất nhận electron để tạo thành kim loại iron.
❌ d. Sai. Từ 240 tấn Fe2O3 => nFe2O3 = 240/160 = 1,5 => nFe = 1,5 .2 = 3 mol. Vậy khối lượng Fe thu được là 168 tấn.
Câu 50 [560700]: Iron được chiết xuất từ quặng hematite (thành phần chính là Fe2O3, ngoài ra còn có sillic dioxide). Nguyên liệu ban đầu gồm có quặng hematite, than cốc và chất phụ gia như đá vôi sẽ sản xuất được hợp kim quan trọng của iron là gang. Quá trình luyện gang trong lò cao với 3 phản ứng chính:
- Phản ứng tạo chất khử CO (1).
- Phản ứng CO khử iron oxide thành iron (2).
- Phản ứng tạo thành xỉ giữa calcium oxide và sillic dioxide (3).
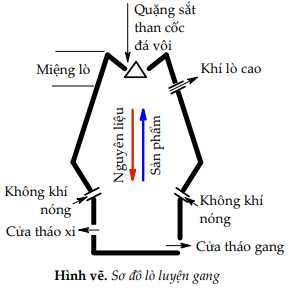
- Phản ứng tạo chất khử CO (1).
- Phản ứng CO khử iron oxide thành iron (2).
- Phản ứng tạo thành xỉ giữa calcium oxide và sillic dioxide (3).

Giai đoạn 1:
C + O2 ⟶ CO2
C + O2 ⟶ CO
Giai đoạn 2 :
3CO + Fe2O3 ⟶ 2Fe + 3CO2
C tăng số oxi hóa trong các giai đoạn ⟶ nhường e
Phân tích các đáp án:
✔️A – Đúng. Phản ứng xảy ra ở (2) là
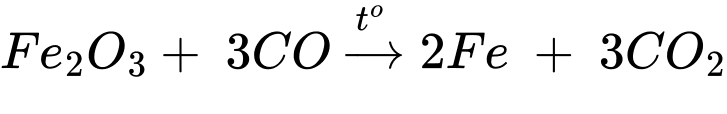
❌B – Sai. Carbon đóng vai trò là chất nhường electron do là chất khử.
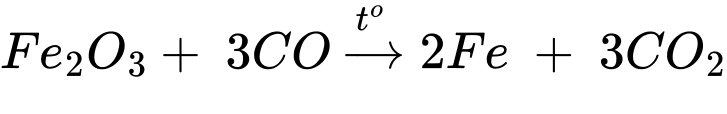
Quá trình oxi hóa: C2+ → C4+ + 2e
Quá trình khử: Fe3+ + 3e → Fe
✔️C – Đúng. Phản ứng tạo thành xỉ là CaO + SiO2 → CaSiO3
✔️D – Đúng. Vai trò của đá vôi là loại bỏ tạp chất sillic dioxide (SiO2) có trong quặng theo quá trình:
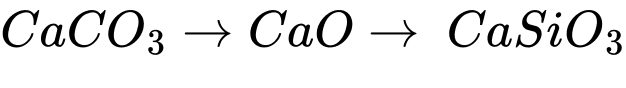
C + O2 ⟶ CO2
C + O2 ⟶ CO
Giai đoạn 2 :
3CO + Fe2O3 ⟶ 2Fe + 3CO2
C tăng số oxi hóa trong các giai đoạn ⟶ nhường e
Phân tích các đáp án:
✔️A – Đúng. Phản ứng xảy ra ở (2) là
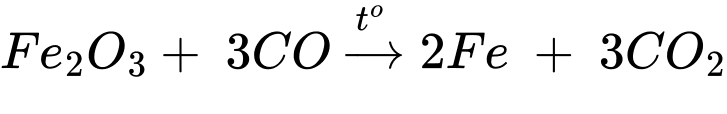
❌B – Sai. Carbon đóng vai trò là chất nhường electron do là chất khử.
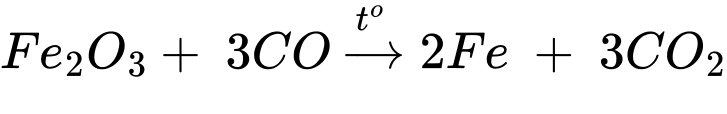
Quá trình oxi hóa: C2+ → C4+ + 2e
Quá trình khử: Fe3+ + 3e → Fe
✔️C – Đúng. Phản ứng tạo thành xỉ là CaO + SiO2 → CaSiO3
✔️D – Đúng. Vai trò của đá vôi là loại bỏ tạp chất sillic dioxide (SiO2) có trong quặng theo quá trình:
Câu 51 [560701]: Trong công nghiệp, nhôm được sản xuất bằng cách điện phân nóng chảy hỗn hợp aluminium oxide (Al2O3) và cryolite (Na3AlF6) còn gọi là quy trình Hall Héroult:
2Al2O3(s)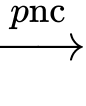 4Al(l) + 3O2(g)
4Al(l) + 3O2(g)
Nhiệt độ nóng chảy của hỗn hợp aluminium oxide và cryolite khoảng 950oC, thấp hơn nhiều so với nhiệt độ nóng chảy của aluminium oxide (> 2000oC); ngoài ra, cryolite còn làm tăng độ dẫn điện của hỗn hợp nóng chảy. Trong quá trình điện phân, cực dương làm bằng graphite bị ăn mòn và liên tục được nhúng xuống bể điện phân. Sau một thời gian, các thanh graphite này sẽ được thay mới.
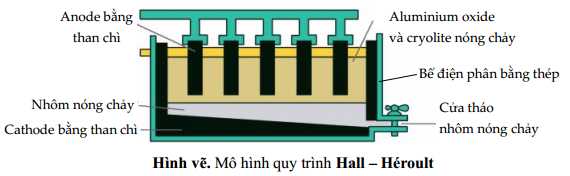
2Al2O3(s)
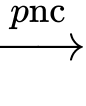 4Al(l) + 3O2(g)
4Al(l) + 3O2(g)Nhiệt độ nóng chảy của hỗn hợp aluminium oxide và cryolite khoảng 950oC, thấp hơn nhiều so với nhiệt độ nóng chảy của aluminium oxide (> 2000oC); ngoài ra, cryolite còn làm tăng độ dẫn điện của hỗn hợp nóng chảy. Trong quá trình điện phân, cực dương làm bằng graphite bị ăn mòn và liên tục được nhúng xuống bể điện phân. Sau một thời gian, các thanh graphite này sẽ được thay mới.

Phân tích các phát biểu:
✔️ a. Đúng. Aluminium kim loại được tách ra tại cathode.
✔️ b. Đúng. Cryloite được thêm vào bể điện phân giúp tiết kiệm năng lượng, giảm chi phí sản xuất.
❌ c. Sai. Khí oxygen có lẫn cả CO và CO2 vì O2 phản ứng với điện cực than chì.
❌ d. Sai. Trong quá trình điện phân nhôm oxit, nhôm kim loại được tạo thành ở cathode và chìm xuống đáy bể do mật độ cao hơn cryolite. Nếu đổi cực, nhôm sẽ di chuyển lên trên, điều này không khả thi vì nó không thể nổi qua lớp cryolite.
✔️ a. Đúng. Aluminium kim loại được tách ra tại cathode.
✔️ b. Đúng. Cryloite được thêm vào bể điện phân giúp tiết kiệm năng lượng, giảm chi phí sản xuất.
❌ c. Sai. Khí oxygen có lẫn cả CO và CO2 vì O2 phản ứng với điện cực than chì.
❌ d. Sai. Trong quá trình điện phân nhôm oxit, nhôm kim loại được tạo thành ở cathode và chìm xuống đáy bể do mật độ cao hơn cryolite. Nếu đổi cực, nhôm sẽ di chuyển lên trên, điều này không khả thi vì nó không thể nổi qua lớp cryolite.
Dạng 3: TRẮC NGHIỆM YÊU CẦU TRẢ LỜI NGẮN
Câu 52 [560702]: Một khoáng chất có chứa 20,93% nhôm; 21,7% silicon và còn lại là oxygen và hydrogen (về khối lượng). Tổng số nguyên tử trong một phân tử khoáng vật (dạng đơn giản nhất) này là
Giả sử ta có 100 gam quặng loại này.
Tính lần lượt số mol các chất đã biết: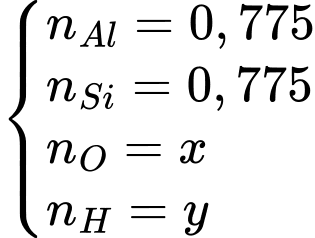
Trong quặng, các nguyên tố sẽ có các số oxi hóa tương ứng Al3+, Si4+, O2-, H+. Ngoài ra, các số oxi hóa này phải đảm bảo cân bằng giữa tổng số oxi hóa âm và dương.
Tóm lại, ta có hệ: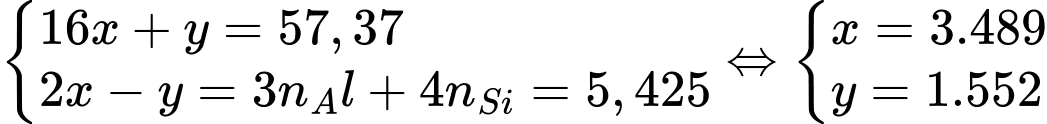
Tỉ lệ nguyên tử Al : Si : O : H = 0,775 : 0,775 : 3,489 : 1,552 = 2 : 2 : 9 : 4
=> Tổng số nguyên tử là 17 nguyên tử.
=> Điền đáp án: 17
Tính lần lượt số mol các chất đã biết:
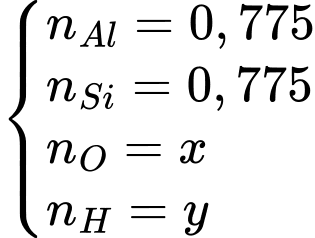
Trong quặng, các nguyên tố sẽ có các số oxi hóa tương ứng Al3+, Si4+, O2-, H+. Ngoài ra, các số oxi hóa này phải đảm bảo cân bằng giữa tổng số oxi hóa âm và dương.
Tóm lại, ta có hệ:
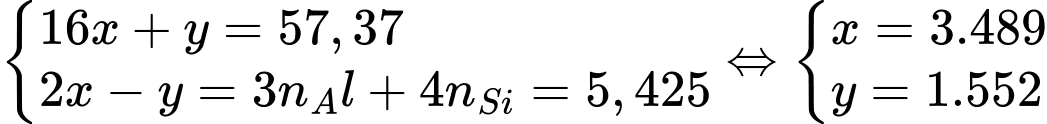
Tỉ lệ nguyên tử Al : Si : O : H = 0,775 : 0,775 : 3,489 : 1,552 = 2 : 2 : 9 : 4
=> Tổng số nguyên tử là 17 nguyên tử.
=> Điền đáp án: 17
Câu 53 [560703]: Một loại khoáng chất X có chứa 13,77% Na; 7,18% Mg; 57,48% O; 2,39% H và còn lại là nguyên tố Y về khối lượng. Số nguyên tử có trong một phân tử khoáng chất X (dạng đơn giản nhất) là
Đặt công thức phân tử là Nax.Mgy.Oz.Ht.Yu
Ta có x : y : z : t : u = (13,77/23) : (7,18/24) : (57,48/16) : (2,39/1) : (19,18/MX)
= 2 : 1 : 12 : 8 : (64/MY)
Vì x, y, z, t, u là những số nguyên nên 64/MY phải là số nguyên.
Biện luận MY có thể là:
+) 2 với u = 32 (loại)
+) 4 với u = 16 (loại)
+) 8 với u = 8 (loại)
+) 16 với u = 4 ⟶ X là O (trùng với oxygen đã có => loại)
+) 32 với u = 2 ⟶ X là S.
+) 64 với u = 1 ⟶ X là Cu (không cân bằng số oxi hóa trong hợp chất => loại)
Vậy, khoáng vật có thể là
Na2MgO12H8S2 (Na2SO4.MgSO4.4H2O)
=> Điền đáp án: 25
Ta có x : y : z : t : u = (13,77/23) : (7,18/24) : (57,48/16) : (2,39/1) : (19,18/MX)
= 2 : 1 : 12 : 8 : (64/MY)
Vì x, y, z, t, u là những số nguyên nên 64/MY phải là số nguyên.
Biện luận MY có thể là:
+) 2 với u = 32 (loại)
+) 4 với u = 16 (loại)
+) 8 với u = 8 (loại)
+) 16 với u = 4 ⟶ X là O (trùng với oxygen đã có => loại)
+) 32 với u = 2 ⟶ X là S.
+) 64 với u = 1 ⟶ X là Cu (không cân bằng số oxi hóa trong hợp chất => loại)
Vậy, khoáng vật có thể là
Na2MgO12H8S2 (Na2SO4.MgSO4.4H2O)
=> Điền đáp án: 25
Câu 54 [560704]: Scheelite là khoáng vật chứa calcium với wolfram với công thức hóa học CaxWyOz và tạp chất. Kết quả phân tích cho thấy trong CaxWyOz có chứa 13,9% là calcium, 63,9% là wolfram còn lại là oxygen về khối lượng. Giá trị (x + y + z) là bao nhiêu?
%O= 100 - 13,9 - 63,9 = 22,2
=> Tỉ lệ: x : y : z =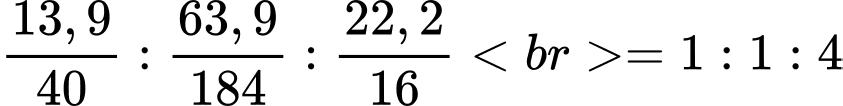
=> Công thức: CaWO4
=> Điền đáp án: 6
=> Tỉ lệ: x : y : z =
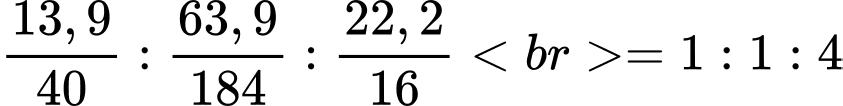
=> Công thức: CaWO4
=> Điền đáp án: 6
Câu 55 [560705]: Phần trăm đồng trong quặng thường khá nhỏ nên việc tái chế đồng là cần thiết và mang lại nhiều hiệu quả về kinh tế. Từ 5 000 kg một quặng loại đồng có thể điều chế được 42,5 kg đồng. Phần trăm theo khối lượng của đồng trong loại quặng trên là bao nhiêu? (làm tròn đến hai chữ số thập phân)
Phần trăm copper trong loại quặng trên là: 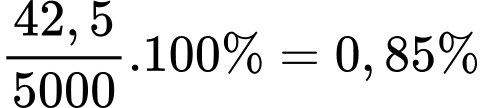
=> Điền đáp án: 0,85
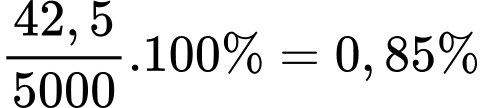
=> Điền đáp án: 0,85
Câu 56 [560706]: Phân tích một loại quặng của titanium thấy rằng cứ 12,0 gam nguyên tử titanium sẽ cần kết hợp với 8,0 gam nguyên tử oxygen. Tổng số nguyên tử trong công thức oxide của titanium ở dạng tối giản nhất là bao nhiêu?
Tỉ lệ Ti : O= 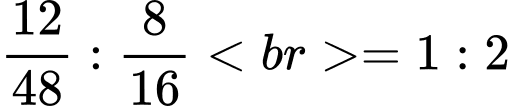
=> Công thức TiO2
=> Điền đáp án: 3
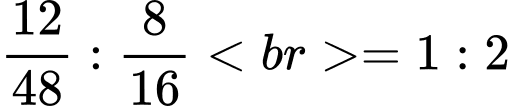
=> Công thức TiO2
=> Điền đáp án: 3
Câu 57 [560707]: Chì được tìm thấy trong vỏ Trái đất dưới dạng quặng. Trong 5 000 kg quặng phát hiện có 48,2 kg kim loại chì. Phần trăm theo khối lượng của chì trong quặng là bao nhiêu? (làm tròn đến hai chữ số thập phân)
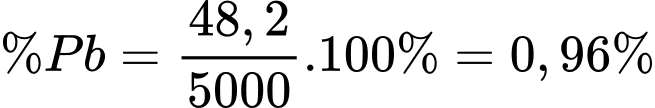
=> Điền đáp án: 0,96
Câu 58 [560708]: Phân tích các mẫu đá Mặt Trăng cho biết thành phần hóa học của bề mặt Mặt Trăng như sau:
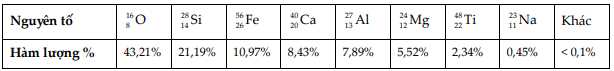
Biết rằng các nguyên tố đều ở dạng oxide, trong đó Ti chỉ ở dạng TiO2. Để xem nguyên tố iron trên bề Mặt Trăng tồn tại chủ yếu ở dạng oxide nào, hãy tính toán giá trị tỉ lệ số mol oxygen và iron (làm tròn đến hàng phần trăm).

Biết rằng các nguyên tố đều ở dạng oxide, trong đó Ti chỉ ở dạng TiO2. Để xem nguyên tố iron trên bề Mặt Trăng tồn tại chủ yếu ở dạng oxide nào, hãy tính toán giá trị tỉ lệ số mol oxygen và iron (làm tròn đến hàng phần trăm).
Giả sử có 100 gam mẫu đá ban đầu.
% oxygen có trong mẫu = tổng % oxygen có trong các oxide.
Số mol oxygen trong các hợp chất = ( khối lượng kim loại / M kim loại ) × số nguyên tử O
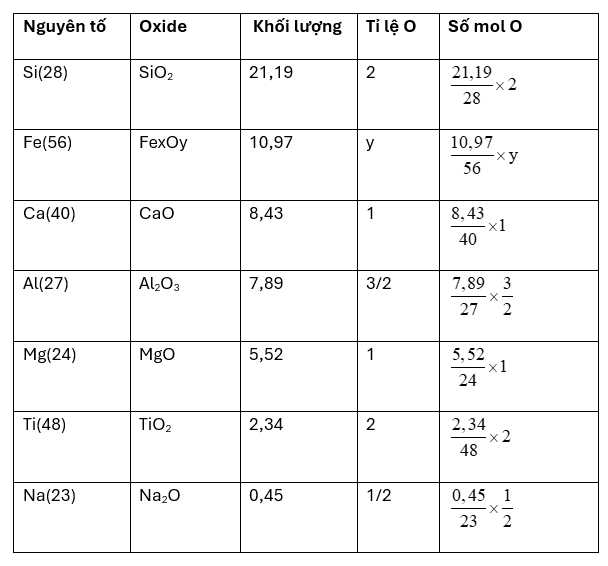
nO = m : M = 43,21 : 16
y = nO - nO trong các hợp chất = (nO - nSiO2 - nCaO - nAl2O3 - nMgO - nTiO2 - nNa2O) / (10,97 : 56)
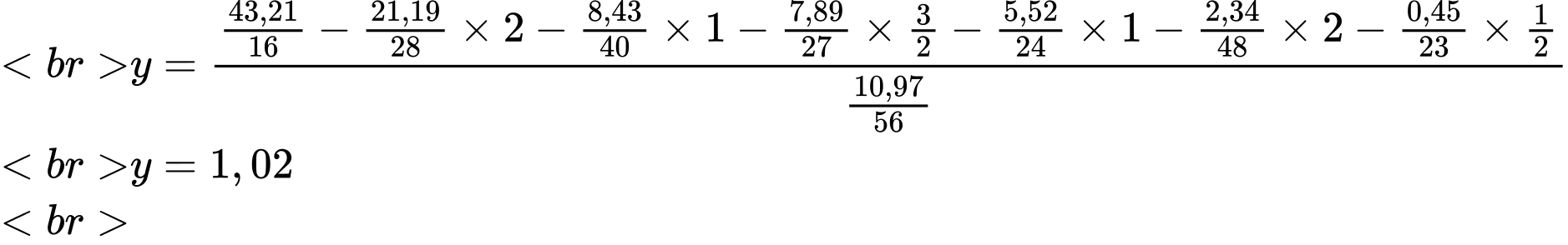
=> Điền đáp án: 1,02
% oxygen có trong mẫu = tổng % oxygen có trong các oxide.
Số mol oxygen trong các hợp chất = ( khối lượng kim loại / M kim loại ) × số nguyên tử O

nO = m : M = 43,21 : 16
y = nO - nO trong các hợp chất = (nO - nSiO2 - nCaO - nAl2O3 - nMgO - nTiO2 - nNa2O) / (10,97 : 56)
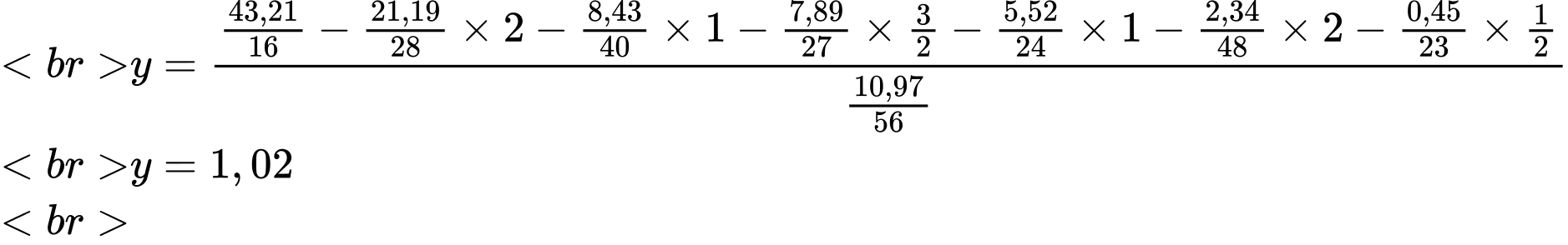
=> Điền đáp án: 1,02
Câu 59 [705793]: Trong công nghiệp, kim loại sắt (Iron, Fe) được sản xuất bằng phương pháp nhiệt luyện quặng hemantite. Với hiệu suất chuyển hóa từ Fe2O3 thành Fe là 75%. Để sản xuất được 5,6 tấn Fe cần dùng bao nhiêu tấn nguyên liệu quặng hematite biết quặng có chưa 70% Fe2O3. (Làm tròn đến hàng phần mười)
Trong Fe2O3 có 2 nguyên tử Fe
Số mol Fe = m ÷ M = 5,6.106 ÷ 56 = 0,1.106 mol
⇒ Số mol Fe2O3 = nFe ÷ 2 ÷ Hiệu suất = 0,1 ÷ 2 ÷ 75%
Do trong quặng chứa 70% Fe2O3
⇒ mquặng = mFe2O3 ÷ 70% = 0,1.106 ÷ 2 ÷ 75% × 160 ÷ 70%
= 15238095 gam ≈ 15,2 tấn
⇒ Điền đáp án : 15,2
Số mol Fe = m ÷ M = 5,6.106 ÷ 56 = 0,1.106 mol
⇒ Số mol Fe2O3 = nFe ÷ 2 ÷ Hiệu suất = 0,1 ÷ 2 ÷ 75%
Do trong quặng chứa 70% Fe2O3
⇒ mquặng = mFe2O3 ÷ 70% = 0,1.106 ÷ 2 ÷ 75% × 160 ÷ 70%
= 15238095 gam ≈ 15,2 tấn
⇒ Điền đáp án : 15,2
Câu 60 [680874]: [TK 2025]: Trong công nghiệp, kim loại nhôm (aluminium, Al) được sản xuất bằng phương pháp điện phân nóng chảy aluminium oxide. Biết hiệu suất của quá trình chuyển hóa Al2O3 thành Al là 95,4 %. Để sản xuất 5,4 tấn Al cần sử dụng bao nhiêu tấn nguyên liệu Al2O3 (làm tròn đến hàng phần mười)?
Sơ đồ phản ứng:
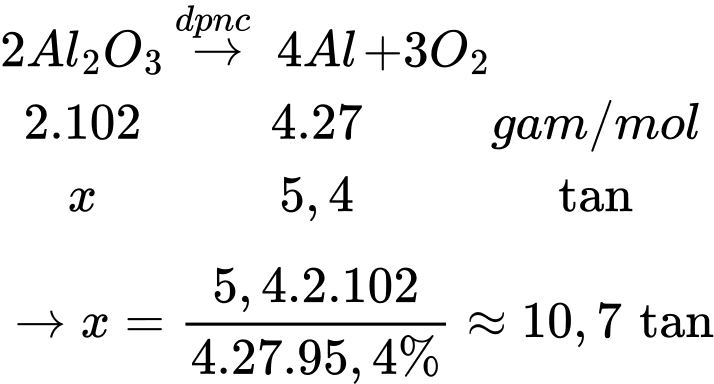
⇒ Điền đáp án: 10,7
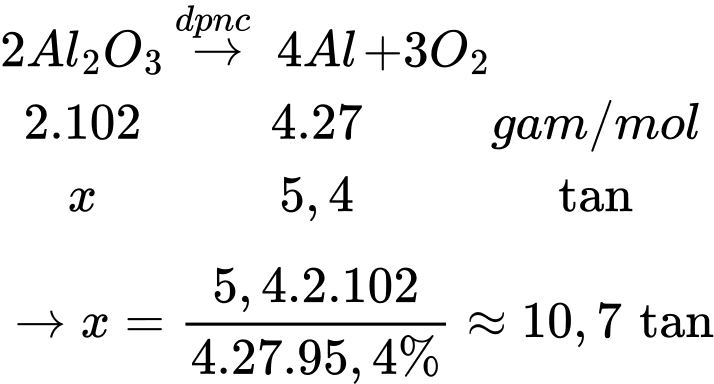
⇒ Điền đáp án: 10,7
Câu 61 [829968]: Xét quá trình sản xuất nhôm được thực hiện theo phương pháp điện phân Al2O3 nóng chảy với điện cực than chì. Trung bình để sản xuất được 1 tấn Al thì khối lượng điện cực than chì bị tiêu hao do phản ứng oxi hóa là bao nhiêu tấn (làm tròn đến hàng phần trăm)? Giả thiết thành phần khí bay ra ở cực dương gồm 50% CO và 50% CO2 về thể tích, không có khí O2 thoát ra.
Khí bay ra ở cực dương gồm 50% CO và 50% CO2 về thể tích, không có khí O2 thoát ra
→ Khí O2 sinh ra phản ứng hoàn toàn với C
Đặt nCO2 = nCO = x mol
Sơ đồ phản ứng:
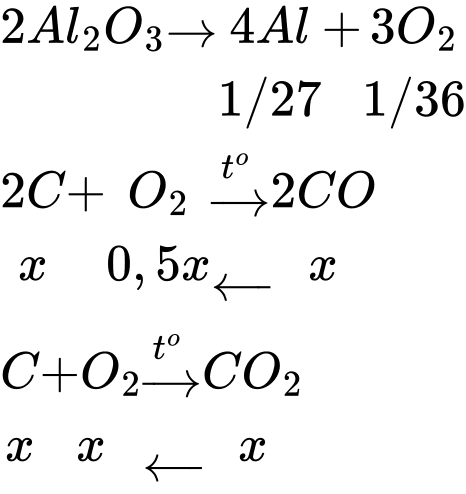
Bảo toàn nguyên tố O: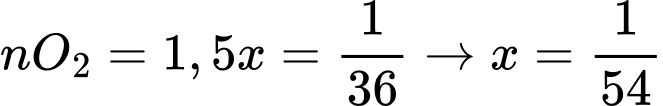
Khối lượng điện cực than chì tiêu hao là mC = 2x.12 = 2.1/54.12 = 0,44.
⟹ Điền đáp án 0,44
→ Khí O2 sinh ra phản ứng hoàn toàn với C
Đặt nCO2 = nCO = x mol
Sơ đồ phản ứng:
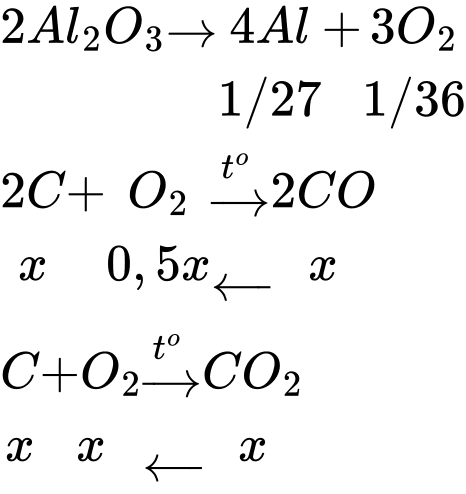
Bảo toàn nguyên tố O:
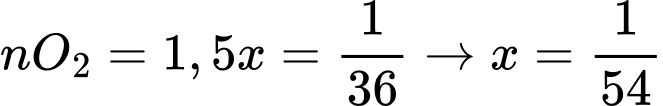
Khối lượng điện cực than chì tiêu hao là mC = 2x.12 = 2.1/54.12 = 0,44.
⟹ Điền đáp án 0,44
Câu 62 [829982]: Người ta mạ nickel lên mặt vật kim loại bằng phương pháp mạ điện, dung dịch điện phân chứa NiSO4, cực dương là Ni kim loại, cực âm là vật kim loại cần mạ. Nếu dòng điện có cường độ 1,5 A chạy qua dung dịch trong 2 giờ thì khối lượng nickel được mạ lên vật là bao nhiêu? (Cho biết khối lượng mol của Ni = 58,7 g/mol, hằng số Faraday F = 96500 C/mol, hiệu suất quá trình điện phân là 100%) (làm tròn kết quả đến hàng phần mười).
Cathode (-) : Ni2+ + 2e → Ni
Áp dụng định luật Faraday
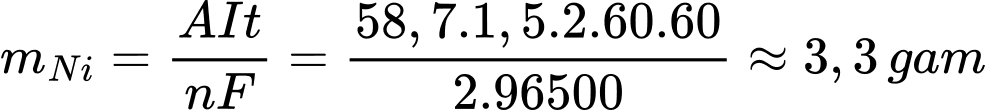
⇒ Điền đáp án: 3,3
Áp dụng định luật Faraday
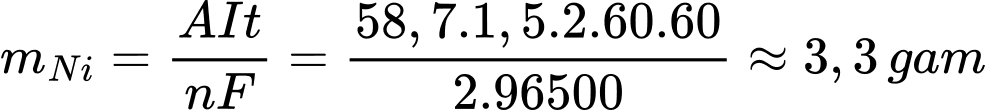
⇒ Điền đáp án: 3,3
Câu 63 [829985]: Hiện nay mạ điện được sử dụng rộng rãi trong thực tế, mạ điện là quá trình phủ một lớp kim loại lên bề mặt kim loại khác bằng phương pháp điện phân. Giả sử người ta cần mạ Ag lên một mặt của một chiếc đĩa kim loại hình tròn có bán kính 20 cm, độ dày lớp mạ là 0,01 mm. Nếu được cung cấp nguồn điện một chiều có cường độ dòng điện I = 2A thì thời gian cần dùng là t giờ. Biết rằng khối lượng riêng của Ag là 10,5 g/cm3; π = 3,14; hằng số Faraday (F = 96500 C/mol) ; hiệu suất điện phân là 100%. Giá trị của t là bao nhiêu (chỉ làm tròn ở phép tính cuối cùng và làm tròn kết quả đến hàng phần trăm)?
Đổi 0,01 mm = 0,001 cm
Thể tích lớp Ag là VAg = 0,001. r2 .π= 0,001.202.3,14 =1,256 cm3
Khối lượng Ag cần mạ là
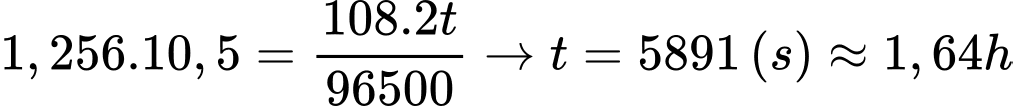
⇒ Điền đáp án: 1,64
Thể tích lớp Ag là VAg = 0,001. r2 .π= 0,001.202.3,14 =1,256 cm3
Khối lượng Ag cần mạ là
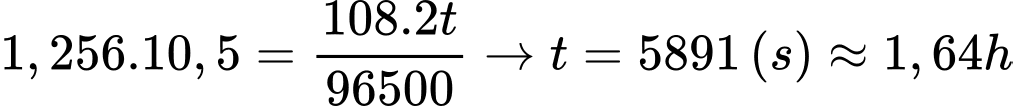
⇒ Điền đáp án: 1,64
Câu 64 [706184]: Việc tái chế nhôm phế liệu chỉ tiêu tốn 5% năng lượng sử dụng để sản xuất nhôm mới. Vì lý do này, hầu hết các loại nhôm thành phẩm được sản xuất từ việc tái chế nhôm phế liệu. Lon nước giải khát là ứng dụng được sử dụng nhiều nhất trong tái chế nhôm và hầu hết các sản phẩm được sản xuất từ phế liệu nhôm đều được sử dụng trở lại cũng là Lon nhôm. Theo EPA (Hiệp hội bảo vệ môi trường Mỹ) tái chế 10 lon bia sẽ tiết kiệm nguồn năng lượng đủ cho 1 chiếc máy tính xách tay hoạt động trong 52 giờ. Một nhà máy phế liệu dùng m tấn phế thải chứa 98% khối lượng Al2O3, còn lại tạp chất trơ không chứa Al để luyện nhôm. Cho biết hàm lượng 1 kg Al sinh ra tương ứng với 30 lon bia. Hiệu suất quá trình phản ứng là 93%. Với lượng phế liệu trên sẽ tiết kiệm năng lượng đủ để cho 1 chiếc máy tính hoạt động trong 78343,2 giờ. Giá trị của m bằng bao nhiêu (làm tròn kết quả đến hàng trăm)?
10 lon bia tiết kiệm năng lượng cho máy tính hoạt động trong 52 giờ
x lon bin tiết kiệm năng lượng cho máy tính hoạt động trong 78343,2 giờ
→ x = 10 × 78343,2 ÷ 52 = 15066 lon
Khối lượng Al là: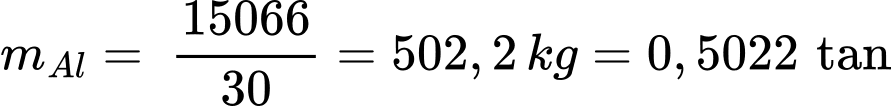
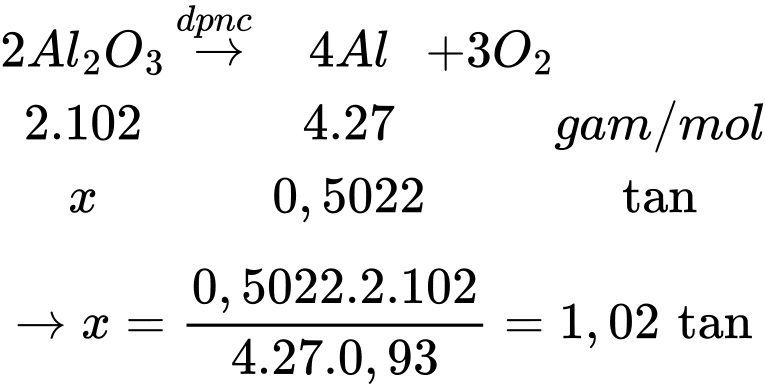
Khối lượng phế liệu là m = 1,02 ÷ 98% ≈ 1,04 tấn
⟹ Điền đáp án: 1,04
x lon bin tiết kiệm năng lượng cho máy tính hoạt động trong 78343,2 giờ
→ x = 10 × 78343,2 ÷ 52 = 15066 lon
Khối lượng Al là:
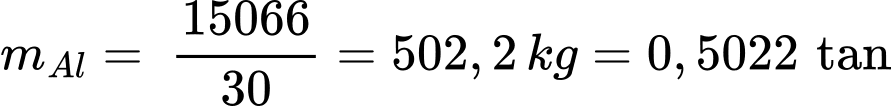
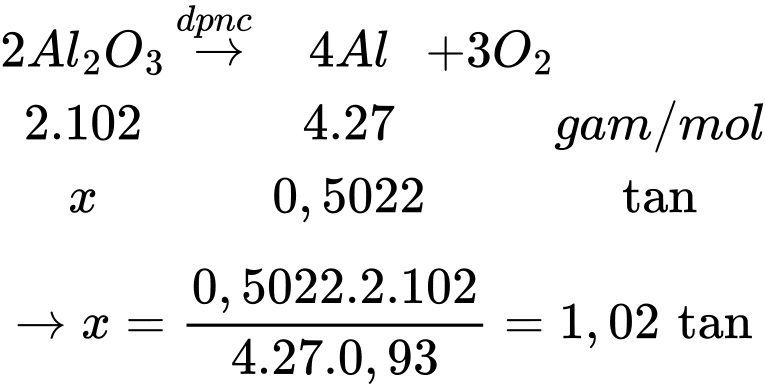
Khối lượng phế liệu là m = 1,02 ÷ 98% ≈ 1,04 tấn
⟹ Điền đáp án: 1,04
Dạng 4: BÀI TẬP ĐỌC HIỂU – đọc thông tin và trả lời các câu hỏi sau đó
TÁI CHẾ KIM LOẠI NHÔM
Lon nước giải khát bằng nhôm hầu như không được biết đến trước những năm 1960; tuy nhiên vào đầu những năm 1970, hơn 1,3 tỷ pound (0,59 triệu tấn) nhôm đã được sử dụng để sản xuất lon nước. Lý do khiến nhôm được ưa chuộng trong ngành đồ uống là vì nó không độc hại, không mùi, không vị và nhẹ. Hơn nữa, nó dẫn nhiệt nên chất lỏng bên trong lon có thể được làm lạnh nhanh chóng. 
Hình ảnh. Tái chế vỏ lon nhôm
Tuy nhiên, nhu cầu về nhôm tăng mạnh cũng có một nhược điểm nhất định. Hơn 3 tỷ pound lon nhôm và tấm kim loại nhôm bị vứt bỏ ở Hoa Kỳ hàng năm. Họ xả rác ở vùng nông thôn và làm tắc nghẽn các bãi chôn lấp. Giải pháp tốt nhất cho vấn đề ô nhiễm môi trường, cũng như tìm cách ngăn chặn sự cạn kiệt nhanh chóng của nguồn tài nguyên hữu hạn nhôm là tái chế. Lợi ích kinh tế của việc tái chế nhôm là gì? Chúng ta hãy so sánh năng lượng tiêu thụ trong quá trình sản xuất nhôm từ quặng bauxite được khai thác từ tự nhiên với năng lượng tiêu thụ khi nhôm được tái chế.
▪ Năng lượng cần thiết để sản xuất 1 mol Al từ quặng bauxite là 297 kJ.
▪ Năng lượng cần thiết để tái chế 1 mol Al là 26,1 kJ.
Để so sánh mức tiêu thụ năng lượng của hai phương pháp này, ta thực hiện phép tính:
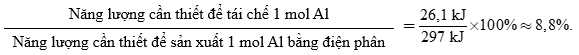
Câu 65 [560709]: Theo bài đọc, nhôm thường được dùng để sản xuất vỏ lon nhôm không phải vì lí do nào sau đây?
A, Nhôm không độc hại.
B, Nhôm thường nhẹ hơn các kim loại khác.
C, Nhôm dẫn nhiệt tốt.
D, Nhôm có giá thành rẻ hơn nhựa.
" Lý do nhôm được ưa chuộng trong nghề đồ uống là vì nó không độc hại, không mùi, không vị và nhẹ. Hơn nữa nó dẫn nhiệt tốt nên chất lỏng bên trong có thể làm lạnh nhanh chóng."
=> Không phải do Nhôm có giá rẻ hơn nhựa.
=> Chọn đáp án D Đáp án: D
=> Không phải do Nhôm có giá rẻ hơn nhựa.
=> Chọn đáp án D Đáp án: D
Câu 66 [560710]: Phản ứng tổng quát của quá trình điều chế nhôm từ quặng bauxite như sau:
2Al2O3 (trong cryolit nóng chảy) + 3C(s)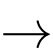 4Al(l) + 3X(g)
4Al(l) + 3X(g)
Khí X được sinh ra trong quá trình trên gây ra hiệu ứng nhà kính. Cho biết X là chất khí nào sau đây?
2Al2O3 (trong cryolit nóng chảy) + 3C(s)
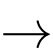 4Al(l) + 3X(g)
4Al(l) + 3X(g)Khí X được sinh ra trong quá trình trên gây ra hiệu ứng nhà kính. Cho biết X là chất khí nào sau đây?
A, CO.
B, CO2.
C, H2.
D, N2.
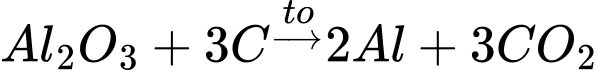
Khí X là CO2
=> Chọn đáp án B Đáp án: B
Câu 67 [560711]: Để tái chế 1 tấn nhôm cần tiêu tốn bao nhiêu năng lượng?
A, 9,67×105 kJ.
B, 5,79×105 kJ.
C, 2,90×105 kJ.
D, 8,45×105 kJ.
nAl= 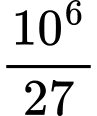 = 37037,04 mol
= 37037,04 mol
=> Năng lượng cần để tái chế 1 tấn Al là 37037,04 . 26,1 = 9,67 . 105
=> Đáp án A Đáp án: A
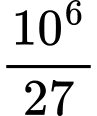 = 37037,04 mol
= 37037,04 mol=> Năng lượng cần để tái chế 1 tấn Al là 37037,04 . 26,1 = 9,67 . 105
=> Đáp án A Đáp án: A
TÁCH VÀ TINH CHẾ KIM LOẠI BẠC
Người ta có thể tách kim loại Ag bằng phương pháp cyanide: 👣 Bước 1: Nghiền nhỏ quặng silver sulfide (Ag2S).
👣 Bước 2: Hòa tan quặng bằng dung dịch sodium cyanide (NaCN), rồi lọc để thu được dung dịch chứa phức chất tan của bạc Na[Ag(CN)2]:
Ag2S(s) + 4NaCN(aq) → 2Na[Ag(CN)2](aq) + Na2S(aq) (I)
Do thế điện cực của cặp oxi hóa – khử Ag+/Ag tương đối lớn nên Ag có thể tồn tại ở dạng đơn chất trong quặng. Tuy nhiên nó sẽ chứa nhiều tạp chất, để tinh chế thì có thể sục khí oxygen vào trong hỗn hợp của quặng chứa bạc với dung dịch NaCN:
4Ag(s) + O2(g) + 8NaCN(aq) + 2H2O(l) → 4Na[Ag(CN)2](aq) + 4NaOH(aq) (II)
👣 Bước 3: Sau đó, ion Ag+ trong phức được khử bằng kim loại kẽm:
2Na[Ag(CN)2](aq) + Zn(s) → Na2[Zn(CN)4](aq) + 2Ag(s) (III)
👣 Bước 4: Cuối cùng người ta dùng dung dịch acid không có tính oxi hoá (HCl, H2SO4 loãng) để loại bỏ kẽm dư, bạc không phản ứng với acid trên nên chất rắn thu được sẽ là kim loại bạc tinh khiết.
Zn(s) + 2HCl(aq) → ZnCl2(aq) + H2(g)
Câu 68 [560712]: Theo phương trình (I), nguyên tử Ag trong silver sulfide sau phản ứng có số oxi hóa
A, tăng.
B, giảm.
C, không đổi.
D, không xác định.
Trong hợp chất Na[Ag(CN)2], số oxi hóa của bạc (Ag) là +1.
Trong hợp chất Ag2S, số oxi hóa của bạc (Ag) là +1.
=> Số oxi hóa của Ag không đổi.
=> Chọn đáp án C Đáp án: C
Trong hợp chất Ag2S, số oxi hóa của bạc (Ag) là +1.
=> Số oxi hóa của Ag không đổi.
=> Chọn đáp án C Đáp án: C
Câu 69 [560713]: Theo phương trình (II), khí oxygen được sục vào dung dịch có tác dụng
A, oxi hóa kim loại bạc.
B, loại bỏ tạp chất không tan.
C, khử NaCN.
D, tạo môi trường base.
Do thế điện cực của cặp oxi hóa - khử Ag+/Ag tương đối lớn nên Ag có thể tồn tại ở dạng đơn chất trong quặng. Tuy nhiên nó sẽ chứa nhiều tạp chất, để tinh chế thì có thể sục khí oxygen vào trong hỗn hợp của quặng chứa bạc với dung dịch NaCN:
4Ag(s) + O2(g) + 8NaCN(aq) + 2H2O(I)
⟶4Na[Ag(CN)2](aq) + 4NaOH(aq) (II).
=> Chọn đáp án B Đáp án: B
4Ag(s) + O2(g) + 8NaCN(aq) + 2H2O(I)
⟶4Na[Ag(CN)2](aq) + 4NaOH(aq) (II).
=> Chọn đáp án B Đáp án: B
Câu 70 [560714]: Theo phương trình (III), giả sử phản ứng xảy ra hoàn toàn thì từ 13 gam kẽm sẽ tạo ra tối đa bao nhiêu gam bạc?
A, 21,6 gam.
B, 86,4 gam.
C, 43,2 gam.
D, 94,8 gam.
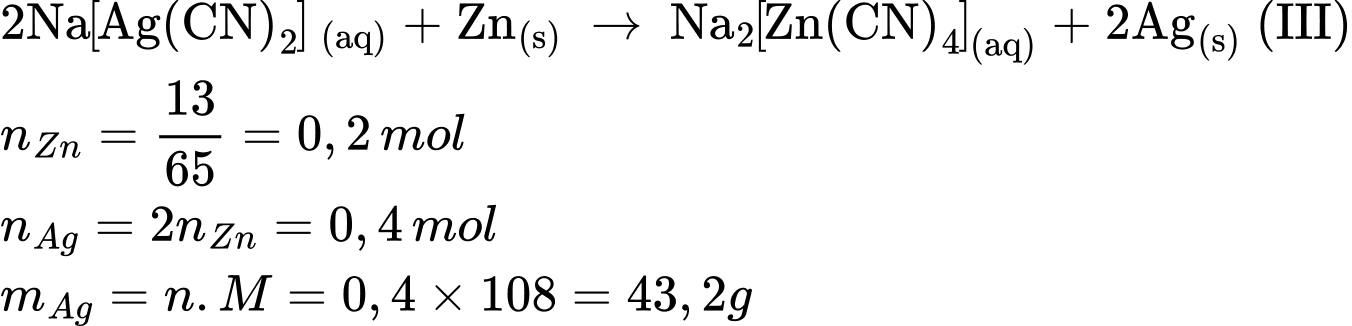
=> Chọn đáp án C Đáp án: C
Dạng 5: CÂU HỎI TỰ LUẬN
Câu 71 [1016802]: Trên thế giới, zinc (kẽm) được sản xuất từ quặng zinc blende. Thành phần chính của quặng zinc blende là ZnS.
 Tách kim loại zinc từ quặng zinc blende bằng phương pháp nhiệt luyện thường được tiến hành theo hai bước chính:
Tách kim loại zinc từ quặng zinc blende bằng phương pháp nhiệt luyện thường được tiến hành theo hai bước chính:
ZnS(s)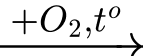 ZnO(s)
ZnO(s) 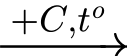 Zn(s).
Zn(s).
Viết phương trình hóa học xảy ra ở các bước.

ZnS(s)
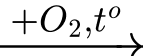 ZnO(s)
ZnO(s) 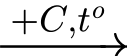 Zn(s).
Zn(s).Viết phương trình hóa học xảy ra ở các bước.
Tách kẽm từ quặng zinc blende được thực hiện theo quy trình:
+) Đốt quặng zinc blende: 2ZnS + 3O2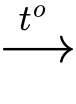 2ZnO + 2SO2. (1)
2ZnO + 2SO2. (1)
+) Phản ứng zinc oxide ở nhiệt độ cao với than cốc: ZnO + C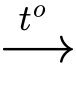 Zn + CO. (2)
Zn + CO. (2)
+) Đốt quặng zinc blende: 2ZnS + 3O2
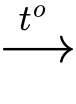 2ZnO + 2SO2. (1)
2ZnO + 2SO2. (1)
+) Phản ứng zinc oxide ở nhiệt độ cao với than cốc: ZnO + C
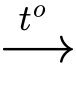 Zn + CO. (2)
Zn + CO. (2)
Câu 72 [1016803]: Quy trình sản xuất đồng (Cu) từ quặng chứa Cu2S được thực hiện như sau:
▪ Giai đoạn 1: Đốt Cu2S bằng khí oxygen theo phản ứng:
2Cu2S + 3O2 → 2Cu2O + 2SO2.
▪ Giai đoạn 2: Copper(I) oxide sẽ phản ứng với phần còn lại của Cu2S theo phản ứng:
2Cu2O + Cu2S → 6Cu + 2SO2.
Quặng đồng chứa khoảng 40% Cu2S theo khối lượng và hiệu suất của quá trình đạt 90%.
a) Ở giai đoạn 1, nếu sử dụng lượng khí O2 dư thì phản ứng có xảy ra được không? Giải thích.
b) Tính khối lượng quặng đồng (theo tấn) cần lấy để điều chế được 1 tấn Cu.
▪ Giai đoạn 1: Đốt Cu2S bằng khí oxygen theo phản ứng:
2Cu2S + 3O2 → 2Cu2O + 2SO2.
▪ Giai đoạn 2: Copper(I) oxide sẽ phản ứng với phần còn lại của Cu2S theo phản ứng:
2Cu2O + Cu2S → 6Cu + 2SO2.
Quặng đồng chứa khoảng 40% Cu2S theo khối lượng và hiệu suất của quá trình đạt 90%.
a) Ở giai đoạn 1, nếu sử dụng lượng khí O2 dư thì phản ứng có xảy ra được không? Giải thích.
b) Tính khối lượng quặng đồng (theo tấn) cần lấy để điều chế được 1 tấn Cu.
a) Phản ứng ở giai đoạn 1 khi dùng dư khí O2
Phản ứng vẫn xảy ra.
Giải thích: Oxy (O2) là một chất tham gia trong phản ứng đốt cháy Cu2S. Theo nguyên lý chuyển dịch cân bằng Le Chatelier, việc tăng nồng độ của một chất phản ứng (sử dụng dư O2) sẽ thúc đẩy phản ứng diễn ra theo chiều thuận, tức là chiều tạo ra sản phẩm.
Tuy nhiên, việc dùng lượng O2 dư thừa có thể gây ra phản ứng phụ không mong muốn, trong đó
Cu2S hoặc sản phẩm Cu2O bị oxy hóa sâu hơn để tạo thành copper(II) oxide (CuO):
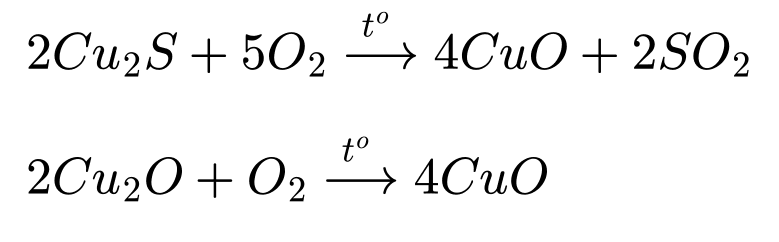
Hợp chất CuO này không tham gia vào phản ứng ở giai đoạn 2 để tạo ra đồng kim loại. Điều này làm lãng phí nguyên liệu và giảm hiệu suất của toàn bộ quá trình sản xuất đồng. Vì vậy, trong thực tế, lượng không khí (chứa oxygen) cần được kiểm soát chặt chẽ.
b) Đổi 1 tấn = 1000000 gam
Số mol của CuO là nCu = 1000000:64 = 15625 mol
Bảo toàn nguyên tố Cu, nCu2S = (nCu ):2 = 15625:2 = 7812,5 mol
Khối lượng của quặng là:
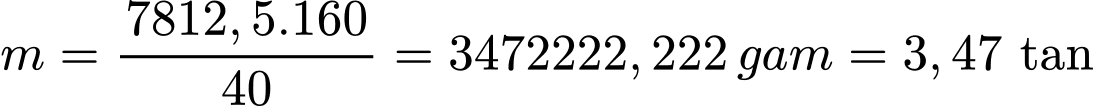
Phản ứng vẫn xảy ra.
Giải thích: Oxy (O2) là một chất tham gia trong phản ứng đốt cháy Cu2S. Theo nguyên lý chuyển dịch cân bằng Le Chatelier, việc tăng nồng độ của một chất phản ứng (sử dụng dư O2) sẽ thúc đẩy phản ứng diễn ra theo chiều thuận, tức là chiều tạo ra sản phẩm.
Tuy nhiên, việc dùng lượng O2 dư thừa có thể gây ra phản ứng phụ không mong muốn, trong đó
Cu2S hoặc sản phẩm Cu2O bị oxy hóa sâu hơn để tạo thành copper(II) oxide (CuO):
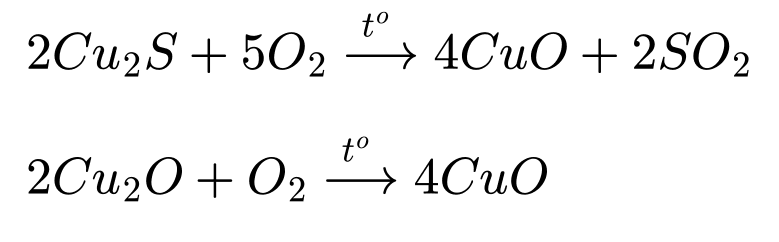
Hợp chất CuO này không tham gia vào phản ứng ở giai đoạn 2 để tạo ra đồng kim loại. Điều này làm lãng phí nguyên liệu và giảm hiệu suất của toàn bộ quá trình sản xuất đồng. Vì vậy, trong thực tế, lượng không khí (chứa oxygen) cần được kiểm soát chặt chẽ.
b) Đổi 1 tấn = 1000000 gam
Số mol của CuO là nCu = 1000000:64 = 15625 mol
Bảo toàn nguyên tố Cu, nCu2S = (nCu ):2 = 15625:2 = 7812,5 mol
Khối lượng của quặng là: