Dạng 1: TRẮC NGHIỆM KHÁCH QUAN: mỗi câu hỏi chỉ có một đáp án đúng.
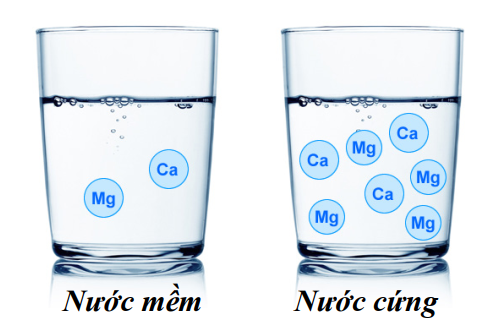
Câu 1 [233830]: Nước tự nhiên chứa nhiều những cation nào sau đây được gọi là nước cứng?
A, Na+, Al3+.
B, Na+, K+.
C, Al3+, K+.
D, Ca2+, Mg2+.
HD: Nước cứng là nước có chứa nhiều ion Ca2+ và Mg2+.
⇝ Chọn đáp án D. Đáp án: D

⇝ Chọn đáp án D. Đáp án: D
Câu 2 [982224]: Cặp chất nào sau đây gây nên tính cứng tạm thời của nước?
A, MgSO4, CaCl2.
B, Mg(HCO3)2, Ca(HCO3)2.
C, NaCl, KCl.
D, Na2SO4, K2SO4.
HD: Bài học phân loại nước cứng:
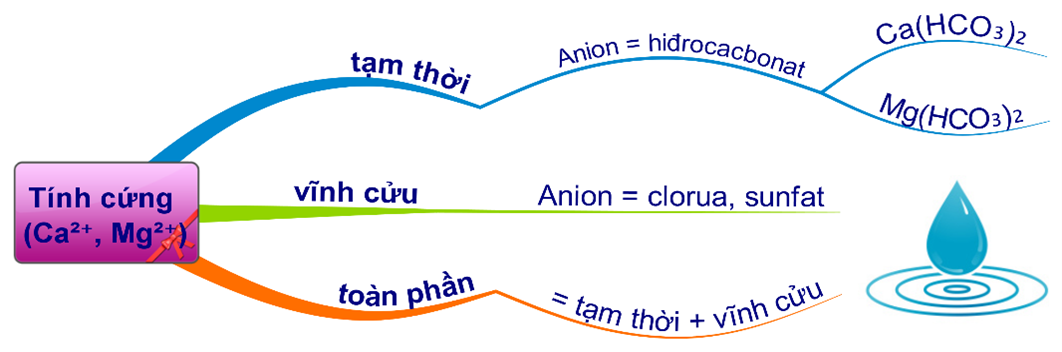
Mg(HCO3)2, Ca(HCO3)2 gây nên tính cứng tạm thời của nước.
⇝ Chọn đáp án B Đáp án: B

Mg(HCO3)2, Ca(HCO3)2 gây nên tính cứng tạm thời của nước.
⇝ Chọn đáp án B Đáp án: B
Câu 3 [983247]: Cặp chất nào sau đây gây nên tính cũng vĩnh cửu của nước?
A, NaNO3, KNO3.
B, NaNO3, KHCO3.
C, MgCl2, CaSO4.
D, NaHCO3, KNO3.
HD: Phân loại nước cứng:

⇝ Cặp chất gây nên tính cũng vĩnh cửu của nước là: MgCl2 và CaSO4
⟹ Chọn đáp án C Đáp án: C

⇝ Cặp chất gây nên tính cũng vĩnh cửu của nước là: MgCl2 và CaSO4
⟹ Chọn đáp án C Đáp án: C
Câu 4 [705857]: Đặc điểm nào sau đây là điểm chung của nước có tính cứng vĩnh cửu và nước có tính cứng toàn phần?
A, Đều có thể làm mềm bằng Na3PO4.
B, Đều không chứa anion HCO3–.
C, Đều bị mất một phần tính cứng khi đun sôi nước.
D, Thành phần anion giống nhau.
Nước cứng toàn phần: Nước cứng thành phần hiểu đơn giản là loại nước cứng bao gồm cả tính cứng tạm thời và tính cứng vĩnh cửu. Do đó thành phần của nó sẽ là các muối Ca(HCO3)2, Mg(HCO3)2, MgCl2, CaCl2, MgSO4, CaSO4.
Nước cứng vĩnh cửu: Nước cứng vĩnh cửu là nước cứng chứa nồng độ cao của các anion, như anion sunfat (SO42-), clorua (Cl-) với thành phần là các muối như MgCl2, CaCl2, MgSO4, CaSO4.
Nguyên tắc làm mềm nước cứng là làm giảm nồng độ của các cation Ca2+ và Mg2+ trong nước cứng. Dùng Na2CO3 hoặc Na3PO4 để làm mất tính cứng tạm thời và tính cứng vĩnh cửu của nước.
Phân tích các đáp án:
✔️A. Cả nước có tính cứng vĩnh cửu và nước có tính cứng toàn phần đều chứa các ion Ca2+,Mg2+. Muối Na3PO4 có thể tạo kết tủa với Ca2+,Mg2+ giúp làm mềm nước.
❌B.Nước có tính cứng vĩnh cửu không chứa HCO3−, nhưng nước có tính cứng toàn phần có thể chứa cả ion này.
❌C.Nước có tính cứng vĩnh cửu chứa ion SO42−,Cl−, không bị loại bỏ khi đun sôi.Chỉ nước có tính cứng tạm thời chứa HCO3− mới mất tính cứng khi đun sôi.
❌D.Nước có tính cứng vĩnh cửu chứa ion SO42−,Cl−, còn nước có tính cứng toàn phần có thể chứa cả HCO3−.Thành phần anion không hoàn toàn giống nhau.
⟹ Chọn đáp án A Đáp án: A
Nước cứng vĩnh cửu: Nước cứng vĩnh cửu là nước cứng chứa nồng độ cao của các anion, như anion sunfat (SO42-), clorua (Cl-) với thành phần là các muối như MgCl2, CaCl2, MgSO4, CaSO4.
Nguyên tắc làm mềm nước cứng là làm giảm nồng độ của các cation Ca2+ và Mg2+ trong nước cứng. Dùng Na2CO3 hoặc Na3PO4 để làm mất tính cứng tạm thời và tính cứng vĩnh cửu của nước.
Phân tích các đáp án:
✔️A. Cả nước có tính cứng vĩnh cửu và nước có tính cứng toàn phần đều chứa các ion Ca2+,Mg2+. Muối Na3PO4 có thể tạo kết tủa với Ca2+,Mg2+ giúp làm mềm nước.
❌B.Nước có tính cứng vĩnh cửu không chứa HCO3−, nhưng nước có tính cứng toàn phần có thể chứa cả ion này.
❌C.Nước có tính cứng vĩnh cửu chứa ion SO42−,Cl−, không bị loại bỏ khi đun sôi.Chỉ nước có tính cứng tạm thời chứa HCO3− mới mất tính cứng khi đun sôi.
❌D.Nước có tính cứng vĩnh cửu chứa ion SO42−,Cl−, còn nước có tính cứng toàn phần có thể chứa cả HCO3−.Thành phần anion không hoàn toàn giống nhau.
⟹ Chọn đáp án A Đáp án: A
Câu 5 [679747]: Đun nước cứng lâu ngày trong ấm nước xuất hiện một lớp cặn. Thành phần chính của lớp cặn đó là
A, CaCl2.
B, CaCO3.
C, Na2CO3.
D, CaO.
HD: Thành phần chính của lớp cặn đó là CaCO3. Nguyên nhân:
Ca(HCO3)2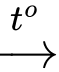 CaCO3↓ + CO2↑ + H2O.
CaCO3↓ + CO2↑ + H2O.
☆ Để làm sạch, có thể sử dụng giấm ăn:
2CH3COOH + CaCO3 → (CH3COO)2Ca + 2H2O.
⇒ Chọn đáp án B Đáp án: B
Ca(HCO3)2
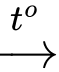 CaCO3↓ + CO2↑ + H2O.
CaCO3↓ + CO2↑ + H2O.☆ Để làm sạch, có thể sử dụng giấm ăn:
2CH3COOH + CaCO3 → (CH3COO)2Ca + 2H2O.
⇒ Chọn đáp án B Đáp án: B
Câu 6 [679600]: Dung dịch nào sau đây được dùng để xử lí lớp cặn CaCO3 bám vào ấm đun nước?
A, Muối ăn.
B, Cồn.
C, Nước vôi trong.
D, Giấm ăn.
HD: Giấm ăn chứa acetic acid: CH3COOH có khả năng hoà tan CaCO3 (thêm nữa là ấm nước dùng để sinh hoạt ăn uống nên cần hoá chất an toàn với sức khoẻ chúng ta, dùng giấm ăn hoặc chanh,... là hợp lý nhất).
Phản ứng xảy ra: 2CH3COOH + CaCO3 → (CH3COO)2Ca + CO2↑ + H2O.
⇒ Chọn đáp án D Đáp án: D
Phản ứng xảy ra: 2CH3COOH + CaCO3 → (CH3COO)2Ca + CO2↑ + H2O.
⇒ Chọn đáp án D Đáp án: D
Câu 7 [60164]: Đặc điểm nào dưới đây không phải của nước cứng?
A, Làm đục nước, gây ngộ độc thực phẩm.
B, Làm mất tính tẩy rửa của xà phòng.
C, Đun nước cứng trong nồi hơi sẽ tạo thành một lớp cặn ở mặt nồi hơi.
D, Nấu đồ ăn bằng nước cứng sẽ lâu chín và giảm mùi vị thực phẩm.
HD:
Nước cứng không gây ngộ độc thực phẩm ⇒ A sai.
Đáp án: A
Nước cứng không gây ngộ độc thực phẩm ⇒ A sai.
Đáp án: A
Câu 8 [60169]: Nước cứng không gây ra tác hại nào dưới đây?
A, Làm cho thực phẩm lâu chín và giảm mùi vị.
B, Làm tắc các đường ống dẫn nước nóng trong sản xuất và trong đời sống.
C, Làm giảm khả năng tẩy rửa của xà phòng.
D, Làm cho nước có mùi khó chịu.
HD:
Nước cứng không gây ra mùi khó chịu.
Đáp án: D
Nước cứng không gây ra mùi khó chịu.
Đáp án: D
Câu 9 [60172]: Sử dụng nước cứng không gây ra tác hại nào sau đây?
A, Đóng cặn nồi hơi gây nguy hiểm.
B, Tốn nhiên liệu, làm giảm hương vị thức ăn.
C, Hao tổn chất giặt rửa tổng hợp.
D, Tắc ống dẫn nước nóng trong nồi hơi.
Nước cứng chỉ gây ra kết tủa với xà phòng, còn với chất giặt rửa tổng hợp thì vẫn bình thường nên không gây hao tổn
⟹ Chọn đáp án C Đáp án: C
⟹ Chọn đáp án C Đáp án: C
Câu 10 [233868]: Chất nào sau đây có khả năng làm mềm được nước cứng vĩnh cửu?
A, NaCl.
B, CaCl2.
C, Na2SO4.
D, Na2CO3.
Dung dịch Na2CO3, Na3PO4 làm mềm nước cứng vĩnh cửu.
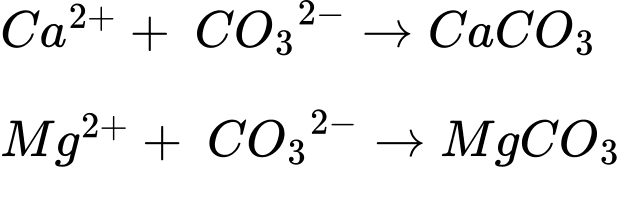
⇒ Chọn đáp án D Đáp án: D
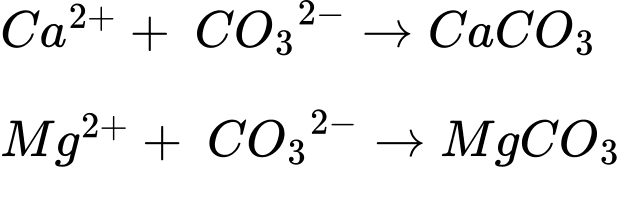
⇒ Chọn đáp án D Đáp án: D
Câu 11 [679845]: Chất nào sau đây được dùng để làm mềm nước có tính cứng tạm thời?
A, CaCO3.
B, MgCl2.
C, NaOH.
D, Fe(OH)2.
Nước cứng tạm thời chứa Ca(HCO3)2 và Mg(HCO3)2, khi sử dụng NaOH:
• 2NaOH + Ca(HCO3)2 → CaCO3↓ + Na2CO3 + 2H2O.
• 2NaOH + Mg(HCO3)2 → MgCO3↓ + Na2CO3 + 2H2O.
Kết tủa các cation Mg2+ và Ca2+ ⇝ làm mềm nước.
⇒ Chọn đáp án C Đáp án: C
• 2NaOH + Ca(HCO3)2 → CaCO3↓ + Na2CO3 + 2H2O.
• 2NaOH + Mg(HCO3)2 → MgCO3↓ + Na2CO3 + 2H2O.
Kết tủa các cation Mg2+ và Ca2+ ⇝ làm mềm nước.
⇒ Chọn đáp án C Đáp án: C
Câu 12 [239359]: Dãy gồm các chất đều có thể làm mất tính cứng tạm thời của nước là:
A, HCl, NaOH, Na2CO3.
B, NaOH, Na3PO4, Na2CO3.
C, KCl, Ca(OH)2, Na2CO3.
D, HCl, Ca(OH)2, Na2CO3.
Ta dùng dãy các chất NaOH, Na3PO4; Na2CO3 có thể làm mất tính cứng tạm thời của nước
Ca(HCO3)2 + 2NaOH → CaCO3↓ + Na2CO3 + H2O
3Mg(HCO2)2 + 2Na3PO4 → Mg3(PO4)2↓ + 6NaHCO3
Ca(HCO3)2 + Na2CO3 → CaCO3↓ + 2NaHCO3
⟹ Chọn đáp án B
Đáp án: B
Ca(HCO3)2 + 2NaOH → CaCO3↓ + Na2CO3 + H2O
3Mg(HCO2)2 + 2Na3PO4 → Mg3(PO4)2↓ + 6NaHCO3
Ca(HCO3)2 + Na2CO3 → CaCO3↓ + 2NaHCO3
⟹ Chọn đáp án B
Đáp án: B
Câu 13 [39681]: Cho mẫu nước cứng chứa các ion: Ca2+, Mg2+ và HCO3–. Hoá chất được dùng để làm mềm mẫu nước cứng trên là
A, HCl.
B, Na2CO3.
C, H2SO4.
D, NaCl.
Mẫu nước cứng chứa các ion: Ca2+, Mg2+ và HCO3-. Hóa chất được dùng để làm mềm nước cứng Na2CO3.
Phương trình phản ứng:
Ca(HCO3)2 + Na2CO3 ⟶ CaCO3 ↓ + 2NaHCO3.
Mg(HCO3)2 + Na2CO3 ⟶ MgCO3 ↓ + 2NaHCO3.
⟹ Chọn đáp án B
Đáp án: B
Phương trình phản ứng:
Ca(HCO3)2 + Na2CO3 ⟶ CaCO3 ↓ + 2NaHCO3.
Mg(HCO3)2 + Na2CO3 ⟶ MgCO3 ↓ + 2NaHCO3.
⟹ Chọn đáp án B
Câu 14 [60186]: Để làm mềm một loại nước cứng có thành phần : Ca2+, Mg2+, Cl-, SO42- nên dùng
A, dung dịch soda.
B, dung dịch nước vôi trong.
C, nước Javel.
D, dung dịch xút ăn da.
Nước cứng là nước chứa các ion Ca2+, Mg2+ (thường kết hợp với các anion như Cl−, SO42−).
Muốn làm mềm nước cứng thường cần loại bỏ hoặc giảm nồng độ Ca2+ và Mg2++ bằng cách kết tủa chúng dưới dạng muối không tan (như CaCO3, Mg(OH)2)
Phân tích các chất:
✔️ A. Dung dịch soda (Na2CO3)
Soda phản ứng với Ca2+ và Mg2+, tạo kết tủa không tan CaCO3 và MgCO3:
Ca2+ + CO32− → CaCO3↓
Mg2+ + CO32− → MgCO3↓
❌ B. Dung dịch nước vôi trong (Ca(OH)2)
Nước vôi trong có thể làm mềm nước cứng tạm thời (nước cứng chứa HCO3−) bằng cách tạo kết tủa CaCO3. Tuy nhiên, với nước cứng chứa Cl− và SO42−, nó không hiệu quả.
❌ C. Nước Javel (NaClO)
Nước Javel là chất oxi hóa, không làm mềm nước cứng vì nó không phản ứng với Ca2+ hoặc Mg2+.
❌ D. Dung dịch xút ăn da (NaOH)
NaOH có thể phản ứng với Mg2+ tạo Mg(OH)2 kết tủa, nhưng không hiệu quả với Ca2+. Hơn nữa, việc sử dụng NaOH có thể làm tăng pH quá cao, gây bất lợi.
⇒ Chọn đáp án A Đáp án: A
Muốn làm mềm nước cứng thường cần loại bỏ hoặc giảm nồng độ Ca2+ và Mg2++ bằng cách kết tủa chúng dưới dạng muối không tan (như CaCO3, Mg(OH)2)
Phân tích các chất:
✔️ A. Dung dịch soda (Na2CO3)
Soda phản ứng với Ca2+ và Mg2+, tạo kết tủa không tan CaCO3 và MgCO3:
Ca2+ + CO32− → CaCO3↓
Mg2+ + CO32− → MgCO3↓
❌ B. Dung dịch nước vôi trong (Ca(OH)2)
Nước vôi trong có thể làm mềm nước cứng tạm thời (nước cứng chứa HCO3−) bằng cách tạo kết tủa CaCO3. Tuy nhiên, với nước cứng chứa Cl− và SO42−, nó không hiệu quả.
❌ C. Nước Javel (NaClO)
Nước Javel là chất oxi hóa, không làm mềm nước cứng vì nó không phản ứng với Ca2+ hoặc Mg2+.
❌ D. Dung dịch xút ăn da (NaOH)
NaOH có thể phản ứng với Mg2+ tạo Mg(OH)2 kết tủa, nhưng không hiệu quả với Ca2+. Hơn nữa, việc sử dụng NaOH có thể làm tăng pH quá cao, gây bất lợi.
⇒ Chọn đáp án A Đáp án: A
Câu 15 [60197]: Phát biểu nào sau đây sai?
A, Nước chứa nhiều ion HCO3– là nước cứng tạm thời.
B, Người ta phân loại nước cứng dựa vào thành phần anion.
C, Dung dịch Na2CO3 có thể làm mềm mọi nước cứng.
D, Người ta có thể sử dụng phương pháo trao đổi ion để làm mềm nước cứng.
HD:
Nước chứa nhiều ion HCO3– là nước cứng tạm thời → SAI.
Nước cứng chứa nhiều ion HCO3– là nước cứng tạm thời → ĐÚNG.
Trước khi xét nước có tính cứng tạm thời/vĩnh cửu/toàn phần thì nước đó phải là nước cứng (chứa Ca2+, Mg2+)!
Đáp án: A
Nước chứa nhiều ion HCO3– là nước cứng tạm thời → SAI.
Nước cứng chứa nhiều ion HCO3– là nước cứng tạm thời → ĐÚNG.
Trước khi xét nước có tính cứng tạm thời/vĩnh cửu/toàn phần thì nước đó phải là nước cứng (chứa Ca2+, Mg2+)!
Đáp án: A
Câu 16 [60207]: Nhận định nào sau đây là đúng?
A, Nước cứng là tác nhân gây ô nhiễm nguồn nước hiện nay.
B, Nước tự nhiên thường có cả tính cứng tạm thời và tính cứng vĩnh cửu.
C, Làm mềm tính cứng của nước cứng vĩnh cửu bằng cách đun nóng.
D, Nước cứng là nước chứa nhiều ion HCO3- và SO42-.
HD:
Nước cứng không phải tác nhân gây ô nhiễm nguồn nước hiện nay. A sai.
Nước tự nhiên thường chứa nhiều ion nên có cả tính cứng tạm thời và vĩnh cửu → cứng toàn phần. B đúng.
Đun nóng chỉ làm mềm được nước cứng tạm thời và làm mềm được 1 phần nước cứng toàn phần. C sai.
Nước cứng là nước chứa nhiều ion Ca2+ và Mg2+, tùy vào các ion âm trong nước cứng mà người ta chia ra các loại nước cứng khác nhau. D sai.
Đáp án: B
Nước cứng không phải tác nhân gây ô nhiễm nguồn nước hiện nay. A sai.
Nước tự nhiên thường chứa nhiều ion nên có cả tính cứng tạm thời và vĩnh cửu → cứng toàn phần. B đúng.
Đun nóng chỉ làm mềm được nước cứng tạm thời và làm mềm được 1 phần nước cứng toàn phần. C sai.
Nước cứng là nước chứa nhiều ion Ca2+ và Mg2+, tùy vào các ion âm trong nước cứng mà người ta chia ra các loại nước cứng khác nhau. D sai.
Đáp án: B
Câu 17 [60221]: Phát biểu nào sau đây đúng?
A, Khi đun nóng nước cứng có tính cứng toàn phần sẽ thu được nước mềm.
B, Có thể làm mất tính cứng vĩnh cửu bằng dung dịch Ca(OH)2.
C, Nước cứng là nguyên nhân chính gây ra các vụ ngộ độc nguồn nước.
D, Tính cứng tạm thời gây nên bởi các muối Ca(HCO3)2 và Mg(HCO3)2.
HD:
Nước cứng tạm thời là nước có chwuas các ion Ca2+, Mg2+, HCO3–
⇒ Tính cứng tạm thời gây nên bởi các muối Ca(HCO3)2 và Mg(HCO3)2.
Đáp án: D
Nước cứng tạm thời là nước có chwuas các ion Ca2+, Mg2+, HCO3–
⇒ Tính cứng tạm thời gây nên bởi các muối Ca(HCO3)2 và Mg(HCO3)2.
Đáp án: D
Câu 18 [706082]: Nước cứng là kết quả tự nhiên tạo ra từ các khoáng chất (calcium và magnesium) tích tụ trong chu trình của nước, chứa một hàm Ca2+ và Mg2+ cao vượt mức tiêu chuẩn. Sử dụng nước cứng lâu ngày sẽ dễ dẫn đến sỏi thận, sỏi tiết niệu hoặc làm tắc thành trọng của động mạch, tĩnh mạch do đóng cặn vôi gây nguy hiểm đến sức khỏe. Tóc khô xơ, mất độ mềm mại.
(a) Nước có chứa nhiều ion HCO3– được gọi là nước có tính cứng tạm thời.
(b) Có thể làm mềm nước có tính cứng tạm thời bằng cách đun sôi nước.
(c) Có thể loại bỏ một phần tính cứng của nước có tính cứng vĩnh cửu bằng cách dùng một lượng vừa đủ Ca(OH)2.
(d) Không thể dùng cách đun sôi để loại bỏ hoàn toàn tính cứng của nước có chứa nhiều các ion sau: Mg2+, Ca2+, Cl–, HCO3–, SO42–.
(e) Nước cứng có thể là nguyên nhân gây nổ nồi hơi.Số phát biểu đúng là
(a) Nước có chứa nhiều ion HCO3– được gọi là nước có tính cứng tạm thời.
(b) Có thể làm mềm nước có tính cứng tạm thời bằng cách đun sôi nước.
(c) Có thể loại bỏ một phần tính cứng của nước có tính cứng vĩnh cửu bằng cách dùng một lượng vừa đủ Ca(OH)2.
(d) Không thể dùng cách đun sôi để loại bỏ hoàn toàn tính cứng của nước có chứa nhiều các ion sau: Mg2+, Ca2+, Cl–, HCO3–, SO42–.
(e) Nước cứng có thể là nguyên nhân gây nổ nồi hơi.Số phát biểu đúng là
A, 1.
B, 2.
C, 3.
D, 4.
Phân tích các phát biểu :
❌(a) – Sai. Nước có chứa nhiều ion Mg2+, Ca2+, HCO3- được gọi là -nước có tính cứng tạm thời.
✔️(b) – Đúng. Có thể làm mềm nước có tính cứng tạm thời bằng cách đun sôi nước.
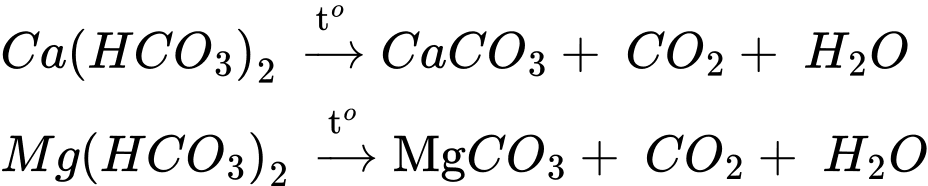
❌(c) – Sai. Không thể loại bỏ tính cứng của nước có tính cứng tạm thời bằng cách dùng một lượng vừa đủ Ca(OH)2.
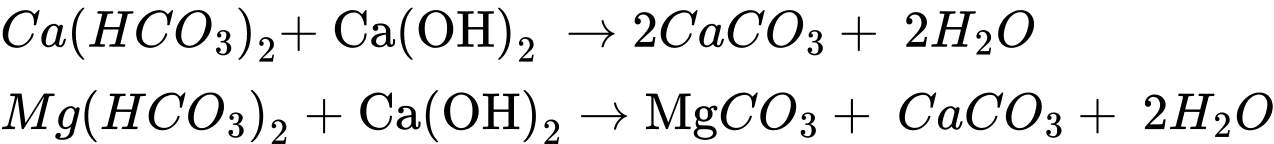
✔️(d) – Đúng. Không thể dùng cách đun sôi để loại bỏ hoàn toàn tính cứng của nước có chứa nhiều các ion sau: Mg2+, Ca2+, Сl-, НСО3- , SO42-. Chỉ loại bỏ được 1 phần Ca2+ và Mg2+ thông qua phản ứng phân hủy Ca(HCO3)2 và Mg(HCO3)2 làm nước cứng chuyển từ nước cứng toàn phần sang nước cứng vĩnh cữu.
✔️(e) – Đúng. nước cứng có thể gây đóng cặn CaCO3, MgCO3 trong nồi hơi tạo thành lớp cách nhiệt ngay dưới đáy nồi, làm cản trở quá trình dẫn nhiệt từ đó có thể gây hiện tượng nổ nồi hơi.
Có 3 phát biểu đúng.
⟹Chọn đáp án C Đáp án: C
❌(a) – Sai. Nước có chứa nhiều ion Mg2+, Ca2+, HCO3- được gọi là -nước có tính cứng tạm thời.
✔️(b) – Đúng. Có thể làm mềm nước có tính cứng tạm thời bằng cách đun sôi nước.
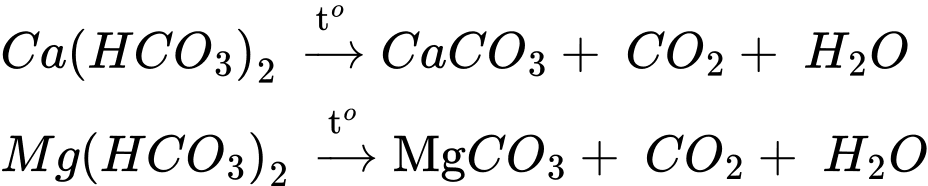
❌(c) – Sai. Không thể loại bỏ tính cứng của nước có tính cứng tạm thời bằng cách dùng một lượng vừa đủ Ca(OH)2.
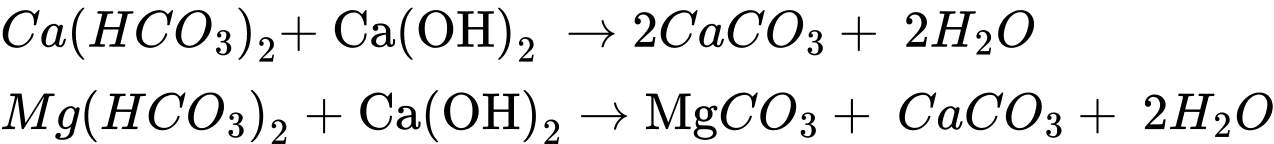
✔️(d) – Đúng. Không thể dùng cách đun sôi để loại bỏ hoàn toàn tính cứng của nước có chứa nhiều các ion sau: Mg2+, Ca2+, Сl-, НСО3- , SO42-. Chỉ loại bỏ được 1 phần Ca2+ và Mg2+ thông qua phản ứng phân hủy Ca(HCO3)2 và Mg(HCO3)2 làm nước cứng chuyển từ nước cứng toàn phần sang nước cứng vĩnh cữu.
✔️(e) – Đúng. nước cứng có thể gây đóng cặn CaCO3, MgCO3 trong nồi hơi tạo thành lớp cách nhiệt ngay dưới đáy nồi, làm cản trở quá trình dẫn nhiệt từ đó có thể gây hiện tượng nổ nồi hơi.
Có 3 phát biểu đúng.
⟹Chọn đáp án C Đáp án: C
Sử dụng đoạn thông tin dưới đây để trả lời câu 19 và câu 20:
Một mẫu nước cứng có nồng độ các ion Na+; Ca2+; Mg2+, Cl–; SO42– và HCO3– tương ứng là 1,2 mM; 3,0 mM; 1,0 mM; 0,6 mM; 0,01 mM và x mM (1 mM = 1 mmol/L), ngoài ra không chứa ion nào khác.
Câu 19 [705576]: Cách nào sau đây không thể làm mất tính cứng của loại nước nào?
A, Sử dụng Na3PO4.
B, Đun sôi.
C, Sử dụng Ca(OH)2.
D, Sử dụng Na2CO3.
Nước cứng tạm thời (do Ca(HCO3)2 và Mg(HCO3)2): có thể khử bằng cách đun sôi.
Nước cứng vĩnh cửu ( do MgSO4, CaCl2, MgCl2): không thể khử bằng đun sôi, cần dùng hóa chất.
⟹ Chọn đáp án B Đáp án: B
Nước cứng vĩnh cửu ( do MgSO4, CaCl2, MgCl2): không thể khử bằng đun sôi, cần dùng hóa chất.
⟹ Chọn đáp án B Đáp án: B
Câu 20 [705577]: Tổng khối lượng chất tan còn lại sau khi đun sôi kỹ 2 lít mẫu nước cứng trên là bao nhiêu? Giả sử các muối MgCO3, CaCO3 hầu như không tan trong nước.
A, 134,52
B, 123,6.
C, 142,2.
D, 141,0 mg.
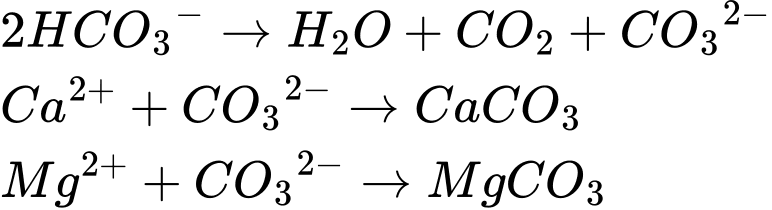
Trong 2L có: Na+ : 2,4mM; Ca2+ : 6,0mM; Mg2+ : 2,0mM; Cl- : 1,2mM; SO42-: 0,02mM; HCO3- : 2x
Bảo toàn điện tích:
1nNa+ + 2nCa2+ + 2nMg2+ = 1nCl- + 2nSO42- + 1nHCO3-
2,4 + 2. 6,0 + 2. 2,0 = 1. 1,2 + 2. 0,02 + 2x
⟹ x = 8,58mM
⟹ Dung dịch sau phản ứng còn:
Na+ : 2,4mM ; Cl- : 1,2mM ; SO42- : 0,02mM ; CO32-: 0,58mM
Khối lượng chất rắn:
m = mNa+ + mCl- + mSO42- + mCO32-
= 2,4 × 23 + 1,2 × 35,5 + 96 × 0,02 + 0,58 × 60
= 134,52
⟹ Chọn đáp án A Đáp án: A
Sử dụng đoạn thông tin dưới đây để trả lời câu 21 và câu 22:
Nồng độ tổng cộng của Ca2+ và Mg2+ trong mẫu nước cứng được xác định bằng cách chuẩn độ 1 lít mẫu nước bằng dung dịch EDTA4– (EDTA4– có khả năng tạo phức với hai cation):
Mg2+ + EDTA4– → [Mg(EDTA)]2–
Ca2+ + EDTA4– → [Ca(EDTA)]2–
Cần 31,5 mL dung dịch EDTA4– 0,0104 M để đạt đến điểm cuối trong quá trình chuẩn độ. Sau đó, mẫu 1 lít thứ hai được xử lý bằng ion sulfate để kết tủa Ca2+ dưới dạng calcium sulfate kết tủa, loại bỏ kết tủa. Sau đó, chuẩn độ Mg2+ bằng 18,7 mL dung dịch EDTA4– 0,0104 M.
Mg2+ + EDTA4– → [Mg(EDTA)]2–
Ca2+ + EDTA4– → [Ca(EDTA)]2–
Cần 31,5 mL dung dịch EDTA4– 0,0104 M để đạt đến điểm cuối trong quá trình chuẩn độ. Sau đó, mẫu 1 lít thứ hai được xử lý bằng ion sulfate để kết tủa Ca2+ dưới dạng calcium sulfate kết tủa, loại bỏ kết tủa. Sau đó, chuẩn độ Mg2+ bằng 18,7 mL dung dịch EDTA4– 0,0104 M.
Câu 21 [704303]: Nguyên tử kim loại trung tâm trong cả hai phức chất [Mg(EDTA)]2– và [Ca(EDTA)]2– đều có số oxi hóa là
A, -2.
B, 0.
C, +1.
D, +2.
- Nguyên tử kim loại trung tâm trong cả hai phức chất [Mg(EDTA)]2– và [Ca(EDTA)]2– đều là Mg và Ca, thuộc nhóm kim loại kiềm thổ trong bảng tuần hoàn.
- Vì EDTA là một phối tử không thay đổi điện tích tổng, nên số oxi hóa của kim loại trong cả hai phức chất này chính là điện tích của ion kim loại trước khi tạo phức, cụ thể là:
+ Mg có số oxi hóa là +2.
+ Ca cũng có số oxi hóa là +2.
Vậy số oxi hóa của nguyên tử kim loại trung tâm trong cả hai phức chất đều là +2.
⇒ Chọn đáp án D Đáp án: D
- Vì EDTA là một phối tử không thay đổi điện tích tổng, nên số oxi hóa của kim loại trong cả hai phức chất này chính là điện tích của ion kim loại trước khi tạo phức, cụ thể là:
+ Mg có số oxi hóa là +2.
+ Ca cũng có số oxi hóa là +2.
Vậy số oxi hóa của nguyên tử kim loại trung tâm trong cả hai phức chất đều là +2.
⇒ Chọn đáp án D Đáp án: D
Câu 22 [704304]: Nồng độ của Mg2+ và Ca2+ trong nước cứng theo mg/L lần lượt là
A, 1,9448×10–4 và 1,3312×10–4.
B, 4,6675 và 5,3248.
C, 8,6258×10–3 và 4,2458×10–3.
D, 1,2458 và 2,4871.
Đổi 31,5 mL = 0,0315 L; 18,7 mL = 0,0187 L
(1) Mg2+ + EDTA4- → [Mg(EDTA)]2-
(2) Ca2+ + EDTA4- → [Ca(EDTA)]2-
+ Xử lí lần 1 thông qua mol của EDTA4- xác định tổng mol của 2 ion Ca2+ và Mg2+
Từ PTHH số mol của tổng mol của 2 ion Ca2+ và Mg2+ là:
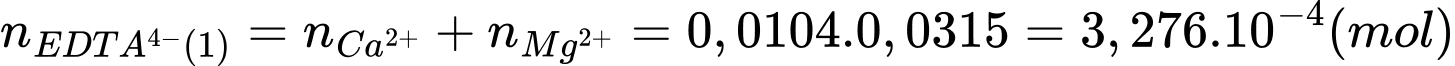
+ Xử lí lần 2: việc tạo kết tủa của ion Ca2+ thành CaSO4 nên thông qua mol của EDTA4- xác định mol của Mg2+
Số mol của Mg2+ là: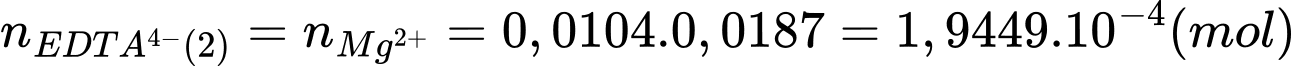
Số mol của Ca2+ trong nước cứng là:
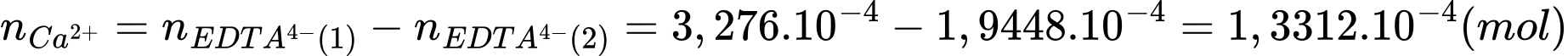
Nồng độ của Mg2+ và Ca2+ trong mẫu nước cứng theo mg/L lần lượt là 4,6675 và 5,3248 mg/L
Nồng độ Mg2+: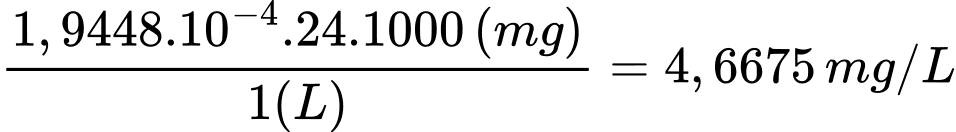
Nồng độ Ca2+: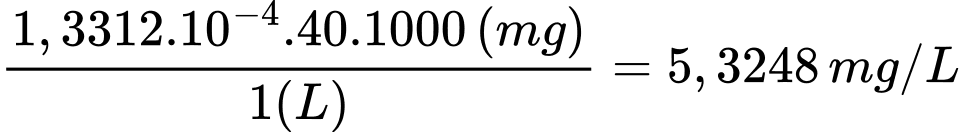
⇒ Chọn đáp án B Đáp án: B
(1) Mg2+ + EDTA4- → [Mg(EDTA)]2-
(2) Ca2+ + EDTA4- → [Ca(EDTA)]2-
+ Xử lí lần 1 thông qua mol của EDTA4- xác định tổng mol của 2 ion Ca2+ và Mg2+
Từ PTHH số mol của tổng mol của 2 ion Ca2+ và Mg2+ là:
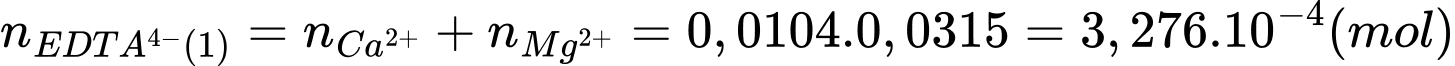
+ Xử lí lần 2: việc tạo kết tủa của ion Ca2+ thành CaSO4 nên thông qua mol của EDTA4- xác định mol của Mg2+
Số mol của Mg2+ là:
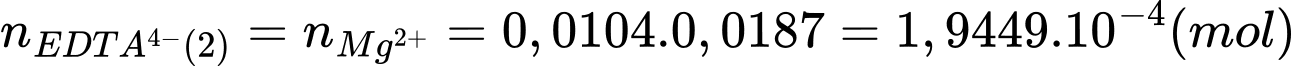
Số mol của Ca2+ trong nước cứng là:
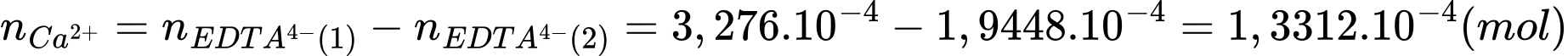
Nồng độ của Mg2+ và Ca2+ trong mẫu nước cứng theo mg/L lần lượt là 4,6675 và 5,3248 mg/L
Nồng độ Mg2+:
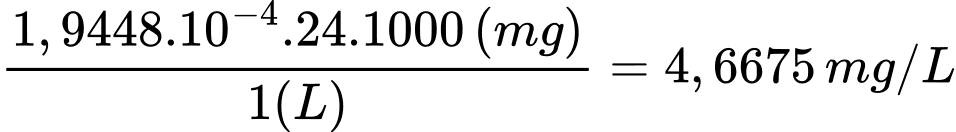
Nồng độ Ca2+:
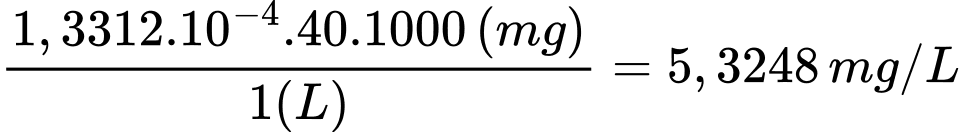
⇒ Chọn đáp án B Đáp án: B
Dạng 2: TRẮC NGHIỆM ĐÚNG SAI – mỗi ý a), b), c), d) chọn đúng hoặc sai.
Câu 23 [560994]: Nước chứa nhiều ion Ca2+ và Mg2+ được gọi là nước cứng. Nước cứng gây nhiều tác hại trong đời sống cũng như trong sản xuất.
a. Nước cứng tạm thời là tính cứng gây nên bởi các muối Ca(HCO3)2 vàMg(HCO3)2.
b. Giặt quần áo bằng nước cứng gây tốn xà phòng và làm quần áo nhanhmục nát, hư hỏng.
c. Nguyên tắc làm mềm nước cứng là làm tăng nồng độ các ion Ca2+vàMg2+trong nước cứng.
d. Có thể dùng K2CO3 (hoặc Na3PO4) để làm mất tính cứng tạm thời hoặctính cứng vĩnh cửu.
a. Nước cứng tạm thời là tính cứng gây nên bởi các muối Ca(HCO3)2 vàMg(HCO3)2.
b. Giặt quần áo bằng nước cứng gây tốn xà phòng và làm quần áo nhanhmục nát, hư hỏng.
c. Nguyên tắc làm mềm nước cứng là làm tăng nồng độ các ion Ca2+vàMg2+trong nước cứng.
d. Có thể dùng K2CO3 (hoặc Na3PO4) để làm mất tính cứng tạm thời hoặctính cứng vĩnh cửu.
- Nước cứng tạm thời: chứa các muối Ca(HCO3)2, Mg(HCO3)2 (gốc anion HCO3-).
- Nước cứng vĩnh cửu: chứa các muối CaCl2, MgSO4 (gốc anion Cl-, SO42-).
- Nước cứng toàn phần: tổng hợp của nước cứng tạm thời và vĩnh cửu.
Phân tích các phát biểu:
✔️a.Đúng. Nước cứng tạm thời: chứa các muối Ca(HCO3)2, Mg(HCO3)2 (gốc anion HCO3-).
✔️b.Đúng. Nước cứng phản ứng với xà phòng tạo ra các muối không tan, làm giảm hiệu quả giặt rửa và gây hao phí xà phòng. Ngoài ra, sự tích tụ các muối này trên vải có thể làm quần áo nhanh mục hơn.
❌c. Sai. Làm mềm nước cứng là quá trình loại bỏ hoặc giảm nồng độ ion Ca2+ và Mg2+ trong nước, chứ không phải làm tăng chúng.
✔️d. Đúng. Có thể dùng K2CO3 (hoặc Na3PO4) để làm mất tính cứng tạm thời hoặctính cứng vĩnh cửu. K2CO3 và Na3PO4 phản ứng với các ion Ca2+ và Mg2+ tạo thành kết tủa không tan (CaCO3, MgCO3) làm giảm nồng độ các ion này trong nước. Các muối này có thể làm mềm cả nước cứng tạm thời và vĩnh cửu.
- Nước cứng vĩnh cửu: chứa các muối CaCl2, MgSO4 (gốc anion Cl-, SO42-).
- Nước cứng toàn phần: tổng hợp của nước cứng tạm thời và vĩnh cửu.
Phân tích các phát biểu:
✔️a.Đúng. Nước cứng tạm thời: chứa các muối Ca(HCO3)2, Mg(HCO3)2 (gốc anion HCO3-).
✔️b.Đúng. Nước cứng phản ứng với xà phòng tạo ra các muối không tan, làm giảm hiệu quả giặt rửa và gây hao phí xà phòng. Ngoài ra, sự tích tụ các muối này trên vải có thể làm quần áo nhanh mục hơn.
❌c. Sai. Làm mềm nước cứng là quá trình loại bỏ hoặc giảm nồng độ ion Ca2+ và Mg2+ trong nước, chứ không phải làm tăng chúng.
✔️d. Đúng. Có thể dùng K2CO3 (hoặc Na3PO4) để làm mất tính cứng tạm thời hoặctính cứng vĩnh cửu. K2CO3 và Na3PO4 phản ứng với các ion Ca2+ và Mg2+ tạo thành kết tủa không tan (CaCO3, MgCO3) làm giảm nồng độ các ion này trong nước. Các muối này có thể làm mềm cả nước cứng tạm thời và vĩnh cửu.
Câu 24 [560995]: Nước cứng được phân làm ba loại: nước có tính cứng tạm thời, nước có tính cứng vĩnh cửu và nước có tính cứng toàn phần.
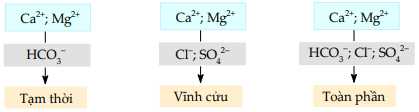
a. Căn cứ để phân loại nước cứng là dựa vào thành phần của anion gốc
acid tạo muối với ion Ca2+
và Mg2+.
b. Nước cứng tạm thời không gây nhiều tác hại như nước có tính cứng
vĩnh cửu hay nước cứng toàn phần.
c. Một dung dịch có chứa hàm lượng lớn các muối CaCl2, Ca(HCO3)2,
MgSO4. Dung dịch này là nước có tính cứng vĩnh cửu.
d. Một dung dịch nước cứng tạm thời có tổng số mol Ca2+
, Mg2+
là
0,2 mol, số mol của anion trong dung dịch là 0,2 mol.

a. Căn cứ để phân loại nước cứng là dựa vào thành phần của anion gốc
acid tạo muối với ion Ca2+
và Mg2+.
b. Nước cứng tạm thời không gây nhiều tác hại như nước có tính cứng
vĩnh cửu hay nước cứng toàn phần.
c. Một dung dịch có chứa hàm lượng lớn các muối CaCl2, Ca(HCO3)2,
MgSO4. Dung dịch này là nước có tính cứng vĩnh cửu.
d. Một dung dịch nước cứng tạm thời có tổng số mol Ca2+
, Mg2+
là
0,2 mol, số mol của anion trong dung dịch là 0,2 mol.
Phân tích các phát biểu:
✔️a.Đúng.Nước cứng được phân loại dựa trên anion đi kèm với ion Ca2+ và Mg2+:
- Nước cứng tạm thời: chứa các muối Ca(HCO3)2, Mg(HCO3)2 (gốc anion HCO3-).
- Nước cứng vĩnh cửu: chứa các muối CaCl2, MgSO4 (gốc anion Cl-, SO42-).
- Nước cứng toàn phần: tổng hợp của nước cứng tạm thời và vĩnh cửu.
❌b. Sai.Tác hại của nước cứng tạm thời, nước cứng vĩnh cửu, và nước cứng toàn phần phụ thuộc vào tổng lượng ion Ca2+, Mg2+ chứ không phụ thuộc loại cứng. Tuy nhiên, nước cứng tạm thời dễ xử lý hơn (bằng cách đun nóng để loại bỏ kết tủa CaCO3, MgCO3).
❌c.Sai. Dung dịch chứa Ca(HCO3)2 (nước cứng tạm thời) và CaCl2, MgSO4 (nước cứng vĩnh cửu), nên đây là nước cứng toàn phần chứ không chỉ là nước cứng vĩnh cửu.
❌d.Sai. Nước cứng tạm thời chứa các ion HCO3- kết hợp với Ca2+, Mg2+. Vì mỗi ion Ca2+hoặc Mg2+ cần 2 ion HCO3- để trung hòa điện tích, số mol anion HCO3- phải gấp 2 số mol cation.Tổng số mol Ca2+, Mg2+ là 0,2 mol thì số mol anion phải là 0,4 mol.
✔️a.Đúng.Nước cứng được phân loại dựa trên anion đi kèm với ion Ca2+ và Mg2+:
- Nước cứng tạm thời: chứa các muối Ca(HCO3)2, Mg(HCO3)2 (gốc anion HCO3-).
- Nước cứng vĩnh cửu: chứa các muối CaCl2, MgSO4 (gốc anion Cl-, SO42-).
- Nước cứng toàn phần: tổng hợp của nước cứng tạm thời và vĩnh cửu.
❌b. Sai.Tác hại của nước cứng tạm thời, nước cứng vĩnh cửu, và nước cứng toàn phần phụ thuộc vào tổng lượng ion Ca2+, Mg2+ chứ không phụ thuộc loại cứng. Tuy nhiên, nước cứng tạm thời dễ xử lý hơn (bằng cách đun nóng để loại bỏ kết tủa CaCO3, MgCO3).
❌c.Sai. Dung dịch chứa Ca(HCO3)2 (nước cứng tạm thời) và CaCl2, MgSO4 (nước cứng vĩnh cửu), nên đây là nước cứng toàn phần chứ không chỉ là nước cứng vĩnh cửu.
❌d.Sai. Nước cứng tạm thời chứa các ion HCO3- kết hợp với Ca2+, Mg2+. Vì mỗi ion Ca2+hoặc Mg2+ cần 2 ion HCO3- để trung hòa điện tích, số mol anion HCO3- phải gấp 2 số mol cation.Tổng số mol Ca2+, Mg2+ là 0,2 mol thì số mol anion phải là 0,4 mol.
Câu 25 [560996]: Nước cứng gây ra nhiều tác hại trong đời sống và sản xuất, vì vậy cần tiến hành các biện pháp xử lí nước phù hợp để làm giảm tính cứng của nước.
a. Có thể làm mềm nước có tính cứng tạm thời bằng cách đun sôi nước.
b. Có thể loại bỏ một phần tính cứng của nước có tính cứng vĩnh cửubằng cách dùng một lượng vừa đủ Ca(OH)2.
c. Có thể loại bỏ tính cứng tạm thời của nước bằng cách dùng lượng vừa đủ Ca(OH)2 hoặc Na2CO3.
d. Có thể dùng cách đun sôi để loại bỏ hoàn toàn tính cứng của nước cóchứa nhiều các ion sau:Mg2+ ,Ca2+ ,Cl- ,HCO3- ,SO42- .
a. Có thể làm mềm nước có tính cứng tạm thời bằng cách đun sôi nước.
b. Có thể loại bỏ một phần tính cứng của nước có tính cứng vĩnh cửubằng cách dùng một lượng vừa đủ Ca(OH)2.
c. Có thể loại bỏ tính cứng tạm thời của nước bằng cách dùng lượng vừa đủ Ca(OH)2 hoặc Na2CO3.
d. Có thể dùng cách đun sôi để loại bỏ hoàn toàn tính cứng của nước cóchứa nhiều các ion sau:Mg2+ ,Ca2+ ,Cl- ,HCO3- ,SO42- .
- Nước cứng tạm thời: chứa các muối Ca(HCO3)2, Mg(HCO3)2 (gốc anion HCO3-).
- Nước cứng vĩnh cửu: chứa các muối CaCl2, MgSO4 (gốc anion Cl-, SO42-).
- Nước cứng toàn phần: tổng hợp của nước cứng tạm thời và vĩnh cửu.
Phân tích các phát biểu:
✔️a.Đúng.Đun sôi nước làm mềm được nước cứng tạm thời.
❌b.Sai. Nước có tính cứng vĩnh cửu có chứa ion: Mg2+, Ca2+, SO42-, Cl- => dùng Na2CO3 và Na3PO4 để làm mềm nước vì tạo ra MgCO3, CaCO3,.. kết tủa. Ca(OH)2 không làm mềm nước cứng vĩnh cửu.
✔️c.Đúng. Ca(OH)2 hoặc Na2CO3 có kết tủa Ca2+,Mg2+ thành CaCO3, MgCO3, giúp làm mềm nước tạm thời.
❌d.Sai. Đun sôi không thể loại bỏ hoàn toàn tính cứng của nước chứa nhiều ion như Cl−, SO42−, do các ion này không bị kết tủa khi đun nóng.
- Nước cứng vĩnh cửu: chứa các muối CaCl2, MgSO4 (gốc anion Cl-, SO42-).
- Nước cứng toàn phần: tổng hợp của nước cứng tạm thời và vĩnh cửu.
Phân tích các phát biểu:
✔️a.Đúng.Đun sôi nước làm mềm được nước cứng tạm thời.
❌b.Sai. Nước có tính cứng vĩnh cửu có chứa ion: Mg2+, Ca2+, SO42-, Cl- => dùng Na2CO3 và Na3PO4 để làm mềm nước vì tạo ra MgCO3, CaCO3,.. kết tủa. Ca(OH)2 không làm mềm nước cứng vĩnh cửu.
✔️c.Đúng. Ca(OH)2 hoặc Na2CO3 có kết tủa Ca2+,Mg2+ thành CaCO3, MgCO3, giúp làm mềm nước tạm thời.
❌d.Sai. Đun sôi không thể loại bỏ hoàn toàn tính cứng của nước chứa nhiều ion như Cl−, SO42−, do các ion này không bị kết tủa khi đun nóng.
Câu 26 [560997]: Tính cứng của nước được phân loại như hình dưới đây:
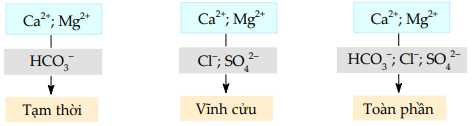
a. Nước cứng là nước chứa nhiều cation Ca2+và Mg2+.
b. Khi đun sôi nước cứng tạm thời và nước cứng toàn phần thấy xuấthiện kết tủa trắng chỉ chứa calcium carbonate.
c. Sử dụng Ca(OH)2 vừa đủ có thể để làm mềm nước có tính cứng vĩnhcửu và nước có tính cứng toàn phần.
d. Cho nước cứng đi qua lớp màng vật liệu có chứa ion Na+(phươngpháp trao đổi ion) có thể làm mềm cả nước cứng tạm thời, nước cứngvĩnh cửu và nước cứng toàn phần.

a. Nước cứng là nước chứa nhiều cation Ca2+và Mg2+.
b. Khi đun sôi nước cứng tạm thời và nước cứng toàn phần thấy xuấthiện kết tủa trắng chỉ chứa calcium carbonate.
c. Sử dụng Ca(OH)2 vừa đủ có thể để làm mềm nước có tính cứng vĩnhcửu và nước có tính cứng toàn phần.
d. Cho nước cứng đi qua lớp màng vật liệu có chứa ion Na+(phươngpháp trao đổi ion) có thể làm mềm cả nước cứng tạm thời, nước cứngvĩnh cửu và nước cứng toàn phần.
- Nước cứng tạm thời: chứa các muối Ca(HCO3)2, Mg(HCO3)2 (gốc anion HCO3-).
- Nước cứng vĩnh cửu: chứa các muối CaCl2, MgSO4 (gốc anion Cl-, SO42-).
- Nước cứng toàn phần: tổng hợp của nước cứng tạm thời và vĩnh cửu.
Phân tích các phát biểu:
✔️a.Đúng: Nước cứng được xác định dựa trên hàm lượng ion Ca2+ và Mg2+ cao trong nước.
❌b.Sai.Nước cứng tạm thời sinh ra kết tủa CaCO3 còn nước cứng toàn phần chỉ có kết tủa từ phần tạm thời, nhưng không chỉ chứa CaCO3 vì nước vĩnh cửu không sinh kết tủa.
❌c.Sai. Ca(OH)2 chỉ được sử dụng để làm mềm nước cứng tạm thời. Đối với nước cứng vĩnh cửu và nước cứng toàn phần, cần sử dụng các phương pháp khác như trao đổi ion hoặc sử dụng hóa chất làm mềm nước.
✔️d.Đúng: Phương pháp trao đổi ion thay thế các ion Ca2+ và Mg2+bằng ion Na+, làm mềm tất cả các loại nước cứng.
- Nước cứng vĩnh cửu: chứa các muối CaCl2, MgSO4 (gốc anion Cl-, SO42-).
- Nước cứng toàn phần: tổng hợp của nước cứng tạm thời và vĩnh cửu.
Phân tích các phát biểu:
✔️a.Đúng: Nước cứng được xác định dựa trên hàm lượng ion Ca2+ và Mg2+ cao trong nước.
❌b.Sai.Nước cứng tạm thời sinh ra kết tủa CaCO3 còn nước cứng toàn phần chỉ có kết tủa từ phần tạm thời, nhưng không chỉ chứa CaCO3 vì nước vĩnh cửu không sinh kết tủa.
❌c.Sai. Ca(OH)2 chỉ được sử dụng để làm mềm nước cứng tạm thời. Đối với nước cứng vĩnh cửu và nước cứng toàn phần, cần sử dụng các phương pháp khác như trao đổi ion hoặc sử dụng hóa chất làm mềm nước.
✔️d.Đúng: Phương pháp trao đổi ion thay thế các ion Ca2+ và Mg2+bằng ion Na+, làm mềm tất cả các loại nước cứng.
Câu 27 [705997]: Vôi tôi cũng được sử dụng rộng rãi trong các nhà máy xử lý nước để làm mềm nước cứng, bao gồm việc loại bỏ các ion như Ca2+ và Mg2+ cản trở hoạt động của chất tẩy rửa. Khi cho vôi vào nước sẽ tạo thành vôi tôi, phản ứng xảy ra là
CaO(s) + H2O(l) Ca(OH)2(aq)
Một mẫu nước cứng chứa các ion HCO3– và Ca2+ sẽ phản ứng với Ca(OH)2, từ đó hình thành kết tủa CaCO3 và giúp lại bỏ ion Ca2+ khỏi nguồn nước cứng.
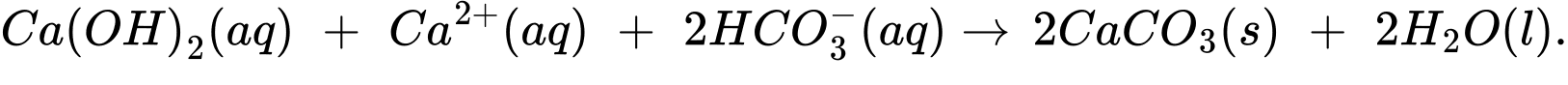 (Dạng nước cứng)
(Dạng nước cứng)
CaO(s) + H2O(l) Ca(OH)2(aq)
Một mẫu nước cứng chứa các ion HCO3– và Ca2+ sẽ phản ứng với Ca(OH)2, từ đó hình thành kết tủa CaCO3 và giúp lại bỏ ion Ca2+ khỏi nguồn nước cứng.
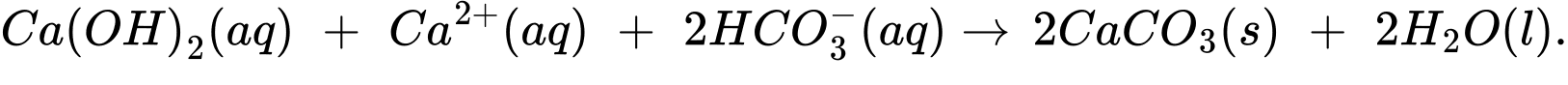 (Dạng nước cứng)
(Dạng nước cứng)
Phân tích các phát biểu :
❌(a) – Sai. Nước cứng trên thuộc loại nước cứng tạm thời do chứa ion Ca2+, Mg2+ và HCO3-.
✔️(b) – Đúng. Nước cứng là loại nước chứa hàm lượng chất khoáng cao, chủ yếu là hai ion calcium (Ca2+) và magnesium (Mg2+).
❌(c) – Sai. Phản ứng của HCl với HCO3- không loại bỏ được ion Ca2+ và Mg2+ làm cho nước cứng tạm thời thành nước cứng vĩnh cửu.
✔️(d) – Đúng. Cứ mỗi mol Ca(OH)2 được dùng thì có 1 mol Ca2+ được loại bỏ khỏi nước cứng.
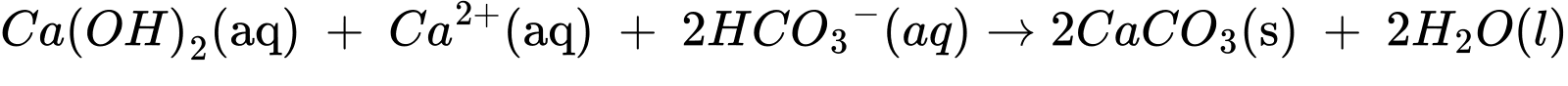
❌(a) – Sai. Nước cứng trên thuộc loại nước cứng tạm thời do chứa ion Ca2+, Mg2+ và HCO3-.
✔️(b) – Đúng. Nước cứng là loại nước chứa hàm lượng chất khoáng cao, chủ yếu là hai ion calcium (Ca2+) và magnesium (Mg2+).
❌(c) – Sai. Phản ứng của HCl với HCO3- không loại bỏ được ion Ca2+ và Mg2+ làm cho nước cứng tạm thời thành nước cứng vĩnh cửu.
✔️(d) – Đúng. Cứ mỗi mol Ca(OH)2 được dùng thì có 1 mol Ca2+ được loại bỏ khỏi nước cứng.
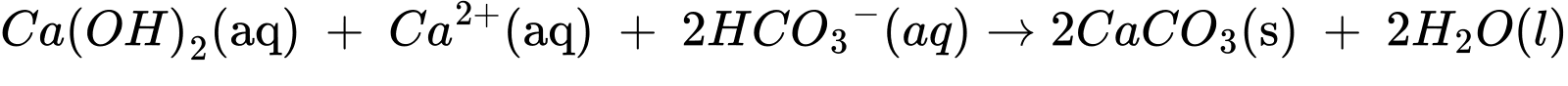
Dạng 3: TRẮC NGHIỆM YÊU CẦU TRẢ LỜI NGẮN
Câu 28 [560998]: Cho những mẫu nước sau, số mẫu nước thuộc vào nước cứng là bao nhiêu?
(a) Nước có chứa nhiều ion .
(b) Nước có chứa nhiều ion .
(c) Nước có chứa ít ion .
(d) Nước có chứa ít ion nhưng chứa nhiều ion và .
(e) Nước chỉ chứa nhiều ion .
Điền đáp án: ..........
(a) Nước có chứa nhiều ion .
(b) Nước có chứa nhiều ion .
(c) Nước có chứa ít ion .
(d) Nước có chứa ít ion nhưng chứa nhiều ion và .
(e) Nước chỉ chứa nhiều ion .
Điền đáp án: ..........
Nước
cứng là nước chứa hàm lượng cao các ion Ca2+
và Mg2+. Sự có mặt của các ion này là nguyên nhân
chính gây ra hiện tượng "độ cứng" của nước.
(a) Nước có chứa nhiều ion Ca2+ => nước cứng.
(b) Nước có chứa nhiều ion Ca2+,Mg2+, HCO3- => nước cứng.
(c) Nước có chứa ít ion Ca2+,Mg2+=> không phải nước cứng.
(d) Nước có chứa ít ion Ca2+nhưng chứa nhiều ion Mg2+và Cl-=> nước cứng.
(e) Nước chỉ chứa nhiều ion Na+,Cu2+, HCO3-.=> không chứa ion Ca2+ và Mg2+ => không phải nước cứng.
=> Có 3 mẫu là nước cứng.
Điền đáp án: 3
(a) Nước có chứa nhiều ion Ca2+ => nước cứng.
(b) Nước có chứa nhiều ion Ca2+,Mg2+, HCO3- => nước cứng.
(c) Nước có chứa ít ion Ca2+,Mg2+=> không phải nước cứng.
(d) Nước có chứa ít ion Ca2+nhưng chứa nhiều ion Mg2+và Cl-=> nước cứng.
(e) Nước chỉ chứa nhiều ion Na+,Cu2+, HCO3-.=> không chứa ion Ca2+ và Mg2+ => không phải nước cứng.
=> Có 3 mẫu là nước cứng.
Điền đáp án: 3
Câu 29 [560999]: Cho các phương pháp làm mềm nước cứng dưới đây
(1) Sử dụng lượng vừa đủ dung dịch HCl.
(2) Sử dụng lượng vừa đủ dung dịch Ca(OH)2.
(3) Cho nước cứng đi qua lớp màng vật liệu có chứa ion Na+.
(4) Sử dụng dung dịch Na3PO4.
(5) Đun sôi nước cứng.
(6) Sử dụng dung dịch Na2CO3.
Số phương pháp có thể áp dụng để làm mất tính cứng của nước có tính cứng có chứa CaCl2, MgSO4.
Điền đáp án: ..........
(1) Sử dụng lượng vừa đủ dung dịch HCl.
(2) Sử dụng lượng vừa đủ dung dịch Ca(OH)2.
(3) Cho nước cứng đi qua lớp màng vật liệu có chứa ion Na+.
(4) Sử dụng dung dịch Na3PO4.
(5) Đun sôi nước cứng.
(6) Sử dụng dung dịch Na2CO3.
Số phương pháp có thể áp dụng để làm mất tính cứng của nước có tính cứng có chứa CaCl2, MgSO4.
Điền đáp án: ..........
Để làm mềm nước cứng có chứa CaCl2 và MgSO4, cần loại bỏ các ion gây cứng như Ca2+và Mg2+. Chúng ta phân tích từng phương pháp:
1.HCl không làm kết tủa Ca2+và Mg2+ mà còn làm tăng nồng độ ion Cl-
=> phương pháp này không phù hợp.
2.Sử dụng lượng vừa đủ dung dịch Ca(OH)2 không làm mất tính cứng của nước cứng vĩnh cửu.
=> phương pháp này không có hiệu quả.
3.Cho nước cứng đi qua lớp màng vật liệu có chứa ion Na+ Đây là phương pháp trao đổi ion, thay thế Ca2+và Mg2+ bằng ion Na+
=> Phương pháp này làm mềm nước hiệu quả.
4.Dung dịch Na3PO4 phản ứng với Ca2+và Mg2+ tạo kết tủa Ca3(PO4)2 và Mg3(PO4)2 loại bỏ được tính cứng của nước.
=> Phương pháp hiệu quả.
5.Khi đun sôi, các ion Ca2+ trong nước có tính cứng tạm thời (do HCO3-) sẽ tạo kết tủa CaCO3. Tuy nhiên, nó không loại bỏ được tính cứng vĩnh cửu do MgSO4
=> phương pháp này không hiệu quả hoàn toàn.
6.Sử dụng dung dịch Na2CO3 phản ứng với Ca2+và Mg2+ tạo kết tủa CaCO3 và MgCO3, loại bỏ tính cứng của nước.
=> Phương pháp này hiệu quả.
Điền đáp án: 3
1.HCl không làm kết tủa Ca2+và Mg2+ mà còn làm tăng nồng độ ion Cl-
=> phương pháp này không phù hợp.
2.Sử dụng lượng vừa đủ dung dịch Ca(OH)2 không làm mất tính cứng của nước cứng vĩnh cửu.
=> phương pháp này không có hiệu quả.
3.Cho nước cứng đi qua lớp màng vật liệu có chứa ion Na+ Đây là phương pháp trao đổi ion, thay thế Ca2+và Mg2+ bằng ion Na+
=> Phương pháp này làm mềm nước hiệu quả.
4.Dung dịch Na3PO4 phản ứng với Ca2+và Mg2+ tạo kết tủa Ca3(PO4)2 và Mg3(PO4)2 loại bỏ được tính cứng của nước.
=> Phương pháp hiệu quả.
5.Khi đun sôi, các ion Ca2+ trong nước có tính cứng tạm thời (do HCO3-) sẽ tạo kết tủa CaCO3. Tuy nhiên, nó không loại bỏ được tính cứng vĩnh cửu do MgSO4
=> phương pháp này không hiệu quả hoàn toàn.
6.Sử dụng dung dịch Na2CO3 phản ứng với Ca2+và Mg2+ tạo kết tủa CaCO3 và MgCO3, loại bỏ tính cứng của nước.
=> Phương pháp này hiệu quả.
Điền đáp án: 3
Câu 30 [561000]: Cho các phương trình hóa học sau:
a) MgSO4(aq) + Na3PO4(aq)
b) MgSO4(aq) + Ca(OH)2(aq)
c) Ca(HCO3)2(aq)
d) Ca(OH)2(aq) + HCl(aq)
e) Mg(HCO3)2 + Ca(OH)2
g) CaCl2 + Na2CO3
Có bao nhiêu phản ứng có thể được sử dụng để làm mềm nước cứng?
Điền đáp án: ..........
a) MgSO4(aq) + Na3PO4(aq)

b) MgSO4(aq) + Ca(OH)2(aq)

c) Ca(HCO3)2(aq)

d) Ca(OH)2(aq) + HCl(aq)

e) Mg(HCO3)2 + Ca(OH)2

g) CaCl2 + Na2CO3

Có bao nhiêu phản ứng có thể được sử dụng để làm mềm nước cứng?
Điền đáp án: ..........
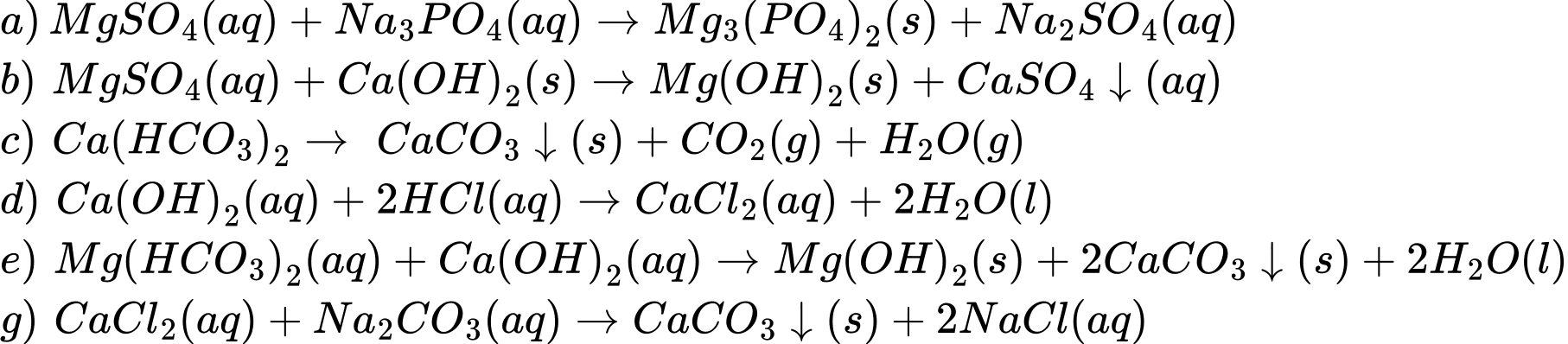
Phương trình được sử dụng trong làm mềm nước cứng là a, c,e,g
Điền đáp án: 4
Câu 31 [561001]: Một mẫu nước cứng có nồng độ các ion như sau: Ca2+ x M; Mg2+ y M; HCO3– 0,005 M; Cl– 0,004 M; SO42– 0,001 M. Để làm mềm 10 L nước này cần dùng tối thiểu bao nhiêu gam sodium carbonate? (Làm tròn đến hai chữ số thập phân)
Điền đáp án: ..........
Điền đáp án: ..........
Bảo toàn điện tích:
2 Ca2+ + 2 Mg2+ = 1 HCO3- + 1 Cl- + 2 SO4 2-
=> 2x + 2y = 0,005.1 + 0,004.1 + 0,001.2
=> 2(x + y) = 0,011
=> x+y = 0,0055
=> n (Ca2+ và Mg2+) = CM.V= 0,0055.10 = 0,055(mol)
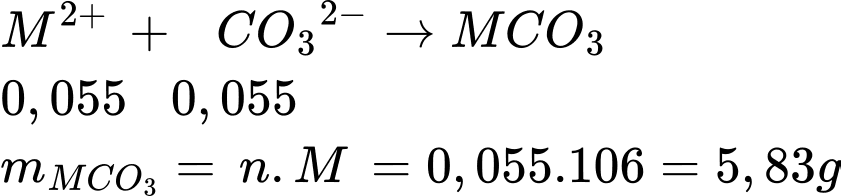
Điền đáp án: 5,8
2 Ca2+ + 2 Mg2+ = 1 HCO3- + 1 Cl- + 2 SO4 2-
=> 2x + 2y = 0,005.1 + 0,004.1 + 0,001.2
=> 2(x + y) = 0,011
=> x+y = 0,0055
=> n (Ca2+ và Mg2+) = CM.V= 0,0055.10 = 0,055(mol)
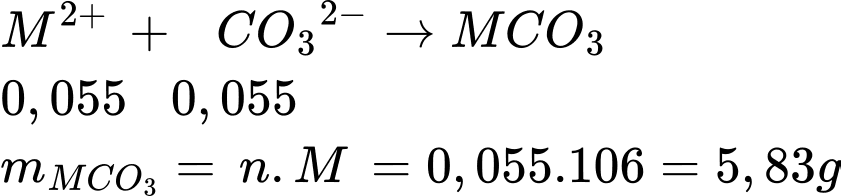
Điền đáp án: 5,8
Câu 32 [705947]: Nước cứng là loại nước chứa hàm lượng chất khoáng cao, chủ yếu là hai ion calcium (Ca2+) và magnesium (Mg2+). Nước cứng là nguyên nhân gây ra nhiều vấn đề nghiêm trọng trong các ngành công nghiệp do đó cần phải được loại bỏ. Phương pháp trao đổi ion để làm mềm nước cứng dựa trên sự thay thế các ion Mg2+ và Ca2+ trong nước cứng (kí hiệu chung là M2+) bằng các cation Na+, H+ có trong các gốc –SO3Na hoặc –SO3H được gắn vào trong nhựa trao đổi ion. Khi nước cứng đi qua nhựa, các ion Ca2+, Mg2+ sẽ được giữ lại và các ion H+, Na+ từ nhựa sẽ đi vào nước theo phản ứng:
M2+ + 2 –SO3X → (–SO3)2M + 2X+ (với X+ là H⁺ hoặc Na+).
Một loại nhựa cationite có phần trăm khối lượng lượng nguyên tố sulfur là 7,94% được sử dụng để loại bỏ các ion Mg2+, Ca2+ trong nước cứng và giả sử nguyên tố sulfur chỉ nằm trong các gốc –SO3X. Nếu khối lượng nhựa cationite đó là 500 gam thì tổng số mol Mg2+, Ca2+ tối đa có thể được loại bỏ là x mol. Giá trị của x là bao nhiêu? (Làm tròn kết quả đến số nguyên)
M2+ + 2 –SO3X → (–SO3)2M + 2X+ (với X+ là H⁺ hoặc Na+).
Một loại nhựa cationite có phần trăm khối lượng lượng nguyên tố sulfur là 7,94% được sử dụng để loại bỏ các ion Mg2+, Ca2+ trong nước cứng và giả sử nguyên tố sulfur chỉ nằm trong các gốc –SO3X. Nếu khối lượng nhựa cationite đó là 500 gam thì tổng số mol Mg2+, Ca2+ tối đa có thể được loại bỏ là x mol. Giá trị của x là bao nhiêu? (Làm tròn kết quả đến số nguyên)
Khối lượng của Sulfur trong nhựa cationite là mS = 500 . 7,94% = 39,7 gam
Số mol của sulfur là nS = 39,7 : 32 = 1,240625 mol
Bảo toàn nguyên tố S: nS = n-SO3X = 1,240625 mol
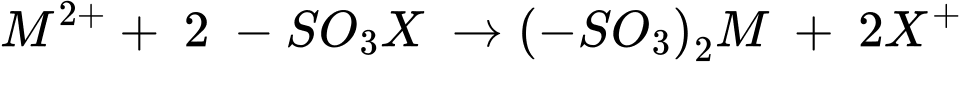
Từ phương trình hóa học tổng số mol của Ca2+ và Mg2+ là nM2+ = 1,240625:2 ≈ 1 mol
Điền đáp án : 1
Số mol của sulfur là nS = 39,7 : 32 = 1,240625 mol
Bảo toàn nguyên tố S: nS = n-SO3X = 1,240625 mol
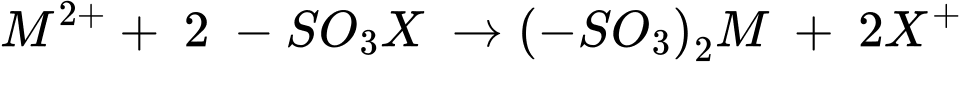
Từ phương trình hóa học tổng số mol của Ca2+ và Mg2+ là nM2+ = 1,240625:2 ≈ 1 mol
Điền đáp án : 1
Câu 33 [1016768]: Sodium carbonate (Na2CO3) là chất thường dùng để làm mềm nước cứng theo phương pháp kết tủa. Độ cứng của nước có thể được tính theo số mg CaCO3 trong 1 lít nước, trong đó độ cứng không vượt quá 60 mg/L là nước mềm. Để xử lí một mẫu nước cứng vĩnh cửu có độ cứng a (mg CaCO3/L) người ta cho 1 L dung dịch Na2CO3 0,020 M vào 19 L mẫu nước cứng, lắc đều, thu được kết tủa CaCO3 và nước mềm Y. Nồng độ Ca2+ và CO32- có trong nước mềm Y lần lượt là 5,00.10-4 M và 8,93.10-6 M. Giả thiết rằng, mẫu nước cứng chứa Ca2+ và các ion khác, các ion khác này không tham gia phản ứng, ion CO32- và ion Ca2+ không bị thuỷ phân trong nước. Tính giá trị của a (làm tròn kết quả đến hàng đơn vị).
Số mol của Na2CO3 là:

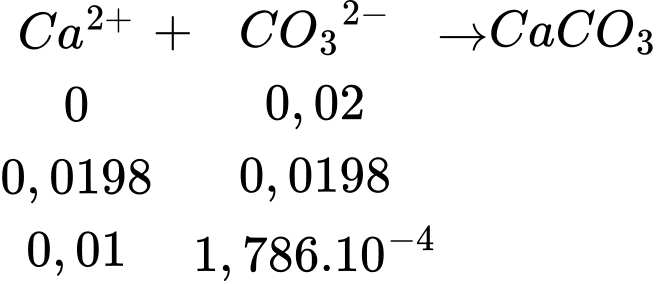
Số mol Ca2+ ban đầu là: nCa2+ = 0,01 + 0,0198 = 0,0298 mol.
Theo phương trình: nCa2+ = nCaCO3 = 0,0298 mol.
Khối lượng của CaCO3 là: mCaCO3 = 0,0298 × 100 = 2,98 gam = 2980 mg
Giá trị của a là: 2980 ÷ 19 = 156,84 ≈ 157
⟹ Điền đáp án 157

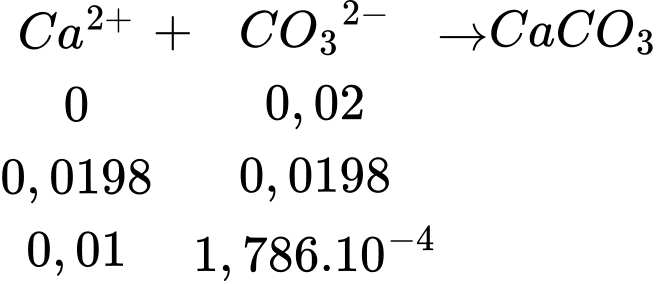
Số mol Ca2+ ban đầu là: nCa2+ = 0,01 + 0,0198 = 0,0298 mol.
Theo phương trình: nCa2+ = nCaCO3 = 0,0298 mol.
Khối lượng của CaCO3 là: mCaCO3 = 0,0298 × 100 = 2,98 gam = 2980 mg
Giá trị của a là: 2980 ÷ 19 = 156,84 ≈ 157
⟹ Điền đáp án 157
Dạng 4: BÀI TẬP ĐỌC HIỂU – đọc thông tin và trả lời các câu hỏi sau đó
LÀM MỀM NƯỚC CỨNG
Vôi tôi cũng được sử dụng rộng rãi trong các nhà máy xử lý nước để làm mềm nước cứng, bao gồm việc loại bỏ các ion như Ca2+ và Mg2+ cản trở hoạt động của chất tẩy rửa. Phương pháp làm mềm thường được sử dụng trong các nhà máy xử lý nước là quá trình vôi-soda, trong đó vôi (CaO) và tro soda (Na2CO3) được thêm vào nước. Ion CO32– khi tan trong nước sẽ có quá trình thủy phân một phần tạo thành ion HCO3–.CO32–(aq) + H2O(l) ⇌ HCO3–(aq)
Khi cho vôi vào nước sẽ tạo thành vôi tôi, phản ứng xảy ra là
CaO(s) + H2O(l) ⇌ Ca(OH)2(aq)
Lúc này có thành phần có trong dung dịch sẽ phản ứng với nhau: Ca(OH)2; HCO3– và Ca2+ có mặt trong nước cứng, từ đó hình thành kết tủa CaCO3 và giúp lại bỏ ion Ca2+ khỏi nguồn nước cứng.
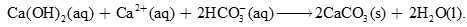
(Dạng nước cứng)
Như vậy, cứ mỗi mol Ca(OH)2 được dùng thì 1 mol Ca2+ được loại bỏ khỏi nước cứng, do đó làm mềm nước. Một số nguồn nước cứng tự nhiên có chứa các ion bicarbonate. Trong trường hợp này, không cần thêm tro soda mà chỉ cần thêm vôi sẽ làm mềm được nước cứng.
Câu 34 [561002]: Nước cứng là nước chứa nhiều ion nào sau đây?
A, Na+ và Mg2+.
B, Ca2+ và Mn2+.
C, Ca2+ và Mg2+.
D, Ba2+ và Mg2+.
Nước cứng là nước chứa nhiều ion Ca2+ và Mg2+.
⇒ Chọn đáp án C Đáp án: C
Câu 35 [561003]: Khi cho vôi CaO vào trong nước thì giá trị pH thay đổi như thế nào?
A, tăng.
B, giảm.
C, không đổi.
D, không xác định.
Khi cho CaO vào nước, pH sẽ tăng lên do tạo thành dung dịch kiềm (Ca(OH)2), và pH có thể đạt đến giá trị trong khoảng 12-12.5 trong điều kiện bão hòa.
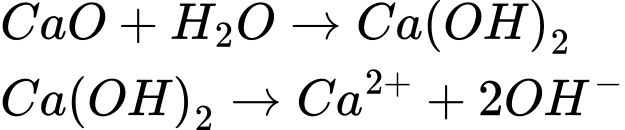
⇒ Chọn đáp án A Đáp án: A
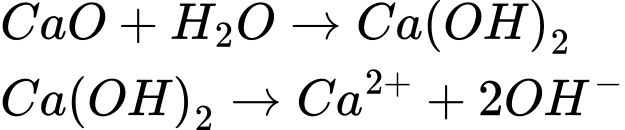
⇒ Chọn đáp án A Đáp án: A
Câu 36 [561004]: Để loại bỏ được 100 g CaCO3 thì cần tiêu tốn mất bao nhiêu g vôi CaO?
A, 28 g.
B, 56 g.
C, 74 g.
D, 92 g.
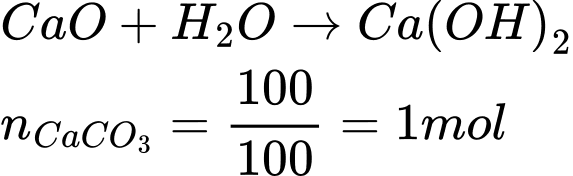
Theo phương trình: nCaO = nCaCO3 = 1 : 2 = 0,5 mol.
Khối lượng CaO là: mCaO = n × M = 0,5 × 56 = 28 gam.
Chọn đáp án A Đáp án: A
VẬT LIỆU TRAO ĐỔI ION
Nước cứng không có nghĩa là băng, là đá. Đó là tên được đặt cho nước chứa nồng độ cao ion Ca2+ và trong một số trường hợp là Mg2+, ngoài ra có thể có các cation kim loại hóa trị II khác. Đi kèm với các cation này sẽ là các anion khác nhau, đặc biệt là anion hydrogencarbonate, HCO3–. Nước thu được từ các hồ chứa nước mưa thường không chứa nồng độ cao các ion này và do đó không được phân loại là "nước cứng". Tuy nhiên, ở nhiều nơi, nguồn cung cấp nước của thành phố được lấy từ tầng nước sâu dưới lòng đất. Nếu nước mưa có chứa một ít CO2 hòa tan phải thấm qua các lớp đá vôi (CaCO3) để vào tầng nước ngầm thì một lượng nhỏ chất rắn sẽ hòa tan do có cân bằng sau:
CaCO3(s) + CO2(aq) + H2O(l) ⇌ Ca2+(aq) + 2HCO3−(aq) (I)
Ở quy mô nhỏ, hầu hết các hệ thống lọc nước gia đình đều sử dụng phương pháp trao đổi ion để làm mềm nước (Hình ảnh)
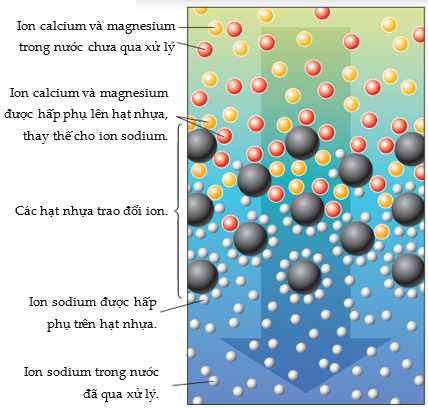
Nguyên tắc của quá trình này là thay thế ion đang được hấp phụ (ion A) trên vật liệu “nhựa trao đổi ion” bằng ion khác trong dung dịch (ion B). Hiện nay, các polyme hữu cơ tổng hợp có các nhóm chức tích điện âm (chẳng hạn như nhóm carboxylate, –CO2–) là loại nhựa được sử dụng phổ biến nhất để tạo ra vật liệu “nhựa trao đổi ion”. Các ion sodium, Na+, có trong nhựa sẽ bao quanh bề mặt của nhựa để trung hòa về mặt điện tích.
Tuy nhiên, tương tác của bề mặt vật liệu với các cation đa điện tích lớn hơn là các cation đơn đơn điện tích. Do đó, khi dung dịch nước cứng đi qua bề mặt nhựa trao đổi ion, ion Ca2+ và Mg2+ (các cation đa điện tích) sẽ dễ dàng thay thế ion Na+ (các cation đơn điện tích) trên bề mặt. Quá trình này có thể được minh họa một cách tổng quát như sau:
2NaX + Ca2+(aq) ⇌ CaX2 + 2Na+(aq)
Trong đó X đại diện cho vị trí hấp phụ trên nhựa trao đổi ion. Trạng thái cân bằng thuận lợi cho sự hấp phụ Ca2+ và giải phóng Na+. Tuy nhiên, trạng thái cân bằng bị đảo ngược nếu ion Na+(aq) hiện diện ở nồng độ cao và điều này cho phép tái sử dụng nhựa trao đổi ion. Dung dịch chứa nồng độ Na+ cao (thường là từ muối NaCl) được đưa qua nhựa để chuyển nhựa trở lại dạng ban đầu.
Câu 37 [561005]: Dựa vào phương trình (I), yếu tố nào sau đây làm tăng sự hòa tan đá vôi?
A, Tăng nồng độ Ca2+.
B, Tăng nồng độ CO2 hòa tan.
C, Tăng nồng độ HCO3–.
D, Thực hiện phản ứng trong điều kiện khô.
Để tăng sự hòa tan đá vôi, nghĩa là cân bằng chuyển dịch theo chiều thuận.
Phân tích các đáp án:
❌A. Tăng nồng độ Ca2+ => Cân bằng dịch chuyển theo chiều giảm nồng độ Ca2+, chiều nghịch.
✔️B. Tăng nồng độ CO2 hòa tan => Cân bằng dịch chuyển theo chiều giảm nồng độ CO2 => chiều thuận.
❌C. Tăng nồng độ HCO3- => Cân bằng dịch chuyển theo chiều giảm nồng độ HCO3- => chiều nghịch.
❌D. Thực hiện phản ứng trong điều kiện khô=> giảm nồng độ nước=> Cân bằng dịch chuyển theo chiều nghịch.
=> Chọn đáp án B Đáp án: B
Phân tích các đáp án:
❌A. Tăng nồng độ Ca2+ => Cân bằng dịch chuyển theo chiều giảm nồng độ Ca2+, chiều nghịch.
✔️B. Tăng nồng độ CO2 hòa tan => Cân bằng dịch chuyển theo chiều giảm nồng độ CO2 => chiều thuận.
❌C. Tăng nồng độ HCO3- => Cân bằng dịch chuyển theo chiều giảm nồng độ HCO3- => chiều nghịch.
❌D. Thực hiện phản ứng trong điều kiện khô=> giảm nồng độ nước=> Cân bằng dịch chuyển theo chiều nghịch.
=> Chọn đáp án B Đáp án: B
Câu 38 [561006]: Để làm mềm nước cứng, ion A có thể là ion nào sau đây?
A, Ca2+.
B, Mg2+.
C, Fe2+.
D, Na+.
Các vật liệu trao đổi ion (như zeolite hoặc nhựa trao đổi ion) thường sử dụng ion Na+ để thay thế Ca2+ và Mg2+, do Na+ không gây ra độ cứng trong nước.
Để làm mềm nước cứng, ion A trong quá trình trao đổi ion thường là ion có khả năng thay thế các ion gây ra độ cứng của nước, chủ yếu là Ca2+ và Mg2+
=> Chọn đáp án D
Để làm mềm nước cứng, ion A trong quá trình trao đổi ion thường là ion có khả năng thay thế các ion gây ra độ cứng của nước, chủ yếu là Ca2+ và Mg2+
=> Chọn đáp án D
Câu 39 [561007]: Giả sử vật liệu trao đổi ion chỉ chứa 10 nhóm carboxylate, sau khi trao đổi ion thì vẫn còn 4 ion Na+ tồn tại trên bề mặt vật liệu. Quá trình này tổng quát như sau:
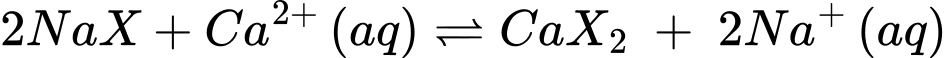
Có bao nhiêu ion Ca2+ tồn tại trên bề mặt vật liệu?
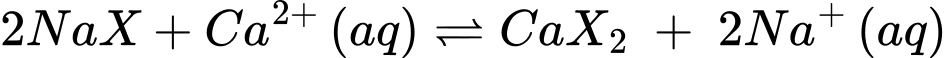
Có bao nhiêu ion Ca2+ tồn tại trên bề mặt vật liệu?
A, 2.
B, 3.
C, 4.
D, 5.
Tổng số nhóm carboxylate: 10.
Số ion Na+ còn lại: 4.
Như vậy, số nhóm carboxylate còn lại liên kết với Ca2+ là: 10−4 = 6 nhóm
Do mỗi ion Ca2+ cần 2 nhóm carboxylate để cân bằng điện tích, số ion Ca2+ trên bề mặt vật liệu sẽ là:
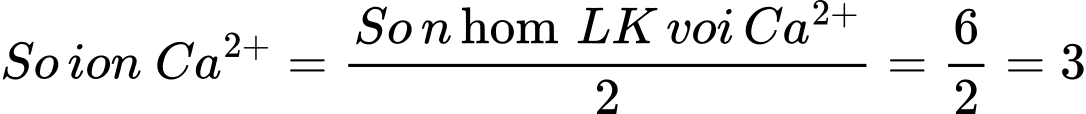
Có 3 ion Ca2+ tồn tại trên bề mặt vật liệu.
=> Chọn đáp án B Đáp án: B
Số ion Na+ còn lại: 4.
Như vậy, số nhóm carboxylate còn lại liên kết với Ca2+ là: 10−4 = 6 nhóm
Do mỗi ion Ca2+ cần 2 nhóm carboxylate để cân bằng điện tích, số ion Ca2+ trên bề mặt vật liệu sẽ là:
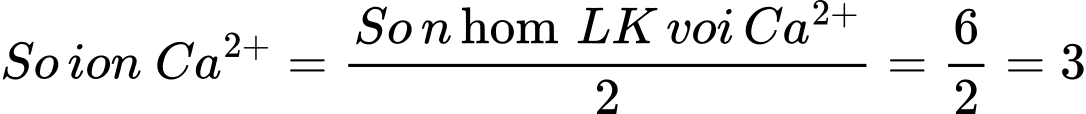
Có 3 ion Ca2+ tồn tại trên bề mặt vật liệu.
=> Chọn đáp án B Đáp án: B
Dạng 5: CÂU HỎI TỰ LUẬN
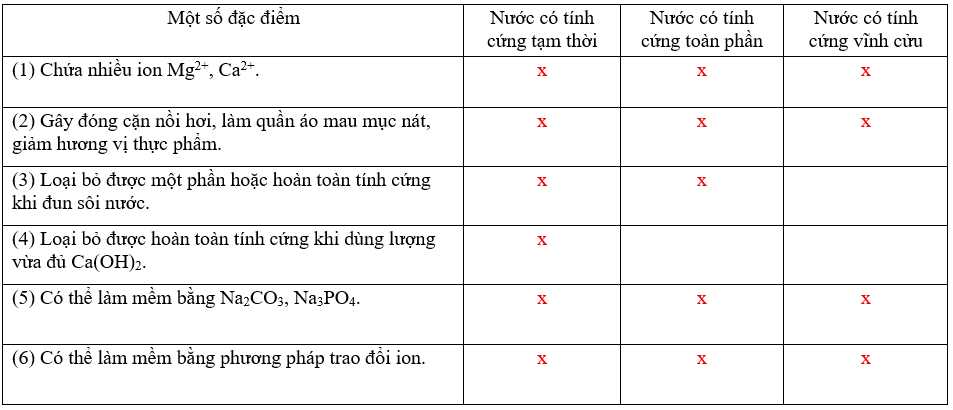
Câu 40 [1016769]: Hoàn thành bảng sau bằng cách điền dấu X vào ô ứng với thông tin đúng.
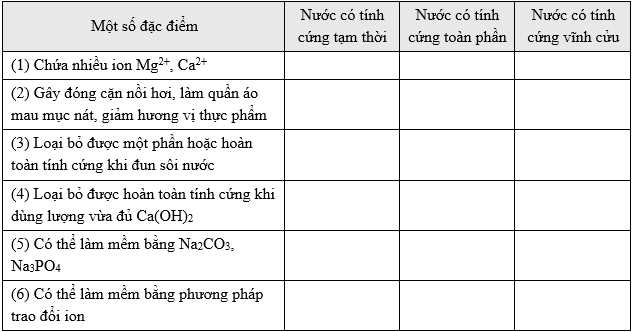

Hoàn thành bảng sau:

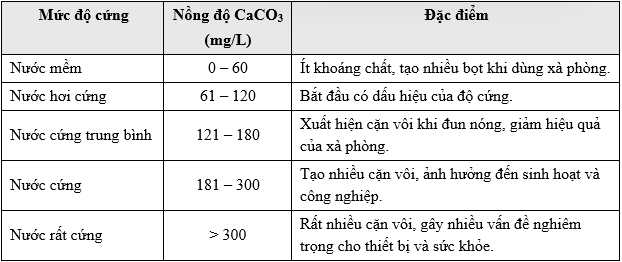
Câu 41 [1016770]: Trong thực tiễn, độ cứng của nước thường được tính theo CaCO3, tức là coi nồng độ mol Ca2+ và Mg2+ thành nồng độ mol của Ca2+, tiếp đó quy đổi nồng độ mol của Ca2+ thành số mg CaCO3 trong 1 lít nước.
Khi phân tích một loại nước tự nhiên thấy đồng thời các muối với khối lượng tương ứng như bảng sau:
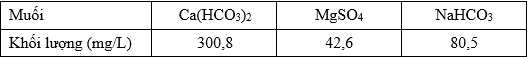
a) Xác định tổng khối lượng của ion Ca2+ và Mg2+ có trong loại nước tự nhiên trên.
b) Nồng độ quy đổi thành số mg CaCO3 trong 1 lít nước của loại nước tự nhiên trên là bao nhiêu? Xác định mức độ cứng tương ứng.
c) Cần bao nhiêu gam NaOH để có thể làm mềm loại nước tự nhiên trên? Coi nồng độ Ca2+ và Mg2+ trong nước mềm là 0.

Khi phân tích một loại nước tự nhiên thấy đồng thời các muối với khối lượng tương ứng như bảng sau:

a) Xác định tổng khối lượng của ion Ca2+ và Mg2+ có trong loại nước tự nhiên trên.
b) Nồng độ quy đổi thành số mg CaCO3 trong 1 lít nước của loại nước tự nhiên trên là bao nhiêu? Xác định mức độ cứng tương ứng.
c) Cần bao nhiêu gam NaOH để có thể làm mềm loại nước tự nhiên trên? Coi nồng độ Ca2+ và Mg2+ trong nước mềm là 0.
a. Tổng khối lượng của ion Ca2+ và Mg2+ có trong loại nước tự nhiên trên là:
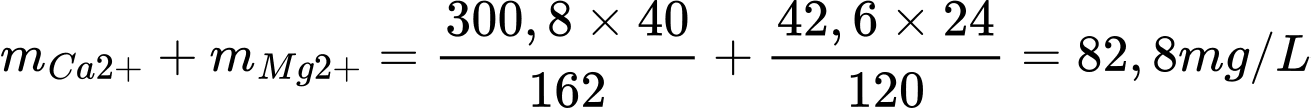
b. Tổng số mol của Ca2+ và Mg2+ là:
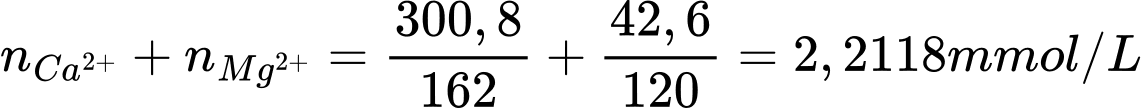 .
.
Quy đổi ra mg CaCO3 trong một lít nước của loại nước tự nhiên trên là:
C = 2,2118. 100 = 221,18 mg/L.
Nằm trong khoảng 181 - 300 nên đượ xếp vào loại nước cứng.
c, Phương trình hoá học:
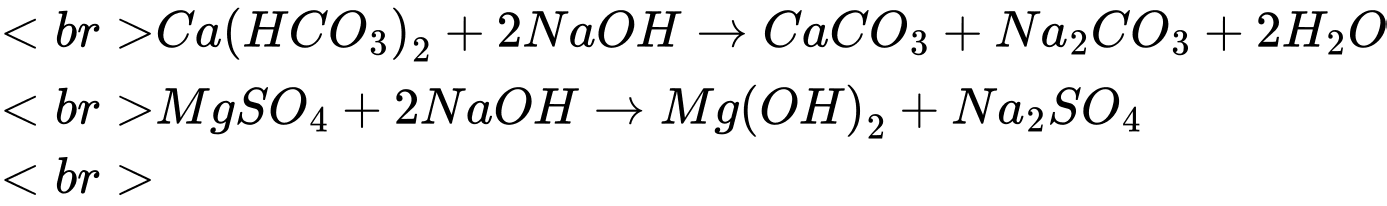
Số mol của NaOH là: 2,2118.2 = 4,4236 mmol
Khối lượng NaOH có thể dùng để làm mềm nước cứng là: 4,4236 x 40 = 176,944 mg =.0,176 g
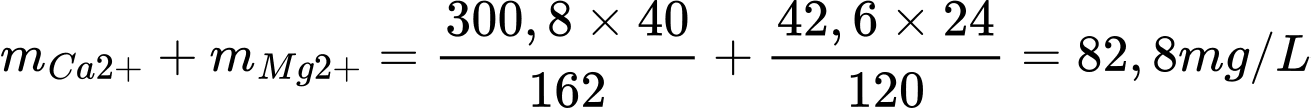
b. Tổng số mol của Ca2+ và Mg2+ là:
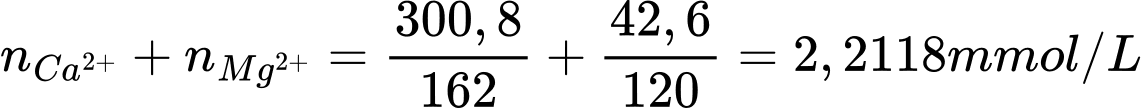 .
.Quy đổi ra mg CaCO3 trong một lít nước của loại nước tự nhiên trên là:
C = 2,2118. 100 = 221,18 mg/L.
Nằm trong khoảng 181 - 300 nên đượ xếp vào loại nước cứng.
c, Phương trình hoá học:
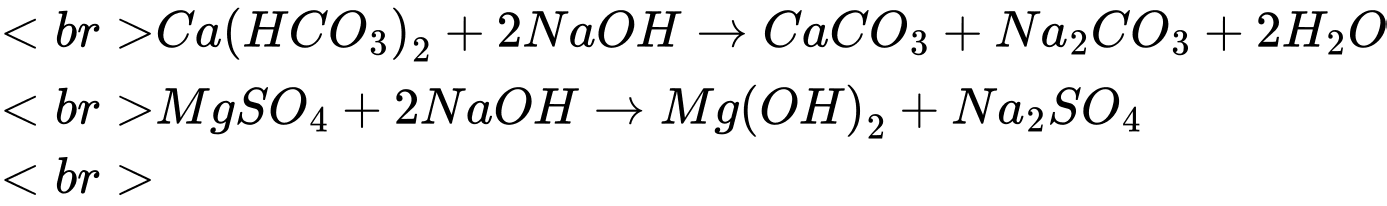
Số mol của NaOH là: 2,2118.2 = 4,4236 mmol
Khối lượng NaOH có thể dùng để làm mềm nước cứng là: 4,4236 x 40 = 176,944 mg =.0,176 g