Dạng 1: TRẮC NGHIỆM KHÁCH QUAN: mỗi câu hỏi chỉ có một đáp án đúng.
Câu 1 [705687]: Trong vỏ Trái Đất, các kim loại …(1)… tồn tại chủ yếu dưới dạng …(2)... Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, Fe và Na, đơn chất.
B, Ag và Cu, hợp chất.
C, K và Li, đơn chất.
D, Au và Ag, đơn chất.
Trong vỏ Trái Đất, các kim loại Au và Ag tồn tại chủ yếu dưới dạng đơn chất.
Phân tích:
Kim loại trong vỏ Trái Đất thường tồn tại dưới dạng hợp chất, trừ một số loại kim có tính khử yếu như vàng (Au), bạc (Ag), bạch kim (Pt),... có thể tồn tại ở dạng đơn chất.
⭐ Fe và Na: Là các loại kim loại hoạt động mạnh, thường tồn tại trong tự nhiên dưới dạng hợp chất chứ không phải chất đơn.
⭐ Ag và Cu: Đồng tồn tại ở dạng hợp chất, nhưng bạc có thể được tìm thấy ở dạng đơn chất trong tự nhiên.
⭐ K và Li: Là loại kim loại kiềm, có tính khử mạnh nên chỉ tồn tại dưới dạng hợp chất .
⭐ Au và Ag: Là những loại kim loại có tính khử yếu, có thể tồn tại ở dạng đơn chất trong tự nhiên.
⇒ Chọn đáp án D Đáp án: D
Phân tích:
Kim loại trong vỏ Trái Đất thường tồn tại dưới dạng hợp chất, trừ một số loại kim có tính khử yếu như vàng (Au), bạc (Ag), bạch kim (Pt),... có thể tồn tại ở dạng đơn chất.
⭐ Fe và Na: Là các loại kim loại hoạt động mạnh, thường tồn tại trong tự nhiên dưới dạng hợp chất chứ không phải chất đơn.
⭐ Ag và Cu: Đồng tồn tại ở dạng hợp chất, nhưng bạc có thể được tìm thấy ở dạng đơn chất trong tự nhiên.
⭐ K và Li: Là loại kim loại kiềm, có tính khử mạnh nên chỉ tồn tại dưới dạng hợp chất .
⭐ Au và Ag: Là những loại kim loại có tính khử yếu, có thể tồn tại ở dạng đơn chất trong tự nhiên.
⇒ Chọn đáp án D Đáp án: D
Câu 2 [628912]: Kim loại nào sau đây là kim loại kiềm?
A, Al.
B, Mg.
C, K.
D, Ca.
Phân nhóm chính IA (kim loại kiềm) bao gồm các nguyên tố:
Li → Li
Na → Na
K → Kéo
Rb → Rèm
Cs → Xe
Fr → Pháp
⟹ Chọn đáp án C Đáp án: C
Li → Li
Na → Na
K → Kéo
Rb → Rèm
Cs → Xe
Fr → Pháp
⟹ Chọn đáp án C Đáp án: C
Câu 3 [233844]: Kim loại nào sau đây là kim loại kiềm?
A, Mg.
B, Ag.
C, Cu.
D, Na.
Kim loại kiềm là các kim loại thuộc nhóm IA trong BTH: Li, K, Na, Rb, Cs.
⟹ Chọn đáp án D Đáp án: D
⟹ Chọn đáp án D Đáp án: D
Câu 4 [59858]: Công thức chung của oxide kim loại thuộc nhóm IA là
A, R2O3.
B, RO2.
C, R2O.
D, RO.
HD Kim loại thuộc nhóm IA có 1 electron ở lớp ngoài cùng → Oxide kim loại thuộc nhóm IA là R2O
→ Chọn đáp án C
Đáp án: C
→ Chọn đáp án C
Đáp án: C
Câu 5 [680857]: Nguyên tố natri (sodium, Na ) có số hiệu nguyên tử là 11 . Ở trạng thái cơ bản, cấu hình electron của ion Na+ là
A, 1s22s22p63s1.
B, 1s22s22p6.
C, 1s22s22p5.
D, 1s22s22p63s2.
Cấu hình electron của Sodium là: 1s22s22p63s1
⟶ Sodium có 1 electron lớp ngoài cùng cần nhường 1 eletron để tạo thành ion Na+
Na ⟶ Na+ + 1e
Cấu hình electron của ion Na+ là: 1s22s22p6
⟹ Chọn đáp án B Đáp án: B
⟶ Sodium có 1 electron lớp ngoài cùng cần nhường 1 eletron để tạo thành ion Na+
Na ⟶ Na+ + 1e
Cấu hình electron của ion Na+ là: 1s22s22p6
⟹ Chọn đáp án B Đáp án: B
Câu 6 [1016754]: Nguyên tố potassium (K) có số hiệu nguyên tử là 19. Ở trạng thái cơ bản, cấu hình electron của nguyên tử K là?
A, [Ar]4s1.
B, [Kr]4s2.
C, [Ar]4s2.
D, [Kr]4s1.
Nguyên tố potassium (K) có số hiệu nguyên tử là 19.
Ở trạng thái cơ bản, cấu hình electron của nguyên tử K là: 1s22s22p63s23p64s1.
Cấu hình electron rút gọn của K là: [Ar]4s1.
⟹ Chọn đáp án A
Đáp án: A
Ở trạng thái cơ bản, cấu hình electron của nguyên tử K là: 1s22s22p63s23p64s1.
Cấu hình electron rút gọn của K là: [Ar]4s1.
⟹ Chọn đáp án A
Đáp án: A
Câu 7 [1016755]: Ở trạng thái cơ bản, cấu hình electron của ion Na+ là 1s22s22p6. Số hạt mang điện trong nguyên tử Na là
A, 18.
B, 11.
C, 9.
D, 22.
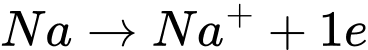
Cấu hình electron của Na là: 1s22s22p63s1 ⟶ Na có số hiệu nguyên tử Z = 11.
Tổng số hạt mamg điện trong nguyên tử Na là: P + E = 2Z = 2.11 = 22 hạt
⟹ Chọn đáp án D Đáp án: D
Câu 8 [1016756]: Cho biết số thứ tự của K trong bảng tuần hoàn là 19. Số electron ở lớp ngoài cùng của nguyên tử K là?
A, 4.
B, 3.
C, 2.
D, 1.
Cho biết số thứ tự của K trong bảng tuần hoàn là 19 ⟶ K có số hiệu nguyên tử Z = 19.
Ở trạng thái cơ bản cấu hình electron của Potassium (K) là: 1s22s22p63s23p64s1.
Nguyên tử K có 1e lớp ngoài cùng.
⟹ Chọn đáp án D Đáp án: D
Ở trạng thái cơ bản cấu hình electron của Potassium (K) là: 1s22s22p63s23p64s1.
Nguyên tử K có 1e lớp ngoài cùng.
⟹ Chọn đáp án D Đáp án: D
Câu 9 [1016757]: Cấu hình electron lớp ngoài cùng của nguyên tử nguyên tố sodium là 3s1. Nguyên tố sodium thuộc
A, chu kì 3 nhóm IIA.
B, chu kì 3 nhóm IA.
C, chu kì 2 nhóm IA.
D, chu kì 2 nhóm IIA.
Cấu hình electron lớp ngoài cùng của nguyên tử nguyên tố sodium là 3s1. Nguyên tố sodium thuộc chu kì 3 nhóm IA.
⟹ Chọn đáp án B
Đáp án: B
⟹ Chọn đáp án B
Đáp án: B
Câu 10 [1016758]: Ở trạng thái cơ bản, nguyên tử của nguyên tố nào sau đây có 1 electron ở lớp ngoài cùng?
A, Ca (Z = 20).
B, Na (Z = 11).
C, Al (Z = 13).
D, Fe (Z = 26).
Phân tích các phát biểu:
❌A. Ca (Z=20). Cấu hình electron của Ca là: 1s22s22p63s23p64s2 . Ca có 2e lớp ngoài cùng.
✔️B. Na (Z=11). Cấu hình electron của Na là: 1s22s22p63s1. Na có 1e lớp ngoài cùng.
❌C. Al (Z=13). Cấu hình electron của Al là: 1s22s22p63s23p1. Al có 3e lớp ngoài cùng.
❌D. Fe (Z=26). Cấu hình electron của Fe là: 1s22s22p63s23p63d64s2. Fe có 2e lớp ngoài cùng.
⟹ Chọn đáp án B Đáp án: B
❌A. Ca (Z=20). Cấu hình electron của Ca là: 1s22s22p63s23p64s2 . Ca có 2e lớp ngoài cùng.
✔️B. Na (Z=11). Cấu hình electron của Na là: 1s22s22p63s1. Na có 1e lớp ngoài cùng.
❌C. Al (Z=13). Cấu hình electron của Al là: 1s22s22p63s23p1. Al có 3e lớp ngoài cùng.
❌D. Fe (Z=26). Cấu hình electron của Fe là: 1s22s22p63s23p63d64s2. Fe có 2e lớp ngoài cùng.
⟹ Chọn đáp án B Đáp án: B
Câu 11 [560785]: Dựa vào cấu hình electron và bán kính nguyên tử, tại sao trong các hợp chất, kim loại nhóm IA đều thể hiện số oxi hoá +1?
A, Bán kính lớn và có 1e hóa trị.
B, Bán kính nhỏ và có 2e hóa trị.
C, Bán kính lớn và có 2e hóa trị.
D, Bán kính nhỏ và cấu hình electron chỉ có 1e.
Các kim loại nhóm IA đều có 1 electron ở lớp ngoài cùng, với cấu hình electron chung là ns1, ví dụ:
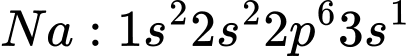
Do dễ mất 1 electron duy nhất ở lớp ngoài cùng do cấu hình electron, bán kính nguyên tử lớn và năng lượng ion hóa thấp là lý do khiến các kim loại nhóm IA luôn thể hiện số oxi hóa +1 trong các hợp chất.
=> Chọn đáp án A Đáp án: A
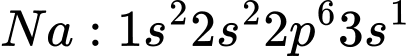
Do dễ mất 1 electron duy nhất ở lớp ngoài cùng do cấu hình electron, bán kính nguyên tử lớn và năng lượng ion hóa thấp là lý do khiến các kim loại nhóm IA luôn thể hiện số oxi hóa +1 trong các hợp chất.
=> Chọn đáp án A Đáp án: A
Câu 12 [560786]: Phát biểu nào sau đây không đúng với kim loại nhóm IA?
A, Có nhiệt độ nóng chảy thấp.
B, Có khối lượng riêng lớn.
C, Đều là các kim loại mềm.
D, Có bán kính nguyên tử lớn nhất so với các nguyên tố cùng chu kì.
Các kim loại nhóm IA đều có độ cứng thấp, dễ nóng chảy, khối lượng riêng nhỏ, dẫn điện tốt. Đáp án: B
Câu 13 [560787]: Vì sao trong tự nhiên không tìm thấy đơn chất kim loại kiềm?
A, Vì kim loại kiềm có 1 electron hóa trị.
B, Vì kim loại kiềm có khối lượng riêng nhỏ.
C, Vì kim loại kiềm có tính khử rất mạnh.
D, Vì kim loại kiềm chỉ có 1 số oxi hóa là +1.
Trong tự nhiên không tìm thấy đơn chất kim loại kiềm vì các kim loại kiềm có tính khử rất mạnh, có khả năng tác dụng với nhiều đơn chất, hợp chất trong môi trường ngay ở điều kiện thường để trở thành hợp chất Đáp án: C
Câu 14 [705741]: “Các kim loại nhóm IA có khối lượng riêng ...(1)... do có bán kính nguyên tử ...(2)... và cấu trúc mạng tinh thể kém đặc khít”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, nhỏ, lớn.
B, lớn, lớn.
C, nhỏ, nhỏ.
D, lớn, nhỏ.
Các kim loại nhóm IA có khối lượng riêng nhỏ do có bán kính nguyên tử lớn và cấu trúc mạng tinh thể kém đặc khít.
Giải thích:
- Kim loại kiềm có bán kính nguyên tử lớn so với nhiều kim loại khác, dẫn đến mật độ nguyên tử trong một đơn vị thể tích nhỏ hơn.
- Kim loại kiềm có cấu trúc mạng tinh thể lập phương tâm khối, không đặc khít bằng các mạng lập phương tâm diện hay lục phương của nhiều kim loại khác như Fe, Cu, Al. Do đó, khoảng cách giữa các nguyên tử trong tinh thể lớn, khiến khối lượng riêng của chúng thấp hơn.
⇒ Chọn đáp án A
Đáp án: A
Giải thích:
- Kim loại kiềm có bán kính nguyên tử lớn so với nhiều kim loại khác, dẫn đến mật độ nguyên tử trong một đơn vị thể tích nhỏ hơn.
- Kim loại kiềm có cấu trúc mạng tinh thể lập phương tâm khối, không đặc khít bằng các mạng lập phương tâm diện hay lục phương của nhiều kim loại khác như Fe, Cu, Al. Do đó, khoảng cách giữa các nguyên tử trong tinh thể lớn, khiến khối lượng riêng của chúng thấp hơn.
⇒ Chọn đáp án A
Đáp án: A
Câu 15 [560788]: Xu hướng biến đổi nhiệt độ nóng chảy của các kim loại nhóm IA từ Li đến Cs là
A, tăng dần.
B, giảm dần.
C, không đổi.
D, không xác định.
Trong nhóm IA, đi từ Li đến Cs: Nhiệt độ nóng chảy và nhiệt độ sôi giảm dần. Đáp án: B
Câu 16 [560789]: Các kim loại kiềm có khối lượng riêng nhỏ và độ cứng thấp hơn nhiều so với các kim loại khác. Nguyên nhân là do:
(1) Tinh thể có kiểu mạng lập phương tâm khối.
(2) Khối lượng nguyên tử nhỏ hơn các kim loại khác.
(3) Có lực liên kết kim loại yếu.
(1) Tinh thể có kiểu mạng lập phương tâm khối.
(2) Khối lượng nguyên tử nhỏ hơn các kim loại khác.
(3) Có lực liên kết kim loại yếu.
A, (1), (2) và (3).
B, (2) và (3).
C, (1) và (3).
D, (1) và (2).
Các kim loại kiềm có khối lượng riêng nhỏ và độ cứng thấp hơn nhiều so với các kim loại khác. Nguyên nhân là do:
(1) Tinh thể có kiểu mạng lập phương tâm khối.
(3) Có lực liên kết kim loại yếu. Đáp án: C
(1) Tinh thể có kiểu mạng lập phương tâm khối.
(3) Có lực liên kết kim loại yếu. Đáp án: C
Câu 17 [560790]: Cho khối lượng riêng của một số kim loại: K (0,86 g/cm3), Na (0,97 g/cm3), Mg (1,74 g/cm3), Fe (7,09 g/cm3). Khi cho từng mẩu kim loại trên vào nước, số kim loại nổi trên nước là
A, 1.
B, 2.
C, 3.
D, 4.
Khối lượng riêng của nước d = 1 g/mL (1 mL 1 cm3).
Kim loại nhẹ hơn nước (khối lượng riêng nhỏ hơn 1,0 g/mL) sẽ nổi lên trên nước.
→ Có 2 kim loain nổi trên nước trong dãy trên là: K (0,86 g/cm3), Na (0,97 g/cm3). Đáp án: B
Kim loại nhẹ hơn nước (khối lượng riêng nhỏ hơn 1,0 g/mL) sẽ nổi lên trên nước.
→ Có 2 kim loain nổi trên nước trong dãy trên là: K (0,86 g/cm3), Na (0,97 g/cm3). Đáp án: B
Câu 18 [705492]: “Các kim loại kiềm có thế điện cực chuẩn …(1)…, do đó chúng đều phản ứng với nước ở điều kiện thường với mức độ …(2)… từ Li đến Cs”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, rất âm, giảm dần.
B, rất dương, giảm dần.
C, rất dương, tăng dần.
D, rất âm, tăng dần.
Các kim loại kiềm có thế điện cực chuẩn rất âm, do đó chúng đều phản ứng với nước ở điều kiện thường với mức độ tăng dần từ Li đến Cs.
Giải thích:
- Thế điện cực chuẩn (Eo) của kim loại kiềm so với cặp M+/M đều có giá trị rất âm, chứng tỏ chúng dễ bị oxi hóa để tạo ion dương, tức kim loại kiềm có tính khử rất mạnh, dễ dàng nhường electron để phản ứng với các chất như nước.
- Bán kính nguyên tử của các kim loại kiềm lớn nên lực liên kết giữa hạt nhân và electron hóa trị nhỏ ⟶ khả năng nhường electron dễ dàng hơn. Vì thế, tính khử mạnh, dẫn đến phản ứng với nước diễn ra mạnh.
⇒ Chọn đáp án D Đáp án: D
Giải thích:
- Thế điện cực chuẩn (Eo) của kim loại kiềm so với cặp M+/M đều có giá trị rất âm, chứng tỏ chúng dễ bị oxi hóa để tạo ion dương, tức kim loại kiềm có tính khử rất mạnh, dễ dàng nhường electron để phản ứng với các chất như nước.
- Bán kính nguyên tử của các kim loại kiềm lớn nên lực liên kết giữa hạt nhân và electron hóa trị nhỏ ⟶ khả năng nhường electron dễ dàng hơn. Vì thế, tính khử mạnh, dẫn đến phản ứng với nước diễn ra mạnh.
⇒ Chọn đáp án D Đáp án: D
Câu 19 [560791]: Tính chất hóa học chung của kim loại kiềm là
A, tính acid.
B, tính base.
C, tính oxi hóa mạnh.
D, tính khử mạnh.
Tính chất hóa học chung của kim loại kiềm là tính khử mạnh.
⇒ Chọn đáp án D Đáp án: D
⇒ Chọn đáp án D Đáp án: D
Câu 20 [560792]: Khi cắt mẩu sodium ở trong không khí, bề mặt vừa cắt có ánh kim lập tức mờ đi. Điều này được giải thích là vì kim loại sodium phản ứng với oxygen trong không khí tạo thành chất X đồng thời mất đi tính ánh kim của kim loại. Chất X là
A, Sodium oxide.
B, Sodium hydroxide.
C, Sodium hydride.
D, Sodium nitride.
HD:
Kim loại sodium phản ứng với oxygen trong không khí tạo thành sodium oxide. Phản ứng xảy ra như sau:
➱ Đáp án đúng. A. sodium oxide Đáp án: A
Kim loại sodium phản ứng với oxygen trong không khí tạo thành sodium oxide. Phản ứng xảy ra như sau:
Na + O2 → Na2O (sodium oxide)
Phản ứng này tạo ra một lớp oxide mỏng trên bề mặt, làm mất đi tính ánh kim ban đầu của sodium, khiến bề mặt vừa cắt bị mờ đi.➱ Đáp án đúng. A. sodium oxide
Câu 21 [560793]: Cho các sơ đồ chuyển hóa sau:
• A + H2O NaOH;
NaOH;
• A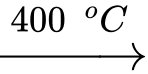 B
B 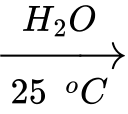 NaOH + O2Chất B được sử dụng để tạo oxygen trong tàu ngầm. Chất A và B lần lượt là
NaOH + O2Chất B được sử dụng để tạo oxygen trong tàu ngầm. Chất A và B lần lượt là
• A + H2O
 NaOH;
NaOH; • A
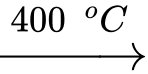 B
B 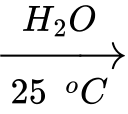 NaOH + O2Chất B được sử dụng để tạo oxygen trong tàu ngầm. Chất A và B lần lượt là
NaOH + O2Chất B được sử dụng để tạo oxygen trong tàu ngầm. Chất A và B lần lượt là A, Na2O2 và Na2O.
B, Na2O và Na2O2.
C, Na2O2 và O2.
D, Na2O và O2.
Phản ứng 1. 
Phản ứng 2: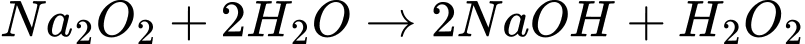
⟹ Chất A là Na2O, chất B là Na2O2.
⟹ Chọn đáp án B Đáp án: B

Phản ứng 2:
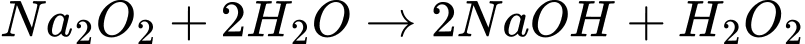
⟹ Chất A là Na2O, chất B là Na2O2.
⟹ Chọn đáp án B Đáp án: B
Câu 22 [560794]: Phương trình hoá học của phản ứng giữa Na với khí Cl2 là
A, 2Na(s) + Cl2(g) → 2NaCl(s).
B, 2Na(s) + Cl2(g) → 2NaCl(g).
C, Na(s) + Cl2(g) → NaCl2(s).
D, 4Na(s) + Cl2(g) → 2Na2Cl(s).
Phản ứng hóa học giữa kim loại Na (s) và khí Cl2 (g) , tạo ra NaCl kết tinh (s)
⟹ chọn đáp án A Đáp án: A
⟹ chọn đáp án A Đáp án: A
Câu 23 [560795]: Lithium rắn phản ứng với nước lạnh tạo thành dung dịch. Phương trình hóa học cân bằng nào đúng cho phản ứng của lithium với nước?
A, Li(s) + H2O(g) → LiOH(aq) + H2(g).
B, Li (s) + H2O(l) → LiOH(aq) + H2(g).
C, 2Li(s) + 2H2O(l) → 2LiOH(aq) + H2(g).
D, 2Li (s) + 2H2O(g) → 2LiOH(aq) + H2(g).
Phản ứng hóa học giữa lithium rắn và nước lạnh tạo thành dung dịch hydroxide và khí hydrogen
⟹ Chọn đáp án C Đáp án: C
⟹ Chọn đáp án C Đáp án: C
Câu 24 [560796]: Khi cho mẩu nhỏ sodium phản ứng với nước, hiện tượng quan sát được là
A, Mẩu sodium chìm xuống đáy và có khí thoát ra.
B, Mẩu sodium bốc cháy, cho ngọn lửa màu tím.
C, Mẩu sodium chạy trên bề mặt nước, có khí không màu thoát ra.
D, Mẩu sodium bốc cháy kèm tiếng nổ nhỏ.
Khi sodium (Na) phản ứng với nước, nó tạo ra natri hydroxide (NaOH) và khí (H2) . Khí hydrogen không màu và mẩu sodium có thể chạy trên bề mặt nước vì phản ứng sinh nhiệt, khiến sodium nổi lên và di chuyển.
⟹ chọn đáp án C Đáp án: C
⟹ chọn đáp án C Đáp án: C
Câu 25 [560797]: Khi thêm lithium vào nước sẽ tạo ra khí. Thí nghiệm và kết quả nào sẽ xác định chính xác loại khí này?
A, Đốt cháy khí sinh ra ở đầu ống dẫn khí thấy có tiếng nổ nhỏ.
B, Dẫn vào dung dịch nước vôi trong thấy xuất hiện vẩn đục.
C, Cho vào quỳ tím ẩm thấy quỳ tím bị mất màu.
D, Đốt cháy khí sinh ra ở đầu ống dẫn khí thấy ngọn lửa có màu tím nhạt.
Khi hydrogen (H₂) bị đốt cháy, nó sẽ phản ứng với oxygen trong không khí và tạo ra nước, đồng thời phát ra tiếng nổ nhỏ đặc trưng. Đáp án: A
Câu 26 [560798]: Trong phòng thí nghiệm, tại sao khi cho kim loại nhóm IA (Li, Na, K) tác dụng với nước thì cần lấy mẫu kim loại nhỏ?
A, Kim loại nhóm IA phản ứng mãnh liệt với nước.
B, Kim loại nhóm IA rất cứng, khó cắt.
C, Kim loại nhóm IA rất mềm, dễ cắt.
D, Kim loại nhóm IA có khối lượng riêng nhỏ.
Các kim loại nhóm IA phản ứng mạnh với nước để tạo ra kiềm (NaOH, KOH,...) và khí hydrogen (H2), đồng thời tỏa ra một lượng nhiệt lớn. Nếu sử dụng mẫu kim loại lớn, phản ứng sẽ sinh nhiệt mạnh hơn, có thể gây nổ hoặc cháy do khí hidro dễ cháy.
⟹ chọn đáp án A Đáp án: A
⟹ chọn đáp án A Đáp án: A
Câu 27 [560799]: Cho một mẩu nhỏ postassium vào nước thu được dung dịch. Giá trị pH của dung dịch sau phản ứng có thể nhận giá trị nào dưới đây?
A, pH = 11.
B, pH = 2.
C, pH = 7.
D, pH = 6.
2K + 2H2O 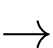 2KOH + H2
2KOH + H2
Phản ứng của K với nước sinh ra KOH tạo môi trường base (kiềm) mạnh nên dung dịch sau phản ứng có thể có giá trị pH = 11.
⇒ Chọn đáp án A Đáp án: A
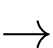 2KOH + H2
2KOH + H2Phản ứng của K với nước sinh ra KOH tạo môi trường base (kiềm) mạnh nên dung dịch sau phản ứng có thể có giá trị pH = 11.
⇒ Chọn đáp án A Đáp án: A
Câu 28 [560800]: Giả sử thế điện hóa quyết định khả năng phản ứng của kim loại kiềm với nước. Cho bảng giá trị sau:
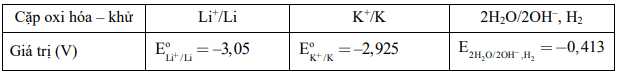
Khi cho potassium và lithium vào trong nước. Nhận định nào sau đây đúng?

Khi cho potassium và lithium vào trong nước. Nhận định nào sau đây đúng?
A, Potassium không phản ứng với nước.
B, Lithium không phản ứng với nước.
C, Potassium phản ứng với nước mạnh hơn lithium.
D, Lithium phản ứng với nước mạnh hơn potassium.
Phân tích các phát biểu:
❌Sai. a. Potassium có thế điện cực chuẩn âm hơn H2O nên có thể phản ứng với H2O tạo H2 và KOH.
❌Sai. b. Lithium có thế điện cực chuẩn âm hơn H2O nên có thể phản ứng với H2O tạo H2 và LiOH.
❌Sai. c. Li+ có thế điện cực chuẩn âm hơn K+ nên phản ứng mạnh hơn.
✔️Đúng. d.(Giải thích giống câu c).
Chọn đáp án D
Đọc thêm: Mặc dù thế điện cực chuẩn của Li+/Li cao hơn của K+/K nhưng trên thực tế potassium phản ứng mạnh với nước hơn so với lithium do năng lượng cần cho sự thuỷ hợp của Li lớn hơn K rất nhiều, hơn nữa sản phẩm LiOH lại là chất tan kém trong nước (so với KOH), sản phẩm này dễ bám vào bề mặt của Li ngăn cản sự tiếp xúc của Li và H2O nên làm giảm tốc độ phản ứng đi nhiều. Theo bảng tuần hoàn, K và Li có cùng chu kỳ và K có Z lớn hơn, vì vậy có khả năng cho e lớp ngoài cùng tốt hơn, ngoài ra K có nhiệt độ nóng chảy thấp (63,65oC so với 180,5oC của Li) nên dễ dàng nóng chảy khi hấp thụ nhiệt toả ra của phản ứng, potassium dạng lỏng này chảy lan ra và làm tăng diện tích bề mặt phản ứng và khiến phản ứng xảy ra dữ dội hơn. Đáp án: C
❌Sai. a. Potassium có thế điện cực chuẩn âm hơn H2O nên có thể phản ứng với H2O tạo H2 và KOH.
❌Sai. b. Lithium có thế điện cực chuẩn âm hơn H2O nên có thể phản ứng với H2O tạo H2 và LiOH.
❌Sai. c. Li+ có thế điện cực chuẩn âm hơn K+ nên phản ứng mạnh hơn.
✔️Đúng. d.(Giải thích giống câu c).
Chọn đáp án D
Đọc thêm: Mặc dù thế điện cực chuẩn của Li+/Li cao hơn của K+/K nhưng trên thực tế potassium phản ứng mạnh với nước hơn so với lithium do năng lượng cần cho sự thuỷ hợp của Li lớn hơn K rất nhiều, hơn nữa sản phẩm LiOH lại là chất tan kém trong nước (so với KOH), sản phẩm này dễ bám vào bề mặt của Li ngăn cản sự tiếp xúc của Li và H2O nên làm giảm tốc độ phản ứng đi nhiều. Theo bảng tuần hoàn, K và Li có cùng chu kỳ và K có Z lớn hơn, vì vậy có khả năng cho e lớp ngoài cùng tốt hơn, ngoài ra K có nhiệt độ nóng chảy thấp (63,65oC so với 180,5oC của Li) nên dễ dàng nóng chảy khi hấp thụ nhiệt toả ra của phản ứng, potassium dạng lỏng này chảy lan ra và làm tăng diện tích bề mặt phản ứng và khiến phản ứng xảy ra dữ dội hơn. Đáp án: C
Câu 29 [679749]: Trong phòng thí nghiệm, kim loại Na được bảo quản bằng cách ngâm trong chất lỏng nào sau đây?
A, Nước.
B, Dầu hỏa.
C, Giấm ăn.
D, Ethanol.
HD: Dầu hoả là các hydrocarbon, không có phản ứng với Na, giúp cách li Na với không khí nên dùng bảo quản Na, còn lại:
❌ A. Nước: 2H2O + 2Na → 2NaOH + H2↑.
❌ C. Giấm ăn: 2CH3COOH + 2Na → 2CH3COONa + H2↑.
❌ D. Ethanol: 2C2H5OH + 2Na → 2C2H5ONa + H2↑.
⟹ Chọn đáp án B Đáp án: B
❌ A. Nước: 2H2O + 2Na → 2NaOH + H2↑.
❌ C. Giấm ăn: 2CH3COOH + 2Na → 2CH3COONa + H2↑.
❌ D. Ethanol: 2C2H5OH + 2Na → 2C2H5ONa + H2↑.
⟹ Chọn đáp án B Đáp án: B
Câu 30 [560802]: Để bảo quản kim loại Na, K người ta ngâm chúng trong dầu hoả. Ngoài yếu tố Na, K không phản ứng với dầu hỏa thì còn một yếu tố quyết định nữa là Na, K có khối lượng riêng
A, Lớn hơn dầu hỏa nên sẽ chìm xuống dưới bề mặt của dầu hỏa.
B, Nhỏ hơn dầu hỏa nên sẽ nổi lên trên bề mặt của dầu hỏa.
C, Nhỏ hơn dầu hỏa nên sẽ chìm xuống dưới bề mặt của dầu hỏa.
D, Lớn hơn dầu hỏa nên sẽ nổi lên trên bề mặt của dầu hỏa.
- Na và K rất dễ phản ứng mạnh với nước và không khí (cụ thể là hơi nước và oxy). Để ngăn cản chúng tiếp xúc với môi trường, người ta ngâm chúng trong dầu hỏa.
- Vì khối lượng riêng của Na, K nặng hơn khối lượng riêng của dầu hỏa, chúng sẽ chìm xuống dưới bề mặt dầu hỏa.
⟹ Chọn đáp án A
Đáp án: A
- Vì khối lượng riêng của Na, K nặng hơn khối lượng riêng của dầu hỏa, chúng sẽ chìm xuống dưới bề mặt dầu hỏa.
⟹ Chọn đáp án A
Đáp án: A
Câu 31 [560803]: Khối lượng riêng của dầu hoả khan khoảng 0,80 g/cm3 và lithium là 0,53 g/cm3. Có thể quan sát được hiện tượng gì khi cho một mẩu lithium vào dầu hoả khan?
A, Mẩu lithium phản ứng tạo thành khí không màu.
B, Mẩu lithium phản ứng tạo thành kết tủa màu trắng.
C, Mẩu lithium không phản ứng và nổi trên mặt lớp dầu hỏa khan.
D, Mẩu lithium không phản ứng và chìm xuống dưới lớp dầu hỏa khan.
- Vì khối lượng riêng của lithium nhỏ hơn khối lượng riêng của dầu hỏa khan, mẩu lithium sẽ nổi trên mặt dầu hỏa khan.
- Trong môi trường dầu hỏa khan, không có nước nên lithium không phản ứng với nước.
⟹ Mẩu lithium không phản ứng và nổi trên mặt lớp dầu hỏa khan.
⟹ Chọn đáp án C Đáp án: C
- Trong môi trường dầu hỏa khan, không có nước nên lithium không phản ứng với nước.
⟹ Mẩu lithium không phản ứng và nổi trên mặt lớp dầu hỏa khan.
⟹ Chọn đáp án C Đáp án: C
Câu 32 [560804]: Tại sao Li không phản ứng với dầu hỏa nhưng không nên bảo quản Li trong dầu hỏa?
A, Li có khối lượng riêng nhỏ hơn dầu hỏa.
B, Li có độ cứng thấp.
C, Li có tính ánh kim.
D, Li có nhiệt độ nóng chảy, nhiệt độ sôi thấp.
Li có khối lượng riêng thấp hơn dầu hỏa, nên nó nổi lên trên dầu hỏa và không phản ứng với dầu hỏa nhưng có thể tham gia phản ứng với oxygen, hơi nước có trong không khí nên không bảo quản trong dầu hỏa.
⟹ Chọn đáp án A
Đáp án: A
⟹ Chọn đáp án A
Đáp án: A
Câu 33 [824948]: Để ngăn ngừa sự hình thành các oxide, peroxide và superoxide, kim loại kiềm đôi khi được bảo quản trong môi trường trơ. Khí nào sau đây không nên dùng để bảo quản lithium
A, Ne.
B, Ar.
C, N2.
D, Kr.
Phân tích các đáp án:
✔️A. Ne. Neon là một khí hiếm, rất trơ và không phản ứng với lithium.
✔️B. Ar. Argon cũng là một khí hiếm, trơ và không phản ứng với lithium.
❌C. N2. Nitrogen là một khí tương đối trơ ở nhiệt độ thường. Tuy nhiên, lithium có khả năng phản ứng trực tiếp với nitrogen để tạo thành lithium nitride : 6Li + N2 ⟶ 2Li3N. Do đó, nitrogen không thích hợp để bảo quản lithium.
✔️D. Kr. Krypton là một khí hiếm, trơ và không phản ứng với lithium.
⟹ Chọn đáp án C
Đáp án: C
✔️A. Ne. Neon là một khí hiếm, rất trơ và không phản ứng với lithium.
✔️B. Ar. Argon cũng là một khí hiếm, trơ và không phản ứng với lithium.
❌C. N2. Nitrogen là một khí tương đối trơ ở nhiệt độ thường. Tuy nhiên, lithium có khả năng phản ứng trực tiếp với nitrogen để tạo thành lithium nitride : 6Li + N2 ⟶ 2Li3N. Do đó, nitrogen không thích hợp để bảo quản lithium.
✔️D. Kr. Krypton là một khí hiếm, trơ và không phản ứng với lithium.
⟹ Chọn đáp án C
Đáp án: C
Câu 34 [560805]: Trong các kim loại sau, kim loại nào thường được dùng làm tế bào quang điện?
A, Na.
B, K.
C, Rb.
D, Cs.
- Cs có khả năng dễ dàng nhả electron khi bị chiếu sáng, có tính năng quang điện tốt.
- Na (Natri), K (Kali) và Rb (Rubidi) không được sử dụng trong các tế bào quang điện chủ yếu vì khó cho electron hơn khi bị chiếu sáng, có tính ổn định kém và hiệu suất kém.
⟹ Chọn đáp án D Đáp án: D
- Na (Natri), K (Kali) và Rb (Rubidi) không được sử dụng trong các tế bào quang điện chủ yếu vì khó cho electron hơn khi bị chiếu sáng, có tính ổn định kém và hiệu suất kém.
⟹ Chọn đáp án D Đáp án: D
Câu 35 [705856]: Cho các phát biểu sau:
(a) Có cấu hình electron lớp ngoài cùng là ns¹ (n > 1).
(b) Có số oxi hoá là +1 hoặc +2 trong các hợp chất.
(c) Có tính khử mạnh.
(d) Có bán kính nguyên tử nhỏ.
(e) Còn được gọi là các kim loại kiềm.
Số phát biểu đúng về các nguyên tố nhóm IA là
(a) Có cấu hình electron lớp ngoài cùng là ns¹ (n > 1).
(b) Có số oxi hoá là +1 hoặc +2 trong các hợp chất.
(c) Có tính khử mạnh.
(d) Có bán kính nguyên tử nhỏ.
(e) Còn được gọi là các kim loại kiềm.
Số phát biểu đúng về các nguyên tố nhóm IA là
A, 1.
B, 2.
C, 3.
D, 4.
Phân tích các đáp án:
✔️(a) – Đúng. Nguyên tố nhóm IA là những nguyên tố s, chỉ có 1 electron hoá trị ở phân lớp ns1 và đứng đầu mỗi chu kì tương ứng.
❌(b) – Sai. trong các phản ứng hoá học, chúng dễ nhường 1 electron, thể hiện tính khử rất mạnh: M ⟶ M+ + 1e .Trong hợp chất, nguyên tử kim loại nhóm IA chỉ thể hiện số oxi hoá +1.
✔️(c) – Đúng. Kim loại nhóm IA là những kim loại hoạt động hoá học mạnh, có tính khử mạnh và tính khử tăng dần từ Li đến Cs.
❌(d) – Sai. Theo định luật tuần hoàn, trong 1 nhóm bán kính các nguyên tố giảm dần theo chiều tăng điện tích hạt, nên các nguyên tố kim loại kiềm đều đứng đầu nhóm nên có bán kính lớn
✔️(e) – Đúng. Các kim loại nhóm IA còn được gọi là kim loại kiềm.
Có 3 đáp án đúng.
⟹ Chọn đáp án C Đáp án: C
✔️(a) – Đúng. Nguyên tố nhóm IA là những nguyên tố s, chỉ có 1 electron hoá trị ở phân lớp ns1 và đứng đầu mỗi chu kì tương ứng.
❌(b) – Sai. trong các phản ứng hoá học, chúng dễ nhường 1 electron, thể hiện tính khử rất mạnh: M ⟶ M+ + 1e .Trong hợp chất, nguyên tử kim loại nhóm IA chỉ thể hiện số oxi hoá +1.
✔️(c) – Đúng. Kim loại nhóm IA là những kim loại hoạt động hoá học mạnh, có tính khử mạnh và tính khử tăng dần từ Li đến Cs.
❌(d) – Sai. Theo định luật tuần hoàn, trong 1 nhóm bán kính các nguyên tố giảm dần theo chiều tăng điện tích hạt, nên các nguyên tố kim loại kiềm đều đứng đầu nhóm nên có bán kính lớn
✔️(e) – Đúng. Các kim loại nhóm IA còn được gọi là kim loại kiềm.
Có 3 đáp án đúng.
⟹ Chọn đáp án C Đáp án: C
Dạng 2: TRẮC NGHIỆM ĐÚNG SAI – mỗi ý a), b), c), d) chọn đúng hoặc sai.
Câu 36 [560825]: Các kim loại nhóm IA và hợp chất của chúng có nhiều ứng dụng trong đời sống.

a. Các kim loại nhóm IA có cấu hình electron lớp ngoài cùng là ns1(với n > 1).
b. Các kim loại nhóm IA có bán kính nguyên tử nhỏ nhất so với cácnguyên tố cùng chu kì.
c. Tính khử giảm dần từ lithium đến ceasium.
d. Các kim loại kiềm có thế điện cực chuẩn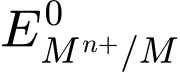 rất nhỏ.
rất nhỏ.

a. Các kim loại nhóm IA có cấu hình electron lớp ngoài cùng là ns1(với n > 1).
b. Các kim loại nhóm IA có bán kính nguyên tử nhỏ nhất so với cácnguyên tố cùng chu kì.
c. Tính khử giảm dần từ lithium đến ceasium.
d. Các kim loại kiềm có thế điện cực chuẩn
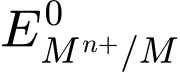 rất nhỏ.
rất nhỏ.
✔️a. Đúng. Các kim loại nhóm IA có cấu hình electron lớp ngoài cùng là ns, với n là số hiệu chu kỳ của nguyên tố.
❌b. Sai. Các kim loại nhóm IA có bán kính nguyên tử lớn hơn các nguyên tố cùng chu kỳ, ngoại trừ lithium.
❌c. Sai. Tính khử tăng dần từ lithium đến cesium vì bán kính nguyên tử tăng lên, làm giảm lực hút giữa hạt nhân và electron ngoài cùng, khiến electron dễ bị mất hơn.
✔️d. Đúng. Các kim loại kiềm có thế điện cực chuẩn (E°) rất nhỏ (thường là âm), phản ánh khả năng dễ bị oxi hóa của chúng.
❌b. Sai. Các kim loại nhóm IA có bán kính nguyên tử lớn hơn các nguyên tố cùng chu kỳ, ngoại trừ lithium.
❌c. Sai. Tính khử tăng dần từ lithium đến cesium vì bán kính nguyên tử tăng lên, làm giảm lực hút giữa hạt nhân và electron ngoài cùng, khiến electron dễ bị mất hơn.
✔️d. Đúng. Các kim loại kiềm có thế điện cực chuẩn (E°) rất nhỏ (thường là âm), phản ánh khả năng dễ bị oxi hóa của chúng.
Câu 37 [560826]: Một số thông số vật lí của kim loại nhóm IA được cho ở bảng dưới đây
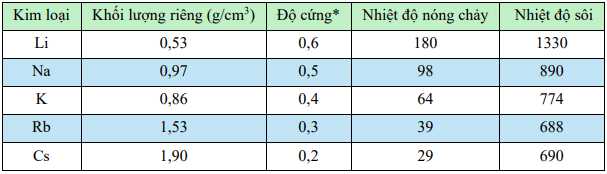
a. Đi từ lithium đến caesium, nhiệt độ nóng chảy giảm dần.
b. Các kim loại nhóm IA đều là kim loại nặng.
c. Các kim loại Li, Na, K, Rb khi phản ứng với nước đều nổi trên bề mặt nước (d = 1,0 g/cm3).
d. Các kim loại nhóm IA đều có độ cứng thấp, dễ dàng dùng dao cắt đượcdo có lực liên kết kim loại yếu.

a. Đi từ lithium đến caesium, nhiệt độ nóng chảy giảm dần.
b. Các kim loại nhóm IA đều là kim loại nặng.
c. Các kim loại Li, Na, K, Rb khi phản ứng với nước đều nổi trên bề mặt nước (d = 1,0 g/cm3).
d. Các kim loại nhóm IA đều có độ cứng thấp, dễ dàng dùng dao cắt đượcdo có lực liên kết kim loại yếu.
✔️a. Đúng. Nhiệt độ nóng chảy của các kim loại nhóm IA giảm dần khi đi từ lithium (Li) đến caesium (Cs).
❌b. Sai. Các kim loại nhóm IA (Li, Na, K, Rb, Cs) là kim loại nhẹ, không phải kim loại nặng.
❌c.Sai. Rb có khối lượng riêng > nước => chìm chứ không nổi trên bề mặt nước
✔️d. Đúng. Các kim loại nhóm IA có độ cứng thấp và dễ cắt vì lực liên kết kim loại giữa các nguyên tử yếu.
❌b. Sai. Các kim loại nhóm IA (Li, Na, K, Rb, Cs) là kim loại nhẹ, không phải kim loại nặng.
❌c.Sai. Rb có khối lượng riêng > nước => chìm chứ không nổi trên bề mặt nước
✔️d. Đúng. Các kim loại nhóm IA có độ cứng thấp và dễ cắt vì lực liên kết kim loại giữa các nguyên tử yếu.
Câu 38 [705409]: Tiến hành cho các kim loại kiềm lithium, sodium, potassium phản ứng với oxygen.
Quy trình tiến hành như sau:
∎ Bước 1: Dùng dao cắt các mẩu kim loại to bằng hạt đậu.
∎ Bước 2: Dùng kẹp lấy mẩu kim loại (Li, Na hoặc K) cho vào muỗng đốt hoá chất (muỗng được xuyên qua một nút cao su). Đốt kim loại trong muỗng trên ngọn lửa đèn cồn và đưa nhanh vào bình tam giác chịu nhiệt chứa khí oxygen.
∎ Bước 3: Đậy nhanh nút cao su gắn với muỗng vào miệng bình tam giác chứa khí oxygen.
Quy trình tiến hành như sau:
∎ Bước 1: Dùng dao cắt các mẩu kim loại to bằng hạt đậu.
∎ Bước 2: Dùng kẹp lấy mẩu kim loại (Li, Na hoặc K) cho vào muỗng đốt hoá chất (muỗng được xuyên qua một nút cao su). Đốt kim loại trong muỗng trên ngọn lửa đèn cồn và đưa nhanh vào bình tam giác chịu nhiệt chứa khí oxygen.
∎ Bước 3: Đậy nhanh nút cao su gắn với muỗng vào miệng bình tam giác chứa khí oxygen.
Phân tích các phát biểu:
✔️ (a) Đúng. Ở nhiệt độ thường hay nhiệt độ cao các kim loại kiềm tác dụng với oxygen tạo oxide base.
✔️ (b) Đúng. Kim loại kiềm hoạt động hóa học rất mạnh và có thể phản ứng với oxygen trong không khí ngay ở nhiệt độ thường.
Khi đốt trên ngọn lửa đèn cồn, phản ứng với oxygen trong không khí sẽ diễn ra trước khi đưa vào bình chứa oxygen nguyên chất.
✔️ (c) Đúng. Cho phần kim loại nóng chảy vào oxygen nguyên chất thì phản ứng mãnh liệt hơn do nồng độ oxygen cao hơn trong không khí dẫn đến phản ứng nhanh hơn.
✔️ (d) Đúng. Kim loại kiềm rất dễ phản ứng với oxygen và hơi nước trong không khí, đặc biệt khi kích thước mẩu kim loại quá nhỏ, diện tích tiếp xúc lớn. Do đó, kim loại có thể phản ứng hết trước khi đưa vào bình chứa khí oxygen.
✔️ (a) Đúng. Ở nhiệt độ thường hay nhiệt độ cao các kim loại kiềm tác dụng với oxygen tạo oxide base.
✔️ (b) Đúng. Kim loại kiềm hoạt động hóa học rất mạnh và có thể phản ứng với oxygen trong không khí ngay ở nhiệt độ thường.
Khi đốt trên ngọn lửa đèn cồn, phản ứng với oxygen trong không khí sẽ diễn ra trước khi đưa vào bình chứa oxygen nguyên chất.
✔️ (c) Đúng. Cho phần kim loại nóng chảy vào oxygen nguyên chất thì phản ứng mãnh liệt hơn do nồng độ oxygen cao hơn trong không khí dẫn đến phản ứng nhanh hơn.
✔️ (d) Đúng. Kim loại kiềm rất dễ phản ứng với oxygen và hơi nước trong không khí, đặc biệt khi kích thước mẩu kim loại quá nhỏ, diện tích tiếp xúc lớn. Do đó, kim loại có thể phản ứng hết trước khi đưa vào bình chứa khí oxygen.
Câu 39 [705725]: Tiến hành cho các kim loại kiềm lithium, sodium, potassium phản ứng với chlorine. Quy trình tiến hành như sau:
∎ Bước 1: Dùng dao cắt các mẩu kim loại to bằng hạt đậu.
∎ Bước 2: Dùng kẹp lấy mẩu kim loại (Li, Na hoặc K) cho vào muỗng đốt hoá chất (muỗng được xuyên qua một nút cao su). Đốt kim loại trong muỗng trên ngọn lửa đèn cồn và đưa nhanh vào bình tam giác chịu nhiệt chứa khí chlorine.
∎ Bước 3: Đậy nhanh nút cao su gắn với muỗng vào miệng bình tam giác chứa khí chlorine.
∎ Bước 1: Dùng dao cắt các mẩu kim loại to bằng hạt đậu.
∎ Bước 2: Dùng kẹp lấy mẩu kim loại (Li, Na hoặc K) cho vào muỗng đốt hoá chất (muỗng được xuyên qua một nút cao su). Đốt kim loại trong muỗng trên ngọn lửa đèn cồn và đưa nhanh vào bình tam giác chịu nhiệt chứa khí chlorine.
∎ Bước 3: Đậy nhanh nút cao su gắn với muỗng vào miệng bình tam giác chứa khí chlorine.
Phân tích các phát biểu:
✔️ a) Đúng. Các kim loại kiềm (Li, Na, K) phản ứng với khí chlorine tạo thành các muối halide tương ứng:
2Li + Cl2 ⟶ 2LiCl
2Na + Cl2 ⟶ 2NaCl
2K + Cl2 ⟶ 2KCl
✔️ b) Đúng. Phản ứng của kim loại kiềm với chlorine là phản ứng tỏa nhiệt mạnh, giải phóng nhiều năng lượng. Do đó, cần dùng bình chịu nhiệt để tránh bị nứt vỡ do nhiệt độ cao.
✔️ c) Đúng. Vai trò của nút cao su không chỉ giúp cố định muỗng đốt mà còn giúp đậy kín bình tam giác, ngăn không cho khí chlorine thoát ra.
✔️ d) Đúng. Trong nhóm IA tính khử của các kim loại kiềm tăng dần nên potassium phản ứng nhanh và mãnh liệt hơn so với lithium và sodium khi tiếp xúc với chlorine.
✔️ a) Đúng. Các kim loại kiềm (Li, Na, K) phản ứng với khí chlorine tạo thành các muối halide tương ứng:
2Li + Cl2 ⟶ 2LiCl
2Na + Cl2 ⟶ 2NaCl
2K + Cl2 ⟶ 2KCl
✔️ b) Đúng. Phản ứng của kim loại kiềm với chlorine là phản ứng tỏa nhiệt mạnh, giải phóng nhiều năng lượng. Do đó, cần dùng bình chịu nhiệt để tránh bị nứt vỡ do nhiệt độ cao.
✔️ c) Đúng. Vai trò của nút cao su không chỉ giúp cố định muỗng đốt mà còn giúp đậy kín bình tam giác, ngăn không cho khí chlorine thoát ra.
✔️ d) Đúng. Trong nhóm IA tính khử của các kim loại kiềm tăng dần nên potassium phản ứng nhanh và mãnh liệt hơn so với lithium và sodium khi tiếp xúc với chlorine.
Câu 40 [704398]: Tiến hành thử nghiệm khả năng phản ứng với nước của các kim loại kiềm (nhóm IA). Quy trình tiến hành như sau:
Chuẩn bị: Kim loại lithium, sodium, potassium, nước, dung dịch phenolphthalein.
▪ Bước 1: Dùng dao cắt các mẩu kim loại to bằng hạt đậu.
▪ Bước 2: Dùng kẹp lấy mẩu kim loại (Li, Na hoặc K) cho vào chậu thuỷ tinh chứa khoảng 1/3 thể tích nước.
▪ Bước 3: Thêm vài giọt dung dịch phenolphthalein vào chậu sau khi kim loại tan hết.
Chuẩn bị: Kim loại lithium, sodium, potassium, nước, dung dịch phenolphthalein.
▪ Bước 1: Dùng dao cắt các mẩu kim loại to bằng hạt đậu.
▪ Bước 2: Dùng kẹp lấy mẩu kim loại (Li, Na hoặc K) cho vào chậu thuỷ tinh chứa khoảng 1/3 thể tích nước.
▪ Bước 3: Thêm vài giọt dung dịch phenolphthalein vào chậu sau khi kim loại tan hết.
Các kim loại nhóm IA phản ứng mạnh với nước, tạo ra dung dịch kiềm và khí hydrogen: 2M + 2H2O ⟶ 2MOH + H2↑.
Mức độ phản ứng của các kim loại điển hình nhóm IA với nước:
☆ Lithium (Li): Phản ứng yếu nhất trong nhóm, sủi bọt nhẹ và tan dần trong nước.
☆ Sodium (Na): Phản ứng mạnh hơn, tạo thành khối cầu, chạy nhanh trên mặt nước do khí hydrogen thoát ra đẩy mẩu kim loại.
☆ Potassium (K): Phản ứng rất mạnh, thường bốc cháy với ngọn lửa màu tím do nhiệt độ sinh ra cao, thậm chí có thể gây nổ.
Phân tích các phát biểu:
✔️ A. Đúng. Mẩu Na phản ứng mạnh với nước, tạo thành khối cầu, chạy nhanh trên mặt nước do khí hydrogen thoát ra đẩy mẩu kim loại.
❌ B. Sai. Khả năng phản ứng với nước tăng dần từ Li đến K nên khả năng phản ứng của K mãnh liệt hơn Li.
✔️ C. Đúng. Phenolphthalein trong cả ba chậu chuyển sang màu hồng vì dung dịch sau phản ứng là kiềm MOH.
✔️ D. Đúng. Từ hiện tượng của thí nghiệm đã phân tích ở trên, có thể kết luận khả năng phản ứng của Li, Na, K với nước tăng dần.
Mức độ phản ứng của các kim loại điển hình nhóm IA với nước:
☆ Lithium (Li): Phản ứng yếu nhất trong nhóm, sủi bọt nhẹ và tan dần trong nước.
☆ Sodium (Na): Phản ứng mạnh hơn, tạo thành khối cầu, chạy nhanh trên mặt nước do khí hydrogen thoát ra đẩy mẩu kim loại.
☆ Potassium (K): Phản ứng rất mạnh, thường bốc cháy với ngọn lửa màu tím do nhiệt độ sinh ra cao, thậm chí có thể gây nổ.
Phân tích các phát biểu:
✔️ A. Đúng. Mẩu Na phản ứng mạnh với nước, tạo thành khối cầu, chạy nhanh trên mặt nước do khí hydrogen thoát ra đẩy mẩu kim loại.
❌ B. Sai. Khả năng phản ứng với nước tăng dần từ Li đến K nên khả năng phản ứng của K mãnh liệt hơn Li.
✔️ C. Đúng. Phenolphthalein trong cả ba chậu chuyển sang màu hồng vì dung dịch sau phản ứng là kiềm MOH.
✔️ D. Đúng. Từ hiện tượng của thí nghiệm đã phân tích ở trên, có thể kết luận khả năng phản ứng của Li, Na, K với nước tăng dần.
Dạng 3: TRẮC NGHIỆM YÊU CẦU TRẢ LỜI NGẮN
Câu 41 [560838]: Khối lượng riêng của một số kim loại kiềm được cho trong bảng sau:
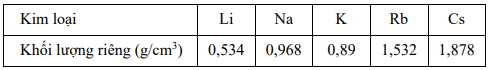
Có bao nhiêu kim loại nổi trên bề mặt của dầu hỏa (d = 0,8 g/cm3)?
Điền đáp án: ..........

Có bao nhiêu kim loại nổi trên bề mặt của dầu hỏa (d = 0,8 g/cm3)?
Điền đáp án: ..........
Nếu khối lượng riêng của kim loại nhỏ hơn khối lượng riêng của dầu hỏa, kim loại đó sẽ nổi trên bề mặt dầu hỏa.
⟹ Chỉ có kim loại Li nổi trên bề mặt dầu hỏa.
⟹ Điền đáp án: 1
⟹ Chỉ có kim loại Li nổi trên bề mặt dầu hỏa.
⟹ Điền đáp án: 1
Câu 42 [560839]: Cho những đặc điểm chung của các kim loại kiềm M như sau:
(a) Kim loại M trong cặp oxi hoá - khử M+/M có thế điện cực chuẩn rất âm.
(b) Mềm và dễ nóng chảy.
(c) Có nhiều electron hoá trị nên dễ dàng nhường electron.
(d) Lực hút của hạt nhân đối với electron hoá trị trong kim loại kiềm yếu hơn so với lực hút tương ứng ở các kim loại nhóm khác.
(đ) Có cấu trúc tinh thể rỗng.
Có bao nhiêu đặc điểm có thể giúp giải thích kim loại kiềm có tính khử mạnh?
Điền đáp án: ..........
(a) Kim loại M trong cặp oxi hoá - khử M+/M có thế điện cực chuẩn rất âm.
(b) Mềm và dễ nóng chảy.
(c) Có nhiều electron hoá trị nên dễ dàng nhường electron.
(d) Lực hút của hạt nhân đối với electron hoá trị trong kim loại kiềm yếu hơn so với lực hút tương ứng ở các kim loại nhóm khác.
(đ) Có cấu trúc tinh thể rỗng.
Có bao nhiêu đặc điểm có thể giúp giải thích kim loại kiềm có tính khử mạnh?
Điền đáp án: ..........
(a)Thế điện cực chuẩn rất âm cho thấy kim loại kiềm dễ bị oxi hóa (nhường electron), do đó đặc điểm này giải thích tính khử mạnh.
→ Phù hợp.
(b)Tính mềm và nhiệt độ nóng chảy thấp là do cấu trúc tinh thể và liên kết kim loại yếu, nhưng không trực tiếp giải thích tính khử mạnh.
→ Không phù hợp.
(c) Kim loại kiềm có một electron hoá trị (ở phân lớp ns), và chính điều này khiến chúng dễ nhường electron. Tuy nhiên, việc nói "nhiều electron hoá trị" không chính xác với kim loại kiềm.
→ Không phù hợp.
(d)Lực hút yếu làm electron hóa trị dễ bị tách ra, điều này giải thích vì sao kim loại kiềm dễ bị oxi hóa và có tính khử mạnh.
→ Phù hợp.
(đ)Cấu trúc tinh thể ảnh hưởng đến tính chất vật lý (như độ mềm), nhưng không trực tiếp giải thích tính khử mạnh.
→ Không phù hợp.
⟹ điền đáp án: 2
→ Phù hợp.
(b)Tính mềm và nhiệt độ nóng chảy thấp là do cấu trúc tinh thể và liên kết kim loại yếu, nhưng không trực tiếp giải thích tính khử mạnh.
→ Không phù hợp.
(c) Kim loại kiềm có một electron hoá trị (ở phân lớp ns), và chính điều này khiến chúng dễ nhường electron. Tuy nhiên, việc nói "nhiều electron hoá trị" không chính xác với kim loại kiềm.
→ Không phù hợp.
(d)Lực hút yếu làm electron hóa trị dễ bị tách ra, điều này giải thích vì sao kim loại kiềm dễ bị oxi hóa và có tính khử mạnh.
→ Phù hợp.
(đ)Cấu trúc tinh thể ảnh hưởng đến tính chất vật lý (như độ mềm), nhưng không trực tiếp giải thích tính khử mạnh.
→ Không phù hợp.
⟹ điền đáp án: 2
Câu 43 [560840]: Kim loại sodium bị xỉn màu trong không khí tạo thành một lớp oxide trên bề mặt của nó. Thấy rằng 0,92 gam sodium kết hợp với 0,32 gam oxygen trong oxide. Trong công thức của oxide này có tổng số nguyên tử là bao nhiêu?
Điền đáp án: ..........
Điền đáp án: ..........
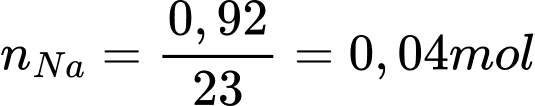
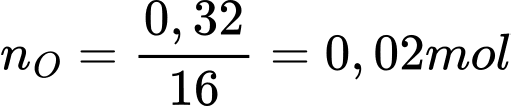
Tỉ lệ mol giữa Na và O là:
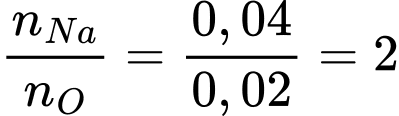
⟹ Công thức của oxide: Na2O
⟹ Tổng số nguyên tử : 2 + 1 = 3
⟹ Điền đáp án: 3
Câu 44 [560841]: Rubidium phản ứng với nước tạo thành rubidium hydroxide và hydrogen. Lấy 8,5 gam rubidium phản ứng hoàn toàn với nước thu được dung dịch có thể tích là 2,5 dm3. Nồng độ của dung dịch rubidium hydroxide (g.dm-3) là bao nhiêu?
Điền đáp án: ..........
Điền đáp án: ..........
Phương trình phản ứng
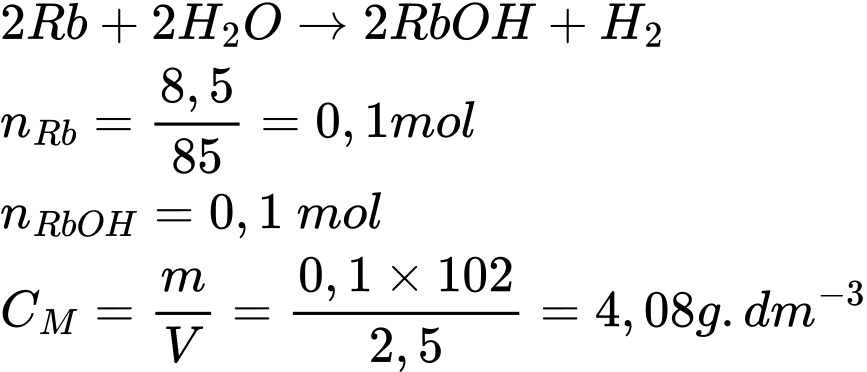
⟹ Điền đáp án: 4,08
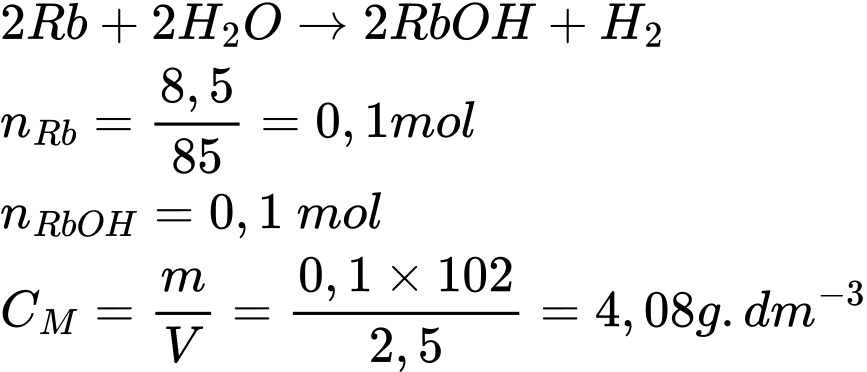
⟹ Điền đáp án: 4,08
Câu 45 [704311]: Các kim loại kiềm có khả năng tác dụng mãnh liệt với oxygen có mặt trong không khí và càng mạnh hơn đối với oxygen tinh khiết. Một nhóm học sinh đã tiến hành các bước thí nghiệm kiểm chứng với ba kim loại kiềm: lithium (Li), sodium (Na) và potassium (K) như sau:
(1) Đốt kim loại trong muỗng trên ngọn lửa đèn cồn thì kim loại sẽ tác dụng với oxygen trong không khí.
(2) Dùng dao cắt các mẩu kim loại to bằng hạt đậu.
(3) Đưa nhanh muỗng chứa kim loại đang cháy vào bình tam giác chịu nhiệt chứa khí oxygen. Đậy nhanh nút cao su gắn với muỗng vào miệng bình tam giác chứa khí oxygen.
(4) Dùng kẹp lấy mẩu kim loại (Li, Na hoặc K) cho vào muỗng đốt hoá chất (muỗng được xuyên qua một nút cao su).
Hãy sắp xếp số thứ tự các bước để thực hiện thí nghiệm theo trình tự dãy bốn số (ví dụ: 1234, 4321, ...).
(1) Đốt kim loại trong muỗng trên ngọn lửa đèn cồn thì kim loại sẽ tác dụng với oxygen trong không khí.
(2) Dùng dao cắt các mẩu kim loại to bằng hạt đậu.
(3) Đưa nhanh muỗng chứa kim loại đang cháy vào bình tam giác chịu nhiệt chứa khí oxygen. Đậy nhanh nút cao su gắn với muỗng vào miệng bình tam giác chứa khí oxygen.
(4) Dùng kẹp lấy mẩu kim loại (Li, Na hoặc K) cho vào muỗng đốt hoá chất (muỗng được xuyên qua một nút cao su).
Hãy sắp xếp số thứ tự các bước để thực hiện thí nghiệm theo trình tự dãy bốn số (ví dụ: 1234, 4321, ...).
Các bước kiểm chứng khả năng tác dụng của kim loại kiềm với oxygen trong không khí và oxygen tinh khiết:
Bước 1: Dùng dao cắt các mẫu kim loại to bằng hạt đậu → ứng với (2)
Bước 2: Dùng kẹp lấy mẫu kim loại (Li, Na hoặc K) cho vào muỗng đốt hóa chất (muỗng được xuyên qua 1 nút cao su) → ứng với (4)
Bước 3: Đốt kim loại trong muỗng trên ngọn lửa đèn cồn thì kim loại tác dụng được với oxygen trong không khí. → ứng với (1)
Bước 4: Đưa nhanh muỗng chứa các kim loại đang cháy vào bình tam giác chịu nhiệt chứa khí oxygen. → ứng với (3)
⇒ Điền đáp án: 2413
Bước 1: Dùng dao cắt các mẫu kim loại to bằng hạt đậu → ứng với (2)
Bước 2: Dùng kẹp lấy mẫu kim loại (Li, Na hoặc K) cho vào muỗng đốt hóa chất (muỗng được xuyên qua 1 nút cao su) → ứng với (4)
Bước 3: Đốt kim loại trong muỗng trên ngọn lửa đèn cồn thì kim loại tác dụng được với oxygen trong không khí. → ứng với (1)
Bước 4: Đưa nhanh muỗng chứa các kim loại đang cháy vào bình tam giác chịu nhiệt chứa khí oxygen. → ứng với (3)
⇒ Điền đáp án: 2413