Dạng 1: TRẮC NGHIỆM KHÁCH QUAN: mỗi câu hỏi chỉ có một đáp án đúng.
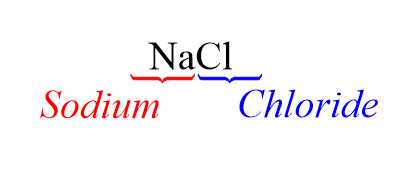
các chất còn lại có tên gọi như sau:
Na2CO3: sodium carbonate
NaHCO3: sodium bicarbonate
KCl: potassium chloride
⇒ Chọn đáp án B Đáp án: B
- Na2SO4 có thể gây mất cân bằng điện giải hoặc kích ứng trong cơ thể khi sử dụng. Nó không có tính chất diệt khuẩn và không phù hợp để duy trì sự ổn định của môi trường sinh lý.
- NaNO3 là một muối nitrat, và muối nitrat có thể tham gia vào các phản ứng tạo ra các hợp chất có thể gây độc hại nếu có mặt trong cơ thể với nồng độ cao.
⟹ NaCl là muối duy nhất trong các lựa chọn này có tính chất tương thích với cơ thể người, giúp duy trì sự cân bằng điện giải (nồng độ ion Na⁺ và Cl⁻ trong cơ thể) và không gây tác dụng phụ.
⟹ Chọn đáp án A Đáp án: A
⤑ Sodium là Na; hydroxide là OH nên sodium hydroxide có công thức là NaOH.
⇒ Chọn đáp án B Đáp án: B
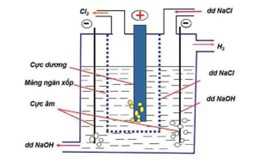
Phương pháp điều chế NaOH trong công nghiệp là Điện phân dung dịch NaCl bão hoà có màng ngăn
⟹ Chọn đáp án C Đáp án: C
Phèn chua là loại muối có tinh thể to nhỏ không đều, không màu hoặc trắng, cũng có thể trong hoặc hơi đục. Phèn chua tan trong nước nhưng không tan trong cồn.
Chọn đáp án D Đáp án: D
Tên của các hợp chất còn lại:
A. KHCO3: Patossium hydrogencarbonate
B. Na2CO3: Sodium carbonate
C. K2CO3: Patossium carbonate
D. NaHCO3: Sodium hydrogencarbonate
⇒ Chọn đáp án D Đáp án: D
Tên các chất còn lại:
A. NaCl: Sodium chloride (hay còn gọi là muối ăn).
B. Na2SO4: Sodium sulfate
C. NaNO3: Sodium nitrate
⟹ Chọn đáp án D Đáp án: D
Loại các đáp án B, C, D vì không có N.
Công thức hóa học của diêm tiêu potassium là KNO3.
⇒ Chọn đáp án A Đáp án: A
⭐ Potassium (K): Thúc đẩy quá trình quang hợp, tăng sức mạnh đề kháng của cây, cải thiện chất lượng và năng suất nông sản.
⭐ Nitrogen (N) dạng nitrate (NO3-): hấp thu dễ dàng và thúc đẩy sự phát triển nhanh chóng của cây.
⇒ Chọn đáp án A Đáp án: A
2NaCl(aq) + 2H2O(1)
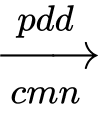 2NaOH(aq) + Cl2(g) + H2(g)
2NaOH(aq) + Cl2(g) + H2(g)Chất nào sau đây không phải là sản phẩm cơ bản của công nghiệp chlorine – kiềm?
B.Khí hydrogen ( H2 )
C.Khí chlorine ( Cl2 )
D.Khí oxygen ( O2 )
⟹ Chọn D vì không có oxygen trong phương trình phản ứng. Đáp án: D
- Khi tan trong nước, Na2CO3 thủy phân tạo ra ion OH⁻, làm cho dung dịch có tính base mạnh.
- Lớp dầu, mỡ là các ester, có thể bị thủy phân trong môi trường base, phá vỡ cấu trúc của chúng và làm sạch bề mặt.
Baking soda (NaHCO3):
- Khi tan trongnước, NaHCO3 chỉ tạo môi trường hơi kiềm, yếu hơn so với Na2CO3. Do đó, khả năng thủy phân dầu, mỡ của NaHCO3 là rất thấp.
⇒ Chọn đáp án A Đáp án: A
 Na2CO3(s) + CO2(g) + H2O(g).
Na2CO3(s) + CO2(g) + H2O(g). Na2O(s) + 2CO2(g) + H2O(g).
Na2O(s) + 2CO2(g) + H2O(g). 2NaHCO3(s).
2NaHCO3(s). Na(s) + CO2(g) + H2O(g).
Na(s) + CO2(g) + H2O(g).⟹ Chọn đáp án A Đáp án: A
- B sai vì sodium có thể phản ứng với một số dung môi hữu cơ, đặc biệt là các dung môi có nhóm chức có thể tương tác với sodium (chẳng hạn như các alcohol hoặc ester).
- C sai vì sodium phản ứng rất mạnh với nước. Khi sodium tiếp xúc với nước.
- D sai vì mục đích sử dụng sodium ở đây là để loại bỏ nước, chứ không phải để phản ứng với chính dung môi hữu cơ.
⟹ Chọn đáp án A. Đáp án: A
Dung dịch NaOH có môi trường bazơ, pH > 7, làm quỳ tím hóa xanh.
Dung dịch KHSO4 có môi trường axit, pH < 7, làm quỳ tím hóa đỏ.
⟹ Chọn đáp án B Đáp án: B
✔️ A. FeCl2 + 2NaOH → Fe(OH)2↓ + 2NaCl.
✔️ B. CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4.
✔️ C. MgCl2 + 2NaOH → Mg(OH)2↓ + 2NaCl.
❌ D. KNO3 + NaOH ⇝ không xảy ra phản ứng.
⟹ Chọn đáp án D Đáp án: D
✔️ CrO3: acidic oxide, phản ứng với NaOH tạo muối tương ứng và nước:
CrO3 + 2NaOH → Na2CrO4 + H2O.
❌❌ Fe và Cr là hai kim loại, không phản ứng với NaOH dù có đun nóng.
✔️ Cr(OH)3: hydroxide lưỡng tính, phản ứng được với cả HCl và NaOH:
Cr(OH)3 + NaOH → NaCrO2 + 2H2O.
⇝ có 2/4 chất thỏa mãn yêu cầu
⇝ Chọn đáp án B Đáp án: B
• HCl + KHCO3 → KCl + CO2↑ + H2O.
⟹ Chọn đáp án A Đáp án: A
Ứng dụng làm thuốc do NaHCO3 có khả năng phản ứng với acid dư trong dạ dày.
⟹ Chọn đáp án B Đáp án: B
⟹ Chọn đáp án D Đáp án: D
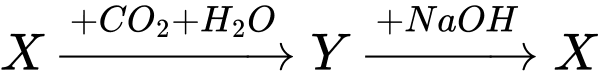
Công thức của X là
Na2CO3 + CO2 + H2O → 2NaHCO3.
NaHCO3 + NaOH → Na2CO3 + H2O.
Đáp án: D
- 2NaOH + CuCl2 → Cu(OH)2↓ + 2NaCl
- 3NaOH + AlCl3 → Al(OH)3↓ + 3NaCl; NaOH + Al(OH)3 → NaAlO2 + 2H2O
- 2NaOH + FeSO4 → Na2SO4 + Fe(OH)2↓
→ Có 3 trường hợp thu được kết tủa
→ Chọn đáp án C
Đáp án: C
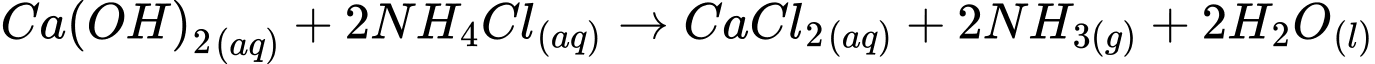
- Calcium chloride (CaCl₂) là sản phẩm chính trong phản ứng này và nó có thể được thải ra trong quá trình Solvay.
Công thức các câu còn lại
- B. Calcium carbonate : CaCO3.
- C. Calcium oxide: CaO.
- D. Calcium hydrogencarbonate: Ca(HCO3)2.
⟹ Chọn đáp án A. Đáp án: A
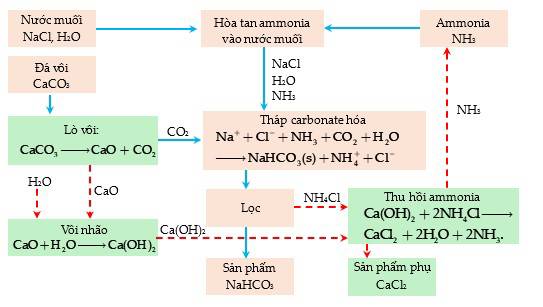
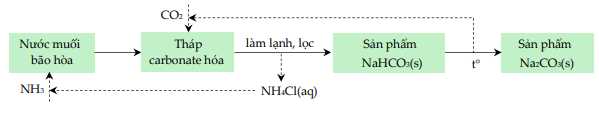
- Ammonia (NH3): Tham gia vào phản ứng với nước muối để tạo ra ammonia và ammonium bicarbonate, một bước quan trọng trong quá trình Solvay.
- Đá vôi (CaCO3): Được sử dụng để tạo ra calcium carbonate (CaCO3) và calcium oxide (CaO) trong quá trình.
- B,C sai vì carbon dioxide ( CO2) là sản phẩm tạo ra trong quá trình.
- D sai vì sodium hydrogencarbonate ( NaHCO3) và calcium oxide ( CaO )
⟹ Chọn đáp án A. Đáp án: A
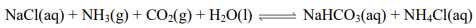
Khi làm lạnh dung dịch trên, muối bị tách ra khỏi dung dịch là
⟹ Chọn đáp án A. Đáp án: A
⟹ Chọn đáp án A Đáp án: A
⟹ Chọn đáp án B Đáp án: B
- Li : đỏ
- Na: vàng
- K: tím
- Sr: đỏ son
⟹ Chọn đáp án A Đáp án: A
- Ngọn lửa màu tím nhạt: KCl
- Ngọn lửa màu vàng: Na2SO4
- Ngọn lửa màu đỏ tía: LiNO3
⟹ Chọn đáp án: D Đáp án: D
– Dung dịch chất X và chất Y đều làm dung dịch phenolphthalein chuyển sang màu hồng.
– Trộn X và Y thu được kết tủa màu trắng.
– Chất X cháy với ngọn lửa màu lục trên đèn khí, trong khi chất Y cháy với ngọn lửa màu tím.
Biết mỗi chất X, Y đều chỉ chứa một loại cation và một loại anion. Phát biểu nào sau đây không đúng?
⟹ Cả X và Y đều có tính base, chứa nhóm OH-
Trộn X và Y thu được kết tủa màu trắng: Phản ứng tạo kết tủa cho thấy có sự kết hợp của cation và anion từ X và Y tạo thành chất không tan.
⟹ có khả năng chứa ion CO32- và SO42-
Tuy nhiên ion CO32- có khả năng :
CO32- + H2O ⟶ HCO3- + OH-
Tạo môi trường base làm đổi màu quỳ tím.
X cháy với ngọn lửa màu lục: Điều này cho thấy X chứa ion (Ba2+).
Y cháy với ngọn lửa màu tím: Điều này cho thấy Y chứa ion (K+).
⟹ Chứa 4 ion K+, Ba2+ , CO32- , OH-
Phân tích các đáp án:
✔️A. ĐÚNG. Phù hợp với kết quả thí nghiệm về màu ngọn lửa.
✔️B. ĐÚNG. Vì X chứa Ba2+ và có tính base (làm phenolphthalein chuyển màu hồng), nên X phải là một base của barium, ví dụ như Ba(OH)2 hoặc BaCO3, không thể là BaCl2 (muối trung tính).
❌C. SAI. Y chứa K+ và có tính base, nhưng không nhất thiết phải là K2CO3. Y có thể là KOH hoặc một base khác của potassium.
✔️D. ĐÚNG. Vì X chứa Ba2+, nên kết tủa tạo thành khi trộn X và Y phải chứa barium.
⟹ Chọn đáp án C Đáp án: C
Có ba ống nghiệm chứa riêng biệt: dung dịch soda, dung dịch lithium chloride, dung dịch potassium carbonate. Với mỗi dung dịch, nhúng đầu dây platinum vào rồi đem đốt trên ngọn lửa đèn khí. Chọn đáp án đúng về hiện tượng thu được tại mỗi thí nghiệm.
- Dung dịch lithium chloride (LiCl): Thành phần chính chứa ion Li+. Khi đốt, ngọn lửa phát ra ánh sáng màu đỏ thẫm đặc trưng của ion Li+.
- Dung dịch potassium carbonate (K2CO3): Thành phần chính chứa ion K+.
Khi đốt, ngọn lửa phát ra ánh sáng màu đỏ tím đặc trưng của ion K+.
⟹ Có thể dựa vào màu ngọn lửa để nhận biết ba dung dịch: soda, lithium chloride, potassium carbonate.
⟹ Chọn đáp án D Đáp án: D
Dạng 2: TRẮC NGHIỆM ĐÚNG SAI – mỗi ý a), b), c), d) chọn đúng hoặc sai.
a. Dịch dạ dày của người bị dư acid có pH thấp.
b. NaHCO3 có tính lưỡng tính nên phản ứng được với ion H+.
c. Khi sử dụng NaHCO3 thì nồng độ H+giảm, từ đó giá trị pH giảm.
d. Các bọt khí sinh ra trong quá trình phản ứng là khí CO2.
✔️b. Đúng. NaHCO3 có thể phản ứng với ion H⁺ (acid) để tạo ra CO2, nước và muối. Đây là lý do tại sao NaHCO3 được dùng để trung hòa acid dạ dày.
❌c. Sai. Khi NaHCO3 phản ứng với acid (H+), nó làm tăng pH, vì NaHCO3 trung hòa acid, làm giảm nồng độ ion H+, do đó pH tăng lên chứ không giảm.
✔️d. Đúng. Khi NaHCO3 phản ứng với acid, khí CO2 sinh ra, và ion H⁺ trong dịch dạ dày bị giảm, dẫn đến tăng pH.
a. Khi cho lithium vào nước sẽ tạo thành lithium hydroxide và khíhydrogen.
b. Dung dịch thu được sau phản ứng có pH < 7.
c. Trong phản ứng với nước, lithium đóng vai trò là chất khử, đã nhậnthêm 1 electron.
d. Thay lithium bằng postassium thấy phản ứng xảy ra mãnh liệt hơn.Điều này cho thấy thế điện cực chuẩn
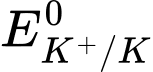 <
< 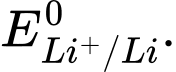
✔️ a. Đúng: Khi lithium (Li) phản ứng với nước (H2O), phản ứng tạo ra lithium hydroxide (LiOH) và khí hydrogen (H2) theo phương trình:
❌ c. Sai: Trong phản ứng này, lithium (Li) đóng vai trò là chất khử, nó mất electron, không nhận electron.
❌ d. Sai: Khi thay lithium bằng potassium (K), phản ứng xảy ra mạnh mẽ hơn. Chứng tỏ thế điện cực của K+/K < Li+/Li. Tuy nhiên, thực tế thế điện cực của Li+/Li = -3,040V < K+/K = -2,924V.
a. Sodium bị hoà tan nhanh chóng là do hiện tượng ăn mòn điện hoá.
b. Cốc nước chuyển từ không màu sang màu hồng.
c. Khí thoát ra trong thí nghiệm là một khí dễ cháy.
d. Nếu thay mẩu sodium bằng mẩu lithium cùng kích thước thì phản ứngdiễn ra chậm hơn.
✔️d. Đúng: Tính khử tăng dần từ Li đến Cs, nên khi thay mẩu sodium bằng lithium, phản ứng sẽ diễn ra chậm hơn.

a. Từ thí nghiệm trên có thể dự đoán các kim loại kiềm đều tham gia phảnứng mãnh liệt với nước ở nhiệt độ thường.
b. Phương trình tổng quát của phản ứng diễn ra trong thí nghiệm như sau:2M + 2H2O → 2MOH + H2.
c. Thí nghiệm trên cho thấy tính khử giảm dần từ Li đến K.
d. Cho quỳ tím vào ba dung dịch sau phản ứng thì quỳ tím đều chuyển hồng.
Điều này chứng tỏ kim loại kiềm tham gia phản ứng mạnh với nước.
❌ c. Sai. Tính khử của các kim loại kiềm tăng dần từ Li đến K. Do tốc độ phản ứng tăng dần từ Li đến K.
❌ d. Sai. Khi cho quỳ tím vào các dung dịch hydroxide của kim loại kiềm (NaOH, KOH,...), quỳ tím sẽ chuyển màu xanh, chứng tỏ các dung dịch này có tính base.
a. Sau khi kim loại tan hết các dung dịch thu được sau phản ứng đều cómàu hồng.
b. Trong nước, potassium tan nhanh hơn so với sodium, sodium tan nhanhhơn so với lithium.
c. Các cặp oxi hoá – khử M+/M (M: Li, Na, K) đều có giá trị thế điện cựcchuẩn lớn hơn giá trị thế điện cực của cặp oxi hoá – khử 2H2O/ H2, 2OH–.
d. Kết quả thí nghiệm cho kết luận tính khử của các kim loại tăng dần theo dãy K, Na, Li.
✔️ b. Đúng. Potassium (K) tan nhanh hơn sodium (Na), và sodium tan nhanh hơn lithium (Li) khi tiếp xúc với nước, vì tính phản ứng của chúng tăng dần từ Li → Na → K.
❌ c. Sai. Các cặp oxi hoá-khử của Li, Na, K (M+/M) có thế điện cực chuẩn lần lượt là: Li+/Li: -3.04 V; Na+/Na: -2.71 V; K+/K: -2.93 V .
❌ d. Sai. Tính khử của các kim loại trong nhóm này tăng dần từ Li, Na đến K.
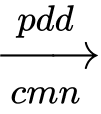 2NaOH(aq) + Cl2(g) + H2(g).
2NaOH(aq) + Cl2(g) + H2(g).a. Anion Cl–bị khử thành khí chlorine tại anode.
b. Tại cathode, thu được sodium hydroxide.
c. Nếu không có màng ngăn xốp, nước Javel được hình thành trong bìnhđiện phân.
d. Hydrogen cũng là một sản phẩm có giá trị của công nghiệp chlorine –kiềm.
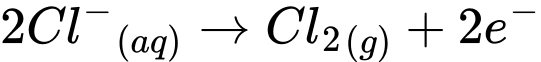
✔️b. Đúng. Tại cathode, nước (H2O) bị khử thành khí hydro (H2) theo phương trình:
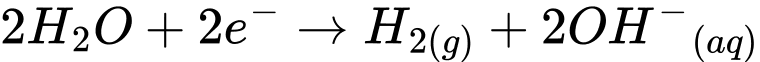
Sodium hydroxide (NaOH) là sản phẩm được tạo thành trong dung dịch do OH- kết hợp với Na+.
✔️c. Đúng. Nếu không có màng ngăn xốp, các sản phẩm chlorine (Cl2) và sodium hydroxide (NaOH) có thể phản ứng với nhau để tạo ra nước Javel, chứa hypochlorite (NaClO), theo phương trình:
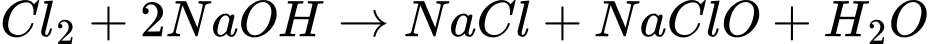
✔️d. Đúng. Hydrogen (H2) là một sản phẩm phụ có giá trị trong quá trình điện phân, thường được thu ở cathode và có nhiều ứng dụng công nghiệp.
Độ tan của NaHCO3 ở t1 = 20 °C và ở t2 = 40 °C lần lượt là 9,6 g/100 g nước và 12,7 g/100 g nước.
a. Đá vôi đóng vai trò cung cấp CO2 cho quá trình Solvay.
b. Phương trình hóa học chuyển hóa NaHCO3 thành Na2CO3 là: 2NaHCO3 (s)
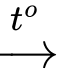 Na2CO3(s) + CO2(g) + H2O(g)
Na2CO3(s) + CO2(g) + H2O(g)c. Quy trình điều chế theo sơ đồ trên có thể tái chế NH3 và CO2.
d. Khi giảm nhiệt độ của 225,4 gam dung dịch NaHCO3 bão hoà từ t2 về t1 thì khối lượng muối NaHCO3 kết tinh là 2,83 gam.
✔️ b. Đúng: Phương trình phản ứng đúng là:
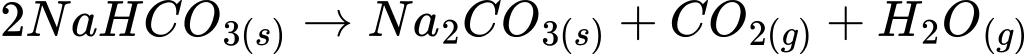
Đây là phản ứng phân hủy nhiệt của NaHCO₃.
✔️ c. Đúng: Quy trình Solvay có thể tái chế ammonia (NH3) để giảm thiểu chi phí và tài nguyên. Trong quá trình này, NH3 được sử dụng để tạo ra amoniac trong dung dịch, sau đó có thể được thu hồi và tái sử dụng.
❌ d. Sai. Khi giảm nhiệt độ của 225,4 gam dung dịch NaHCO3 bão hoà từ t2 về t1 thì khối lượng muối NaHCO3 kết tinh là 6,2 gam.
Lượng NaHCO3 bão hoà trong 225,4 g dung dịch ở 40 oC là:
(225,4. 12,7): (100 + 12,7) = 25,40 (g).
Gọi x là lượng bị tách ra khỏi dung dịch, ta có:
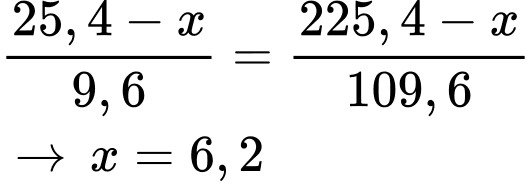
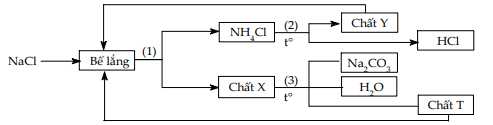
a. Chất X, Y, T lần lượt là NaHCO3, CO2, NH3.
b. Trong sơ đồ trên hai hóa chất được tái sử dụng là chất T và chất Y.
c. Phương trình phản ứng ở (1) là NaCl + NH3 + CO2 + H2O → NaHCO3 + NH4Cl.
d. Nguyên liệu ban đầu cần dùng duy nhất trong quy trình Solvay là NaCl.
- CO2 (chất T): Được sử dụng trong các bước để tạo NaHCO3.
- NH3 (chất Y): Được tái sử dụng sau các phản ứng.
❌ a. Sai. Chất X,Y,T lần lượt là NaHCO3, NH3, CO2.
✔️b.Đúng. Hai hóa chất được tái sử dụng là chất T và chất Y
- NH3 (chất Y) được tái sử dụng và CO2 (chất T)
✔️c.Đúng. Phương trình phản ứng (1) là
NaCl + NH3 + CO2 + H2O ⟶ NaHCO3 + NH4Cl.
❌ d. Sai. Nguyên liệu ban đầu cần duy nhất trong quy trình Solvay là NaCl. Ngoài NaCl, quy trình còn cần CO2 và NH3 từ bên ngoài, không chỉ dựa duy nhất vào NaCl.
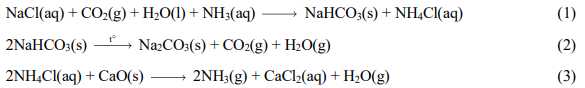
a. Phản ứng (1) cho thấy H2CO3 (CO2 + H2O) có tính acid mạnh hơndung dịch HCl.
b. Muối sodium hydrogencarbonate ít tan trong nước và kém bền khi bịnung nóng.
c. Phản ứng (3) nhằm thu hồi và tái sử dụng NH3.
d. Trong phản ứng (2) khối lượng chất rắn giảm 45% sau khi nung (giảsử hiệu suất nung là 100%).
✔️b. Đúng. NaHCO3 ít tan trong nước và dễ bị phân hủy khi nung để tạo Na2CO3, CO2, H2O
✔️c. Đúng. Phản ứng này tái sinh NH3, giúp tiết kiệm và duy trì chu trình sản xuất.
❌d. Sai. Tính toán cho thấy khối lượng giảm khoảng 37%, không phải 45%.

Tỉ lệ khối lượng ban đầu và sau phản ứng: 2. 84g = 106g
Khối lượng giảm =
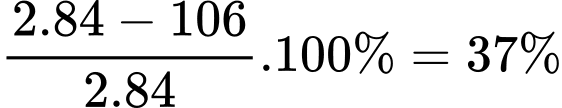

a. Quá trình hình thành muối NaHCO3 từ các đơn chất thuận lợi về nănglượng hơn so với quá trình hình thành muối Na2CO3 từ các đơn chất.
b. Giá trị biến thiên enthalpy chuẩn của phản ứng2NaHCO3(s) → Na2CO3(s) + H2O(l) + CO2(g) là –91,28 kJ.
c. Phản ứng Na2CO3(s) → Na2O(s) + CO2(g) không thuận lợi về mặtnăng lượng.
d. Muối Na2CO3 có độ bền nhiệt cao hơn muối NaHCO3.
❌b. Sai. Giá trị biến thiên enthalpy chuẩn của phản ứng là 91,58 kJ
✔️c. Đúng. Na2CO3 không thuận lợi về mặt năng lượng.
Δf Ho 298 = Δf Ho Na2O + Δf Ho CO2 - Δf Ho Na2CO3
= - 414,2 + (-393,51) - (-1130,7) = 322,99 kJ > 0
⟶ Không thuận lợi về mặt năng lượng
✔️d. Đúng. Dựa vào giá trị Δf Ho , ta thấy quá trình hình thành Na2CO3 tỏa ra nhiều nhiệt hơn, tức là Na2CO3 bền hơn NaHCO3. Khi đun nóng, chất kém bền hơn (NaHCO3) sẽ phân hủy trước.
■ Bước 1: Nhúng đầu que đốt bằng platinum đã được rửa sạch bằng nước vào dung dịch lithium chloride nồng độ khoảng 25% rồi đưa lên ngọn lửa đèn khí.
■ Bước 2: Thực hiện thao tác tương tự đối với mỗi dung dịch sodium chloride 25% và dung dịch potassium chloride 25%.
Phân tích các phát biểu:
✔️ a) Đúng. Que nhúng vào dung dịch lithium chloride sẽ cháy với ngọn lửa màu đỏ tía.
✔️ b) Đúng. Platinum (Pt) ở dạng tinh khiết, không bị oxi hóa ở bất cứ nhiệt độ nào. Kim loại này khó bị ăn mòn, chịu được nhiệt độ cao nên được dùng để làm que đốt.
❌ c) Sai. Các kim loại kiềm tự do cũng như hợp chất của chúng khi bị đốt sẽ cháy cho ngọn lửa có màu đặc trưng nên nếu thay NaCl bằng NaNO3 thì que nhúng vào dung dịch vẫn sẽ cháy với ngọn lửa màu vàng chứ không phải màu tím.
✔️ d) Đúng. Các kim loại kiềm tự do cũng như hợp chất của chúng khi bị đốt sẽ cháy cho ngọn lửa có màu đặc trưng nên có thể nhận biết riêng từng cation kim loại
Dạng 3: TRẮC NGHIỆM YÊU CẦU TRẢ LỜI NGẮN
Cho các chất sau:
(1) Potassium iodide.
(2) Sodium iodide.
(3) Sodium phosphate.
(4) Potassium phosphate.
(5) Sodium chloride.
(6) Potassium chloride.
Có bao nhiêu chất X thỏa mãn thí nghiệm trên?
Điền đáp án: ..........
Chất X thỏa mãn phải đảm bảo 2 điều kiện:
1, tạo kết tủa vàng với AgNO3 => Dung dịch X phải chứa gốc phosphate hoặc gốc iodide => loại chất (5), (6) do tạo kết tủa trắng khi phản ứng với dung dịch AgNO3
2, X cháy với ngọn lửa màu vàng trong đèn khí => X phải là hợp chất của kim loại Na => loại các chất (1), (4)
Vậy có 2 chất thỏa mãn
⟹ Điền đáp án: 2
(1) Đưa que đốt bằng platinum đã nhúng dung dịch lên ngọn lửa đèn khí.
(2) Chuẩn bị dung dịch các muối lithium chloride, sodium chloride, potassium chloride nồng độ khoảng 25%.
(3) Quan sát màu ngọn lửa để phân biệt màu sắt đặc trưng của các muối ion kim loại kiềm.
(4) Nhúng đầu que đốt bằng platinum đã được rửa sạch bằng nước vào các dung dịch muối.
Hãy sắp xếp số thứ tự các bước để thực hiện quy trình phân biệt các ion kim loại kiềm và sắp xếp theo trình tự dãy bốn số (ví dụ: 1234, 4321, ...).
Bước 1: Chuẩn bị:
Chuẩn bị dung dịch các muối lithium chloride, sodium chloride, potassium chloride nồng độ khoảng 25% → ứng với (2)
Bước 2: Lấy dung dịch muối để chuẩn bị đốt:
Nhúng đầu que đốt bằng platinum đã được rửa sạch (do Pt trơ về mặt hóa học) bằng nước vào các dung dịch muối. → ứng với (4)
Bước 3: Thực hiện đốt:
Đưa que đốt bằng platinum đã nhúng dung dịch muối lên ngọn lửa đèn khí → ứng với (1)
Bước 4: Quan sát:
Quan sát màu ngọn lửa để phân biệt màu sắc đặc trưng của các muối ion kim loại kiềm. → ứng với (3)
⇒ Điền đáp án: 2413
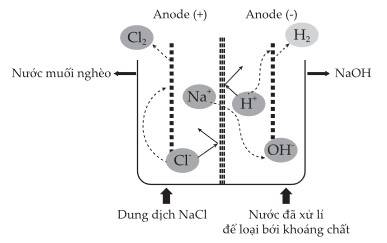
Khối lượng NaCl đã bị điện phân : 300 – 220 = 80g
nNaCl = m : M = 80 : 58,5 = nNaOH
⟹ m NaOH = n.M = 80/58,5 × 40 × 80% = 43,7606...≈ 43,8g
⟹ Điền đáp án: 43,8
Điền đáp án: ..........
- Nồng độ của dung dịch NaHCO3 bão hoà ở 20oC là: (9,6) / (9,6 + 100) = 1200/137 (%)
- Nồng độ của dung dịch NaHCO3 bão hoà ở 40oC là: (12,7 / 12,7 + 100) = 12700/1127 (%)
⟹ Khối lượng muối NaHCO3 có trong 112,7 gam dung dịch NaHCO3 bão hoà ở 40oC là: 112,7 . (12700/1127)(%) = 12,7 (g)
- Giả sử khối lượng NaHCO3 tách ra là x gam.
- Khối lượng muối còn lại là: 12,7 - x (g)
- Khối lượng dung dịch còn lại là: 112,7 - x (g)
Lượng muối tách ra vừa đủ để khiến cho dung dịch về đến 20 độ C đạt đến trạng thái bão hoà nên nồng độ của dung dịch sau khi làm lạnh xuống 20 độ C bằng 1200/137 (%)
⟹ (12,7 - x) / (112,7 - x) = 1200/137 (%) ⟹ x = 3,1
⟹ Điền đáp án: 3
Điền đáp án: ..........
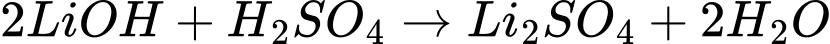

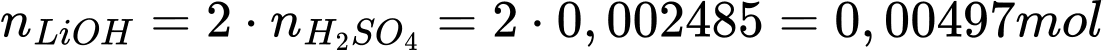
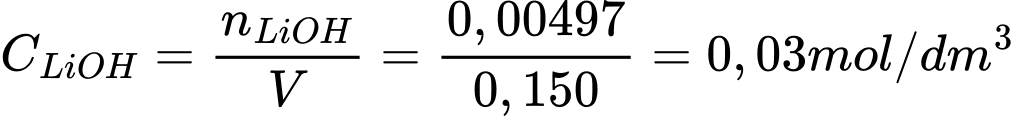
Điền đáp án: 0,03

Điền đáp án: ..........
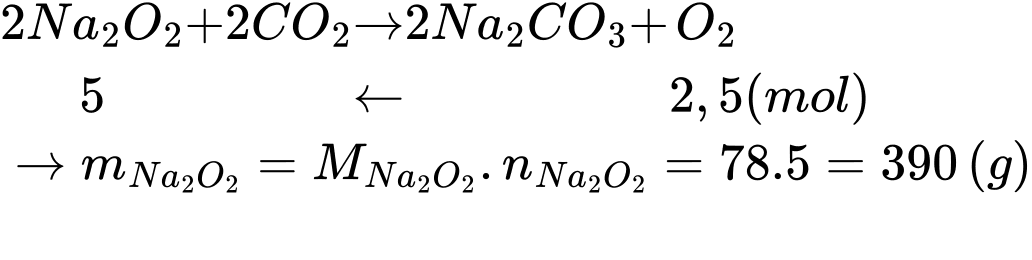
⇒ Điền đáp án: 390
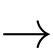 NaOH (aq) có giá trị là bao nhiêu kJ?
NaOH (aq) có giá trị là bao nhiêu kJ?(Làm tròn đến giá trị nguyên).
Điền đáp án: ..........
- Khối lượng của 20 mL nước là m = V × D = 20 × 1 = 20 gam.
Lượng nhiệt nước nhận được trong quá trình
hòa tan:
Q = m × ∆T × C = 20 × (34,6 – 25) × 4,184 = 803,328 J.
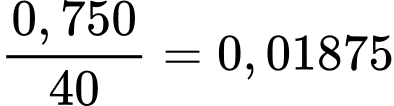 molNaOH rắn giải phóng nhiệt lượng là 803,328 J.
molNaOH rắn giải phóng nhiệt lượng là 803,328 J.⟹ 1 mol NaOH rắn giải phóng
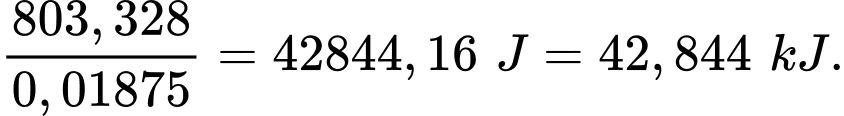
⟹ Điền đáp án: 42,8
Điền đáp án: ..........
Số mol của HCl là nHCl = 0,025 . 1 = 0,025 mol.
Số mol của NaOH là nNaOH = 0,025 . 1 = 0,025 mol.
HCl và NaOH phản ứng với nhau vừa đủ.
Ta có: NaOH(aq) + HCl(aq) NaCl(aq) + H2O(l).
0,025 mol 0,025 mol 0,025 mol
Thể tích dung dịch sau phản ứng là V = 50,0 mL.
mdung dịch = 50 gam (giả thiết khối lượng riêng của dung dịch là 1,00 g/cm3).
Q = m × C × ΔT = 50,0 × 4,18 × (29,3 – 22,7) = 1379,4 J.
Ta thấy cứ tạo thành 0,025 mol H2O thì lượng nhiệt thay đổi là –1379,4J (do phản ứng trên là phản ứng tỏa nhiệt).
Vậy lượng nhiệt cần thiết cho quá trình tạo thành 1 mol H2O là –1379,4 : 0,025 = –55176 J.
⟹ Điền đáp án: -55176
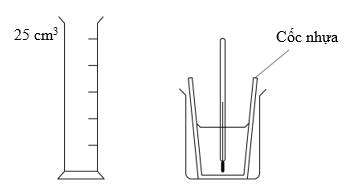

 khối lượng 1 cm3 của nước là 1 gam.
khối lượng 1 cm3 của nước là 1 gam.Điền đáp án: ..........
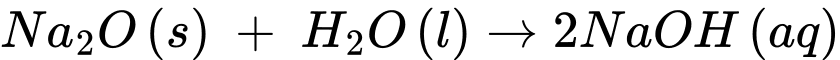
Biết rằng khối lượng 1 cm3 của nước là 1 gam
Đổi 50 cm3 = 50 gam
Nhiệt năng (Q) tỏa ra trong thí nghiệm này là:
Q = m . Delta T . C = 50. 4,2.(30,5 - 19,5 ) = 2310 J
⇒ Điền đáp án: 2310
NaCl(s) + H2SO4(l) + MnO2(s) → Na2SO4(s) + MnCl2(aq) + H2O(l) + Cl2(g)
Giá trị biến thiên enthalpy cho phản ứng trên là bao nhiêu kJ?. Biết enthalpy tạo thành chuẩn của các chất được cho trong bảng sau:
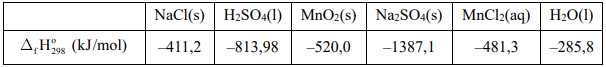
Điền đáp án: ..........
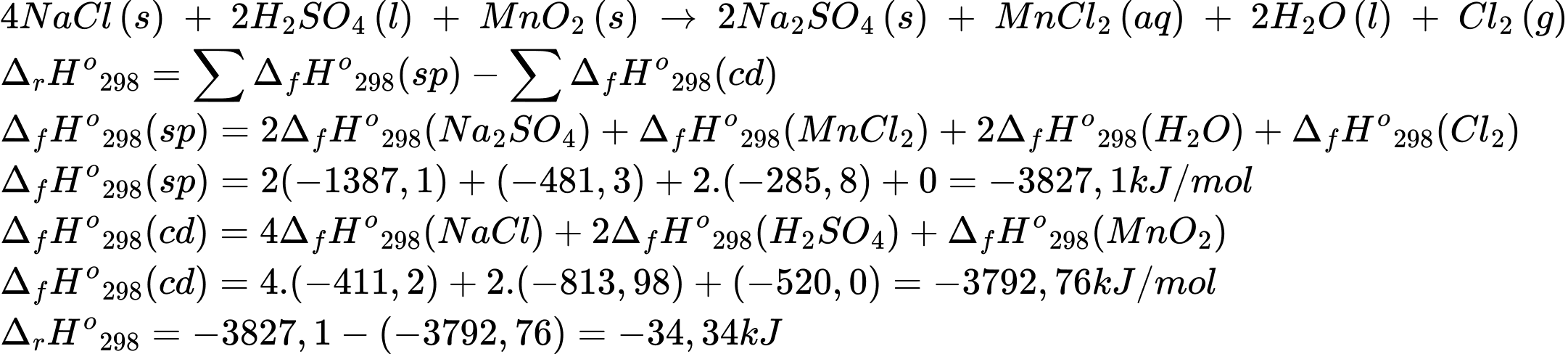
Giá trị biến thiên enthalpy cho phản ứng trên là 34,3kJ
Điền đáp án: 34,3
(Làm tròn kết quả đến hàng phần chục)
Điền đáp án: ..........
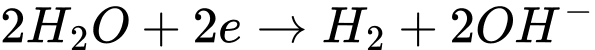
Phản ứng tại cực dương ( anode):
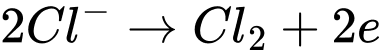
Q= I.t = 0,81.150 = 121,5 C
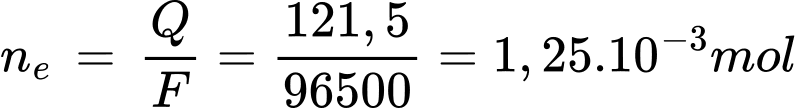
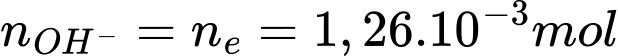
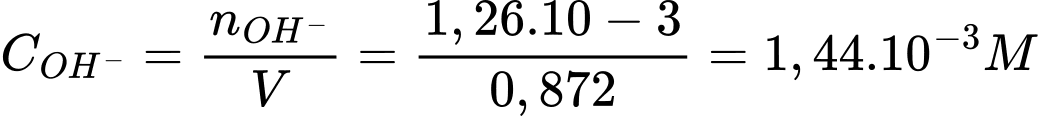
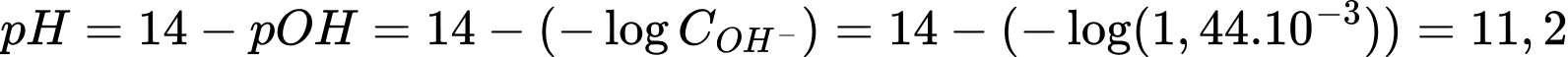
Điền đáp án: 11,2
(Làm tròn kết quả đến hàng phần chục)
Điền đáp án: ..........
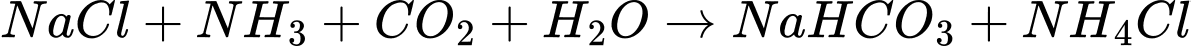
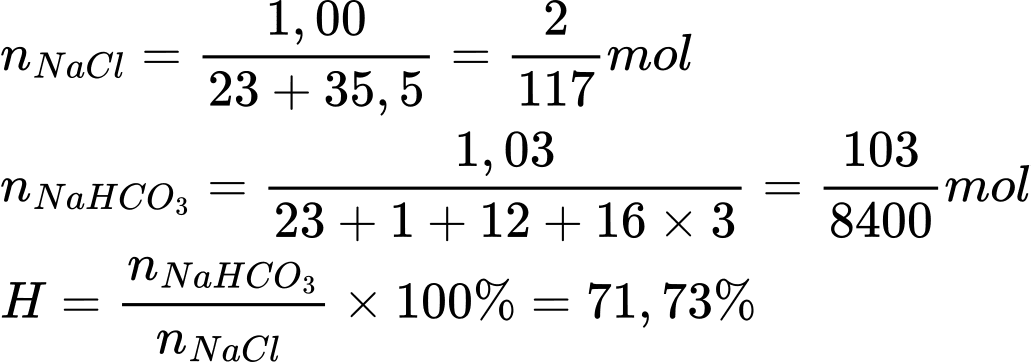
Điền đáp án: 71,7
Điền đáp án: ..........
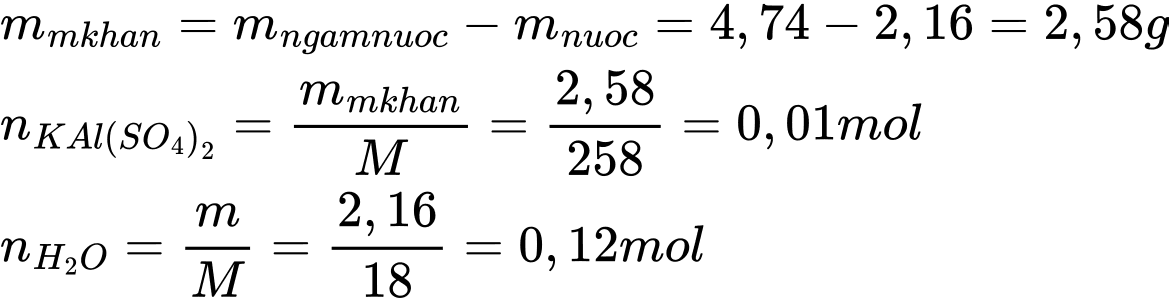
Trong công thức KAl(SO4)2⋅xH2O, số mol H2O tỉ lệ với số mol KAl(SO4)2
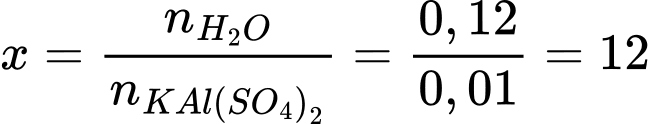
Công thức của hợp chất ngậm nước là KAl(SO4)2.12H2O
Điền đáp án: 12
2NaHCO3(s)
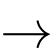 Na2CO3(s) + CO2(g) + H2O(g)
Na2CO3(s) + CO2(g) + H2O(g)Đun nóng 1,7184 g mẫu NaHCO3 không tinh khiết thu được 0,196 g CO2. Phần trăm khối lượng của NaHCO3 trong mẫu ban đầu là bao nhiêu?
Điền đáp án: ..........
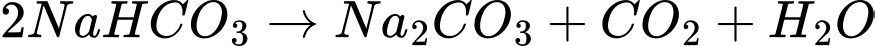
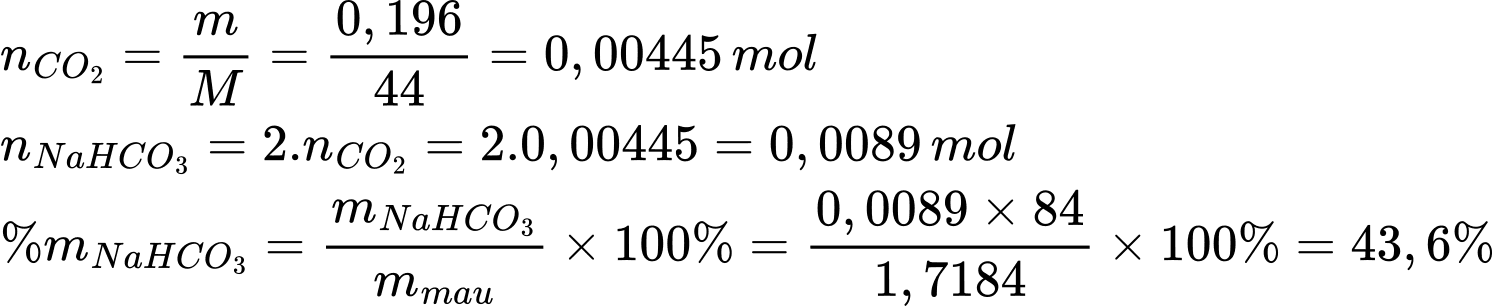
Điền đáp án: 43,6
I2(aq) + 2S2O32–(aq)
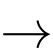 2I–(aq) + S4O62–(aq)
2I–(aq) + S4O62–(aq)Hòa tan 3,232 g mẫu chất không tinh khiết chứa Na2S2O3 vào nước để tạo thành 100 mL dung dịch X. Nếu bạn sử dụng hết 40,21 mL dung dịch I2 0,246 M trong phép chuẩn độ 100 mL X thì phần trăm khối lượng của Na2S2O3 trong 3,232 g mẫu chất không tinh khiết là bao nhiêu?
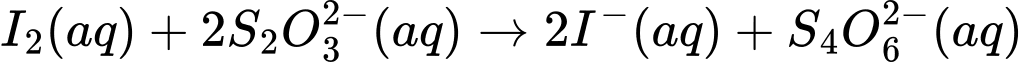
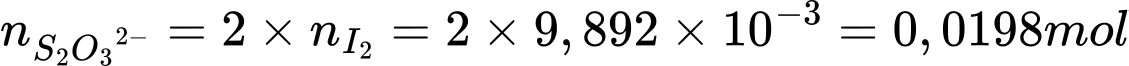
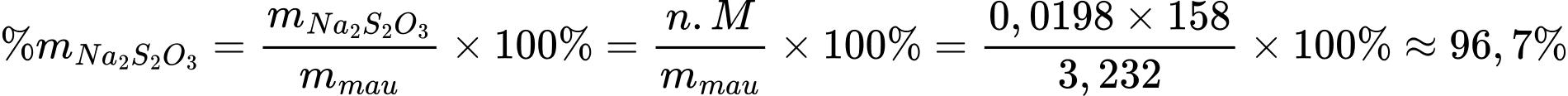
⟹ Điền đáp án: 96,7
CsOH(aq) + HCl(aq)
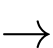 CsCl(aq) + H2O(l)
CsCl(aq) + H2O(l)Nhiệt độ của dung dịch trước khi trộn là 22,50 °C và sau khi trộn là 24,28 °C. Biến thiên enthalpy chuẩn của phản ứng là bao nhiêu kJ trên mỗi mol CsOH? Giả sử khối lượng riêng của dung dịch là 1,00 g/mL và nhiệt dung riêng của các dung dịch là 4,2 J/g.K.
Điền đáp án: ..........
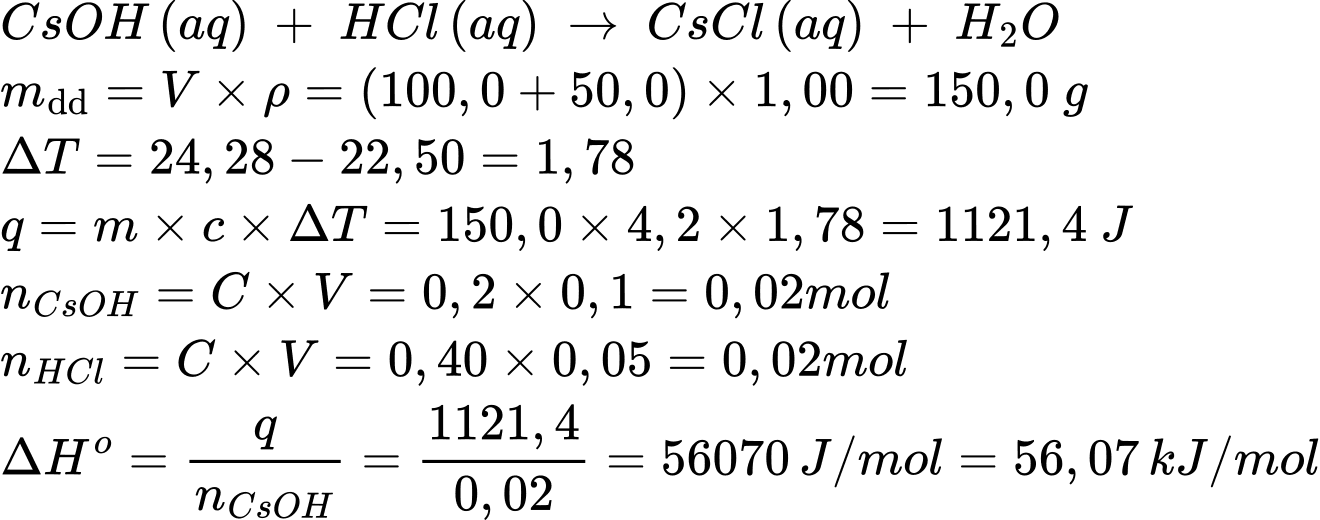
Vì phản ứng là tỏa nhiệt nên delta H>0
Điền đáp án: -56,1
Bước 1: Cân 30 gam “muối i-ốt” rồi hòa tan trong nước cất thu được 100 mL dung dịch X đựng trong bình nón 250 mL (có nút nhám) thêm dung dịch KI 1 M (dư), dung dịch H2SO4 1 M.
5KIO3 + KI + 3H2SO4
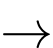 3K2SO4 + 3I2 + 3H2O
3K2SO4 + 3I2 + 3H2OBước 2: Đậy nắp và lắc nhanh mẫu, để mẫu yên tĩnh nơi tối 5 phút. Sau 5 phút, thêm 1 mL dung dịch hồ tinh bột 1%, rồi đem chuẩn độ chậm (4 giây một giọt) bằng dung dịch Na2S2O3 0,005 M tới khi mất màu thì thể tích dung dịch Na2S2O3 đã dùng là 11,0 mL.
I2 + 2Na2S2O3
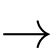 2NaI + Na2S4O6
2NaI + Na2S4O6Tính hàm lượng iodine (mg/kg muối) trong KIO3 của mẫu “muối i-ốt” trên (làm tròn đến số nguyên).
(2) 2Na2S2O3 + I2 → Na2S4O6 + 2NaI
Đổi 11 mL = 0,011 L
Số mol Na2S2O3 đã phản ứng là nNa2S2O3 = 0,011.0,005 = 5,5.10-5 mol
Số mol I2 = nNa2S2O3 : 2 = 2,75×10−5 mol
Từ PTHH (1) và (2) số mol của KIO3 là 4,583×10−5 mol
Hàm lượng iodine trong muối trên là:
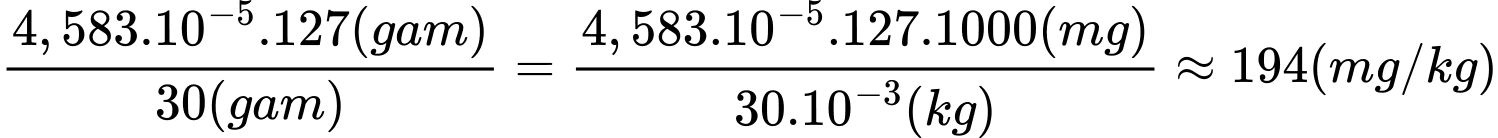
⟹Điền đáp án : 194
Dạng 4: BÀI TẬP ĐỌC HIỂU – đọc thông tin và trả lời các câu hỏi sau đó
Lithium chloride (LiCl) và potassium chloride (KCl) đặc biệt giống với sodium chloride về hình thức và mùi vị, và cả hai đều được sử dụng làm chất thay thế muối cho những người có chế độ ăn ít sodium. Khi bạn ăn một bữa ăn có lượng muối quá cao hoặc tiêu thụ quá nhiều muối trong một ngày, sẽ gây ra cảm giác đầy hơi do thận không thể lọc hết lượng sodium dư thừa ra khỏi máu. Dư thừa sodium sẽ dẫn tới tăng huyết áp, dẫn đến tai biến mạch máu não, nhồi máu cơ tim và nhiều bệnh tim mạch khác.
Lithium chloride được sử dụng trong thời gian ngắn như một chất thay thế muối vào những năm 1940, tuy nhiên nó tỏ ra nguy hiểm và việc sử dụng nó đã dẫn đến các trường hợp nhiễm độc lithium nghiêm trọng, trong đó có một số trường hợp gây tử vong. Ngày nay, các chất thay thế muối như chất thay thế muối Morton và Nu-Salt sẽ có chứa potassium chloride.

Sr là kim loại nhóm IIA
=> Chọn đáp án C Đáp án: C
=> Chọn đáp án B Đáp án: B
Khối lượng NaCl trong sản phẩm thay thế = 0,75x
Khối lượng NaCl ban đầu là 100 kg và toàn bộ được sử dụng để tạo ra sản phẩm thay thế.
0,75.x=100 => x =133 kg
=> Chọn đáp án C Đáp án: C

Do lo ngại của Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ, lithium đã bị loại bỏ khỏi 7UP vào đầu những năm 1950. Gần như cùng lúc đó, các bác sĩ tâm thần phát hiện ra rằng các ion lithium có tác dụng chữa bệnh đáng chú ý đối với tình trạng tâm thần gọi là rối loạn lưỡng cực. Những người mắc chứng rối loạn tâm thần này sẽ trải qua những thay đổi tâm trạng nghiêm trọng từ hưng phấn đến trầm cảm sâu sắc. Ion lithium làm dịu những thay đổi tâm trạng này, cho phép bệnh nhân lưỡng cực hoạt động hiệu quả hơn trong cuộc sống hàng ngày.
Vì quá liều lithium có thể gây ra tác dụng phụ nghiêm trọng ở người, bao gồm suy thận và tử vong, nên muối lithium không được chấp thuận làm thuốc chống loạn thần cho người cho đến năm 1970. Ngày nay Li+ thường được dùng qua đường uống dưới dạng Li2CO3, đây là hoạt chất trong thuốc kê đơn. Thuốc lithium có hiệu quả đối với khoảng 70% bệnh nhân lưỡng cực dùng thuốc.
Trong thời đại công nghệ sinh học và thiết kế thuốc phức tạp này, ion lithium đơn giản vẫn là phương pháp điều trị hiệu quả nhất cho chứng rối loạn tâm thần tàn khốc. Điều đáng chú ý là dù đã nghiên cứu chuyên sâu nhưng các nhà khoa học vẫn chưa hiểu hết tác dụng sinh hóa dẫn đến tác dụng chữa bệnh của lithium. Do tương tự như Na+, Li+ được tích hợp vào huyết tương, nơi nó có thể ảnh hưởng đến hoạt động của các tế bào thần kinh và cơ. Nhưng Li+ có bán kính nhỏ hơn Na+, nên cách Li+ tương tác với các phân tử trong tế bào người khác với cách Na+ tương tác với các phân tử.
=> Chọn đáp án A Đáp án: A
=> Chọn đáp án C Đáp án: C
Khi đi xuống trong cùng một nhóm, số lớp electron tăng, dẫn đến kích thước ion tăng.
=> Chọn đáp án C Đáp án: C
Dạng 5: CÂU HỎI TỰ LUẬN
∎ Thí nghiệm 1: Cho một mẫu (A) nặng 1,287 g phản ứng với lượng dư hydrochloric acid thì có 111,555 mL khí giải phóng (đo ở điều kiện chuẩn).
∎ Thí nghiệm 2: Phân hủy một mẫu (B) khác nặng 0,715 g bởi 50 mL sulfuric acid 0,2 M. Sau khi phân hủy hoàn toàn, cần 150 mL dung dịch sodium hydroxide 0,1 M để trung hòa acid dư.
a) Viết phương trình hóa học cho các thí nghiệm.
b) Xác định thành phần của hai mẫu soda (Na2CO3) kết tinh hydrate A và B.
Na2CO3.xH2O + 2HCl ⟶ 2NaCl + H2O + CO2
Đổi 111,555 mL = 0,111555L
Số mol của CO2 là: nCO2 = 0,111555 ÷ 24,79 =0,0045 mol
Theo phương trình: nNa2CO3 = nCO2 = 0,0045 mol.
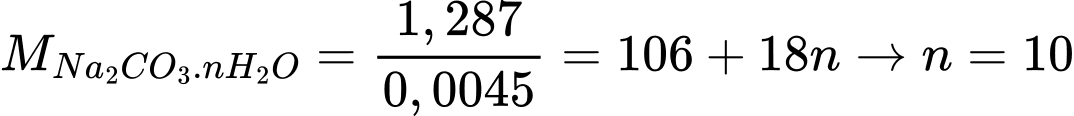
⭐Thí nghiệm 2: Phương trình phản ứng:
Đổi 50 mL = 0,05 L; 150 mL = 0,15 L
(1) Na2CO3 + H2SO4 → Na2SO4 + H2O + CO2
(2) 2NaOH + H2SO4 → Na2SO4 + 2H2O
Số mol của H2SO4 là nH2SO4 = 0,2 × 0,05 = 0,01 mol
Số mol của NaOH phản ứng với H2SO4 dư là:
nH2SO4 = 0,15 × 0,1 = 0,015 mol
Số mol H2SO4 phản ứng với NaOH là nH2SO4 = 0,0075 mol
Số mol H2SO4 phản ứng với Na2CO3 là nH2SO4 = 0,01 – 0,0075 = 0,0025 mol
Số mol của Na2CO3 là nNa2CO3 = 0,0075 mol
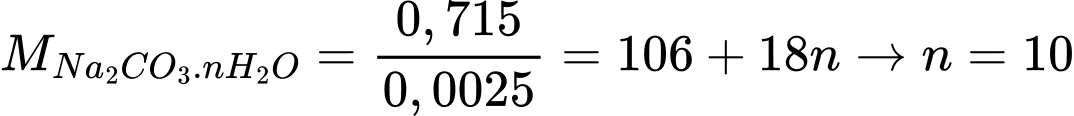
b. Hai mẫu soda (Na2CO3) có thành phần muối kết tinh giống nhau: Na2CO3.10H2O.
∎ Bước 1: Cân khối lượng của bình cân rỗng.
∎ Bước 2: Cân khối lượng của một bình cân chứa X2CO3.
∎ Bước 3: Chuyển 50,0 mL hydrochloric acid 2 M (dư) vào bình hình nón dung tích 250 mL.
∎ Bước 4: Thêm sodium carbonate vào trong bình nón chứa acid để làm bão hòa carbon dioxide tan trong dung dịch.
∎ Bước 5: Đặt một nút bông gòn vào cổ bình nón và cân bình nón (chứa acid).
∎ Bước 6: Thêm X2CO3 vào bình nón chứa acid và nhanh chóng đậy nút bông gòn vào cổ bình.
∎ Bước 7: Khi phản ứng trong bình dừng lại, để yên bình trong 10 phút để carbon dioxide khuếch tán ra khỏi bình. Đo khối lượng của bình nón chứa hỗn hợp sau phản ứng.

Các kết quả cân khối lượng được cho trong bảng sau:

a) Viết các phương trình hóa học cho thí nghiệm.
b) Theo tính toán, kết quả nguyên tử khối của kim loại X gần nhất với nguyên tử khối của kim loại kiềm nào?
c) Tại sao phải cho Na2CO3 phản ứng với acid HCl trước X2CO3?
X2CO3 + 2HCl → 2XCl + CO2↑ + H2O
Khối lượng muối là:
mbình cân + X2CO3 – mbình rỗng = 14,29 – 11,48 = 2,81 (gam)
Gọi khối lượng khí thoát ra là x (gam)
Áp dụng định luật bảo toàn khối lượng:
mbình nón + mdd acid + mmuối = mbình nón + mdd sau phản ứng + mCO2
⇔ 221,35 + 2,81 = 223,21 + x
→ x = 0,95 (gam)
Từ phương trình hóa học
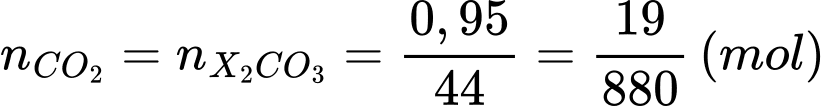
→
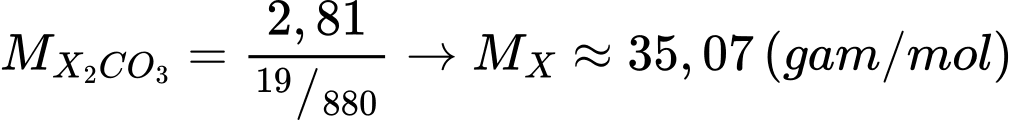
→ Phân tử khối của X (35,07) gần nhất với potassium (39) nên X có khả năng là potassium.
c. Cho Na2CO3 phản ứng trước với HCl mục đích để tạo môi trường bão hòa CO2 trong dung dịch acid.