Dạng 1: TRẮC NGHIỆM KHÁCH QUAN: mỗi câu hỏi chỉ có một đáp án đúng.
Câu 1 [706035]: Các kim loại kiềm thổ có cấu hình electron lớp ngoài cùng là?
A, ns1.
B, ns2.
C, ns2np1.
D, ns2np2.
Cấu hình electron lớp ngoài cùng của nguyên tố nhóm IIA là ns2.
Kim loại nhóm IIA thể hiện tính khử mạnh:
M ⟶ M2+ + 2e
Trong hợp chất, nguyên tử nhóm IIA thể hiện số oxi hoá đặc trưng là +2.
⟹Chọn đáp án B Đáp án: B
Kim loại nhóm IIA thể hiện tính khử mạnh:
M ⟶ M2+ + 2e
Trong hợp chất, nguyên tử nhóm IIA thể hiện số oxi hoá đặc trưng là +2.
⟹Chọn đáp án B Đáp án: B
Câu 2 [243433]: Nguyên tố calcium có số hiệu nguyên tử là 20. Khi calcium tham gia phản ứng tạo hợp chất ion thì cấu hình electron của cation là
A, 1s22s22p63s23p64s1.
B, 1s22s22p6.
C, 1s22s22p63s23p6.
D, 1s22s22p63s23p63d10.
Nguyên tố calcium có số hiệu nguyên tử là 20 nên khi tham gia phản ứng sẽ có xu hướng nhường đi 2 electron để đạt cấu hình của nguyên tử khí hiếm gần nhất là Argon (Z = 18), tạo thành cation Ca2+.
→ Cấu hình electron của cation Ca2+ là: 1s22s22p63s23p6.
⇒ Chọn đáp án C Đáp án: C
→ Cấu hình electron của cation Ca2+ là: 1s22s22p63s23p6.
⇒ Chọn đáp án C Đáp án: C
Câu 3 [575649]: Cấu hình electron của nguyên tử calcium là 1s22s22p63s23p64s2. Vị trí của calcium trong bảng tuần hoàn là
A, ô số 20, chu kì 4, nhóm IIA.
B, ô số 18, chu kì 3, nhóm VA.
C, ô số 2, chu kì 4, nhóm IIA.
D, ô số 22, chu kì 3, nhóm IIIA.
Cấu hình electron của calcium 1s2 2s2 2p6 3s2 3p6 4s2:
- Calcium có 20e → Số hiệu nguyên tử là 20 → Ô thứ 20 trong bảng tuần hoàn.
- Calcium có 4 lớp 4 → Thuộc chu kì 4.
- Calcium thuộc nguyên tố s, có 2 electron lớp ngoài cùng → Thuộc nhóm IIA
⇒ Chọn đáp án A Đáp án: A
- Calcium có 20e → Số hiệu nguyên tử là 20 → Ô thứ 20 trong bảng tuần hoàn.
- Calcium có 4 lớp 4 → Thuộc chu kì 4.
- Calcium thuộc nguyên tố s, có 2 electron lớp ngoài cùng → Thuộc nhóm IIA
⇒ Chọn đáp án A Đáp án: A
Câu 4 [243436]: Nguyên tử magnesium có cấu hình electron là: 1s22s22p63s2. Sau khi tạo liên kết ion, điện tích của ion magnesium là
A, 2+.
B, 2.
C, 2–.
D, 3+.
Nguyên tử magnesium có 12 electron nên khi tham gia liên kết có xu hướng nhường đi 2 electron để đạt cấu hình của nguyên tử nguyên tố khí hiếm gần nhất là neon (Z = 10), tạo thành cation Mg2+.
⇒ Chọn đáp án A Đáp án: A
⇒ Chọn đáp án A Đáp án: A
Câu 5 [233243]: Kim loại nào sau đây là kim loại kiềm thổ?
A, Ag.
B, Cu.
C, Ca.
D, Na.
Mẹo: "Bé Mang Cá Sang Bà Rán" ⇄ Be Mg Ca Sr Ba Rn.
⇒ Kim loại kiềm thổ xuất hiện trong 4 phương án là Ca (canxi).
⟹ Chọn đáp án C Đáp án: C
⇒ Kim loại kiềm thổ xuất hiện trong 4 phương án là Ca (canxi).
⟹ Chọn đáp án C Đáp án: C
Câu 6 [60057]: Hai kim loại đều thuộc nhóm IIA trong bảng tuần hoàn là
A, Sr, K.
B, Be, Al.
C, Ca, Ba.
D, Na, Ba.
Phân tích các đáp án:
❌A. Sr, K: Sr thuộc nhóm IIA, K thuộc nhóm IA.
❌B. Be, Al: Be thuộc nhóm IIA, Al thuộc nhóm IIIA.
✔️C. Ca, Ba đều thuộc nhóm IIA.
❌D. Na, Ba: Na thuộc nhóm IA, Ba thuộc nhóm IIA.
⟹ Chọn đáp án C Đáp án: C
❌A. Sr, K: Sr thuộc nhóm IIA, K thuộc nhóm IA.
❌B. Be, Al: Be thuộc nhóm IIA, Al thuộc nhóm IIIA.
✔️C. Ca, Ba đều thuộc nhóm IIA.
❌D. Na, Ba: Na thuộc nhóm IA, Ba thuộc nhóm IIA.
⟹ Chọn đáp án C Đáp án: C
Câu 7 [703943]: Trong cơ thể người, sự thiếu hụt nguyên tố nào sau đây có thể gây ra bệnh loãng xương?
A, Barium.
B, Magnesium.
C, Beryllium.
D, Calcium.
Canlcium là thành phần chính của xương và răng, đóng vai trò quan trọng trong việc duy trì cấu trúc xương nên sự thiếu hụt canlcium (Ca) trong cơ thể có thể gây ra bệnh loãng xương.
⇒ Chọn đáp án D Đáp án: D
⇒ Chọn đáp án D Đáp án: D
Câu 8 [705829]: Calcium là nguyên tổ kim loại đóng vai trò thiết yếu cho việc phát triển cơ thể động vật, đồng thời góp phần duy trì hoạt động của cơ bắp, truyền dẫn thần kinh, tăng cường khả năng miễn dịch,... Trong cơ thể người, phần lớn lượng calcium tập trung ở
A, xương, răng.
B, máu.
C, cơ bắp.
D, tóc, móng.
Khoảng 99% lượng calcium trong cơ thể người tập trung ở xương và răng, đóng vai trò chính trong việc duy trì cấu trúc và độ cứng. Chỉ 1% còn lại tồn tại trong máu, cơ và dịch ngoại bào, tham gia vào các quá trình sinh lý quan trọng
Chọn đáp án A Đáp án: A
Chọn đáp án A Đáp án: A
Câu 9 [61786]: Quặng dolomite bao gồm các chất
A, CaO và BaO.
B, CaCO3 và BaCO3.
C, MgCO3 và CaCO3.
D, BaCO3 và MgCO3.
HD: Quặng dolomite bao gồm MgCO3 và CaCO3.
⟹ Chọn đáp án C
Đáp án: C
⟹ Chọn đáp án C
Đáp án: C
Câu 10 [61754]: Trong các khoáng vật dưới đây, khoáng vật nào không chứa CaCO3?
A, Calcite.
B, Dolomite.
C, Đá hoa.
D, Magnesite.
HD: Thành phần chính của các khoảng vật:
✔️ A. Calcite: CaCO3.
✔️ B. Dolomite: CaCO3.MgCO3.
✔️ C. Đá hoa: CaCO3.
❌ D. Magnesite: MgCO3.
⇒ Chọn đáp án D Đáp án: D
✔️ A. Calcite: CaCO3.
✔️ B. Dolomite: CaCO3.MgCO3.
✔️ C. Đá hoa: CaCO3.
❌ D. Magnesite: MgCO3.
⇒ Chọn đáp án D Đáp án: D
Câu 11 [560889]: Vì sao các khoáng vật calcite, dolomite,... hầu như không tan trong nước?

Một mẫu khoáng vật calcite ở vùng Balkal, Nga

Một mẫu khoáng vật calcite ở vùng Balkal, Nga
A, Vì khoáng vật calcite, dolomite chứa muối carbonate không tan.
B, Vì khoáng vật calcite, dolomite chứa muối hydrogencarbonate không tan.
C, Vì khoáng vật calcite, dolomite chứa muối nitrate không tan.
D, Vì khoáng vật calcite, dolomite chứa muối chlorine không tan.
- Khoáng vật calcite có thành phần chủ yếu là CaCO3.
- Khoáng vật dolomite có thành phần chủ yếu là MgCO3.CaCO3.
- Mà CaCO3 và MgCO3 đều không tan trong nước.
⟶ Các khoáng vật calcite, dolomite,... hầu như không tan trong nước.
Chọn đáp án A Đáp án: A
- Khoáng vật dolomite có thành phần chủ yếu là MgCO3.CaCO3.
- Mà CaCO3 và MgCO3 đều không tan trong nước.
⟶ Các khoáng vật calcite, dolomite,... hầu như không tan trong nước.
Chọn đáp án A Đáp án: A
Câu 12 [560890]: Nguyên tố nhóm IIA được tìm thấy trong tự nhiên dưới dạng nào?
(1) Các cation M2+ trong nước ao hồ, nước ngầm.
(2) Các khoáng vật ít tan như carbonate, sulfate, silicate.
(3) Các hợp chất ít tan trong răng, xương động vật.
(1) Các cation M2+ trong nước ao hồ, nước ngầm.
(2) Các khoáng vật ít tan như carbonate, sulfate, silicate.
(3) Các hợp chất ít tan trong răng, xương động vật.
A, (1) và (2).
B, (1) và (3).
C, (1), (2) và (3).
D, (2) và (3).
Nguyên tố nhóm IIA được tìm thấy trong tự nhiên dưới dạng:
(1) Các cation M2+ trong nước ao hồ, nước ngầm.
(2) Các khoáng vật ít tan như carbonate, sulfate, silicate.
(3) Các hợp chất ít tan trong răng, xương động vật.
Chọn đáp án C Đáp án: C
(1) Các cation M2+ trong nước ao hồ, nước ngầm.
(2) Các khoáng vật ít tan như carbonate, sulfate, silicate.
(3) Các hợp chất ít tan trong răng, xương động vật.
Chọn đáp án C Đáp án: C
Câu 13 [560891]: Nhiệt độ nóng chảy của các kim loại nhóm IIA từ Be đến Ba có xu hướng biến đổi như thế nào?
A, Tăng dần.
B, Giảm dần.
C, Không đổi.
D, Không xác định.
Các kim loại nhóm IIA có nhiệt độ nóng chảy cao hơn so với kim loại nhóm IA, nhưng tươngđối thấp so với các kim loại khác.
⟶ Tuy nhiên, nhiệt độ nóng chảy của kim loại trong cùng nhóm IIA biến đổi không theo xuhướng rõ rệt. Ví dụ từ Be đến Mg có nhiệt độ nóng chảy giảm nhưng Mg đến Ca nhiệt độ nóng chảy lại tăng. Sau đó từ Ca đến Sr, Ba thì nhiệt độ nóng chảy giảm.
⟹ Chọn đáp án D Đáp án: D
⟶ Tuy nhiên, nhiệt độ nóng chảy của kim loại trong cùng nhóm IIA biến đổi không theo xuhướng rõ rệt. Ví dụ từ Be đến Mg có nhiệt độ nóng chảy giảm nhưng Mg đến Ca nhiệt độ nóng chảy lại tăng. Sau đó từ Ca đến Sr, Ba thì nhiệt độ nóng chảy giảm.
⟹ Chọn đáp án D Đáp án: D
Câu 14 [560892]: Magnesium là kim loại cơ bản trong hợp kim dùng để chế tạo khung và cánh của các thiết bị bay.

Ứng dụng trên không dựa vào tính chất vật lí nào của hợp kim magnesium?

Ứng dụng trên không dựa vào tính chất vật lí nào của hợp kim magnesium?
A, cứng.
B, bền.
C, nhẹ.
D, ánh kim.
Kim loại Mg có độ bền và nhẹ, khó bị oxi hóa nên được dùng để chế tạo khung và cánh của các thiết bị bay, không liên quan đến tính chất vật lí ánh kim của Mg.
Chọn đáp án D Đáp án: D
Chọn đáp án D Đáp án: D
Câu 15 [560893]: Biểu đồ hình bên thể hiện sự biến đổi một tính chất của các nguyên tố nhóm IIA. Tính chất phù hợp với sự biến đổi trong biểu đồ là
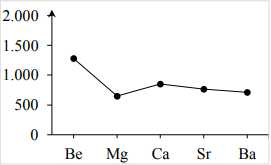

A, độ âm điện.
B, nhiệt độ nóng chảy.
C, bán kính nguyên tử.
D, tính kim loại.
Các kim loại nhóm IIA có nhiệt độ nóng chảy cao hơn so với kim loại nhóm IA, nhưng tương
đối thấp so với các kim loại khác.
➢ Tuy nhiên, nhiệt độ nóng chảy của kim loại trong cùng nhóm IIA biến đổi không theo xu hướng rõ rệt nên được biểu diễn như biểu đồ trên.
Chọn đáp án B Đáp án: B
➢ Tuy nhiên, nhiệt độ nóng chảy của kim loại trong cùng nhóm IIA biến đổi không theo xu hướng rõ rệt nên được biểu diễn như biểu đồ trên.
Chọn đáp án B Đáp án: B
Câu 16 [560894]: Đồ thị nào biểu diễn đúng sự thay đổi nhiệt độ nóng chảy của các kim loại nhóm IIA?
A, 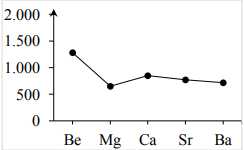

B, 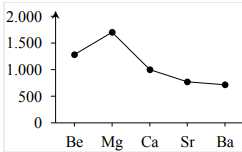

C, 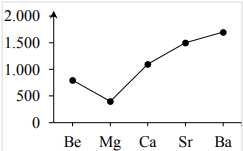

D, 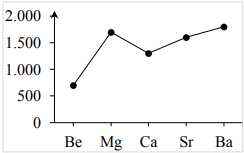

Sự biến đổi nhiệt độ nóng chảy của kim loại nhóm IIA không theo quy luật vì cấu trúc mạng tinh thể của kim loại nhóm IIA khác nhau.
Nên nhiệt độ nóng chảy từ Be đến Ba do sự giảm dần của lực liên kết kim loại khi di chuyển xuống nhóm 2 trong bảng tuần hoàn.
Chọn đáp án A Đáp án: A
Nên nhiệt độ nóng chảy từ Be đến Ba do sự giảm dần của lực liên kết kim loại khi di chuyển xuống nhóm 2 trong bảng tuần hoàn.
Chọn đáp án A Đáp án: A
Câu 17 [560895]: Tính chất hoá học đặc trưng của kim loại nhóm IIA là
A, Tính oxi hóa.
B, Tính khử.
C, Tính acid.
D, Tính base.
Các kim loại nhóm IIA như Be, Mg, Ca, Sr, Ba có xu hướng nhường 2 electron ở lớp ngoài cùng để đạt cấu hình bền vững của khí hiếm:
M ⟶ M2+ + 2e
⇒ Đóng vai trò chất khử trong phản ứng.
⇒ Chọn đáp án B Đáp án: B
M ⟶ M2+ + 2e
⇒ Đóng vai trò chất khử trong phản ứng.
⇒ Chọn đáp án B Đáp án: B
Câu 18 [706127]: Magnesium là kim loại có độ hoạt động hoá học mạnh hơn nhôm (aluminium) thì
A, 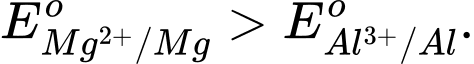
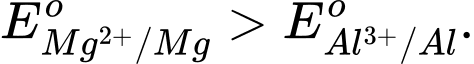
B, 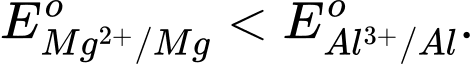
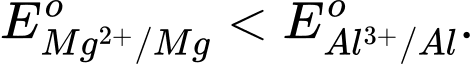
C, 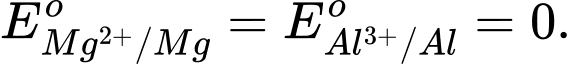
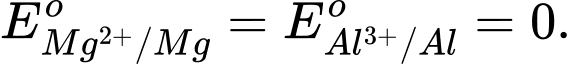
D, 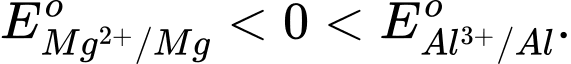
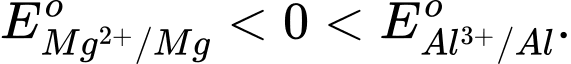
Phân tích các đáp án:
❌ A. Sai. Vì Mg hoạt động hóa học mạnh hơn Al nên thế điện cực chuẩn của Mg phải nhỏ hơn Al.
✔️ B. Đúng. Mg hoạt động hóa học mạnh hơn Al nên thế điện cực chuẩn của Mg nhỏ hơn Al.
❌ C. Sai. Thế điện cực chuẩn của Mg và Al khác 0.
❌ D. Sai. Mặc dù đúng là Mg có tính khử mạnh hơn Al, điều này không có nghĩa là thế điện cực chuẩn của Al luôn dương.
⟹Chọn đáp án B Đáp án: B
❌ A. Sai. Vì Mg hoạt động hóa học mạnh hơn Al nên thế điện cực chuẩn của Mg phải nhỏ hơn Al.
✔️ B. Đúng. Mg hoạt động hóa học mạnh hơn Al nên thế điện cực chuẩn của Mg nhỏ hơn Al.
❌ C. Sai. Thế điện cực chuẩn của Mg và Al khác 0.
❌ D. Sai. Mặc dù đúng là Mg có tính khử mạnh hơn Al, điều này không có nghĩa là thế điện cực chuẩn của Al luôn dương.
⟹Chọn đáp án B Đáp án: B
Câu 19 [560896]: Phương trình hoá học nào sau đây biểu diễn đúng khi cho kim loại Ba tác dụng với khí oxygen?
A, 2Ba(s) + H2O(l) 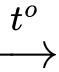 Ba2O(s) + H2(g).
Ba2O(s) + H2(g).
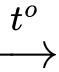 Ba2O(s) + H2(g).
Ba2O(s) + H2(g).B, Ba(s) + 2H2O(l) 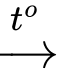 Ba(OH)2(s) + H2(g).
Ba(OH)2(s) + H2(g).
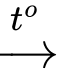 Ba(OH)2(s) + H2(g).
Ba(OH)2(s) + H2(g).C, 2Ba(s) + O2(g) 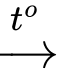 2BaO(s).
2BaO(s).
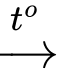 2BaO(s).
2BaO(s).D, 4Ba(s) + O2(g) 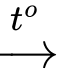 2Ba2O(s).
2Ba2O(s).
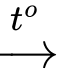 2Ba2O(s).
2Ba2O(s).
Khi kim loại Ba tác dụng với khí oxygen ở điều kiện thường, sản phẩm là barium oxide (BaO).
PTHH:
2Ba(s) + O2(g)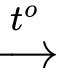 2BaO(s).
2BaO(s).
Chọn đáp án C Đáp án: C
PTHH:
2Ba(s) + O2(g)
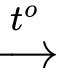 2BaO(s).
2BaO(s).Chọn đáp án C Đáp án: C
Câu 20 [560897]: Lần lượt cho một mẩu Ba và các dung dịch K2SO4, NaHCO3, HNO3 và NH4Cl. Số trường hợp xuất hiện kết tủa là
A, 3.
B, 4.
C, 2.
D, 1.
Trong dung dịch, Ba phản ứng với nước theo phương trình:
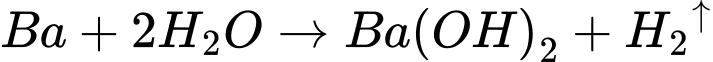
Xét các phản ứng:
✔️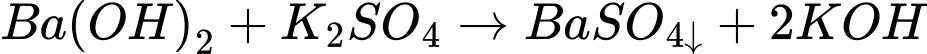
✔️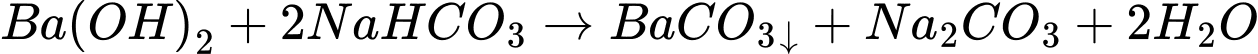
❌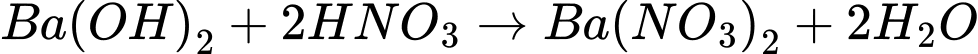
❌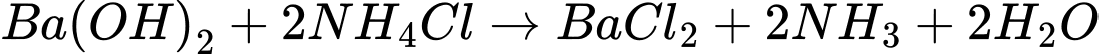
⟹ Có 2 phản ứng tạo kết tủa.
⟹ Chọn đáp án C Đáp án: C
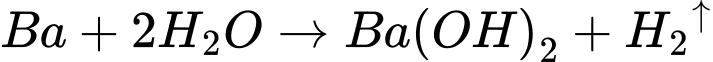
Xét các phản ứng:
✔️
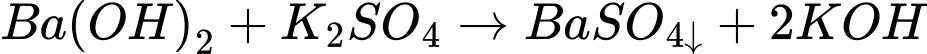
✔️
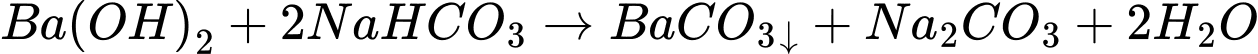
❌
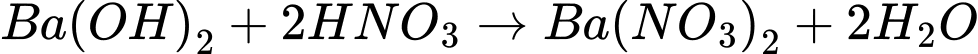
❌
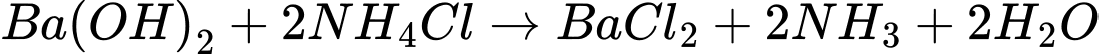
⟹ Có 2 phản ứng tạo kết tủa.
⟹ Chọn đáp án C Đáp án: C
Câu 21 [560898]: Dựa vào giá trị thế điện cực chuẩn của kim loại sau và giá trị thế điện cực chuẩn của quá trình 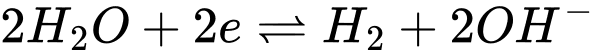 là
là 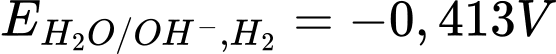 ở pH = 7
ở pH = 7
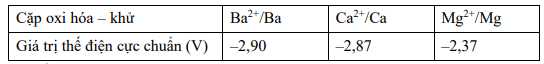
Hãy cho biết kim loại nào sau đây tác dụng được với nước?
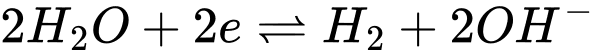 là
là 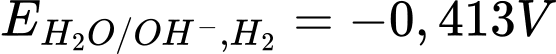 ở pH = 7
ở pH = 7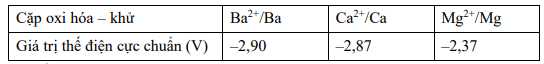
Hãy cho biết kim loại nào sau đây tác dụng được với nước?
A, Ba.
B, Mg.
C, Ca
D, Cả A, B và C.
Kim loại có Eo của cặp oxi hóa khử M2+/M < Eo (H2/H+) có khả năng khử H2 từ nước hoặc từ ion H+.
Cả Ba, Ca, Mg đều có Eo < Eo (H2O), dó đó có khả năng khử nước tạo H2.
⟹ Chọn đáp án D Đáp án: D
Cả Ba, Ca, Mg đều có Eo < Eo (H2O), dó đó có khả năng khử nước tạo H2.
⟹ Chọn đáp án D Đáp án: D
Câu 22 [560899]: Dựa vào bảng độ tan của hydroxide của nhóm IIA sau đây:
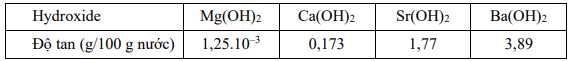
Xu hướng biến đổi độ tan của các hydroxide nhóm IIA là

Xu hướng biến đổi độ tan của các hydroxide nhóm IIA là
A, tăng.
B, giảm.
C, không đổi.
D, không xác định.
Chỉ số độ tan càng lớn => tan càng tốt.
Độ tan tăng dần từ Mg < Ca < Sr < Ba.
⟹ Chọn đáp án A Đáp án: A
Độ tan tăng dần từ Mg < Ca < Sr < Ba.
⟹ Chọn đáp án A Đáp án: A
Câu 23 [560900]: Dựa vào độ tan của barium hydroxyde và magnesium hydroxide như sau:
• Barium hydroxyde tan trong nước tạo dung dịch điện li mạnh.
• Magnesium hydroxide không tan trong nước.
Khả năng phản ứng với barium với nước như nào so với magnesium với nước?
• Barium hydroxyde tan trong nước tạo dung dịch điện li mạnh.
• Magnesium hydroxide không tan trong nước.
Khả năng phản ứng với barium với nước như nào so với magnesium với nước?
A, Mạnh hơn.
B, Yếu hơn.
C, Không xác định.
D, Bằng nhau.
Barium hydroxyde hòa tan trong nước tạo thành dung dịch điện phân mạnh. Magnesium hydroxide không tan trong nước.
⇒ Ba(OH)2 phản ứng với nước mạnh hơn Mg(OH)2 do có độ hòa tan cao hơn và tính chất base mạnh hơn.
⇒ Chọn đáp án A Đáp án: A
⇒ Ba(OH)2 phản ứng với nước mạnh hơn Mg(OH)2 do có độ hòa tan cao hơn và tính chất base mạnh hơn.
⇒ Chọn đáp án A Đáp án: A
Câu 24 [560901]: Vì sao magnesium phản ứng rất chậm với nước?

Một số bọt khí hydrogen xuất hiện khi cho magnesium vào nước ở điều kiện thường

Một số bọt khí hydrogen xuất hiện khi cho magnesium vào nước ở điều kiện thường
A, do tạo thành hợp chất không tan trong nước.
B, do tạo thành hợp chất tan trong nước.
C, do magnesium có thế điện cực oxi hóa khử âm.
D, do bọt khí hydrogen xuất hiện cản trở magnesium tiếp xúc với nước.
- Magnesium nhanh chóng tạo một lớp màng MgO hoặc Mg(OH)2 mỏng trên bề mặt khi tiếp xúc với không khí hoặc nước.
- Lớp màng này không tan trong nước, bền và có tác dụng ngăn cản sự tiếp xúc giữa kim loại Mg với nước, làm chậm phản ứng.
⟹ Chọn đáp án A. Đáp án: A
- Lớp màng này không tan trong nước, bền và có tác dụng ngăn cản sự tiếp xúc giữa kim loại Mg với nước, làm chậm phản ứng.
⟹ Chọn đáp án A. Đáp án: A
Câu 25 [706203]: Barium phản ứng với nước dễ dàng hơn so với magnesium ở điều kiện thường là do các nguyên nhân nào sau đây?
(1) Barium có tính khử mạnh hơn magnesium.
(2) Độ tan của barium hydroxide trong nước cao hơn nhiều so với magnesium hydroxide.
(3) Bọt khí hydrogen sinh ra bám trên bề mặt magnesium nhiều hơn, cản trở phản ứng tiếp diễn.
(1) Barium có tính khử mạnh hơn magnesium.
(2) Độ tan của barium hydroxide trong nước cao hơn nhiều so với magnesium hydroxide.
(3) Bọt khí hydrogen sinh ra bám trên bề mặt magnesium nhiều hơn, cản trở phản ứng tiếp diễn.
A, (1).
B, (1), (2) và (3).
C, (1) và (3).
D, (1) và (2).
Phân tích các phát biểu:
✔️ (1) Đúng. Barium nằm ở vị trí dưới Magnesium trong bảng tuần hoàn, do đó nó có tính khử mạnh hơn, dễ dàng nhường electron hơn để phản ứng với nước.
✔️ (2) Đúng. Ba(OH)2 tan tốt hơn Mg(OH)2, tạo điều kiện cho phản ứng tiếp diễn nhanh hơn.
❌ (3) Sai. Khi Mg phản ứng với nước, sinh ra Mg(OH)2 ít tan bám trên bề mặt kim loại Mg ngăn cản Mg phản ứng với nước dẫn đến làm chậm phản ứng.
Có 2 phát biểu đúng.
⟹ Chọn đáp án D Đáp án: D
✔️ (1) Đúng. Barium nằm ở vị trí dưới Magnesium trong bảng tuần hoàn, do đó nó có tính khử mạnh hơn, dễ dàng nhường electron hơn để phản ứng với nước.
✔️ (2) Đúng. Ba(OH)2 tan tốt hơn Mg(OH)2, tạo điều kiện cho phản ứng tiếp diễn nhanh hơn.
❌ (3) Sai. Khi Mg phản ứng với nước, sinh ra Mg(OH)2 ít tan bám trên bề mặt kim loại Mg ngăn cản Mg phản ứng với nước dẫn đến làm chậm phản ứng.
Có 2 phát biểu đúng.
⟹ Chọn đáp án D Đáp án: D
Câu 26 [560902]: Cho một mẩu nhỏ calcium vào cốc nước có thêm vài giọt dung dịch phenolphthalein. Khi kết thúc phản ứng
A, dung dịch trong cốc trong suốt, màu hồng và có pH lớn hơn 7.
B, dung dịch trong cốc có màu xanh và trong suốt.
C, chất trong cốc có màu hồng và vẩn đục.
D, dung dịch trong cốc có màu hồng và trong suốt.
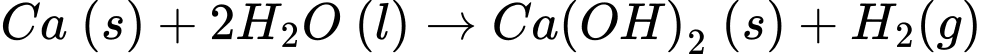
- Ca(OH)2 chỉ tan một phần, nên dung dịch sẽ có màu hồng nhạt do phenolphthalein đổi màu trong môi trường base.
- Do Ca(OH)2 không tan hết, trong cốc sẽ có hiện tượng vẩn đục do Ca(OH)2 rắn lắng xuống.
⟹ Chọn đáp án C Đáp án: C
Câu 27 [560903]: Barium phản ứng với nước dễ dàng hơn so với magnesium ở điều kiện thường là do các nguyên nhân nào sau đây?
(1) Barium có tính khử mạnh hơn magnesium.
(2) Độ tan của barium hydroxide trong nước cao hơn nhiều so với magnesium hydroxide.
(3) Bọt khí hydrogen sinh ra bám trên bề mặt magnesium nhiều hơn, cản trở phản ứng tiếp diễn.
(1) Barium có tính khử mạnh hơn magnesium.
(2) Độ tan của barium hydroxide trong nước cao hơn nhiều so với magnesium hydroxide.
(3) Bọt khí hydrogen sinh ra bám trên bề mặt magnesium nhiều hơn, cản trở phản ứng tiếp diễn.
A, (1).
B, (1), (2) và (3).
C, (1) và (3).
D, (1) và (2).
Phân tích các ý:
✔️ 1. Ba có tính khử mạnh hơn Mg: Đây là đúng vì trong nhóm kim loại kiềm thổ, tính khử tăng dần từ trên xuống dưới bảng tuần hoàn. Ba nằm dưới Mg nên có tính khử mạnh hơn.
✔️ 2. Độ tan của barium hydroxide (Ba(OH2) cao hơn nhiều so với magnesium hydroxide (Mg(OH)2): Đúng vì Ba(OH)2 tan tốt trong nước, trong khi Mg(OH)2 rất ít tan, làm cho phản ứng của Ba diễn ra dễ hơn.
❌3. Ba hoạt động hoá học mạnh hơn nên tốc độ thoát khí của H2 mạnh hơn magnesium.
Chọn đáp án D Đáp án: D
✔️ 1. Ba có tính khử mạnh hơn Mg: Đây là đúng vì trong nhóm kim loại kiềm thổ, tính khử tăng dần từ trên xuống dưới bảng tuần hoàn. Ba nằm dưới Mg nên có tính khử mạnh hơn.
✔️ 2. Độ tan của barium hydroxide (Ba(OH2) cao hơn nhiều so với magnesium hydroxide (Mg(OH)2): Đúng vì Ba(OH)2 tan tốt trong nước, trong khi Mg(OH)2 rất ít tan, làm cho phản ứng của Ba diễn ra dễ hơn.
❌3. Ba hoạt động hoá học mạnh hơn nên tốc độ thoát khí của H2 mạnh hơn magnesium.
Chọn đáp án D Đáp án: D
Câu 28 [560904]: Phát biểu nào không đúng?
A, Beryllium sẽ không phản ứng với nước lạnh.
B, Strontium có bán kính nguyên tử lớn hơn calcium.
C, Barium chloride không tan trong nước lạnh.
D, Radium phản ứng mạnh với nước.
Phân tích các phát biểu:
✔️ A. Đúng. Beryllium sẽ không phản ứng với nước lạnh: Beryllium (Be) không phản ứng với nước lạnh, vì nó có lớp vỏ oxide bảo vệ bề mặt kim loại, ngăn cản phản ứng với nước.
✔️ B. Đúng. Strontium có bán kính nguyên tử lớn hơn calcium: Strontium (Sr) nằm dưới calcium (Ca) trong bảng tuần hoàn, vì vậy bán kính nguyên tử của strontium lớn hơn calcium.
❌ C. Sai. Barium chloride (BaCl2) tan tốt trong nước, ngay cả ở nhiệt độ lạnh.
✔️ D. Đúng. Radium phản ứng mạnh với nước: Radium (Ra) là một kim loại kiềm thổ nặng, và nó phản ứng mạnh với nước, tạo ra radium hydroxide và khí hydrogen.
Chọn đáp án C Đáp án: C
✔️ A. Đúng. Beryllium sẽ không phản ứng với nước lạnh: Beryllium (Be) không phản ứng với nước lạnh, vì nó có lớp vỏ oxide bảo vệ bề mặt kim loại, ngăn cản phản ứng với nước.
✔️ B. Đúng. Strontium có bán kính nguyên tử lớn hơn calcium: Strontium (Sr) nằm dưới calcium (Ca) trong bảng tuần hoàn, vì vậy bán kính nguyên tử của strontium lớn hơn calcium.
❌ C. Sai. Barium chloride (BaCl2) tan tốt trong nước, ngay cả ở nhiệt độ lạnh.
✔️ D. Đúng. Radium phản ứng mạnh với nước: Radium (Ra) là một kim loại kiềm thổ nặng, và nó phản ứng mạnh với nước, tạo ra radium hydroxide và khí hydrogen.
Chọn đáp án C Đáp án: C
Câu 29 [704025]: Kim loại magnesium và hợp kim của nó là những chất nguy hiểm dễ nổ; chúng rất dễ cháy ở dạng tinh khiết khi nóng chảy. Ở nhiệt độ này, kim loại magnesium phản ứng được với các chất có thể coi là trơ như H2O, SiO2, CO2,… Tuy nhiên, để bắt đầu phản ứng cháy, kim loại magnesium cần phải được cung cấp một nguồn năng lượng nhiệt ban đầu và do đó khi ở nhiệt độ phòng thì magnesium sẽ ít tham gia phản ứng. Năng lượng tỏa ra khi kim loại magnesium rất lớn, nó phát ra ánh sáng trắng sáng chứa tia cực tím có thể gây tổn thương vĩnh viễn cho mắt. Các đám cháy kim loại magnesium gần như không thể bị dập tắt mà chỉ có thể hạn chế bằng cách không để đám cháy lan rộng và đợi cho kim loại magnesium phản ứng hết. Cho các phát biểu sau:
(a) Cần sử dụng kính an toàn có bảo vệ mắt khi đốt magnesium.
(b) Các đám cháy magnesium tỏa ra một lượng nhiệt rất lớn.
(c) Có thể dập tắt các đám cháy kim loại magnesium bằng nước, cát.
(d) Khi có đám cháy kim loại cần làm mát các khu vực tiếp xúc và đảm bảo đám cháy không lan sang các khu vực xung quanh.
Các phát biểu đúng là
(a) Cần sử dụng kính an toàn có bảo vệ mắt khi đốt magnesium.
(b) Các đám cháy magnesium tỏa ra một lượng nhiệt rất lớn.
(c) Có thể dập tắt các đám cháy kim loại magnesium bằng nước, cát.
(d) Khi có đám cháy kim loại cần làm mát các khu vực tiếp xúc và đảm bảo đám cháy không lan sang các khu vực xung quanh.
Các phát biểu đúng là
A, (a), (b), (c).
B, (a), (b), (d).
C, (a), (c), (d).
D, (b), (c), (d).
Phân tích các phát biểu:
✔️ (a) Đúng. Khi cháy magnisium phát ra ánh sáng chứa tia cực tím có thể gây tổn thương cho mắt.
✔️ (b) Đúng. Khi cháy magnisium tỏa ra lượng nhiệt rất lớn.
❌ (c) Sai. Không dùng nước, cát khô để dập tắt đám cháy magie vì magie phản ứng với nước, cát nóng sinh ra hydrogen, silicon có thể xảy ra một vụ nổ hơi làm văng các kim loại này đi khắp nơi dẫn đến đám cháy lan rộng.
Mg + H2O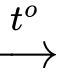 MgO + H2
MgO + H2
SiO2 + 2Mg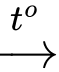 2MgO + Si
2MgO + Si
✔️ (d) Đúng. Đám cháy Mg gần như không thể dập tắt, chỉ có thể hạn chế bằng cách không để đám cháy lan rộng và đợi cho kim loại Mg phản ứng hết.
⟶ Các phát biểu đúng là (a) (b) (d)
⇒ Chọn đáp án B Đáp án: B
✔️ (a) Đúng. Khi cháy magnisium phát ra ánh sáng chứa tia cực tím có thể gây tổn thương cho mắt.
✔️ (b) Đúng. Khi cháy magnisium tỏa ra lượng nhiệt rất lớn.
❌ (c) Sai. Không dùng nước, cát khô để dập tắt đám cháy magie vì magie phản ứng với nước, cát nóng sinh ra hydrogen, silicon có thể xảy ra một vụ nổ hơi làm văng các kim loại này đi khắp nơi dẫn đến đám cháy lan rộng.
Mg + H2O
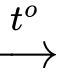 MgO + H2
MgO + H2SiO2 + 2Mg
 2MgO + Si
2MgO + Si✔️ (d) Đúng. Đám cháy Mg gần như không thể dập tắt, chỉ có thể hạn chế bằng cách không để đám cháy lan rộng và đợi cho kim loại Mg phản ứng hết.
⟶ Các phát biểu đúng là (a) (b) (d)
⇒ Chọn đáp án B Đáp án: B
Dạng 2: TRẮC NGHIỆM ĐÚNG SAI – mỗi ý a), b), c), d) chọn đúng hoặc sai.
Câu 30 [560929]: Bảng dưới đây trình bày một số đặc điểm chung của kim loại nhóm IIA.
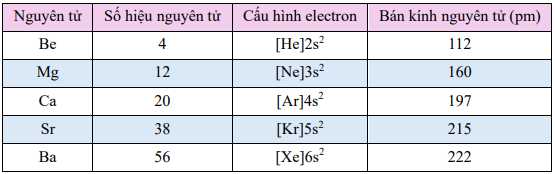
a. Cấu hình electron lớp ngoài cùng của các kim loại nhóm IIA có dạng ns2.
b. Số oxi hóa đặc trưng của các nguyên tố nhóm IIA là +2.
c. Bán kính nguyên tử tăng dần từ Be đến Ba do sự tăng số lớp electron.
d. Tính khử giảm dần từ Be đến Ba.

a. Cấu hình electron lớp ngoài cùng của các kim loại nhóm IIA có dạng ns2.
b. Số oxi hóa đặc trưng của các nguyên tố nhóm IIA là +2.
c. Bán kính nguyên tử tăng dần từ Be đến Ba do sự tăng số lớp electron.
d. Tính khử giảm dần từ Be đến Ba.
Phân tích các phát biểu:
✔️ a. Đúng. Tất cả các nguyên tố nhóm IIA (Be, Mg, Ca, Sr, Ba) đều có 2 electron ở lớp ngoài cùng với cấu hình electron dạng ns2, như bảng đã nêu.
✔️ b. Đúng. Các nguyên tố nhóm IIA dễ dàng mất 2 electron ở lớp ngoài cùng để tạo ion M2+ nên số oxi hóa đặc trưng là +2.
✔️ c. Đúng. Khi đi từ Be (Z=4) đến Ba (Z=56), số lớp electron tăng từ 2 (Be) lên 6 (Ba), dẫn đến bán kính nguyên tử tăng.
❌ d. Sai. Từ Be đến Ba, năng lượng ion hóa giảm do bán kính nguyên tử tăng, lực hút hạt nhân lên electron ngoài cùng yếu hơn, nên tính khử tăng dần từ Be đến Ba chứ không giảm.
✔️ a. Đúng. Tất cả các nguyên tố nhóm IIA (Be, Mg, Ca, Sr, Ba) đều có 2 electron ở lớp ngoài cùng với cấu hình electron dạng ns2, như bảng đã nêu.
✔️ b. Đúng. Các nguyên tố nhóm IIA dễ dàng mất 2 electron ở lớp ngoài cùng để tạo ion M2+ nên số oxi hóa đặc trưng là +2.
✔️ c. Đúng. Khi đi từ Be (Z=4) đến Ba (Z=56), số lớp electron tăng từ 2 (Be) lên 6 (Ba), dẫn đến bán kính nguyên tử tăng.
❌ d. Sai. Từ Be đến Ba, năng lượng ion hóa giảm do bán kính nguyên tử tăng, lực hút hạt nhân lên electron ngoài cùng yếu hơn, nên tính khử tăng dần từ Be đến Ba chứ không giảm.
Câu 31 [560930]: Một số thông số vật lí của kim loại nhóm IIA được trình bày trong bảng.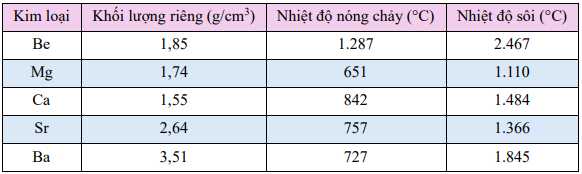
a. Các kim loại nhóm IIA đều là kim loại nhẹ.
b. Các kim loại nhóm IIA có nhiệt độ nóng chảy, nhiệt độ sôi giảm dần từBe đến Ba.
c. Các kim loại nhóm IIA có nhiệt độ nóng chảy cao hơn kim loại nhóm IA.
d. Các kim loại nhóm IIA dễ nhường electron hơn các kim loại nhóm IAthuộc cùng một chu kì.

a. Các kim loại nhóm IIA đều là kim loại nhẹ.
b. Các kim loại nhóm IIA có nhiệt độ nóng chảy, nhiệt độ sôi giảm dần từBe đến Ba.
c. Các kim loại nhóm IIA có nhiệt độ nóng chảy cao hơn kim loại nhóm IA.
d. Các kim loại nhóm IIA dễ nhường electron hơn các kim loại nhóm IAthuộc cùng một chu kì.
Phân tích các phát biểu:
✔️ a. Đúng. Khối lượng riêng của các kim loại nhóm IIA (Be, Mg, Ca, Sr, Ba) đều tương đối nhỏ, từ 1,55 g/cm3 (Ca) đến 3,51 g/cm3 (Ba). Đây là các kim loại nhẹ (Kim loại nhẹ là kim loại có khối lượng riêng < 5g/cm3)
❌ b. Sai.
+) Nhiệt độ nóng chảy: Giảm từ Be (1.287 oC) đến Mg (651 oC), nhưng sau đó dao động không đều (Ca: 842 oC, Sr: 757 oC, Ba: 727 oC).
+) Nhiệt độ sôi: Không giảm dần từ Be đến Ba (Be: 2.467 oC, Mg: 1.110 oC, Ca: 1.484 oC, Sr: 1.366 oC, Ba: 1.845 oC).
→ Không có xu hướng giảm dần rõ ràng.
✔️ c. Đúng. Kim loại nhóm IIA có nhiệt độ nóng chảy cao hơn kim loại nhóm IA do liên kết kim loại mạnh hơn, nhờ vào mật độ electron cao hơn và ion dương có kích thước nhỏ hơn.
❌ d. Sai. Kim loại nhóm IA (như Li, Na, K) dễ nhường electron hơn nhóm IIA (như Be, Mg, Ca) cùng chu kì vì kim loại nhóm IA có bán kính nguyên tử lớn hơn, dẫn đến lực hút của hạt nhân đến electron ở lớp ngoài cùng yếu hơn nên chúng dễ nhường electron hơn.
✔️ a. Đúng. Khối lượng riêng của các kim loại nhóm IIA (Be, Mg, Ca, Sr, Ba) đều tương đối nhỏ, từ 1,55 g/cm3 (Ca) đến 3,51 g/cm3 (Ba). Đây là các kim loại nhẹ (Kim loại nhẹ là kim loại có khối lượng riêng < 5g/cm3)
❌ b. Sai.
+) Nhiệt độ nóng chảy: Giảm từ Be (1.287 oC) đến Mg (651 oC), nhưng sau đó dao động không đều (Ca: 842 oC, Sr: 757 oC, Ba: 727 oC).
+) Nhiệt độ sôi: Không giảm dần từ Be đến Ba (Be: 2.467 oC, Mg: 1.110 oC, Ca: 1.484 oC, Sr: 1.366 oC, Ba: 1.845 oC).
→ Không có xu hướng giảm dần rõ ràng.
✔️ c. Đúng. Kim loại nhóm IIA có nhiệt độ nóng chảy cao hơn kim loại nhóm IA do liên kết kim loại mạnh hơn, nhờ vào mật độ electron cao hơn và ion dương có kích thước nhỏ hơn.
❌ d. Sai. Kim loại nhóm IA (như Li, Na, K) dễ nhường electron hơn nhóm IIA (như Be, Mg, Ca) cùng chu kì vì kim loại nhóm IA có bán kính nguyên tử lớn hơn, dẫn đến lực hút của hạt nhân đến electron ở lớp ngoài cùng yếu hơn nên chúng dễ nhường electron hơn.
Câu 32 [560931]: Một số thông số vật lí của kim loại nhóm IIA được trình bày trong bảng.
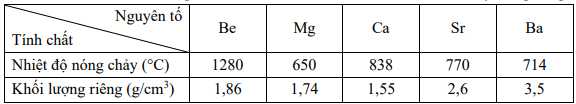
a. Beryllium là kim loại nhẹ nhất trong các kim loại nhóm IIA.
b. Magnesium là kim loại có nhiệt độ nóng chảy thấp nhất trong nhóm IIA.
c. Các kim loại nhóm IIA đều dẫn điện.
d. Các kim loại nhóm IIA có cùng kiểu mạng tinh thể.

a. Beryllium là kim loại nhẹ nhất trong các kim loại nhóm IIA.
b. Magnesium là kim loại có nhiệt độ nóng chảy thấp nhất trong nhóm IIA.
c. Các kim loại nhóm IIA đều dẫn điện.
d. Các kim loại nhóm IIA có cùng kiểu mạng tinh thể.
Phân tích các phát biểu:
❌ a. Sai. Beryllium có khối lượng riêng là 1,86 g/cm3, nhưng magnesium nhẹ hơn với khối lượng riêng là 1,74 g/cm3.
✔️ b. Đúng. Magnesium có nhiệt độ nóng chảy là 650 oC, thấp nhất trong các kim loại nhóm IIA.
✔️ c. Đúng. Các kim loại nhóm IIA đều có các electron tự do nên có khả năng dẫn điện tốt. Mặc dù mỗi kim loại trong nhóm IIA có các tính chất vật lí khác nhau, nhưng tất cả đều có khả năng dẫn điện.
❌ d. Sai. Các kim loại nhóm IIA có mạng tinh thể khác nhau. Ví dụ, Beryllium có mạng tinh thể lục phương chặt khít, trong khi các kim loại khác (như calcium) có cấu trúc lập phương tâm khối.
❌ a. Sai. Beryllium có khối lượng riêng là 1,86 g/cm3, nhưng magnesium nhẹ hơn với khối lượng riêng là 1,74 g/cm3.
✔️ b. Đúng. Magnesium có nhiệt độ nóng chảy là 650 oC, thấp nhất trong các kim loại nhóm IIA.
✔️ c. Đúng. Các kim loại nhóm IIA đều có các electron tự do nên có khả năng dẫn điện tốt. Mặc dù mỗi kim loại trong nhóm IIA có các tính chất vật lí khác nhau, nhưng tất cả đều có khả năng dẫn điện.
❌ d. Sai. Các kim loại nhóm IIA có mạng tinh thể khác nhau. Ví dụ, Beryllium có mạng tinh thể lục phương chặt khít, trong khi các kim loại khác (như calcium) có cấu trúc lập phương tâm khối.
Câu 33 [560932]: Bảng dưới đây trình bày một số đặc điểm của kim loại nhóm IIA.
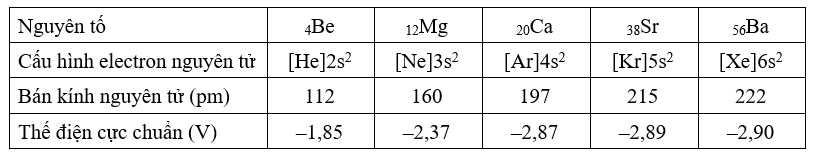
a. Các nguyên tố nhóm IIA thuộc vào nguyên tố s.
b. Các kim loại nhóm IIA đều có 2 electron độc thân.
c. Do bán kính nguyên tử có xu hướng tăng dần từ Be đến Ba nên khả năng nhường electron tăng dần từ Be đến Ba.
d. Khi tham gia phản ứng với H2O, magnessium phản ứng mãnh liệt hơn barium.

a. Các nguyên tố nhóm IIA thuộc vào nguyên tố s.
b. Các kim loại nhóm IIA đều có 2 electron độc thân.
c. Do bán kính nguyên tử có xu hướng tăng dần từ Be đến Ba nên khả năng nhường electron tăng dần từ Be đến Ba.
d. Khi tham gia phản ứng với H2O, magnessium phản ứng mãnh liệt hơn barium.
Phân tích các phát biểu:
✔️ a. Đúng. Các nguyên tố nhóm IIA thuộc vào nguyên tố s do có electron cuối dùng điền vào phân lớp s, có cấu hình ns2.
❌ b. Sai. Các nguyên tố nhóm IIA có cấu hình electron kết thúc ở ns2, tức là có 2 electron ở lớp vỏ ngoài cùng điền đủ vào một ô orbital nên không có electron độc thân.
✔️ c. Đúng. Khi bán kính nguyên tử tăng, lực hút electron yếu hơn, các electron ở lớp ngoài cùng dễ bị tách ra hơn. Điều này làm cho khả năng nhường electron (tính kim loại) tăng dần từ Be đến Ba.
❌ d. Sai. Barium phản ứng mạnh mẽ hơn magnesium khi tiếp xúc với nước vì các electron ngoài cùng của Ba dễ dàng bị nhường hơn.
✔️ a. Đúng. Các nguyên tố nhóm IIA thuộc vào nguyên tố s do có electron cuối dùng điền vào phân lớp s, có cấu hình ns2.
❌ b. Sai. Các nguyên tố nhóm IIA có cấu hình electron kết thúc ở ns2, tức là có 2 electron ở lớp vỏ ngoài cùng điền đủ vào một ô orbital nên không có electron độc thân.
✔️ c. Đúng. Khi bán kính nguyên tử tăng, lực hút electron yếu hơn, các electron ở lớp ngoài cùng dễ bị tách ra hơn. Điều này làm cho khả năng nhường electron (tính kim loại) tăng dần từ Be đến Ba.
❌ d. Sai. Barium phản ứng mạnh mẽ hơn magnesium khi tiếp xúc với nước vì các electron ngoài cùng của Ba dễ dàng bị nhường hơn.
Câu 34 [704378]: Các kim loại nhóm IIA (trừ beryllium) phản ứng với nước tạo ra khí hydrogen và hydroxide kim loại. Mức độ của phản ứng này thường liên quan đến độ tan của hydroxide tạo thành: hydroxide có độ tan lớn hơn thì phản ứng của kim loại đó với nước thuận lợi hơn. Độ tan trong nước của các hydroxide nhóm IIA ở 20 °C cho trong bảng sau:
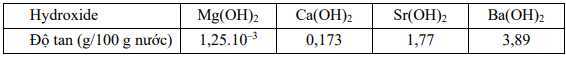

Phân tích các phát biểu:
❌ a. Sai. Phản ứng tổng quát với nước của kim loại nhóm IIA (trừ Be) là: M + 2H2O → M(OH)2 + H2.
Beryllium không phản ứng với nước, kể cả khi đun nóng.
✔️ b. Đúng. Dựa vào bảng độ tan trên, thấy độ tan của các hydroxide nhóm IIA tăng dần từ Mg(OH)2 đến Ba(OH)2.
❌ c. Sai. Mức độ của phản ứng với nước thường liên quan đến độ tan của hydroxide tạo thành: hydroxide
có độ tan lớn hơn thì phản ứng của kim loại đó với nước thuận lợi hơn nên bọt khí xuất hiện nhanh nhất trên bề mặt kim loại Ba.
❌ d. Sai. Có 3 kim loại (Ca, Sr, Ba) đều phản ứng nhanh với nước ở nhiệt độ thường.
❌ a. Sai. Phản ứng tổng quát với nước của kim loại nhóm IIA (trừ Be) là: M + 2H2O → M(OH)2 + H2.
Beryllium không phản ứng với nước, kể cả khi đun nóng.
✔️ b. Đúng. Dựa vào bảng độ tan trên, thấy độ tan của các hydroxide nhóm IIA tăng dần từ Mg(OH)2 đến Ba(OH)2.
❌ c. Sai. Mức độ của phản ứng với nước thường liên quan đến độ tan của hydroxide tạo thành: hydroxide
có độ tan lớn hơn thì phản ứng của kim loại đó với nước thuận lợi hơn nên bọt khí xuất hiện nhanh nhất trên bề mặt kim loại Ba.
❌ d. Sai. Có 3 kim loại (Ca, Sr, Ba) đều phản ứng nhanh với nước ở nhiệt độ thường.
Câu 35 [704184]: Kim loại có khả năng tác dụng được với các phi kim trong các điều kiện phù hợp. Tiến hành hai thí nghiệm sau:
▪ Thí nghiệm 1: Dùng kẹp gắp dây kim loại magnesium, đốt nóng trong không khí.
▪ Thí nghiệm 2: Lấy sợi dây sắt cuốn thành hình lò xo. Dùng kẹp gắp dây sắt, nung nóng đỏ sợi dây sắt trên ngọn lửa đèn cồn, đưa nhanh vào bình chứa khí chlorine.
▪ Thí nghiệm 1: Dùng kẹp gắp dây kim loại magnesium, đốt nóng trong không khí.
▪ Thí nghiệm 2: Lấy sợi dây sắt cuốn thành hình lò xo. Dùng kẹp gắp dây sắt, nung nóng đỏ sợi dây sắt trên ngọn lửa đèn cồn, đưa nhanh vào bình chứa khí chlorine.
Thí nghiệm 1: 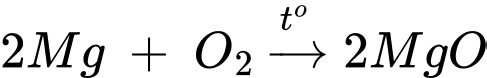
Khi đốt cháy kim loại Magnessium bằng oxygen không khí thì phản ứng xảy ra mãnh liệt, tỏa nhiều nhiệt, phát ra ánh sáng chói và giàu tia tử ngoại.
Thí nghiệm 2: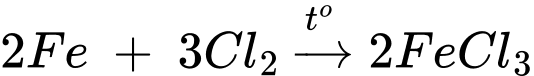
Hiện tượng là sắt cháy sáng và tạo ra khói màu vàng nâu.
Phân tích các phát biểu:
✔️ a. Đúng. Thí nghiệm 1 phản ứng xuất hiện ánh sáng chói và tia tử ngoại.
❌ b. Sai. Thí nghiệm 2, Fe bị oxi hóa lên số oxi hóa +3.
✔️ c. Đúng. Mg có số oxi hóa tăng từ 0 lên +2 và Fe có số oxi hóa tăng từ 0 lên +3 nên cả hai thí nghiệm đều chứng minh tính khử của kim loại.
❌ d. Sai. Hiện tượng khói màu vàng nâu do có FeCl3 sinh ra nên khi thay sợi dây sắt ở thí nghiệm 2 bằng dây magnesium thì hiện tượng thu được không có khói màu vàng nâu.
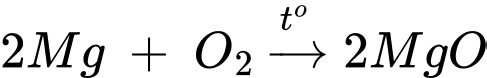
Khi đốt cháy kim loại Magnessium bằng oxygen không khí thì phản ứng xảy ra mãnh liệt, tỏa nhiều nhiệt, phát ra ánh sáng chói và giàu tia tử ngoại.
Thí nghiệm 2:
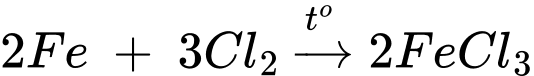
Hiện tượng là sắt cháy sáng và tạo ra khói màu vàng nâu.
Phân tích các phát biểu:
✔️ a. Đúng. Thí nghiệm 1 phản ứng xuất hiện ánh sáng chói và tia tử ngoại.
❌ b. Sai. Thí nghiệm 2, Fe bị oxi hóa lên số oxi hóa +3.
✔️ c. Đúng. Mg có số oxi hóa tăng từ 0 lên +2 và Fe có số oxi hóa tăng từ 0 lên +3 nên cả hai thí nghiệm đều chứng minh tính khử của kim loại.
❌ d. Sai. Hiện tượng khói màu vàng nâu do có FeCl3 sinh ra nên khi thay sợi dây sắt ở thí nghiệm 2 bằng dây magnesium thì hiện tượng thu được không có khói màu vàng nâu.
Dạng 3: TRẮC NGHIỆM YÊU CẦU TRẢ LỜI NGẮN
Câu 36 [560948]: Barium tham gia phản ứng mãnh liệt với nước ở nhiệt độ thường. Tiến hành cho 0,20 gam barium phản ứng với 250 cm3 nước. Biết nồng độ mol (mol/L) của dung dịch thu được là a x 10-3, coi thể tích dung dịch không đổi. Giá trị của a là bao nhiêu?
(Làm tròn kết quả đến hàng phần trăm)
Điền đáp án: ..........
(Làm tròn kết quả đến hàng phần trăm)
Điền đáp án: ..........
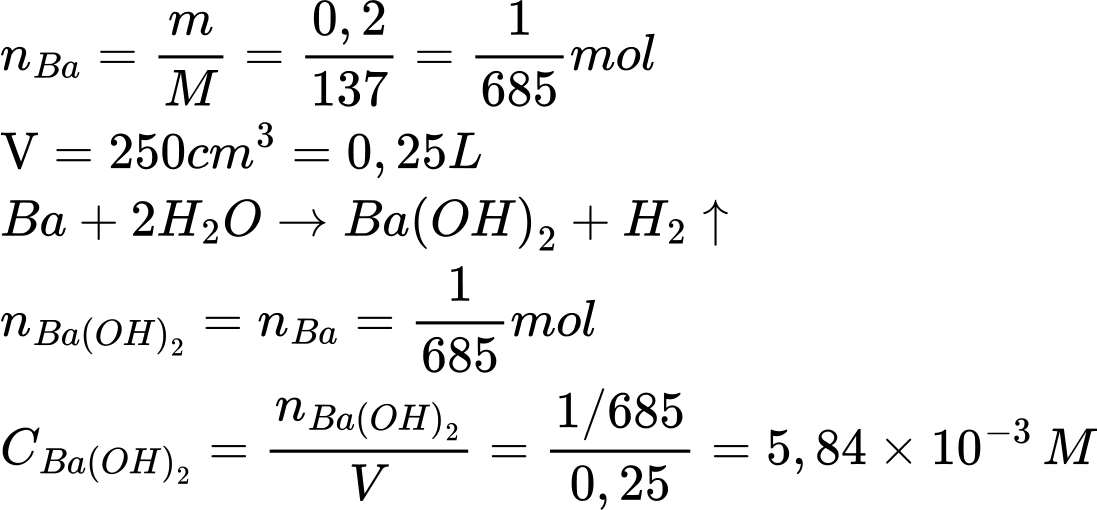
Điền đáp án: 5,84
Câu 37 [560949]: Bảng dưới đây cho biết độ tan của các hydroxide nhóm IIA ở 20oC trong 1000 gam nước.
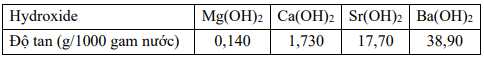
Học sinh Moon tiến hành thí nghiệm thấy rằng trong 50 mL một dung dịch có chứa 802 mg hydroxide của một kim loại nhóm IIA. Khối lượng phân tử của hydroxide trên là bao nhiêu? ( làm tròn đến hàng đơn vị )
Điền đáp án: ..........

Học sinh Moon tiến hành thí nghiệm thấy rằng trong 50 mL một dung dịch có chứa 802 mg hydroxide của một kim loại nhóm IIA. Khối lượng phân tử của hydroxide trên là bao nhiêu? ( làm tròn đến hàng đơn vị )
Điền đáp án: ..........
Khối lượng hydroxide trong 50 mL: 802 (mg) = 0.802 (g)
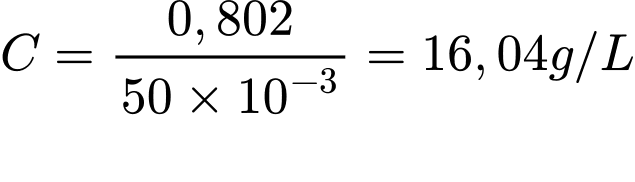
Với giá trị C=16.04 g/LC = 16.04 đối chiếu với bảng:
• Mg(OH)2: 0.140 (không khớp).
• Ca(OH)2: 1.730 (không khớp).
• Sr(OH)2: 17.70 (khớp gần nhất).
• Ba(OH)2: 38.90 (quá cao).
Do đó, chất tan là Sr(OH)2
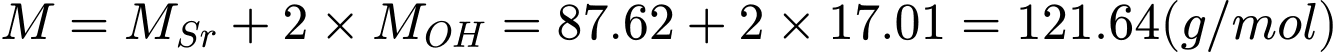
Điền đáp án: 122
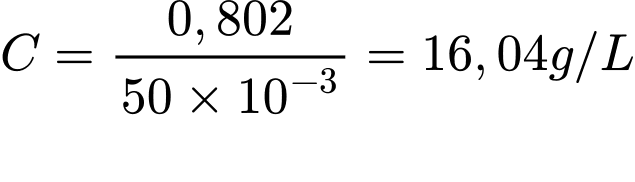
Với giá trị C=16.04 g/LC = 16.04 đối chiếu với bảng:
• Mg(OH)2: 0.140 (không khớp).
• Ca(OH)2: 1.730 (không khớp).
• Sr(OH)2: 17.70 (khớp gần nhất).
• Ba(OH)2: 38.90 (quá cao).
Do đó, chất tan là Sr(OH)2
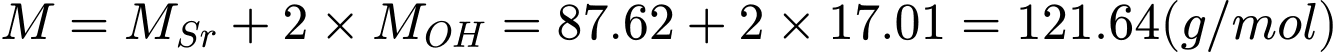
Điền đáp án: 122
Câu 38 [560957]: Magnesium hydroxide có thể sử dụng để làm thuốc chữa đầy bụng, khó tiêu do xảy ra phản ứng trung hòa hydrochloric acid trong dạ dày. Lượng magnesium hydroxide cần dùng để trung hòa 0,210 mol hydrochloric acid là bao nhiêu? Làm tròn kết quả đến phần chục.
Điền đáp án: ..........
Điền đáp án: ..........
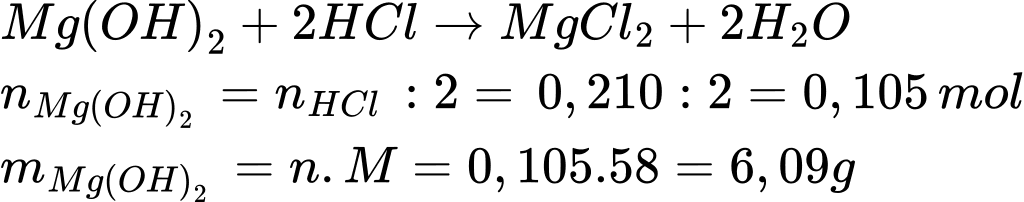
Điền đáp án: 6,1
Câu 39 [706180]: Calcium là nguyên tố cần thiết đối với cơ thể con người, là thành phần chủ yếu cấu tạo nên xương và răng, không thể thiếu trong quá trình đông máu. Theo khuyến cáo của Viện Dinh dưỡng Quốc gia Việt Nam, mỗi ngày người lớn cũng như trẻ em cần khoảng 500 mg calcium dưới dạng ion Ca2+. Hãy số mol calcium được đưa vào cơ thể khi một người uống 300 g sữa bò, biết nồng độ ion calcium trong sữa bò là 2%.
Khối lượng của Ca2+ trong 300 gam sữa bò là:
mCa2+ = 300 × 2% = 6 gam
Số mol của Ca2+ là nCa2+ = 6 ÷ 40 = 0,15 mol
⟹ Điền đáp án: 0,15
mCa2+ = 300 × 2% = 6 gam
Số mol của Ca2+ là nCa2+ = 6 ÷ 40 = 0,15 mol
⟹ Điền đáp án: 0,15
Câu 40 [704018]: Thực phẩm đóng hộp tự sôi (self-heating food packaging) là sản phẩm đóng gói tiện dụng, nhanh chóng với khả năng làm nóng bên trong thực phẩm mà không cần nguồn nhiệt bên ngoài hoặc nguồn điện. Nguồn nhiệt thương mại để đóng gói thực phẩm: vôi sống và nước, có đặc điểm là giá thành rẻ cũng như nguồn cung sẵn có, thường được FDA công nhận là an toàn. Kim loại magnesium dạng bột mịn với một lượng nhỏ sắt và muối ăn, hoạt động bằng cách thêm nước.
Một gói làm nóng thức ăn có trong lẩu tự sôi, chứa khoảng 10 gam hỗn hợp (Mg 90%, Fe 4%, NaCl 6% về khối lượng), khi tiếp xúc với nước, xảy ra phản ứng, phản ứng này toả nhiều nhiệt và làm nóng phần nước lẩu bên trên.
Mg(s) + H2O(l) → Mg(OH)2(s) + H2(g)
Biết rằng enthalpy tạo thành chuẩn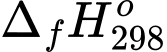 của Mg(OH)2(s) và H2O(l) lần lượt là –928,4 kJ/mol và –285,8 kJ/mol. Gói FRH trên có thể làm nóng bao nhiêu mL nước từ 30 °C lên 100 °C (làm tròn kết quả đến hàng đơn vị hay đến số tự nhiên gần nhất). Biết nhiệt dung của nước khoảng 4,2 J/(g.°C), giả sử phần nước bên trên chỉ nhận được tối đa 60% lượng nhiệt toả ra, phần nhiệt còn lại làm nóng các vật dụng khác và thất thoát vào môi trường.
của Mg(OH)2(s) và H2O(l) lần lượt là –928,4 kJ/mol và –285,8 kJ/mol. Gói FRH trên có thể làm nóng bao nhiêu mL nước từ 30 °C lên 100 °C (làm tròn kết quả đến hàng đơn vị hay đến số tự nhiên gần nhất). Biết nhiệt dung của nước khoảng 4,2 J/(g.°C), giả sử phần nước bên trên chỉ nhận được tối đa 60% lượng nhiệt toả ra, phần nhiệt còn lại làm nóng các vật dụng khác và thất thoát vào môi trường.
Một gói làm nóng thức ăn có trong lẩu tự sôi, chứa khoảng 10 gam hỗn hợp (Mg 90%, Fe 4%, NaCl 6% về khối lượng), khi tiếp xúc với nước, xảy ra phản ứng, phản ứng này toả nhiều nhiệt và làm nóng phần nước lẩu bên trên.
Mg(s) + H2O(l) → Mg(OH)2(s) + H2(g)
Biết rằng enthalpy tạo thành chuẩn
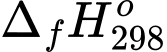 của Mg(OH)2(s) và H2O(l) lần lượt là –928,4 kJ/mol và –285,8 kJ/mol. Gói FRH trên có thể làm nóng bao nhiêu mL nước từ 30 °C lên 100 °C (làm tròn kết quả đến hàng đơn vị hay đến số tự nhiên gần nhất). Biết nhiệt dung của nước khoảng 4,2 J/(g.°C), giả sử phần nước bên trên chỉ nhận được tối đa 60% lượng nhiệt toả ra, phần nhiệt còn lại làm nóng các vật dụng khác và thất thoát vào môi trường.
của Mg(OH)2(s) và H2O(l) lần lượt là –928,4 kJ/mol và –285,8 kJ/mol. Gói FRH trên có thể làm nóng bao nhiêu mL nước từ 30 °C lên 100 °C (làm tròn kết quả đến hàng đơn vị hay đến số tự nhiên gần nhất). Biết nhiệt dung của nước khoảng 4,2 J/(g.°C), giả sử phần nước bên trên chỉ nhận được tối đa 60% lượng nhiệt toả ra, phần nhiệt còn lại làm nóng các vật dụng khác và thất thoát vào môi trường.
Mg(s) + 2H2O(l) ⟶ Mg(OH)2(s) + H2(g)
Biến thiên ethalpy chuẩn của phản ứng trên là:
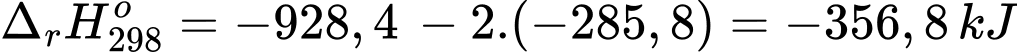
Số mol của Mg trong gói tự sôi trên là:
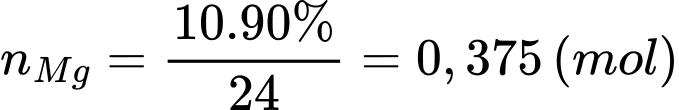
Lượng nhiệt tỏa ra khi sử dụng 1 mol Mg là 356,8 kJ
Lượng nhiệt tỏa ra khi sử dụng 0,375 mol Mg làm nóng nước là:
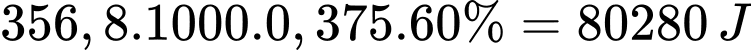
Khối lượng nước tối đa làm nóng từ 0,375 mol Mg là:
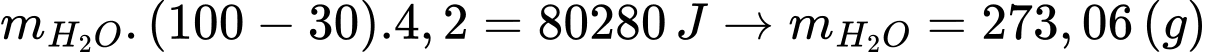
Thể tích nước là:
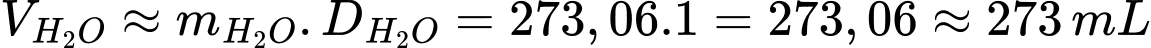
⇒ Điền đáp án: 273
Biến thiên ethalpy chuẩn của phản ứng trên là:
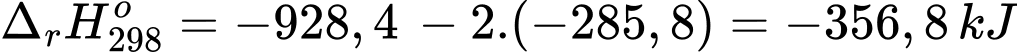
Số mol của Mg trong gói tự sôi trên là:
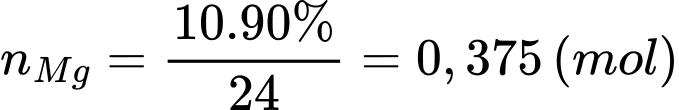
Lượng nhiệt tỏa ra khi sử dụng 1 mol Mg là 356,8 kJ
Lượng nhiệt tỏa ra khi sử dụng 0,375 mol Mg làm nóng nước là:
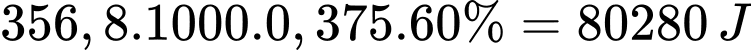
Khối lượng nước tối đa làm nóng từ 0,375 mol Mg là:
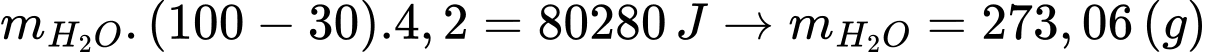
Thể tích nước là:
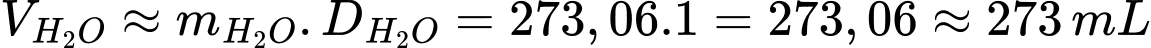
⇒ Điền đáp án: 273
Dạng 4: CÂU HỎI TỰ LUẬN
Câu 41 [1016761]: Sơ đồ dưới đây là các thiết bị được sử dụng để thu thập và đo thể tích khí hydrogen thoát ra khi một mẫu kim loại nhóm IIA phản ứng với hydrochloric acid loãng:
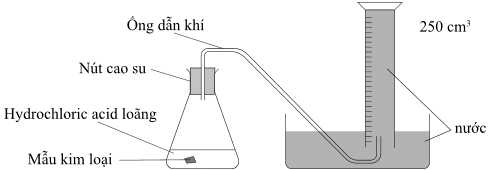
Các bước tiến hành:
Bước 1: Một mẫu kim loại được cân và sau đó đặt vào bình tam giác.
Bước 2: Cho một lượng acid dư vào bình tam giác, nắp bằng nút cao su có dây dẫn khí ra ngoài.
Bước 3: Thu khí bằng phương pháp đẩy nước. Khi phản ứng hoàn tất và khí thu được đã nguội đến nhiệt độ phòng, ghi lại thể tích khí thu được trong ống đong chia vạch.
Giả sử 1 mol hydrogen có thể tích là 24,0 dm3 trong điều kiện thực nghiệm. Kết quả được ghi lại trong bảng sau:

a) Có thể thay dung dịch hydrochloric acid loãng bằng dung dịch sulfuric acid loãng không? Giải thích.
b) Từ kết quả của thí nghiệm, nguyên tử khối của X gần nhất với nguyên tử khối của kim loại nhóm IIA nào?
c) Ngoài thu bằng phương pháp đẩy nước, có thể thu được khí H2 bằng phương pháp đẩy khí ngửa bình không? Giải thích.

Các bước tiến hành:
Bước 1: Một mẫu kim loại được cân và sau đó đặt vào bình tam giác.
Bước 2: Cho một lượng acid dư vào bình tam giác, nắp bằng nút cao su có dây dẫn khí ra ngoài.
Bước 3: Thu khí bằng phương pháp đẩy nước. Khi phản ứng hoàn tất và khí thu được đã nguội đến nhiệt độ phòng, ghi lại thể tích khí thu được trong ống đong chia vạch.
Giả sử 1 mol hydrogen có thể tích là 24,0 dm3 trong điều kiện thực nghiệm. Kết quả được ghi lại trong bảng sau:

a) Có thể thay dung dịch hydrochloric acid loãng bằng dung dịch sulfuric acid loãng không? Giải thích.
b) Từ kết quả của thí nghiệm, nguyên tử khối của X gần nhất với nguyên tử khối của kim loại nhóm IIA nào?
c) Ngoài thu bằng phương pháp đẩy nước, có thể thu được khí H2 bằng phương pháp đẩy khí ngửa bình không? Giải thích.
a. Có thể thay thế dung dịch hydrochloric acid bằng dung dịch sulfuric acid vì cả hai đều cung cấp ion H+ giải phóng ra khí H2.
b.Đổi 230 cm3 = 0,23 dm3
Gọi kim loại cần tìm là X.
2X + 2nHCl → 2XCln + nH2
Số mol của khí là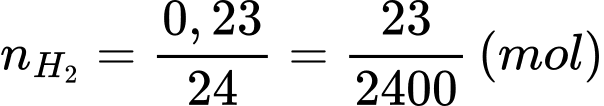
→ Số mol của X là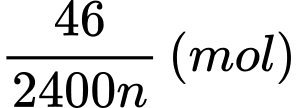
Khối lượng của kim loại là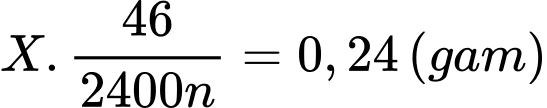 .
.
Ta có bảng sau:

→ X có thể Mg.
c. H2 nhẹ hơn không khí, nếu dùng phương pháp đẩy không khí ngửa bình thì sẽ bay hết ra ngoài.
b.Đổi 230 cm3 = 0,23 dm3
Gọi kim loại cần tìm là X.
2X + 2nHCl → 2XCln + nH2
Số mol của khí là
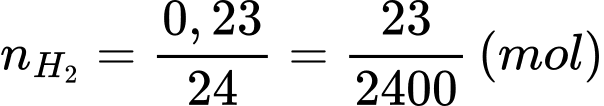
→ Số mol của X là
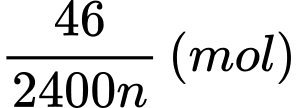
Khối lượng của kim loại là
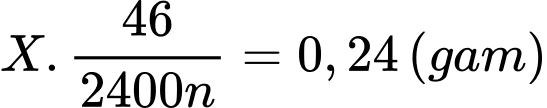 .
.
Ta có bảng sau:

→ X có thể Mg.
c. H2 nhẹ hơn không khí, nếu dùng phương pháp đẩy không khí ngửa bình thì sẽ bay hết ra ngoài.