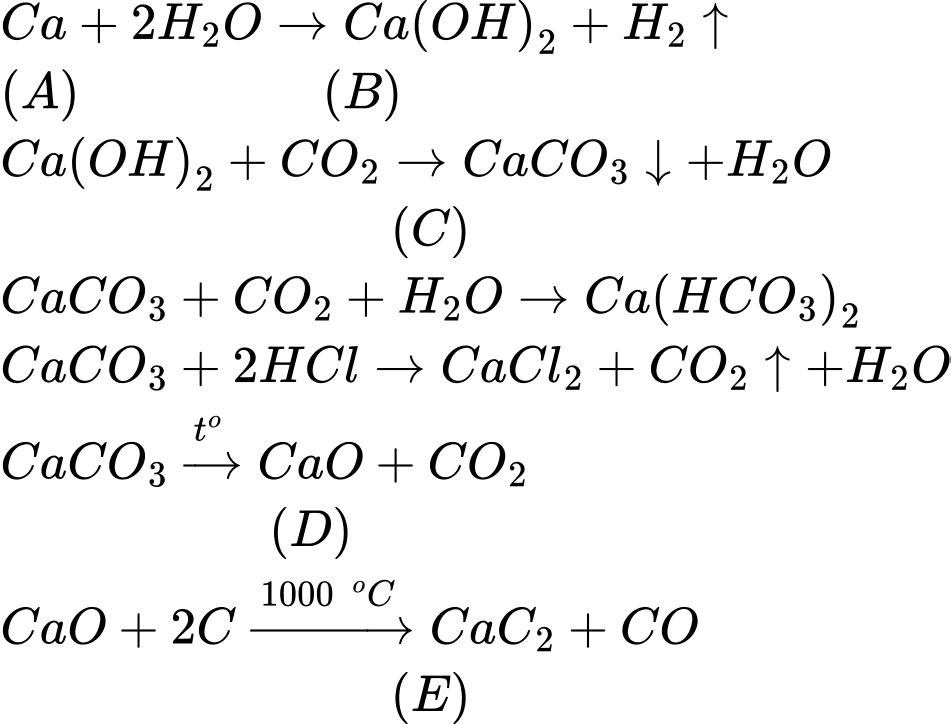Dạng 1: TRẮC NGHIỆM KHÁCH QUAN: mỗi câu hỏi chỉ có một đáp án đúng.
| Công thức | A. CaSO4. | B. CaO. | C. Ca(OH)2. | D. CaCO3. |
| Tên gọi | calcium sulfate | calcium oxide | calcium hydroxide | calcium carbonate |
⇒ Chọn đáp án A Đáp án: A
| Công thức | A. Ca(OH)2. | B. CaO. | C. CaSO4. | D. CaCO3. |
| Tên gọi | canxi hiđroxit | canxi oxit | canxi sunfat | canxi cacbonat |
| Tên gọi khác | vôi tôi | vôi sống | thạch cao | đá vôi |
⇝ Chọn đáp án A. Đáp án: A
❌A. Bauxite là Al2O3.2H2O.
❌B. Đá vôi là CaCO3.
❌C. Thạch cao nung là CaSO4.H2O.
✔️D. Thạch cao sống là CaSO4.2H2O.
⇒ Chọn đáp án D.
Đáp án: D

⇒ Đúc tượng, bó bột khi gãy xương dùng thạch cao nung: CaSO4.H2O.
⇒ Chọn đáp án A Đáp án: A
⇒ Biện pháp khắc phục là bón vôi tôi (CaO) bởi CaO + H2O → Ca(OH)2 có tính base ⇝ tăng tính kiềm cho đất cũng như giúp khử chua (loại bỏ các acid trong đất).
⇒ Chọn đáp án A Đáp án: A
Các hydroxide khác:
NaOH (sodium hydroxide) và KOH (potassium hydroxide): Mặc dù cũng là các base mạnh và có nhiều ứng dụng, nhưng thường có giá thành cao hơn Ca(OH)2 .
Ba(OH)2 (barium hydroxide): Có tính base mạnh nhưng độc hại và ít được sử dụng rộng rãi hơn Ca(OH)2 .
⟹ Chọn đáp án C Đáp án: C
► Các chất như CaO, CaOCl2 không được sử dụng do khi hút ẩm sẽ gây ảnh hưởng đến da tay.
⇒ Chọn đáp án A Đáp án: A
Các ứng dụng khác cũng có nhưng không phải là chủ yếu.
⟹ Chọn đáp án A Đáp án: A
- BaSO4 là muối ít tan và không có tính kiềm mạnh, nên không có tác dụng với việc trung hòa acid trong dạ dày.
⟹ Chọn đáp án B Đáp án: B
❌B. Thuốc tẩy rửa : (NaOH) hoặc (KOH) thường được sử dụng làm chất tẩy rửa mạnh vì chúng có tính kiềm cao, giúp phân hủy dầu mỡ và chất bẩn.
❌C. Thường là các hợp chất như (H2O2), Ethanol (C2H5OH) hoặc (Cl2) có khả năng diệt khuẩn.
❌D. Thuốc giảm đau: Paracetamol (C8H9NO2) hoặc Aspirin (C9H8O4) là các chất phổ biến dùng để giảm đau và hạ sốt.
Chọn đáp án A Đáp án: A
❌ B. Barium chloride (BaCl2): Là một muối tan trong nước, không có đặc tính phù hợp với yêu cầu của thuốc diệt chuột.
❌ C. Barium hydroxide (Ba(OH)2): Là một base mạnh, tan trong nước và có tính kiềm cao, không phù hợp để làm thuốc diệt chuột.
❌ D. Barium sulfate (BaSO4): Là một muối không tan trong nước và cũng không có tính độc hại ở nồng độ bình thường, không phù hợp với mục đích diệt chuột.
⟹ Chọn đáp án A. Đáp án: A
❌ B. Sai. Mg(OH)2 mới được dùng trong các thuốc chữa chứng khó tiêu).
✔️ C. Đúng. SrCO3 (Strontium carbonate) được sử dụng trong ngành công nghiệp pháo hoa và pháo sáng, tạo ra màu đỏ đặc trưng khi đốt cháy.
❌ D. Sai. BaCl2 (Barium chloride) không được dùng làm "bột barium" trong y học mà (BaSO4) mới được sử dụng trong y học để chụp X-quang (chủ yếu để tạo hình ảnh trong chụp cắt lớp).
⟹ Chọn đáp án C Đáp án: C
Vì vậy, oxide tạo ra dung dịch bão hòa có pH cao nhất sẽ là BaO (aq), do nó tạo ra dung dịch kiềm mạnh với nồng độ OH⁻ cao nhất.
⟹ Chọn đáp án D. Đáp án: D
Giấm có tính acid của CH3COOH nên phản ứng với CaCO3 giải phóng khí carbon dioxide (CO2).
PTHH:
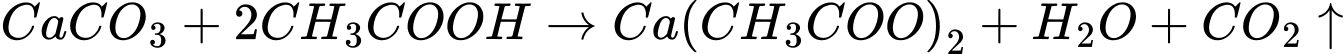
Chọn đáp án C Đáp án: C
❌ A. NaOH + Ba(HCO3)2 → NaOH + BaCO3↓ + H2O.
❌ B. 2HCl + Ba(HCO3)2 → BaCl2 + 2CO2↑ + 2H2O.
❌ C. Ca(OH)2 + Ba(HCO3)2 → BaCO3↓ + CaCO3↓ + 2H2O.
✔️ D. H2SO4 + Ba(HCO3)2 → BaSO4↓ + 2CO2↑ + 2H2O.
⟹ Chọn đáp án D Đáp án: D
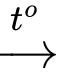 CaO + CO2↑.
CaO + CO2↑.⟶ Ngoài CO2, chất còn lại là CaO.
⟹ Chọn đáp án D Đáp án: D
Hoặc khi CaO hút ẩm: CaO + H2O → Ca(OH)2
|⇝ Sau đó: Ca(OH)2 + CO2 → CaCO3 + H2O.
⟹ Chọn đáp án C Đáp án: C
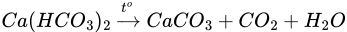
Hiện tượng sủi bọt khí không màu CO2↑ và có kết tủa trắng CaCO3↓ → Đáp án đúng là đáp án B
Đáp án: B
⇝ Hiện tượng: xuát hiện kết tủa trắng CaCO3↓. ❒ Đáp án: C
Chọn C.
Đáp án: C

Hình ảnh. Phần núi đá vôi trong nước biển dễ bị xói mòn
Phương trình nào sau đây biểu diễn cho quá trình nói trên?
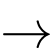 Ca(HCO3)2(aq).
Ca(HCO3)2(aq).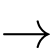 Ca(HCO3)2(aq).
Ca(HCO3)2(aq).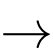 CaO(s) + CO2(g).
CaO(s) + CO2(g).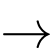 Ca(HCO3)2(aq).
Ca(HCO3)2(aq).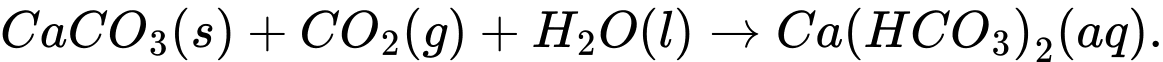
Chọn đáp án C Đáp án: D
PTHH:
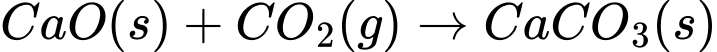
⟹ Chọn đáp án C
Đáp án: C
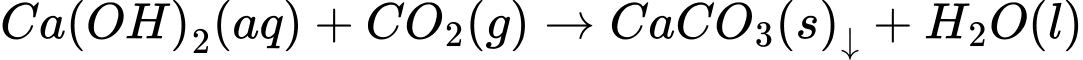
→ Chất X là CaCO3.
⟹ Chọn đáp án C Đáp án: C
- Z là CO2 (carbon dioxide), không phải là khí duy trì sự sống (oxygen, O2). CO2 là khí gây ra hiệu ứng nhà kính và không hỗ trợ sự sống của hầu hết các sinh vật trên trái đất.
Phương trình phản ứng giữa Y (CaCO3) và acid mạnh (ví dụ, hydrochloric acid HCl) để tạo ra Z (CO2) và các sản phẩm khác:
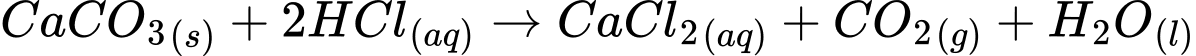
⟹ Chọn đáp án B Đáp án: B
✔️ Nước không có phản ứng đặc trưng với cả hai hợp chất. Nhưng khi hòa tan thì MgCO3 không tan trong nước, còn Mg(NO3)2 tan tạo thành dung dịch.
❌ Khí oxygen không phản ứng đặc biệt với MgCO3 hoặc Mg(NO3)2.
❌ NaOH rắn không dụng với MgCO3, với Mg(NO3)2.
⟹ Chọn đáp án B
Đáp án: B




B.
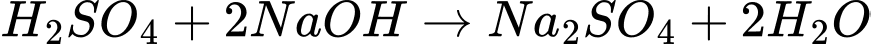
C.
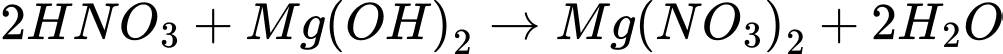
D.
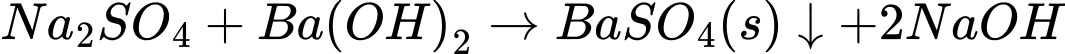
Phản ứng D sinh ra chất không tan là BaSO4.
⟹ Chọn đáp án D
Đáp án: D
MgCO3(s)
 X(s) + Y(g).
X(s) + Y(g).Hợp chất X và Y lần lượt là
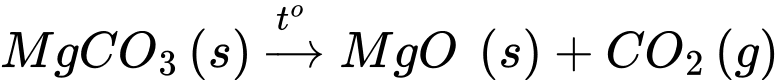
X là magnesium oxide (MgO) và hợp chất Y là khí carbon dioxide (CO2).
⟹ Chọn đáp án A Đáp án: A
Dựa vào bảng thông tin dưới đây để trả lời các câu hỏi 29 – 30:


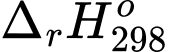 (kJ/mol) của phản ứng nhiệt phân MCO3 phải có giá trị lớn nhất.
(kJ/mol) của phản ứng nhiệt phân MCO3 phải có giá trị lớn nhất. Dựa vào bảng thông tin ta thấy giá trị 271,5 kJ/mol lớn nhất tương ứng với muối BaCO3.
⟹ Chọn đáp án D Đáp án: D

Dựa vào bảng thông tin ta thấy muối BaCO3 cần hấp thụ nhiều năng lượng nhất (271,5 kJ/mol) để phân hủy.
⟹ Chọn đáp án D Đáp án: D
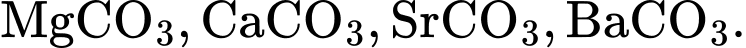

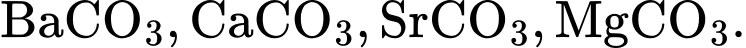
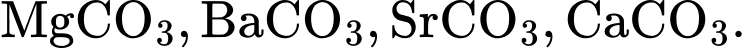
Nhiệt độ phân huỷ thành oxide của các muối carbonate của kim loại nhóm IIA giảm dần theo dãy
BaCO3 > SrCO3 > CaCO3 > MgCO3
⟹ Chọn đáp án B
Dựa vào bảng thông tin dưới đây để trả lời các câu hỏi 32 – 33:
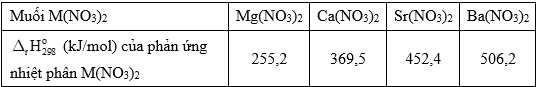
Phân hủy 1 mol muối nitrate của nguyên tố nhóm IIA thì hợp chất Ba(NO3)2 hấp thụ nhiều năng lượng nhất.
⟹ Chọn đáp án D Đáp án: D
Muối có độ bền nhiệt cao nhất là Ba(NO3)2.
⟹ Chọn đáp án D Đáp án: D
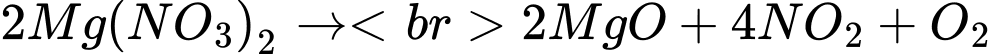
nNO2 = 2nMg(NO3)2 = 0,05.2 = 0,1 mol
nO2 = 0,05.1/2 = 0,025 mol
nhỗn hợp = 0,1 + 0,025 = 0,125 mol.
⟹ V = 0,125.24,79 ≈ 3,1 L
⟹ Chọn đáp án A
Đáp án: A
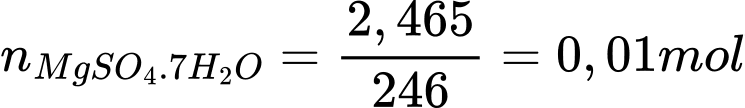
Phương trình phản ứng:
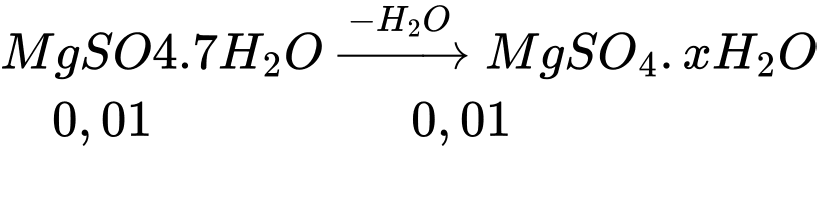
Khối lượng muối tạo thành
mMgSO4.xH2O =1,744 = 0,01.(24 + 96 + 18.x) ⟹ x = 3
Công thức của muối sau khi mất đi một vài phân tử nước là: MgSO4.3H2O
⟹ Chọn đáp án D.
Đáp án: D
⟹ Chọn đáp án B
Đáp án: B
❌ B. Dung dịch NH3: Dung dịch NH3 có thể phân biệt được dung dịch CaCl2 và BaCl2. Khi thêm dung dịch NH3 vào dung dịch CaCl2, sẽ không xảy ra hiện tượng gì rõ rệt.
✔️ C. Na2CrO4: Dung dịch Na2CrO4 sẽ tạo ra kết tủa màu vàng với dung dịch BaCl2 (do tạo ra BaCrO4), nhưng không phản ứng với CaCl2.
❌ D. Na2CO3: Khi thêm Na2CO3 vào dung dịch CaCl2, cả 2 sẽ tạo ra kết tủa CaCO3, BaCO3 trắng.
⟹ Chọn đáp án C
Đáp án: C
1. CaCl2 (Calcium chloride): Khi đốt, tạo ra màu cam đặc trưng.
2. BaCl2 (Barium chloride): Khi đốt, tạo ra màu lục
3. KCl (Potassium chloride): Khi đốt, tạo ra màu tím.
4. NaCl, Na2CO3 Khi đốt, tạo ra màu vàng đặc trưng.
⟹ Có thể phân biệt 3 chất.
⟹ Chọn đáp án B
Đáp án: B
✔️ A. Đúng. Các muối nitrate của nhóm IIA (ví dụ: Mg(NO3)2, Ca(NO3)2, Ba(NO3)2) đều tan tốt trong nước. Đây là quy tắc chung cho tất cả các muối nitrate (NO3-), chúng đều hòa tan trong nước.
✔️ B. Đúng. Muối magnesium sulfate (MgSO4) là chất tan trong nước, trong khi đó muối barium sulfate (BaSO4) lại là chất không tan trong nước.
✔️ C. Đúng. Các muối carbonate của nhóm IIA (MgCO3, CaCO3, SrCO3, BaCO3) đều không tan trong nước.
❌ D. Sai. Các hydroxide của nhóm IA (NaOH, KOH, LiOH) đều tan rất tốt trong nước. Tuy nhiên, hydroxide của nhóm IIA có độ tan khác nhau. Ví dụ, Mg(OH)2 rất ít tan.
⟹ Chọn đáp án D Đáp án: D
❌ A. Sai. Ca(OH)2 hay vôi tôi thường được sử dụng trong nông nghiệp để trung hòa đất acid và cải thiện độ pH của đất.
✔️ B. Đúng. Mg(OH)2 là thành phần phổ biến trong các thuốc antacid (thuốc trung hòa acid dạ dày) dùng để chữa chứng khó tiêu, trào ngược acid hoặc đau dạ dày.
✔️ C. Đúng. Anion hydroxide trong Ba(OH)2 là OH-. Nguyên tử O: Có 8 electron + Nguyên tử H: Có 1 electron + Ion OH⁻ mang điện tích -1: (nghĩa là ion
OH⁻ đã nhận thêm 1 electron so với trạng thái trung hòa).
Tổng = 10
⟹ Chọn đáp án A
Đáp án: A
Mật độ điện tích của ion bằng điện tích của ion chia cho thể tích của ion đó. Ion được coi có dạng cầu nên thể tích của ion liên hệ với bán kính ion bởi công thức:
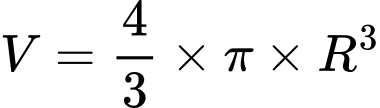 với R là bán kính ion.
với R là bán kính ion. Trong các phát biểu sau:
(a) Phần trăm khối lượng của beryllium trong beryllium carbonate tinh khiết khan là 6,25%.
(b) BeCO3 thường được bảo quản trong khí quyển tạo bởi chất X là carbon dioxide.
(c) Cation Be2+ dễ bị thuỷ phân hơn so với cation Ca2+ là do mật độ điện tích trên cation Be2+ nhỏ hơn so với cation Ca2+.
(d) Cation Be2+ có khả năng thay thế nguyên tử trung tâm magnesium của phức chất trong một số enzyme, tạo phức chất bền hơn.
Các phát biểu đúng là
❌A.Sai. Phần trăm khối lượng của beryllium trong beryllium carbonate tinh khiết khan là 13,04%.
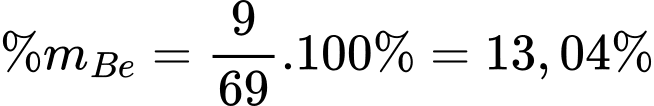
✔️B. Đúng. Beryllium carbonate (BeCO3 với M = 69 g/mol) khan là chất bột màu trắng, dễ phân huỷ ngay trong điều kiện thường, tạo thành BeO nên cần bảo quản trong CO2 để cân bằng chuyển dịch để tạo BaCO3.
❌C. Sai. Cation Be2+ dễ bị thuỷ phân hơn so với cation Ca2+ là do mật độ điện tích trên cation Be2+ lớn hơn so với cation Ca2+. Nguyên do Be2+ và Ca2+ có cùng tổng điện tích 2+ nhưng Be2+ có bán kính nhỏ hơn Ca2+ nên có mật độ điện tích lớn hơn Ca2+.
✔️D. Đúng. Cation Be2+ có khả năng thay thế nguyên tử trung tâm magnesium của phức chất trong một số enzyme, tạo phức chất bền hơn. cation Be2+ có thể vô hiệu hoá chức năng của các enzyme, đặc biệt là các enzyme chứa phức chất có nguyên tử trung tâm được hình thành từ cation Mg2+.
Chọn đáp án C Đáp án: C
Dạng 2: TRẮC NGHIỆM ĐÚNG SAI – mỗi ý a), b), c), d) chọn đúng hoặc sai.
(1) X
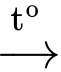 Y + Z.
Y + Z.(2) Y + H2O
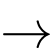 T.
T.(3) T + F → G + X + H2O.
(4) T + 2F
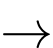 H + X + 2H2O.
H + X + 2H2O.Biết X là thành phần chính của đá vôi, F là hợp chất của Na; Y được dùng để khử chua đất trồng.
a. Chất Z là nguyên nhân gây ra hiện tượng hiệu ứng nhà kính.
b. Chất F được sử dụng trong quy trình solvay để điều chế soda.
c. Ở điều kiện thường, chất F là chất rắn, tan nhiều trong nước.
d. T được ứng dụng để khử chua, làm mềm nước cứng.

2.

3.
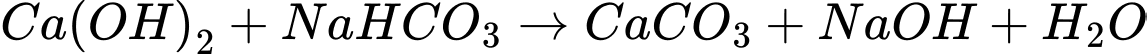
4.
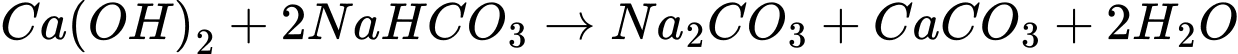
X là CaCO3
Y là CaO ; Z là CO2 ; T là Ca(OH)2 ; G là NaOH
F là NaHCO3 ; G là NaOH ; H là Na2CO3
Phân tích các phát biểu:
✔️ a. Đúng – Z là CO2, nguyên nhân chính gây ra hiệu ứng nhà kính.
✔️ b. Đúng – F (NaHCO3) được sử dụng trong quy trình Solvay để điều chế soda.
❌ c. Sai – F (NaHCO3) là chất rắn,ít tan trong nước.
✔️ d. Đúng – T (Ca(OH)2) được ứng dụng để khử chua và làm mềm nước cứng.
a. Dung dịch chuyển từ không màu sang màu hồng.
b. Phản ứng xảy ra nhanh hơn khi đun nóng nên đây là phản ứng thu nhiệt.
c. Sản phẩm thu được sau phản ứng có thể khử chua đất, làm mềm nước cứng.
d. Nếu cho bằng giấy quỳ tím vào dung dịch sau phản ứng thì có màu hồng.

Phân tích các phát biểu:
✔️a. Đúng. Dung dịch chuyển từ không màu sang màu hồng do tạo Ca(OH)2 là base mạnh.
❌b.Sai. Phản ứng xảy ra nhanh hơn khi đun nóng và là phản ứng tỏa nhiệt (delta H < 0).
✔️c. Đúng. Sản phẩm thu được sau phản ứng Ca(OH)2 có thể khử chua đất, làm mềm nước cứng.
❌d.Sai. Nếu cho giấy quỳ tím vào dung dịch sau phản ứng thì có màu xanh do Ca(OH)2 là base mạnh.
Thí nghiệm 2: Cho mẩu nhỏ kim loại barium (khoảng 2 g) vào chậu thuỷ tinh chứa khoảng 500 mL nước và vài giọt dung dịch phenolphthalein.
a. Ở cả thí nghiệm 1 và thí nghiệm 2, dung dịch sau phản ứng đều bị đục.
b. Mẩu calcium ở thí nghiệm 1 tan nhanh hơn mẩu barium ở thí nghiệm 2.
c. Hai thí nghiệm này chứng minh rằng calcium và barium là các kim loạicó thế khử chuẩn âm.
d. Ở cả thí nghiệm 1 và thí nghiệm 2, dung dịch sau phản ứng có màu hồng.
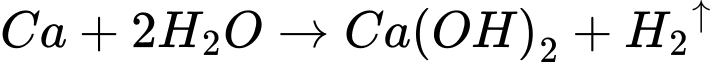
Thí nghiệm 2: Barium phản ứng với nước:
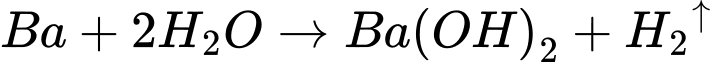
Phân tích các phát biểu
✔️a. Đúng: Dung dịch sau phản ứng bị đục vì có sự tạo thành kết tủa Ca(OH)2, Ba(OH)2 .
❌b. Sai: Mặc dù Ca nhẹ hơn Ba, nhưng Ba phản ứng với nước mạnh hơn Ca. Do đó, mẩu Ba sẽ tan nhanh hơn mẩu Ca.
✔️c. Đúng: Cả Ca và Ba phản ứng với nước, giải phóng khí H2. Điều này chứng minh rằng chúng là các kim loại có thế khử chuẩn âm.
✔️d. Đúng: Dung dịch sau phản ứng có màu hồng do Ca(OH)2 và Ba(OH)2 đều là các base mạnh.

a. Phương trình nhiệt phân muối carbonate của các chất trên là:MCO3
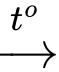 t MO + CO2.
t MO + CO2.b. Độ bền nhiệt của muối tăng từ MgCO3 đến BaCO3.
c. Giá trị biến thiên enthalpy chuẩn của phản ứng lớn hơn 0 nên phản ứngsẽ tỏa nhiệt.
d. Phản ứng nhiệt phân 21 gam MgCO3 tỏa ra nhiệt lượng là 200,14 kJ/mol.
✔️a.Đúng. Đây là phương trình đúng cho phản ứng nhiệt phân muối carbonate của kim loại kiềm thổ (Ca, Sr, Ba, Mg).
✔️b. Đúng.Từ MgCO3 đến BaCO3, bán kính ion kim loại tăng dần, khả năng phân cực giảm, nên độ bền nhiệt tăng.
❌c.Sai. Biến thiên enthalpy chuẩn (ΔH 0 ) của phản ứng dương (>0) có nghĩa là phản ứng thu nhiệt (không tỏa nhiệt).
❌d. Sai.
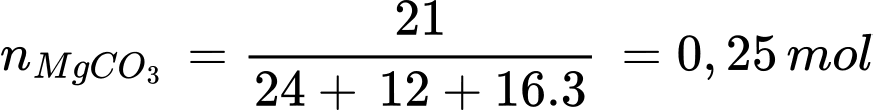
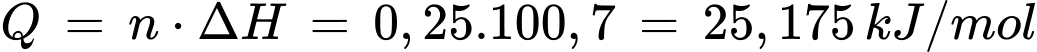
Bước 1: Đặt 2 ống nghiệm vào giá. Thêm khoảng 2 mL dung dịch CaCl2 vào ống nghiệm (1), 2 mL dung dịch BaCl2 vào ống nghiệm (2).
Bước 2: Nhỏ từ từ từng giọt dung dịch CuSO4 vào mỗi ống nghiệm cho đến khi xuất hiện kết tủa.
a. Thí nghiệm trên có thể tiến hành để so sánh độ tan giữa calcium sulfate
và barium sulfate.
b. Ống nghiệm (1) thấy xuất hiện kết tủa nhanh hơn so với ống nghiệm (2).
c. Nếu thay dung dịch CuSO4 bằng Na2CO3 thì hiện tượng quan sát được là
tương tự.
d. CaSO4 có độ tan lớn hơn độ tan của BaSO4.
✔️a. Đúng.
Vì CaSO4 và có độ tan khác nhau, hiện tượng kết tủa xảy ra sẽ khác biệt, từ đó có thể so sánh được độ tan.❌b. Sai. có độ tan nhỏ hơn rất nhiều, nên kết tủa ở ống (2) (chứa ) sẽ xuất hiện nhanh hơn.
❌c. Sai.Dung dịch CuSO4 có màu xanh, hiện tượng khi phản ứng với BaCl2 và CaCl2 hiện tượng xuất hiện kết tủa trắng mà xanh của dung dịch nhạt dần. Dung dịch không màu cũng tạo kết tủa với và , tương ứng là và BaCO3 màu trắng.
✔️d.Đúng. Theo bảng độ tan, B rất ít tan (gần như không tan), trong khi có độ tan lớn hơn một chút.
Bước 1: Cho khoảng 1 mL dung dịch Na2CO3 1M vào ống nghiệm, thêm tiếp khoảng 1 mL dung dịch CaCl2 1 M, lắc đều.
Bước 2: Thêm tiếp 2 mL dung dịch HCl 2 M vào ống nghiệm, lắc đều.
a. Sau bước 1, thấy xuất hiện kết tủa có màu trắng hơi xanh.
b. Sau bước 2 thấy kết tủa tan dần, sủi bọt khí không màu.
c. Thí nghiệm trên tiến hành để nhận biết sự có mặt của ion Ca2+.
d. Nếu thay dung dịch CaCl2 bằng Ca(NO3)2 thì hiện tượng quan sát đượclà tương tự.
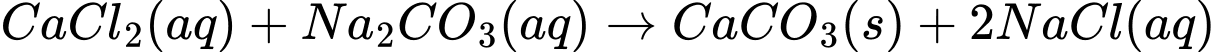
Bước 2. Phản ứng:
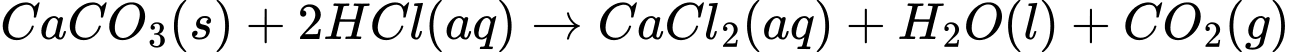
Phân tích các phát biểu:
❌a. Sau bước 1, kết tủa trắng là do sự tạo thành CaCO3 (canxi cacbonat) từ phản ứng giữa Na2CO3 và CaCl2.
✔️b. Sau khi thêm HCl, kết tủa tan và khí CO2 được giải phóng, gây hiện tượng sủi bọt khí không màu.
✔️c. Thí nghiệm này giúp nhận biết ion Ca2+, vì chỉ có ion Ca2+ mới tạo kết tủa trắng với Na2CO3 và tan khi có HCl.
✔️d. Nếu thay CaCl2 bằng Ca(NO3)2, phản ứng vẫn xảy ra tương tự vì ion Ca2+ từ cả hai muối đều có khả năng tạo kết tủa với Na2CO3 và phản ứng với HCl.
- Dung dịch chất X và chất Y đều làm dung dịch phenolphthalein chuyển sang màu hồng.
- Trộn X và Y thu được kết tủa màu trắng.
- Chất X cháy với ngọn lửa màu lục trên đèn khí, trong khi chất Y cháy với ngọn lửa màu tím.
Biết mỗi chất X, Y đều chỉ chứa một loại cation và một loại anion.
a. Chất X có chứa cation Ba2+, chất Y chứa cation K+.
b. Chất X không thể là barium chloride.
c. Chất Y phải là potassium carbonate.
d. Kết tủa màu trắng phải là hợp chất của barium.
=> X và Y đều là các chất bazơ, cụ thể là các dung dịch chứa ion OH−
- Khi trộn dung dịch X và Y, thu được kết tủa màu trắng:
=> Kết tủa màu trắng có thể là một muối ít tan
- Ngọn lửa màu lục đặc trưng cho ion Ba2+ (barium).
- Ngọn lửa màu tím đặc trưng cho ion K+ (potassium).
Phân tích các phát biểu:
✔️(a) Đúng vì X cháy cho ngọn lửa màu lục, Y cháy cho ngọn lửa màu tím.
✔️(b) Đúng vì X chuyển phenolphtalein sang màu hồng.
❌(c) Sai, Y có thể là KHCO3, K2SO3, K3PO4…
✔️(d) Đúng vì các hợp chất của K (Y) tan trong nước.
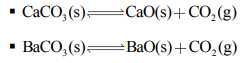
Biến thiên enthalpy chuẩn
 của phản ứng thuận ở mỗi cân bằng (1) và (2) khi phân huỷ 1 mol mỗi chất lần lượt có giá trị là 108,7 kJ và 271,5 kJ.A
của phản ứng thuận ở mỗi cân bằng (1) và (2) khi phân huỷ 1 mol mỗi chất lần lượt có giá trị là 108,7 kJ và 271,5 kJ.Aa. Nhiệt lượng toả ra khi phân huỷ 1 mol BaCO3 lớn hơn nhiệt lượng toảra khi phân huỷ 1 mol CaCO3.
b. BaCO3 bị phân huỷ ở nhiệt độ cao hơn CaCO3.
c. Khi tăng nhiệt độ, cả hai phản ứng đều dịch chuyển theo chiều thuận.
d. CO2 cần được lấy ra khỏi lò nung để tăng hiệu suất của phản ứng.
❌a.Sai. Tiêu chuẩn enthalpy biến thiên của phản ứng phân hủy BaCO3 là 271,5 kJ/mol > CaCO3 là 108,7 kJ/mol. Do đó, nhiệt lượng toả khi phân hủy 1 mol BaCO3 > 1 mol CaCO3.Nhưng 2 phản ứng là phản ứng thu nhiệt, không phải tỏa nhiệt.
✔️b. Đúng. Phản ứng BaCO3 có enthalpy giá trị cao hơn, điều này cho thấy BaCO3 cần có nhiệt độ cao hơn để phân hủy so với CaCO3.
✔️c. Đúng. Cả 2 là phản ứng thu nhiệt ( enthalpy > 0 ). Khi nhiệt độ tăng, cả hai phản ứng đều dịch chuyển theo chiều thuận.
✔️d. Đúng.Việc loại bỏ CO2 sẽ làm giảm nồng độ CO2 trong hệ, cân bằng dịch chuyển theo chiều tăng nồng độ CO2, nghĩa là chiều thuận.
Cho dãy chuyển hóa sau: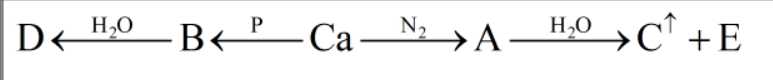
a. Sản phẩm E thu được trong dung dịch gọi là nước vôi trong.
b. Quan sát màu có thể phân biệt được hai khí C và D.
c. Các phản ứng xảy ra trong dãy chuyển hóa đều là phản ứng oxi hóa - khử.
d. Khí D có khả năng tự bốc cháy trong không khí khi có mặt P2H4
(1)
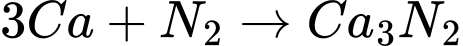 (A)
(A)(2)
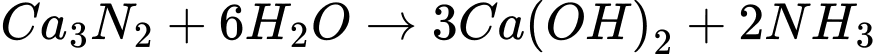 (C)
(C)(3)
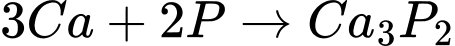 (B)
(B)(4)
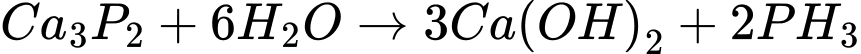
Phân tích các phát biểu:
✔️a. Đúng. Sản phẩm E ( Ca(OH)2) thu được trong dung dịch gọi là nước vôi trong.
❌b.Sai. Quan sát màu không thể phân biệt được hai khí C và D do cả 2 đều không màu.
❌c. Sai. Các phản ứng xảy ra trong dãy chuyển hóa có 2 phản ứng là phản ứng oxi hóa - khử là 1 và 3.
✔️d. Đúng. Khí D là PH3 có khả năng tự bốc cháy trong không khí khi có mặt P2H4
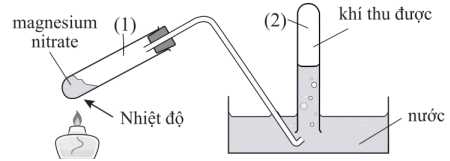
Thu lấy ống nghiệm (2) chứa sản phẩm khí, đưa một que diêm đang cháy lên miệng ống nghiệm và quan sát. Đồng thời tiến hành đo giá trị pH của dung dịch trong máng.
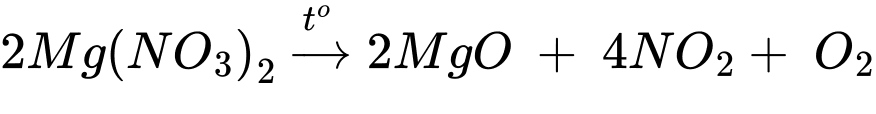
Phân tích các phát biểu:
❌ (a) Sai. Sau phản ứng nhiệt phân hoàn toàn chất rắn còn lại trong ống nghiệm (1) là oxide kim loại MgO.
❌ (b) Sai. Khí thu được trong ống nghiệm (2) là hỗn hợp NO2 và O2. O2 duy trì sự cháy, do đó que diêm có thể bùng cháy mạnh hơn nếu có đủ lượng O2.
✔️ (c) Đúng. Giá trị pH của dung dịch trong máng sau khi nung nóng sẽ nhỏ hơn 7 nguyên nhân có phản ứng hình thành nitric acid.
2H2O + O2 + 4NO2 ⟶ 4HNO3
✔️ (d) Đúng. Tỉ lệ của các chất khí sinh ra ở ống nghiệm (1) 1:4 ứng với O2 và NO2 khác với ở ống nghiệm (2) sau phản ứng của NO2 và O2 với nước tạo ra HNO3 còn lại khí NO và O2.
2H2O + O2 + 4NO2 ⟶ 4HNO3
NO2 + H2O ⟶ HNO3 + NO
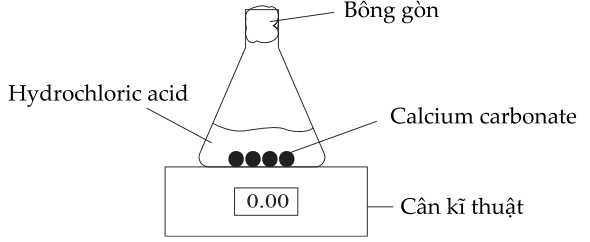
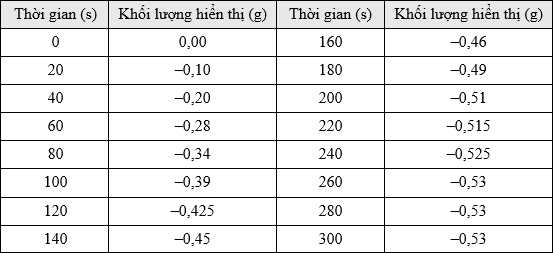
Bình chứa hydrochloric acid được đặt trên một chiếc cân kỹ thuật số. Thêm calcium carbonate và cân ngay lập tức được đặt về số 0. Các phép đo được thực hiện sau mỗi 20 giây và giá trị hiển thị trên cân kỹ thuật số được ghi lại.
Thể tích khí sinh ra được đưa vào một quả bóng bay. Giả sử các thí nghiệm đều được đo ở điều kiện chuẩn.
✔️A. Đúng. Khối lượng bị mất trong quá trình thí nghiệm. Nguyên do HCl phản ứng với CaCO3 tạo ra khí CO2 làm giảm khối lượng.
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
✔️B. Đúng.
Sau khi kết thúc phản ứng là thì khối lượng giảm 0,53 gam là khối lượng của CO2 thoát ra
Số mol của CO2 là nCO2 = 0,53:44 = 0,01205 mol
Thể tích khí CO2 là VCO2 = 0,01205.24,79 = 0,298 L
❌C. Sai. Trong 40 giây đầu tiên từ 0-20, 2-40s tốc độ phản ứng xảy ra nhanh nhất.
❌D. Sai. Từ số liệu ta nhận thấy khi thời gian phản ứng đến giây thứ 260 thì phản ứng đã dừng.
- Hợp chất Q là muối carbonate trung hòa của kim loại nhẹ hơn Al, được kết hợp với Al tạo các bộ phận máy bay, vỏ ô tô.
- Hợp chất R được sử dụng làm vật liệu xây dựng. Nung R ở nhiệt độ cao tạo thành hợp chất S, hydrate hóa S tạo thành hợp chất T có thể dùng khử chua, làm mềm nước cứng.
a. Tổng số nguyên tử trong phân tử chất Q và chất R là bằng nhau.
b. Khối lượng phân tử của Q lớn hơn khối lượng phân tử của R.
c. Nguyên tố kim loại trong S phản ứng với nước mãnh liệt hơn nguyêntố kim loại trong Q.
d. Nếu lấy cùng 1 gam chất Q và R tham gia phản ứng với dung dịchHCl thì chất R cần lượng HCl lớn hơn
+ Hợp chất Q là muối carbonate trung hòa của kim loại nhẹ hơn Al và kết hợp với Al tạo các bộ phận máy bay, vỏ ô tô. Đây là đặc trưng của Mg
Q = MgCO3.
+ Hợp chất R được sử dụng làm vật liệu xây dựng, và khi nung R ở nhiệt độ cao tạo thành hợp chất S. Đây là một đặc trưng của vôi sống (CaO), là sản phẩm của quá trình nung CaCO3. Vôi sống được sử dụng rộng rãi trong xây dựng và xử lý nước.
R = CaCO3.
+ Hợp chất S được tạo thành khi nung R (CaCO3) ở nhiệt độ cao, tạo thành CaO. Khi hydrate hóa CaO, nó sẽ tạo ra hợp chất Ca(OH)2, một chất dùng để khử chua và làm mềm nước cứng.
S = CaO.
+ Hợp chất T là sản phẩm hydrate của S, có thể dùng khử chua và làm mềm nước cứng. Hợp chất này chính là Ca(OH)2, chất dùng trong các ứng dụng khử chua đất và làm mềm nước.
T = Ca(OH)2
Phân tích các phát biểu:
✔️a.Đúng. Với Q là MgCO3 có 5 nguyên tử; R là CaCO3 có 5 nguyên tử.
Vậy tổng số nguyên tử trong phân tử của Q và R bằng nhau.
❌b. Sai. Khối lượng phân tử của Q là 84 g/mol < của R là 100 g/mol.
✔️c. Đúng. S có Ca phản ứng với nước mãnh liệt hơn Q có Mg.
❌d. Sai. Vì cả Mg và Ca đều phản ứng với HCl theo tỷ lệ 1:2, nhưng khối lượng phân tử của Ca lớn hơn Mg, do đó, 1 gam Ca sẽ cần ít mol HCl hơn so với 1 gam Mg.
Dạng 3: TRẮC NGHIỆM YÊU CẦU TRẢ LỜI NGẮN
(a) Potassium carbonate và calcium hydroxide.
(b) Sodium phosphate và barium chloride.
(c) Magnesium hydrogencarbonate và sulfuric acid.
(d) Sodium hydrogencarbonate và barium hydroxide.
(e) Barium hydroxide và nitric acid.
Có bao nhiêu phản ứng sau khi kết thúc thu được kết tủa?
Điền đáp án: ..........

(b) Sodium phosphate (Na3PO4)+ barium chloride (BaCl2)
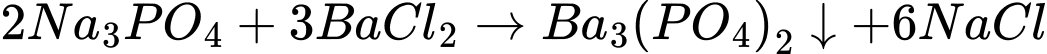
(c) Magnesium hydrogencarbonate (Mg(HCO3)2) + sulfuric acid (H2SO4)
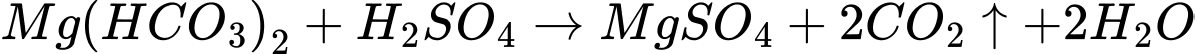
(d) Sodium hydrogencarbonate (NaHCO3) + barium hydroxide (Ba(OH)2)
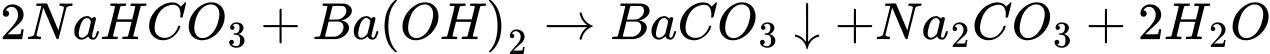
(e) Barium hydroxide (Ba(OH)2) + nitric acid (HNO3)
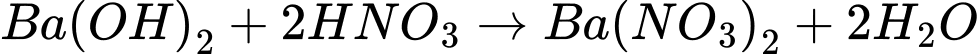
Có 3 phản ứng tạo kết tủa là a,b,d
Điền đáp án: 3
Điền đáp án: ..........
1. Dung dịch NaOH: tạo Ba(OH)2 tan tốt trong nước, do đó không tạo kết tủa với Ba2+.
2. Dung dịch Na2CO3:
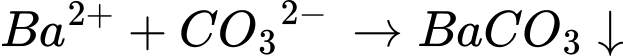
3. Dung dịch K3PO4:
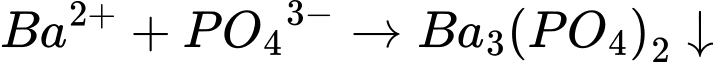 ;
;4. Dung dịch HCl: tạo BaCl2 tan tốt trong nước, không tạo kết tủa.
5. Dung dịch H2SO4:
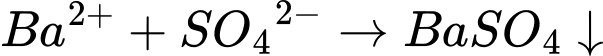
6. Dung dịch NaCl: tạo BaCl2 tan tốt trong nước, không tạo kết tủa.
Có 3 dung dịch có thể dùng để nhận biết Ba2+
Điền đáp án: 3
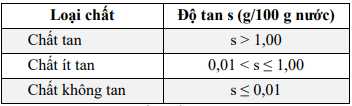
Cho bảng độ tan (g/100 g nước) của một số muối trong nước ở 20 °C như sau:

Có bao nhiêu chất ít tan trong số các chất trên?
Điền đáp án: ..........
=> Có 2 chất ít tan là CaSO4 ( 0,2) và SrSO4 (0,013)
⟹ Điền đáp án: 2
(1) Tiếp tục thêm vào khoảng 10 giọt dung dịch HCl để hòa tan kết tủa, lắc đều.
(2) Thêm từ từ cho đến hết khoảng 10 giọt dung dịch Na2CO3 lắc đều thì xuất hiện kết tủa.
(3) Quan sát màu sắc của kết tủa và hiện tượng các bong bóng khí xuất hiện.
(4) Cho vào ống nghiệm khoảng 2 mL dung dịch CaCl2.
Gán số thứ tự các bước trên theo dãy bốn số để có thứ tự quy trình đúng (ví dụ: 1234, 4321, ...).
Bước 1: Cho vào ống nghiệm khoảng 2 mL dung dịch CaCl2 ⟶ (4)
Bước 2: Thêm từ từ cho đến hết 10 giọt dung dịch Na2CO3 lắc đều thì xuất hiện kết tủa ⟶ (2)
Bước 3: Tiếp tục thêm vào khoảng 10 giọt dung dịch HCl để hòa tan kết tủa, lắc đều ⟶ (1)
Bước 4: Quan sát màu sắc của kết tủa và hiện tượng các bong bóng khí xuất hiện ⟶ (3)
⇒ Điền đáp án: 4213
Điền đáp án: ..........
1. Phân bón ammonium sulfate (NH4)2SO4 là chất có tính acid khi tan trong nước, làm tăng tính acid của đất => pH giảm.
2. Muối ăn NaCl là muối trung tính, không ảnh hưởng đáng kể đến pH của đất => không ảnh hưởng tới pH.
3. Đá vôi CaCO3 là chất có tính kiềm yếu, có khả năng ổn định pH trong đất => tăng pH.
4. Vôi sống CaO là oxit bazơ mạnh, phản ứng với nước tạo thành Ca(OH)2, có tính kiềm mạnh, trung hòa acid hiệu quả => tăng pH.
5. Vôi tôi Ca(OH)2 là bazơ mạnh, có khả năng trung hòa acid => tăng pH.
6. Soda Na2CO3 là muối có tính kiềm, tan trong nước tạo môi trường base, có thể trung hòa acid => tăng pH.
7. Baking soda NaHCO3 là muối axit yếu, nhưng có tính kiềm nhẹ, có thể trung hòa acid yếu => tăng pH.
8. Phèn nhôm KAl(SO4)2⋅12H2O. Khi tan trong nước, giải phóng ion H+ làm tăng tính acid của đất => giảm pH
- Al3+ + H2O → Al(OH)2+ + H+
9. Phèn sắt FeSO4⋅7H2O.Khi tan trong nước, giải phóng ion H+ làm tăng tính acid của đất => giảm pH.
- Fe2+ + H2O → FeOH+ + H+
=> Các chất có thể làm tăng pH của đất là: 3,4,5,6,7
Điền đáp án: 5
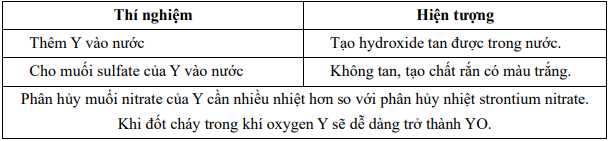
Nguyên tử khối của Y là bao nhiêu?
Điền đáp án: ..........
2. Cho muối sulfate của Y vào nước: tạo kết tủa trắng => Có thể là SrSO4, BaSO4. Do CaSO4 là chất in tan, tan một phần trong nước => Y không thể là Ca.
3.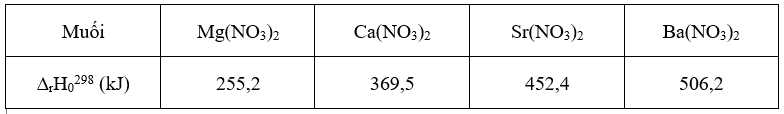
- Phân hủy nhiệt nitrate của Y cần nhiều nhiệt hơn so với Sr => Y nhẹ hơn Sr vì kim loại nhẹ hơn cần nhiệt độ cao hơn để phân hủy nitrate. => Ba
4. Đốt cháy dễ tạo thành YO => BaO
=> Nguyên tử khối của Ba là 137
Điền đáp án: 137
 MgO(s) + CO2(g)
MgO(s) + CO2(g)Nhiệt tạo thành chuẩn của MgCO3(s), MgO(s) và CO2(s) lần lượt là –1096 (kJ.mol-1); –601,8 (kJ.mol-1) và –393,5 (kJ.mol-1) (làm tròn kết quả đến hàng đơn vị).
Điền đáp án: ..........
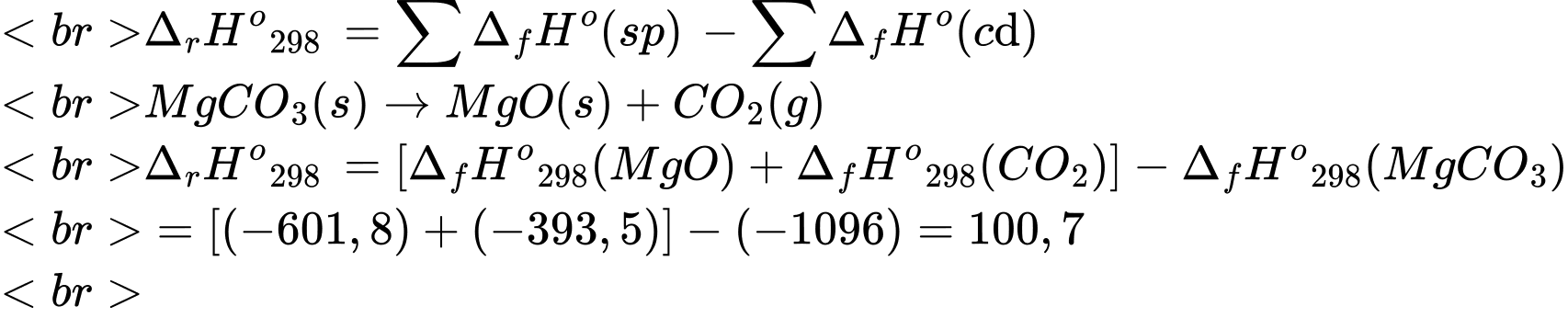
Điền đáp án: 101
 CaO(s) + CO2(g)
CaO(s) + CO2(g)Nhiệt tạo thành chuẩn của CaCO3(s), CaO(s) và CO2(s) lần lượt là –1207,6 (kJ.mol-1); –634,9 (kJ.mol-1) và –393,5 (kJ.mol-1). Năng lượng cần cung cấp (kJ) để quá trình phân hủy 200 g CaCO3 ở điều kiện chuẩn là bao nhiêu? (làm tròn tới hàng đơn vị).
Điền đáp án: ..........
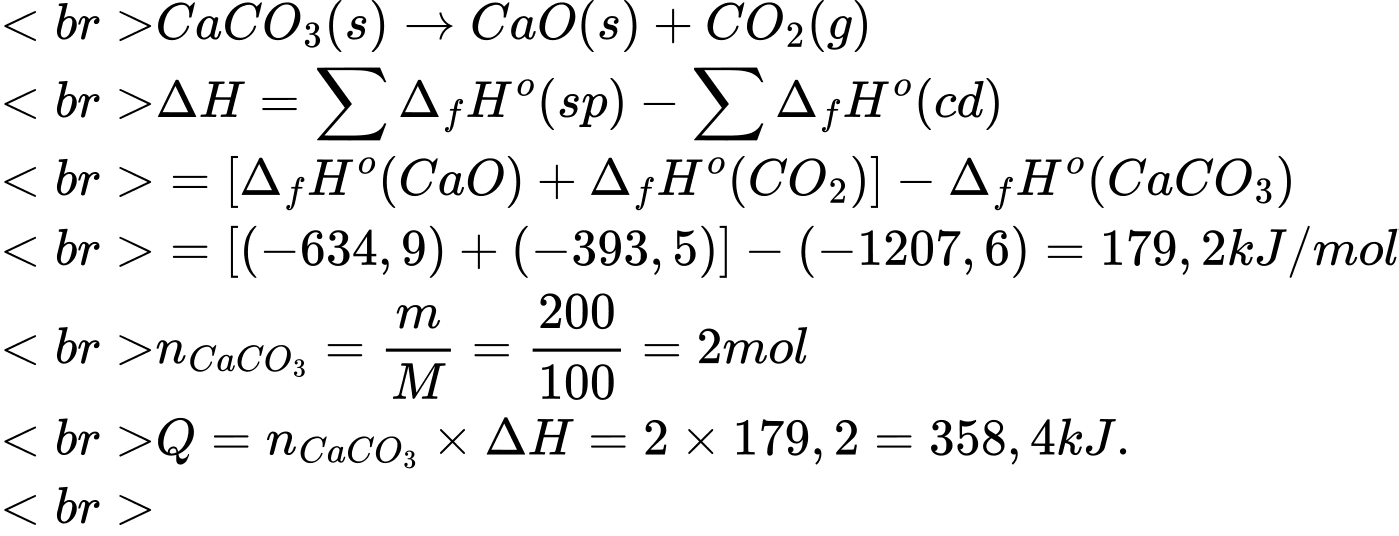
Điền đáp án: 358
Điền đáp án: ..........
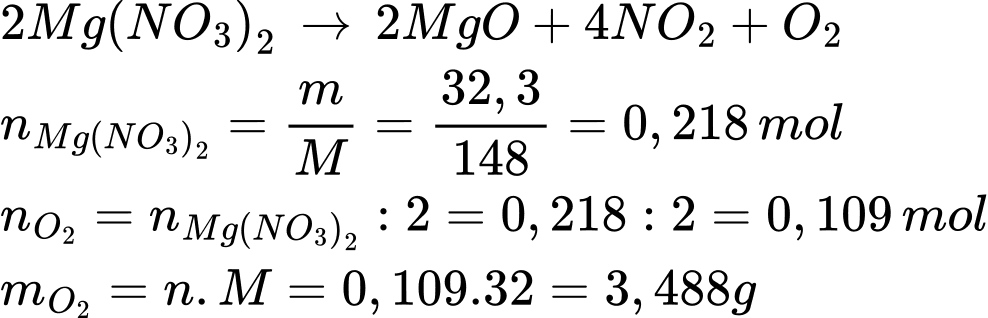
Điền đáp án: 3,5
Điền đáp án: ..........
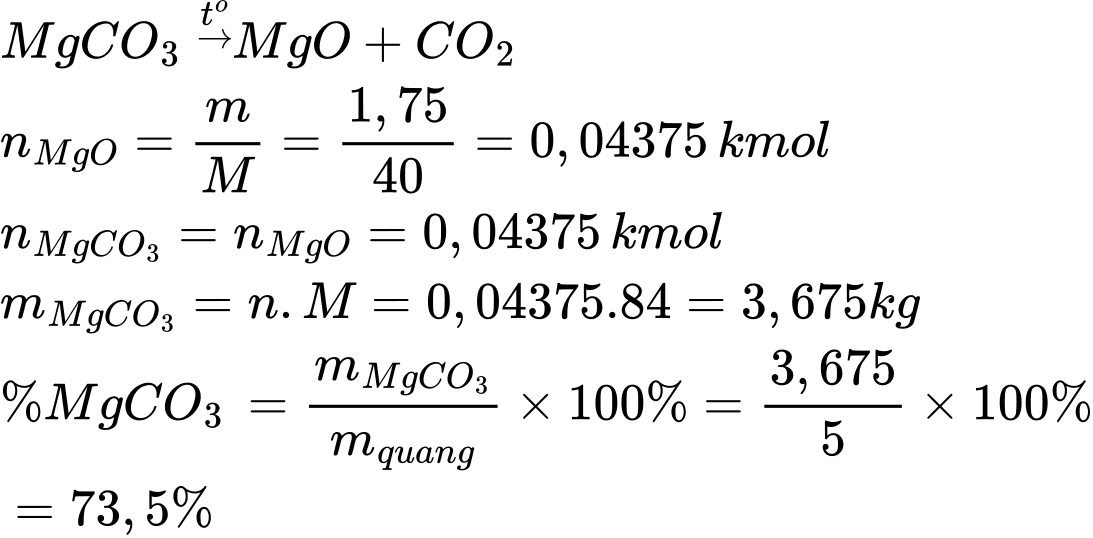
Điền đáp án: 73,5
 SrO(s) + N2(g) + 2CO2(g) + CO(g)
SrO(s) + N2(g) + 2CO2(g) + CO(g)Thể tích khí thoát ra (đkc) khi trộn 10,6 gam stronium nitrate với hỗn hợp pháo hoa.(làm tròn đến phần chục).
Điền đáp án: ..........
Số mol của Sr(NO3)2
n =10.6 : 211.6 = 0.05 mol.
Theo phương trình, số mol khí sinh ra:
nkhí = 4×nSr(NO3)2 = 4×0.05 = 0.2 mol.
V = nkhí×24,79 = 0,2.24,79 = 4,958L
Điền đáp án: 5,0
Điền đáp án: ..........
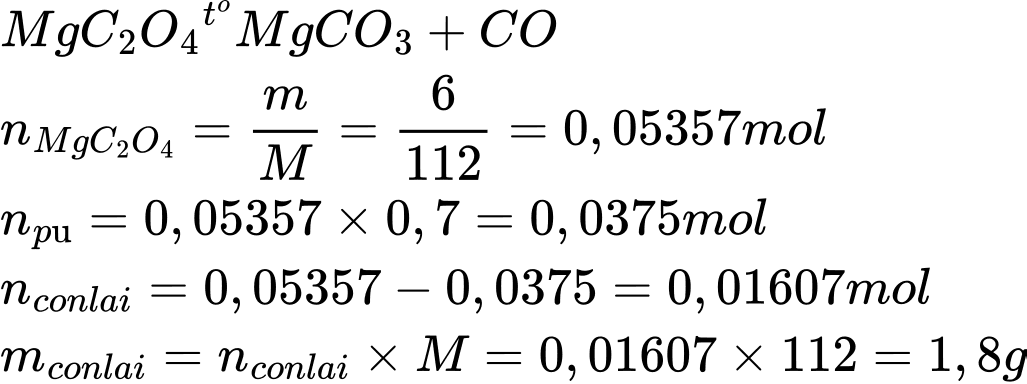
Điền đáp án: 1,8
Điền đáp án: ..........
m Ba(NO3)2 = x
⟹x : ( 109,02 – x ) × 100 = 9,02
⟹ m Ba(NO3)2 = x = 9,02 g
⟹m H2O = 100g
Gọi số mol Ba(NO3)2 .6H2O kết tinh là a
Ở 10oC, m Ba(NO3)2 = 9,02 - 261a
⟹ m H2O = 100 – 6ax18
⟹ ( 9,02 – 261a ) : ( 100 – 6× 18a ) × 100 = 6,67
⟹ A = 9,26 × 10 -3
Vậy khối lượng Ba(NO3)2 .6H2O kết tinh là : 369a = 3,42 g
Điền đáp án: 3,42

Tiến hành làm lạnh 200 gam dung dịch BaCl2 bão hòa từ 100 oC xuống 20 oC. Phần dung dịch còn lại ở 20 oC có khối lượng 163 gam và chất rắn tách ra là BaCl2.nH2O. Giá trị của n là bao nhiêu (Làm tròn đến số nguyên)?
100 gam nước sẽ hòa tan tối đa là 59,4 gam BaCl2 thu được 159,4 gam dung dịch BaCl2
Vậy 200 gam dung dịch BaCl2 bão hoà sẽ chứa
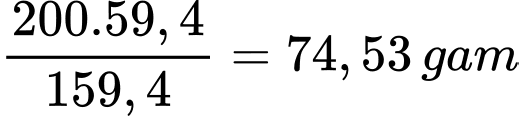
Tại 20oC
100 gam nước sẽ hòa tan tối đa là 35,8 gam BaCl2 thu được 135,8 gam dung dịch BaCl2
Vậy 163 gam dung dịch BaCl2 sẽ hòa tan tối đa là
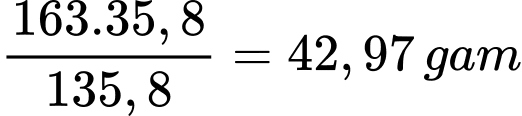
Khối lượng BaCl2 tách ra là 74,53 – 42,97 = 31,56 gam.
Khối lượng H2O tách ra là 200 – 163 – 31,56 = 5,44 gam.
→ Số mol BaCl2 tách ra là nBaCl2 = 31,65:208 = 0,1517 mol
Số mol H2O tách ra là nH2O = 5,44:18 = 0,3022 mol
Ta thấy: nH2O : nBaCl2 = 0,3022:0,1517 ≈ 2
Công thức chất rắn BaCl2. 2H2O.
⟹Điền đáp án : 2
Điền đáp án: ..........
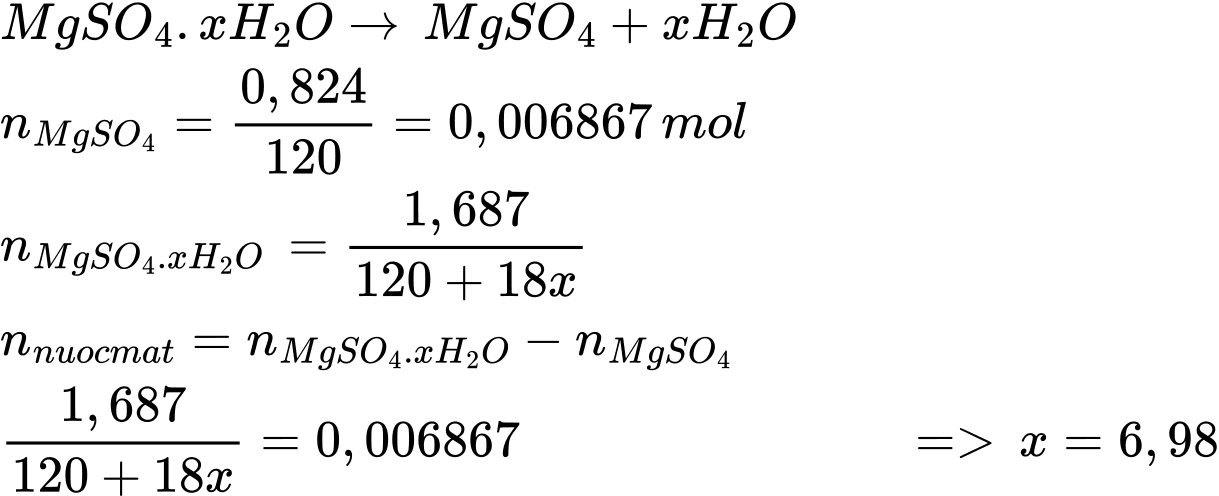
Điền đáp án: 7
CaO(s) + 2NH4Cl(s)
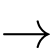 2NH3(g) + H2O(g) + CaCl2(s)
2NH3(g) + H2O(g) + CaCl2(s)Nếu trộn 112 gam CaO và 224 gam NH4Cl để thực hiện phản ứng nhưng chỉ thu được 16,3 gam NH3 thì hiệu suất của phản ứng là bao nhiêu? (làm tròn đến hàng đơn vị)
Điền đáp án: ..........
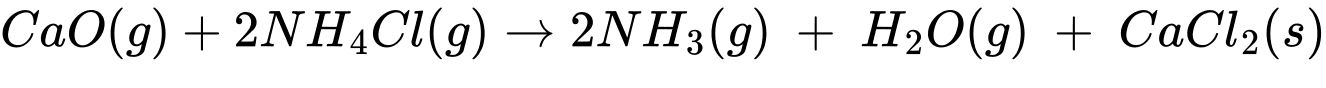
Số mol của CaO và NH4Cl lần lượt là
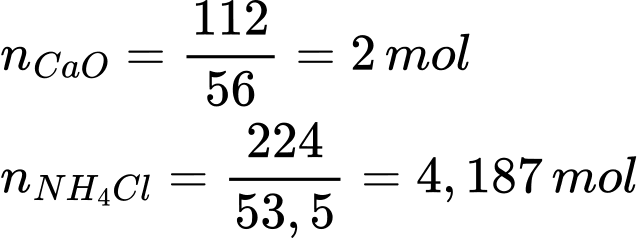
Ta có:
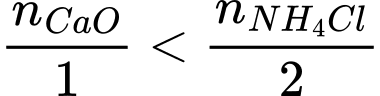
→ CaO hết, NH4Cl dư
Từ phương trình hóa học số mol của NH3 là: nNH3 = 2nCaO = 4 mol
Hiệu suất của phản ứng là:
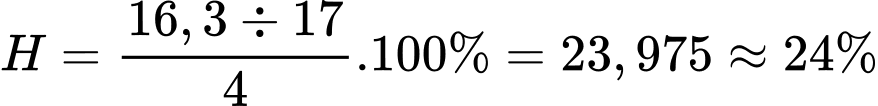
⇒ Điền đáp án: 24
CaCO3(s)
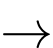 CaO (s) + CO2(g)
CaO (s) + CO2(g)Lấy 1,506 g mẫu đá vôi trên nung nóng thì thu được 0,558 g CO2. Phần trăm khối lượng của CaCO3 trong mẫu đá vôi là bao nhiêu? (làm tròn tới hàng phần mười)
Điền đáp án: ..........
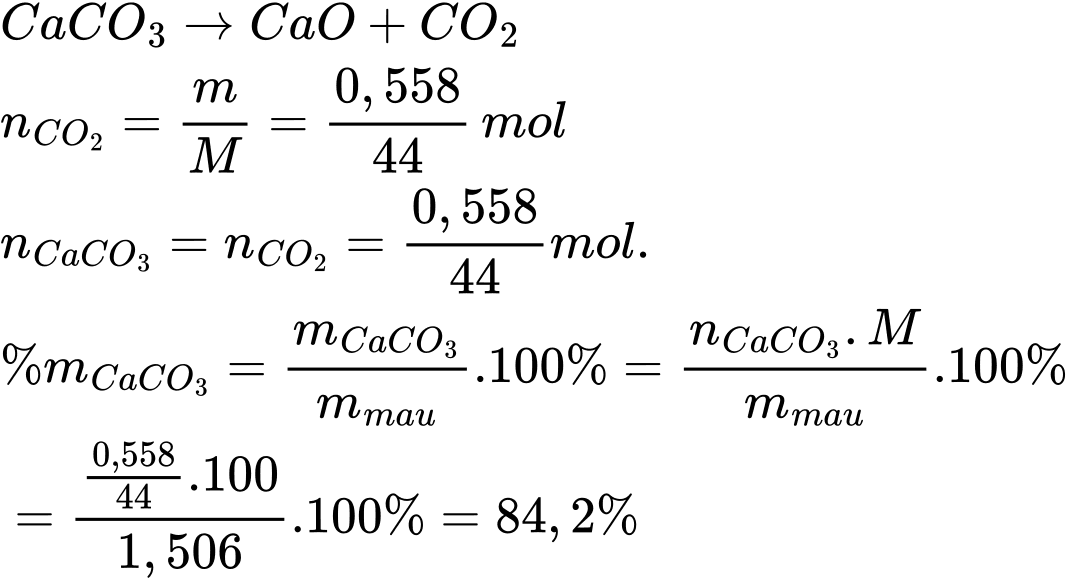
Điền đáp án: 84,2
2Al(s) + 3Ca(OH)2(s) + 6 H2O(l)
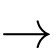 3CaO.Al2O3.6H2O(s) + 3H2(g)
3CaO.Al2O3.6H2O(s) + 3H2(g)Giả sử hỗn hợp các chất phản ứng chứa 0,56 g Al và lượng calcium hydroxide, nước dùng dư cho mỗi viên gạch. Thế tích khí hydrogen tối đa có thể tạo ra ở điều kiện chuẩn là bao nhiêu?
(Làm tròn đến hai chữ số thập phân)
Điền đáp án: ..........
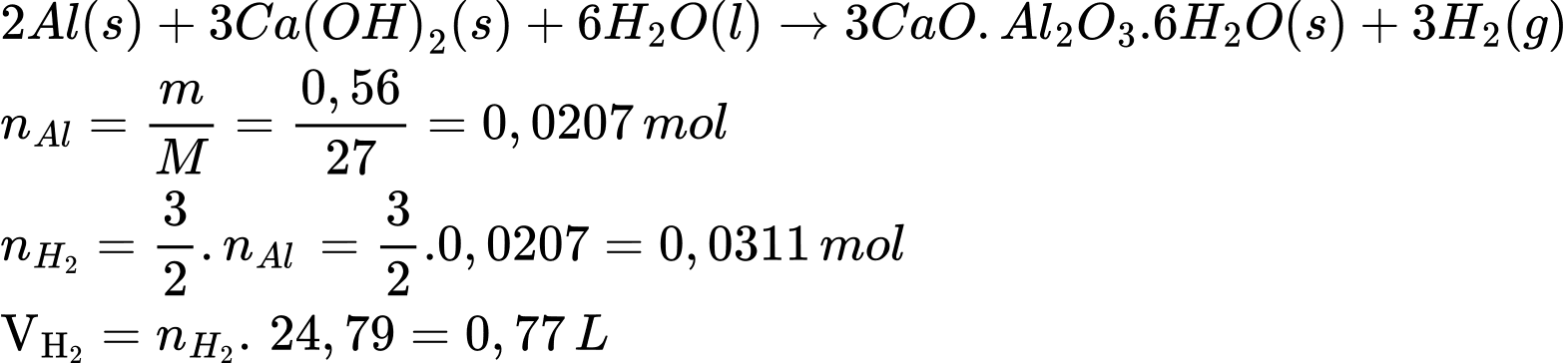
Điền đáp án: 0,77
Ca(OCl)2 + 2H2O → 2HClO + Ca(OH)2
Calcium hypochlorite phản ứng với nước tạo hypochlorous acid là một tác nhân hoạt động. Ở pH bằng 7,0 có 27,5% acid ion hoá thành ion hypochlorite không hoạt động. Phần hypochlorous acid còn lại (72,5%) chuyển thành chlorine dùng làm sạch hồ bơi.Trong hồ bơi, mức chlorine được duy trì ở 3 ppm. Cần bao nhiêu gam calcium hypochlorite để thêm vào hồ chứa 80 m3 nước để mức chlorine đạt tiêu chuẩn vệ sinh là 3 ppm ở pH bằng 7,0? Biết 1 ppm = 1 g chlorine trên 1 m3 nước (Làm tròn đến số nguyên).
Khối lượng chlorine trong hồ bơi là 80.3 = 240 gam
Bảo toàn nguyên tố Cl: nCl = nHClO = 240 : 35,5 = 480/71 mol
số mol của HClO ban đầu là
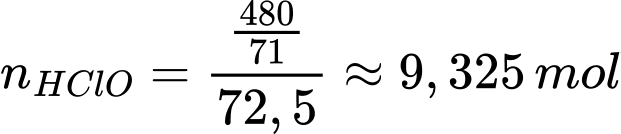
Từ phương trình số mol của Ca(OCl)2 là 4,6625 mol
Khối lượng của Ca(OCl)2 cần dùng là mCa(OCl)2 = 4,6625.143 = 666,7375 gam = 667 gam
Điền đáp án: 667
Bước 1: Lấy 1,0 gam và trứng khô, đã được làm sạch, hòa tan hoàn toàn trong 50 mL dung dịch HCl 0,4 M. Lọc dung dịch sau phản ứng thu được 50 mL dung dịch X.
Bước 2: Lấy 10,0 mL X cho vào bình tam giác, thêm 1 – 2 giọt phenolphthalein.
Bước 3: Tiếp theo nhỏ từng giọt dung dịch NaOH 0,1M vào bình tam giác đến khi dung dịch xuất hiện màu hồng thấy hết 5,6 mL dung dịch NaOH.
Giả thiết các tạp chất khác trong vỏ trứng không tác dụng với HCl. Xác định hàm lượng CaCO3 có trong vỏ trứng.
Số mol của HCl ban đầu là nHCl = 0,05.0,4 = 0,02 mol
Số mol của NaOH là nNaOH = 0,0056.0,1 = 0,00056 mol
(1) 2HCl + CaCO3 → CaCl2 + H2O + CO2
(2) HCl + NaOH → NaCl + H2O
Số mol HCl tham gia phản ứng trong pt(1) là
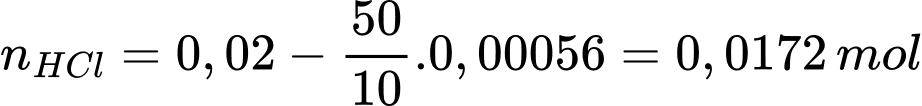
Từ PTHH (1) số mol của CaCO3 là n CaCO3 = 0,0086 gam
Hàm lượng CaCO3 trong vỏ trứng là
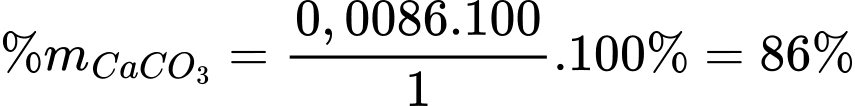
⟹Điền đáp án : 86
2KMnO4 + 5CaC2O4 + 8H2SO4 → 5CaSO4 + K2SO4 + 2MnSO4 + 10CO2 + 8H2O
Giả sử calcium oxalate kết tủa từ 1 mL máu một người tác dụng vừa hết với 1,95 mL dung dịch potassium permanganate (KMnO4) 4,98×10–4 M. Xác định nồng độ ion calcium trong máu người đó bằng đơn vị mg Ca2+/100 mL máu (Làm tròn đến hàng phần trăm).
Đổi 1,95 mL = 0,00195 L
Số mol của KMnO4 là nKMnO4 = 0,00195,4,98.10-4 = 9,711.10-7 mol
Số mol Ca2+ trong 1 mL máu là nCa2+ = 9,711.10-7 × 5 ÷ 2 = 2,42775×10-6 gam
Nồng độ ion calcium trong máu là
mCa2+ (100mL) = 2,422775×10-6 × 40 × 100 = 9,711×10-3 (gam) ≈ 9,71
⟹Điền đáp án : 9,71
Dạng 4: BÀI TẬP ĐỌC HIỂU – đọc thông tin và trả lời các câu hỏi sau đó
Sau khi thu lấy Mg(OH)2 thì cho HCl vào để hòa tan tạo muối chloride của magnesim MgCl2. Vì Mg là kim loại có tính khử mạnh nên để thu được Mg kim loại từ MgCl2 thì cần điện phân nóng chảy. Quá trình sản xuất kim loại Mg từ nước biển được đưa dưới đây:
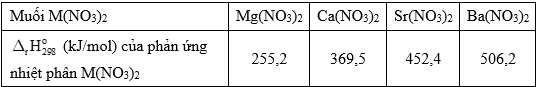
=> Chọn đáp án A Đáp án: A
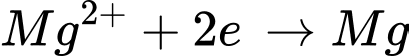
+ Điện cực dương (anode): Ion Cl- bị oxy hóa để tạo thành khí Cl2.
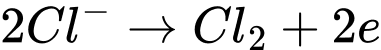
Phương trình tổng quát:
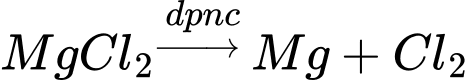
Ở cathode thu được Mg
Chọn đáp án B Đáp án: B
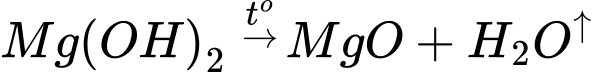
Điện phân MgO:
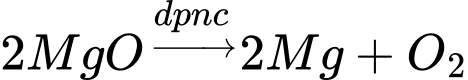
X là MgO
=> Chọn đáp án B Đáp án: B
Dạng 5: CÂU HỎI TỰ LUẬN
∎ Bước 1: Trộn dung dịch của hai chất X và Y theo tỉ lệ hợp thức thì có 1,25 g kết tủa được tạo thành, chứa một muối của kim loại M (hóa trị II).
∎ Bước 2: Lọc, tách riêng phần kết tủa và phần dịch lọc.
∎ Bước 3: Nung nóng kết tủa đến 1100 oC thì kết tủa bị phân hủy thành 0,70 g oxide kim loại rắn MO và một oxide khí K.
∎ Bước 4: Làm bay hơi phần dịch lọc, còn lại một chất rắn D nặng 2,0 g, chất này tạo thành hai sản phẩm khi phân hủy nhiệt ở 215 oC gồm một oxide khí L và 0,90 g hơi nước. Tổng thể tích hỗn hợp khí và hơi là 1,86 L (đkc).
a) Viết các phương trình phản ứng.
b) Xác định công thức của X, Y, M, K, L, D.
Chất rắn B
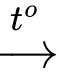 Chỉ gồm 2 sản phẩm (Oxide khí L + Hơi nước).
Chỉ gồm 2 sản phẩm (Oxide khí L + Hơi nước).Ta có:
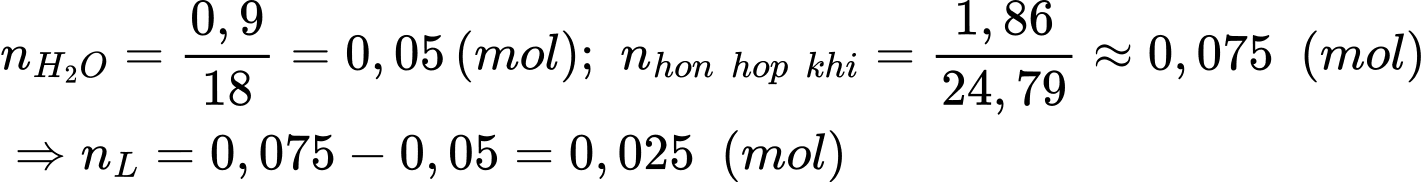
Áp dụng định luật bảo toàn khối lượng:
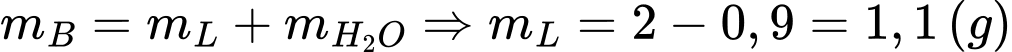
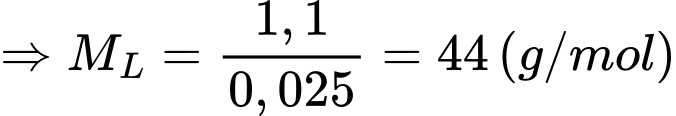 ⟶ Vậy khí L là N2O, chất rắn B là NH4NO3.
⟶ Vậy khí L là N2O, chất rắn B là NH4NO3.PTHH: NH4NO3
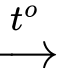 N2O + 2H2O
N2O + 2H2O• Ở bước 3: Kết tủa
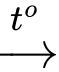 Oxide kim loại (MO) + Oxide khí K.⟶ Kết tủa là muối carbonate của kim loại M (MCO3).
Oxide kim loại (MO) + Oxide khí K.⟶ Kết tủa là muối carbonate của kim loại M (MCO3).• Ở bước 1: Trộn X + Y ⟶ MCO3 (1,25 gam) + NH4NO3.⟶ X và Y có công thức là M(NO3)2 và (NH4)2CO3.
PTHH: M(NO3)2 + (NH4)2CO3 ⟶ MCO3 + 2NH4NO3.
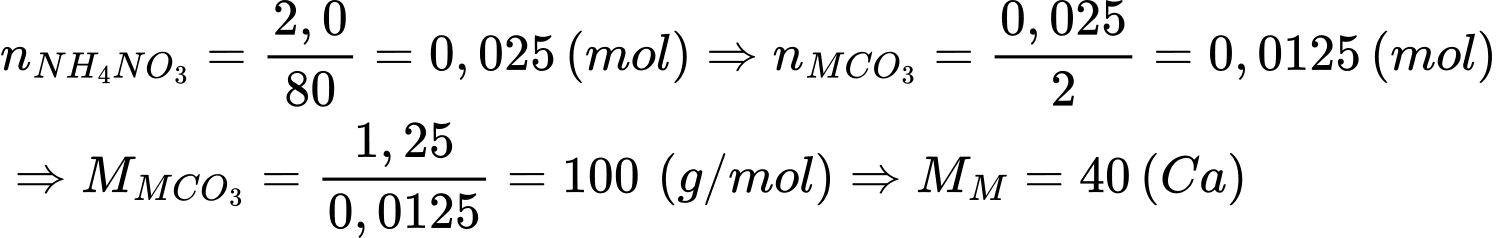
Các PTHH xảy ra:
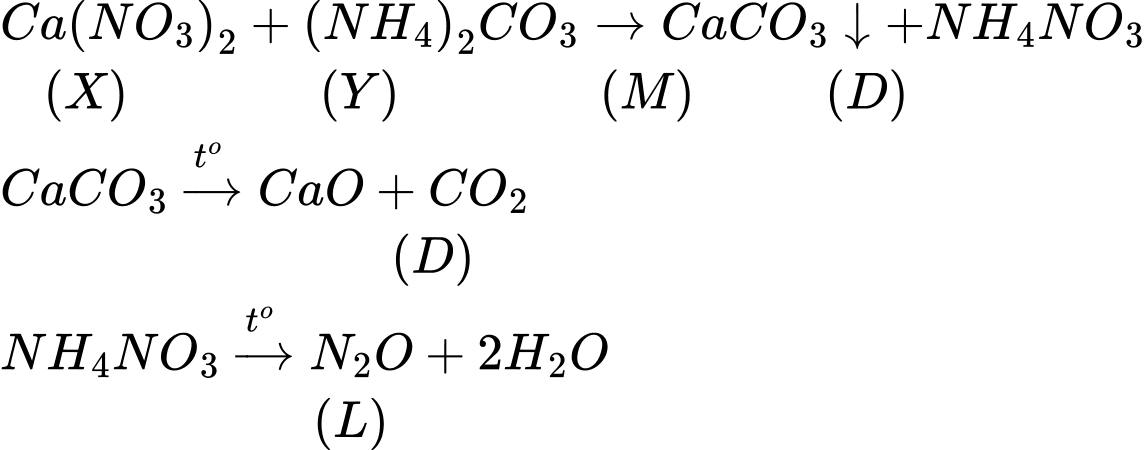
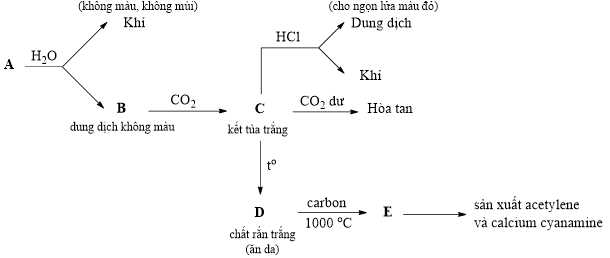
a) Viết các phương trình phản ứng.
b) Hợp chất đốt cháy trên ngọn lửa đèn Bunsen cho màu đỏ gạch có thể là hợp chất của ion kim loại nào?
c) Xác định công thức của A, B, C, D, E.
• Phương trình hoá học: