Câu 1 [680879]: Khi bảo quản trong phòng thí nghiệm, muối Mohr (FeSO4.(NH4)2SO4.6H2O) bị hút ẩm và bị oxi hóa một phần bởi O2 trong không khí thành hỗn hợp X. Để xác định phần trăm khối lượng muối Mohr trong X, tiến hành hòa tan hoàn toàn 2,656 gam X trong nước rồi pha thành 100,0 mL dung dịch Y. Chuẩn độ 10,00 mL dung dịch Y (trong môi trường sulfuric acid loãng, dư) bằng dung dịch KMnO4 nồng độ 0,012 M đến khi xuất hiện màu hồng nhạt thì dừng. Lặp lại thí nghiệm chuẩn độ thêm 2 lần nữa. Thể tích trung bình của dung dịch KMnO4 sau 3 lần chuẩn độ là 9,72 mL. Phần trăm khối lượng của muối Mohr trong X là a %. Tính giá trị của a (làm tròn đến hàng phần muời).
Phương trình phản ứng:
5Fe2+ + MnO4- + 8H+ → Mn2+ + 5Fe3+ + 4H2O
Đổi 9,72 mL = 0,00972 L
Số mol của KMnO4 là nKMnO4 = 0,00972 × 0,012 = 0,00011664 mol
Từ phương trình hóa học số mol của Fe2+ là 0,0005832 mol
Phần trăm khối lượng của muối Mohr trong X là
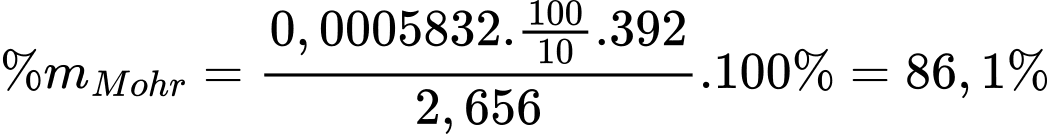
⟹ Điền đáp án 86,1
5Fe2+ + MnO4- + 8H+ → Mn2+ + 5Fe3+ + 4H2O
Đổi 9,72 mL = 0,00972 L
Số mol của KMnO4 là nKMnO4 = 0,00972 × 0,012 = 0,00011664 mol
Từ phương trình hóa học số mol của Fe2+ là 0,0005832 mol
Phần trăm khối lượng của muối Mohr trong X là
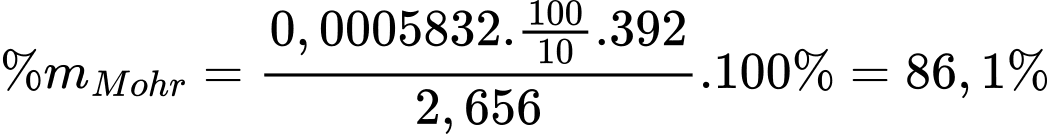
⟹ Điền đáp án 86,1
Câu 2 [830090]: Tiến hành thí nghiệm chuẩn độ dung dịch FeSO4 nồng độ a M theo các bước sau:
Bước 1: Dùng pipette hút chính xác 5,00 mL dung dịch FeSO4 nồng độ a M cho vào bình định mức loại 50 mL. Thêm tiếp nước cất vào bình định mức đến vạch, lắc đều, thu được 50 mL dung dịch Y.
Bước 2: Lấy 10,00 mL dung dịch Y cho vào bình tam giác, thêm H2SO4 loãng. Tiến hành chuẩn độ và ghi kết quả thể tích dung dịch KMnO4 0,02M ở bảng sau:
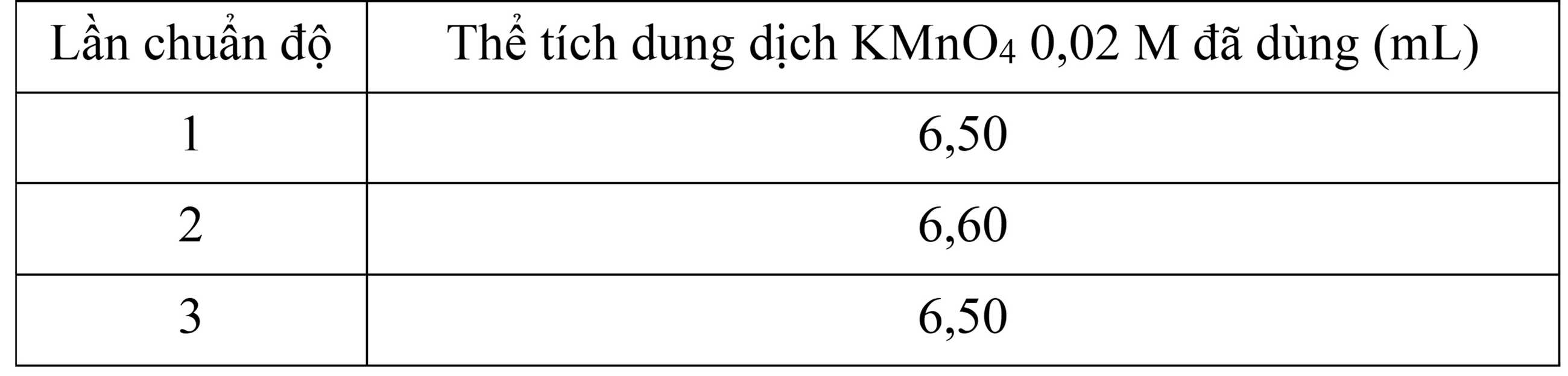
Xác định giá trị của a.
Bước 1: Dùng pipette hút chính xác 5,00 mL dung dịch FeSO4 nồng độ a M cho vào bình định mức loại 50 mL. Thêm tiếp nước cất vào bình định mức đến vạch, lắc đều, thu được 50 mL dung dịch Y.
Bước 2: Lấy 10,00 mL dung dịch Y cho vào bình tam giác, thêm H2SO4 loãng. Tiến hành chuẩn độ và ghi kết quả thể tích dung dịch KMnO4 0,02M ở bảng sau:

Xác định giá trị của a.
Đổi 5 mL = 0,005 L
Thể tích trung bình của KMnO4 là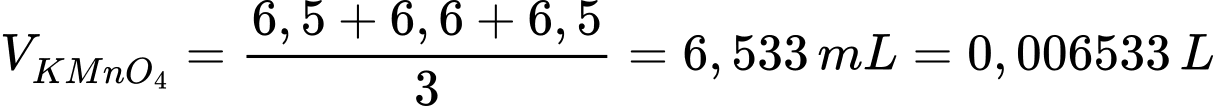
Phương trình phản ứng:
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Số mol của KMnO4 là nKMnO4 = 0,006533 × 0,02 = 0,00013066 mol
Theo phương trình số mol của FeSO4 là 0,0006533 mol
Nồng độ của dung dịch FeSO4 ban đầu là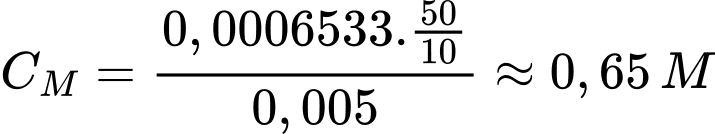
⟹ Điền đáp án 0,65
Thể tích trung bình của KMnO4 là
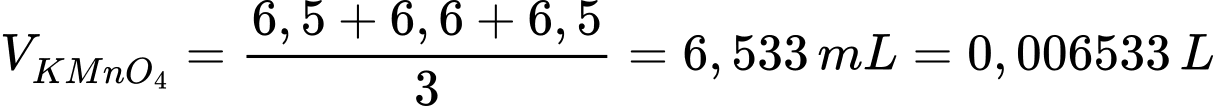
Phương trình phản ứng:
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Số mol của KMnO4 là nKMnO4 = 0,006533 × 0,02 = 0,00013066 mol
Theo phương trình số mol của FeSO4 là 0,0006533 mol
Nồng độ của dung dịch FeSO4 ban đầu là
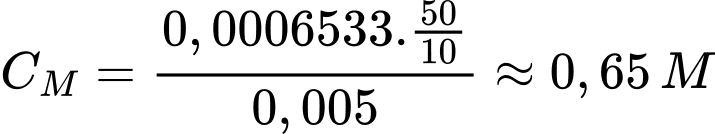
⟹ Điền đáp án 0,65
Câu 3 [830093]: Trong quá trình bảo quản, một mẫu muối FeSO4.7H2O bị oxy hóa bởi oxy không khí tạo thành hỗn hợp X chứa các hợp chất của Fe(II) và Fe(III). Hòa tan toàn bộ X trong dung dịch loãng chứa 0,05 mol H2SO4, thu được 100 mL dung dịch Y. Tiến hành hai thí nghiệm với Y:
Thí nghiệm 1: Cho BaCl2 vào 25 mL dung dịch Y, thu được 0,0425 mol kết tủa.
Thí nghiệm 2: Thêm dung dịch H2SO4 loãng vào 25 mL dung dịch Y, thu được dung dịch Z. Nhỏ từ từ dung dịch KMnO4 0,04 M vào Z đến khi phản ứng vừa đủ thì hết 120 mL.
Tính phần trăm số mol Fe(II) đã bị oxi hóa trong không khí (làm tròn đến hàng đơn vị).
Thí nghiệm 1: Cho BaCl2 vào 25 mL dung dịch Y, thu được 0,0425 mol kết tủa.
Thí nghiệm 2: Thêm dung dịch H2SO4 loãng vào 25 mL dung dịch Y, thu được dung dịch Z. Nhỏ từ từ dung dịch KMnO4 0,04 M vào Z đến khi phản ứng vừa đủ thì hết 120 mL.
Tính phần trăm số mol Fe(II) đã bị oxi hóa trong không khí (làm tròn đến hàng đơn vị).
Thí nghiệm 1:
SO42- + Ba2+ → BaSO4
Bảo toàn gốc SO42- ta có: nFeSO4.7H2O + 0,05 × 25/100 = 0,0425 mol
→ nFeSO4.7H2O = 0,03 mol
Thí nghiệm 2:
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Đổi 120 mL = 0,12 L
Số mol của KMnO4 là nKMnO4 = 0,12 × 0,04 = 0,0048 mol
Theo phương trình số mol của FeSO4 là 0,024 mol
Phần trăm số mol Fe(II) đã bị oxi hóa trong không khí là
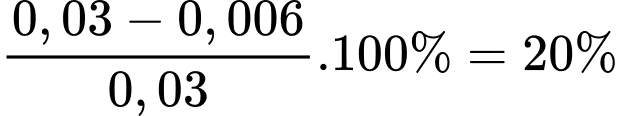 .
.
⟹ Điền đáp án 20
SO42- + Ba2+ → BaSO4
Bảo toàn gốc SO42- ta có: nFeSO4.7H2O + 0,05 × 25/100 = 0,0425 mol
→ nFeSO4.7H2O = 0,03 mol
Thí nghiệm 2:
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Đổi 120 mL = 0,12 L
Số mol của KMnO4 là nKMnO4 = 0,12 × 0,04 = 0,0048 mol
Theo phương trình số mol của FeSO4 là 0,024 mol
Phần trăm số mol Fe(II) đã bị oxi hóa trong không khí là
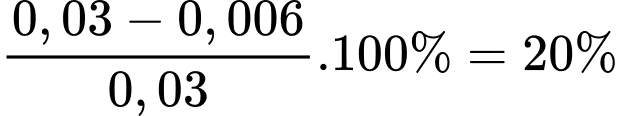 .
. ⟹ Điền đáp án 20
Câu 4 [830091]: Muối Mohr có công thức (NH4)2Fe(SO4)2.6H2O. Để xác định độ tinh khiết của một loại muối Mohr (cho rằng trong muối Mohr chỉ có muối kép ngậm nước nêu trên và tạp chất trơ), một học sinh tiến hành các thí nghiệm sau: Cân chính xác 7,237 gam muối Mohr, pha thành 100 mL dung dịch X. Lấy chính xác 10,0 mL dung dịch X, thêm 10,0 mL dung dịch H2SO4 10%, được dung dịch Y. Chuẩn độ dung dịch Y bằng dung dịch chuẩn KMnO4 0,023 M. Thực hiện chuẩn độ 3 lần. Kết quả đạt được như sau:
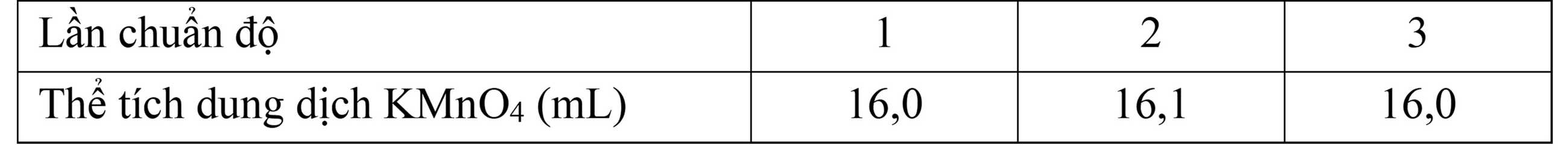
Độ tinh khiết (phần trăm khối lượng (NH4)2Fe(SO4)2.6H2O) của muối Mohr là bao nhiêu (làm tròn đến hàng phần mười)?

Độ tinh khiết (phần trăm khối lượng (NH4)2Fe(SO4)2.6H2O) của muối Mohr là bao nhiêu (làm tròn đến hàng phần mười)?
Đổi 5 mL = 0,005 L
Thể tích trung bình của KMnO4 là
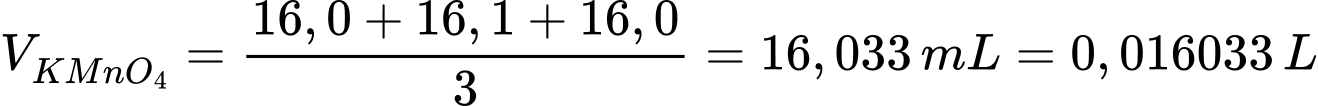
Phương trình phản ứng:
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Số mol của KMnO4 là nKMnO4 = 0,016033 × 0,023 = 0,0003688 mol
Từ phương trình hóa học số mol của FeSO4 là 0,001844 mol
Độ tinh khiết (phần trăm khối lượng (NH4)2Fe(SO4)2.6H2O) của muối Mohr là
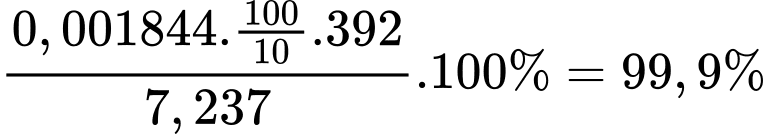
⟹ Điền đáp án 99,9
Thể tích trung bình của KMnO4 là
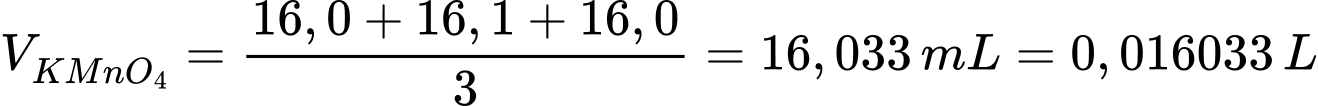
Phương trình phản ứng:
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Số mol của KMnO4 là nKMnO4 = 0,016033 × 0,023 = 0,0003688 mol
Từ phương trình hóa học số mol của FeSO4 là 0,001844 mol
Độ tinh khiết (phần trăm khối lượng (NH4)2Fe(SO4)2.6H2O) của muối Mohr là
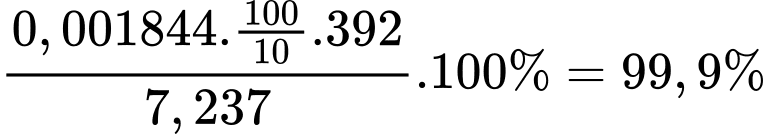
⟹ Điền đáp án 99,9
Câu 5 [830094]: Trong quá trình bảo quản, một mẫu muối FeSO4.7H2O bị oxi hóa bởi oxygen trong không khí tạo thành hỗn hợp X chứa các hợp chất của Fe(II) và Fe(III). Hòa tan hoàn toàn X trong dung dịch loãng chứa 0,05 mol H2SO4, thu được 100 mL dung dịch Y. Tiến hành hai thí nghiệm với dung dịch Y:
▪ Thí nghiệm 1: Cho lượng dư dung dịch Ba(NO3)2 vào 25,0 mL dung dịch Y, thu được 6,99 gam kết tủa.
▪ Thí nghiệm 2: Thêm dung dịch H2SO4 (loãng, dư) vào 25,0 mL dung dịch Y, thu được dung dịch Z. Nhỏ từ từ dung dịch KMnO4 0,1 M vào Z đến khi phản ứng vừa đủ thì hết 30,0 mL. Tính phần trăm số mol Fe(II) đã bị oxi hóa trong không khí (làm tròn đến hàng phần mười).
▪ Thí nghiệm 1: Cho lượng dư dung dịch Ba(NO3)2 vào 25,0 mL dung dịch Y, thu được 6,99 gam kết tủa.
▪ Thí nghiệm 2: Thêm dung dịch H2SO4 (loãng, dư) vào 25,0 mL dung dịch Y, thu được dung dịch Z. Nhỏ từ từ dung dịch KMnO4 0,1 M vào Z đến khi phản ứng vừa đủ thì hết 30,0 mL. Tính phần trăm số mol Fe(II) đã bị oxi hóa trong không khí (làm tròn đến hàng phần mười).
Thí nghiệm 1:
SO42- + Ba2+ → BaSO4
Đặt số mol của FeSO4 và Fe2(SO4)3 trong 25 mL dung dịch lần lượt là a và b mol
Số mol của BaSO4 là nBaSO4 = 6,99 ÷ 233 = 0,03 mol
Bảo toàn gốc SO42- ta có: nFeSO4.7H2O + 0,05 × 25/100 = 0,03 mol
→ nFeSO4.7H2O = 0,0175 mol.
Thí nghiệm 2:
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Đổi 30 mL = 0,03 L
Số mol của KMnO4 là nKMnO4 = 0,03 × 0,1 = 0,003 mol
Theo phương trình số mol của FeSO4 là 0,015 mol
Phần trăm số mol Fe(II) đã bị oxi hóa trong không khí là
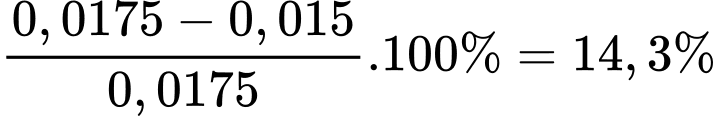 .
.
⟹ Điền đáp án 14,3
Câu 6 [703981]: Sự gia tăng hàm lượng nitrate trong nước là một trong những nguyên nhân của hiện tượng phú dưỡng. Để xác định hàm lượng nitrate trong nước, người ta tiến hành các thí nghiệm như sau:
Thí nghiệm 1: Lấy 10,0 mL dung dịch muối Mohr (NH4)2SO4.FeSO4.6H2O, thêm dung dịch H2SO4 1 M vào và chuẩn độ bằng dung dịch KMnO4.
Thí nghiệm 2: Lấy 10,0 mL dung dịch muối Mohr cho vào 100 mL nước chứa ion nitrate, sau đó thêm NaOH(s) vào để đạt khoảng 28%, khi đó muối Mohr khử nitrate thành ammonia theo các phản ứng:
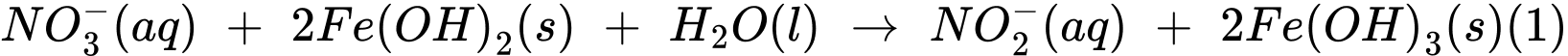
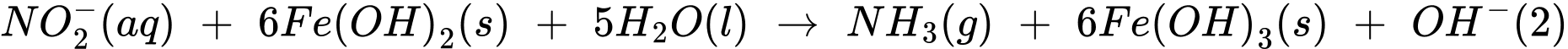
Sau khi các phản ứng (1) và (2) xảy ra hoàn toàn, lọc bỏ kết tủa, acid hoá dung dịch bằng dung dịch H2SO4 1M và chuẩn độ lượng Fe2+ dư bằng dung dịch KMnO4 (Các chất và ion khác trong dung dịch không phản ứng với KMnO4). Hãy cho biết mỗi mmol KMnO4 chênh lệch giữa thí nghiệm 1 với thí nghiệm 2 sẽ tương ứng với bao nhiêu mg có trong mẫu nước (làm tròn đến hàng phần mười).
có trong mẫu nước (làm tròn đến hàng phần mười).
Thí nghiệm 1: Lấy 10,0 mL dung dịch muối Mohr (NH4)2SO4.FeSO4.6H2O, thêm dung dịch H2SO4 1 M vào và chuẩn độ bằng dung dịch KMnO4.
Thí nghiệm 2: Lấy 10,0 mL dung dịch muối Mohr cho vào 100 mL nước chứa ion nitrate, sau đó thêm NaOH(s) vào để đạt khoảng 28%, khi đó muối Mohr khử nitrate thành ammonia theo các phản ứng:
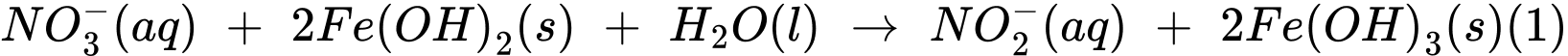
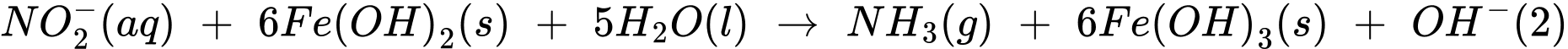
Sau khi các phản ứng (1) và (2) xảy ra hoàn toàn, lọc bỏ kết tủa, acid hoá dung dịch bằng dung dịch H2SO4 1M và chuẩn độ lượng Fe2+ dư bằng dung dịch KMnO4 (Các chất và ion khác trong dung dịch không phản ứng với KMnO4). Hãy cho biết mỗi mmol KMnO4 chênh lệch giữa thí nghiệm 1 với thí nghiệm 2 sẽ tương ứng với bao nhiêu mg
 có trong mẫu nước (làm tròn đến hàng phần mười).
có trong mẫu nước (làm tròn đến hàng phần mười).
Gọi tổng số mol MnO4- cần dùng trong thí nghiệm 1 là a (mol), ta có:
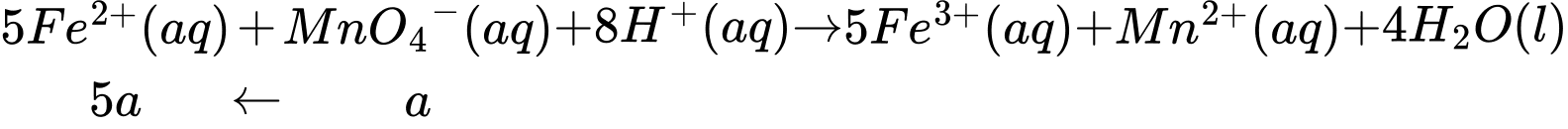
Gọi số mol NO3- đã dùng ở thí nghiệm 2 là b (mol), ta có:
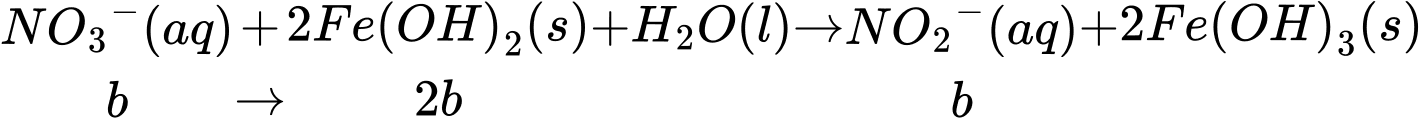
Lượng NO2- sinh ra là b (mol) tiếp tục phản ứng với Fe(OH)2
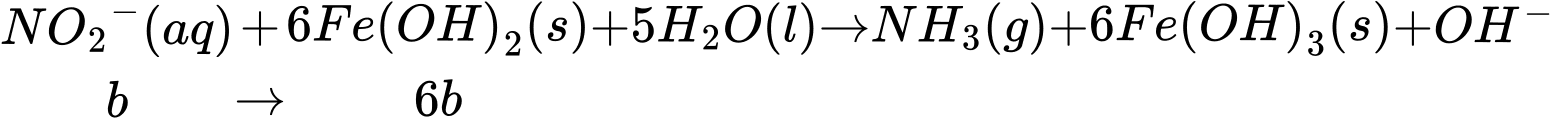
Thấy ban đầu ta có tổng số mol Fe2+ = 5a (mol), đã dùng hết (2b + 6b) mol ở thí nghiệm 2 nên lượng Fe2+ dư còn lại là:
nFe2+ dư = 5a - 8b (mol). Khi này, quá trình lọc bỏ kết tủa, acid hoá dung dịch bằng dung dịch H2SO4 1M và chuẩn độ lượng Fe2+ dư bằng dung dịch KMnO4 xảy ra như sau:
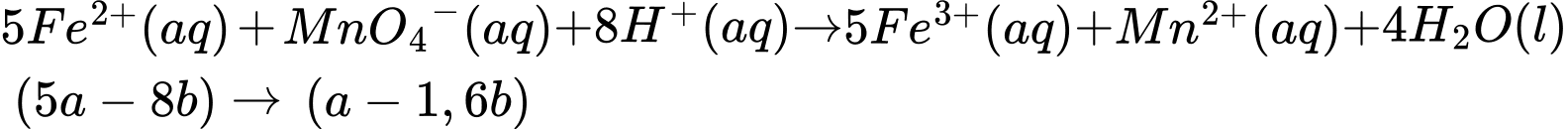
⇒ Số mol MnO4- chênh lệch là: nMnO4- (TN1) - nMnO4- (TN2) = a - (a - 1,6b) = 1,6b (mol)
Coi 1,6b (mol) = 1 (mmol) = 1x10-3 (mol) ⟶ b = 6,25x10-4 (mol)
Khối lượng NO3- có trong mẫu nước tương ứng với số mol MnO4- chênh lệch là:
mNO3- = 62.b = 62 . 6,25x10-4 = 0,03875 (g) = 38,75 (mg) ≈ 38,8 (mg)
⇒ Điền đáp án: 38,8
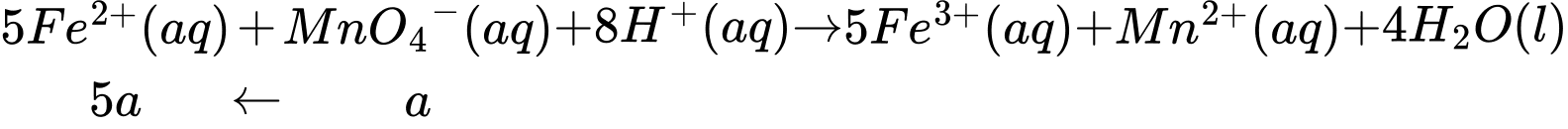
Gọi số mol NO3- đã dùng ở thí nghiệm 2 là b (mol), ta có:
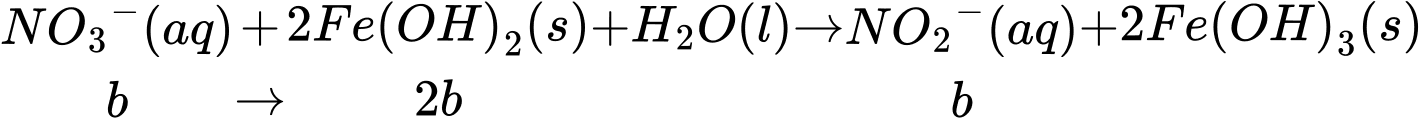
Lượng NO2- sinh ra là b (mol) tiếp tục phản ứng với Fe(OH)2
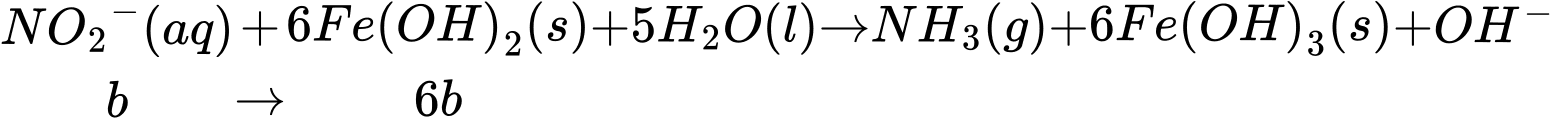
Thấy ban đầu ta có tổng số mol Fe2+ = 5a (mol), đã dùng hết (2b + 6b) mol ở thí nghiệm 2 nên lượng Fe2+ dư còn lại là:
nFe2+ dư = 5a - 8b (mol). Khi này, quá trình lọc bỏ kết tủa, acid hoá dung dịch bằng dung dịch H2SO4 1M và chuẩn độ lượng Fe2+ dư bằng dung dịch KMnO4 xảy ra như sau:
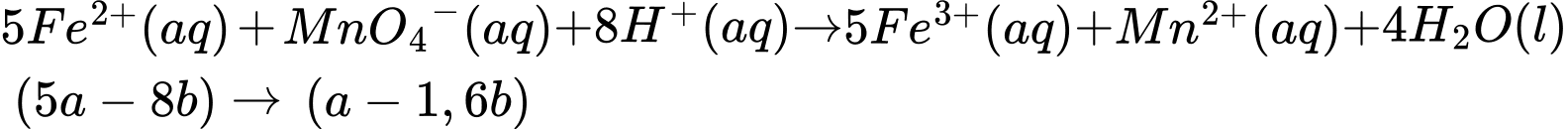
⇒ Số mol MnO4- chênh lệch là: nMnO4- (TN1) - nMnO4- (TN2) = a - (a - 1,6b) = 1,6b (mol)
Coi 1,6b (mol) = 1 (mmol) = 1x10-3 (mol) ⟶ b = 6,25x10-4 (mol)
Khối lượng NO3- có trong mẫu nước tương ứng với số mol MnO4- chênh lệch là:
mNO3- = 62.b = 62 . 6,25x10-4 = 0,03875 (g) = 38,75 (mg) ≈ 38,8 (mg)
⇒ Điền đáp án: 38,8
Câu 7 [830098]: Siderite là một khoáng vật quan trọng trong ngành công nghiệp và khai thác quặng sắt, có thành chính là FeCO3. Hàm lượng sắt trong quặng này có thể được xác định bằng phương pháp chuẩn độ. Người ta tiến hành thí nghiệm như sau:
▪ Bước 1: Cân chính xác 1,095 gam mẫu quặng siderite đã nghiền mịn và chuyển toàn bộ sang cốc thủy tinh 100 mL.
▪ Bước 2: Thêm 50 mL dung dịch H2SO4 loãng vào cốc, đun nhẹ để hòa tan quặng và đuổi khí CO2. Sau khi hòa tan hoàn toàn, lọc lấy dung dịch và loại bỏ phần không tan. Sau đó định mức thành 100 mL dung dịch.
FeCO3 + H2SO4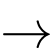 FeSO4 + CO2 + H2O
FeSO4 + CO2 + H2O
▪ Bước 3: Hút chính xác 10,00 mL dung dịch sau khi định mức cho vào bình tam giác, thêm 2 mL dung dịch H2SO4 loãng và thêm tiếp 10 giọt dung dịch H3PO4 (để che màu vàng của ion Fe3+). Đun nóng bình tam giác đến 60 oC, chuẩn độ bằng dung dịch KMnO4 nồng độ 0,015 M đến khi xuất hiện màu hồng nhạt bên trong 10 giây thì dừng lại.
10FeSO4 + 2KMnO4 + 8H2SO4 5Fe2(SO4)3 + 2MnSO4 + K2SO4 + 8H2O
5Fe2(SO4)3 + 2MnSO4 + K2SO4 + 8H2O
Lặp lại bước 3 thêm hai lần nữa. Thể tích trung bình của dung dịch KMnO4 sau ba lần chuẩn độ là 10,06 mL. Phần trăm khối lượng sắt trong quặng siderite là bao nhiêu phần trăm (làm tròn kết quả đến hàng phần mười)?
▪ Bước 1: Cân chính xác 1,095 gam mẫu quặng siderite đã nghiền mịn và chuyển toàn bộ sang cốc thủy tinh 100 mL.
▪ Bước 2: Thêm 50 mL dung dịch H2SO4 loãng vào cốc, đun nhẹ để hòa tan quặng và đuổi khí CO2. Sau khi hòa tan hoàn toàn, lọc lấy dung dịch và loại bỏ phần không tan. Sau đó định mức thành 100 mL dung dịch.
FeCO3 + H2SO4
 FeSO4 + CO2 + H2O
FeSO4 + CO2 + H2O▪ Bước 3: Hút chính xác 10,00 mL dung dịch sau khi định mức cho vào bình tam giác, thêm 2 mL dung dịch H2SO4 loãng và thêm tiếp 10 giọt dung dịch H3PO4 (để che màu vàng của ion Fe3+). Đun nóng bình tam giác đến 60 oC, chuẩn độ bằng dung dịch KMnO4 nồng độ 0,015 M đến khi xuất hiện màu hồng nhạt bên trong 10 giây thì dừng lại.
10FeSO4 + 2KMnO4 + 8H2SO4
 5Fe2(SO4)3 + 2MnSO4 + K2SO4 + 8H2O
5Fe2(SO4)3 + 2MnSO4 + K2SO4 + 8H2OLặp lại bước 3 thêm hai lần nữa. Thể tích trung bình của dung dịch KMnO4 sau ba lần chuẩn độ là 10,06 mL. Phần trăm khối lượng sắt trong quặng siderite là bao nhiêu phần trăm (làm tròn kết quả đến hàng phần mười)?
Phương trình phản ứng:
FeCO3 + H2SO4 →FeSO4 + CO2 + H2O
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Đổi 10,06 mL = 0,01006 L
Số mol của KMnO4 là n KMnO4 = 0,01006 × 0,015 = 0,0001509 mol
Từ phương trình hóa học số mol của FeCO3 là 0,0007545 mol
Phần trăm khối lượng sắt trong quặng siderite là
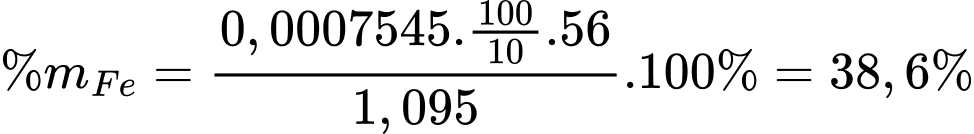
⟹ Điền đáp án 38,6
FeCO3 + H2SO4 →FeSO4 + CO2 + H2O
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Đổi 10,06 mL = 0,01006 L
Số mol của KMnO4 là n KMnO4 = 0,01006 × 0,015 = 0,0001509 mol
Từ phương trình hóa học số mol của FeCO3 là 0,0007545 mol
Phần trăm khối lượng sắt trong quặng siderite là
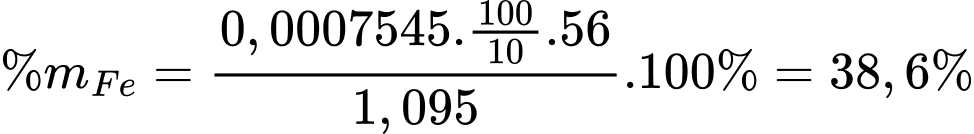
⟹ Điền đáp án 38,6
Câu 8 [830100]: Chuẩn độ dung dịch H2C2O4 bằng dung dịch KMnO4:
▪ Bước 1: Rót dung dịch KMnO4 0,002M vào burette (tối màu), điều chỉnh đến vạch ‘0’.
▪ Bước 2: Dùng pipete lấy 10 mL dung dịch mẫu chứa H2C2O4 (nồng độ Co) cho vào bình định mức, sau đó cho tiếp nước cất đến vạch định mức 100 mL (lắc đều). Lấy 10 mL dung dịch từ bình định mức cho vào bình tam giác, cho thêm 5 mL dung dịch HClO4 (dùng dư so với lượng phản ứng), rồi cho thêm nước cất đến khoảng 25 mL.
▪ Bước 3: Cho từ từ dung dịch KMnO4 0,002 M từ burette vào bình tam giác đã chứa hỗn hợp H2C2O4 và HClO4 ở bước 2 và lắc đều cho đến khi dung dịch chuyển sang màu hồng (bền trong 30 s) thì dừng chuẩn độ.
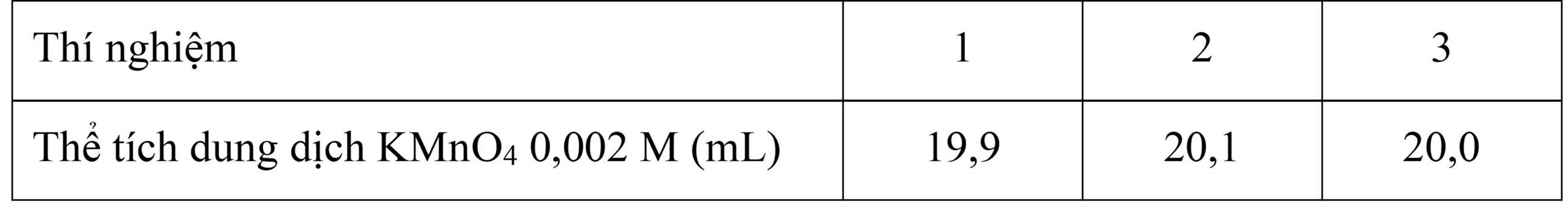
Lặp lại thí nghiệm trên thêm 2 lần nữa, kết quả ghi nhận được thể tích dung dịch KMnO4 0,002 M như sau:
Tính nồng độ Co (mol/L) của dung dịch H2C2O4 ban đầu.
▪ Bước 1: Rót dung dịch KMnO4 0,002M vào burette (tối màu), điều chỉnh đến vạch ‘0’.
▪ Bước 2: Dùng pipete lấy 10 mL dung dịch mẫu chứa H2C2O4 (nồng độ Co) cho vào bình định mức, sau đó cho tiếp nước cất đến vạch định mức 100 mL (lắc đều). Lấy 10 mL dung dịch từ bình định mức cho vào bình tam giác, cho thêm 5 mL dung dịch HClO4 (dùng dư so với lượng phản ứng), rồi cho thêm nước cất đến khoảng 25 mL.
▪ Bước 3: Cho từ từ dung dịch KMnO4 0,002 M từ burette vào bình tam giác đã chứa hỗn hợp H2C2O4 và HClO4 ở bước 2 và lắc đều cho đến khi dung dịch chuyển sang màu hồng (bền trong 30 s) thì dừng chuẩn độ.
Lặp lại thí nghiệm trên thêm 2 lần nữa, kết quả ghi nhận được thể tích dung dịch KMnO4 0,002 M như sau:

Tính nồng độ Co (mol/L) của dung dịch H2C2O4 ban đầu.
Đổi 5 mL = 0,005 L
Thể tích trung bình của KMnO4 là
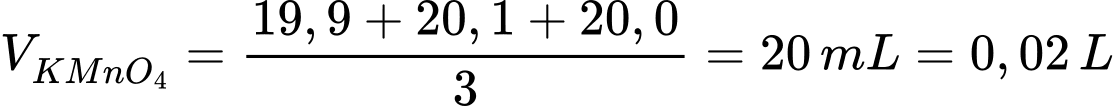
Phương trình phản ứng:
2KMnO4 + 5H2C2O4 + 6H+ → 2Mn2+ + 8H2O + 10CO2 + 2K+
Số mol của KMnO4 là nKMnO4 = 0,02 × 0,002 = 0,00004 mol
Từ phương trình hóa học số mol của H2C2O4 là 0,0001 mol
Nồng độ Co (mol/L) của dung dịch H2C2O4 ban đầu là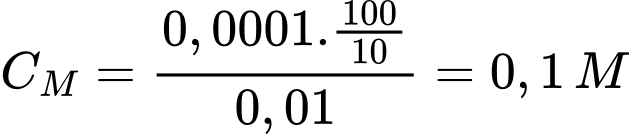
⟹ Điền đáp án 0,1
Thể tích trung bình của KMnO4 là
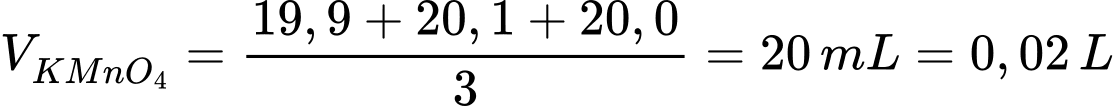
Phương trình phản ứng:
2KMnO4 + 5H2C2O4 + 6H+ → 2Mn2+ + 8H2O + 10CO2 + 2K+
Số mol của KMnO4 là nKMnO4 = 0,02 × 0,002 = 0,00004 mol
Từ phương trình hóa học số mol của H2C2O4 là 0,0001 mol
Nồng độ Co (mol/L) của dung dịch H2C2O4 ban đầu là
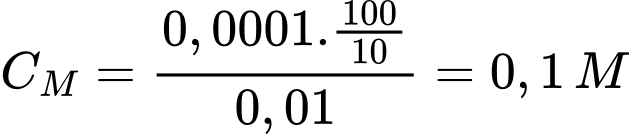
⟹ Điền đáp án 0,1
Câu 9 [830115]: Hàm lượng cho phép của lưu huỳnh (sulfur) trong nhiên liệu là 0,3% về khối lượng. Để xác định hàm lượng lưu huỳnh trong một loại nhiên liệu người ta lấy 100,0 gam nhiên liệu đó và đốt cháy hoàn toàn. Khí tạo thành chỉ chứa carbon dioxide, sulfur dioxide và hơi nước được dẫn vào nước tạo ra 500,0 mL dung dịch. Biết rằng tất cả sulfur dioxide đã tan vào dung dịch. Lấy 10,0 mL dung dịch này cho tác dụng với dung dịch KMnO4 5,00×10–3 mol/L thì thể tích dung dịch KMnO4 cần dùng là 12,5 mL. Phần trăm khối lượng của lưu huỳnh trong nhiên liệu trên là bao nhiêu?
Phương trình phản ứng:
5SO2 + 2KMnO4 + 2H2O → 2MnSO4 + K2SO4 + 2H2SO4
Đổi 12,5 mL = 0,0125 L
Số mol của KMnO4 là nKMnO4 = 0,0125 × 0,005 = 0,0000625 mol
Từ phương trình hóa học số mol của SO2 là 1,5625.10-4 mol
Phần trăm khối lượng của lưu huỳnh trong nhiên liệu là
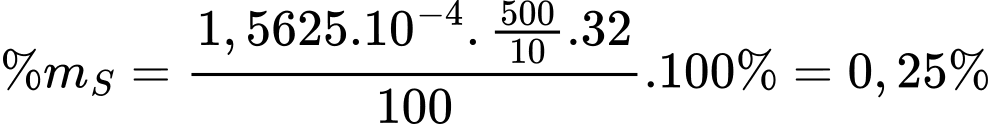
⟹ Điền đáp án 0,25
5SO2 + 2KMnO4 + 2H2O → 2MnSO4 + K2SO4 + 2H2SO4
Đổi 12,5 mL = 0,0125 L
Số mol của KMnO4 là nKMnO4 = 0,0125 × 0,005 = 0,0000625 mol
Từ phương trình hóa học số mol của SO2 là 1,5625.10-4 mol
Phần trăm khối lượng của lưu huỳnh trong nhiên liệu là
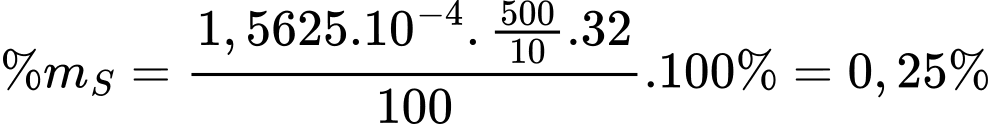
⟹ Điền đáp án 0,25
Câu 10 [830099]: Để xác định hàm lượng oxygen (O2) tan trong nước, người ta lấy 100,0 mL nước rồi cho ngay manganese sulphate (MnSO4, dư) và sodium hydroxide (NaOH) vào nước. Sau khi lắc kĩ (không cho tiếp xúc với không khí), manganese(II) hydroxide (Mn(OH)2) bị O2 oxi hóa thành manganese oxohydroxide (MnO(OH)2). Thêm acid (dư) và cho tiếp potassium iodide (KI, dư) vào hỗn hợp, thì ion idodine (I–) bị MnO(OH)2 oxi hóa thành iodine (I2). Lượng I2 sinh ra phản ứng vừa đủ với 10,5 ml dung dịch Na2S2O3 0,01 M (sodium thiosulphate). Biết các phản ứng xảy ra như sau:
Mn2+ + 2OH– → Mn(OH)2 (1)
2Mn(OH)2 + O2 → 2MnO(OH)2 (2)
MnO(OH)2 + 2I– + 4H+ → Mn2+ + I2 + 3H2O (3)
I2 + 2Na2S2O3 → Na2S4O6 + 2NaI (4)
Hàm lượng O2 tan trong nước (tính theo mg O2/1 L) là a. Giá trị của a là bao nhiêu (làm tròn kết quả đến hàng phần mười)?
Mn2+ + 2OH– → Mn(OH)2 (1)
2Mn(OH)2 + O2 → 2MnO(OH)2 (2)
MnO(OH)2 + 2I– + 4H+ → Mn2+ + I2 + 3H2O (3)
I2 + 2Na2S2O3 → Na2S4O6 + 2NaI (4)
Hàm lượng O2 tan trong nước (tính theo mg O2/1 L) là a. Giá trị của a là bao nhiêu (làm tròn kết quả đến hàng phần mười)?
(1) Mn2+ + 2OH– → Mn(OH)2
(2) 2Mn(OH)2 + O2 → 2MnO(OH)2
(3) MnO(OH)2 + 2I– + 4H+ → Mn2+ + I2 + 3H2O
(4) I2 + 2Na2S2O3 → Na2S4O6 + 2NaI
Đổi 10,5 mL = 0,0105 L
Số mol của Na2S2O3 là nNa2S2O3 = 0,0105 × 0,01 = 0,000105 mol
Từ phương trình hóa học số mol của O2 là 0,00002625 mol
Hàm lượng O2 tan trong nước (tính theo mg O2/1 L)
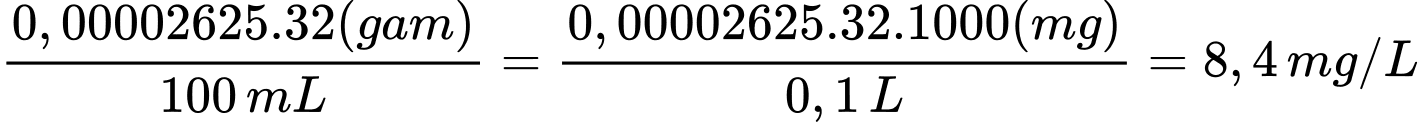 .
.
⟹ Điền đáp án 8,4
(2) 2Mn(OH)2 + O2 → 2MnO(OH)2
(3) MnO(OH)2 + 2I– + 4H+ → Mn2+ + I2 + 3H2O
(4) I2 + 2Na2S2O3 → Na2S4O6 + 2NaI
Đổi 10,5 mL = 0,0105 L
Số mol của Na2S2O3 là nNa2S2O3 = 0,0105 × 0,01 = 0,000105 mol
Từ phương trình hóa học số mol của O2 là 0,00002625 mol
Hàm lượng O2 tan trong nước (tính theo mg O2/1 L)
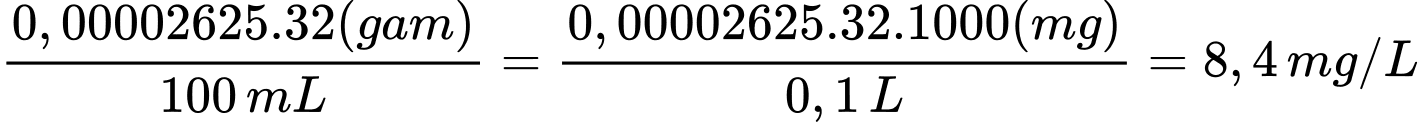 .
.⟹ Điền đáp án 8,4