PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1 [1029221]: Định luật Boyle được áp dụng trong quá trình biến đổi trạng thái của một lượng khí xác định khi
A, nhiệt độ không đổi.
B, thể tích không đổi.
C, áp suất không đổi.
D, khối khí giãn nở tự do.
Định luật Boyle được áp dụng trong quá trình biến đổi trạng thái của một lượng khí xác định khi nhiệt độ không đổi.
Chọn A Đáp án: A
Chọn A Đáp án: A
Câu 2 [1029222]: Để bơm đầy một khí cầu (chưa có khí bên trong) đến thể tích 100 m3 có áp suất 1,2 atm ở nhiệt độ không đổi người ta dùng các ống khí helium có thể tích 50 lít ở áp suất 100 atm cùng nhiệt độ với khí cầu. Số ống khí Helium cần để bơm khí cầu là
A, 48 ống.
B, 2 ống.
C, 12 ống.
D, 24 ống.
Gọi số ống khí Helium là 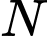
Trạng thái của cầu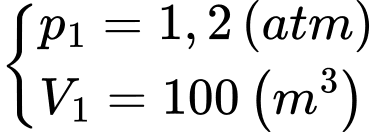
Trạng thái của các ống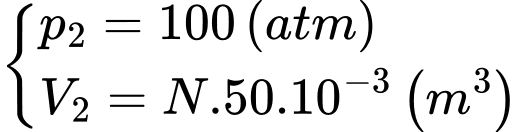
Áp dụng định luật Boyle ta có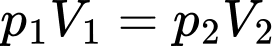
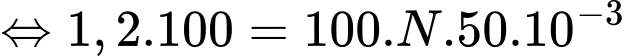
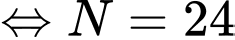
Chọn D
Đáp án: D
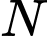
Trạng thái của cầu
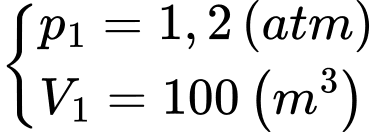
Trạng thái của các ống
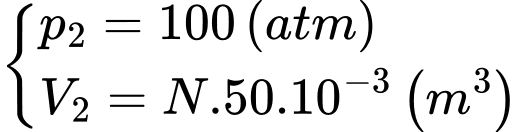
Áp dụng định luật Boyle ta có
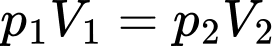
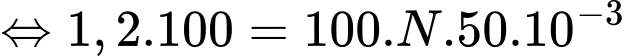
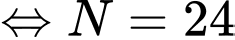
Chọn D
Đáp án: D
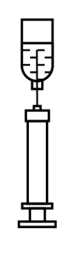
Câu 3 [1029223]: Để thuận tiện cho việc rút thuốc từ lọ thuốc kín, y tá thường sử dụng ống tiêm để bơm một lượng nhỏ không khí vào lọ thuốc như hình bên. Xét một lọ thuốc có dung tích 0,9 ml và chứa 0,5 ml dung dịch thuốc, áp suất của phần không khí trong lọ là 105 Pa. Người y tá sử dụng ống tiêm để bơm từ từ một lượng không khí có thể tích 0,12 cm3 và áp suất ban đầu 105 Pa vào lọ thuốc. Biết nhiệt độ bên trong và bên ngoài lọ thuốc bằng nhau và không thay đổi. Áp suất của không khí trong lọ thuốc sau khi bơm hết là bao nhiêu? (coi không khí được đề cập trong bài là khí lý tưởng).

A, 3,5.105 Pa.
B, 7,7.105 Pa.
C, 5,7.105 Pa.
D, 1,3.105 Pa.
Khi bơm không khí vào lọ thuốc:
+) Áp suất không đổi mà chỉ tăng thể tích
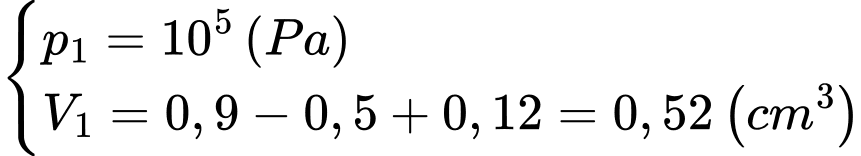
+) Thể tích không đổi mà chỉ tăng áp suất
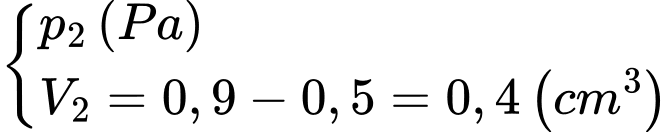
+) Áp dụng định luật Boyle ta có
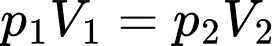
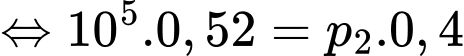
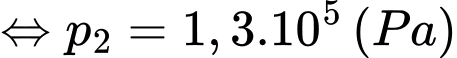
Chọn D
Đáp án: D
+) Áp suất không đổi mà chỉ tăng thể tích
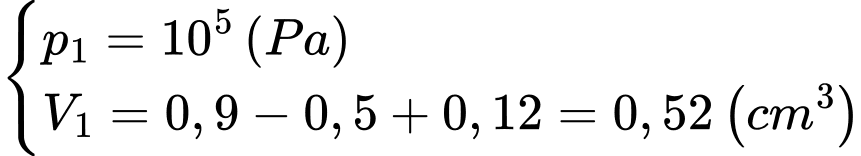
+) Thể tích không đổi mà chỉ tăng áp suất
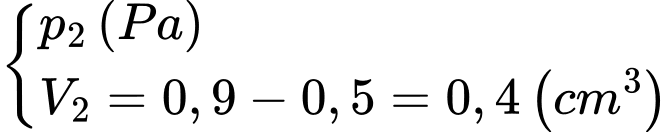
+) Áp dụng định luật Boyle ta có
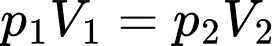
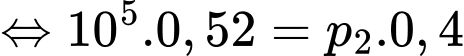
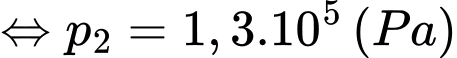
Chọn D
Đáp án: D
Câu 4 [1029224]: Ở nhiệt độ 27 °C, thể tích của một lượng khí là 30 lít. Ở nhiệt độ 227 °C và áp suất khí không đổi, thể tích của lượng khí đó là
A, 252 lít.
B, 18 lít.
C, 50 lít.
D, 200 lít.
Áp dụng định luật Charles ta có 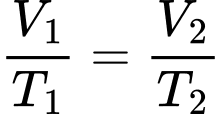
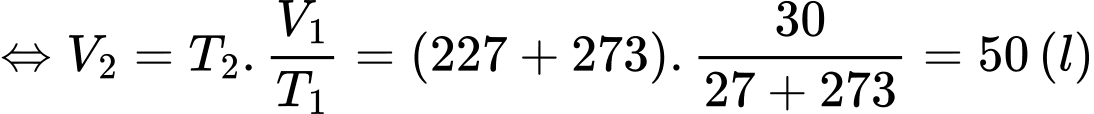
Chọn C Đáp án: C
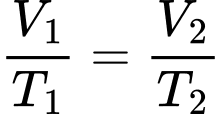
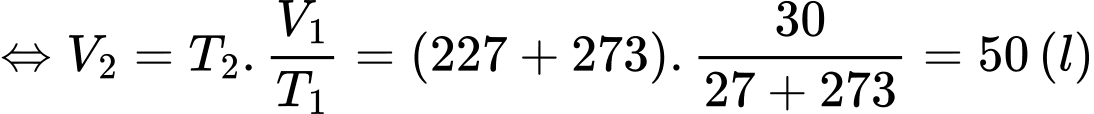
Chọn C Đáp án: C
Câu 5 [1029225]: Hình nào dưới đây biểu diễn đúng quá trình biến đổi đẳng áp của một lượng khí?
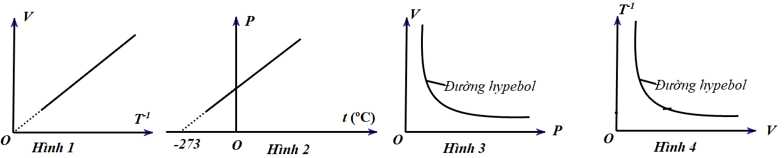

A, Hình 2.
B, Hình 1.
C, Hình 3.
D, Hình 4.
Hình 2 biểu diễn đúng quá trình biến đổi đẳng áp của 1 lượng khí.
Chọn A Đáp án: A
Chọn A Đáp án: A
Câu 6 [1029226]: Một bình kín chứa một lượng khí Hydrogen xác định có T1 = 500K, p1 = 105 N/m2 người ta làm nóng khí đến T2 = 1000 K. Coi thể tích, khối lượng khí Hydrogen không đổi. Áp suất p2 của khí Hydrogen là
A, 2.105 N/m2.
B, 4.105 N/m2.
C, 8.105 N/m2.
D, 105 N/m2.
Áp dụng quá trình biến đổi đẳng tích cho khối khí ta có
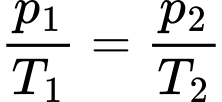
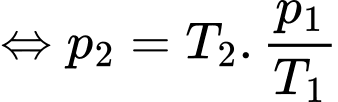
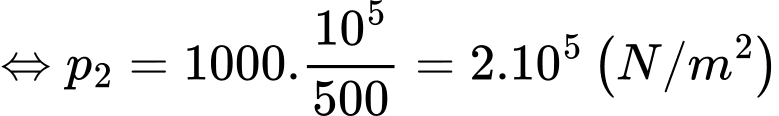
Chọn A
Đáp án: A
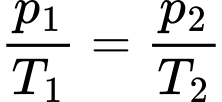
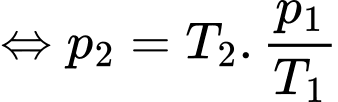
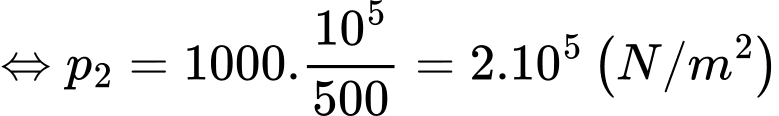
Chọn A
Đáp án: A
Câu 7 [1029227]: Khi lái xe dưới trời nắng nóng, nhiệt độ ngoài trời và mặt đường tăng cao làm cho nhiệt độ khối khí bên trong lốp xe cũng tăng theo. Điều này ảnh hưởng như thế nào đến áp suất khí trong lốp xe và cần lưu ý gì khi di chuyển?
A, Áp suất khí trong lốp xe tăng và cao su bị mềm, nên kiểm tra và điều chỉnh áp suất của lốp tránh bơm quá căng gây nguy hiểm.
B, Áp suất khí trong lốp xe tăng, điều này có lợi cho việc di chuyển vì giảm ma sát.
C, Cao su ở lốp xe bị mềm và dãn ra làm giảm áp suất, cần bơm thêm khí vào lốp trước khi di chuyển.
D, Áp suất khí trong lốp xe không thay đổi vì khối lượng khí bên trong lốp không đổi.
Khi lái xe dưới trời nắng nóng, nhiệt độ ngoài trời và mặt đường tăng cao làm cho nhiệt độ khối khí bên trong lốp xe cũng tăng theo. Điều này dẫn đến áp suất khí trong lốp xe tăng và cao su bị mềm, nên kiểm tra và điều chỉnh áp suất của lốp để tránh bơm căng quá gây nguy hiểm.
Chọn A
Chọn A
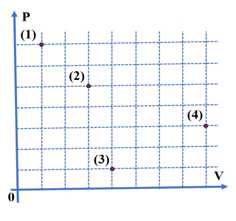
Câu 8 [1029228]: Xét quá trình biến đổi trạng thái của một khối khí lí tưởng. Áp suất và thể tích của khối khí ở các trạng thái (1), (2), (3), và (4) được biểu diễn trong hình bên. Trong số các trạng thái đã cho, trạng thái mà khối khí có nhiệt độ lớn nhất là

A, 1.
B, 2.
C, 4.
D, 3.
Ta có 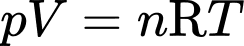
Để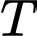 đạt max
đạt max 
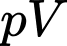 đạt max
đạt max
+)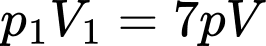
+)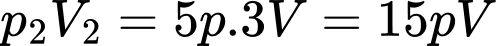
+)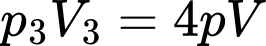
+)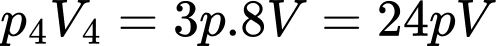
 Trạng thái khối khí có nhiệt độ lớn nhất là trạng thái 4.
Trạng thái khối khí có nhiệt độ lớn nhất là trạng thái 4.
Chọn C Đáp án: C
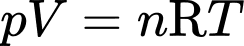
Để
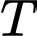 đạt max
đạt max 
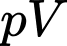 đạt max
đạt max
+)
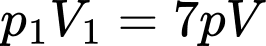
+)
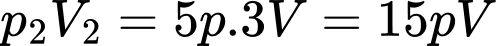
+)
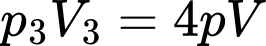
+)
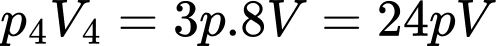
 Trạng thái khối khí có nhiệt độ lớn nhất là trạng thái 4.
Trạng thái khối khí có nhiệt độ lớn nhất là trạng thái 4.
Chọn C Đáp án: C
Câu 9 [1029229]: Trong một động cơ điêzen, khối khí có nhiệt độ ban đầu là 32 °C được nén để thể tích giảm bằng 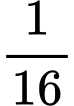 thể tích ban đầu và áp suất tăng 48,5 lần áp suất ban đầu. Nhiệt độ khí sau khi nén có giá trị xấp xỉ bằng
thể tích ban đầu và áp suất tăng 48,5 lần áp suất ban đầu. Nhiệt độ khí sau khi nén có giá trị xấp xỉ bằng
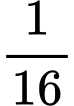 thể tích ban đầu và áp suất tăng 48,5 lần áp suất ban đầu. Nhiệt độ khí sau khi nén có giá trị xấp xỉ bằng
thể tích ban đầu và áp suất tăng 48,5 lần áp suất ban đầu. Nhiệt độ khí sau khi nén có giá trị xấp xỉ bằng A, 132 °C.
B, 97 °C.
C, 652 °C.
D, 1552 °C.
Trạng thái ban đầu 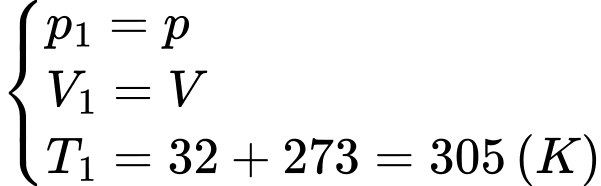
Trạng thái lúc sau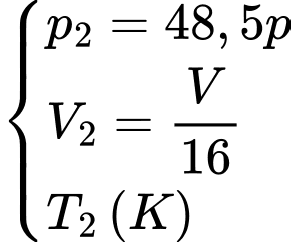
Áp dụng phương trình trạng thái ta có
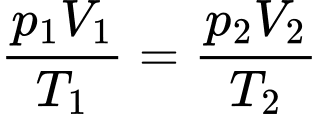
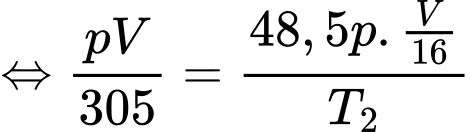
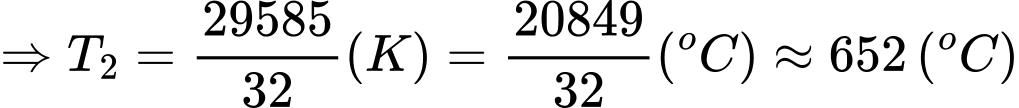
Chọn C Đáp án: C
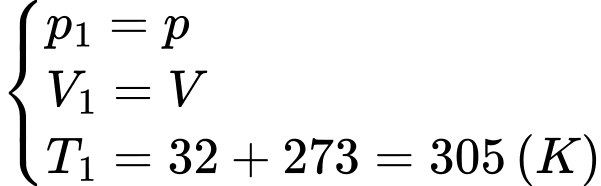
Trạng thái lúc sau
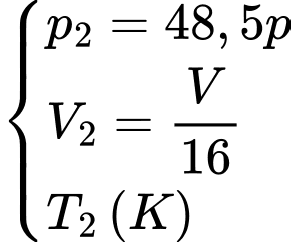
Áp dụng phương trình trạng thái ta có
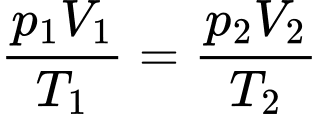
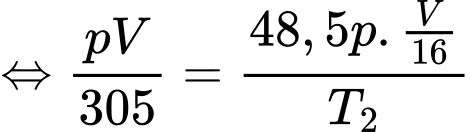
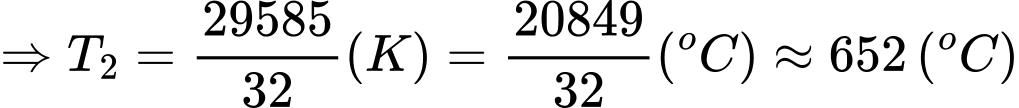
Chọn C Đáp án: C
Câu 10 [1029230]: Cho quá trình biến đổi trạng thái của một lượng khí xác định được biểu diễn trong hệ tọa độ áp suất P - thể tích V như hình vẽ. Trong các quá trình trên, nhiệt độ cao nhất và thấp nhất của khối khí đạt được lần lượt tại các điểm nào sau đây?
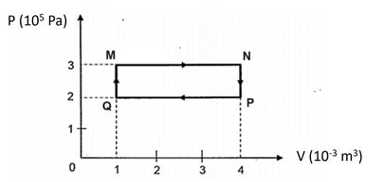

A, Q và P.
B, M và N.
C, N và Q.
D, M và P.
Ta có 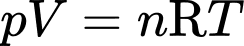
Để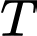 đạt max (min)
đạt max (min) 
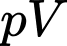 đạt max (min)
đạt max (min)
Nhận xét: Nhiệt độ đạt max hay min tại các đỉnh của hình chữ nhật.
+) Tại M:
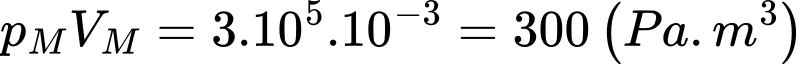
+) Tại N: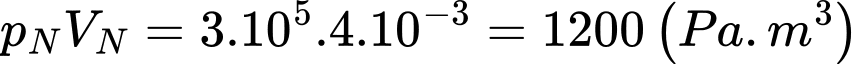
+) Tại P: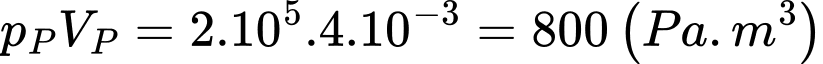
+) Tại Q:
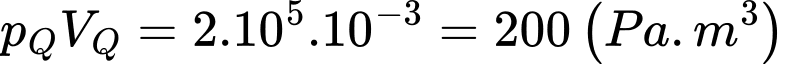
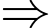 Nhiệt độ lớn nhất và nhỏ nhất của khối khí đạt được tại các điểm N và Q
Nhiệt độ lớn nhất và nhỏ nhất của khối khí đạt được tại các điểm N và Q
Chọn C Đáp án: C
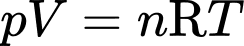
Để
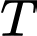 đạt max (min)
đạt max (min) 
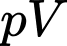 đạt max (min)
đạt max (min)
Nhận xét: Nhiệt độ đạt max hay min tại các đỉnh của hình chữ nhật.
+) Tại M:
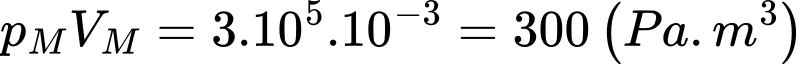
+) Tại N:
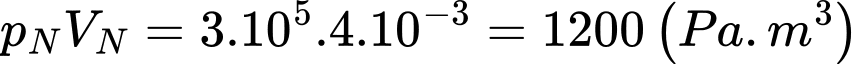
+) Tại P:
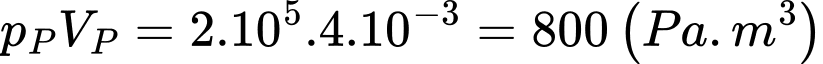
+) Tại Q:
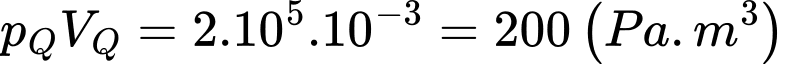
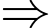 Nhiệt độ lớn nhất và nhỏ nhất của khối khí đạt được tại các điểm N và Q
Nhiệt độ lớn nhất và nhỏ nhất của khối khí đạt được tại các điểm N và Q
Chọn C Đáp án: C
Câu 11 [1029231]: Gọi p, V và T lần lượt là áp suất, thể tích và nhiệt độ tuyệt đối của n mol khí lí tưởng. Biết hằng số khí lí tưởng là R. Phương trình Clapeyron của khối khí này là
A, pV=nRT.
B, VT=nRp.
C, 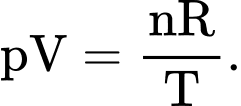
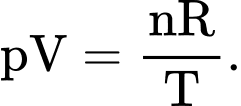
D, 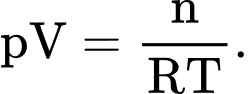
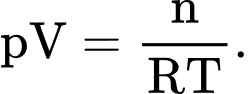
Phương trình Clapeyron của khối khí này là pV=nRT.
Chọn A
Chọn A
Câu 12 [1029232]: Một bình kim loại chứa khí lí tưởng ở nhiệt độ 27 °C và áp suất 8.105 Pa. Nếu 25% lượng khí trong bình thoát ra và lượng khí còn lại trong bình có nhiệt độ 12 °C thì sẽ có áp suất là
A, 2,85.105 Pa.
B, 0,95.105 Pa.
C, 5,7.105 Pa.
D, 1,425.105 Pa.
Gọi thể tích bình kim loại là 
+) Trạng thái ban đầu của 75% lượng khí trong bình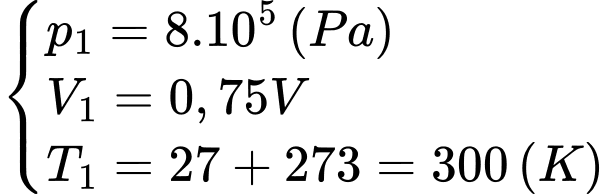
Sau khi 25% lượng khí thoát ra ngoài thì 75% lượng khí ban đầu sẽ chiếm toàn bộ bình chứa
 Trạng thái lúc sau của 75% lượng khí trong bình
Trạng thái lúc sau của 75% lượng khí trong bình 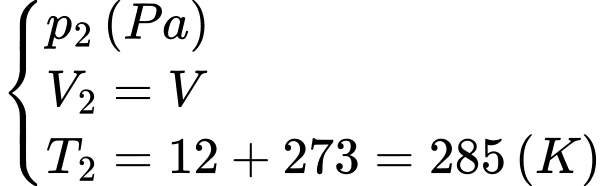
Áp dụng phương trình trạng thái khí lí tưởng ta có
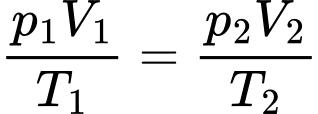
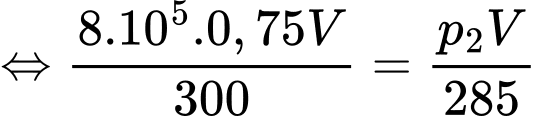
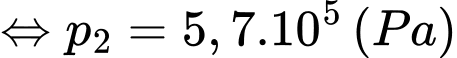
Chọn C Đáp án: C

+) Trạng thái ban đầu của 75% lượng khí trong bình
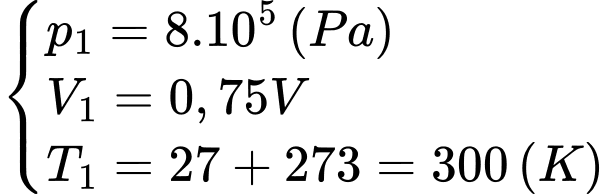
Sau khi 25% lượng khí thoát ra ngoài thì 75% lượng khí ban đầu sẽ chiếm toàn bộ bình chứa
 Trạng thái lúc sau của 75% lượng khí trong bình
Trạng thái lúc sau của 75% lượng khí trong bình 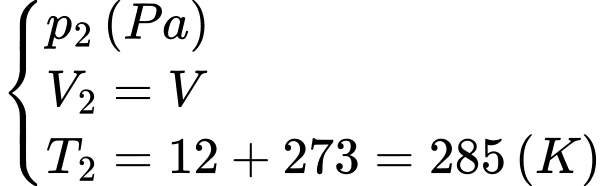
Áp dụng phương trình trạng thái khí lí tưởng ta có
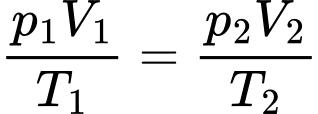
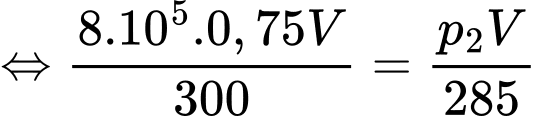
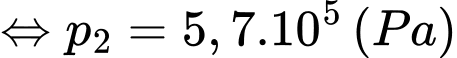
Chọn C Đáp án: C
Câu 13 [1029233]: Một lượng khí CO2 trong bình kín có khối lượng là 10 kg. Biết 1 mol khí có NA = 6,02.1023 phân tử. Khối lượng mol của Carbon là 12 g/mol và của Oxygen là 16 g/mol. Số phân tử khí có trong bình là
A, 2,15.1023.
B, 1,37.1026.
C, 1,37.1023.
D, 2,15.1026.
Số phân tử khí 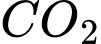 có trong bình là
có trong bình là
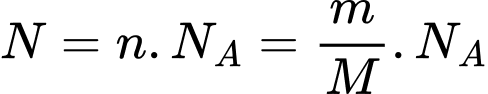
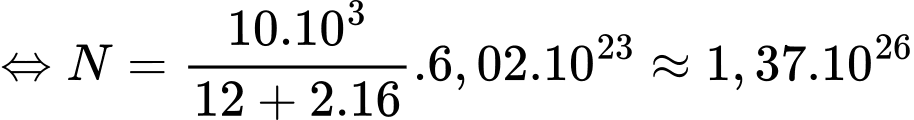
Chọn B Đáp án: B
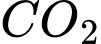 có trong bình là
có trong bình là
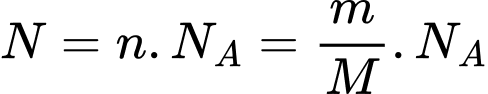
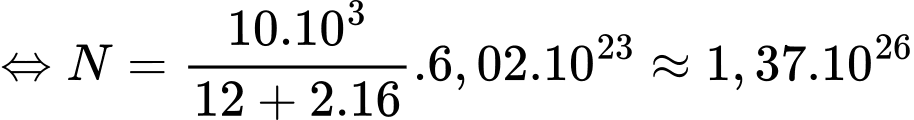
Chọn B Đáp án: B
Câu 14 [1029234]: Động năng tịnh tiến trung bình của phân tử khí phụ thuộc
A, vào bản chất chất khí.
B, nhiệt độ của khối khí.
C, áp suất chất khí.
D, mật độ phân tử khí.
Ta có 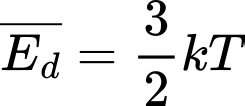
 Động năng tịnh tiến trung bình của các phân tử khí phụ thuộc vào nhiệt độ của khối khí.
Động năng tịnh tiến trung bình của các phân tử khí phụ thuộc vào nhiệt độ của khối khí.
Chọn B Đáp án: B
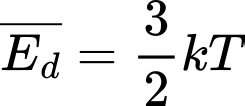
 Động năng tịnh tiến trung bình của các phân tử khí phụ thuộc vào nhiệt độ của khối khí.
Động năng tịnh tiến trung bình của các phân tử khí phụ thuộc vào nhiệt độ của khối khí.
Chọn B Đáp án: B
Câu 15 [1029235]: Gọi k là hằng số Boltzmann, T là nhiệt độ tuyệt đối. Động năng tịnh tiến trung bình của phân tử khí được xác định bởi công thức
A, 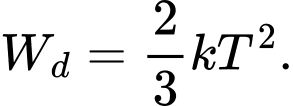
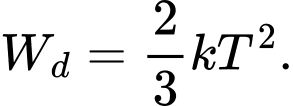
B, 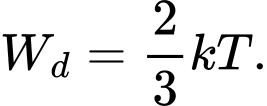
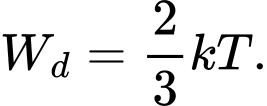
C, 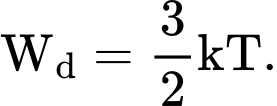
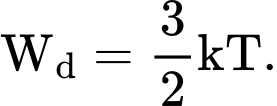
D, 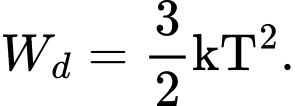
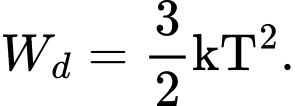
Động năng tịnh tiến trung bình của các phân tử khí được xác định bởi công thức:
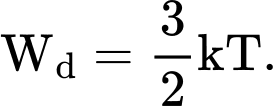
Chọn C Đáp án: C
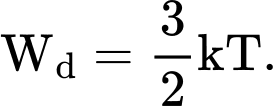
Chọn C Đáp án: C
Câu 16 [1029236]: Mối quan hệ giữa áp suất của chất khí tác dụng lên thành bình (p), mật độ phân tử khí (µ) và động năng trung bình của phân tử khí  là
là
 là
là A, 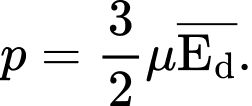
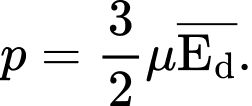
B, 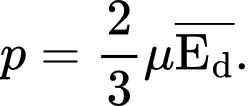
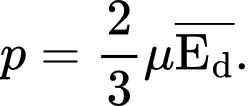
C, 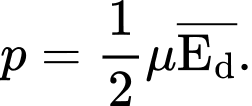
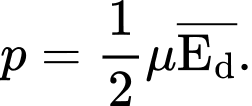
D, 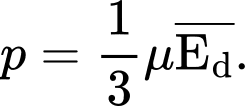
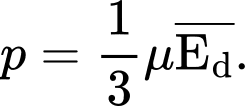
Mối quan hệ giữa áp suất của chất khí tác dụng lên thành bình, mật độ phân tử khí và động năng tịnh tiến trung bình là:
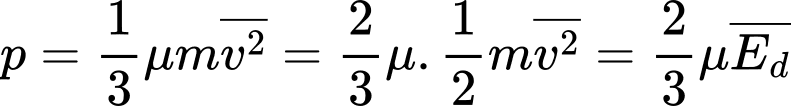
Chọn B Đáp án: B
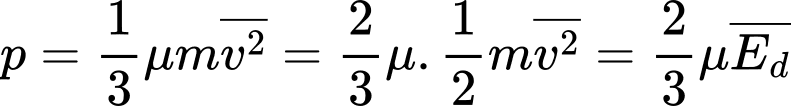
Chọn B Đáp án: B
Câu 17 [1029237]: Ở điều kiện nhiệt độ phòng 27 °C và áp suất khí quyển 1,0 atm, một phân tử oxygen có tốc độ trung bình 450 m/s và quãng đường tự do trung bình (quãng đường đi giữa giữa hai lần va chạm liên tiếp) là 1,1.10-7 m. Trung bình mỗi giây, một phân tử oxy thực hiện khoảng bao nhiêu va chạm?
A, 8,2.109 lần.
B, 4,1.109 lần.
C, 2,0.109 lần.
D, 5,0.109 lần.
Quãng đường phân tử khí Oxy đi được là 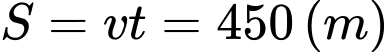
Số quãng đường tự do nó đi được là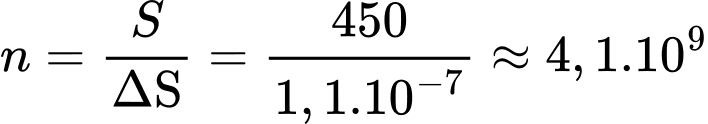
Vì mỗi quãng đường tự do cho 1 va chạm nên số va chạm là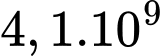
Chọn B Đáp án: B
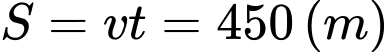
Số quãng đường tự do nó đi được là
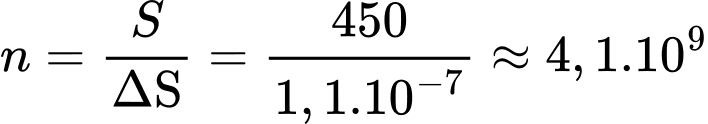
Vì mỗi quãng đường tự do cho 1 va chạm nên số va chạm là
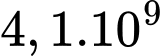
Chọn B Đáp án: B
Câu 18 [1029238]: Một mol chất khí ở 0°C các phân tử có tốc độ căn quân phương là 460 m/s. Tốc độ căn quân phương của các phân tử khí này ở nhiệt độ 819 °C là
A, 1380 m/s.
B, 1806 m/s.
C, 920 m/s.
D, 795 m/s.
Ta có 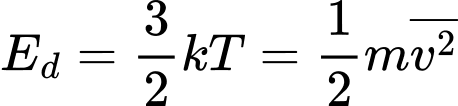
Vì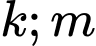 là các hằng số nên
là các hằng số nên 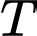 tỉ lệ thuận với
tỉ lệ thuận với 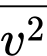
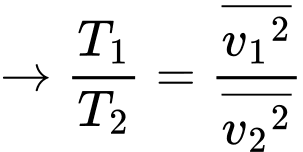
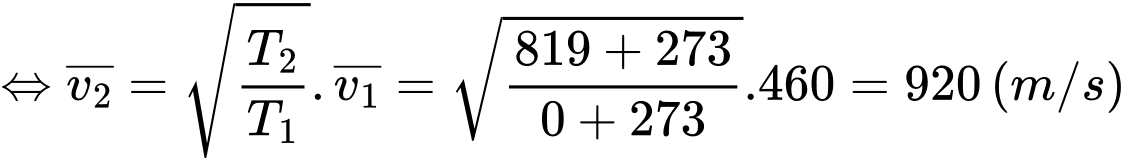
Chọn C Đáp án: C
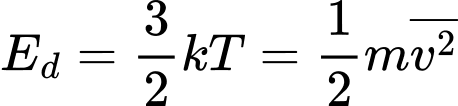
Vì
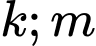 là các hằng số nên
là các hằng số nên 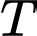 tỉ lệ thuận với
tỉ lệ thuận với 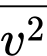
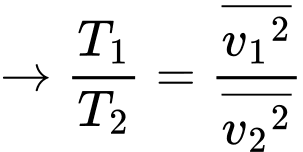
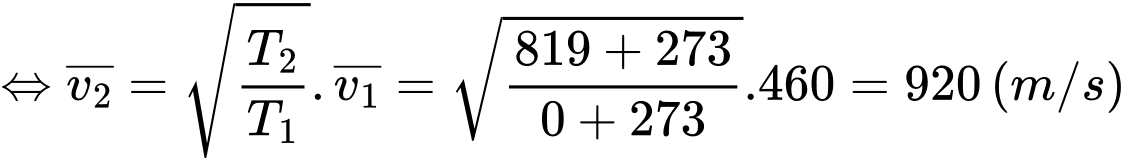
Chọn C Đáp án: C
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 19 [1029239]: Cho các phát biểu về đường đẳng nhiệt của một lượng khí xác định. Phát biểu nào sau đây là đúng, phát biểu nào là sai?
a. Đúng. Đường đẳng nhiệt trong hệ toạ độ (p,V) là 1 cung hypebol.
b. Sai. Đường đẳng nhiệt trong hệ toạ độ (V,T) là 1 đoạn thẳng vuông góc với trục OT.
c. Sai. Đường đẳng nhiệt trong hệ toạ độ (p,T) là 1 đoạn thẳng song song với trục Op.
d. Sai. Ứng với các nhiệt độ khác nhau của cùng 1 lượng khí có các đường đẳng nhiệt là khác nhau.
b. Sai. Đường đẳng nhiệt trong hệ toạ độ (V,T) là 1 đoạn thẳng vuông góc với trục OT.
c. Sai. Đường đẳng nhiệt trong hệ toạ độ (p,T) là 1 đoạn thẳng song song với trục Op.
d. Sai. Ứng với các nhiệt độ khác nhau của cùng 1 lượng khí có các đường đẳng nhiệt là khác nhau.
Câu 20 [1029240]: Có thể sử dụng bộ thí nghiệm (hình bên) để tìm hiểu về mối liên hệ giữa nhiệt độ và thể tích của một lượng khí xác định khi giữ áp suất của khí không đổi.
Trình tự thí nghiệm:
+ Mở van áp kế, dùng tay quay dịch chuyển piston để lấy một lượng khí xác định.
+ Đổ nước nóng vào hộp chứa nước sao cho xilanh ngập hoàn toàn trong nước.
+ Khi nhiệt độ không tăng nữa, đóng van áp kế, ghi giá trị thể tích và áp suất của khí.
+ Sau khoảng 5 phút, dịch chuyển piston để áp suất trở lại giá trị ban đầu, ghi giá trị thể tích và nhiệt độ của khí.
+ Làm lại bước cuối cùng một số lần nữa và ghi kết quả như bảng bên.
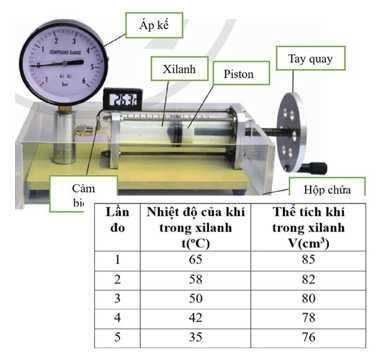
Trình tự thí nghiệm:
+ Mở van áp kế, dùng tay quay dịch chuyển piston để lấy một lượng khí xác định.
+ Đổ nước nóng vào hộp chứa nước sao cho xilanh ngập hoàn toàn trong nước.
+ Khi nhiệt độ không tăng nữa, đóng van áp kế, ghi giá trị thể tích và áp suất của khí.
+ Sau khoảng 5 phút, dịch chuyển piston để áp suất trở lại giá trị ban đầu, ghi giá trị thể tích và nhiệt độ của khí.
+ Làm lại bước cuối cùng một số lần nữa và ghi kết quả như bảng bên.

a. Đúng. Áp suất của lượng khí trong các lần đo được giữ cố định.
b. Đúng. Thí nghiệm này kiểm chứng định luật Charles.
c. Sai. Ta có
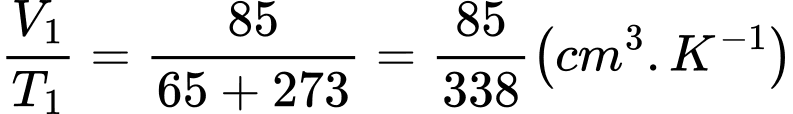
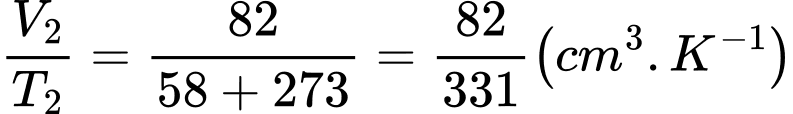
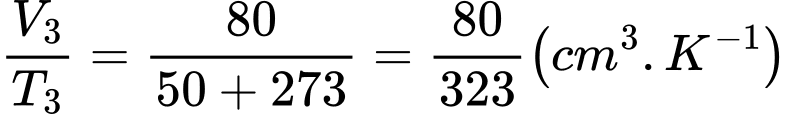
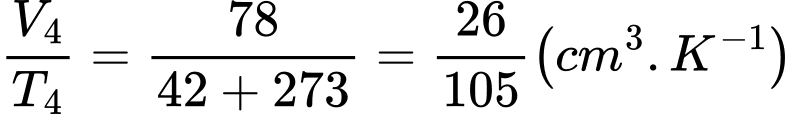
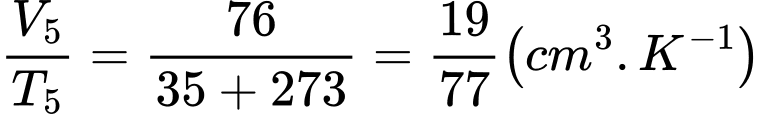
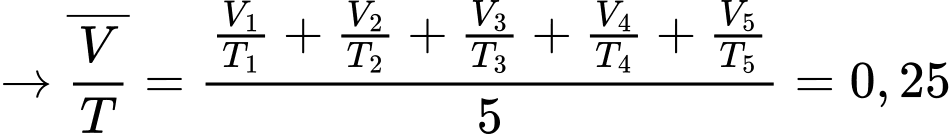
(Trong bảng trên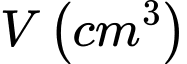 có 2 chữ số có ý nghĩa,
có 2 chữ số có ý nghĩa, 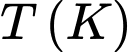 có 3 chữ số có ý nghĩa. Nếu tính giá trị trung bình của phép tính có xuất hiện tích giữa
có 3 chữ số có ý nghĩa. Nếu tính giá trị trung bình của phép tính có xuất hiện tích giữa  và
và 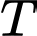 , ta phải làm tròn đến số chữ số có ý nghĩa của đại lượng có số chữ số có ý nghĩa nhỏ hơn ở đây là 2).
, ta phải làm tròn đến số chữ số có ý nghĩa của đại lượng có số chữ số có ý nghĩa nhỏ hơn ở đây là 2).
d. Sai. Ta có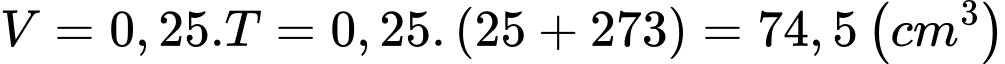
b. Đúng. Thí nghiệm này kiểm chứng định luật Charles.
c. Sai. Ta có
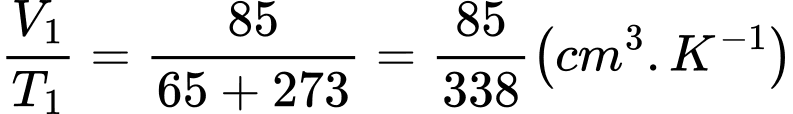
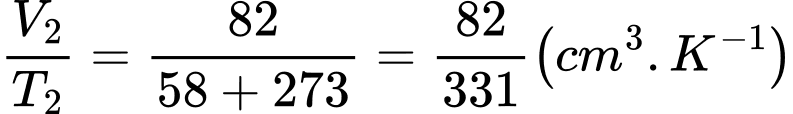
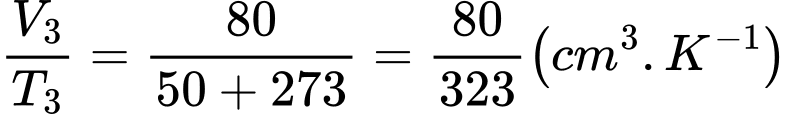
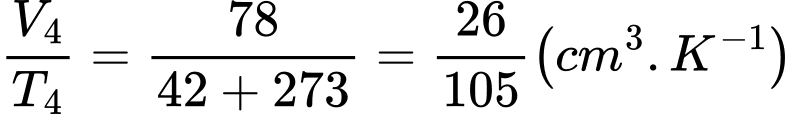
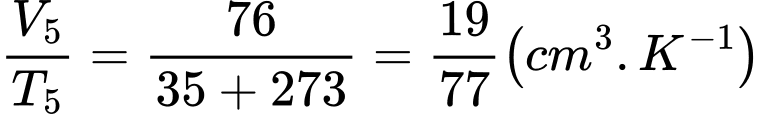
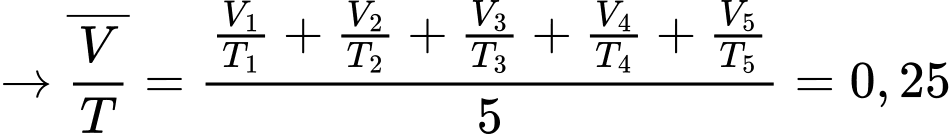
(Trong bảng trên
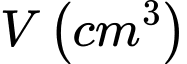 có 2 chữ số có ý nghĩa,
có 2 chữ số có ý nghĩa, 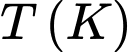 có 3 chữ số có ý nghĩa. Nếu tính giá trị trung bình của phép tính có xuất hiện tích giữa
có 3 chữ số có ý nghĩa. Nếu tính giá trị trung bình của phép tính có xuất hiện tích giữa  và
và 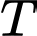 , ta phải làm tròn đến số chữ số có ý nghĩa của đại lượng có số chữ số có ý nghĩa nhỏ hơn ở đây là 2).
, ta phải làm tròn đến số chữ số có ý nghĩa của đại lượng có số chữ số có ý nghĩa nhỏ hơn ở đây là 2).
d. Sai. Ta có
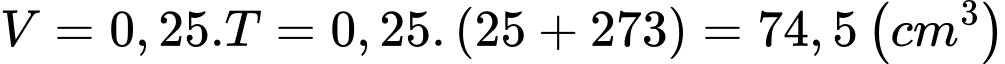
Câu 21 [1029241]: Đồ thị hình bên miêu tả quá trình biến đổi trạng thái của một lượng khí lí tưởng. Trạng thái (1) khối khí có nhiệt độ 27 °C.
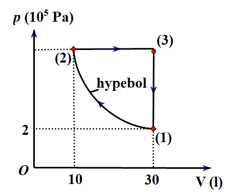

a. Sai.  là quá trình đẳng nhiệt
là quá trình đẳng nhiệt  Khối khí không toả nhiệt hay thu nhiệt trong giai đoạn này.
Khối khí không toả nhiệt hay thu nhiệt trong giai đoạn này.
b. Sai. Áp dụng định luật Boyle cho 2 trạng thái và
và  ta có
ta có
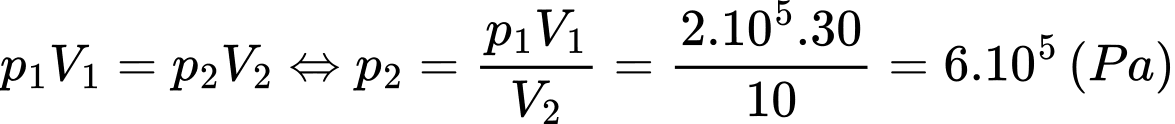
c. Đúng. Ta có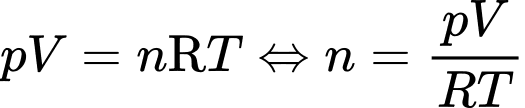
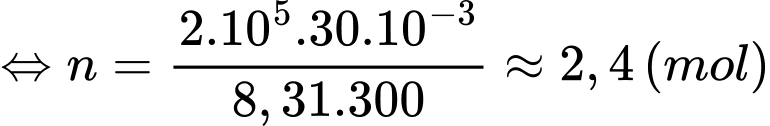
d. Sai. Xét quá trình
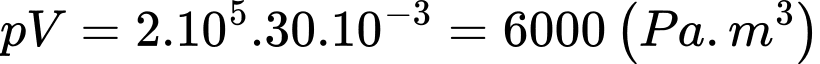
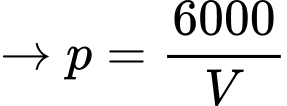
+) Quá trình khối khí nhận công (Vì thể tích giảm)
khối khí nhận công (Vì thể tích giảm)
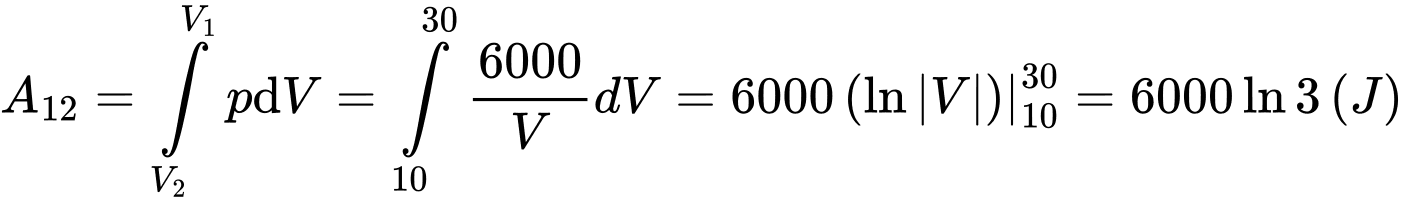
+) Quá trình khối khí sinh công (Vì thể tích tăng)
khối khí sinh công (Vì thể tích tăng)
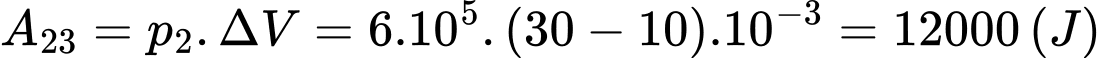
+) Quá trình khối khí không thay đổi thể tích nên không sinh hay nhận công.
khối khí không thay đổi thể tích nên không sinh hay nhận công.
Ta có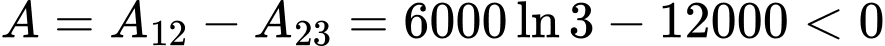 (vật nhận công lấy dấu dương, vật sinh công lấy dấu âm).
(vật nhận công lấy dấu dương, vật sinh công lấy dấu âm).
 Cả quá trình trên khối khí sinh công.
Cả quá trình trên khối khí sinh công.
 là quá trình đẳng nhiệt
là quá trình đẳng nhiệt  Khối khí không toả nhiệt hay thu nhiệt trong giai đoạn này.
Khối khí không toả nhiệt hay thu nhiệt trong giai đoạn này.
b. Sai. Áp dụng định luật Boyle cho 2 trạng thái
 và
và  ta có
ta có
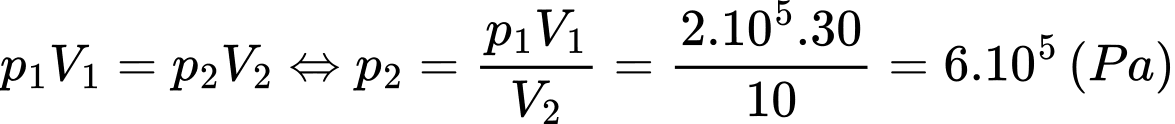
c. Đúng. Ta có
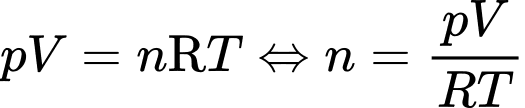
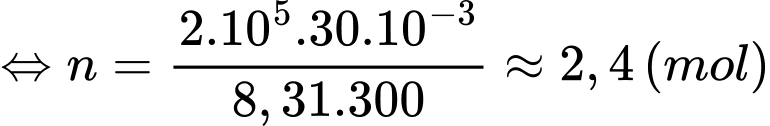
d. Sai. Xét quá trình

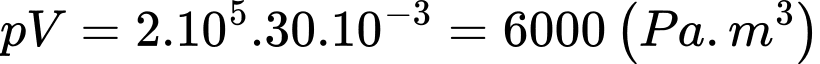
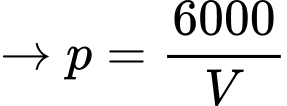
+) Quá trình
 khối khí nhận công (Vì thể tích giảm)
khối khí nhận công (Vì thể tích giảm)
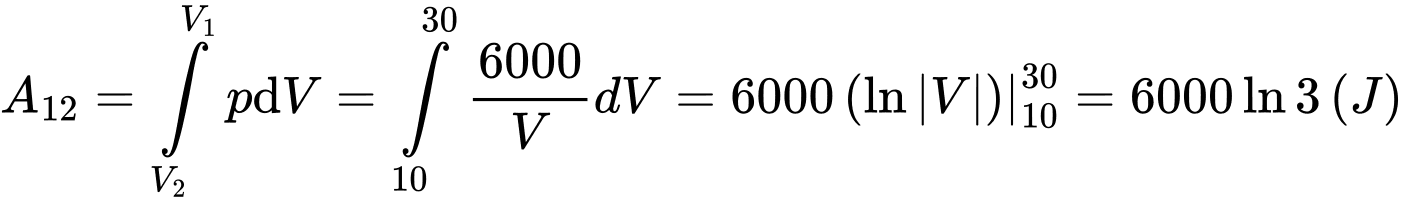
+) Quá trình
 khối khí sinh công (Vì thể tích tăng)
khối khí sinh công (Vì thể tích tăng)
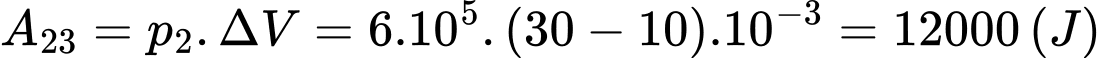
+) Quá trình
 khối khí không thay đổi thể tích nên không sinh hay nhận công.
khối khí không thay đổi thể tích nên không sinh hay nhận công.
Ta có
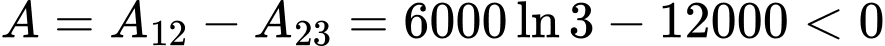 (vật nhận công lấy dấu dương, vật sinh công lấy dấu âm).
(vật nhận công lấy dấu dương, vật sinh công lấy dấu âm).
 Cả quá trình trên khối khí sinh công.
Cả quá trình trên khối khí sinh công.
Câu 22 [1029242]: Một bình tích áp được dùng trong máy lọc nước có hai phần: bóng chứa nước và bóng chứa khí như hình bên. Khi chưa chứa nước, bóng chứa khí chiếm toàn bộ thể tích trong bình là 12 lít, áp suất 120 kPa. Đường ống dẫn nước vào, ra bóng chứa nước có gắn rơ le áp suất điều khiển đóng mở mạch điện. Khi lượng nước trong bóng chứa nước tăng đến 9 lít thì áp suất nước đạt cực đại, rơ le ngắt mạch, máy ngừng cung cấp nước vào bình. Khi lượng nước trong bình giảm đến 6 lít, rơ le tự động đóng mạch để máy cung cấp nước trở lại. Coi nhiệt độ trong bóng chứa khí không đổi. Các bóng mềm, tổng thể tích nước và khí bằng thể tích bình, mặt tiếp xúc của bóng chứa nước và chứa khí luôn có dạng phẳng.
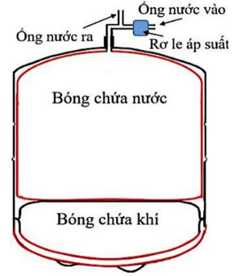

a. Đúng. Khi nhiệt độ không đổi, nước được bơm vào bình  Thể tích bóng chứa khí giảm
Thể tích bóng chứa khí giảm  Áp suất chất khí trong bóng chứa khí tăng.
Áp suất chất khí trong bóng chứa khí tăng.
b. Sai. Khi nước trong bình giảm, thể tích khí trong bóng chứa khí tăng mà khối lượng khí không đổi Mật độ phân tử khí trong bóng chứa khí giảm.
Mật độ phân tử khí trong bóng chứa khí giảm.
c. Sai.
Trạng thái 1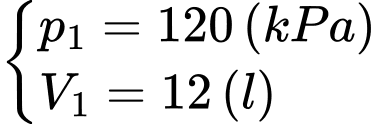
Trạng thái 2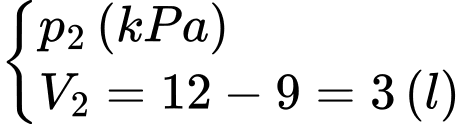
Áp dụng định luật Boyle ta có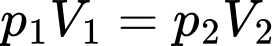
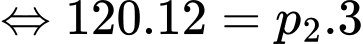
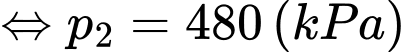
d. Đúng.
+) Áp suất khối khí tại thời điểm rơ-le đóng mạch để máy cung cấp nước trở lại là:
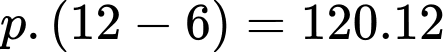
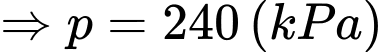
+) Rơ-le áp suất luôn đóng tại cùng 1 áp suất
 Thể tích của khối khí trước khi giảm khí tại áp suất
Thể tích của khối khí trước khi giảm khí tại áp suất 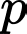 là
là 
 Thể tích của khối khí sau khi giảm khí tại áp suất
Thể tích của khối khí sau khi giảm khí tại áp suất 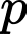 là
là
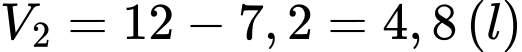
Ta có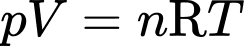
+) Tại thời điểm rơ-le đóng mạch để máy cung cấp nước trở lại,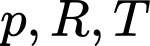 không đổi
không đổi 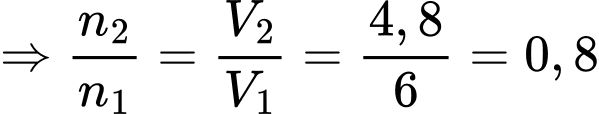
 Lượng khí thoát ra chiếm 20% lượng khí ban đầu.
Lượng khí thoát ra chiếm 20% lượng khí ban đầu.
 Thể tích bóng chứa khí giảm
Thể tích bóng chứa khí giảm  Áp suất chất khí trong bóng chứa khí tăng.
Áp suất chất khí trong bóng chứa khí tăng.
b. Sai. Khi nước trong bình giảm, thể tích khí trong bóng chứa khí tăng mà khối lượng khí không đổi
 Mật độ phân tử khí trong bóng chứa khí giảm.
Mật độ phân tử khí trong bóng chứa khí giảm.
c. Sai.
Trạng thái 1
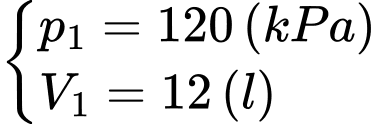
Trạng thái 2
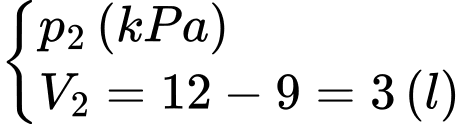
Áp dụng định luật Boyle ta có
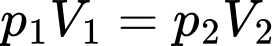
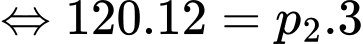
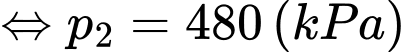
d. Đúng.
+) Áp suất khối khí tại thời điểm rơ-le đóng mạch để máy cung cấp nước trở lại là:
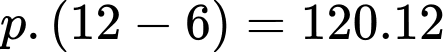
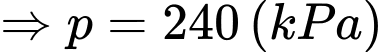
+) Rơ-le áp suất luôn đóng tại cùng 1 áp suất
 Thể tích của khối khí trước khi giảm khí tại áp suất
Thể tích của khối khí trước khi giảm khí tại áp suất 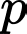 là
là 
 Thể tích của khối khí sau khi giảm khí tại áp suất
Thể tích của khối khí sau khi giảm khí tại áp suất 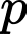 là
là
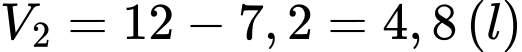
Ta có
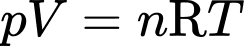
+) Tại thời điểm rơ-le đóng mạch để máy cung cấp nước trở lại,
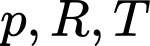 không đổi
không đổi 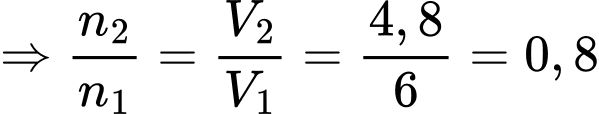
 Lượng khí thoát ra chiếm 20% lượng khí ban đầu.
Lượng khí thoát ra chiếm 20% lượng khí ban đầu.
PHẦN III. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 23 [1029243]: Một khối lượng khí có thể tích 9 lít ở nhiệt độ 27 °C. Nung nóng đẳng áp khối khí này tới 127 °C thì thể tích của nó bằng bao nhiêu lít?
Áp dụng định luật Charles ta có 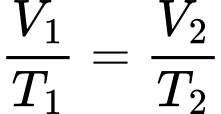
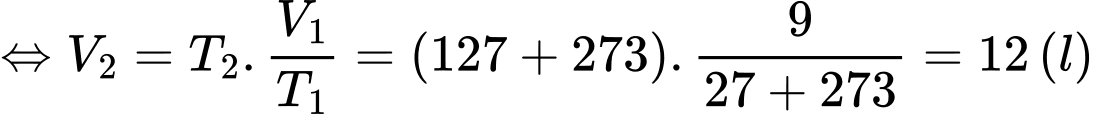
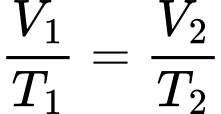
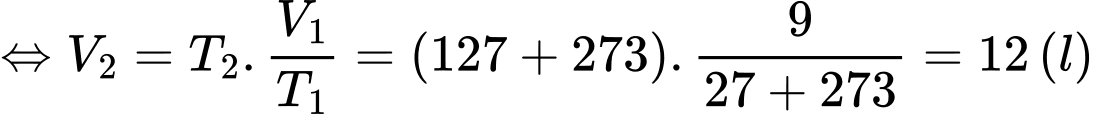
Câu 24 [1029244]: Một bình kín chứa khí lí tưởng ở nhiệt độ 27 °C và áp suất 2 atm. Nếu nung nóng đẳng tích khí tới nhiệt độ 87 °C thì áp suất của khí trong bình khi đó là bao nhiêu atm? (Kết quả làm tròn đến chữ số hàng phần mười).
Áp dụng quá trình đẳng tích ta có 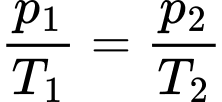
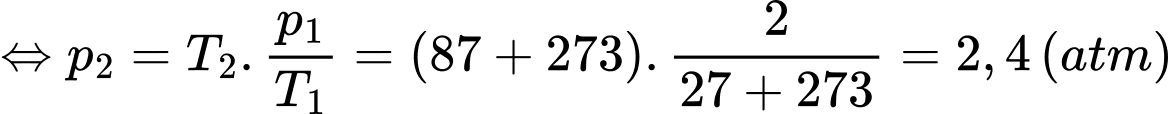
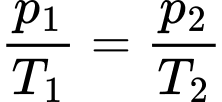
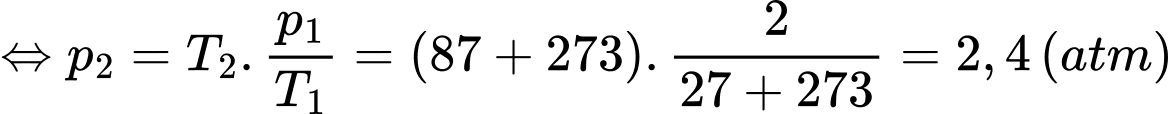
Câu 25 [1029245]: Ở điều kiện tiêu chuẩn (áp suất là latm), khối lượng riêng của khí hydrogen là 9.10-2 kg/m3. Tốc độ căn quân phương của phân tử khí hydrogen là X.103 m/s. Tìm X. (Kết quả làm tròn đến 2 chữ số thập phân).
Ta có 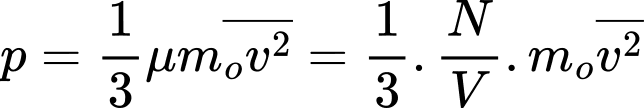
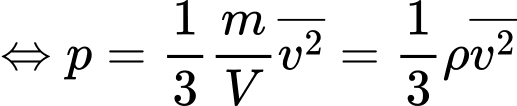
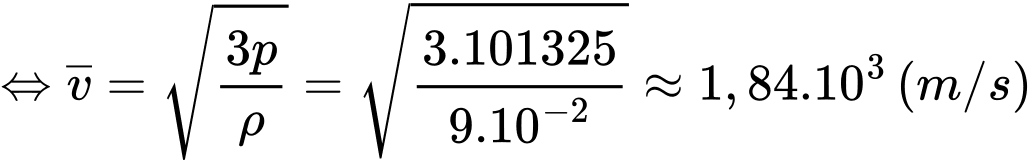
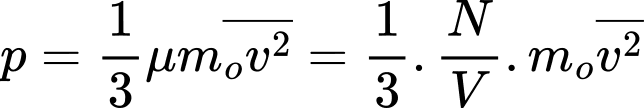
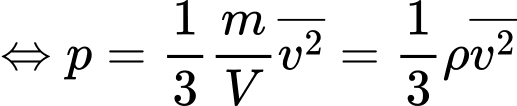
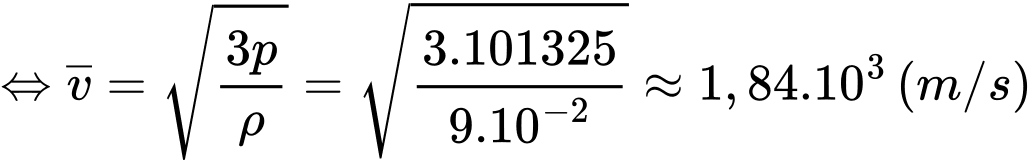
Sử dụng thông tin sau cho câu 4 và câu 5:
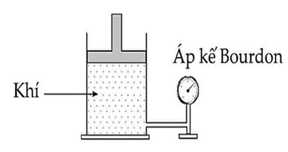
Một loại khí chứa trong một xilanh được lắp một pít-tông như hình bên. Thể tích của nó trong xilanh là 1,5 lít. Chỉ số áp suất trên đồng hồ đo bằng áp kế Bourdon là 2,54.105 N/m2.

Câu 26 [1029246]: Nếu di chuyển pít-tông để thể tích của khí giảm một nửa thể tích ban đầu mà không làm thay đổi nhiệt độ. Áp suất mới của khối khí là x.103 N/m2. Giá trị của x là?
Theo định luật Boyle áp suất tỉ lệ nghịch với thể tích. Nếu thể tích giảm 2 lần  Áp suất tăng 2 lần.
Áp suất tăng 2 lần.
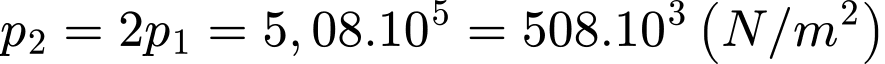
 Áp suất tăng 2 lần.
Áp suất tăng 2 lần.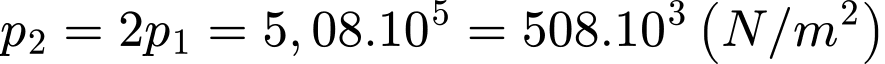
Câu 27 [1029247]: Nếu nhiệt độ của khối khí tăng từ giá trị ban đầu 27 °C lên đến 327 °C nhưng thể tích giữ nguyên. Áp suất mới của lượng khí là bao nhiêu atm? (kết quả làm tròn đến chữ số hàng phần trăm)? Biết 1 atm = 101325 Pa.
Áp dụng quá trình đẳng tích ta có 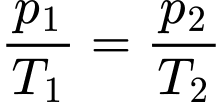
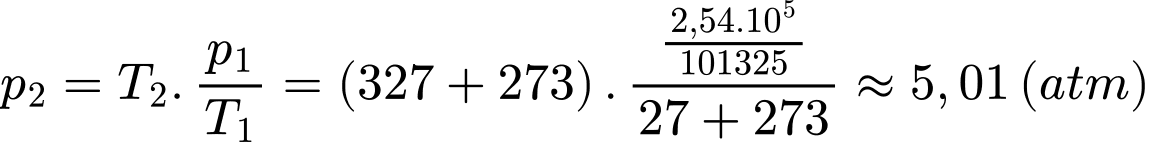
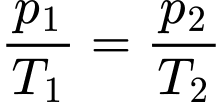
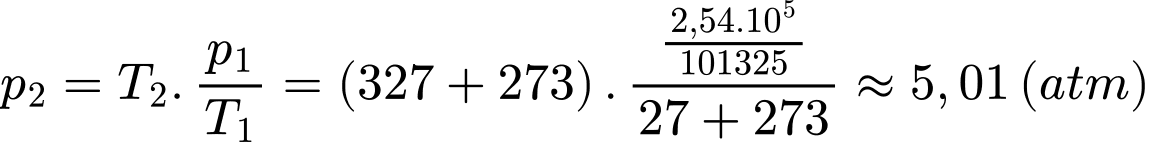
Câu 28 [1029248]: Tại các bệnh viện, oxygen được nén và lưu trữ trong các bình thép. Mỗi bình có thể tích 10 lít và chứa khí oxygen ở áp suất 15 MPa, ở nhiệt độ phòng 27 °C. Giả sử khí oxygen trong bình tuân theo định luật khí lý tưởng. Số phân tử khí oxygen chứa trong bình là x.1024 phân tử. Tìm x (làm tròn kết quả đến chữ số hàng phần mười).
Áp dụng phương trình Claperyon ta có
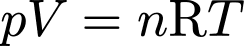
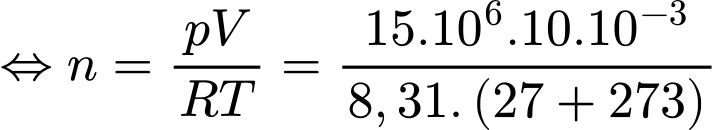
Số phân tử khí Oxygen chứa trong bình là
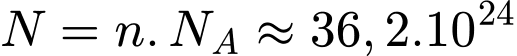
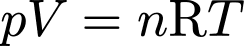
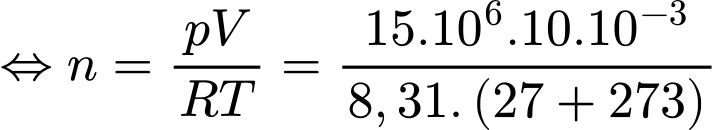
Số phân tử khí Oxygen chứa trong bình là