MÔ HÌNH NGUYÊN TỬ
Vào đầu thế kỉ 20, một số mô hình nguyên tử được ra đời để giải thích cho cấu tạo của nguyên tử nhưng tuy nhiên các mô hình này không cung cấp một mô tả đầy đủ về trạng thái của các electron trong nguyên tử cũng như nhiều tính chất khác.Từ đó dẫn đến việc phải có một mô hình mới ra đời: Mô hình hiện đại được đề xuất bởi nhà vật lý người Áo Erwin Schrödinger vào năm 1926. Theo mô hình hiện đại về nguyên tử, electron chuyển động rất nhanh trong cả khu vực không gian xung quanh hạt nhân với xác xuất tìm thấy các hạt electron là khác nhau, sự chuyển động này không theo một quỹ đạo nhất định và nó tạo thành một hình ảnh giống như đám mây electron (Hình vẽ dưới). Tuy nhiên, ta có thể xác định được vùng không gian xung quanh hạt nhân mà tại đó xác xuất tìm thấy electron là lớn nhất (khoảng 90%) và vùng không gian này gọi là Orbital nguyên tử (Atomic orbital – kí hiệu là AO).

Hình vẽ. Đám mây electron
Các electron sẽ được chia thành các lớp gọi là lớp electron. Số lớp electron (n) thể hiện kích thước của orbital nguyên tử. Giá trị n càng nhỏ thì kích thước orbital nguyên tử càng nhỏ, electron thuộc các lớp này càng gần hạt nhân và sẽ càng bị hút mạnh hơn về phía hạt nhân, dẫn đến electron sẽ có mức năng lượng thấp hơn so với electron thuộc các lớp ở xa hạt nhân, giá trị n lớn. Số lớp electron có thể có các giá trị nguyên là 1, 2, 3, …
Câu 1 [382276]: Orbital nguyên tử là gì?
A, Khu vực không gian xung quanh hạt nhân có thể tìm thấy electron.
B, Khu vực không gian xung quanh hạt nhân.
C, Khu vực không gian xung quanh hạt nhân mà tại đó xác xuất tìm thấy electron khoảng 90%.
D, Khu vực không gian xung quanh hạt nhân mà tại đó xác xuất tìm thấy electron khoảng 95%.
HƯỚNG DẪN GIẢI:
- Orbital nguyên tử (AO - Atomic Orbital) là vùng không gian xung quanh hạt nhân nguyên tử, nơi có xác suất cao nhất tìm thấy electron, khoảng trên 90%
⇒ Chọn đáp án C Đáp án: C
- Orbital nguyên tử (AO - Atomic Orbital) là vùng không gian xung quanh hạt nhân nguyên tử, nơi có xác suất cao nhất tìm thấy electron, khoảng trên 90%
⇒ Chọn đáp án C Đáp án: C
Câu 2 [382277]: Theo mô hình hiện đại và mô hình Rutherford – Bohr
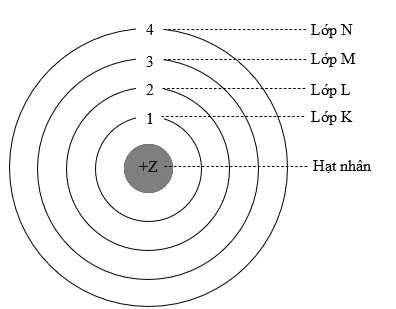
Electron thuộc lớp n = 1 sẽ có mức năng lượng như thế nào so với electron thuộc lớp n = 4?

Electron thuộc lớp n = 1 sẽ có mức năng lượng như thế nào so với electron thuộc lớp n = 4?
A, Bằng nhau.
B, Lớn hơn.
C, Nhỏ hơn.
D, Không xác định.
HƯỚNG DẪN GIẢI:
n = 1 có mức năng lượng thấp nhất, vì gần hạt nhân nhất.
n = 4 xa hạt nhân hơn, lực hút yếu hơn, dễ bị kích thích hoặc tách ra khỏi nguyên tử hơn.
⇒ Chọn đáp án C Đáp án: C
n = 1 có mức năng lượng thấp nhất, vì gần hạt nhân nhất.
n = 4 xa hạt nhân hơn, lực hút yếu hơn, dễ bị kích thích hoặc tách ra khỏi nguyên tử hơn.
⇒ Chọn đáp án C Đáp án: C
Câu 3 [382278]: Mỗi một lớp electron chỉ chứa được một lượng electron nhất định. Số electron tối đa trên một lớp được tính bằng công thức: a = 2×n2 với 
Trong đó: a là số electron tối đa trong một lớp.
n là số thứ tự của lớp electron.
Nguyên tử bromine (Br) có số hiệu nguyên tử là 35, số lớp electron tối thiểu cần để chứa hết các electron trong nguyên tử bromine là

Trong đó: a là số electron tối đa trong một lớp.
n là số thứ tự của lớp electron.
Nguyên tử bromine (Br) có số hiệu nguyên tử là 35, số lớp electron tối thiểu cần để chứa hết các electron trong nguyên tử bromine là
A, 4 lớp.
B, 3 lớp.
C, 5 lớp.
D, 2 lớp.
- Số hiệu nguyên tử của Br là 35, thay n = 4 vào công thức ta có:
a = 2×n2 = 2×42 = 32 < 35
- Nếu thay n = 5 thì a = 50 > 35 ( loại )
⇒ Chọn đáp án A Đáp án: A
a = 2×n2 = 2×42 = 32 < 35
- Nếu thay n = 5 thì a = 50 > 35 ( loại )
⇒ Chọn đáp án A Đáp án: A