ENTHALPY
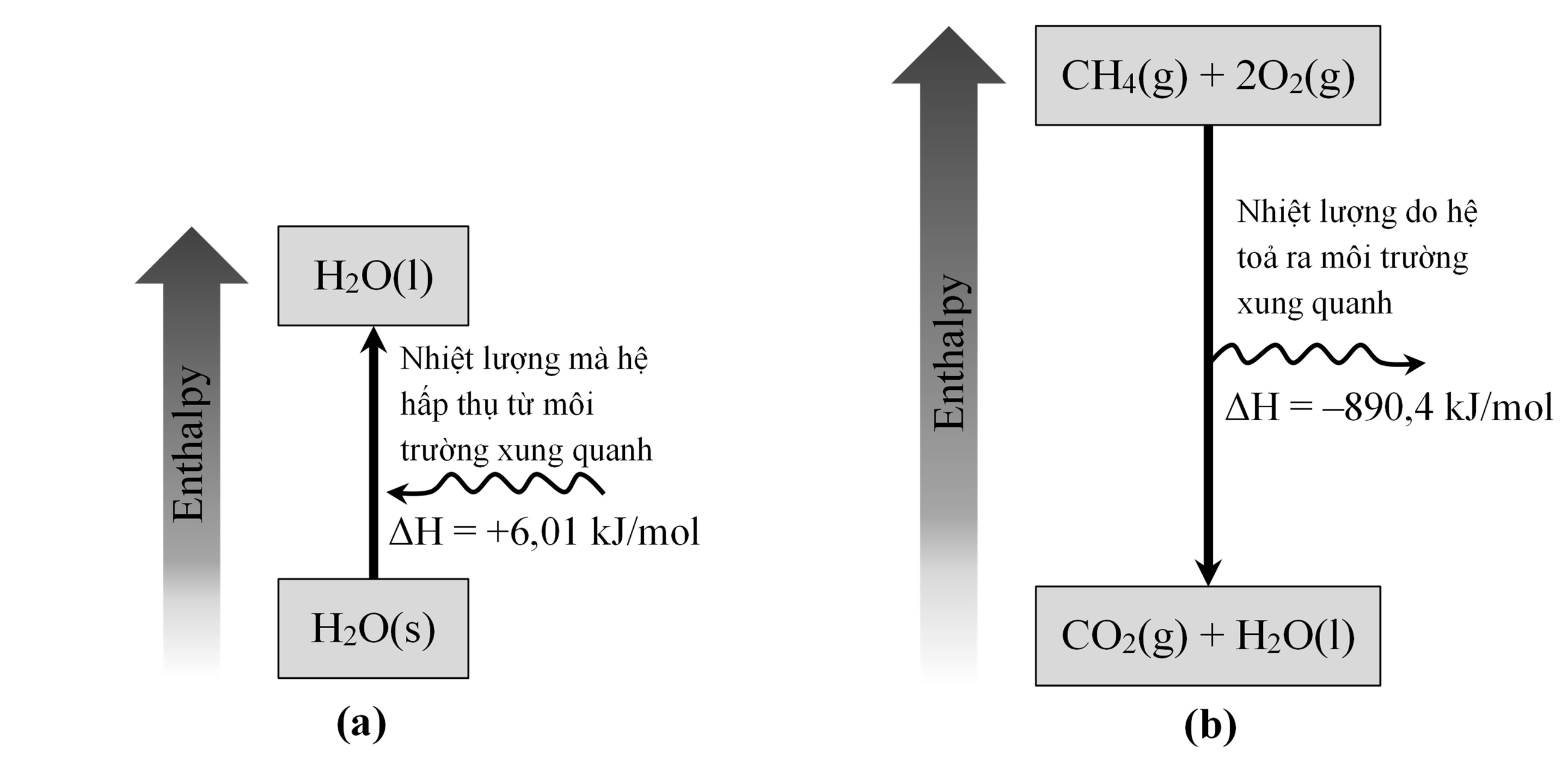
Trong điều kiện khí quyển bình thường ở mực nước biển, băng tan chảy tạo thành nước lỏng khi tiếp xúc với nhiệt độ trên 0 °C. Các phép đo cho thấy rằng cứ mỗi một mol băng chuyển thành nước lỏng trong điều kiện này thì hệ (một mol băng) hấp thụ 6,01 kJ năng lượng nhiệt.Enthalpy (ΔH) là lượng nhiệt kèm theo của quá trình. Đây là một quá trình thu nhiệt
(ΔH > 0), vì nhiệt được băng hấp thụ từ môi trường xung quanh để chuyển thành nước lỏng [Hình (a)]. Phương trình cho sự thay đổi vật lý này là
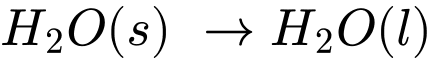
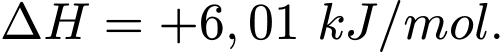
Bây giờ hãy xem xét quá trình đốt cháy khí methane (CH4), thành phần chính của khí tự nhiên:
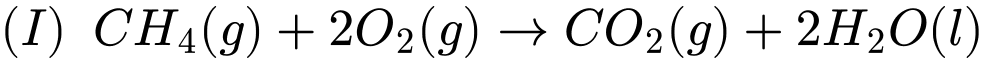
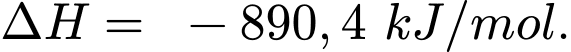
Theo những gì đã trải nghiệm, chúng ta biết rằng việc đốt khí tự nhiên sẽ thải nhiệt ra môi trường xung quanh nên đây là một quá trình tỏa nhiệt [Hình (b)]. Khi 1 mol CH4(g) phản ứng với 2 mol O2(g) tạo ra 1 mol CO2(g) và 2 mol H2O(l), 890,4 kJ nhiệt được giải phóng ra môi trường xung quanh.
Giá trị ΔH tính bằng kJ/mol không có nghĩa đây là năng lượng trên mỗi một mol của một chất phản ứng hay một chất sản phẩm cụ thể nào cả. Nó sẽ liên quan đến tất cả các chất trong một phản ứng với số lượng mol được xác định bởi các hệ số trong phương trình hóa học. Do đó, đối với quá trình đốt cháy khí methane, giá trị ΔH −890,4 kJ/mol có thể được biểu thị theo bất kỳ cách nào sau đây:
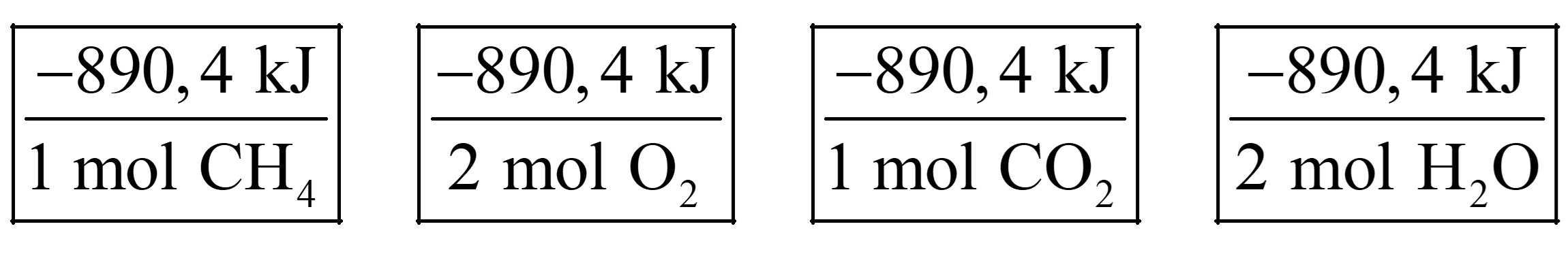
Khi viết phương trình nhiệt hóa học, chúng ta phải luôn phải xác định trạng thái vật lý của tất cả các chất phản ứng và sản phẩm, vì chúng giúp xác định sự thay đổi enthalpy thực tế. Ví dụ, trong phương trình đốt cháy khí methane, việc thay đổi sản phẩm nước ở thể lỏng thành nước ở thể hơi sẽ làm thay đổi giá trị của ΔH.
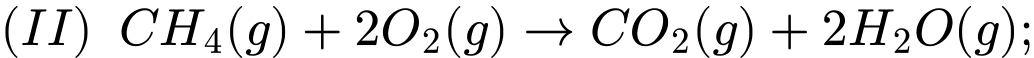
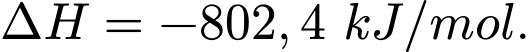
Câu 1 [382523]: Một quá trình có giá trị enthalpy âm thì quá trình đó
A, thu nhiệt.
B, tỏa nhiệt.
C, không trao đổi nhiệt.
D, có thể xảy ra.
Biến thiên enthalpy của phản ứng có giá trị âm thì phản ứng là phản ứng tỏa nhiệt. Biến thiên enthalpy càng âm, phản ứng tỏa ra càng nhiều nhiệt.
⇒ Chọn đáp án B Đáp án: B
⇒ Chọn đáp án B Đáp án: B
Câu 2 [382524]: Dựa vào các giá trị enthalpy của phương trình (I) và (II), xác định giá trị enthalpy của quá trình sau:
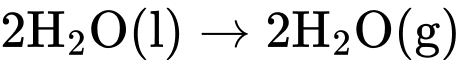
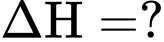
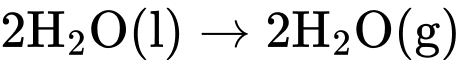
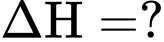
A, +44.0 kJ/mol.
B, +88.0 kJ/mol.
C, –68.0 kJ/mol.
D, –50.0 kJ/mol.
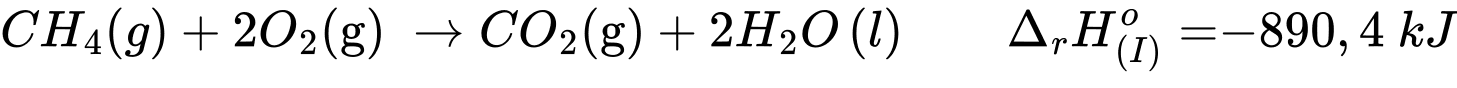
→ Khi đảo ngược lại phải ứng
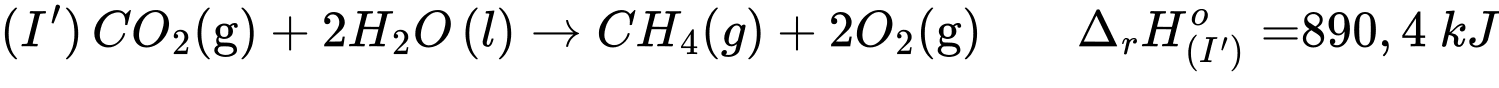
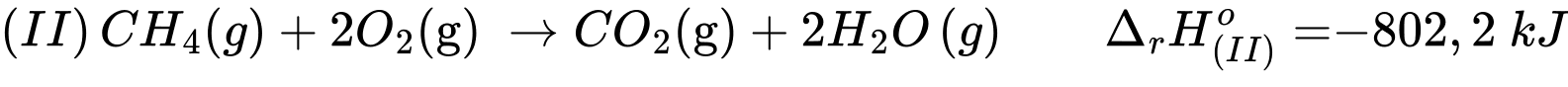
Ta có: Khi phương trình (I) + (II)
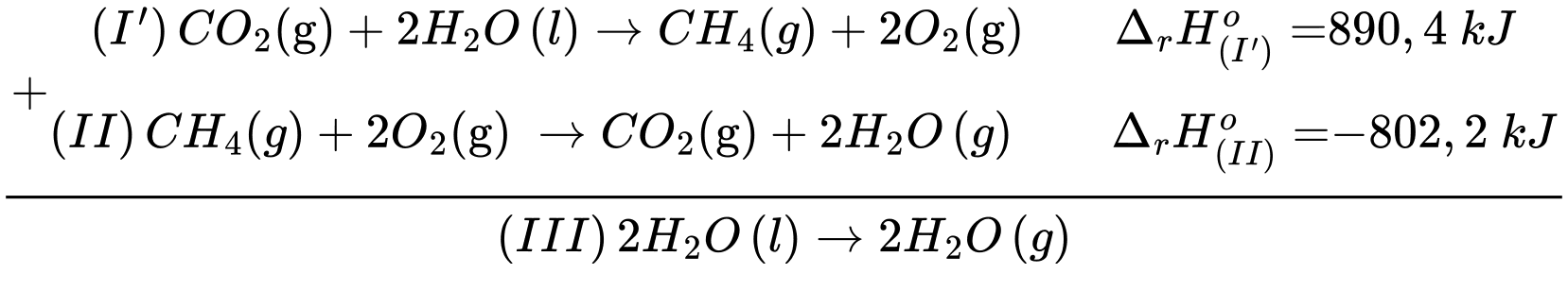
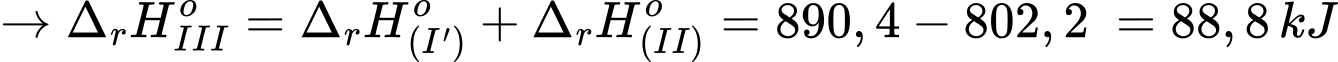
⇒ Chọn đáp án B Đáp án: B
Câu 3 [382525]: Cho sơ đồ thể hiện các chất trong hệ trước và sau phản ứng của hai quá trình hóa học liên quan như sau:
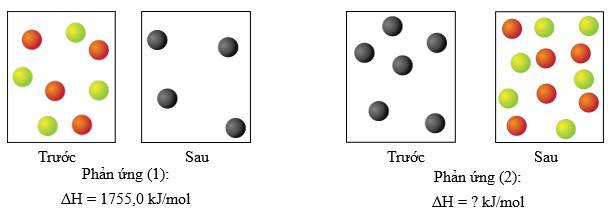
Cho biết ΔH của phản ứng đầu tiên là 1755,0 kJ/mol. Giá trị ∆H của phản ứng thứ hai là

Cho biết ΔH của phản ứng đầu tiên là 1755,0 kJ/mol. Giá trị ∆H của phản ứng thứ hai là
A, +2452.3 kJ/mol.
B, +1569.6 kJ/mol.
C, –4263,0 kJ/mol.
D, –2632.5 kJ/mol.
Phản ứng (1) ngược lại so với phản ứng (2) → phản ứng số (2) là phản ứng tỏa nhiệt
Số phân tử của phản ứng số (2) gấp 1,5 lần số phân tử của phản ứng số (1)
→ Biến thiên enthalpy của phản ứng số (2) là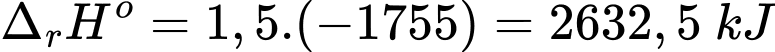
⇒ Chọn đáp án D Đáp án: D
Số phân tử của phản ứng số (2) gấp 1,5 lần số phân tử của phản ứng số (1)
→ Biến thiên enthalpy của phản ứng số (2) là
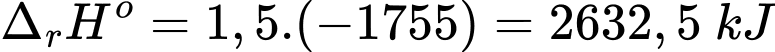
⇒ Chọn đáp án D Đáp án: D