BIẾN THIÊN ENTROPY
Biến thiên entropy tiêu chuẩn (ΔSo) của một phản ứng là đại lượng đặc trưng cho mức độ hỗn loạn của hệ.▪ ΔSo > 0: Mức độ hỗn loạn của hệ tăng.
▪ ΔSo < 0: Mức độ hỗn loạn của hệ giảm.
Để nghiên cứu sự biến đổi giá trị entropy tiêu chuẩn (ΔSo) của một phản ứng, tiến hành thí nghiệm như sau: Nung một mẫu khí SiH4 ở nhiệt độ cao, lúc này SiH4 bị phân hủy tạo thành silicon rắn và khí hydrogen.
SiH4(khí) → Si(rắn) + 2H2(khí) (*)
Bảng dưới đây cho biết giá trị entropy tiêu chuẩn của các chất.

Câu 1 [1073352]: Quá trình phân hủy SiH4 xảy ra sẽ có sự chuyển đổi mol khí như thế nào?
A, 1 mol khí → 2 mol khí.
B, 2 mol khí → 1 mol khí.
C, 2 mol khí → 2 mol khí.
D, 2 mol khí → 3 mol khí.
Nung một mẫu khí SiH4 ở nhiệt độ cao, lúc này SiH4 bị phân hủy tạo thành silicon rắn và khí hydrogen.
SiH4(khí) Si(rắn) + 2H2(khí)
Si(rắn) + 2H2(khí)
=> 1 mol SiH4 tạo 2 mol H2
Đáp án đúng là A Đáp án: A
SiH4(khí)
 Si(rắn) + 2H2(khí)
Si(rắn) + 2H2(khí)=> 1 mol SiH4 tạo 2 mol H2
Đáp án đúng là A Đáp án: A
Câu 2 [1073353]: Hệ có càng nhiều số mol chất khí thì mức độ hỗn loạn của hệ
A, càng tăng.
B, càng giảm.
C, không đổi.
D, không xác định.
Đáp án đúng là: A. càng tăng.
Mức độ hỗn loạn của hệ (hay còn gọi là độ hỗn loạn, entropy – S) phụ thuộc vào số cách sắp xếp vi mô mà các hạt có thể có. Khi số mol chất khí tăng, nghĩa là số lượng phân tử khí tăng, các hạt có nhiều cách phân bố trong không gian hơn, do đó entropy (độ hỗn loạn) tăng.
→ Mức độ hỗn loạn của hệ càng lớn. Đáp án: A
Mức độ hỗn loạn của hệ (hay còn gọi là độ hỗn loạn, entropy – S) phụ thuộc vào số cách sắp xếp vi mô mà các hạt có thể có. Khi số mol chất khí tăng, nghĩa là số lượng phân tử khí tăng, các hạt có nhiều cách phân bố trong không gian hơn, do đó entropy (độ hỗn loạn) tăng.
→ Mức độ hỗn loạn của hệ càng lớn. Đáp án: A
Câu 3 [1073354]: Xác định giá trị biến thiên entropy của phản ứng (*) và cho biết xu hướng biến đổi mức độ hỗn loạn của hệ.
A, ΔSo = 75 J/mol.K và mức độ hỗn loạn của hệ tăng.
B, ΔSo = 110 J/mol.K và mức độ hỗn loạn của hệ giảm.
C, ΔSo = –50 J/mol.K và mức độ hỗn loạn của hệ tăng.
D, ΔSo = –145 J/mol.K và mức độ hỗn loạn của hệ giảm.
SiH4(khí)  Si(rắn) + 2H2(khí) (*)
Si(rắn) + 2H2(khí) (*)
Xác định giá trị biến thiên entropy của phản ứng (*)
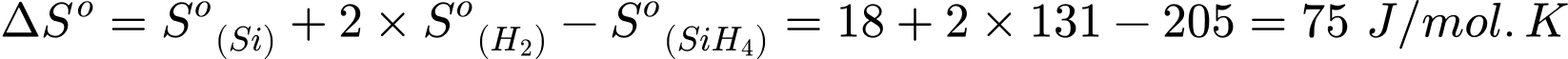
Sau phản ứng số mol khí tăng, mức độ hỗn loạn của hệ tăng.
Đáp án: A. ΔSo = 75 J/mol.K và mức độ hỗn loạn của hệ tăng. Đáp án: A
 Si(rắn) + 2H2(khí) (*)
Si(rắn) + 2H2(khí) (*)Xác định giá trị biến thiên entropy của phản ứng (*)
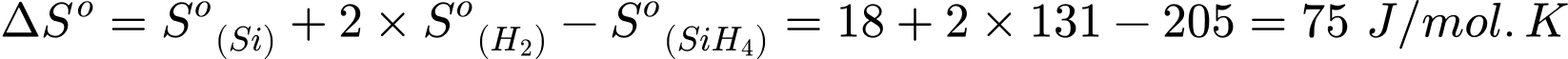
Sau phản ứng số mol khí tăng, mức độ hỗn loạn của hệ tăng.
Đáp án: A. ΔSo = 75 J/mol.K và mức độ hỗn loạn của hệ tăng. Đáp án: A