CẤU TRÚC LEWIS
Entropy (kí hiệu là S) là thước đo độ hỗn loạn (mất trật tự) của hệ số chứa lượng lớn hạt như nguyên tử, phân tử hoặc ion. Entropy gắn với độ tự do trong chuyển động của các phân tử, độ tự do càng cao thì entropy càng lớn.
Biết với phản ứng tổng quát: aA + bB → cC + cD. Entropy chuẩn của một phản ứng sẽ được tính bởi công thức sau:
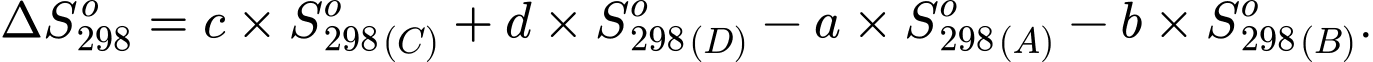
Câu 1 [1073355]: Entropy của cùng một chất ở ba thể rắn, lỏng, khí thay đổi như thế nào so với nhau?
A, Rắn > Lỏng > Khí.
B, Khí > Lỏng > Rắn.
C, Khí = Lỏng > Rắn.
D, Khí > Lỏng = Rắn.
Đáp án đúng là: B. Khí > Lỏng > Rắn.
Entropy (độ hỗn loạn) biểu thị mức độ mất trật tự của các hạt trong hệ:
- Chất rắn: các hạt sắp xếp chặt chẽ, dao động quanh vị trí cố định → độ hỗn loạn thấp → entropy nhỏ.
- Chất lỏng: các hạt chuyển động tự do hơn → độ hỗn loạn cao hơn rắn → entropy tăng.
- Chất khí: các hạt chuyển động hỗn loạn trong không gian → độ hỗn loạn lớn nhất → entropy cao nhất. Đáp án: B
Entropy (độ hỗn loạn) biểu thị mức độ mất trật tự của các hạt trong hệ:
- Chất rắn: các hạt sắp xếp chặt chẽ, dao động quanh vị trí cố định → độ hỗn loạn thấp → entropy nhỏ.
- Chất lỏng: các hạt chuyển động tự do hơn → độ hỗn loạn cao hơn rắn → entropy tăng.
- Chất khí: các hạt chuyển động hỗn loạn trong không gian → độ hỗn loạn lớn nhất → entropy cao nhất. Đáp án: B
Câu 2 [1073356]: Cho entropy của một số chất trong điều kiện chuẩn 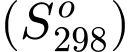 của một số chất như sau:
của một số chất như sau:
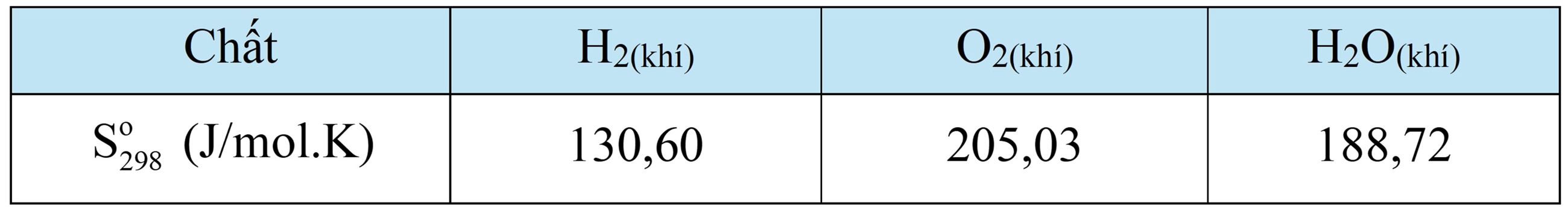
Tính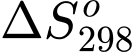 của phản ứng sau: H2(khí) + O2(khí) → H2O(khí).
của phản ứng sau: H2(khí) + O2(khí) → H2O(khí).
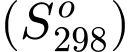 của một số chất như sau:
của một số chất như sau:
Tính
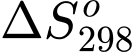 của phản ứng sau: H2(khí) + O2(khí) → H2O(khí).
của phản ứng sau: H2(khí) + O2(khí) → H2O(khí). A, 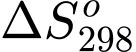 = –146,91 (J/mol.K).
= –146,91 (J/mol.K).
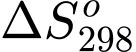 = –146,91 (J/mol.K).
= –146,91 (J/mol.K).B, 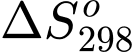 = –88,79 (J/mol.K).
= –88,79 (J/mol.K).
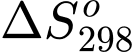 = –88,79 (J/mol.K).
= –88,79 (J/mol.K).C, 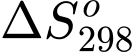 = 146,91 (J/mol.K).
= 146,91 (J/mol.K).
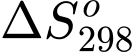 = 146,91 (J/mol.K).
= 146,91 (J/mol.K).D, 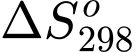 = 88,79 (J/mol.K).
= 88,79 (J/mol.K).
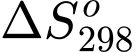 = 88,79 (J/mol.K).
= 88,79 (J/mol.K).
2H2(khí) + O2(khí)  2H2O(khí).
2H2O(khí).
Xác định giá trị biến thiên entropy của phản ứng là:
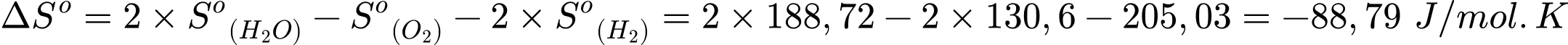 .
.
Đáp án: B.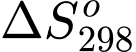 = –88,79 (J/mol.K).
Đáp án: B
= –88,79 (J/mol.K).
Đáp án: B
 2H2O(khí).
2H2O(khí).Xác định giá trị biến thiên entropy của phản ứng là:
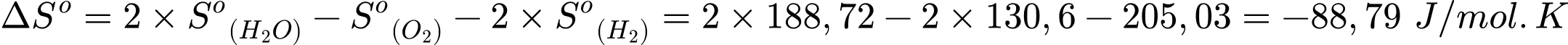 .
.Đáp án: B.
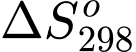 = –88,79 (J/mol.K).
Đáp án: B
= –88,79 (J/mol.K).
Đáp án: B
Câu 3 [1073357]: Thả một vài tinh thể potassium dichromate (K2Cr2O7) màu cam đỏ vào nước.
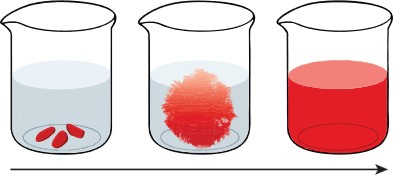
Entropy của quá trình hoà tan này sẽ có xu hướng

Entropy của quá trình hoà tan này sẽ có xu hướng
A, tăng lên.
B, giảm đi.
C, không đổi.
D, không xác định.
Đáp án đúng là: A. tăng lên
Khi các tinh thể K₂Cr₂O₇ rắn được hòa tan trong nước, các ion K⁺ và Cr₂O₇²⁻ tách ra và phân tán đều trong dung dịch.
→ Trật tự trong tinh thể bị phá vỡ, các hạt trở nên chuyển động tự do hơn và phân bố ngẫu nhiên hơn.
→ Mức độ hỗn loạn của hệ tăng, tức là entropy (S) tăng. Đáp án: A
Khi các tinh thể K₂Cr₂O₇ rắn được hòa tan trong nước, các ion K⁺ và Cr₂O₇²⁻ tách ra và phân tán đều trong dung dịch.
→ Trật tự trong tinh thể bị phá vỡ, các hạt trở nên chuyển động tự do hơn và phân bố ngẫu nhiên hơn.
→ Mức độ hỗn loạn của hệ tăng, tức là entropy (S) tăng. Đáp án: A