BIẾN THIÊN NĂNG LƯỢNG TỰ DO GIBBS
Biến thiên năng lượng tự do Gibbs (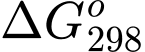 ) cho biết khả năng tự xảy ra của một phản ứng hóa học và nó được liên hệ bởi các yếu tố: nhiệt độ T, biến thiên enthalpy và biến thiên entropy của quá trình tại nhiệt độ tương ứng là
) cho biết khả năng tự xảy ra của một phản ứng hóa học và nó được liên hệ bởi các yếu tố: nhiệt độ T, biến thiên enthalpy và biến thiên entropy của quá trình tại nhiệt độ tương ứng là 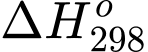 ;
; 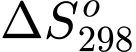 như sau:
như sau: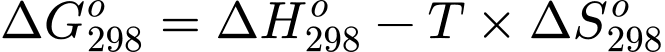
Trong đó: T là nhiệt độ tính theo thang Kelvin (K). Đơn vị của
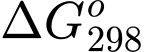 thường là J và giá trị
thường là J và giá trị 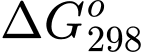 càng âm thì phản ứng diễn ra càng thuận lợi. Ở 1 bar, nhiệt độ a oC quá trình nước lỏng chuyển thành nước dạng hơi có thể tự diễn ra:
càng âm thì phản ứng diễn ra càng thuận lợi. Ở 1 bar, nhiệt độ a oC quá trình nước lỏng chuyển thành nước dạng hơi có thể tự diễn ra:H2O(l) → H2O(g) (*)
Biết rằng biến thiên enthalpy và biến thiên entropy của quá trình trên lần lượt là
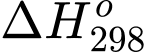 = 44,01 kJ;
= 44,01 kJ; 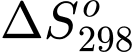 = 118,74 J.K–1. Giả sử biến thiên enthalpy và biến thiên entropy của quá trình không phụ thuộc vào nhiệt độ.
= 118,74 J.K–1. Giả sử biến thiên enthalpy và biến thiên entropy của quá trình không phụ thuộc vào nhiệt độ.
Câu 1 [1073358]: Ở 1 bar, nhiệt độ 298 K, nước tồn tại chủ yếu ở dạng
A, rắn.
B, lỏng.
C, khí.
D, không xác định.
Đáp án: B. lỏng.
- Ở áp suất 1 bar (≈ 1 atm) và nhiệt độ 298 K (25°C) — tức là điều kiện thường trong phòng thí nghiệm — nước tồn tại chủ yếu ở thể lỏng.
- Nước rắn (băng) chỉ tồn tại ổn định dưới 0°C, còn hơi nước chỉ chiếm lượng rất nhỏ trong không khí ở 25°C. Đáp án: B
- Ở áp suất 1 bar (≈ 1 atm) và nhiệt độ 298 K (25°C) — tức là điều kiện thường trong phòng thí nghiệm — nước tồn tại chủ yếu ở thể lỏng.
- Nước rắn (băng) chỉ tồn tại ổn định dưới 0°C, còn hơi nước chỉ chiếm lượng rất nhỏ trong không khí ở 25°C. Đáp án: B
Câu 2 [1073359]: Với giá trị a bằng bao nhiêu thì quá trình (*) có thể tự xảy ra?
A, 80,14.
B, 97,64.
C, 105,97.
D, 158,74.
Để phản ứng tự xảy ra thì 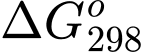 < 0: Phản ứng tự xảy ra.
< 0: Phản ứng tự xảy ra.
Ta có:
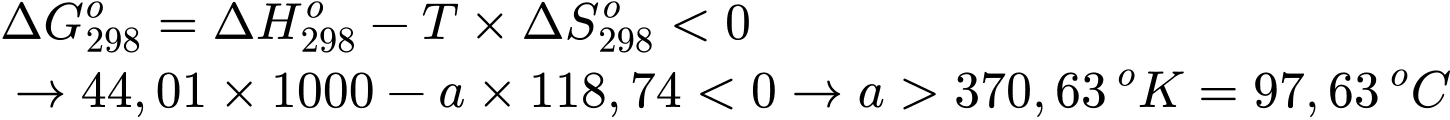
Với giá trị a bằng 97,64 thì quá trình (*) có thể tự xảy ra
Đáp án: B. 97,64. Đáp án: B
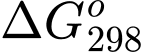 < 0: Phản ứng tự xảy ra.
< 0: Phản ứng tự xảy ra.Ta có:
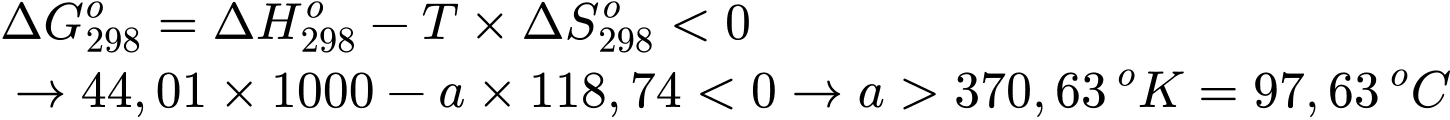
Với giá trị a bằng 97,64 thì quá trình (*) có thể tự xảy ra
Đáp án: B. 97,64. Đáp án: B
Câu 3 [1073360]: Cho các phát biểu sau:
(a)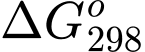 lớn hơn 0 thì quá trình không tự diễn ra.
lớn hơn 0 thì quá trình không tự diễn ra.
(b) Nhiệt độ càng cao thì quá trình (*) diễn ra càng thuận lợi.
(c) Quá trình (*) có thể tự xảy ra ở nhiệt độ 25 oC.
(d) Nếu phản ứng có giá trị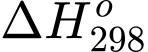 dương và
dương và 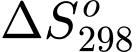 âm thì nhiệt độ càng cao, phản ứng diễn ra càng khó khăn.
âm thì nhiệt độ càng cao, phản ứng diễn ra càng khó khăn.
Các phát biểu đúng là
(a)
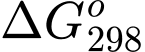 lớn hơn 0 thì quá trình không tự diễn ra.
lớn hơn 0 thì quá trình không tự diễn ra.(b) Nhiệt độ càng cao thì quá trình (*) diễn ra càng thuận lợi.
(c) Quá trình (*) có thể tự xảy ra ở nhiệt độ 25 oC.
(d) Nếu phản ứng có giá trị
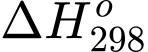 dương và
dương và 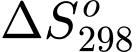 âm thì nhiệt độ càng cao, phản ứng diễn ra càng khó khăn.
âm thì nhiệt độ càng cao, phản ứng diễn ra càng khó khăn.Các phát biểu đúng là
A, (a), (b).
B, (b), (d).
C, (a), (b), (d).
D, (b), (c), (d).
- Nhận định (a) – Đúng. ΔG > 0 thì quá trình không tự diễn ra
- Nhận định (b) – Đúng. Chỉ đúng khi ΔS > 0 (tức quá trình làm tăng độ hỗn loạn), vì khi đó -T∆S làm giảm ΔG. → Vì đề không nói ngược lại (nghĩa là với ΔS > 0 thì tăng T giúp quá trình thuận lợi hơn)
- Nhận định (c) – Sai. Ở 25°C, nước không tự bay hơi hoàn toàn, nên nói rằng quá trình “có thể tự xảy ra” là không đúng — nó chỉ xảy ra một phần đến khi đạt cân bằng hơi – lỏng.
- Nhận định (d) – Đúng. ΔH > 0 (thu nhiệt), ΔS < 0 → ΔG = ΔH - TΔS = ΔH + T|ΔS| luôn dương, và T càng cao → ΔG càng lớn → càng khó xảy ra.
Đáp án: C. (a), (b), (d). Đáp án: C
- Nhận định (b) – Đúng. Chỉ đúng khi ΔS > 0 (tức quá trình làm tăng độ hỗn loạn), vì khi đó -T∆S làm giảm ΔG. → Vì đề không nói ngược lại (nghĩa là với ΔS > 0 thì tăng T giúp quá trình thuận lợi hơn)
- Nhận định (c) – Sai. Ở 25°C, nước không tự bay hơi hoàn toàn, nên nói rằng quá trình “có thể tự xảy ra” là không đúng — nó chỉ xảy ra một phần đến khi đạt cân bằng hơi – lỏng.
- Nhận định (d) – Đúng. ΔH > 0 (thu nhiệt), ΔS < 0 → ΔG = ΔH - TΔS = ΔH + T|ΔS| luôn dương, và T càng cao → ΔG càng lớn → càng khó xảy ra.
Đáp án: C. (a), (b), (d). Đáp án: C