Khi hoàn tan vào nước, muối ăn NaCl sẽ có sự phân li được biểu diễn bằng phương trình:
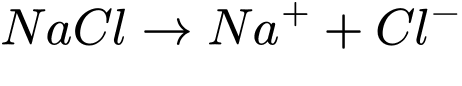
Dựa vào phương trình này, ta có thể thấy cation Na+ mang điện tích dương còn anion Cl– mang điện âm. Hai ion này mang điện tích trái dấu nên sẽ có sự hút nhau (tương tác tĩnh điện). Vậy câu hỏi được đặt ra là tại sao hai ion không hút nhau để kết hợp ngược lại trở thành NaCl ban đầu?
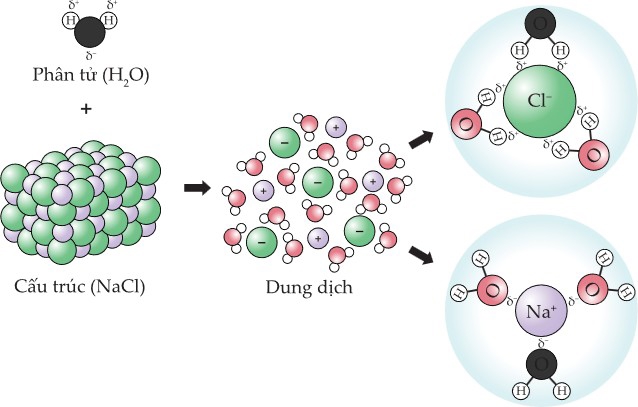
Để trả lời được câu hỏi này thì chúng ta cùng đi tìm hiểu vai trò của nước trong dung dịch chất điện li. Nước H2O ngoài đóng vai trò làm môi trường điện li thì nó còn có một vai trò quan trọng khác đó chính là kéo các ion ra khỏi cấu trúc tinh thể ban đầu và bao quanh lấy các ion đó.
Trong phân tử H2O, nguyên tử H mang một phần điện tích dương có thể tương tác với các anion, nguyên tử O mang một phần điện tích âm sẽ tương tác với các cation. Vì thế phân tử H2O có thể bao quanh cả cation và anion. Từ đó làm hạn chế, cản trở việc cation Na+ và anion Cl– hút nhau để kết hợp ngược trở lại thành phân tử NaCl ban đầu.
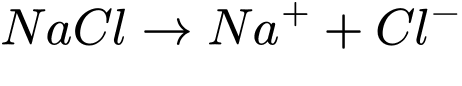
Dựa vào phương trình này, ta có thể thấy cation Na+ mang điện tích dương còn anion Cl– mang điện âm. Hai ion này mang điện tích trái dấu nên sẽ có sự hút nhau (tương tác tĩnh điện). Vậy câu hỏi được đặt ra là tại sao hai ion không hút nhau để kết hợp ngược lại trở thành NaCl ban đầu?

Để trả lời được câu hỏi này thì chúng ta cùng đi tìm hiểu vai trò của nước trong dung dịch chất điện li. Nước H2O ngoài đóng vai trò làm môi trường điện li thì nó còn có một vai trò quan trọng khác đó chính là kéo các ion ra khỏi cấu trúc tinh thể ban đầu và bao quanh lấy các ion đó.
Trong phân tử H2O, nguyên tử H mang một phần điện tích dương có thể tương tác với các anion, nguyên tử O mang một phần điện tích âm sẽ tương tác với các cation. Vì thế phân tử H2O có thể bao quanh cả cation và anion. Từ đó làm hạn chế, cản trở việc cation Na+ và anion Cl– hút nhau để kết hợp ngược trở lại thành phân tử NaCl ban đầu.
Câu 1 [382577]: Cation là
A, ion mang điện tích dương (+).
B, ion mang điện tích âm (–).
C, hạt không mang điện.
D, phân tử không mang điện.
Cation là ion mang điện tích dương (+).
Chọn đáp án A Đáp án: A
Chọn đáp án A Đáp án: A
Câu 2 [244128]: Liên kết hoá học giữa các nguyên tử trong phân tử H2O là liên kết
A, cộng hoá trị không phân cực.
B, hydrogen.
C, cộng hoá trị có cực.
D, ion.
HƯỚNG DẪN GIẢI:
- Công thức Lewis của phân tử H2O là:
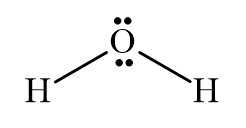
- Liên kết trong phân tử H2O được hình thành bằng sự dùng chung cặp electron giữa O và H nên đây là liên kết cộng hoá trị.
- Do O có độ âm điện lớn hơn H nên cặp electron dùng chung lệch về nguyên tử O ⟹ Phân tử H2O phân cực
⟹ Chọn đáp án: C
Đáp án: C
- Công thức Lewis của phân tử H2O là:

- Liên kết trong phân tử H2O được hình thành bằng sự dùng chung cặp electron giữa O và H nên đây là liên kết cộng hoá trị.
- Do O có độ âm điện lớn hơn H nên cặp electron dùng chung lệch về nguyên tử O ⟹ Phân tử H2O phân cực
⟹ Chọn đáp án: C
Đáp án: C
Câu 3 [186269]: Cho sơ đồ sự phân li của NaCl trong môi trường H2O:
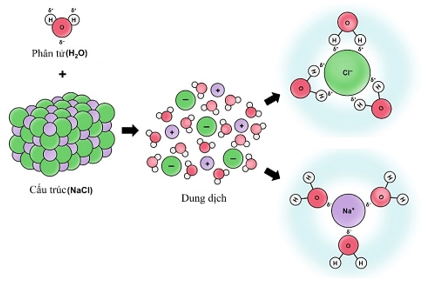
Cho các phát biểu:
(a) Các phân tử H2O có tương tác với các ion.
(b) H2O là một chất phân cực, nguyên tử H mang một phần điện tích âm, nguyên tử O mang một phần điện tích dương.
(c) Các phân tử H2O sẽ kéo ion ra khỏi cấu trúc tinh thể NaCl
(d) Các phân tử H2O sẽ bao quanh các ion Na+ và Cl–.
Trong các phát biểu trên, số phát biểu đúng là

Cho các phát biểu:
(a) Các phân tử H2O có tương tác với các ion.
(b) H2O là một chất phân cực, nguyên tử H mang một phần điện tích âm, nguyên tử O mang một phần điện tích dương.
(c) Các phân tử H2O sẽ kéo ion ra khỏi cấu trúc tinh thể NaCl
(d) Các phân tử H2O sẽ bao quanh các ion Na+ và Cl–.
Trong các phát biểu trên, số phát biểu đúng là
A, 1.
B, 2.
C, 3.
D, 4.
Đáp án C.
Các phát biểu đúng: (a), (c), (d). Đáp án: C
Các phát biểu đúng: (a), (c), (d). Đáp án: C