TỔNG HỢP AMMONIA
Quy trình Haber được sử dụng trong công nghiệp để sản xuất ra ammonia, phần lớn dùng để sản xuất phân bón, phương trình được biểu diễn như sau: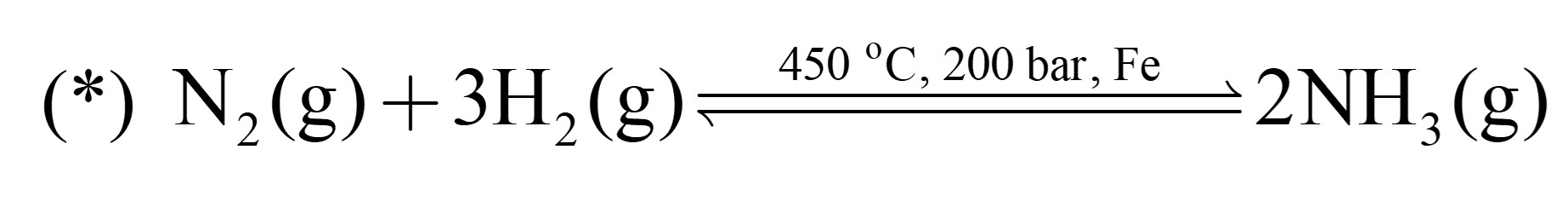
Mô tả quá trình Haber tổng hợp ammonia:
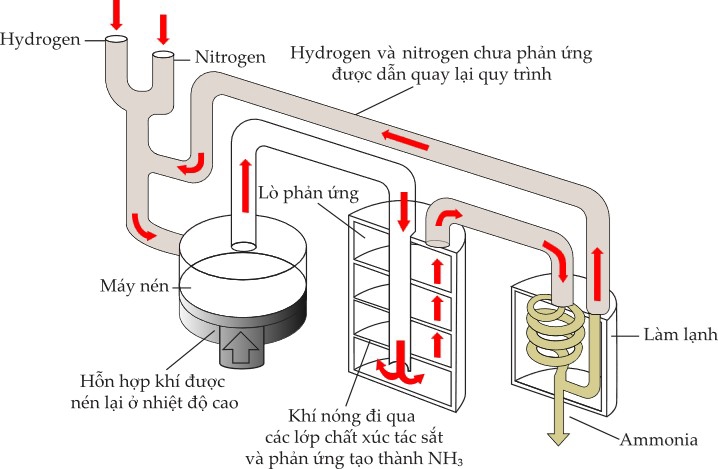
Phản ứng của nitrogen N2 và hydrogen H2 để điều chế ra ammonia NH3 là một phản ứng thuận nghịch. Trong quá trình nghiên cứu, các nhà khoa học đã tìm ra các yếu tố ảnh hưởng đến quá trình tổng hợp NH3 gồm:
▪ Yếu tố 1 – Áp suất: Khi tăng áp suất của hệ lên gần 200 bar thì hiệu suất của phản ứng tăng do khi tăng áp suất cân bằng chuyển dịch theo chiều làm giảm số mol khí (chiều thuận).
▪ Yếu tố 2 – Nhiệt độ: Theo như nghiên cứu, phản ứng tổng hợp cần phải thực hiện ở nhiệt độ thấp để làm tăng hiệu suất. Tuy nhiên, nếu thực hiện phản ứng ở nhiệt độ thấp thì tốc độ của phản ứng lại quá chậm, tốn nhiều thời gian, hiệu quả kinh tế thấp nên phải lựa chọn nhiệt độ phù hợp, khoảng 400 oC – 600 oC.
▪ Yếu tố 3 – Chất xúc tác: Bột sắt là chất xúc tác được sử dụng để giúp cho phản ứng nhanh đạt đến trạng thái cân bằng.
▪ Yếu tố 4 – Tái sử dụng hóa chất: NH3 trong hỗn hợp sau phản ứng được tách ra bằng cách hoá lỏng, N2 và H2 dư được đưa trở lại ban đầu để tái sử dụng.
Câu 1 [382565]: Phản ứng tổng hợp NH3 từ N2 và H2 có
A, giá trị ΔH < 0, phản ứng tỏa nhiệt.
B, giá trị ΔH < 0, phản ứng thu nhiệt.
C, giá trị ΔH > 0, phản ứng tỏa nhiệt.
D, giá trị ΔH > 0, phản ứng thu nhiệt.
– Nhiệt độ: Theo như nghiên cứu, phản ứng tổng hợp cần phải thực hiện ở nhiệt độ thấp để làm tăng hiệu suất.
→ Khi nhiệt độ thấp cân bằng bằng chuyển dịch theo chiều thuận → phản ứng tổng hợp NH3 là phản ứng tỏa nhiệt.
– Tuy nhiên, nếu thực hiện phản ứng ở nhiệt độ thấp thì tốc độ của phản ứng lại quá chậm, tốn nhiều thời gian, hiệu quả kinh tế thấp nên phải lựa chọn nhiệt độ phù hợp, khoảng 400 oC - 600 oC.
⇒ Chọn đáp án A Đáp án: A
→ Khi nhiệt độ thấp cân bằng bằng chuyển dịch theo chiều thuận → phản ứng tổng hợp NH3 là phản ứng tỏa nhiệt.
– Tuy nhiên, nếu thực hiện phản ứng ở nhiệt độ thấp thì tốc độ của phản ứng lại quá chậm, tốn nhiều thời gian, hiệu quả kinh tế thấp nên phải lựa chọn nhiệt độ phù hợp, khoảng 400 oC - 600 oC.
⇒ Chọn đáp án A Đáp án: A
Câu 2 [704201]: Phản ứng tổng hợp ammonia trong công nghiệp hiện nay là
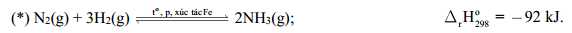
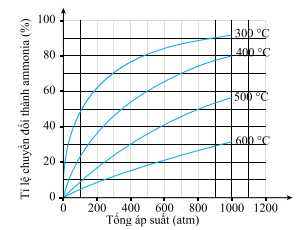
Đồ thị phần trăm chuyển hóa NH3 phụ thuộc vào nhiệt độ và áp suất tổng của phản ứng (*) được cho dưới đây:
Bỏ qua các yếu về tốc độ phản ứng, nếu áp suất là 200 atm thì nhiệt độ nào sau đây sẽ được chọn để phần trăm chuyển hóa NH3 là cao nhất?
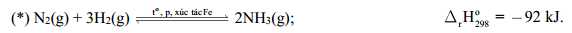
Đồ thị phần trăm chuyển hóa NH3 phụ thuộc vào nhiệt độ và áp suất tổng của phản ứng (*) được cho dưới đây:

Bỏ qua các yếu về tốc độ phản ứng, nếu áp suất là 200 atm thì nhiệt độ nào sau đây sẽ được chọn để phần trăm chuyển hóa NH3 là cao nhất?
A, 300 oC.
B, 400 oC.
C, 500 oC.
D, 600 oC.
Xét hiệu suất tại áp suất 200 atm:
- Tại 300 oC, hiệu suất chuyển hóa NH3 hơn 60% ⟶ Cao nhất.
- Tại 400 oC, hiệu suất chuyển hóa NH3 gần 40%.
- Tại 500 oC, hiệu suất chuyển hóa NH3 gần 20%.
- Tại 600 oC, hiệu suất chuyển hóa NH3 gần 10%.
⇒ Chọn đáp án A Đáp án: A
- Tại 300 oC, hiệu suất chuyển hóa NH3 hơn 60% ⟶ Cao nhất.
- Tại 400 oC, hiệu suất chuyển hóa NH3 gần 40%.
- Tại 500 oC, hiệu suất chuyển hóa NH3 gần 20%.
- Tại 600 oC, hiệu suất chuyển hóa NH3 gần 10%.
⇒ Chọn đáp án A Đáp án: A
Câu 3 [382567]: Thực hiện phản ứng giữa H2 và N2 (tỉ lệ mol tương ứng 4 : 1), trong bình kín có xúc tác, thu được hỗn hợp khí, đồng thời thấy áp suất giảm 9% so với ban đầu (trong cùng điều kiện). Hiệu suất phản ứng tổng hợp là
A, 20%.
B, 22,5%.
C, 25%.
D, 27%.
Tỉ lệ mol của H2 và N2 là 4:1
Giả sử có 4 mol H2 và 1 mol N2
Gọi áp xuất ban đầu là p
Áp suất tỉ lệ thuận với số mol khí → 4 + 1 = p (1)
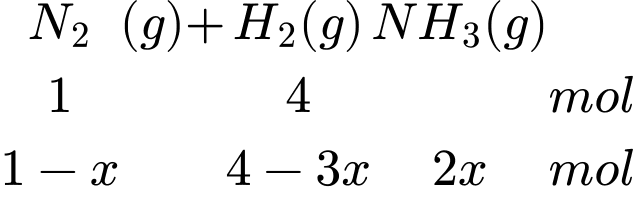
Tổng số mol khí sau phản ứng là: nH2 + nN2 + nNH3 = 4 – 3x + 1 – x + 2x = 5 – 2x (mol)
Sau phản ứng số áp suất khí của hệ giảm đi 9% so với ban đầu → 5 – 2x = 0,91p (2)
Ta có: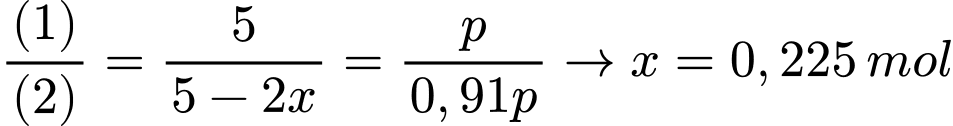
Hiệu suất của phản ứng là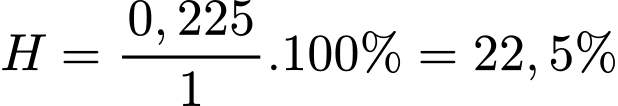
⇒ Chọn đáp án B Đáp án: B
Giả sử có 4 mol H2 và 1 mol N2
Gọi áp xuất ban đầu là p
Áp suất tỉ lệ thuận với số mol khí → 4 + 1 = p (1)
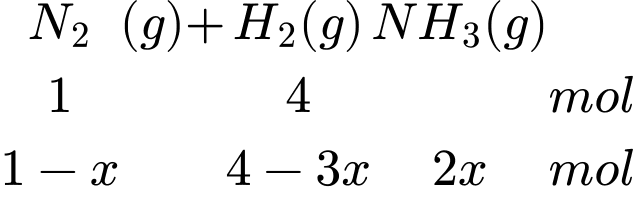
Tổng số mol khí sau phản ứng là: nH2 + nN2 + nNH3 = 4 – 3x + 1 – x + 2x = 5 – 2x (mol)
Sau phản ứng số áp suất khí của hệ giảm đi 9% so với ban đầu → 5 – 2x = 0,91p (2)
Ta có:
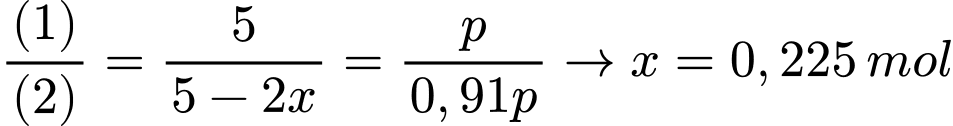
Hiệu suất của phản ứng là
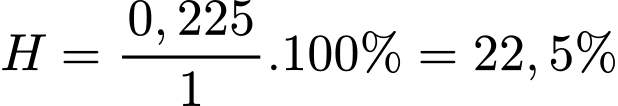
⇒ Chọn đáp án B Đáp án: B