BÁN KÍNH NGUYÊN TỬ
Theo trực giác, chúng ta thường nghĩ bán kính nguyên tử (r) là khoảng cách giữa hạt nhân của một nguyên tử với lớp vỏ electron hóa trị của nó (tức là lớp vỏ ngoài cùng bị chiếm giữ bởi một hoặc nhiều electron), điều này cũng dễ hiểu bởi vì chúng ta thường hình dung các nguyên tử giống như những quả cầu có ranh giới rời rạc.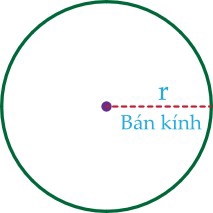
Tuy nhiên, theo mô hình cơ học lượng tử của nguyên tử, không có khoảng cách cụ thể nào từ hạt nhân mà ngoài đó không thể tìm thấy electron. Do đó, bán kính nguyên tử đòi hỏi phải có một định nghĩa cụ thể.
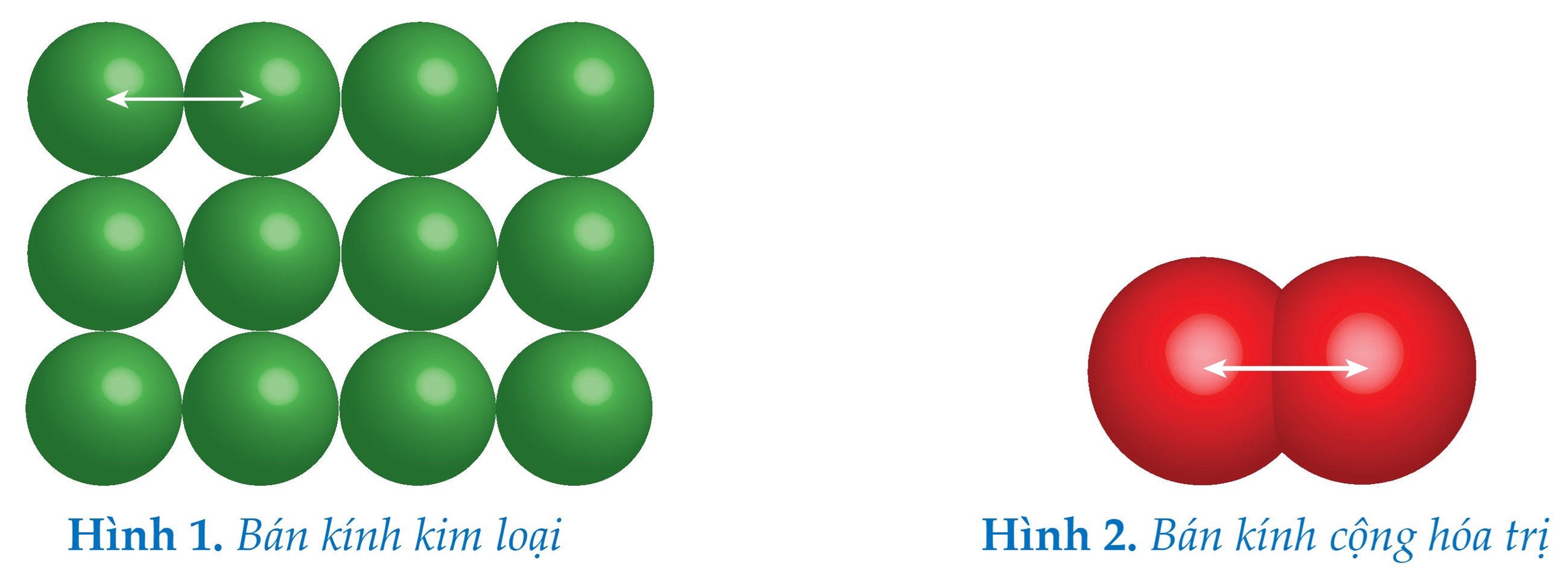
Có hai cách xác định bán kính nguyên tử. Một là bán kính kim loại, bằng một nửa khoảng cách giữa hạt nhân của hai nguyên tử kim loại giống hệt nhau và liền kề với nhau hình 1. Cách còn lại là bán kính cộng hóa trị, bằng một nửa khoảng cách giữa các hạt nhân giống hệt nhau, liền kề nhau trong một phân tử hình 2.
Hình 3 cho thấy bán kính nguyên tử của các nguyên tố nhóm chính theo vị trí của chúng trong bảng tuần hoàn. Có hai xu hướng biến đổi riêng biệt: Xu hướng biến đổi theo chu kì và xu hướng biến đổi theo nhóm.
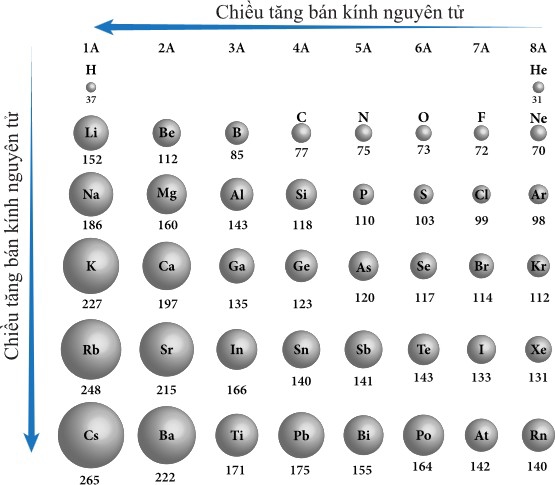
Hình 3. Xu hướng biến đổi bán kính nguyên tử của các nguyên tố nhóm chính
Câu 1 [382291]: Một nửa khoảng cách giữa các hạt nhân giống hệt nhau, liền kề nhau trong một phân tử gọi là
A, Bán kính phân tử.
B, Bán kính kim loại.
C, Đường kính nguyên tử.
D, Bán kính cộng hóa trị.
HƯỚNG DẪN GIẢI:
- Gọi bán kính của một nguyên tử (khoảng cách từ hạt nhân đến lớp ngoài cùng) là R.
- Khoảng cách giữa hai hạt nhân giống hệt nhau, hai nguyên tử đặt cạnh nhau là 2R. Vậy một nửa của 2R là R, tức là bán kính nguyên tử, hay bán kính cộng hóa trị.
⟹ Chọn đáp án: D Đáp án: D
- Gọi bán kính của một nguyên tử (khoảng cách từ hạt nhân đến lớp ngoài cùng) là R.
- Khoảng cách giữa hai hạt nhân giống hệt nhau, hai nguyên tử đặt cạnh nhau là 2R. Vậy một nửa của 2R là R, tức là bán kính nguyên tử, hay bán kính cộng hóa trị.
⟹ Chọn đáp án: D Đáp án: D
Câu 2 [382292]: Dựa vào kích thước và chỉ sử dụng hình 7.6, hãy chỉ ra rằng:
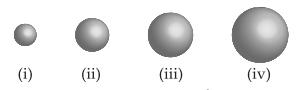
Các nguyên tử của các nguyên tố: Al, B, Mg và Sr tương ứng với quả cầu nào?

Các nguyên tử của các nguyên tố: Al, B, Mg và Sr tương ứng với quả cầu nào?
A, Quả cầu (iv) là Mg.
B, Quả cầu (i) là Al.
C, Quả cầu (iii) là Mg.
D, Quả cầu (ii) là B.
HƯỚNG DẪN GIẢI:
- Sr nằm cùng nhóm với Mg và có ZSr > ZMg nên RSr > RMg
- Mg nằm cùng chu kỳ với Al và có ZMg < ZAl nên RMg > RAl
- Al nằm cùng nhóm với B và có ZAl > ZB nên RAl > RB
⟹ Vậy RSr > RMg > RAl > RB
⟹ Chọn đáp án: C Đáp án: C
- Sr nằm cùng nhóm với Mg và có ZSr > ZMg nên RSr > RMg
- Mg nằm cùng chu kỳ với Al và có ZMg < ZAl nên RMg > RAl
- Al nằm cùng nhóm với B và có ZAl > ZB nên RAl > RB
⟹ Vậy RSr > RMg > RAl > RB
⟹ Chọn đáp án: C Đáp án: C
Câu 3 [247358]: Khẳng định nào đúng khi nói về bán kính nguyên tử?
A, Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, bán kính nguyên tử có xu hướng tăng dần.
B, Trong một nhóm, theo chiều từ trên xuống dưới, bán kính nguyên tử có xu hướng giảm dần.
C, Trong một chu kì, số lớp electron giữ nguyên, điện tích hạt nhân tăng dần làm tăng lực hút, dẫn tới bán kính nguyên tử giảm dần.
D, Trong một nhóm, theo chiều từ trên xuống dưới, số lớp electron tăng dần nên bán kính nguyên tử có xu hướng giảm dần.
Trong 1 chu kì theo chiều tăng dần điện tích hạt nhân, bán kính nguyên tử giảm dần do số lớp electron giữ nguyên, điện tích hạt nhân tăng dần làm tăng lực hút, dẫn tới bán kính nguyên tử giảm dần. Đáp án: C