Khi thực hiện phản ứng cho kim loại iron (sắt – Fe) dung dịch copper(II) chloride (CuCl2). Phương trình ion của phản ứng này là:
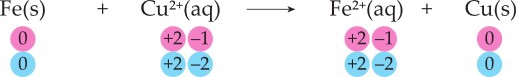
Đây là một ví dụ về phản ứng oxi hóa khử. Sắt thay thế đồng trong dung dịch muối bằng cách oxy hóa từ Fe thành Fe2+. Đồng bị đẩy khỏi muối (và bị loại khỏi dung dịch) bằng cách khử từ Cu2+ thành Cu. Chloride (Cl−), chất không bị oxy hóa cũng không bị khử, đóng vai trò như là một ion quan sát trong phản ứng này.
Vậy điều gì sẽ xảy ra nếu cho kim loại đồng vào dung dịch chứa sắt(II) chloride (FeCl2)? Liệu Cu(s) có bị oxy hóa thành Cu2+(aq) bởi Fe2+(aq) giống như cách Fe(s) bị oxy hóa thành Fe2+(aq) bởi Cu2+(aq) không? Câu trả lời là không. Trên thực tế, sẽ không có phản ứng nào xảy ra nếu chúng ta nhúng kim loại đồng vào dung dịch FeCl2.

Hình 1. Một số kim loại như đồng kém phản ứng đến mức chúng tồn tại trong tự nhiên ở đơn chất.
Cu(s) + Fe2+(aq) → không phản ứng.
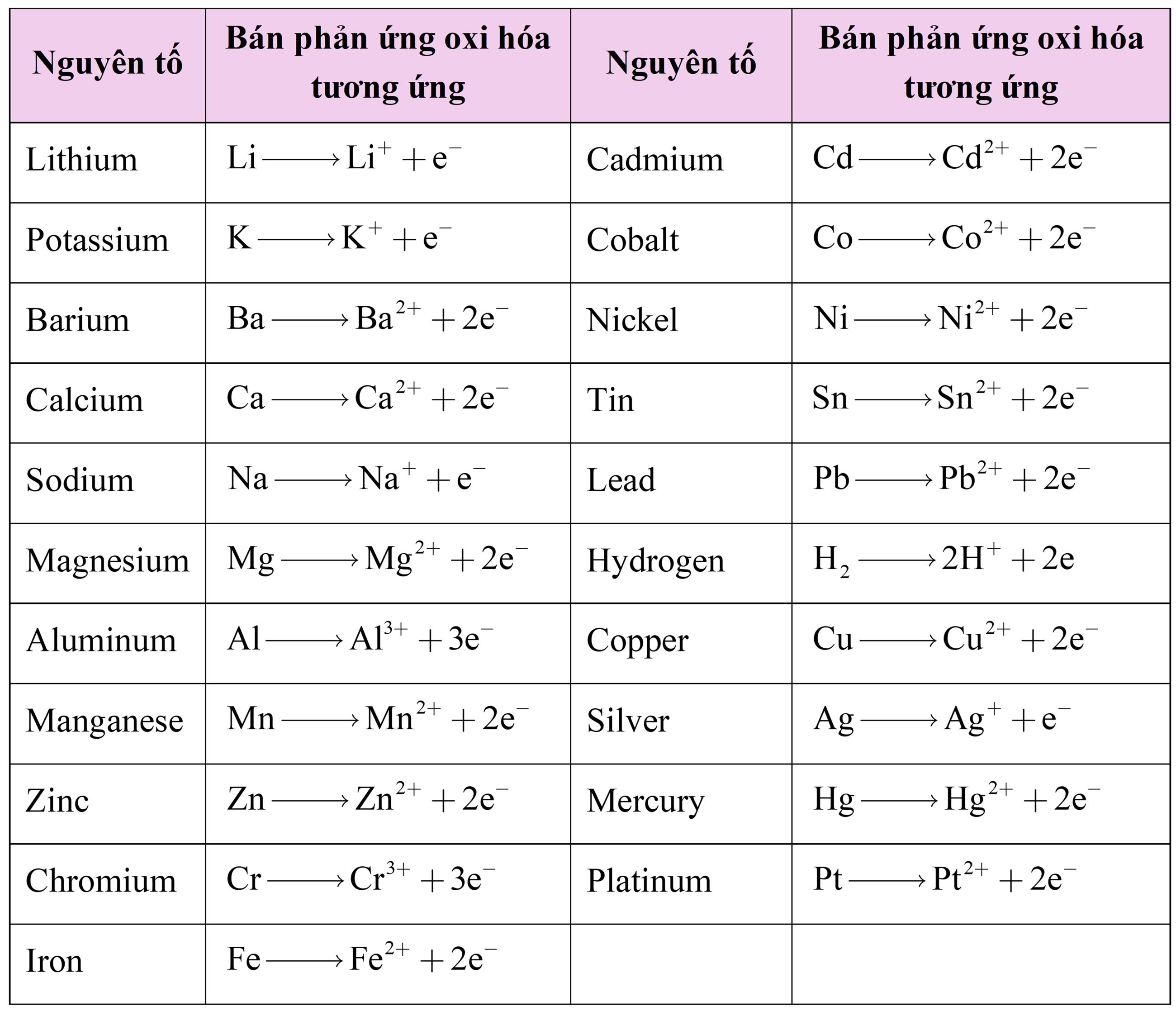
Dãy hoạt động hóa học của kim loại (Bảng 2) là danh sách các kim loại (và hydrogen) được sắp xếp từ trên xuống dưới theo chiều dễ bị oxy hóa giảm dần. Cột thứ hai hiển thị bán phản ứng oxy hóa tương ứng với từng nguyên tố trong cột đầu tiên. Lưu ý vị trí của sắt và đồng trong bảng. Sắt xuất hiện ở vị trí cao hơn trong bảng và do đó dễ bị oxy hóa hơn. Trên thực tế, một nguyên tố trong dãy sẽ bị oxy hóa bởi các ion của bất kỳ nguyên tố nào xuất hiện bên dưới nó. Do đó, theo bảng 2, kim loại sắt sẽ bị oxy hóa bởi dung dịch chứa bất kỳ ion nào sau đây: Cr3+, Fe2+, Cd2+, Co2+, Ni2+, Sn2+, H+, Cu2+, Ag+, Hg2+, Pt2+, hoặc Au3+. Mặt khác, sắt sẽ không bị oxy hóa bởi dung dịch chứa các ion Mn2+, Al3+, Mg2+, Na+, Ca2+, Ba2+, K+, Li+.

Đây là một ví dụ về phản ứng oxi hóa khử. Sắt thay thế đồng trong dung dịch muối bằng cách oxy hóa từ Fe thành Fe2+. Đồng bị đẩy khỏi muối (và bị loại khỏi dung dịch) bằng cách khử từ Cu2+ thành Cu. Chloride (Cl−), chất không bị oxy hóa cũng không bị khử, đóng vai trò như là một ion quan sát trong phản ứng này.
Vậy điều gì sẽ xảy ra nếu cho kim loại đồng vào dung dịch chứa sắt(II) chloride (FeCl2)? Liệu Cu(s) có bị oxy hóa thành Cu2+(aq) bởi Fe2+(aq) giống như cách Fe(s) bị oxy hóa thành Fe2+(aq) bởi Cu2+(aq) không? Câu trả lời là không. Trên thực tế, sẽ không có phản ứng nào xảy ra nếu chúng ta nhúng kim loại đồng vào dung dịch FeCl2.

Hình 1. Một số kim loại như đồng kém phản ứng đến mức chúng tồn tại trong tự nhiên ở đơn chất.
Cu(s) + Fe2+(aq) → không phản ứng.
Dãy hoạt động hóa học của kim loại (Bảng 2) là danh sách các kim loại (và hydrogen) được sắp xếp từ trên xuống dưới theo chiều dễ bị oxy hóa giảm dần. Cột thứ hai hiển thị bán phản ứng oxy hóa tương ứng với từng nguyên tố trong cột đầu tiên. Lưu ý vị trí của sắt và đồng trong bảng. Sắt xuất hiện ở vị trí cao hơn trong bảng và do đó dễ bị oxy hóa hơn. Trên thực tế, một nguyên tố trong dãy sẽ bị oxy hóa bởi các ion của bất kỳ nguyên tố nào xuất hiện bên dưới nó. Do đó, theo bảng 2, kim loại sắt sẽ bị oxy hóa bởi dung dịch chứa bất kỳ ion nào sau đây: Cr3+, Fe2+, Cd2+, Co2+, Ni2+, Sn2+, H+, Cu2+, Ag+, Hg2+, Pt2+, hoặc Au3+. Mặt khác, sắt sẽ không bị oxy hóa bởi dung dịch chứa các ion Mn2+, Al3+, Mg2+, Na+, Ca2+, Ba2+, K+, Li+.

Câu 1 [382315]: Trong phản ứng giữa kim loại Fe dung dịch CuCl2 ,
A, Fe đóng vai trò chất oxi hóa.
B, ion Cl– đóng vai trò là chất khử.
C, Cu đóng vai trò là ion quan sát.
D, ion Cu2+ đóng vai trò là chất oxi hóa.
Fe + Cu2+ ⟶ Fe2+ + Cu
Sắt (Fe) từ trạng thái 0 lên +2 (mất electron), nên bị oxi hóa → Fe là chất khử.
Ion Cu2+ từ +2 xuống 0 (nhận electron), nên bị khử → Cu 2+là chất oxi hóa.
⇒ Chọn đáp án D Đáp án: D
Sắt (Fe) từ trạng thái 0 lên +2 (mất electron), nên bị oxi hóa → Fe là chất khử.
Ion Cu2+ từ +2 xuống 0 (nhận electron), nên bị khử → Cu 2+là chất oxi hóa.
⇒ Chọn đáp án D Đáp án: D
Câu 2 [382316]: Dựa vào bảng trên, hãy cho biết kim loại thiếc Sn không phản ứng được với dung dịch chứa ion nào dưới đây?
A, Pb2+.
B, H+.
C, Ag+.
D, Co2+.
Vì Eo Co2+/Co < Eo Sn2+/Sn nên Co có tính khử mạnh hơn Sn.
⇒ Sn không phản ứng được với dung dịch chứa ion Co2+
⇒ Chọn đáp án D Đáp án: D
⇒ Sn không phản ứng được với dung dịch chứa ion Co2+
⇒ Chọn đáp án D Đáp án: D
Câu 3 [382317]: Dữ liệu cho thấy kết quả của sự kết hợp giữa kim loại và ion kim loại như sau:
Thí nghiệm 1: A(s) + D+(aq) →A+(aq) + D(s).
Thí nghiệm 2: C(s) + B+(aq) → C+(aq) + B(s).
Thí nghiệm 3: D(s) + B+(aq) → không phản ứng.
Thí nghiệm 4: C(s) + A+(aq) → không phản ứng.
Thí nghiệm 5: B(s) + E+(aq) → B+(aq) + E(s).
Thí nghiệm 6: D(s) + E+ (aq) → không có phản ứng.
Khả năng hoạt động hóa học đối với năm kim loại: A, B, C, D và E theo thứ tự giảm dần là
Thí nghiệm 1: A(s) + D+(aq) →A+(aq) + D(s).
Thí nghiệm 2: C(s) + B+(aq) → C+(aq) + B(s).
Thí nghiệm 3: D(s) + B+(aq) → không phản ứng.
Thí nghiệm 4: C(s) + A+(aq) → không phản ứng.
Thí nghiệm 5: B(s) + E+(aq) → B+(aq) + E(s).
Thí nghiệm 6: D(s) + E+ (aq) → không có phản ứng.
Khả năng hoạt động hóa học đối với năm kim loại: A, B, C, D và E theo thứ tự giảm dần là
A, A > C > B > E > D.
B, A > B > C > E > D.
C, D > C > B > E > A.
D, B > C > A > D > E.
Thí nghiệm 1: A(s) + D+(aq) → A+(aq) + D(s)
⟹ A có tính khử mạnh hơn D ⇒ A > D
Thí nghiệm 2: C(s) + B+(aq) → C+(aq) + B(s)
⟹ C có tính khử mạnh hơn B ⇒ C > B
Thí nghiệm 5: B(s) + E+(aq) → B+(aq) + E(s)
⟹ B có tính khử mạnh hơn E ⇒ B > E
Thí nghiệm 4: C(s) + A+(aq) → không phản ứng
⟹ C < A
⟹ A > C > B > E
Thí nghiệm 6: D(s) + E+ (aq) → không có phản ứng
⟹ E > D
⟹ A > C > B > E > D
⇒ Chọn đáp án A
Đáp án: A
⟹ A có tính khử mạnh hơn D ⇒ A > D
Thí nghiệm 2: C(s) + B+(aq) → C+(aq) + B(s)
⟹ C có tính khử mạnh hơn B ⇒ C > B
Thí nghiệm 5: B(s) + E+(aq) → B+(aq) + E(s)
⟹ B có tính khử mạnh hơn E ⇒ B > E
Thí nghiệm 4: C(s) + A+(aq) → không phản ứng
⟹ C < A
⟹ A > C > B > E
Thí nghiệm 6: D(s) + E+ (aq) → không có phản ứng
⟹ E > D
⟹ A > C > B > E > D
⇒ Chọn đáp án A
Đáp án: A