Trong các phản ứng hóa học chỉ có các electron thuộc các lớp bên ngoài (liên kết với hạt nhân yếu nhất) là có khả năng tham gia vào việc tạo liên kết hóa học, những electron này được gọi là electron hóa trị.
Trong tự nhiên, người ta nhận thấy chỉ có các nguyên tử khí hiếm là tồn tại độc lập mà không liên kết với các nguyên tử khác. Sở dĩ như vậy là vì chúng có lớp electron ngoài cùng có cấu hình ns2np6 (8 electron) bền vững có trạng thái năng lượng thấp.

Gilbert Newton Lewis
(1875-1946)
Vào năm 1916, Gilbert N. Lewis xây dựng Quy tắc octet. Quy tắc này phát biểu như sau: “Trong các phản ứng hóa học, các nguyên tử có xu hướng hình thành lớp vỏ bền vững như của khí hiếm”. Như vậy, trong quá trình hình thành liên kết hóa học,
các nguyên tử có xu hướng nhường, nhận hoặc góp chung electron để đạt được cấu hình bền vững như của khí hiếm gần nhất với 8 electron ở lớp ngoài cùng (hoặc 2 electron ở lớp ngoài cùng như của helium).
Trong tự nhiên, người ta nhận thấy chỉ có các nguyên tử khí hiếm là tồn tại độc lập mà không liên kết với các nguyên tử khác. Sở dĩ như vậy là vì chúng có lớp electron ngoài cùng có cấu hình ns2np6 (8 electron) bền vững có trạng thái năng lượng thấp.

Gilbert Newton Lewis
(1875-1946)
Vào năm 1916, Gilbert N. Lewis xây dựng Quy tắc octet. Quy tắc này phát biểu như sau: “Trong các phản ứng hóa học, các nguyên tử có xu hướng hình thành lớp vỏ bền vững như của khí hiếm”. Như vậy, trong quá trình hình thành liên kết hóa học,
các nguyên tử có xu hướng nhường, nhận hoặc góp chung electron để đạt được cấu hình bền vững như của khí hiếm gần nhất với 8 electron ở lớp ngoài cùng (hoặc 2 electron ở lớp ngoài cùng như của helium).
Câu 1 [242095]: Khuynh hướng nào dưới đây không xảy ra trong quá trình hình thành liên kết hóa học?
A, Chia tách electron.
B, Nhường và nhận electron.
C, Góp chung electron.
D, Dùng chung electron tự do.
HƯỚNG DẪN GIẢI:
- Có hai khuynh hướng trong quá trình hình thành liên kết hoá học:
+) Nhường và nhận electron: Các nguyên tử nhường hoặc nhận thêm e để đạt cấu hình bền vững giống khí hiếm.
VD K → K+ +1e, cấu hình e của K+ là 1s22s22p63s23p6, giống cấu hình của Ar.
+) Dùng chung electron: Các nguyên tử dùng chung e để đạt cấu hình bền vững
VD H-Cl: H đưa 1 electron, Cl đưa 1 electron, hai nguyên tử này "dùng chung" e của nhau. Lúc này xung quanh H có 2e, Cl có 8e, đạt cấu hình bền vững.
- "Dùng chung electron tự do" giống với "Góp chung electron".
⟹ Chọn đáp án: A Đáp án: A
- Có hai khuynh hướng trong quá trình hình thành liên kết hoá học:
+) Nhường và nhận electron: Các nguyên tử nhường hoặc nhận thêm e để đạt cấu hình bền vững giống khí hiếm.
VD K → K+ +1e, cấu hình e của K+ là 1s22s22p63s23p6, giống cấu hình của Ar.
+) Dùng chung electron: Các nguyên tử dùng chung e để đạt cấu hình bền vững
VD H-Cl: H đưa 1 electron, Cl đưa 1 electron, hai nguyên tử này "dùng chung" e của nhau. Lúc này xung quanh H có 2e, Cl có 8e, đạt cấu hình bền vững.
- "Dùng chung electron tự do" giống với "Góp chung electron".
⟹ Chọn đáp án: A Đáp án: A
Câu 2 [242094]: Vì sao các nguyên tử (không xét các nguyên tử khí hiếm) lại thường có xu hướng liên kết với nhau thành phân tử?
A, Để mỗi nguyên tử trong phân tử đạt được cơ cấu electron ổn định, bền vững.
B, Để mỗi nguyên tử trong phân tử đều đạt được được cấu hình bền vững ở lớp ngoài cùng.
C, Để tổng số electron ngoài cùng của các nguyên tử trong phân tử là 8.
D, Để lớp ngoài cùng của mỗi nguyên tử trong phân tử có nhiều electron độc thân nhất.
HƯỚNG DẪN GIẢI:
- Phân tích các đáp án:
❌ A SAI. "Cơ cấu electron ổn định" nghĩa là số electron bằng số proton. Điều này xảy ra ở các nguyên tử chưa kết hợp với nhau.
✔️ B ĐÚNG. Các nguyên tử luôn "cố gắng" đạt được cấu hình electron bền vững ở lớp ngoài cùng.
❌ C SAI. Không phải lúc nào quy tắc Octet cũng được thoả mãn. Ví dụ phân tử BF3, Boron chỉ có 6 electron xung quanh.
❌ C SAI. Hầu hết các trường hợp các nguyên tử luôn muốn đạt được "Octet", tức là đủ 8 electron ở lớp ngoài cùng.
⟹ Chọn đáp án: B Đáp án: B
- Phân tích các đáp án:
❌ A SAI. "Cơ cấu electron ổn định" nghĩa là số electron bằng số proton. Điều này xảy ra ở các nguyên tử chưa kết hợp với nhau.
✔️ B ĐÚNG. Các nguyên tử luôn "cố gắng" đạt được cấu hình electron bền vững ở lớp ngoài cùng.
❌ C SAI. Không phải lúc nào quy tắc Octet cũng được thoả mãn. Ví dụ phân tử BF3, Boron chỉ có 6 electron xung quanh.
❌ C SAI. Hầu hết các trường hợp các nguyên tử luôn muốn đạt được "Octet", tức là đủ 8 electron ở lớp ngoài cùng.
⟹ Chọn đáp án: B Đáp án: B
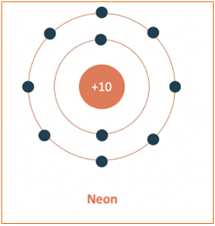
Câu 3 [242098]: Nguyên tử của nguyên tố nào sau đây có xu hướng đạt cấu hình electron bền vững của khí hiếm Neon khi tham gia hình thành liên kết hoá học?

A, Hydro (Z = 1).
B, Fluorine (Z = 9).
C, Chlorine (Z = 17).
D, Potassium (Z = 19).
HƯỚNG DẪN GIẢI:
- Cấu hình electron bền vững của khí hiếm Neon có 10 electron nên nguyên tử của nguyên tố Fluorine (Z = 9) có xu hướng nhận thêm 1 electron để đạt cấu hình electron bền vững của khí hiếm Neon khi tham gia hình thành liên kết hoá học.
⟹ Chọn đáp án: B Đáp án: B
- Cấu hình electron bền vững của khí hiếm Neon có 10 electron nên nguyên tử của nguyên tố Fluorine (Z = 9) có xu hướng nhận thêm 1 electron để đạt cấu hình electron bền vững của khí hiếm Neon khi tham gia hình thành liên kết hoá học.
⟹ Chọn đáp án: B Đáp án: B