Nước Javel là dung dịch chứa hỗn hợp muối NaCl và NaClO. Trong khi, NaCl không thể hiện tính oxy hoá thì NaClO thì thể hiện rất “mạnh mẽ” tính chất này, nó giúp phá vỡ cấu trúc của các phân tử có màu, chính vì vậy nước Javel có khả năng tẩy trắng vải, sợi và sát trùng nước sinh hoạt,… Tiến hành phân tích nồng độ ClO– trong nước Javel theo các bước sau:
▪ Bước 1: Pha loãng 10,00 mL dung dịch Javel với nước thu được 100 mL dung dịch X.
▪ Bước 2: Lấy 10,00 mL dung dịch X cho vào bình tam giác, sau đó thêm 10,00 mL dung dịch acetic acid 20%, lắc đều bình tam giác thu được dung dịch Y.
▪ Bước 3: Thêm tiếp 10,00 mL dung dịch KI 2,0 M vào dung dịch Y, lắc đều thu được dung dịch Z.
Các phương trình xảy ra như sau:
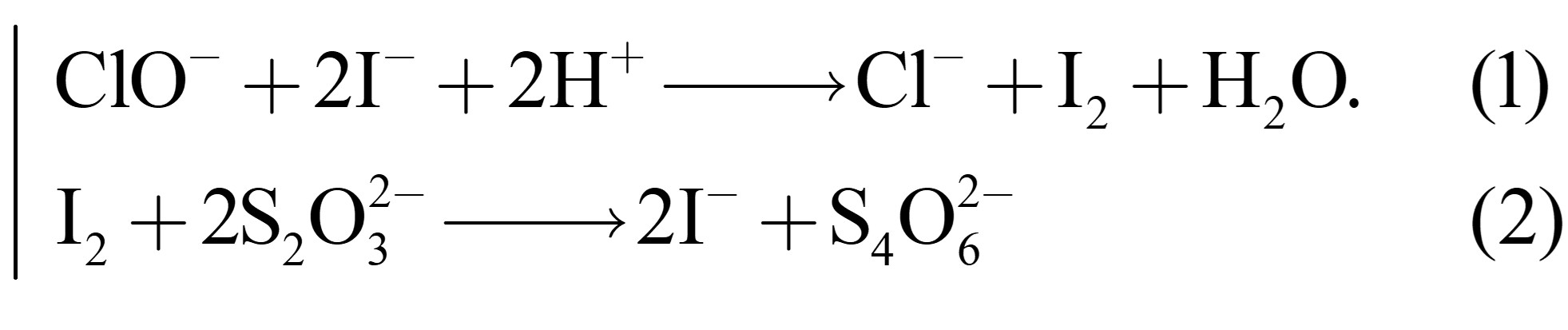
▪ Bước 1: Pha loãng 10,00 mL dung dịch Javel với nước thu được 100 mL dung dịch X.
▪ Bước 2: Lấy 10,00 mL dung dịch X cho vào bình tam giác, sau đó thêm 10,00 mL dung dịch acetic acid 20%, lắc đều bình tam giác thu được dung dịch Y.
▪ Bước 3: Thêm tiếp 10,00 mL dung dịch KI 2,0 M vào dung dịch Y, lắc đều thu được dung dịch Z.
Các phương trình xảy ra như sau:
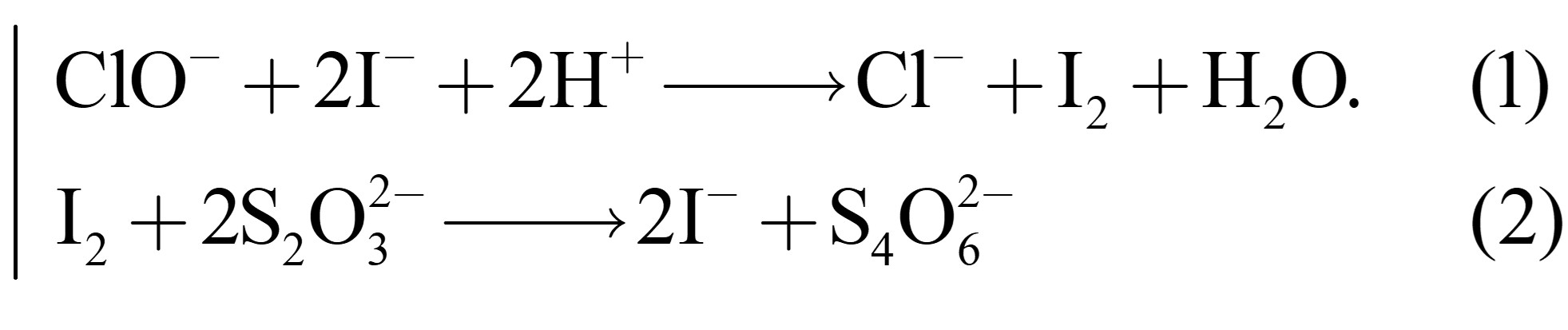
Câu 1 [382658]: Phát biểu nào sau đây là đúng?
A, Nếu thêm nhiều hơn 10,00 mL dung dịch KI 2,0 M vào dung dịch Y, kết quả phân tích hàm lượng NaClO cao hơn thực tế.
B, Nếu thêm nhiều hơn 10,00 mL dung dịch KI 2,0 M vào dung dịch Y, kết quả phân tích hàm lượng NaClO ít hơn thực tế.
C, Nếu thêm ít hơn 10,00 mL dung dịch KI 2,0 M vào dung dịch Y, kết quả phân tích hàm lượng NaClO nhiều hơn thực tế.
D, Nếu thêm nhiều hơn 10,00 mL dung dịch KI 2,0 M vào dung dịch Y, kết quả phân tích hàm lượng NaClO không thay đổi.
Đáp án: D. Nếu thêm nhiều hơn 10,00 mL dung dịch KI 2,0 M vào dung dịch Y, kết quả phân tích hàm lượng NaClO không thay đổi.
Phản ứng chính:
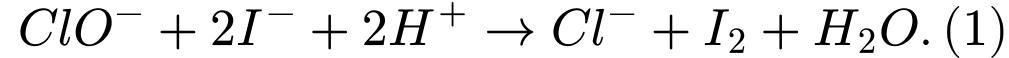
Nếu cho quá nhiều KI thì chỉ có lợi I⁻ ở dư, phản ứng vẫn bị giới hạn bởi ClO^-. Do đó tăng lượng KI vượt mức cần thiết không làm thay đổi lượng I₂ sinh ra (và kết quả phân tích), miễn là ban đầu lượng KI đủ để phản ứng hoàn toàn. Đáp án: D
Phản ứng chính:
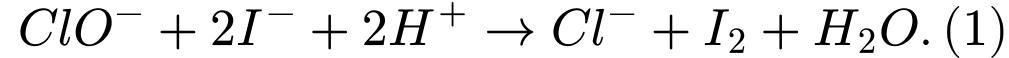
Nếu cho quá nhiều KI thì chỉ có lợi I⁻ ở dư, phản ứng vẫn bị giới hạn bởi ClO^-. Do đó tăng lượng KI vượt mức cần thiết không làm thay đổi lượng I₂ sinh ra (và kết quả phân tích), miễn là ban đầu lượng KI đủ để phản ứng hoàn toàn. Đáp án: D
Câu 2 [382659]: Cho các dung dịch sau:
(1) dung dịch HNO3 4M;
(3) dung dịch HCl 2M;
(2) dung dịch H2SO4 đậm đặc;
(4) dung dịch HCl/HClO.
Số dung dịch có thể thay thế dung dịch acetic acid ở trên là
(1) dung dịch HNO3 4M;
(3) dung dịch HCl 2M;
(2) dung dịch H2SO4 đậm đặc;
(4) dung dịch HCl/HClO.
Số dung dịch có thể thay thế dung dịch acetic acid ở trên là
A, 1.
B, 2.
C, 3.
D, 4.
HNO₃ (tính oxi hóa mạnh) → không được (oxi hóa I⁻).
HCl (có Cl⁻) → không được (Cl⁻ + ClO⁻ trong môi trường acid cho Cl₂, gây sai).
HCl/HClO chứa HOCl (tính oxi hóa mạnh) → không được.
H₂SO₄ (cung cấp H⁺, bản thân không ôxi hóa I⁻ trong điều kiện lạnh/pha lỏng dùng ở phòng thí nghiệm) có thể thay acetic acid (lưu ý thực nghiệm chọn nồng độ/điều kiện phù hợp).
Đáp án: A. 1. Đáp án: A
HCl (có Cl⁻) → không được (Cl⁻ + ClO⁻ trong môi trường acid cho Cl₂, gây sai).
HCl/HClO chứa HOCl (tính oxi hóa mạnh) → không được.
H₂SO₄ (cung cấp H⁺, bản thân không ôxi hóa I⁻ trong điều kiện lạnh/pha lỏng dùng ở phòng thí nghiệm) có thể thay acetic acid (lưu ý thực nghiệm chọn nồng độ/điều kiện phù hợp).
Đáp án: A. 1. Đáp án: A
Câu 3 [382660]: Biết để phản ứng hoàn toàn lượng iot trong dung dịch Z cần 30,00 mL dung dịch Na2S2O3 0,1 M. Nồng độ của ClO– trong dung dịch nước Javen ở trên là
A, 1,5 M.
B, 0,5 M.
C, 2,0 M.
D, 1,25 M.
Số mol của Na2S2O3 là: nNa2S2O3 = 0,03.0,1 = 0,003 mol
$\left| \begin{align}
& \,\,Cl{{O}^{-}}+2{{I}^{-}}+2{{H}^{+}}\xrightarrow{{}}C{{l}^{-}}+{{I}_{2}}+{{H}_{2}}O.(1) \\
& \,\,{{I}_{2}}+2{{S}_{2}}O_{3}^{2-}\xrightarrow[{}]{{}}2{{I}^{-}}+{{S}_{4}}O_{6}^{2-}(2) \\
\end{align} \right$
Theo PTHH số mol của ClO- là 0,0015 mol
Quy đổi về nồng độ trong dung dịch Javel ban đầu: lượng ClO⁻ này xuất phát từ 1,00 mL mẫu Javel ban đầu (vì: 10 mL Javel pha tới 100 mL X → lấy 10 mL X tương đương 1 mL Javel).
Nồng độ của ClO– trong dung dịch nước Javel ở trên là:
${{C}_{M}}=\frac{0,0015}{0,001}=1,5\,M$
Đáp án: A. 1,5 M.
Đáp án: A
$\left| \begin{align}
& \,\,Cl{{O}^{-}}+2{{I}^{-}}+2{{H}^{+}}\xrightarrow{{}}C{{l}^{-}}+{{I}_{2}}+{{H}_{2}}O.(1) \\
& \,\,{{I}_{2}}+2{{S}_{2}}O_{3}^{2-}\xrightarrow[{}]{{}}2{{I}^{-}}+{{S}_{4}}O_{6}^{2-}(2) \\
\end{align} \right$
Theo PTHH số mol của ClO- là 0,0015 mol
Quy đổi về nồng độ trong dung dịch Javel ban đầu: lượng ClO⁻ này xuất phát từ 1,00 mL mẫu Javel ban đầu (vì: 10 mL Javel pha tới 100 mL X → lấy 10 mL X tương đương 1 mL Javel).
Nồng độ của ClO– trong dung dịch nước Javel ở trên là:
${{C}_{M}}=\frac{0,0015}{0,001}=1,5\,M$
Đáp án: A. 1,5 M.
Đáp án: A