NƯỚC CỨNG
Nước cứng không có nghĩa là băng, là đá. Đó là tên được đặt cho nước chứa nồng độ cao ion Ca2+ và trong một số trường hợp là Mg2+, ngoài ra có thể có các cation kim loại hóa trị II khác. Đi kèm với các cation này sẽ là các anion khác nhau, đặc biệt là anion hydrogencarbonate, HCO3–. Nước thu được từ các hồ chứa nước mưa thường không chứa nồng độ cao các ion này và do đó không được phân loại là "nước cứng". Tuy nhiên, ở nhiều nơi, nguồn cung cấp nước của thành phố được lấy từ tầng nước sâu dưới lòng đất. Nếu nước mưa có chứa một ít CO2 hòa tan phải thấm qua các lớp đá vôi (CaCO3) để vào tầng nước ngầm thì một lượng nhỏ chất rắn sẽ hòa tan do có cân bằng sau:
CaCO3(s) + CO2(aq) + H2O(l)
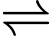 Ca2+(aq) + 2HCO3−(aq) (I)
Ca2+(aq) + 2HCO3−(aq) (I)Ở quy mô nhỏ, hầu hết các hệ thống lọc nước gia đình đều sử dụng phương pháp trao đổi ion để làm mềm nước (Hình ảnh).
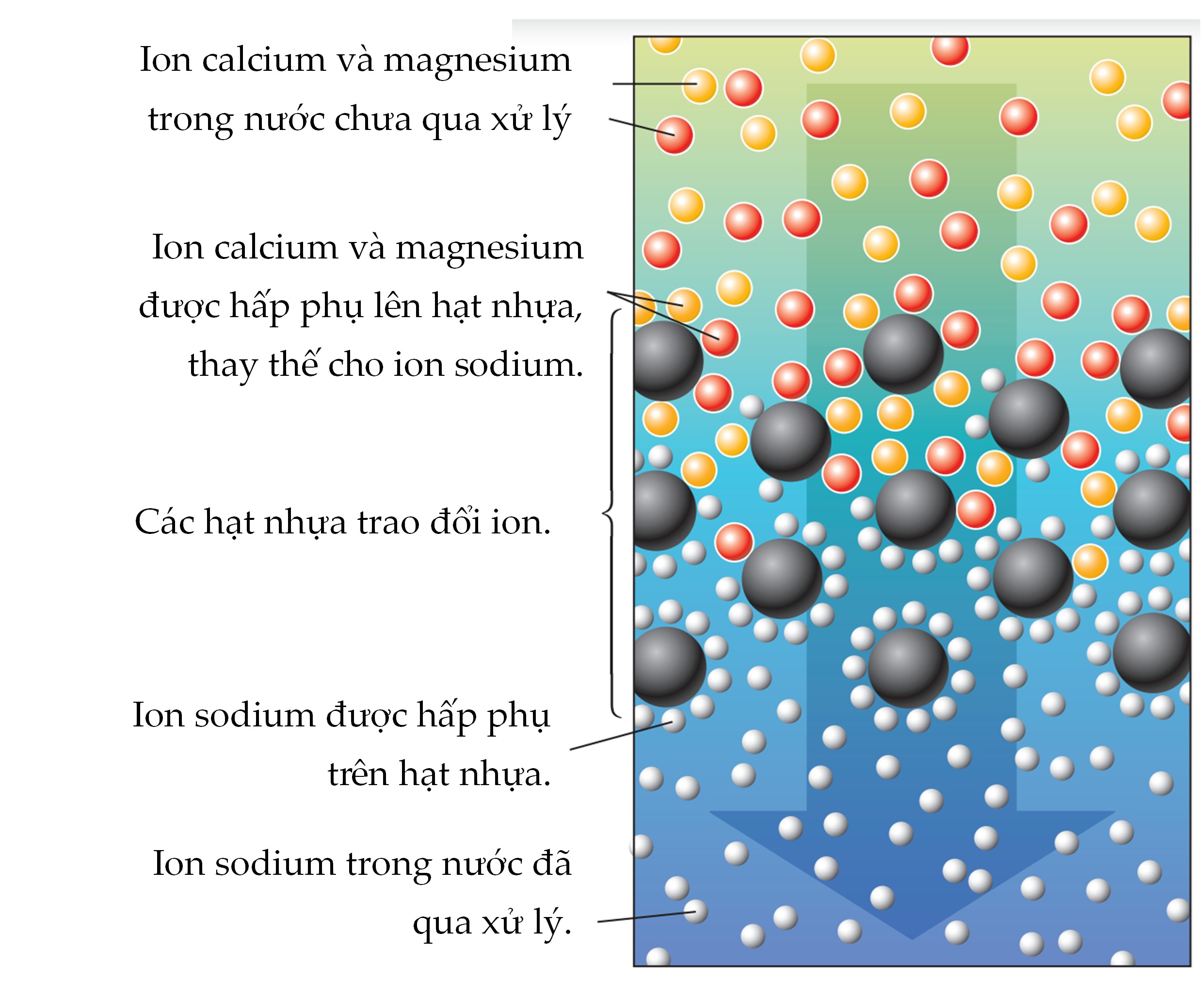
Nguyên tắc của quá trình này là thay thế ion đang được hấp phụ (ion A) trên vật liệu “nhựa trao đổi ion” bằng ion khác trong dung dịch (ion B). Hiện nay, các polymer hữu cơ tổng hợp có các nhóm chức tích điện âm (chẳng hạn như nhóm carboxylate, –CO2–) là loại nhựa được sử dụng phổ biến nhất để tạo ra vật liệu “nhựa trao đổi ion”. Các ion sodium, Na+, có trong nhựa sẽ bao quanh bề mặt của nhựa để trung hòa về mặt điện tích.
Tuy nhiên, tương tác của bề mặt vật liệu với các cation đa điện tích lớn hơn là các cation đơn điện tích. Do đó, khi dung dịch nước cứng đi qua bề mặt nhựa trao đổi ion, ion Ca2+ và Mg2+ (các cation đa điện tích) sẽ dễ dàng thay thế ion Na+ (các cation đơn điện tích) trên bề mặt. Quá trình này có thể được minh họa một cách tổng quát như sau:
2NaX + Ca2+(aq)
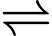 CaX2 + 2Na+(aq)
CaX2 + 2Na+(aq)Trong đó X đại diện cho vị trí hấp phụ trên nhựa trao đổi ion. Trạng thái cân bằng thuận lợi cho sự hấp phụ Ca2+ và giải phóng Na+. Tuy nhiên, trạng thái cân bằng bị đảo ngược nếu ion Na+(aq) có trong dung dịch ở nồng độ cao và điều này cho phép tái sử dụng nhựa trao đổi ion. Dung dịch chứa nồng độ Na+ cao (thường là từ muối NaCl) được đưa qua nhựa để chuyển nhựa trở lại dạng ban đầu.
Câu 1 [561005]: Dựa vào phương trình (I), yếu tố nào sau đây làm tăng sự hòa tan đá vôi?
A, Tăng nồng độ Ca2+.
B, Tăng nồng độ CO2 hòa tan.
C, Tăng nồng độ HCO3–.
D, Thực hiện phản ứng trong điều kiện khô.
Để tăng sự hòa tan đá vôi, nghĩa là cân bằng chuyển dịch theo chiều thuận.
Phân tích các đáp án:
❌A. Tăng nồng độ Ca2+ => Cân bằng dịch chuyển theo chiều giảm nồng độ Ca2+, chiều nghịch.
✔️B. Tăng nồng độ CO2 hòa tan => Cân bằng dịch chuyển theo chiều giảm nồng độ CO2 => chiều thuận.
❌C. Tăng nồng độ HCO3- => Cân bằng dịch chuyển theo chiều giảm nồng độ HCO3- => chiều nghịch.
❌D. Thực hiện phản ứng trong điều kiện khô=> giảm nồng độ nước=> Cân bằng dịch chuyển theo chiều nghịch.
=> Chọn đáp án B Đáp án: B
Phân tích các đáp án:
❌A. Tăng nồng độ Ca2+ => Cân bằng dịch chuyển theo chiều giảm nồng độ Ca2+, chiều nghịch.
✔️B. Tăng nồng độ CO2 hòa tan => Cân bằng dịch chuyển theo chiều giảm nồng độ CO2 => chiều thuận.
❌C. Tăng nồng độ HCO3- => Cân bằng dịch chuyển theo chiều giảm nồng độ HCO3- => chiều nghịch.
❌D. Thực hiện phản ứng trong điều kiện khô=> giảm nồng độ nước=> Cân bằng dịch chuyển theo chiều nghịch.
=> Chọn đáp án B Đáp án: B
Câu 2 [561006]: Để làm mềm nước cứng, ion A có thể là ion nào sau đây?
A, Ca2+.
B, Mg2+.
C, Fe2+.
D, Na+.
Các vật liệu trao đổi ion (như zeolite hoặc nhựa trao đổi ion) thường sử dụng ion Na+ để thay thế Ca2+ và Mg2+, do Na+ không gây ra độ cứng trong nước.
Để làm mềm nước cứng, ion A trong quá trình trao đổi ion thường là ion có khả năng thay thế các ion gây ra độ cứng của nước, chủ yếu là Ca2+ và Mg2+
=> Chọn đáp án D Đáp án: D
Để làm mềm nước cứng, ion A trong quá trình trao đổi ion thường là ion có khả năng thay thế các ion gây ra độ cứng của nước, chủ yếu là Ca2+ và Mg2+
=> Chọn đáp án D Đáp án: D
Câu 3 [561007]: Giả sử vật liệu trao đổi ion chỉ chứa 10 nhóm carboxylate, sau khi trao đổi ion thì vẫn còn 4 ion Na+ tồn tại trên bề mặt vật liệu. Quá trình này tổng quát như sau:
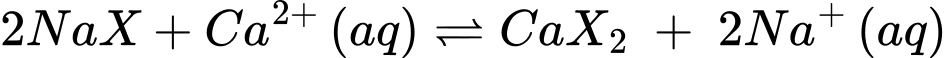
Có bao nhiêu ion Ca2+ tồn tại trên bề mặt vật liệu?
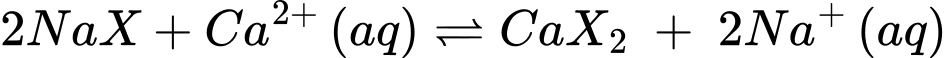
Có bao nhiêu ion Ca2+ tồn tại trên bề mặt vật liệu?
A, 2.
B, 3.
C, 4.
D, 5.
Tổng số nhóm carboxylate: 10.
Số ion Na+ còn lại: 4.
Như vậy, số nhóm carboxylate còn lại liên kết với Ca2+ là: 10−4 = 6 nhóm
Do mỗi ion Ca2+ cần 2 nhóm carboxylate để cân bằng điện tích, số ion Ca2+ trên bề mặt vật liệu sẽ là:
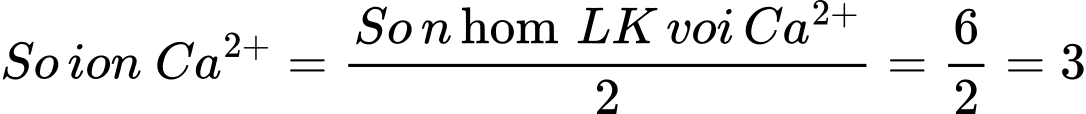
Có 3 ion Ca2+ tồn tại trên bề mặt vật liệu.
=> Chọn đáp án B Đáp án: B
Số ion Na+ còn lại: 4.
Như vậy, số nhóm carboxylate còn lại liên kết với Ca2+ là: 10−4 = 6 nhóm
Do mỗi ion Ca2+ cần 2 nhóm carboxylate để cân bằng điện tích, số ion Ca2+ trên bề mặt vật liệu sẽ là:
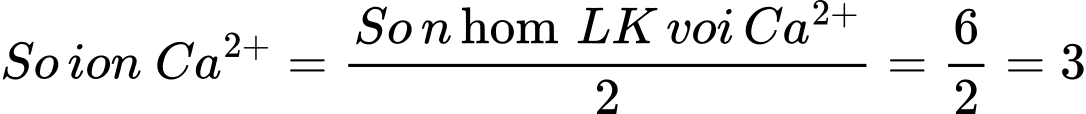
Có 3 ion Ca2+ tồn tại trên bề mặt vật liệu.
=> Chọn đáp án B Đáp án: B