Phần 1: Lấy 20 mL dung dịch X chuẩn độ với dung dịch EDTA 0,01 M, thì dùng hết 1,85 mL dung dịch EDTA.
Phần 2: Lấy 20 mL dung dịch X, điểu chỉnh pH của dung dịch bằng cách thêm NaOH 0,2 M sao cho Ca2+ không kết tủa nhưng có thể loại ion Mg²⁺ dưới dạng kết tủa Mg(OH)2. Sau khi tách kết tủa, cũng tiến hành chuẩn độ với dung dịch EDTA 0,01 M thì thấy dùng hết 1,24 mL dung dịch EDTA. Phương trình chuẩn độ xảy ra như sau:
Mg2+(aq) + EDTA2–(aq) → Mg(EDTA)(aq)
Ca2+(aq) + EDTA2–(aq) → Ca(EDTA)(aq)
Khi
pha loãng 50 mL nước khoáng thành 100 mL dung dịch X, dung dịch X so với mẫu nước
ban đầu đã thay đổi nồng độ giảm một nửa.
Đáp án: B. Giảm một nửa.
- Thêm NaOH để điều chỉnh pH sao cho:
+ Ca²⁺ không kết tủa → pH < pH kết tủa Ca(OH)₂
+ Mg²⁺ kết tủa dưới dạng Mg(OH)₂ → Mg²⁺ bị loại bỏ
- Tách kết tủa Mg(OH)₂ → trong dung dịch còn lại chỉ còn Ca²⁺.
- Chuẩn độ bằng EDTA → EDTA chỉ phản ứng với ion Ca²⁺ còn trong dung dịch.
Kết luận: Dung dịch EDTA lúc này chỉ chuẩn độ với Ca²⁺.
Đáp án: B. Chỉ Ca2+.
Đáp án: BMg2+(aq) + EDTA2–(aq)  Mg(EDTA)(aq)
Mg(EDTA)(aq)
Ca2+(aq) + EDTA2–(aq)  Ca(EDTA)(aq)
Ca(EDTA)(aq)
Phần 1: số mol của EDTA2- là nEDTA2- = 0,01.0,00185 = 1,85.10-5 mol
Theo PTHH: nCa2+ + nMg2+ = 1,85.10-5 mol
Phần 2: số mol của EDTA2- là nEDTA 2- = 0,01.0,00124 = 1,24.10-5 mol = nCa2+
=> Số mol của Mg2+ là: 1,85.10-5 - 1,24.10-5 = 6,1.10-6 mol
=> Nồng độ Mg2+ trong 20 mL dung dịch X là:
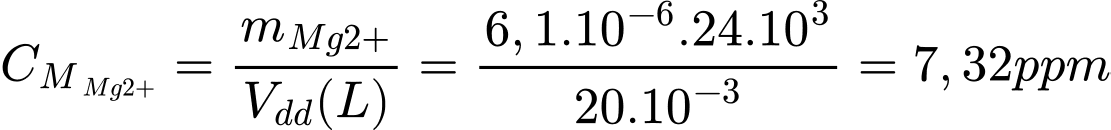
=> Nồng độ Mg2+ (ppm) trong mẫu nước khoáng ban đầu là:
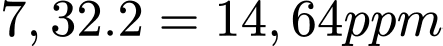
Đáp án: A. 14,64.