Một học sinh pha dung dịch thuốc tím, KMnO4 (có thể biểu diễn dưới dạng ion là MnO4–) để thực hiện các thí nghiệm. Yêu cầu cần có dung dịch MnO4– với nồng độ 1,0×10–2 M. Tuy nhiên trong phòng thí nghiệm chỉ có dung dịch MnO4– nồng độ 1,5×10–2 M. Do đó, một bạn học sinh bắt đầu tiến hành pha loãng để có dung dịch theo yêu cầu.
Câu 1 [382697]: Sử dụng ống đong có vạch chia độ 100,0 mL để đong 100,0 mL dung dịch MnO4– (aq) nồng độ 1,5 × 10-2 M. Kết quả thu được như hình bên, thể tích dung dịch MnO4– (aq) nồng độ 1,5 × 10-2 M thực tế đã lấy được là
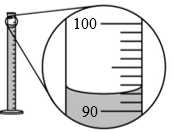

A, 93,0 mL.
B, 100,0 mL.
C, 92,0 mL.
D, 95,0 mL.
Từ hình vẽ thể tích thật dụng dịch MnO4- đã lấy là 92,0 mL.
⇒ Chọn đáp án C Đáp án: C
⇒ Chọn đáp án C Đáp án: C
Câu 2 [382698]: Giả sử đã lấy được đúng 100 ml dung dịch MnO4−(aq) nồng độ 1,5 × 10-2 M. Thể tích nước cần thêm để thu được dung dịch MnO4– (aq) với nồng độ 1,0 × 10-2 M là
A, 50,0 mL.
B, 100,0 mL.
C, 150,0 mL.
D, 40,0 mL.
Giả sử đã lấy được đúng 100 ml dung dịch MnO4−(aq) nồng độ 1,5 × 10-2 M
Gọi thể tích nước cần thêm để thu được dung dịch MnO4−(aq) nồng độ 1,0 × 10-2 M M là x (L)
Đổi 100 mL = 0,1 L
Số mol của MnO4- là: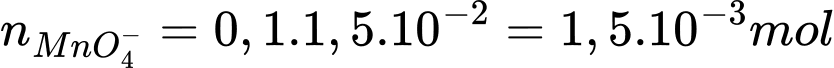
Ta có: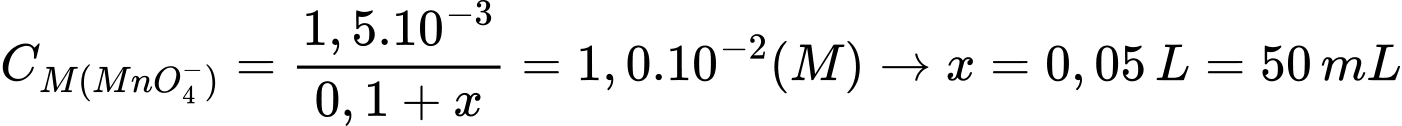
⇒ Chọn đáp án A Đáp án: A
Gọi thể tích nước cần thêm để thu được dung dịch MnO4−(aq) nồng độ 1,0 × 10-2 M M là x (L)
Đổi 100 mL = 0,1 L
Số mol của MnO4- là:
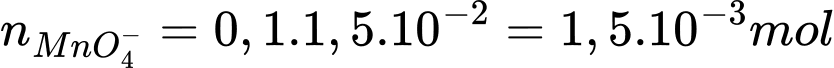
Ta có:
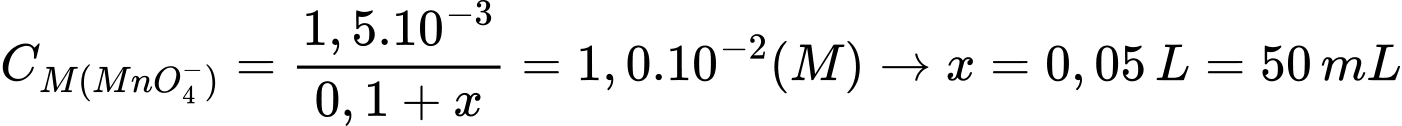
⇒ Chọn đáp án A Đáp án: A
Câu 3 [382699]: Hoà tan 0,315 gam oxalic acid ngậm nước H2C2O4.nH2O vào nước thu được 100,0 mL dung dịch X (sự thay đổi thể tích không đáng kể). Lấy 10,0 mL dung dịch X chuẩn độ bằng dung dịch MnO4– nồng độ 1,0×10–2 M trong môi trường H2SO4. Kết thúc chuẩn độ, thấy dùng hết 10,0 mL dung dịch MnO4–. Biết phương trình phản ứng:
2KMnO4 + 5H2C2O4 + 3H2SO4 → 2MnSO4 + K2SO4 + 10CO2 + 8H2O
Giá trị của n là
2KMnO4 + 5H2C2O4 + 3H2SO4 → 2MnSO4 + K2SO4 + 10CO2 + 8H2O
Giá trị của n là
A, 2.
B, 3.
C, 4.
D, 6.
Đổi 10 ml = 0,01 L
5H2C2O4 + 2MnO4− + 6H+ ⟶ 10CO2 + 2Mn2+ + 8H2O
Số mol MnO4− phản ứng là: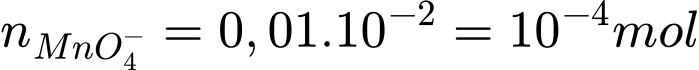
Từ PTHH số mol của H2C2O4 là: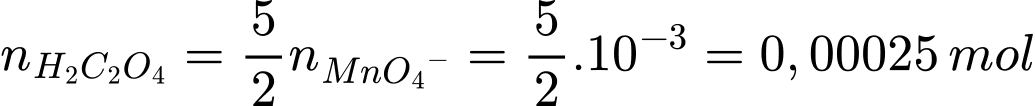
Ta có: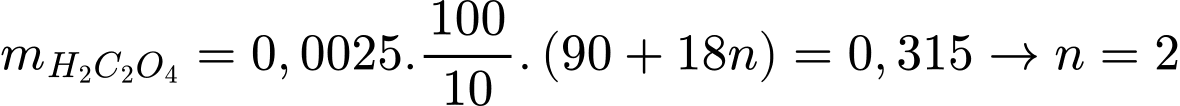
⇒ Chọn đáp án A Đáp án: A
5H2C2O4 + 2MnO4− + 6H+ ⟶ 10CO2 + 2Mn2+ + 8H2O
Số mol MnO4− phản ứng là:
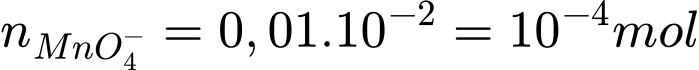
Từ PTHH số mol của H2C2O4 là:
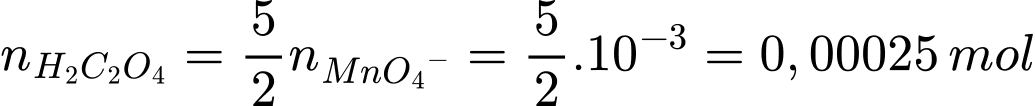
Ta có:
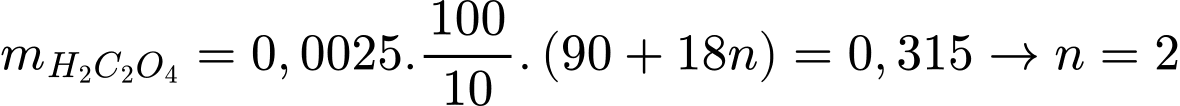
⇒ Chọn đáp án A Đáp án: A