Thể tích khí tạo ra bởi phản ứng hóa học có thể được đo và thu bằng phương pháp đẩy nước được thực hiện như trong dưới đây:
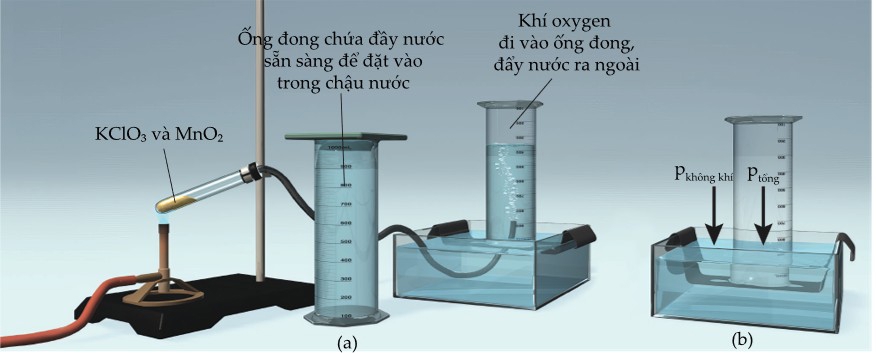
Hình ảnh. Thiết bị đo lượng khí sinh ra trong phản ứng hóa học (hình a). Khi mực nước bên trong và bên ngoài bình thu bằng nhau, áp suất bên trong bình bằng áp suất khí quyển (hình b).
Định luật áp suất riêng phần của Dalton hữu ích trong việc giúp xác định lượng khí sản phẩm do quá trình hóa học sinh ra. Ví dụ, sự phân hủy potassium chlorate (KClO3), phản ứng được sử dụng để tạo ra nguồn oxygen trong trường hợp khẩn cấp trên máy bay:
2KClO3(s) 2KCl(s) + 3O2(g).
2KCl(s) + 3O2(g).
Thể tích nước bị khí chiếm chỗ bằng thể tích khí tạo ra. Chú ý trước khi đọc thể tích khí, phải điều chỉnh mức của bình chia độ sao cho mực nước bên trong và bên ngoài bình bằng nhau. Điều này đảm bảo áp suất bên trong bình chia độ bằng với áp suất khí quyển [Hình b]. Tuy nhiên, vì thể tích đo được chứa cả oxygen tạo ra bởi phản ứng và hơi nước nên áp suất tác dụng bên trong bình chia độ là tổng áp suất riêng phần của hai khí:
Ptổng = PO₂ + PH₂O
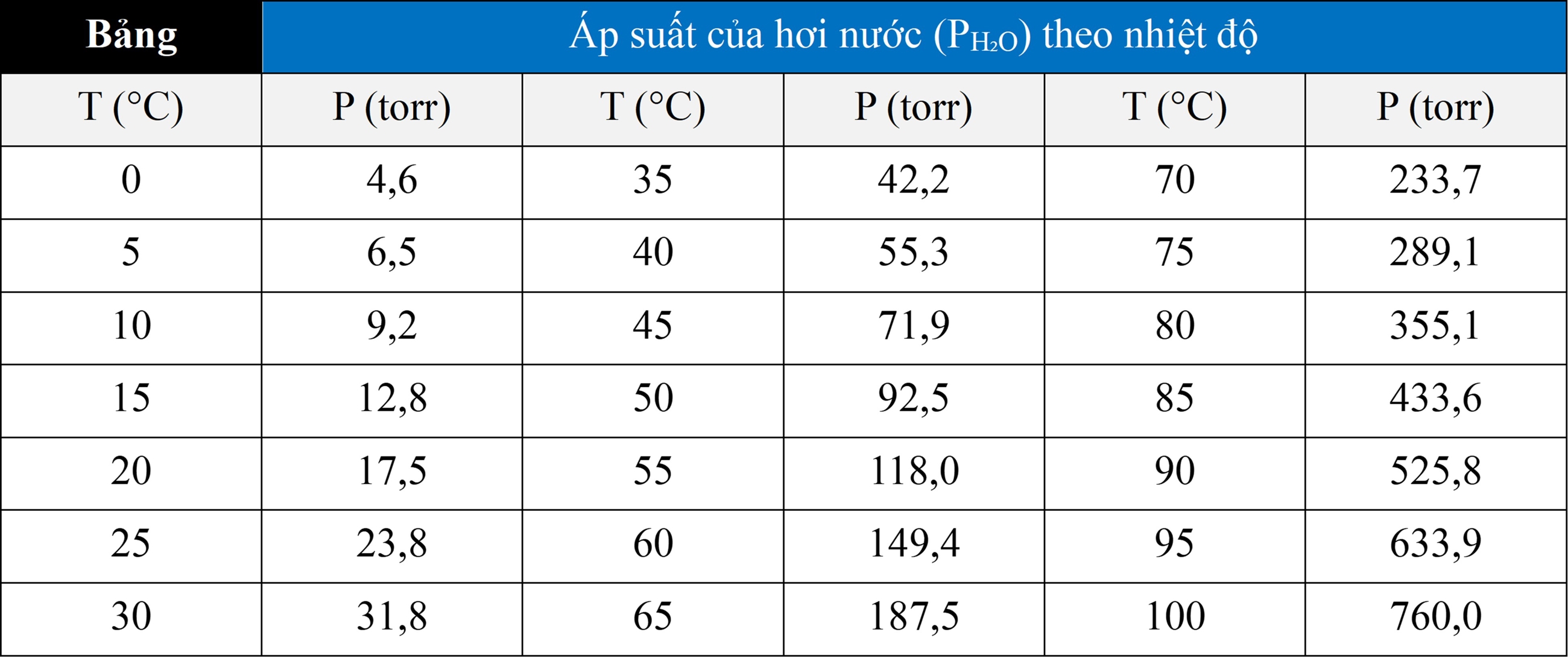
Bằng cách trừ áp suất riêng phần của nước khỏi áp suất tổng (bằng với áp suất khí quyển), chúng ta có thể xác định áp suất riêng phần của oxygen. Chúng ta có thể xác định áp suất riêng phần của nước, phụ thuộc vào nhiệt độ, từ bảng giá trị sau:

Hình ảnh. Thiết bị đo lượng khí sinh ra trong phản ứng hóa học (hình a). Khi mực nước bên trong và bên ngoài bình thu bằng nhau, áp suất bên trong bình bằng áp suất khí quyển (hình b).
Định luật áp suất riêng phần của Dalton hữu ích trong việc giúp xác định lượng khí sản phẩm do quá trình hóa học sinh ra. Ví dụ, sự phân hủy potassium chlorate (KClO3), phản ứng được sử dụng để tạo ra nguồn oxygen trong trường hợp khẩn cấp trên máy bay:
2KClO3(s)
 2KCl(s) + 3O2(g).
2KCl(s) + 3O2(g).Thể tích nước bị khí chiếm chỗ bằng thể tích khí tạo ra. Chú ý trước khi đọc thể tích khí, phải điều chỉnh mức của bình chia độ sao cho mực nước bên trong và bên ngoài bình bằng nhau. Điều này đảm bảo áp suất bên trong bình chia độ bằng với áp suất khí quyển [Hình b]. Tuy nhiên, vì thể tích đo được chứa cả oxygen tạo ra bởi phản ứng và hơi nước nên áp suất tác dụng bên trong bình chia độ là tổng áp suất riêng phần của hai khí:
Ptổng = PO₂ + PH₂O
Bằng cách trừ áp suất riêng phần của nước khỏi áp suất tổng (bằng với áp suất khí quyển), chúng ta có thể xác định áp suất riêng phần của oxygen. Chúng ta có thể xác định áp suất riêng phần của nước, phụ thuộc vào nhiệt độ, từ bảng giá trị sau:

Câu 1 [585132]: Tại sao có thể thu được khí oxygen bằng phương pháp đẩy nước?
A, Khí oxygen không phân cực.
B, Khí oxygen nhẹ hơn không khí.
C, Khí oxygen có tính oxi hóa mạnh.
D, Khí oxygen có thể làm khô bằng CaO.
Khí oxygen không phân cực nên không tan trong nước ⟶ có thể thu được khí oxygen bằng phương pháp đẩy nước.
⇒ Chọn đáp án A Đáp án: A
⇒ Chọn đáp án A Đáp án: A
Câu 2 [585133]: Chúng ta có thể xác định áp suất riêng phần của nước, phụ thuộc vào nhiệt độ, từ bảng giá trị sau:
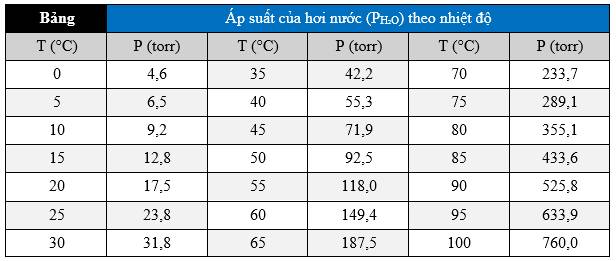

* Biết 1 atm = 760 torr.
Xác định khối lượng O2 sinh ra ở 25°C với áp suất khí quyển là 0,967 atm và thể tích khí thu được bên trong bình là 525 mL. A, 0,345 g.
B, 0,643 g.
C, 0,840 g.
D, 0,136 g.
Đổi đơn vị: T = 25oC = 298 K
Số mol của O2 trong bình là:
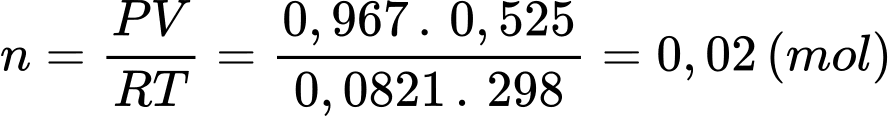
(R là hằng số khí lý tưởng: R = 0,0821 L.atm/mol.K)
→ mO2 = n.M = 0,02 . 32 = 0,64 (gam)
⇒ Chọn đáp án B Đáp án: B
Số mol của O2 trong bình là:
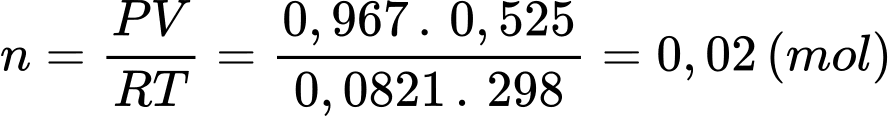
(R là hằng số khí lý tưởng: R = 0,0821 L.atm/mol.K)
→ mO2 = n.M = 0,02 . 32 = 0,64 (gam)
⇒ Chọn đáp án B Đáp án: B